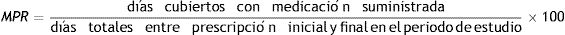Estimar la tasa de adherencia al tratamiento antiasmático con corticoide inhalado en condiciones de práctica clínica habitual, así como su relación con las exacerbaciones, el uso de recursos y los costes.
Material y métodosEstudio observacional retrospectivo realizado en el ámbito de Badalona Serveis Assistencials. Se incluyeron pacientes≥15 años con diagnóstico confirmado de asma que iniciaron tratamiento con corticoide inhalado entre enero 2010-diciembre 2011. El periodo de seguimiento fue de 24 meses. La adherencia al tratamiento se midió con la tasa de posesión de medicación, estableciéndose 2 grupos: pacientes adherentes (ADH; tasa de posesión de medicación≥80%) y no adherentes (no-ADH; tasa de posesión de medicación<80%). Se recogieron las variables demográficas y clínicas, las exacerbaciones, el uso de recursos sanitarios y no sanitarios (días de baja laboral) y los costes.
ResultadosSe incluyeron 2.303 pacientes, con una edad media de 48,6 años, un 64,3% fueron mujeres y un 52,6% presentaban asma persistente moderada. Un 51,0% eran ADH al tratamiento. De los pacientes no-ADH, un 63,4% presentó exacerbaciones durante el periodo de estudio frente al 37,4% de los pacientes ADH (p<0,001), presentando, además, un mayor consumo de recursos sanitarios, especialmente visitas a Atención Primaria (22,5 vs. 17,4%), especializada (3,3 vs. 2,5%) y urgencias (1,4% vs. 0,2%) (p<0,001 en todos los casos). No se encontraron diferencias estadísticamente significativas en los días de baja laboral. El coste total anual fue de 1.431€/paciente no-ADH frente a 722€/paciente ADH (p<0,001).
ConclusiónLa falta de adherencia se relacionó con un aumento de la tasa de exacerbaciones, así como del consumo de recursos sanitarios y costes.
To estimate adherence to asthma treatment with inhaled corticosteroid in clinical daily practice, and its relationship with exacerbations, as well as its use of resources and costs.
Material and methodsAn observational, retrospective study using the electronic medical records of the Badalona Health Service provider. The study included patients≥15 years old with a confirmed diagnosed of asthma, and who initiated treatment with an inhaled corticosteroid between January 2010 and December 2011. The follow-up period was 24 months. Adherence to treatment was measured using the medication possession ratio. Two groups were established: adherent (ADH; medication possession ratio≥80%) and non-adherent (non-ADH; medication possession ratio<80%) patients. The main demographic and clinical variables, including exacerbations, were collected, along with the healthcare and non-healthcare (days of absence from work) resource use, and costs.
ResultsThe study included a total of 2,303 patients, with a mean age of 48.6 years, and 64.3% females. Just over half (52.6%) of the patients had moderate persistent asthma, and 51.0% of patients adhered to treatment. In the non-ADH patients, 63.4% suffered at least one exacerbation in the follow-up period, compared with 37.4% of the adherent patients (P<.001). The non-ADH patients also consumed a higher percentage of healthcare resources in Primary Care (22.5 vs. 17.4%), secondary care (3.3 vs. 2.5%), and emergency visits (1.4 vs. 0.2%) during the follow-up period (P<.001 in all cases). No statistical significance differences were observed in the days of absence from work. Mean annual cost of non-ADH patients was 1,431€/patient, compared with 722€/patient (P<.001) of ADH patients.
ConclusionLack of adherence was associated with an increase in exacerbation rates, as well as healthcare resource consumption and costs.
El asma es una enfermedad inflamatoria crónica de las vías respiratorias que cursa con hiperrespuesta bronquial y una obstrucción variable al flujo aéreo. Sus síntomas más comunes incluyen sibilancias, disnea, tos y opresión torácica. Además, los pacientes asmáticos pueden experimentar exacerbaciones, caracterizadas por un empeoramiento de los síntomas basales, que requieren una modificación en el tratamiento1.
Es una de las enfermedades respiratorias más comunes. En España se ha estimado una prevalencia del 4,9%, si bien existe variabilidad entre comunidades autónomas2. Se asocia con una importante morbilidad; los pacientes asmáticos indican ver afectada la realización de sus actividades diarias, físicas y sociales debido a su enfermedad3. Además, genera un elevado consumo de recursos sanitarios, estimándose el coste medio anual de un paciente asmático para el Sistema Nacional de Salud en 1.533€4.
El objetivo principal del tratamiento del asma es lograr y mantener el control de la enfermedad. La base del tratamiento farmacológico de mantenimiento son los corticoides inhalados (CI), que ayudan a controlar los síntomas y reducir el riesgo de exacerbaciones1.
A pesar de la existencia de diferentes tratamientos con eficacia demostrada, algunos estudios indican que alrededor de la mitad de los pacientes presentan un asma no controlada5. Se han identificado diversos factores que pueden influir en la falta de control, como pueden ser la exposición a alérgenos, la dificultad en el manejo de los dispositivos de inhalación y la falta de adherencia1. De hecho, la adherencia se ha identificado como un factor fundamental para la obtención del control clínico, incluso en pacientes que presentan otros factores asociados a un mal control, como puede ser la exposición a alérgenos6.
Estudios publicados indican que la adherencia a los tratamientos asmáticos es baja7–9. La falta de adherencia no solo tiene impacto en el control de la enfermedad, sino que también se ha asociado con un aumento del consumo de recursos sanitarios y costes10,11.
En España, existe una evidencia limitada sobre la tasa de adherencia en pacientes asmáticos, así como sobre su relación con el uso de recursos o costes asociados. Es por ello que se diseñó este estudio con el objetivo de estimar la tasa de adherencia al tratamiento antiasmático con CI en condiciones de práctica clínica habitual, así como su relación con los resultados clínicos (exacerbaciones) y con el uso de recursos sanitarios y no sanitarios y costes asociados.
Material y métodosEstudio observacional longitudinal realizado a partir de la revisión retrospectiva de los registros médicos electrónicos de pacientes seguidos en régimen ambulatorio. La población de estudio fueron pacientes pertenecientes a 7 centros de Atención Primaria y un centro hospitalario, el Hospital Municipal de Badalona, gestionados por Badalona Serveis Assistencials S. A. El estudio fue aprobado por el Comité Ético de Investigación Clínica del Hospital Germans Trias i Pujol.
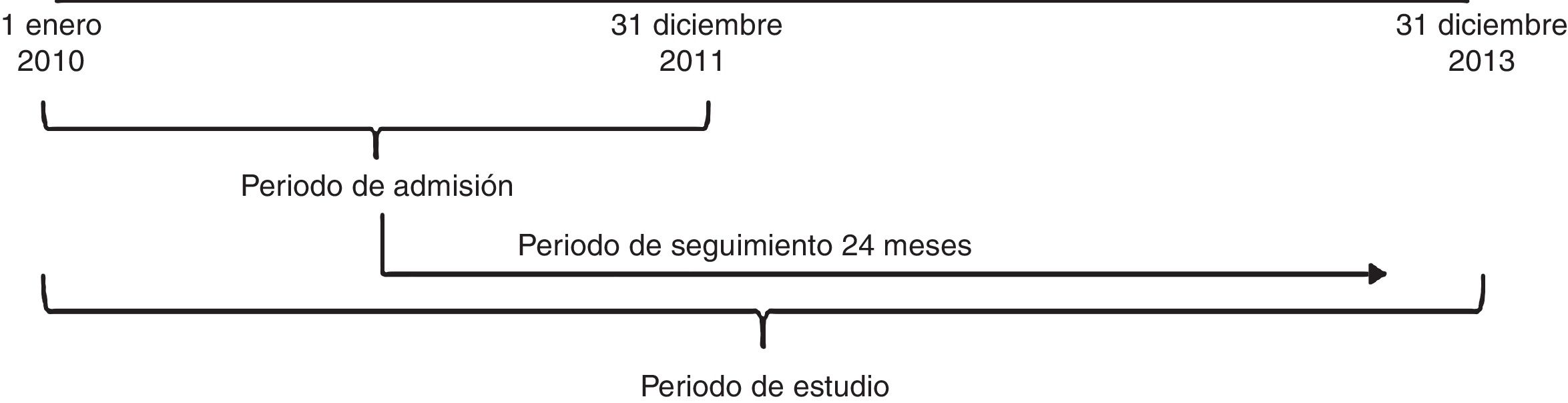
El periodo de admisión del estudio fue de enero de 2010 a diciembre de 2011. Para ser incluidos en el estudio, los pacientes debieron cumplir los criterios de inclusión y exclusión y tener una primera prescripción de un CI, en monoterapia o en combinación con otro tratamiento, durante el periodo de admisión. El periodo de seguimiento de cada paciente fue de 24 meses desde dicha primera prescripción (fig. 1).
Población de estudioSe incluyeron todos los pacientes≥15 años de edad que demandaron asistencia sanitaria y que tenían un diagnóstico de asma (código CIE-9-MC 493.x o CIAP-2 R96) confirmado con espirometría y que iniciaron tratamiento con un CI durante el periodo de estudio. Además, los pacientes debían estar incluidos en el programa de prescripción-dispensación de Badalona Serveis Assistencials S. A. para la obtención de recetas médicas, y tener al menos 2 prescripciones de un CI durante el periodo de admisión, con registro constatado de la dosis diaria, el intervalo de tiempo y la duración del tratamiento. Se excluyeron los pacientes que hubieran recibido tratamiento con el mismo CI en los 12 meses previos al periodo de admisión para evitar un sesgo de inclusión de pacientes no adherentes que hubiesen iniciado y discontinuado el tratamiento con el mismo CI en el pasado, los pacientes con pérdida de seguimiento los 12 primeros meses del periodo de estudio y los pacientes con un código diagnóstico de EPOC, enfisema pulmonar, bronquiectasia, fibrosis quística y neoplasia bronquial.
Medidas de adherenciaComo variable principal de medida de adherencia se seleccionó la tasa de posesión de medicación (MPR), calculada de acuerdo a la siguiente fórmula:
El punto de corte para considerar a un paciente como adherente se estableció en el 80%, valor normalmente considerado para el cálculo de la adherencia debido a su capacidad para predecir hospitalizaciones en enfermedades crónicas prevalentes12.
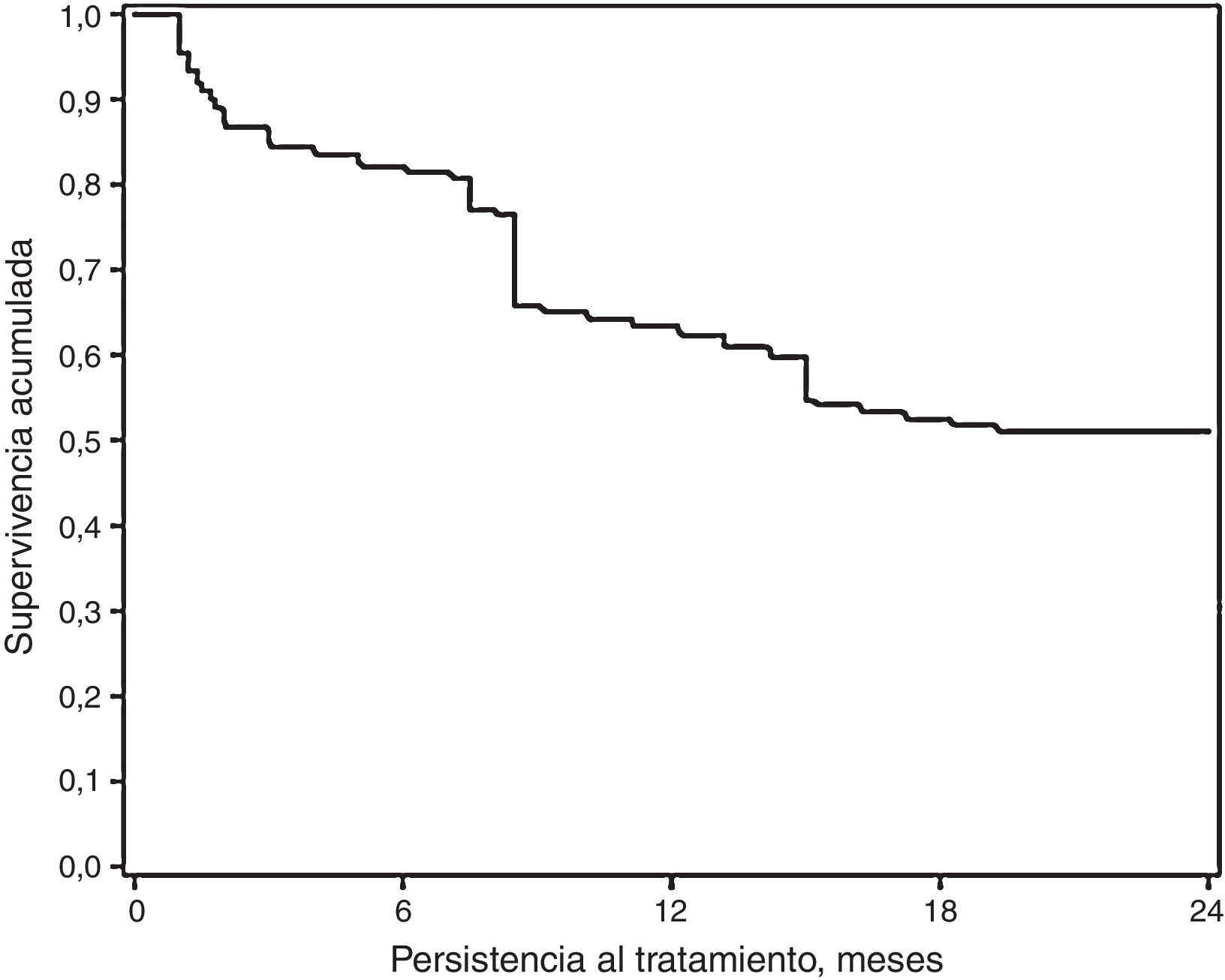
Como variable secundaria se calculó la tasa de persistencia al tratamiento a los 12 y a los 24 meses de seguimiento, calculada como el porcentaje de pacientes que renovaron las prescripciones subsiguientes sin un intervalo de tiempo mayor de 30 días, así como el tiempo (meses) sin abandono del tratamiento inicial o sin cambio de medicación utilizando el análisis de supervivencia de Kaplan-Meier.
Adicionalmente, como variable exploratoria, se revisaron los pacientes que tuvieran un registro electrónico disponible del cuestionario de adherencia Morisky-Green. Dicho cuestionario valora el cumplimiento terapéutico directamente del paciente y está validado para su uso en enfermedades crónicas. Consta de 4 preguntas con respuesta dicotómica sí/no que reflejan la conducta del paciente respecto al cumplimiento del tratamiento. Un paciente se considera adherente cuando responde de forma correcta las 4 preguntas planteadas en el cuestionario13. En el caso de que un paciente tuviese varios registros disponibles durante el periodo de estudio, el análisis se realizó con el último.
Variables de estudioSe recogieron las principales variables demográficas de los pacientes en el momento de la inclusión en el estudio, incluyendo edad, sexo, índice de masa corporal y principales comorbilidades. Como resumen de la comorbilidad general del paciente se calculó el índice de comorbilidad de Charlson14 y el índice de casuística individual, obtenido a partir de los adjusted clinical groups, que es un sistema de clasificación de pacientes por isoconsumo de recursos15; cada paciente, en función de su morbilidad general, queda agrupado en una de las 5 categorías mutuamente excluyentes (1: sanos o morbilidad muy baja; 2: morbilidad baja; 3: morbilidad moderada; 4: morbilidad elevada, y 5: morbilidad muy elevada).
Las variables clínicas recogidas fueron el tiempo desde el diagnóstico de asma y la gravedad en el momento de la inclusión en el estudio según criterios de las guías de práctica clínica1,6 (intermitente, persistente leve, persistente moderada, persistente grave), reflejada en la codificación de gravedad incluida en la propia historia clínica. Asimismo, se recogieron todos los episodios registrados de exacerbaciones durante el periodo de seguimiento. La exacerbación se definió como todo evento en el curso natural de la enfermedad caracterizado por la agudización de esta, identificada por un aumento progresivo en la dificultad para respirar, sensación de falta de aire, sibilancias, tos y opresión torácica, o una combinación de todos estos síntomas.
El tratamiento farmacológico dispensado durante el periodo de seguimiento se recogió a partir de los registros procedentes de la dispensación farmacológica de medicamentos, emitida por la aplicación RCMPS de CatSalut.
Se recogió el consumo de recursos sanitarios y no sanitarios asociados al asma durante el periodo de seguimiento. En el caso de los recursos sanitarios, se incluyeron las visitas médicas a Atención Primaria o Especializada, visitas a Urgencias, pruebas realizadas, hospitalizaciones y uso de medicación de rescate. Como recursos no sanitarios se consideró la pérdida de productividad laboral medida en días de incapacidad laboral (días de baja laboral).
Análisis estadísticoLa población de estudio se dividió en 2 grupos: pacientes adherentes (MPR≥80%) y no adherentes (MPR<80%).
Tanto para la población de estudio total como para cada grupo de pacientes, se realizó un análisis descriptivo univariante de las características sociodemográficas y clínicas, así como del uso de recursos, incluyendo valores de media, desviación estándar, intervalo de confianza al 95%, mediana y rango intercuartílico en el caso de variables continuas, y frecuencia en el caso de variables categóricas. La normalidad de la distribución se comprobó con la prueba de Kolmogorov-Smirnov.
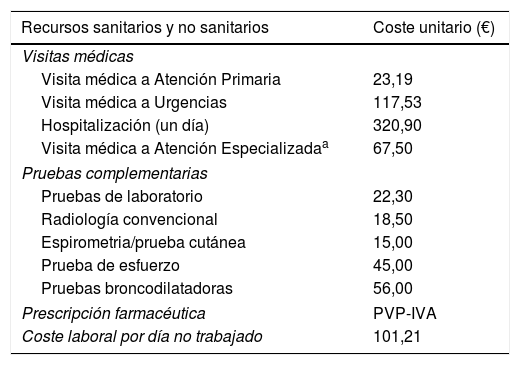
A partir del uso de recursos recogido se cuantificaron los costes sanitarios y no sanitarios. La unidad de producto que sirvió de base para el cálculo final fue el paciente atendido. El coste fue expresado en coste medio por paciente durante todo el periodo de estudio (24 meses), obtenido multiplicando el coste unitario de los recursos sanitarios y no sanitarios por su frecuencia de utilización. El coste unitario se obtuvo a partir de la contabilidad analítica de Badalona Serveis Assistencials S. A., excepto la medicación y los costes indirectos (días de baja laboral) (tabla 1). Las prescripciones se cuantificaron según el precio de venta al público (PVP-IVA) por envase en el momento de la dispensación, incluyendo la aportación del usuario. Los costes indirectos se cuantificaron a partir del salario mínimo interprofesional16.
Coste unitario de recursos sanitarios y no sanitarios evaluados
| Recursos sanitarios y no sanitarios | Coste unitario (€) |
|---|---|
| Visitas médicas | |
| Visita médica a Atención Primaria | 23,19 |
| Visita médica a Urgencias | 117,53 |
| Hospitalización (un día) | 320,90 |
| Visita médica a Atención Especializadaa | 67,50 |
| Pruebas complementarias | |
| Pruebas de laboratorio | 22,30 |
| Radiología convencional | 18,50 |
| Espirometria/prueba cutánea | 15,00 |
| Prueba de esfuerzo | 45,00 |
| Pruebas broncodilatadoras | 56,00 |
| Prescripción farmacéutica | PVP-IVA |
| Coste laboral por día no trabajado | 101,21 |
IVA: impuesto sobre el valor añadido; PVP: precio de venta al público.
Fuente: Contabilidad Analítica Badalona Serveis Assistencials S. A. Año 2013. Instituto Nacional de Estadística.
Las diferencias entre los 2 grupos de pacientes fueron evaluadas mediante la prueba de chi-cuadrado o la de Fisher para las variables categóricas, y mediante la prueba de Wilcoxon o t de Student para las variables continuas. En el caso de los costes las diferencias se evaluaron mediante la prueba de Wilcoxon o la t de Student. Los diferentes componentes del coste se corrigieron mediante un análisis de covarianza ANCOVA utilizando como covariables el sexo, la edad, la comorbilidad general (BUR), el tiempo desde el diagnóstico, la gravedad del asma, el MPR y la presencia de exacerbaciones (procedimiento: estimación de medias marginales, ajuste de Bonferroni).
El análisis estadístico se realizó con el programa estadístico SPSSWIN v17, estableciéndose una significación estadística para valores de p<0,05.
ResultadosDe una población inicial de 97.554 sujetos≥15 años, 75.158 demandaron atención sanitaria durante el periodo de inclusión del estudio (de enero de 2010 a diciembre de 2011). De estos, 5.305 tenían un diagnóstico de asma (prevalencia 5,4%; intervalo de confianza al 95% 4,8-5,9). Finalmente se incluyeron en el análisis 2.303 pacientes que cumplieron todos los criterios de inclusión/exclusión y pudieron seguirse durante el periodo de estudio (fig. 2).
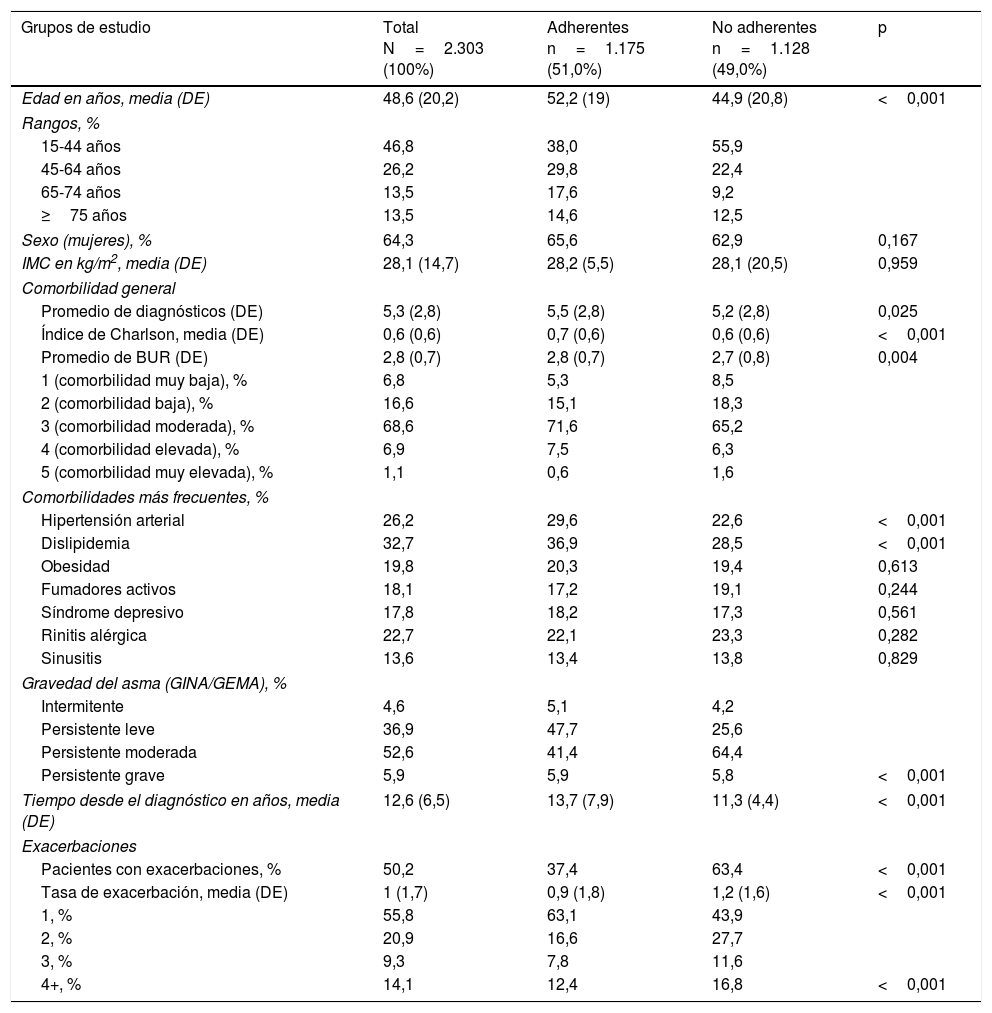
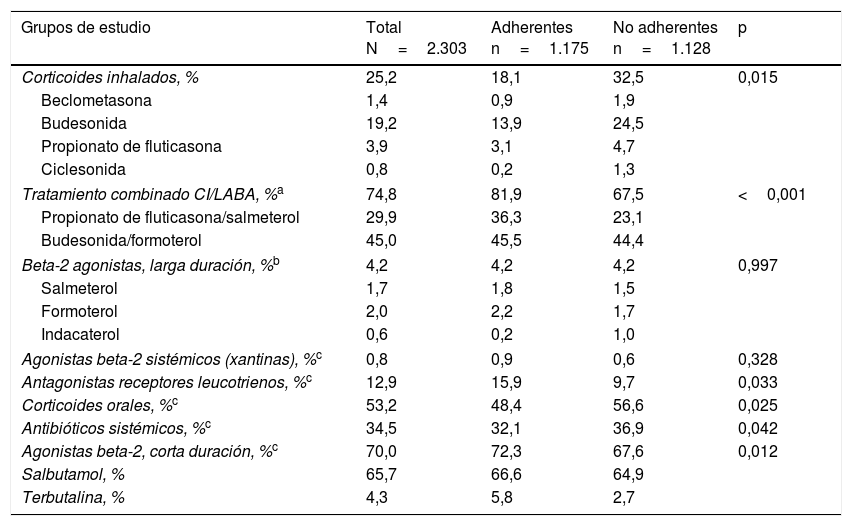
La edad media de los pacientes incluidos fue de 48,6 (20,2) años; un 64,3% eran mujeres. Las comorbilidades más frecuentes fueron la dislipidemia, la hipertensión arterial y la rinitis alérgica. El 52,6% de los pacientes presentaban un asma persistente moderada (tabla 2). El 25,2% de los pacientes incluidos iniciaron tratamiento con CI en monoterapia o en combinación abierta (en diferente dispositivo) con un agonista beta-2 de larga duración (LABA), mientras que el 74,8% lo hicieron en combinación a dosis fija CI/LABA (escalones 3 a 5 guía GEMA1) (tabla 3).
Características basales de la población incluida y presencia de exacerbaciones durante el periodo de estudio
| Grupos de estudio | Total N=2.303 (100%) | Adherentes n=1.175 (51,0%) | No adherentes n=1.128 (49,0%) | p |
|---|---|---|---|---|
| Edad en años, media (DE) | 48,6 (20,2) | 52,2 (19) | 44,9 (20,8) | <0,001 |
| Rangos, % | ||||
| 15-44 años | 46,8 | 38,0 | 55,9 | |
| 45-64 años | 26,2 | 29,8 | 22,4 | |
| 65-74 años | 13,5 | 17,6 | 9,2 | |
| ≥75 años | 13,5 | 14,6 | 12,5 | |
| Sexo (mujeres), % | 64,3 | 65,6 | 62,9 | 0,167 |
| IMC en kg/m2, media (DE) | 28,1 (14,7) | 28,2 (5,5) | 28,1 (20,5) | 0,959 |
| Comorbilidad general | ||||
| Promedio de diagnósticos (DE) | 5,3 (2,8) | 5,5 (2,8) | 5,2 (2,8) | 0,025 |
| Índice de Charlson, media (DE) | 0,6 (0,6) | 0,7 (0,6) | 0,6 (0,6) | <0,001 |
| Promedio de BUR (DE) | 2,8 (0,7) | 2,8 (0,7) | 2,7 (0,8) | 0,004 |
| 1 (comorbilidad muy baja), % | 6,8 | 5,3 | 8,5 | |
| 2 (comorbilidad baja), % | 16,6 | 15,1 | 18,3 | |
| 3 (comorbilidad moderada), % | 68,6 | 71,6 | 65,2 | |
| 4 (comorbilidad elevada), % | 6,9 | 7,5 | 6,3 | |
| 5 (comorbilidad muy elevada), % | 1,1 | 0,6 | 1,6 | |
| Comorbilidades más frecuentes, % | ||||
| Hipertensión arterial | 26,2 | 29,6 | 22,6 | <0,001 |
| Dislipidemia | 32,7 | 36,9 | 28,5 | <0,001 |
| Obesidad | 19,8 | 20,3 | 19,4 | 0,613 |
| Fumadores activos | 18,1 | 17,2 | 19,1 | 0,244 |
| Síndrome depresivo | 17,8 | 18,2 | 17,3 | 0,561 |
| Rinitis alérgica | 22,7 | 22,1 | 23,3 | 0,282 |
| Sinusitis | 13,6 | 13,4 | 13,8 | 0,829 |
| Gravedad del asma (GINA/GEMA), % | ||||
| Intermitente | 4,6 | 5,1 | 4,2 | |
| Persistente leve | 36,9 | 47,7 | 25,6 | |
| Persistente moderada | 52,6 | 41,4 | 64,4 | |
| Persistente grave | 5,9 | 5,9 | 5,8 | <0,001 |
| Tiempo desde el diagnóstico en años, media (DE) | 12,6 (6,5) | 13,7 (7,9) | 11,3 (4,4) | <0,001 |
| Exacerbaciones | ||||
| Pacientes con exacerbaciones, % | 50,2 | 37,4 | 63,4 | <0,001 |
| Tasa de exacerbación, media (DE) | 1 (1,7) | 0,9 (1,8) | 1,2 (1,6) | <0,001 |
| 1, % | 55,8 | 63,1 | 43,9 | |
| 2, % | 20,9 | 16,6 | 27,7 | |
| 3, % | 9,3 | 7,8 | 11,6 | |
| 4+, % | 14,1 | 12,4 | 16,8 | <0,001 |
BUR: bandas de utilización de recursos; DE: desviación estándar; GEMA: Guía Española para el Manejo del Asma; GINA: Global Initiative for Asthma; IMC: índice de masa corporal.
Tratamiento inicial prescrito
| Grupos de estudio | Total N=2.303 | Adherentes n=1.175 | No adherentes n=1.128 | p |
|---|---|---|---|---|
| Corticoides inhalados, % | 25,2 | 18,1 | 32,5 | 0,015 |
| Beclometasona | 1,4 | 0,9 | 1,9 | |
| Budesonida | 19,2 | 13,9 | 24,5 | |
| Propionato de fluticasona | 3,9 | 3,1 | 4,7 | |
| Ciclesonida | 0,8 | 0,2 | 1,3 | |
| Tratamiento combinado CI/LABA, %a | 74,8 | 81,9 | 67,5 | <0,001 |
| Propionato de fluticasona/salmeterol | 29,9 | 36,3 | 23,1 | |
| Budesonida/formoterol | 45,0 | 45,5 | 44,4 | |
| Beta-2 agonistas, larga duración, %b | 4,2 | 4,2 | 4,2 | 0,997 |
| Salmeterol | 1,7 | 1,8 | 1,5 | |
| Formoterol | 2,0 | 2,2 | 1,7 | |
| Indacaterol | 0,6 | 0,2 | 1,0 | |
| Agonistas beta-2 sistémicos (xantinas), %c | 0,8 | 0,9 | 0,6 | 0,328 |
| Antagonistas receptores leucotrienos, %c | 12,9 | 15,9 | 9,7 | 0,033 |
| Corticoides orales, %c | 53,2 | 48,4 | 56,6 | 0,025 |
| Antibióticos sistémicos, %c | 34,5 | 32,1 | 36,9 | 0,042 |
| Agonistas beta-2, corta duración, %c | 70,0 | 72,3 | 67,6 | 0,012 |
| Salbutamol, % | 65,7 | 66,6 | 64,9 | |
| Terbutalina, % | 4,3 | 5,8 | 2,7 | |
CI: corticoide inhalado; LABA: agonista beta-2 de larga duración.
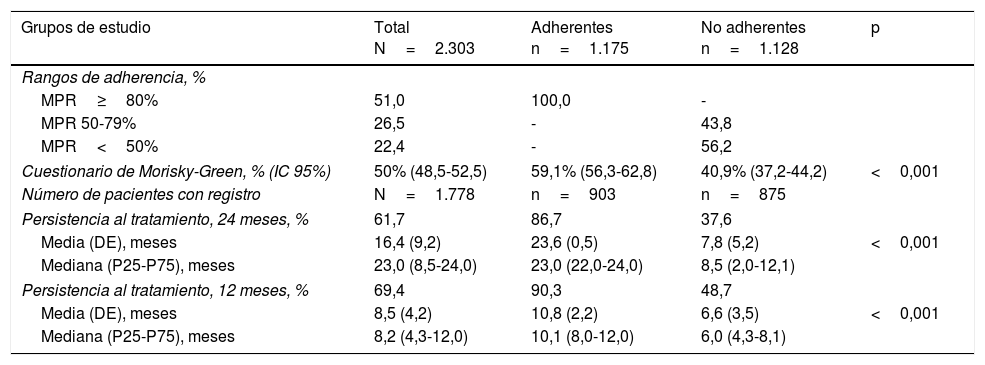
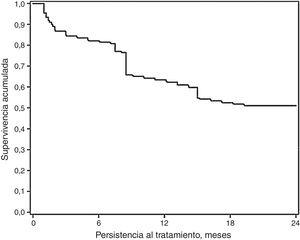
Un 51% de los pacientes incluidos en el estudio fueron adherentes al tratamiento con CI (MPR≥80%). Un 69,4% de los pacientes mostraron persistencia al tratamiento a los 12 meses, siendo el tiempo medio de persistencia de 8,5 (4,2) meses. A los 24 meses, un 61,7% de los pacientes mostraron persistencia al tratamiento, con un tiempo medio de 16,4 (9,2) meses (tabla 4 y fig. 3).
Adherencia y persistencia al tratamiento
| Grupos de estudio | Total N=2.303 | Adherentes n=1.175 | No adherentes n=1.128 | p |
|---|---|---|---|---|
| Rangos de adherencia, % | ||||
| MPR≥80% | 51,0 | 100,0 | - | |
| MPR 50-79% | 26,5 | - | 43,8 | |
| MPR<50% | 22,4 | - | 56,2 | |
| Cuestionario de Morisky-Green, % (IC 95%) | 50% (48,5-52,5) | 59,1% (56,3-62,8) | 40,9% (37,2-44,2) | <0,001 |
| Número de pacientes con registro | N=1.778 | n=903 | n=875 | |
| Persistencia al tratamiento, 24 meses, % | 61,7 | 86,7 | 37,6 | |
| Media (DE), meses | 16,4 (9,2) | 23,6 (0,5) | 7,8 (5,2) | <0,001 |
| Mediana (P25-P75), meses | 23,0 (8,5-24,0) | 23,0 (22,0-24,0) | 8,5 (2,0-12,1) | |
| Persistencia al tratamiento, 12 meses, % | 69,4 | 90,3 | 48,7 | |
| Media (DE), meses | 8,5 (4,2) | 10,8 (2,2) | 6,6 (3,5) | <0,001 |
| Mediana (P25-P75), meses | 8,2 (4,3-12,0) | 10,1 (8,0-12,0) | 6,0 (4,3-8,1) | |
DE: desviación estándar; IC: intervalo de confianza; MPR: tasa de posesión de medicación; P: percentil.
Analizando las características demográficas y clínicas por grupos (pacientes adherentes y no adherentes), los pacientes clasificados como no adherentes presentaron una menor edad media (44,9 vs. 52,2 años), un menor tiempo desde el diagnóstico (11,3 vs. 13,7 años), un menor número de comorbilidades y una mayor gravedad del asma respecto a los pacientes adherentes, siendo estas diferencias estadísticamente significativas (tabla 2). Respecto al tratamiento, un 81,9% de los pacientes adherentes recibieron tratamiento CI/LABA frente a un 67,5% de los pacientes no adherentes (p<0,001) (tabla 3). Los pacientes no adherentes mostraron una menor persistencia al tratamiento que los pacientes adherentes tanto a los 12 como a los 24 meses (p<0,001) (tabla 4).
Alrededor de un 77% de los pacientes de ambos grupos tenían al menos un registro electrónico disponible del cuestionario Morisky-Green. De acuerdo con los resultados de este cuestionario, un 40,9% de los pacientes no adherentes consideraron que eran adherentes al tratamiento con base en la respuesta del cuestionario. En el caso de los pacientes adherentes, un 59,1% se consideró adherente, indicando una baja relación entre ambas medidas de adherencia (tabla 4).
En relación con las exacerbaciones, un 63,4% de los pacientes no adherentes tuvieron al menos una exacerbación durante el periodo de estudio respecto al 37,4% de los adherentes. La tasa de exacerbaciones por paciente también fue mayor entre los pacientes no adherentes (1,2 vs. 0,9 exacerbaciones/año, p<0,001) (tabla 2).
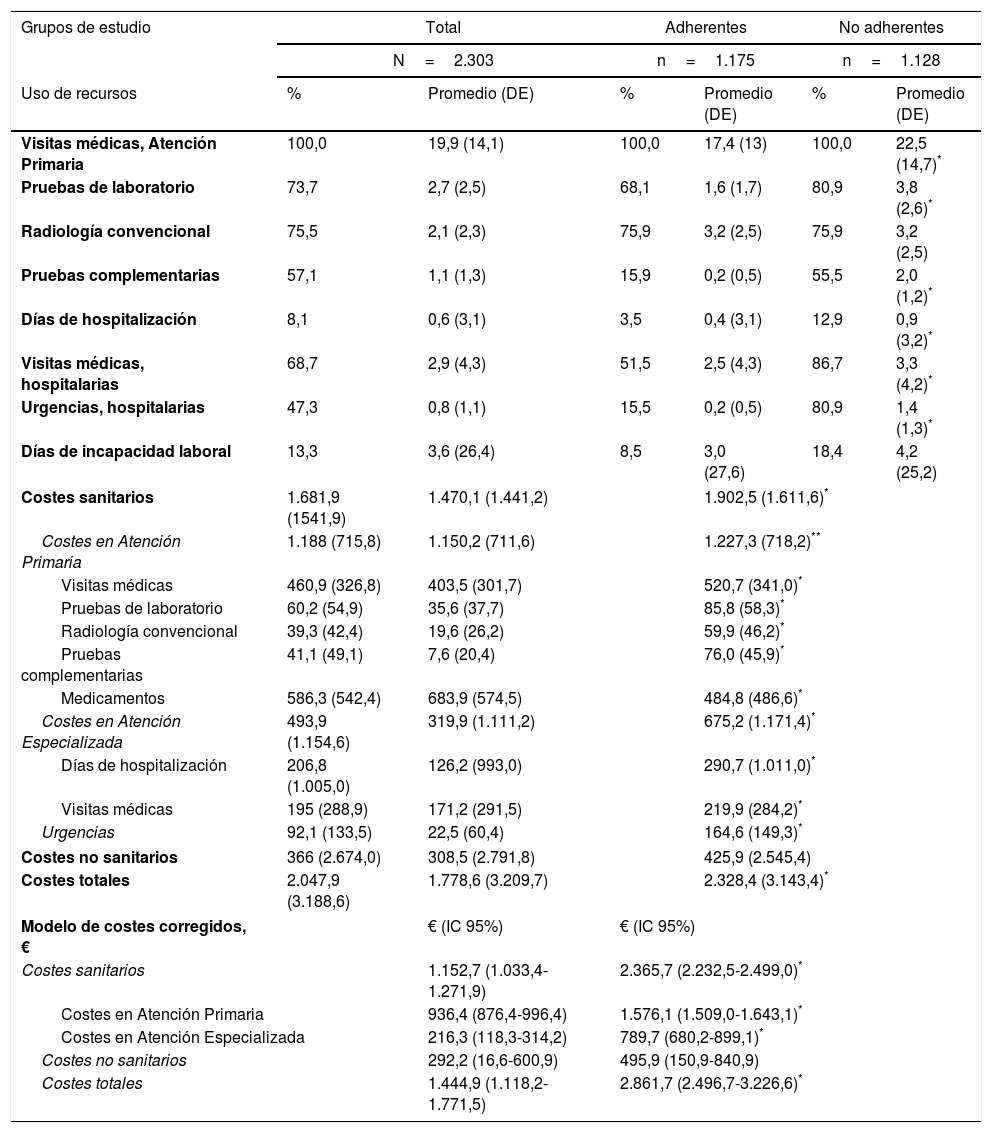
La tabla 5 recoge el uso de recursos sanitarios y no sanitarios, así como los costes asociados para los 2 grupos de pacientes. Los pacientes no adherentes mostraron un mayor consumo de recursos sanitarios que los adherentes, especialmente visitas a Atención Primaria (22,5 vs. 17,4), Especializada (3,3 vs. 2,5) y Urgencias (1,4 vs. 0,2), siendo estas diferencias estadísticamente significativas. Una mayor proporción de pacientes no adherentes fueron hospitalizados (12,9 vs. 3,5%), siendo también mayor el número de días de hospitalización en los pacientes no adherentes (0,9 vs. 0,4, p<0,001). Asimismo, un mayor número de pacientes no adherentes (18,4 vs. 8,5%) presentaron una pérdida de productividad, siendo también mayor los días de incapacidad laboral (4,2 vs. 3,0) frente a los pacientes adherentes, si bien estas diferencias no fueron estadísticamente significativas.
Uso de recursos sanitarios y no sanitarios y costes asociados
| Grupos de estudio | Total | Adherentes | No adherentes | |||
|---|---|---|---|---|---|---|
| N=2.303 | n=1.175 | n=1.128 | ||||
| Uso de recursos | % | Promedio (DE) | % | Promedio (DE) | % | Promedio (DE) |
| Visitas médicas, Atención Primaria | 100,0 | 19,9 (14,1) | 100,0 | 17,4 (13) | 100,0 | 22,5 (14,7)* |
| Pruebas de laboratorio | 73,7 | 2,7 (2,5) | 68,1 | 1,6 (1,7) | 80,9 | 3,8 (2,6)* |
| Radiología convencional | 75,5 | 2,1 (2,3) | 75,9 | 3,2 (2,5) | 75,9 | 3,2 (2,5) |
| Pruebas complementarias | 57,1 | 1,1 (1,3) | 15,9 | 0,2 (0,5) | 55,5 | 2,0 (1,2)* |
| Días de hospitalización | 8,1 | 0,6 (3,1) | 3,5 | 0,4 (3,1) | 12,9 | 0,9 (3,2)* |
| Visitas médicas, hospitalarias | 68,7 | 2,9 (4,3) | 51,5 | 2,5 (4,3) | 86,7 | 3,3 (4,2)* |
| Urgencias, hospitalarias | 47,3 | 0,8 (1,1) | 15,5 | 0,2 (0,5) | 80,9 | 1,4 (1,3)* |
| Días de incapacidad laboral | 13,3 | 3,6 (26,4) | 8,5 | 3,0 (27,6) | 18,4 | 4,2 (25,2) |
| Costes sanitarios | 1.681,9 (1541,9) | 1.470,1 (1.441,2) | 1.902,5 (1.611,6)* | |||
| Costes en Atención Primaria | 1.188 (715,8) | 1.150,2 (711,6) | 1.227,3 (718,2)** | |||
| Visitas médicas | 460,9 (326,8) | 403,5 (301,7) | 520,7 (341,0)* | |||
| Pruebas de laboratorio | 60,2 (54,9) | 35,6 (37,7) | 85,8 (58,3)* | |||
| Radiología convencional | 39,3 (42,4) | 19,6 (26,2) | 59,9 (46,2)* | |||
| Pruebas complementarias | 41,1 (49,1) | 7,6 (20,4) | 76,0 (45,9)* | |||
| Medicamentos | 586,3 (542,4) | 683,9 (574,5) | 484,8 (486,6)* | |||
| Costes en Atención Especializada | 493,9 (1.154,6) | 319,9 (1.111,2) | 675,2 (1.171,4)* | |||
| Días de hospitalización | 206,8 (1.005,0) | 126,2 (993,0) | 290,7 (1.011,0)* | |||
| Visitas médicas | 195 (288,9) | 171,2 (291,5) | 219,9 (284,2)* | |||
| Urgencias | 92,1 (133,5) | 22,5 (60,4) | 164,6 (149,3)* | |||
| Costes no sanitarios | 366 (2.674,0) | 308,5 (2.791,8) | 425,9 (2.545,4) | |||
| Costes totales | 2.047,9 (3.188,6) | 1.778,6 (3.209,7) | 2.328,4 (3.143,4)* | |||
| Modelo de costes corregidos, € | € (IC 95%) | € (IC 95%) | ||||
| Costes sanitarios | 1.152,7 (1.033,4-1.271,9) | 2.365,7 (2.232,5-2.499,0)* | ||||
| Costes en Atención Primaria | 936,4 (876,4-996,4) | 1.576,1 (1.509,0-1.643,1)* | ||||
| Costes en Atención Especializada | 216,3 (118,3-314,2) | 789,7 (680,2-899,1)* | ||||
| Costes no sanitarios | 292,2 (16,6-600,9) | 495,9 (150,9-840,9) | ||||
| Costes totales | 1.444,9 (1.118,2-1.771,5) | 2.861,7 (2.496,7-3.226,6)* | ||||
DE: desviación estándar; IC: intervalo de confianza.
El mayor consumo de recursos entre los pacientes no adherentes se tradujo en un mayor coste por paciente. En el modelo de costes ajustado por las principales covariables, el coste de seguimiento durante el periodo de estudio de un paciente no adherente fue de 2.861,7€ (2.496,7-3.226,6€) frente a 1.444,9€ (1.118,2-1.771,5€) en el caso de paciente adherente (p<0,001), lo que supone un coste anual/paciente de 1.431 y 722€, respectivamente.
DiscusiónDe acuerdo con los resultados de este estudio longitudinal retrospectivo realizado en condiciones de práctica clínica habitual, la falta de adherencia al tratamiento con CI (en monoterapia o combinado con un LABA) se relacionó con peores resultados clínicos, medidos en exacerbaciones, así como con un aumento del consumo de recursos y costes asociados. Hasta la fecha, la evidencia publicada en España acerca de la tasa de adherencia en pacientes asmáticos en condiciones reales, así como su relación con el consumo de recursos es escasa, lo que puede conferir a este estudio un cierto atractivo conceptual y metodológico.
Un 51% de los pacientes del estudio mostraron adherencia al tratamiento, con una persistencia media de 16 meses en el periodo de estudio (24 meses). Esta cifra está dentro del rango reportado en estudios previos, encontrándose incluso dentro del rango alto. Así, estudios previos reportan una adherencia al tratamiento con CI que oscila entre 15-54% en adultos y entre un 20-34% en niños9. Los pacientes no adherentes en el presente estudio eran más jóvenes, con un menor tiempo desde el diagnóstico, menos comorbilidades y una mayor gravedad del asma respecto a los pacientes adherentes. En la literatura, la edad, el género, la gravedad de la enfermedad y la presencia de comorbilidades se han identificado como variables relacionadas con la adherencia en el asma. En cuanto a la edad, si bien en el estudio de Krigsman et al.17 los pacientes de mayor edad presentaban una menor tasa de adherencia, en el estudio realizado por Williams et al.18, la menor edad fue un predictor de peor adherencia, en línea con los resultados aquí obtenidos. Por otro lado, en el estudio publicado por Engelkes et al.19 realizado en niños, las características de los pacientes adherentes eran compatibles con las de mayor gravedad de la enfermedad, lo que podría evidenciar que la adherencia está dirigida por la necesidad de tratamiento. Los resultados del presente estudio muestran una relación opuesta, pues los pacientes adherentes presentaron una menor gravedad de la enfermedad (persistente moderado) frente a los no adherentes (persistente grave). En este caso, la falta de adherencia podría estar impactando la gravedad de la enfermedad, si bien esta hipótesis no es posible demostrarla debido al diseño del estudio, y el tratamiento recibido podría estar influyendo en esta asociación.
Cabe destacar que un mayor número de pacientes adherentes estaba en tratamiento con combinación a dosis fija CI/LABA, mientras que un porcentaje mayor de pacientes no adherentes estaban en tratamiento con CI en monoterapia o en combinación abierta CI+LABA. Estudios previos indican que la adherencia a largo plazo de CI/LABA es superior tanto a CI en monoterapia19–21 como en asociación abierta21,22. Se han identificado diferentes motivos para este hecho. Por un lado, la adición del tratamiento broncodilatador (LABA) podría proporcionar al paciente un beneficio sintomático inmediato, lo que haría que tomase la medicación de forma más regular20. Por otro lado, la combinación a dosis fija podría simplificar el régimen de tratamiento comparado con el uso de 2 tratamientos por separado con inhaladores diferentes, facilitando la adherencia22.
Los pacientes no adherentes presentaron una mayor tasa de exacerbaciones, así como un mayor consumo de recursos sanitarios, lo que se tradujo en un coste total 2 veces mayor en comparación con los pacientes adherentes. Estos resultados son consistentes con estudios previos realizados en otros países9,11,20,22, donde la falta de adherencia a CI se asoció con un mal control de la enfermedad, un aumento de la tasa de exacerbaciones, así como un incremento del consumo de recursos y los costes, estimándose que la falta de adherencia es responsable de un 60% de las hospitalizaciones por asma20. Si bien un porcentaje mayor de pacientes no adherentes precisaron una baja laboral debido al asma, no se observaron diferencias estadísticamente significativas en el número de días de baja ni en los costes no sanitarios asociados.
El conocimiento de la adherencia en condiciones de práctica clínica habitual y su relación con resultados tanto clínicos como económicos podría tener implicaciones en el manejo del paciente asmático. En la literatura23,24 se han descrito diferentes intervenciones que podrían tener un impacto sobre la adherencia, como visitas de seguimiento presenciales o telefónicas para revisar el correcto uso de la medicación, simplificación de los regímenes de tratamiento, aplicaciones informáticas, así como programas educacionales y motivacionales.
Este estudio presenta una serie de limitaciones que deben ser tenidas en cuenta. En primer lugar, el propio diseño retrospectivo del estudio a través del análisis de registros médicos informatizados puede hacer que haya un infrarregistro tanto de los pacientes asmáticos como de los recursos consumidos, lo que podría estar infraestimando los resultados obtenidos. Por otro lado, la medida de adherencia utilizada se basa en la medicación dispensada, lo que puede no reflejar la adherencia real. Así, la dispensación no garantiza que el paciente tome la medicación ni, en el caso de tratamientos inhalados, que la técnica utilizada sea correcta. Además, el punto de corte de 80%, si bien ha demostrado ser útil y razonablemente preciso en estudios previos9, su cálculo deriva de otras enfermedades crónicas como la diabetes o la hipertensión, por lo que podría no ser necesariamente el mismo en el asma.
En conclusión, la falta de adherencia se relacionó con un incremento en la tasa de exacerbaciones y un aumento de los recursos sanitarios y los costes asociados. Estrategias encaminadas a mejorar la adherencia podrían contribuir a reducir la carga económica para los sistemas sanitarios.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónGlaxoSmithKline S. A.
Conflicto de interesesLa autora A. Huerta es empleada y posee opciones de acciones de GlaxoSmithKline. El resto de los autores recibieron honorarios durante la realización del estudio y declaran no tener ningún otro conflicto de intereses adicional.