Valorar los parámetros perioperatorios y los resultados clínicos y radiológicos de la cirugía de revisión de las prótesis de superficie de hombro recambiadas hacia prótesis invertida no cementada con vástago corto.
Material y métodosEntre 2005 y 2012, se realizaron 23 revisiones de prótesis de superficie de hombro a prótesis invertidas. La edad media fue 70,3 años±11,95. Un 82,6% (19/23) de los recambios se realizaron por rotura secundaria del manguito rotador; 13,04% (3/23) por aflojamiento aséptico del componente glenoideo más insuficiencia del manguito y 4,35% (1/23) por fractura periprotésica. Se documentaron: necesidad de ventanas humerales y aloinjerto estructural, duración del procedimiento, pérdidas hemáticas, transfusiones y fracturas intraoperatorias. Seguimiento mínimo de 25 meses.
ResultadosEn ninguno de los casos se necesitó realizar una ventana humeral para la extracción del implante de superficie, así como tampoco aloinjerto estructural. En 8,69% (2/23) de los casos se requirió aloinjerto para reconstrucción glenoidea. La duración del procedimiento fue 113,35±21,30 min. Las pérdidas hemáticas intraoperatorias fueron 374±245,09mls. Se requirió hemotransfusión en un caso. Se produjo una fractura intraoperatoria. El Constant mejoró de 17,32 a 59,78 (ajustado por sexo y edad, 84). La satisfacción general aumentó de 1,37 a 8,04. El recorrido articular aumentó 79,57° en elevación anterior; 72,88° en abducción; 38,06° en rotación interna; y 13,57° en rotación externa. No hubo evidencia de radiolucencias, hundimientos, ni resorción ósea.
ConclusiónLa artroplastia de revisión de las prótesis de superficie de hombro recambiadas hacia prótesis invertida no cementada con vástago corto ofrece buenos resultados clínicos y radiológicos, representando una técnica con complejidades intraoperatorias mínimas.
Nivel de evidenciaIV, serie de casos.
To assess the surgical parameters and the clinical and radiological outcomes of revisions of resurfacing shoulder arthroplasty to non-cemented short-stem reverse total shoulder arthroplasty.
Material and methodsA total of 23 revisions from resurfacing shoulder arthroplasty to reverse total shoulder arthroplasty were performed. The mean age was 70.3±11.95 years. The patients included 82.6% (19/23) revised for cuff failure; 13.04% (3/23) cuff failure and aseptic loosening, and 4.35% (1/23) peri-prosthetic fracture. The need for humeral osteotomy or structural allograft, operation length, blood loss, blood transfusions and intraoperative fractures were recorded. Minimum follow-up 25 months.
ResultsNo humeral osteotomy or humeral structural allograft was required, and 2/23 (8.69%) required allograft for glenoid reconstruction. The mean operation time was 113.35±21.30minutes. Intra-operative blood loss was 374±245.09 mls. Blood transfusion was required in one case. Intra-operative fracture occurred in 1 case. The Constant score improved from 17.32 to 59.78 (age/sex adjusted, 84). Overall satisfaction improved from 1.37 to 8.04. The range of motion increased 79.57° in forward elevation; 72.88° in abduction; 38.06° in internal rotation; and 13.57° in external rotation. There was no evidence of radiolucency, subsidence, or bone resorption.
ConclusionRevisions of resurfacing implants to non-cemented short-stem reverse prosthesis show good clinical and radiological outcomes, with minimal intra-operative complexities.
Level of evidenceIV, case series.
La indicación más frecuente para la cirugía de revisión de una prótesis de hombro es la rotura secundaria e insuficiencia del manguito rotador1. La ausencia del efecto depresor del manguito sobre la cabeza humeral condiciona un ascenso de la misma, lo cual finalmente se traduce en conflicto subacromial, dolor e impotencia funcional. Dichos motivos representan finalmente la indicación para la artroplastia de revisión.
Una artroplastia de hombro de revisión representa un procedimiento complejo con potenciales complicaciones. La pérdida del stock óseo tanto a nivel de la diáfisis humeral como a nivel de la glenoides, la afectación de las partes blandas y los pormenores técnicos relacionados con la extracción de los implantes, hacen que la técnica sea muy demandante.
Cuando una prótesis de hombro de superficie fracasa, la artroplastia de revisión hacia una prótesis anatómica o invertida solo supone la extracción del implante de superficie de la cabeza del húmero. El hecho de que la prótesis de superficie carezca de vástago evita la necesidad obligada de realizar un sarcófago a nivel de la diáfisis humeral. Asimismo, el hecho de que no sea necesaria la cementación de la prótesis de superficie permite la preservación del stock óseo y la anatomía del húmero2.
Los resultados de las artroplastias de hombro de revisión hacia prótesis anatómicas son decepcionantes3,4. Se han descrito buenos resultados clínicos a medio plazo con el uso de la prótesis invertida de hombro como implante primario en la artropatía secundaria a insuficiencia del manguito rotador5–7. Diversos estudios han demostrado que la prótesis invertida representa una alternativa que puede ofrecer una mejoría del dolor y de la función articular, cuando se emplea como implante de revisión8–10. A pesar de que los resultados de la prótesis invertida como implante de revisión son inferiores a los resultados que se obtienen cuando se emplea como implante primario11; y a pesar de que la información respecto a los resultados a largo plazo es aún muy limitada12; la prótesis invertida de hombro es considerada actualmente como la mejor alternativa en la cirugía de revisión10.
La tasa de complicaciones reportadas en relación con las artroplastia de hombro de revisión hacia prótesis invertida oscila en torno a 36-48%13–15. Estas complicaciones están en relación con la duración de los procedimientos quirúrgicos, con la necesidad de extraer un vástago humeral bien fijado (bien sea cementado o no cementado) y con la necesidad de lidiar con una importante afectación del stock óseo, situaciones que finalmente pueden ir en detrimento del resultado clínico16. La artroplastia de revisión de una prótesis de superficie de hombro, que carece de vástago y que no implica la obligada utilización de cemento, puede considerarse como un procedimiento quirúrgico menos agresivo.
Las ventajas que puede comportar la prótesis de superficie de hombro son: se evita el «stress shielding» en la cortical lateral del húmero, se preserva la diáfisis humeral para futuras artroplastias de revisión y supone un menor riesgo de que se produzcan fracturas periprotésicas diafisarias17. Cabe destacar también que la prótesis de superficie de hombro no altera la anatomía metafisaria del húmero, a diferencia de lo que ocurre con las prótesis anatómicas con vástago17.
El propósito del presente estudio fue valorar los parámetros perioperatorios y los resultados clínicos y radiológicos de la cirugía de revisión de las prótesis de superficie de hombro recambiadas hacia prótesis invertidas.
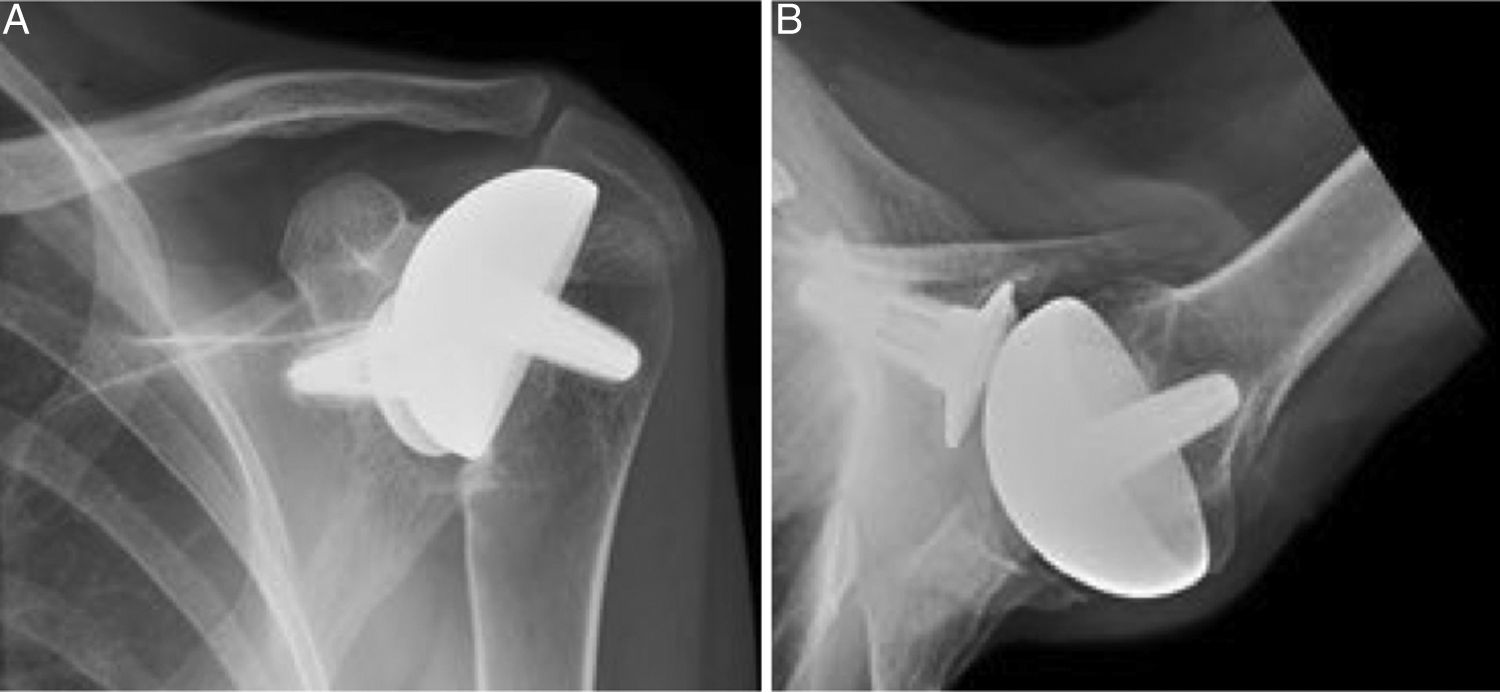
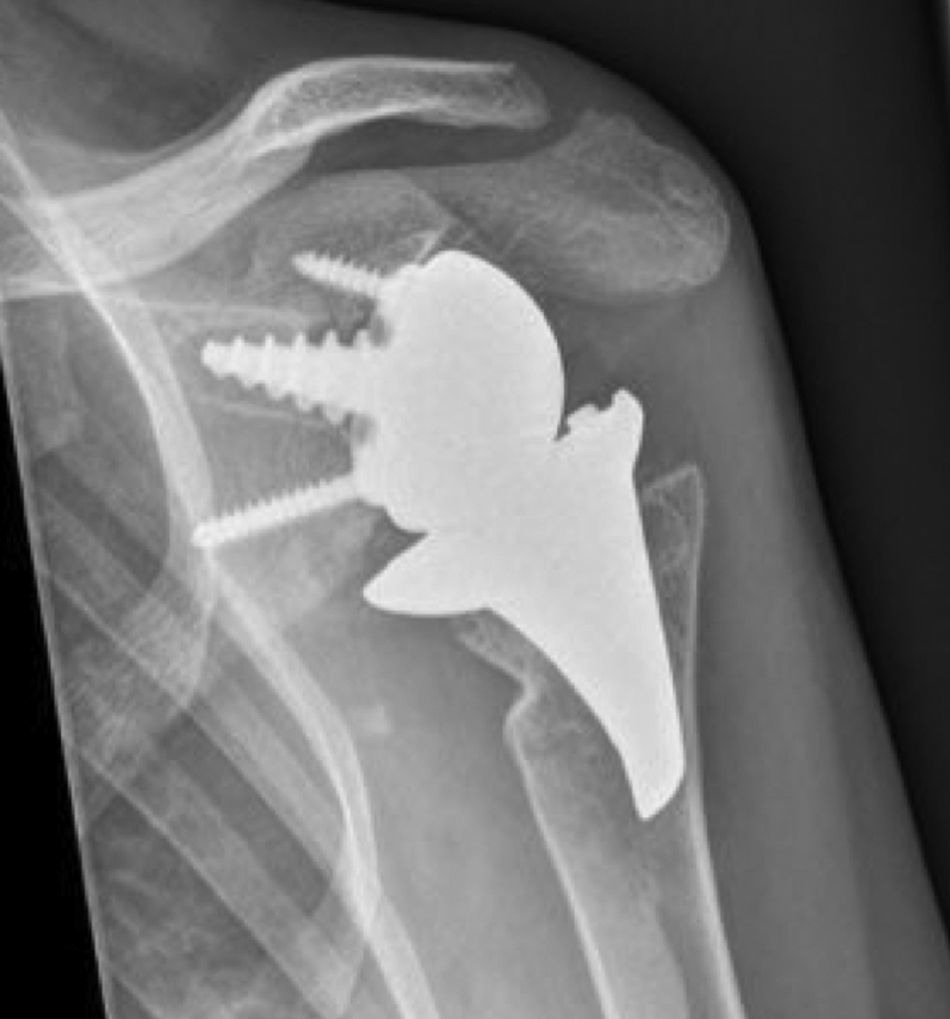
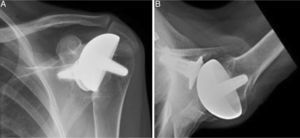
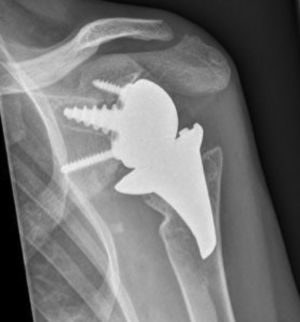
Materiales y métodosEntre 2005 y 2012, 23 recambios de prótesis de superficie de hombro hacia prótesis invertida no cementada con vástago corto se llevaron a cabo por el cirujano senior OL en «Reading Shoulder Unit» (Royal Berkshire Hospital and Berkshire Indepent Hospital), Reino Unido. Se incluyeron pacientes de ambos sexos, y cuyo implante primario hubiese sido una prótesis de superficie de hombro Copeland® (Biomet, Swindon, Reino Unido), recambiada hacia una prótesis invertida Verso® (Innovative Design Orthopaedics, Londres, Reino Unido [anteriormente, Biomet, Swindon, Reino Unido]). Para los propósitos de este estudio, se excluyeron aquellos casos en los que el recambio partió de un implante primario con vástago, o de una prótesis invertida recambiada hacia otra prótesis invertida. La edad media fue de 70,3±11,95 años. Fueron 19 mujeres y 4 hombres. Las indicaciones para el implante primario (prótesis de superficie) se encuentran reflejadas en la tabla 1. Todas las prótesis primarias de superficie era Copeland®: 18 hemiartroplastias y 5 artroplastias totales. El seguimiento medio tras la revisión fue de 43,4 meses (rango, 25 meses a 8 años y 5 meses). En el 86,6% (19/23) de los casos la indicación para la artroplastia de revisión fue rotura secundaria e insuficiencia del manguito rotador. Un 13,04% (3/23) fueron recambiados por aflojamiento aséptico más insuficiencia del manguito rotador (figs 1A y 1B); y 4,35% (1/23) de los recambios se llevaron a cabo tras una fractura periprotésica. Las indicaciones para la artroplastia de revisión hacia prótesis invertida se encuentran reflejadas en la tabla 2. La prótesis invertida de hombro empleada en todos los casos fue el sistema Verso® (fig. 2).
Indicaciones de las prótesis de superficie
| Indicación | n=23 | |
|---|---|---|
| Hemiartroplastia de superficie de la cabeza del húmero | Prótesis total con implante de superficie | |
| Artrosis primaria | 14 | 4 |
| Artritis reumatoide | 2 | 1 |
| Necrosis avascular | 1 | 0 |
| Secuela de fractura | 1 | 0 |
| Artropatía por insuficiencia del manguito | 1* | 0 |
| Total | 18 | 5 |
* Artroplastia de superficie de hombro, por artropatía secundaria a insuficiencia del manguito rotador.
Radiografías de hombro izquierdo de mujer de 45 años de edad (artritis reumatoide juvenil), A) anteroposterior y B) axilar en las que se aprecia artroplastia total de superficie de hombro Copeland®, previa a cirugía de revisión por rotura secundaria del manguito rotador y aflojamiento del componente glenoideo.
Indicaciones para la artroplastia de revisión hacia prótesis invertida no cementada con vástago corto
| Indicación | n=23 | |
|---|---|---|
| Hemiartroplastia de superficie de la cabeza del húmero | Prótesis total con implante de superficie | |
| Insuficiencia secundaria del manguito rotador | 18 | 1 |
| Insuficiencia del manguito + aflojamiento aséptico | 0 | 3 |
| Insuficiencia del manguito + fractura periprotésica | 0 | 1 |
| Total | 18 | 5 |
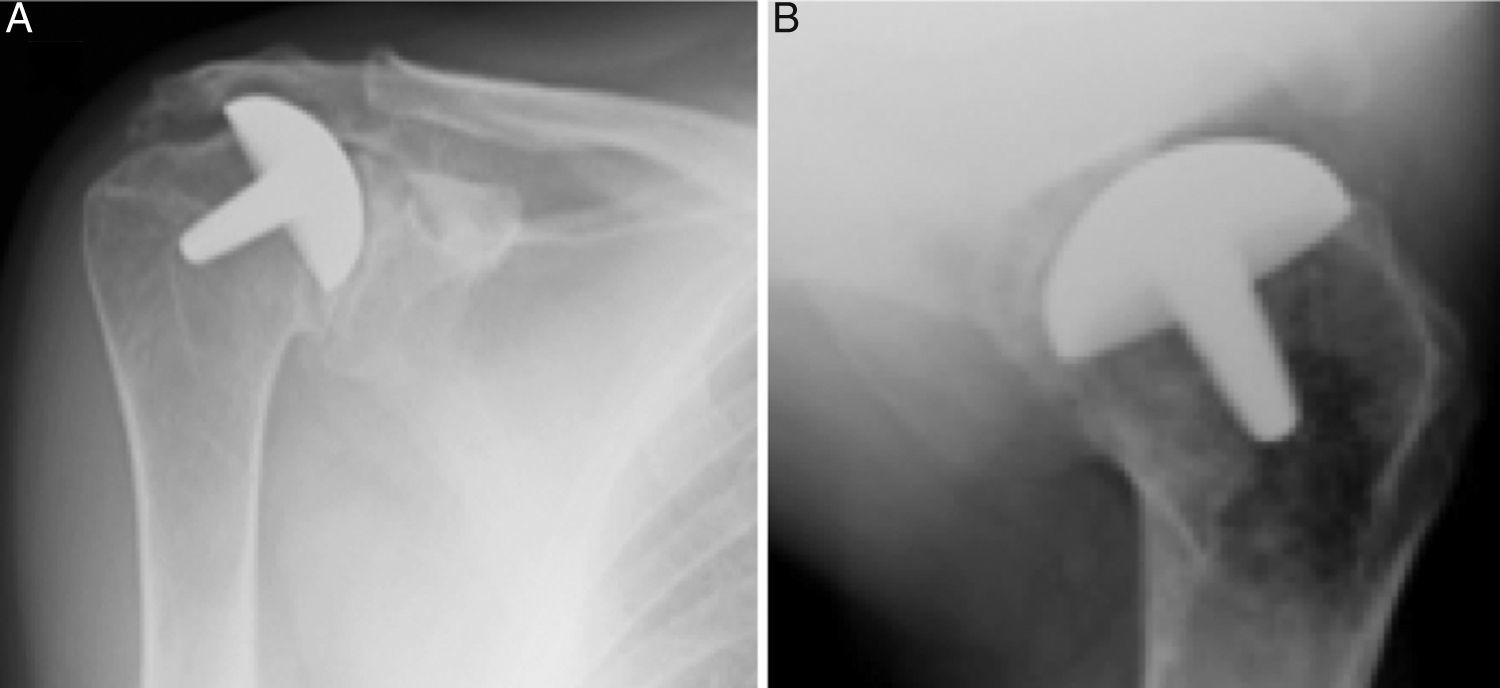
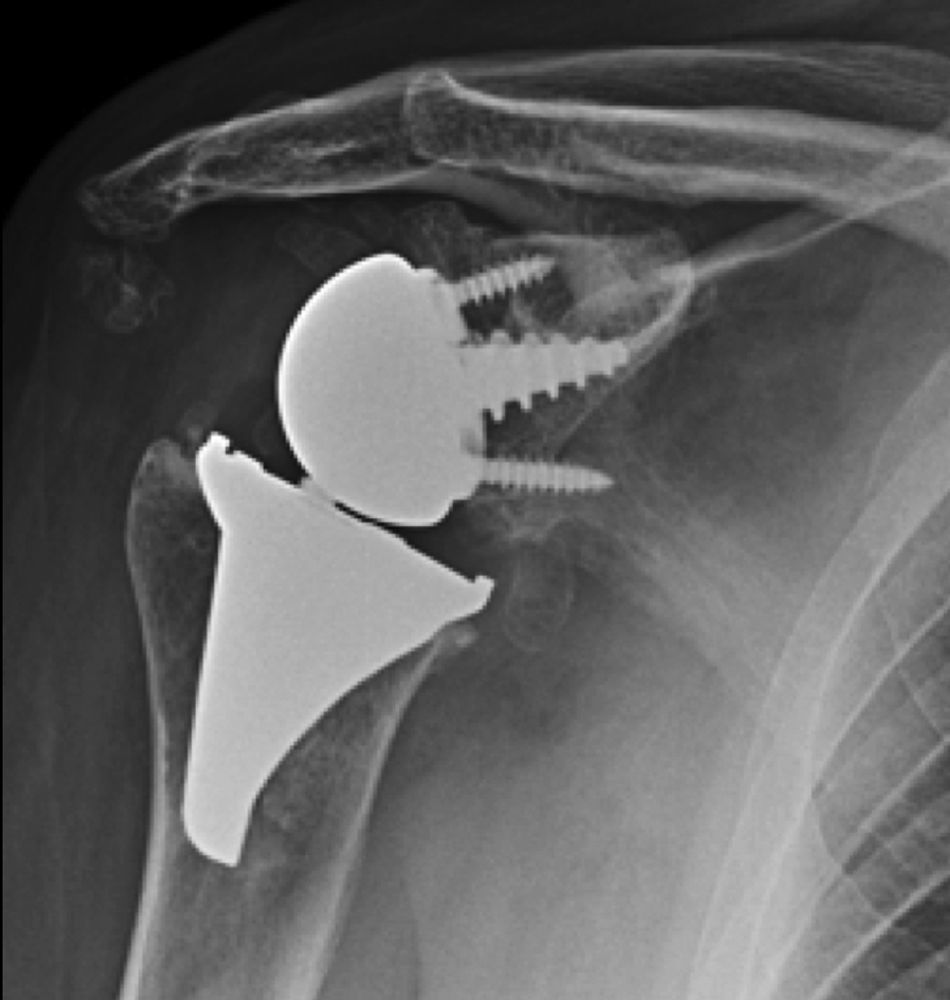
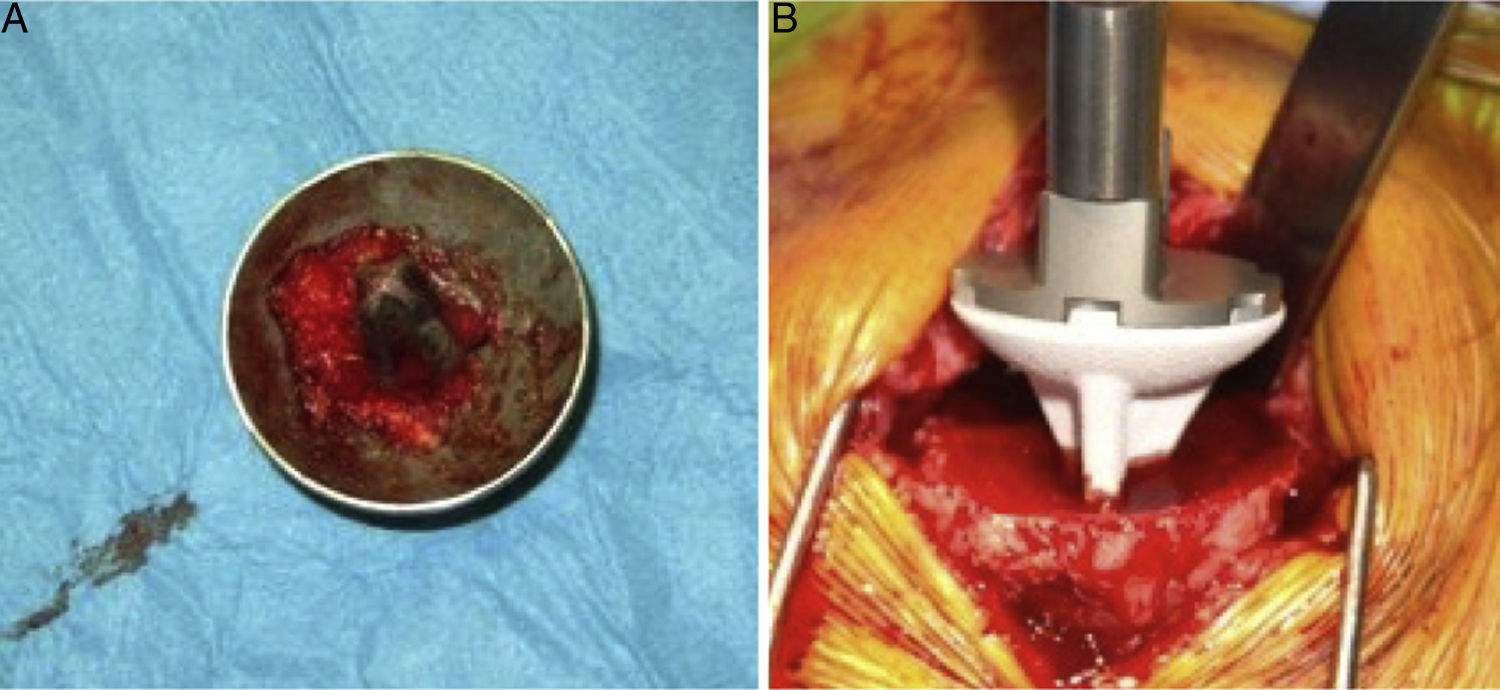
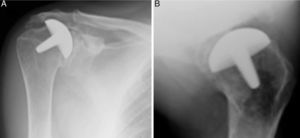
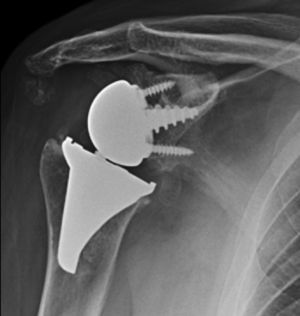
El abordaje quirúrgico (Neviaser MacKenzie)18 que se empleó para la implantación del implante primario (prótesis de superficie de hombro [figs 3A y 3B]) fue el mismo que se empleó en la artroplastia de revisión (sistema Verso® de prótesis invertida de hombro [fig. 4]). En todos los casos se observó hueso esponjoso fijado en la porción inferior del implante de superficie (fig. 5A). El sistema Verso® empleado en todas las revisiones de esta serie, consiste en un implante con un minivástago recubierto de hidroxiapatita, diseñado para evitar la necesidad de fresar el canal medular del húmero y así evitar la pérdida de stock óseo, y que no requiere del empleo de cemento para su fijación (fig. 5B). En todos los casos se realizó impactación de autoinjerto óseo a nivel de la metáfisis, obtenido del centro de la cabeza humeral resecada.
Radiografías de hombro derecho de hombre de 58 años de edad, en proyección anteroposterior A) y axilar B), en las que se aprecia hemiartroplastia de superficie Copeland®, previa a cirugía de revisión por rotura secundaria e insuficiencia del manguito rotador. En la figuraA) se puede apreciar el acentuado ascenso de la cabeza humeral.
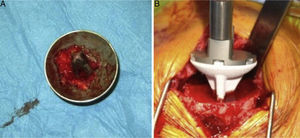
A) Foto clínica intraoperatoria mostrando perspectiva superior de componente humeral de prótesis de superficie de hombro «Copeland mark-3®», en la que se puede apreciar buena fijación, hueso esponjoso de la cabeza humeral en la porción caudal del implante, recubierta por hidroxiapatita.
B) Imagen intraoperatoria en la que se puede apreciar la introducción en la metáfisis humeral del vástago corto no cementado recubierto de hidroxiapatita.
El concepto de este implante supone una transferencia directa de los vectores de fuerza hacia la metáfisis humeral, lo cual reduce el «stress shielding» y conlleva a una mejor calidad ósea debajo del implante. El componente glenoideo tampoco requiere una fijación con cemento, ya que el tornillo tronco-cónico central recubierto de hidroxiapatita le confiere una fijación biológica. El diseño del inserto contempla un borde medial de bajo perfil, el cual le confiere un mejor encaje, una mayor estabilidad y evita el notching glenoideo.
Rehabilitación postoperatoriaTodos los pacientes fueron inmovilizados con un cabestrillo en rotacio¿n interna que empezó a retirarse progresivamente de la tercera semana postopeartoria en adelante. Se iniciaron los movimientos pendulares desde el primer día del postoperatorio, y los movimientos pasivos sin restricciones se autorizaron entre la primera y tercera semana del postoperatorio. La movilidad activa se empezó a trabajar entre la segunda y cuarta semana tras la cirugi¿a y la ganancia de fuerza muscular de la tercera semana en adelante.
Parámetros intraoperatorios y complicacionesLos parámetros registrados para valorar las complicaciones perioperatorias fueron: duración de la intervención, cuantía de las pérdidas hemáticas, días de estancia hospitalaria, la necesidad de transfusión perioperatoria, la necesidad de realizar una ventana humeral para extraer el implante, la necesidad de emplear aloinjerto para reponer el stock óseo y la producción de fracturas intraoperatorias. Las complicaciones tardías y las reintervenciones fueron registradas.
Valoración clínica y radiológicaLas valoraciones clínicas y radiológicas se llevaron a cabo tras un seguimiento mínimo de 25 meses. La valoración clínica y funcional preoperatoria, así como en la última visita de seguimiento, se basó en el test de Constant19. Dicho cuestionario consta de un máximo de 100 puntos y en todos los casos el cálculo se ajustó por edad y sexo. La puntuación ajustada se expresa como un porcentaje de la puntuación prevista para la edad y sexo del paciente20. El nivel de satisfacción del paciente se valoró con una medición subjetiva en una escala de 0 (completamente insatisfecho) a 10 (máxima satisfacción).
El seguimiento radiológico consistió en proyecciones radiográficas a los 3, 6, 9, y 12 meses después de la intervención y anualmente a partir de entonces. Las proyecciones realizadas fueron: anteroposterior, axilar y en rotaciones interna y externa.
Análisis estadísticoLos datos se analizaron mediante el uso del SPSS 19 (SPSS Inc., Chicago, Illinois). El t-test se aplicó para analizar variables cuantitativas y el X2 para las variables categóricas.
Se utilizó la prueba de X2 y el análisis de varianza para comparar los resultados preoperatorios y postoperatorios. Las variables continuas se encuentran expresadas como media y desviación estándar. Las variables categóricas se encuentran expresadas como porcentajes y frecuencias.
La relación entre las variables se analizó con tablas de contingencia para las variables categóricas, y la inferencia se estudió con la prueba de X2 o la prueba exacta de Fisher. La inferencia de las variables continuas se calculó con el t-test y sus resultados se encuentran expresados con sus correspondientes desviaciones estándar. El nivel de significación se fijó en 5% (α=0,05).
ResultadosTodos los pacientes pudieron ser contactados para la valoración de los resultados radiológicos y funcionales.
Parámetros intraoperatoriosLa duración media de la cirugía de recambio hacia el sistema Verso® fue de 113,35±21,30 min (rango 60-145 min). Las pérdidas hemáticas intraoperatorias medias fueron de 374±245,09 mls. En ninguno de los casos se tuvo que realizar una osteotomía a nivel de húmero para extraer el implante. En 8,69% (2/23) de las revisiones se utilizó aloinjerto estructural a nivel de la glenoides. Los parámetros intraoperatorios se encuentran reflejados en la tabla 3.
Parámetros intraoperatorios
| Variable | |
|---|---|
| Duración de la intervención (minutos) | 113,35±21,30 |
| Días de hospitalización | 4,90±5,85 |
| Pérdidas hemáticas intraoperatorias (mls) | 374±245,09 |
| Hb preop | 12,83±1,49 |
| Hb postop | 10,57±1,78 |
| Descenso postop de la Hb | 2,26±0,87 |
| Transfusiones | 4,38% (1/23) |
| Fracturas intraoperatorias | 4,38% (1/23) |
| Osteotomía humeral | 0% |
| Aloinjerto masivo (húmero) | 0% |
| Aloinjerto masivo (glenoides) | 8,69% (2/23) |
Se produjeron fracturas intraoperatorias en 4,30% (1/23) de las revisiones. Dicha fractura fue a nivel de la metáfisis humeral y se trató mediante sutura ósea.
Complicaciones tardías y reintervencionesLa tasa general de rerrevisión fue de 8,7% (2/23). En 2 de los pacientes se tuvieron que llevar a cabo 2 rerrevisiones del componente humeral. Uno de los pacientes reintervenidos había presentado 2 episodios de luxación (el primer episodio fue tratado mediante reducción cerrada) a causa de un osteofito medial remanente que estaba condicionando impingement a dicho nivel. El tratamiento consistió en el cambio y reorientación del inserto humeral. El otro paciente presentó una fractura periprotésica traumática y la reintervención consistió en la colocación de una prótesis invertida Verso® con vástago.
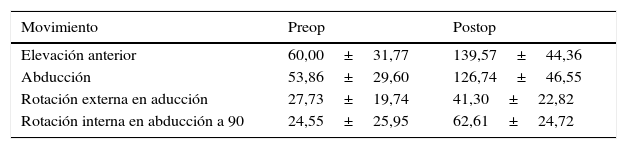
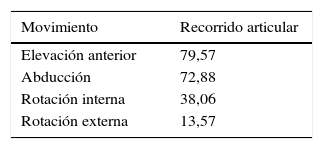
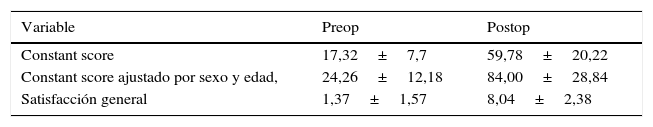
Resultados funcionalesLos resultados clínicos postoperatorios se encuentran reflejados en la tabla 4. Se evidenciaron mejorías en casi todos los parámetros. La ganancia de recorrido articular (valor postop - valor preop) se encuentra reflejada en la tabla 5. El test de Constant y la satisfacción general se encuentran reflejados en la tabla 6.
No se evidenciaron radiolucencias, ni hundimientos, ni osteólisis metafisaria indicativa de «stress shielding». Hubo evidencia de notching glenoideo (Nerot-Sirveaux)21 en 8,7% (2/23) de los pacientes: grado 1 en uno de los casos, y grado 2 en el otro. En este último caso, el paciente padecía de artritis reumatoide juvenil y en la artroplastia de revisión se empleó un polietileno retentivo.
DiscusiónEl principal hallazgo del presente estudio es que la cirugía de revisión de las prótesis de superficie de hombro recambiadas hacia prótesis invertida puede no implicar la realización de una ventana ósea a nivel de la metáfisis humeral para extraer el implante, ni tampoco el uso de aloinjerto óseo estructural para restaurar el stock óseo.
Las indicaciones de la artroplastia de superficie de hombro son las mismas que las de la prótesis anatómica con vástago: dolor y disfunción secundaria a artrosis primaria, artritis reumatoide y otras artritis inflamatorias, artritis postraumática, necrosis avascular y artropatía por inestabilidad22. Los resultados descritos en las series de casos en los que la artropatía degenerativa primaria del hombro ha sido tratada mediante un implante de superficie son comparables a aquellos resultados obtenidos con prótesis anatómicas con vástago23. La tasa descrita de cirugías de revisión a 6 años para la prótesis de superficie de hombro es de 5%22. Huguet et al. concluyeron tras un seguimiento medio de 45 meses de 63 pacientes tratados mediante prótesis de superficie de hombro, que los resultados preliminares apuntan hacia una mejoría funcional comparable a aquella que se obtendría mediante el empleo de implantes con vástago de tercera y cuarta generación24. De la misma manera, Habermeyer et al. describen los resultados de una serie de 78 pacientes con un seguimiento medio de 72 meses, similares a los obtenidos con implantes con vástago de última generación, empleados en casos de artrosis primaria y postraumática17. Dichos autores describen que la tasa de aflojamiento de estos implantes podría ser menor a la de los implantes con vástago de última generación17. En todos los pacientes que se presentan en «Reading Shoulder Unit» y que tienen indicación de artroplastia de hombro, se considera como primera opción la prótesis de superficie. Solo se considera la implantación de una prótesis anatómica con vástago en los pacientes con pérdida severa del stock óseo, con fracturas, o seudoartrosis.
Se ha descrito que los fracasos de las artroplastias de hombro (hemi- o total) se deben en su mayoría a insuficiencia secundaria del manguito rotador25. La migración craneal de la cabeza humeral representa la causa principal de dolor. En nuestra serie 91,3% (21/23) de las revisiones se llevaron a cabo por insuficiencia secundaria del manguito rotador. Otras causas pueden estar en relación con el componente glenoideo o con la glenoides nativa. Favard et al. describen que la tasa de revisiones quirúrgicas por fracaso del componente glenoideo fue de 5,6% y por glenoiditis dolorosa en las hemiartroplastias de 7,4%26. En nuestra serie 60% (3/5) de los pacientes del grupo de prótesis total, tuvieron que ser recambiados por ambos motivos: insuficiencia secundaria del manguito rotador y aflojamiento aséptico del componente glenoideo.
La artroplastia de hombro de revisión es considerada un procedimiento quirúrgico técnicamente complejo, que puede implicar complicaciones perioperatorias potenciales y que ofrece resultados funcionales mucho menos predecibles que los de las artroplastias invertidas de hombro primarias. Austin et al. revisaron retrospectivamente los resultados de 28 prótesis invertidas de hombro de revisión y los compararon con un grupo de 28 prótesis invertidas de hombro primarias8. Dichos autores describen que en esa serie el grupo de las prótesis invertidas de hombro de revisión tuvieron resultados clínicos más pobres, así como una mayor tasa de complicaciones, alcanzando el 35,7%8. A pesar de que los resultados funcionales que se obtienen tras la implantación de una prótesis invertida de hombro de revisión son claramente inferiores a los de la prótesis invertida primaria5–7,27, la prótesis invertida es considerada como la mejor alternativa para la cirugía de revisión9,28.
Con respecto a las complicaciones perioperatorias de la artroplastia de hombro de revisión, Flury et al. han descrito una tasa de complicaciones intraoperatorias de 43% y postoperatorias de 38%16. Wall et al. han reportado una tasa de complicaciones a 40 meses de 36,7%29. Boileau et al. han descrito una tasa de complicaciones postoperatorias de 47%5, y Levy et al. de 48%30. Walker et al. posteriormente han descrito una tasa global de complicaciones más baja (22,7%) en una serie retrospectiva de 24 prótesis invertidas de hombro de revisión31. Posteriormente, Patel et al. describieron complicaciones en solo 10,7% (3/28) de los recambios de su serie32. El descenso progresivo en el tiempo de la tasa de complicaciones perioperatorias en los casos de artroplastias invertidas de hombro de revisión, puede ser el reflejo de la experiencia que ha ido ganando la comunidad de cirujanos de hombro desde la aprobación de dicho implante por la «Food and Drug Administration » en el año 200432. La tasa global de complicaciones en nuestra serie fue de 13% (3/23): 4,35% intraoperatorias (1/23) y 8,7% postoperatorias (2/23). Creemos que la baja tasa de complicaciones perioperatorias registradas en nuestra serie puede ser el resultado del uso de implantes cuyo diseño ha sido pensado para tal fin: implantes primarios de superficie que no requieren del uso de vástago ni de cemento y prótesis invertida de revisión con un inserto de bajo perfil medial para evitar el notching y el desgaste, así como la liberación de partículas y el subsiguiente aflojamiento.
En la cirugía de revisión, la realización de osteotomías y ventanas humerales puede ser necesaria para la extracción de los vástagos humerales33. En la serie de Sperling et al., en 9,95% (20/201) de las artroplastias de revisión fue necesaria la realización de una osteotomía humeral para extraer el implante (los 201 casos de la serie consistían en implantes humerales con vástago); mientras que en nuestra serie (a pesar de que está compuesta por un menor número de casos), no fue necesaria la realización de osteotomía humeral para la extracción de ninguno de los implantes de superficie. La extracción de un vástago humeral bien fijado, bien sea cementado o no, implica complejidades técnicas y puede requerir un tiempo quirúrgico prolongado. Hasta donde tenemos conocimiento, aparte de nuestra serie, no hay más estudios en los que se haya registrado la duración media de la artroplastia de hombro de revisión.
La pérdida intraoperatoria de stock óseo a nivel del húmero proximal, especialmente en la tuberosidad mayor, puede ser una consecuencia esperable cuando se presentan dificultades técnicas relacionadas con la extracción del cemento. La disminución del stock óseo puede conllevar a la necesidad de emplear aloinjerto estructural. En la serie de artroplastias de revisión de Walker et al., en el 62,5% (15/24) de los casos fue necesario el empleo de aloinjerto óseo, siendo estructural en el 41,7% (10/24)31. En nuestra serie, solo se utilizó aloinjerto estructural en 8,69% (2/23) de las revisiones y a nivel de la glenoides.
La principal complicación intraoperatoria de la artroplastia de hombro de revisión es la fractura de la diáfisis humeral, situación que se traduce en un procedimiento quirúrgico prolongado con importantes pérdidas hemáticas. Boileau et al. describen una serie de artroplastias invertidas de hombro de revisión en la que se registró un 10,53% (2/19) de fracturas intraoperatorias, mientras que en nuestra serie se registró un 4,34% (1/23). Dicha diferencia puede deberse al hecho de que los implantes primarios recambiados en nuestra serie carecían de vástago y de cemento. Teniendo en cuenta que se ha descrito que los resultados de los implantes primarios cementados y con vástago son comparables a los de los implantes primarios de superficie17, pensamos que en la artrosis primaria de hombro se debería considerar cada vez que tenga cabida, la implantación de una prótesis de superficie en vez de una prótesis anatómica con vástago.
Se ha descrito un riesgo alto de complicaciones infecciosas en el contexto de las prótesis invertidas de hombro de revisión34. Boileau et al. describen una tasa de infecciones del 16% a 40 meses5. En nuestra serie no hemos registrado ningún caso de infección tras un seguimiento medio de 43,4 meses. Pensamos que el hecho de que el tiempo quirúrgico de las cirugías de recambio que parten de un implante primario no cementado y sin vástago sea potencialmente menor, puede suponer una disminución de la posibilidad de desarrollar una complicación infecciosa en el periodo postoperatorio.
El uso de cemento en las artroplastias de hombro primarias y de revisión afecta potencialmente la densidad ósea. Ni las prótesis de superficie de hombro Copeland® ni el diseño de prótesis invertida Verso® requieren de cemento para su fijación, por lo que ambos sistemas se podrían considerar como implantes preservadores de hueso. En las artroplastias de recambio, la extracción incompleta del cemento podría conducir al aflojamiento de los componentes de revisión, debido a que el cemento remanente impediría el crecimiento óseo hacia la hidroxiapatita31. Por estos motivos, consideramos que en la medida de lo posible, habría de evitarse el uso de cemento e implantes con vástago en la artropatía glenohumeral primaria y secundaria a insuficiencia del manguito rotador.
En relación a las rerrevisiones, Melis et al. reportan una tasa de 22%12, mientras que la tasa registrada en nuestro estudio es de 8,7%. Estas diferencias podrían estar en relación con el diseño de los implantes empleados en nuestra serie. Un inserto de bajo perfil medial que limita el notching y el desgaste, así como la liberación de partículas y los consiguientes aflojamientos; y un componente glenoideo no cementado con un tornillo tronco-cónico central recubierto, que proporciona una fijación primaria de gran fortaleza. El uso de una prótesis invertida con vástago corto y no cementado mantiene abiertas las posibilidades, en caso de que puedan requerirse futuras revisiones35,36.
El presente estudio no se encuentra exento de limitaciones. Se trata de una revisión retrospectiva. Para los propósitos de este estudio, no se dispuso de un grupo control. Sin embargo, los resultados expuestos en el presente estudio pueden ser contrastados con aquellos descritos en las series de pacientes tratados mediante implantes con vástago.
Concluimos que la artroplastia de revisión de las prótesis de superficie de hombro recambiadas hacia prótesis invertida no cementada con vástago corto ofrece excelentes resultados clínicos y radiológicos, representando una técnica con complejidades intraoperatorias mínimas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLuis Natera MD, Juan Bruguera MD PhD y Ehud Atoun MD declaran no tener conflicto de intereses en relacio¿n con el presente estudio.
Ofer Levy, MD MCh(Orth) FRCS, recibe regali¿as por parte de Innovative Design Orthopaedics® (IDO), por derechos de patente como cirujano implicado en el diseño de los implantes contemplados en este artículo.