Realizar una evaluación clínica y paraclínica y establecer la supervivencia del injerto y del paciente a 3 años de seguimiento de pacientes trasplantados.
Materiales y métodosEstudio descriptivo de corte transversal retrospectivo en pacientes trasplantados del Hospital Universitario de Neiva, desde febrero de 2007 hasta el cumplimiento de los 3 años de seguimiento en diciembre de 2014. Se realizó caracterización sociodemográfica, de variables clínicas y paraclínicas pretrasplante y postrasplante (al mes, a los 6 meses, al año y a los 3 años de seguimiento), comparaciones con los valores pretrasplante y análisis de sobrevida del injerto y del paciente a 3 años de seguimiento por el método de Kaplan-Meier.
ResultadosPara el año 2014, un total de 140 pacientes habían cumplido mínimo 3 años postrasplante. A los 3 años de seguimiento hay diferencias estadísticamente significativas en los valores de porcentaje de neutrófilos, hemoglobina, creatinina y tasa de filtración glomerular y las variables clínicas de presión arterial sistólica, presión arterial diastólica e índice de masa corporal. La sobrevida del injerto a 3 años de seguimiento alcanzó el 84,5%, con 21 pérdidas, y la sobrevida del paciente fue del 87,4%, con 16 defunciones.
ConclusionesSe evidencian positivas diferencias estadísticamente significativas en las variables hemoglobina, creatinina y tasa de filtración glomerular, y en los valores de presión arterial sistólica y diastólica e incremento del índice de masa corporal. La sobrevida del injerto y del paciente a 3 años de seguimiento es similar a la reportada por la literatura mundial.
To carry out a clinical and paraclinical assessment, and establish graft survival, after a 3 years follow-up of transplant patients at the Hospital of Neiva.
Materials and methodsA descriptive retrospective cross-sectional study was conducted on transplant patients at the University Hospital of Neiva, from february 2007 until the completion of 3 years of follow-up to december 2014. An analysis was performed using the socio-demographic, clinical and paraclinical variables, pre-transplant and post-transplant, (one month, 6 months, one year, and 3 years of follow-up), as well as comparisons with pre-transplant values. An analysis of graft and patient survival at 3 years follow-up using the Kaplan-Meier method was also performed.
ResultsIn 2014, a total of 140 patients had completed at least 3 years post-transplant. At 3 years follow-up, there were statistically significant differences in the values of percentage of neutrophils, haemoglobin, creatinine, and glomerular filtration rate, as well as in 3 clinical variables (systolic blood pressure, diastolic blood pressure, and body mass index). Graft survival at 3 years of follow-up was 84.5%, with 21 losses, and patient survival was 87.4%, with 16 deaths.
ConclusionsPositive statistically significant differences were observed in haemoglobin, creatinine, and glomerular filtration rate, as well as the systolic and diastolic blood pressure, and increase in body mass index. Graft and patient survival at 3 years of follow-up is similar to that reported in the world literature.
La enfermedad renal crónica definida como el daño renal por más de 3 meses con alteración funcional o estructural del riñón es una enfermedad de muy alto impacto en la salud y calidad de vida de los pacientes y sus familias, y su impacto económico para el Sistema de Salud es considerable, representando entre el 2 y el 4% del total del gasto en salud del país1. De acuerdo al documento Situación de la enfermedad renal crónica en Colombia 20132, la prevalencia de la enfermedad renal crónica estadio 5 en el país es de 65,9 por 100.000 habitantes. En el departamento del Huila ocupa el séptimo lugar a nivel nacional, con una prevalencia de 69,2 por 100.000 habitantes, y para Neiva se reporta una incidencia de 118,7 por 100.000 habitantes, ocupando el tercer lugar entre las ciudades capitales, solo superada por Medellín y Popayán.
Se ha evidenciado en múltiples estudios que el trasplante renal es el tratamiento más costo-efectivo para el manejo de la enfermedad renal terminal, seguido por la diálisis peritoneal y la hemodiálisis3-5. En consecuencia, el trasplante renal se plantea como una alternativa viable altamente costo-efectiva para el manejo de la enfermedad renal crónica1.
Los pacientes con enfermedad renal crónica presentan alteraciones hematológicas, metabólicas y clínicas significativas6. La anemia es una complicación frecuente asociada a la afectación renal con la disminuida capacidad en la producción de eritropoyetina. El estado metabólico, incluyendo el perfil lipídico y la glucosa, es considerado un factor de riesgo cardiovascular que se suma a la hipertensión arterial propia del paciente nefrópata, constituyendo importantes marcadores para el seguimiento paraclínico y clínico del paciente renal7.
En el paciente trasplantado estas mismas variables son objeto de seguimiento junto con los paraclínicos de medición de la función renal, con variada periodicidad y con el claro propósito de vigilar el estado clínico del paciente y de su injerto8. Adicionalmente, se hace necesario seguir la sobrevida del injerto y del paciente a los 6 meses, al año, a los 3 años, 5 años y 10 años, mediante el análisis de Kaplan-Meier, según las recomendaciones a nivel nacional9.
En el departamento del Huila, la Unidad de Trasplante Renal del Hospital Universitario de Neiva fue pionera en la región en este tipo de intervenciones y desde el año 2007 hasta la fecha ha venido realizando un promedio de 28 trasplantes al año. Los pacientes trasplantados deben llevar un seguimiento periódico con el propósito de evaluar su estado clínico y paraclínico y para comprobar el adecuado funcionamiento del injerto, siendo este el objetivo del presente estudio: evaluar el comportamiento de variables paraclínicas y clínicas definidas, al igual que establecer la sobrevida del injerto y del paciente en 3 años de seguimiento.
Materiales y métodosSe realizó un estudio descriptivo de corte transversal retrospectivo sobre la base de datos de seguimiento de los pacientes trasplantados por la Unidad de Trasplante Renal del Hospital Universitario de Neiva, desde febrero de 2007 (fecha de inicio de trasplantes en la unidad) hasta el 31 de diciembre de 2014, identificando un total de 140 pacientes con al menos 3 años postrasplante. Las variables seleccionadas para la caracterización sociodemográfica fueron: edad, sexo, área de residencia, aseguramiento, estrato, escolaridad, ocupación y estado civil. Las variables de seguimiento paraclínico fueron: cuadro hemático (leucocitos, neutrófilos, linfocitos, hemoglobina y plaquetas), creatinina, tasa de filtración glomerular (calculada con fórmula Crockford-Gault), glucemia, colesterol total y triglicéridos; las variables clínicas fueron: presión arterial (PA) sistólica (PAS) y diastólica (PAD) e índice de masa corporal (IMC). A las variables cualitativas se les estimó la proporción y a las variables cuantitativas se les realizó análisis de normalidad y descripción de las medidas principales de tendencia central y dispersión (rango, media, mediana y DE). Se realizó un análisis comparativo con la prueba correspondiente (paramétrica o no paramétricas) de acuerdo al análisis de normalidad entre los valores pretrasplante y los valores al mes, a los 6 meses, al año y a los 3 años de seguimiento, indicando mediante la observación de los intervalos de confianza y los valores de p de las pruebas la presencia de diferencias estadísticamente significativas. Adicionalmente, se realizó análisis de sobrevida o supervivencia del injerto y del paciente a 3 años de seguimiento por el método de Kaplan-Meier. La información fue recopilada en una base de datos en Microsoft Excel 2010 y para el análisis de la información se utilizó el mismo programa y el programa IBM SPSS Statistics v. 19.0.0.
ResultadosUn total de 140 pacientes en diciembre de 2014 alcanzaron al menos 3 años postrasplante: 18 en el año 2007, 29 en 2008 y 2009, 37 en el año 2010 y 27 durante el año 2011. Todos los pacientes recibieron injerto de donante cadavérico.
Caracterización sociodemográfica. Las variables caracterizadas fueron: edad, sexo, área de residencia, aseguramiento en salud, estrato socioeconómico, escolaridad, ocupación y estado civil (tabla 1).
Caracterización sociodemográfica de los pacientes trasplantados con seguimiento de 3 años
| Variable | Valor |
|---|---|
| N | 140 |
| Edad (años), media (DE; IC 95% media) | |
| General | 41,9 (13,1; 39,8-44,1) |
| Hombres | 43,3 (13,8; 40,3-46,2) |
| Mujeres | 39,9 (11,7; 39,8-44,1) |
| Rango | 20,0-81,1 (61,1) |
| Sexo, n (%) | |
| Masculino | 84 (60,0) |
| Femenino | 56 (40,0) |
| Área de residencia, n (%) | |
| Urbano | 92 (79,3) |
| Rural | 24 (20,7) |
| Aseguramiento, n (%) | |
| Contributivo | 68 (48,6) |
| Subsidiado | 64 (45,7) |
| No asegurado | 6 (4,3) |
| Excepción | 2 (1,4) |
| Estrato, n (%) | |
| 1 | 71 (50,7) |
| 2 | 55 (39,3) |
| 3 | 13 (9,3) |
| 4 | 1 (0,7) |
| Escolaridad, n (%) | |
| Ninguna | 5 (3,6) |
| Primaria | 43 (30,7) |
| Secundaria | 69 (49,3) |
| Superior | 23 (16,4) |
| Ocupación, n (%) | |
| Trabaja | 66 (47,1) |
| Desempleado | 23 (16,4) |
| Hogar | 37 (26,4) |
| Pensionado | 11 (7,9) |
| Sin dato | 3 (2,1) |
| Estado civil, n (%) | |
| Soltero | 39 (27,9) |
| Casado | 61 (43,6) |
| Separado | 8 (5,7) |
| Unión libre | 30 (21,4) |
| Viudo | 2 (1,4) |
La edad promedio del paciente trasplantado fue de 42 años, con un rango entre 20 y 81 años. La edad promedio en hombres fue aproximadamente 3 años mayor a la edad promedio en mujeres.
Con relación al sexo, 3 de cada 5 pacientes trasplantados son hombres; cerca de 8 de cada 10 viven en zona urbana y cerca del 95% se distribuyen en los regímenes subsidiado y contributivo con porcentajes muy similares; la mitad de los pacientes tienen nivel de escolaridad secundaria y 16% tienen formación universitaria. En la variable ocupación, 47% trabajan; una cuarta parte se dedica al hogar y el 8% son pensionados; alrededor del 55% de los pacientes generan ingreso familiar (empleados y pensionados). En cuanto al estado civil, el 65% tienen alguna forma de unión marital, incluyendo pacientes casados y en unión libre (tabla 1).
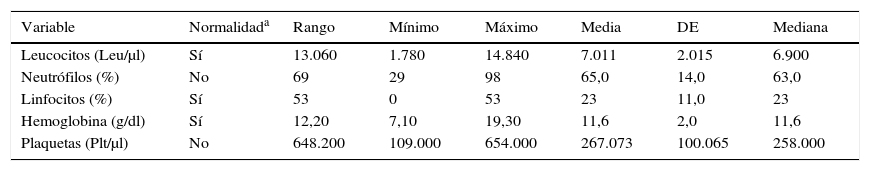
Caracterización pretrasplante. Todos los pacientes trasplantados recibieron como terapia de inducción alemtuzumab. El cuadro hemático del paciente pretrasplantado presentó una media de 7.000 leucocitos, con 63% de neutrófilos y 23% de linfocitos en promedio; la hemoglobina, con una media de 11,6mg/dl, fue la única variable del cuadro hemático en valores de anormalidad, dentro del rango de anemia leve según la OMS10; las plaquetas tuvieron una media de 258.000, valor muy similar a la mediana de 267.000Plt/μl (tabla 2).
Valores del cuadro hemático pretrasplante de los receptores
| Variable | Normalidada | Rango | Mínimo | Máximo | Media | DE | Mediana |
|---|---|---|---|---|---|---|---|
| Leucocitos (Leu/μl) | Sí | 13.060 | 1.780 | 14.840 | 7.011 | 2.015 | 6.900 |
| Neutrófilos (%) | No | 69 | 29 | 98 | 65,0 | 14,0 | 63,0 |
| Linfocitos (%) | Sí | 53 | 0 | 53 | 23 | 11,0 | 23 |
| Hemoglobina (g/dl) | Sí | 12,20 | 7,10 | 19,30 | 11,6 | 2,0 | 11,6 |
| Plaquetas (Plt/μl) | No | 648.200 | 109.000 | 654.000 | 267.073 | 100.065 | 258.000 |
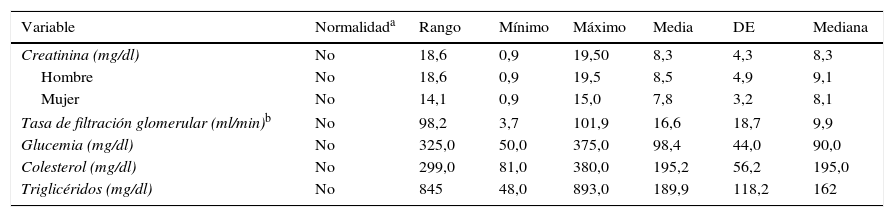
El colesterol presentó una media de 195mg/dl, los triglicéridos 189mg/dl de media y 162mg/dl de mediana, señalando la distribución anormal de sus valores. La glucemia obtuvo un valor promedio de 92mg/dl, con una DE 44mg/dl (tabla 3), evidenciando valores cercanos a los valores promedio de la población general.
Valores del perfil renal y del perfil lipídico pretrasplante de los receptores
| Variable | Normalidada | Rango | Mínimo | Máximo | Media | DE | Mediana |
|---|---|---|---|---|---|---|---|
| Creatinina (mg/dl) | No | 18,6 | 0,9 | 19,50 | 8,3 | 4,3 | 8,3 |
| Hombre | No | 18,6 | 0,9 | 19,5 | 8,5 | 4,9 | 9,1 |
| Mujer | No | 14,1 | 0,9 | 15,0 | 7,8 | 3,2 | 8,1 |
| Tasa de filtración glomerular (ml/min)b | No | 98,2 | 3,7 | 101,9 | 16,6 | 18,7 | 9,9 |
| Glucemia (mg/dl) | No | 325,0 | 50,0 | 375,0 | 98,4 | 44,0 | 90,0 |
| Colesterol (mg/dl) | No | 299,0 | 81,0 | 380,0 | 195,2 | 56,2 | 195,0 |
| Triglicéridos (mg/dl) | No | 845 | 48,0 | 893,0 | 189,9 | 118,2 | 162 |
En la creatinina y la TFG se observaron valores indicativos de enfermedad renal terminal (tabla 3), como es el caso de los pacientes trasplantados. La creatinina obtuvo un valor promedio de 8,3mg/dl y la TFG alcanzó una media de 16. Se observaron pacientes con valores de creatinina y TFG en rangos de normalidad, como se observa en los valores mínimos, identificando quienes venían recibiendo terapias de reemplazo renal tipo diálisis o hemodiálisis.
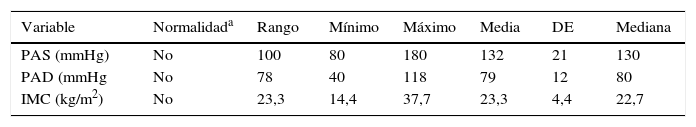
En los valores de PA e IMC, las medias reflejan un comportamiento dentro de los valores considerados como normales; 132/79 fueron las medias de PAS y PAD (tabla 4).
Variables de presión arterial e IMC pretrasplante
| Variable | Normalidada | Rango | Mínimo | Máximo | Media | DE | Mediana |
|---|---|---|---|---|---|---|---|
| PAS (mmHg) | No | 100 | 80 | 180 | 132 | 21 | 130 |
| PAD (mmHg | No | 78 | 40 | 118 | 79 | 12 | 80 |
| IMC (kg/m2) | No | 23,3 | 14,4 | 37,7 | 23,3 | 4,4 | 22,7 |
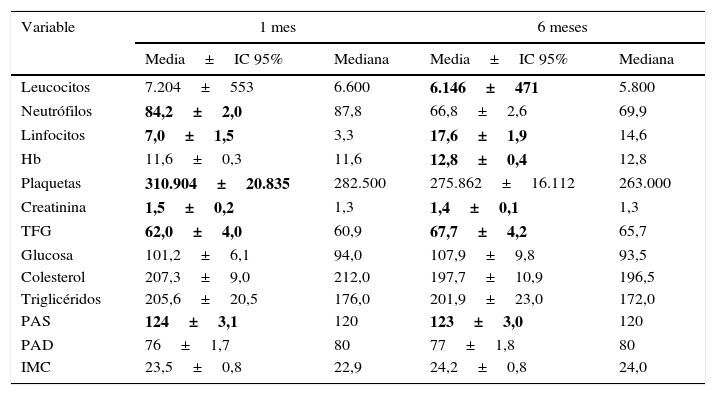
Seguimiento de las variables paraclínicas y clínicas de los pacientes trasplantados. En las tablas 5 y 6 se presentan la media con su respectivo intervalo de confianza y la mediana del seguimiento a 1 mes, 6 meses, 1 año y 3 años de las variables clínicas y paraclínicas evaluadas en el postrasplante.
Medidas de tendencia central de algunas variables clínicas y paraclínicas de los pacientes trasplantados con 3 años de seguimiento: 1 mes y 6 meses
| Variable | 1 mes | 6 meses | ||
|---|---|---|---|---|
| Media±IC 95% | Mediana | Media±IC 95% | Mediana | |
| Leucocitos | 7.204±553 | 6.600 | 6.146±471 | 5.800 |
| Neutrófilos | 84,2±2,0 | 87,8 | 66,8±2,6 | 69,9 |
| Linfocitos | 7,0±1,5 | 3,3 | 17,6±1,9 | 14,6 |
| Hb | 11,6±0,3 | 11,6 | 12,8±0,4 | 12,8 |
| Plaquetas | 310.904±20.835 | 282.500 | 275.862±16.112 | 263.000 |
| Creatinina | 1,5±0,2 | 1,3 | 1,4±0,1 | 1,3 |
| TFG | 62,0±4,0 | 60,9 | 67,7±4,2 | 65,7 |
| Glucosa | 101,2±6,1 | 94,0 | 107,9±9,8 | 93,5 |
| Colesterol | 207,3±9,0 | 212,0 | 197,7±10,9 | 196,5 |
| Triglicéridos | 205,6±20,5 | 176,0 | 201,9±23,0 | 172,0 |
| PAS | 124±3,1 | 120 | 123±3,0 | 120 |
| PAD | 76±1,7 | 80 | 77±1,8 | 80 |
| IMC | 23,5±0,8 | 22,9 | 24,2±0,8 | 24,0 |
Nota: Los valores en negrita son los que presentan diferencia estadísticamente significativa con base en la comparación con los valores pretrasplante mediante los intervalos de confianza.
Hb: hemoglobina; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAS: presión arterial sistólica; TFG: tasa de filtración glomerular.
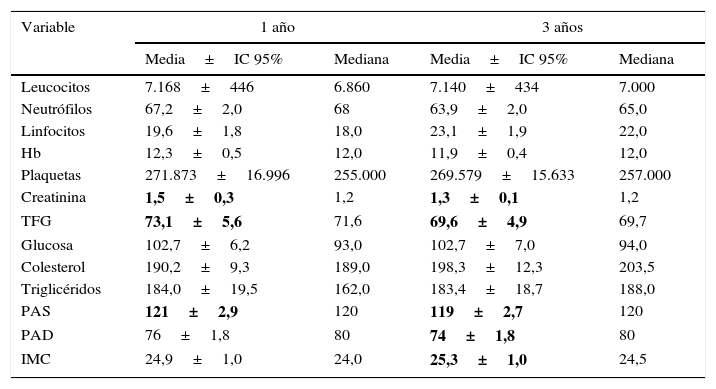
Medidas de tendencia central de algunas variables clínicas y paraclínicas de los pacientes trasplantados con 3 años de seguimiento: 1 año y 3 años
| Variable | 1 año | 3 años | ||
|---|---|---|---|---|
| Media±IC 95% | Mediana | Media±IC 95% | Mediana | |
| Leucocitos | 7.168±446 | 6.860 | 7.140±434 | 7.000 |
| Neutrófilos | 67,2±2,0 | 68 | 63,9±2,0 | 65,0 |
| Linfocitos | 19,6±1,8 | 18,0 | 23,1±1,9 | 22,0 |
| Hb | 12,3±0,5 | 12,0 | 11,9±0,4 | 12,0 |
| Plaquetas | 271.873±16.996 | 255.000 | 269.579±15.633 | 257.000 |
| Creatinina | 1,5±0,3 | 1,2 | 1,3±0,1 | 1,2 |
| TFG | 73,1±5,6 | 71,6 | 69,6±4,9 | 69,7 |
| Glucosa | 102,7±6,2 | 93,0 | 102,7±7,0 | 94,0 |
| Colesterol | 190,2±9,3 | 189,0 | 198,3±12,3 | 203,5 |
| Triglicéridos | 184,0±19,5 | 162,0 | 183,4±18,7 | 188,0 |
| PAS | 121±2,9 | 120 | 119±2,7 | 120 |
| PAD | 76±1,8 | 80 | 74±1,8 | 80 |
| IMC | 24,9±1,0 | 24,0 | 25,3±1,0 | 24,5 |
Nota: Los valores en negrita son los que presentan diferencia estadísticamente significativa con base en la comparación con los valores pretrasplante mediante los intervalos de confianza.
Hb: hemoglobina; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAS: presión arterial sistólica; TFG: tasa de filtración glomerular.
Se han dividido las variables en cuadro hemático (leucocitos, neutrófilos, linfocitos, hemoglobina y plaquetas), química sanguínea (creatinina, TFG calculada, glucemia, colesterol y triglicéridos) y variables clínicas (PAS, PAD e IMC).
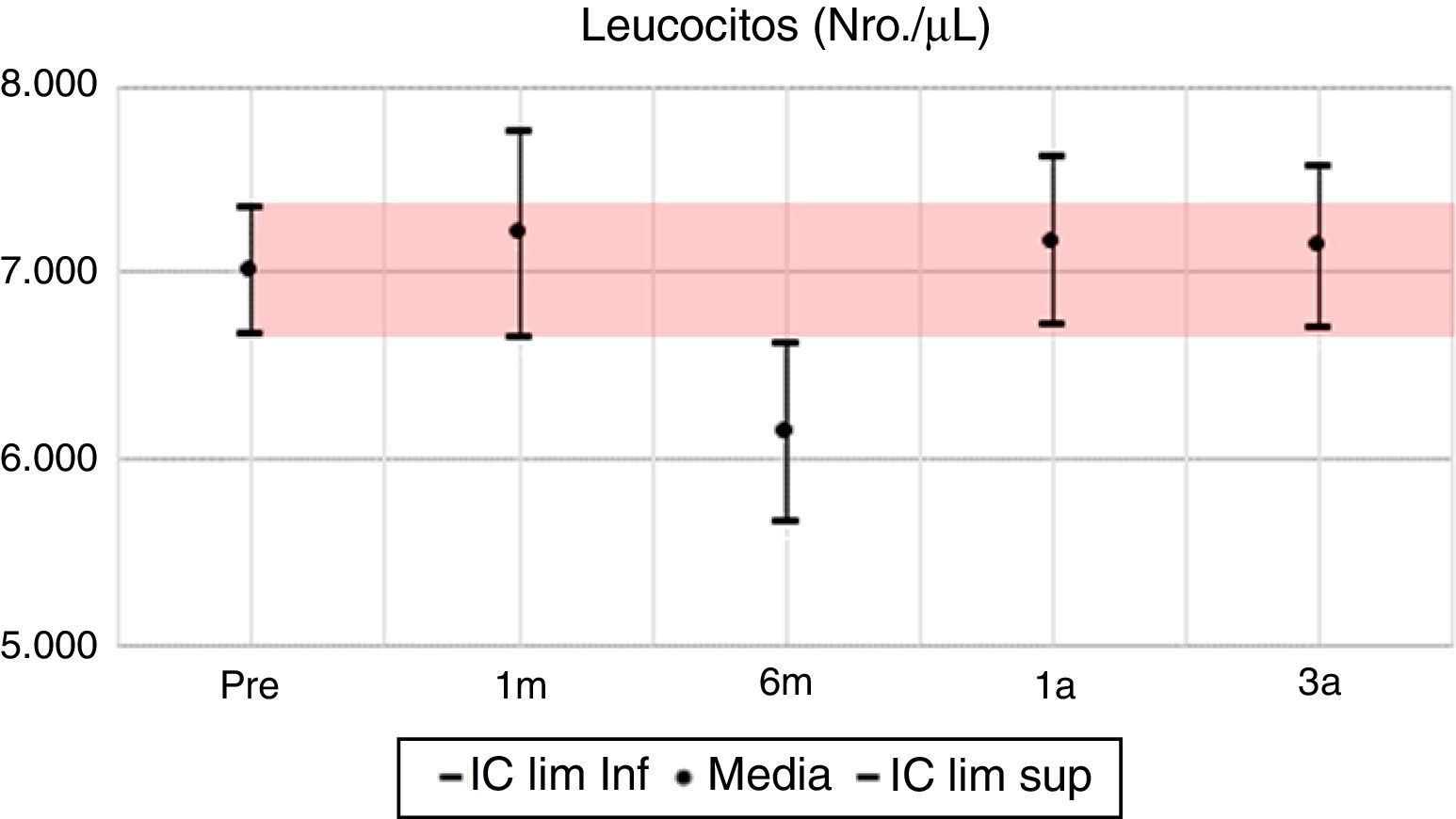
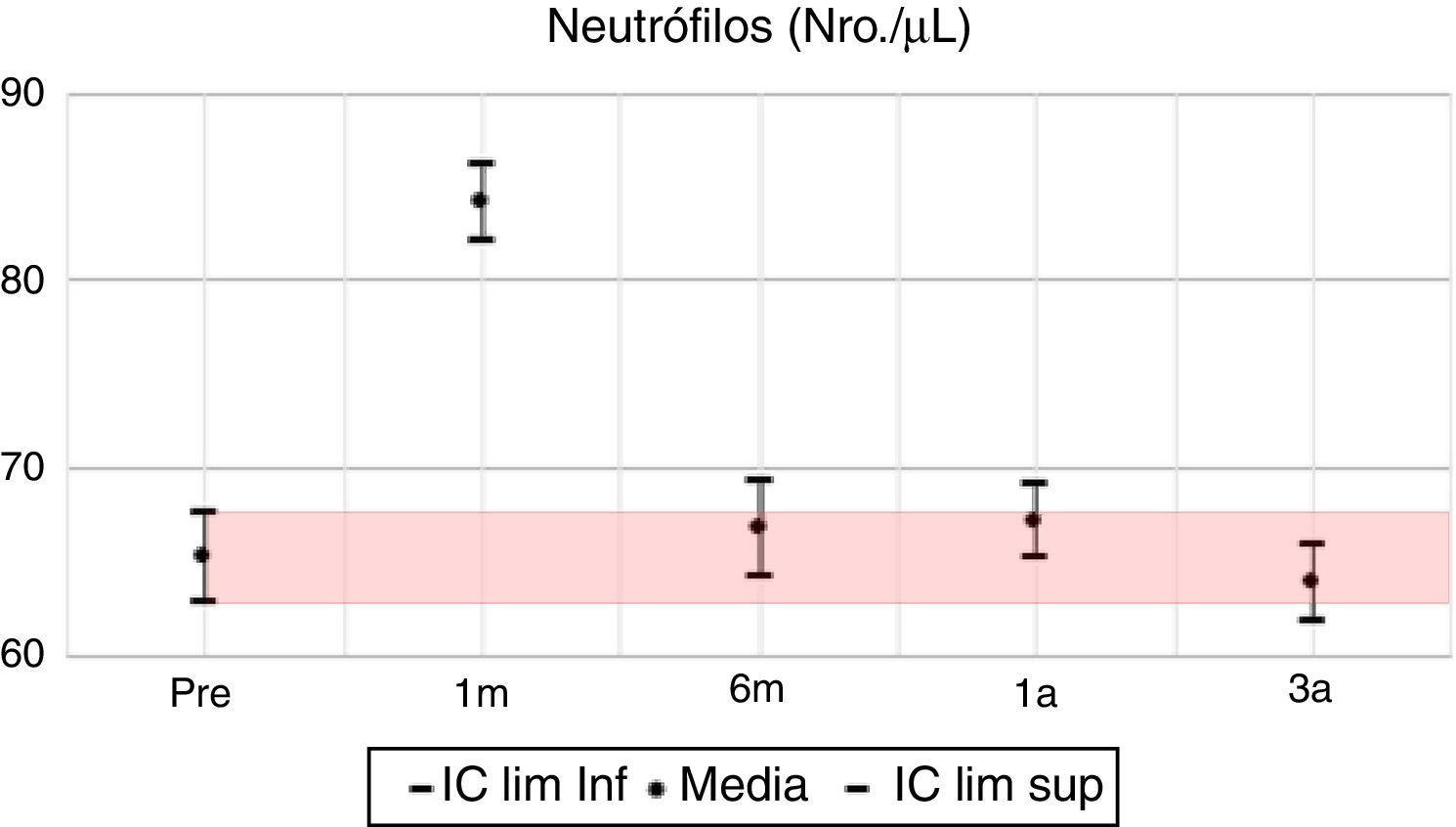
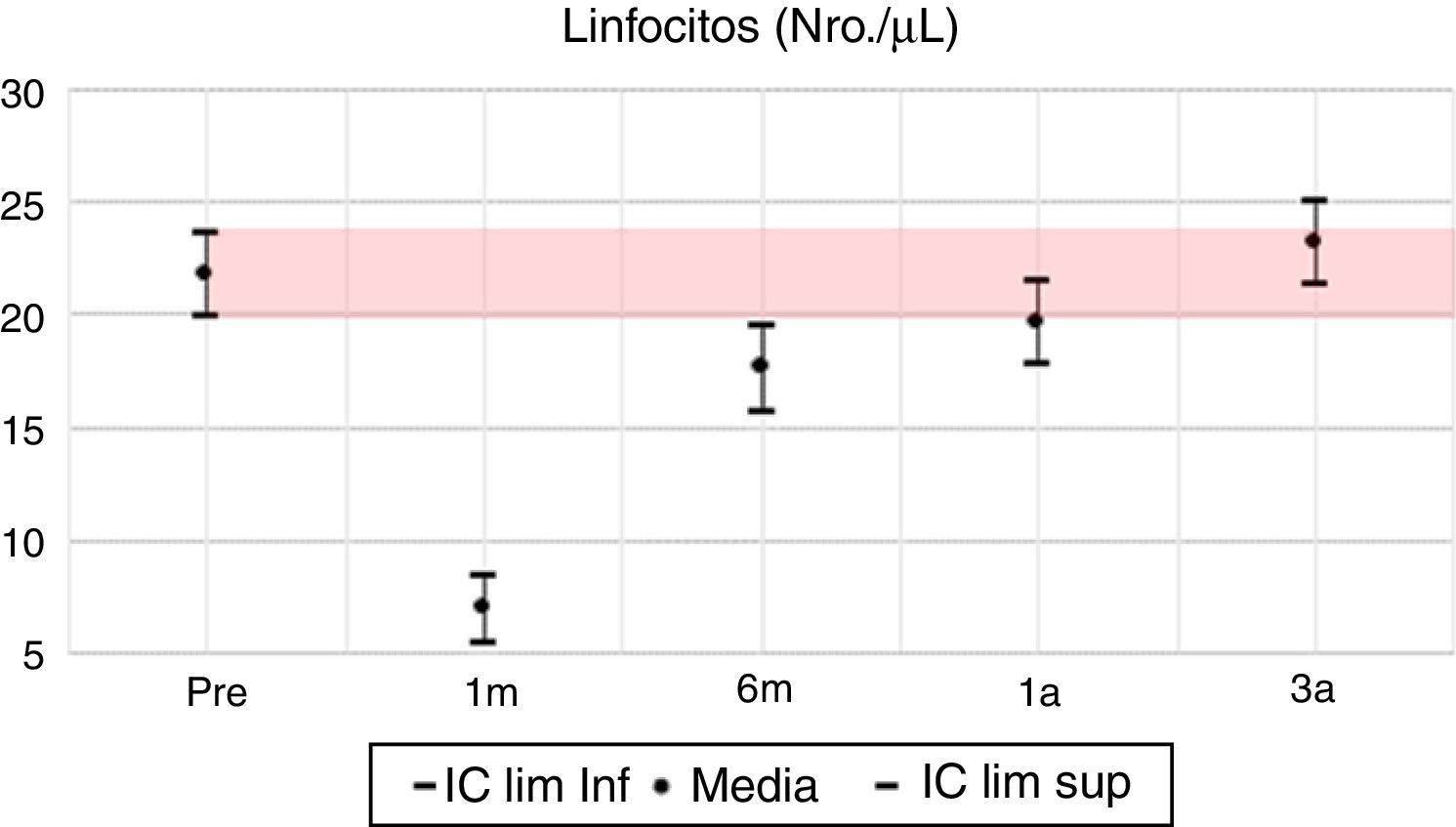
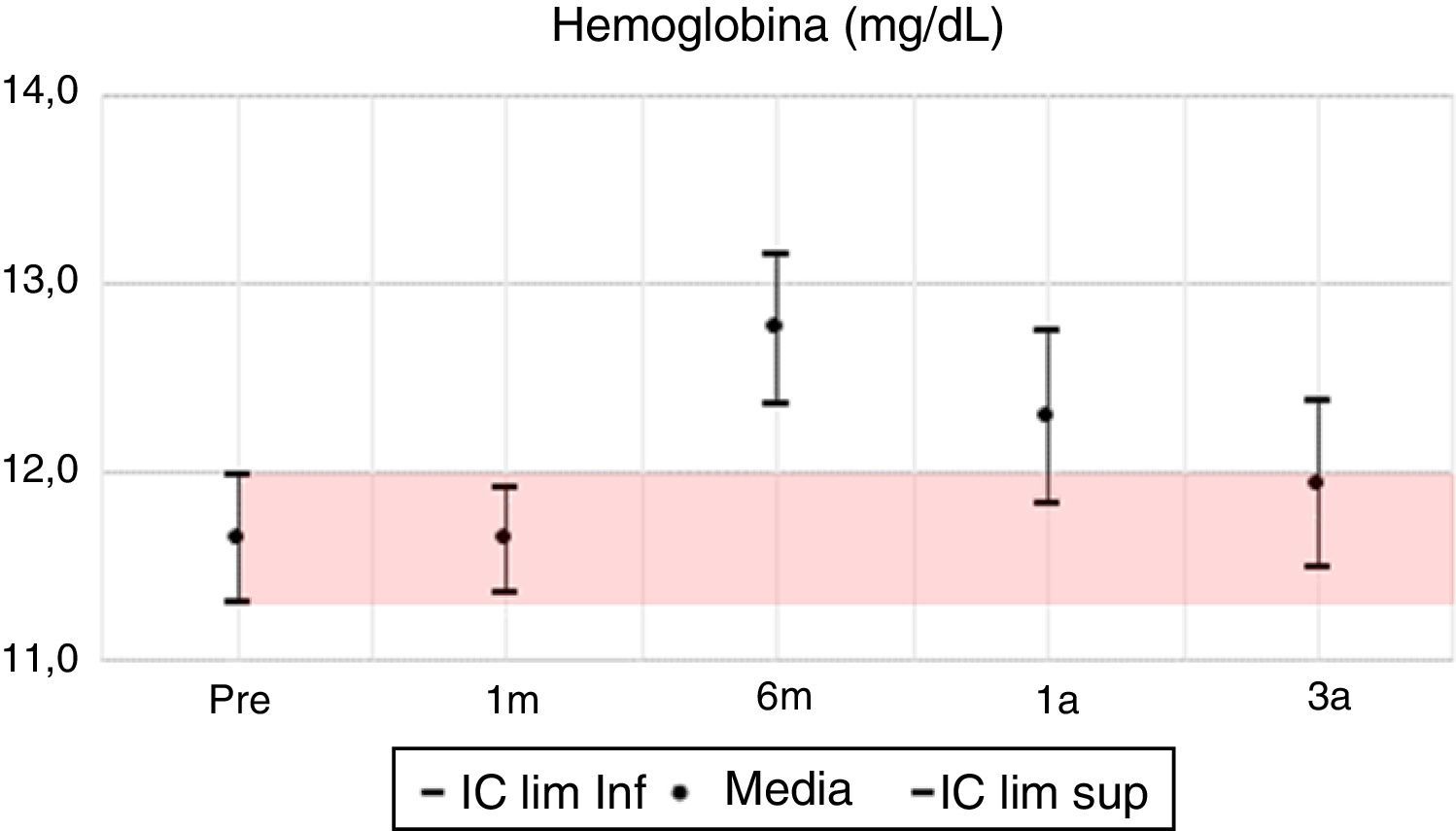
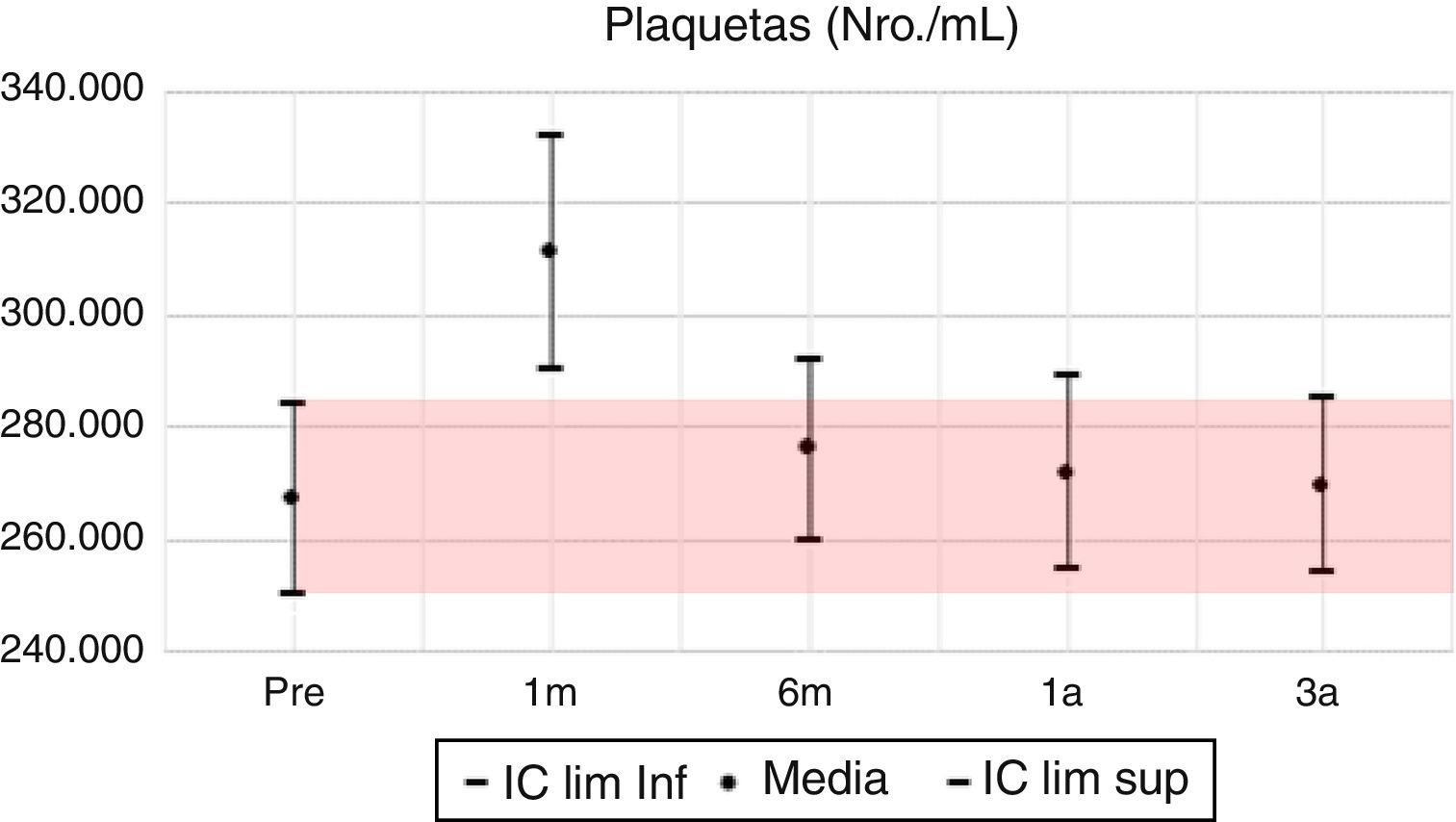
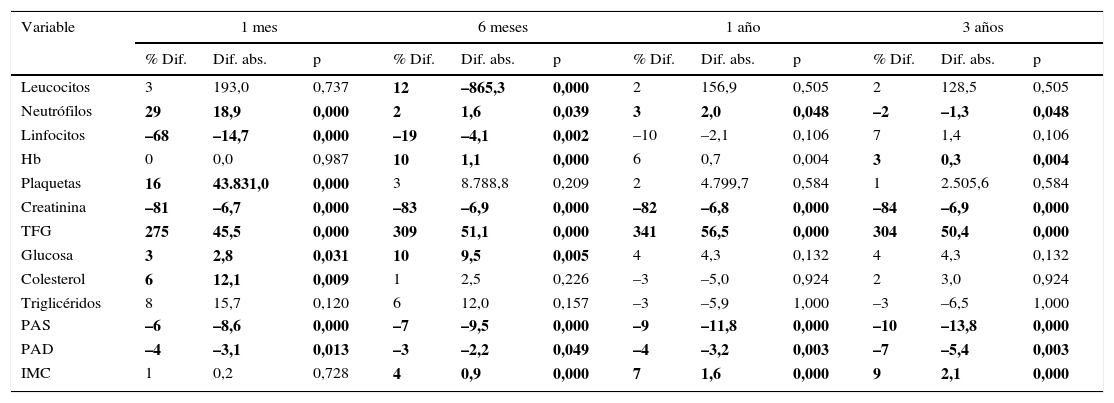
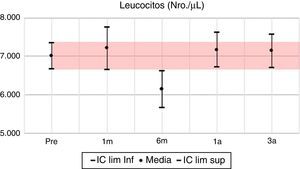
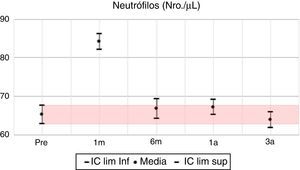
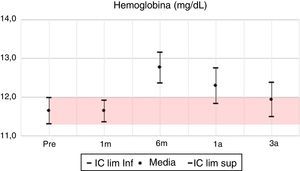
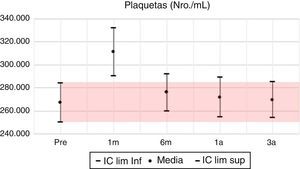
Los valores del cuadro hemático en su línea blanca presentan sus mayores variaciones en los primeros 6 meses; se evidencia al primer mes una inversión en la distribución porcentual de neutrófilos y linfocitos, volviendo a la normalidad al año y continuando a los 3 años con valores muy similares al pretrasplante. Respecto a la hemoglobina, la mayor variación positiva se observa a los 6 meses, con un incremento del 10% de su valor basal pretrasplante, mostrando a partir de este momento diferencias positivas estadísticamente significativas con el valor basal. Se parte de un porcentaje de anemia pretrasplante del 55,4%, para descender a un 27% al sexto mes postrasplante, 33,1% en el primer año y llega a un 42% al tercer año, con una diferencia positiva de 0,3mg/dl en la media de hemoglobina para este año.
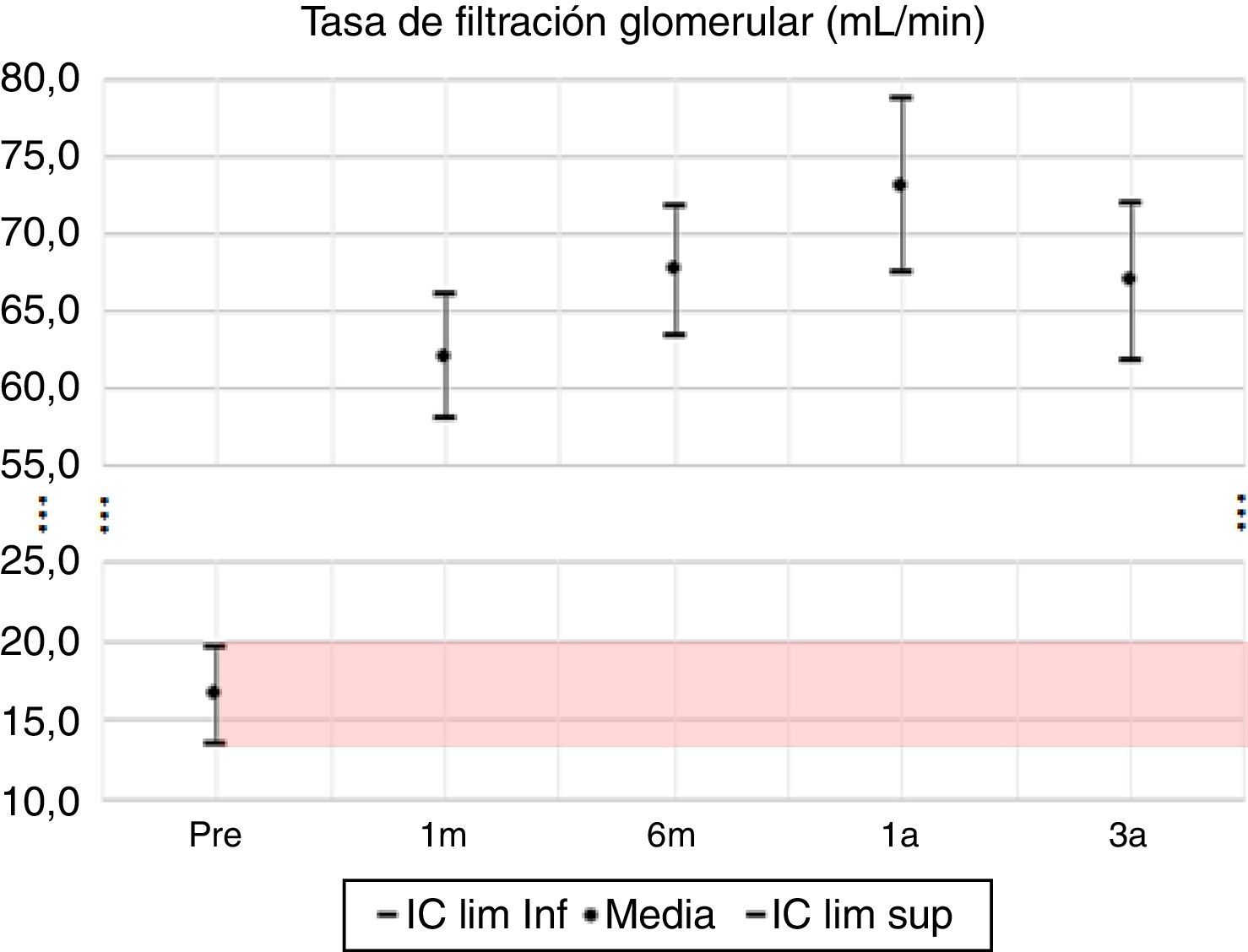
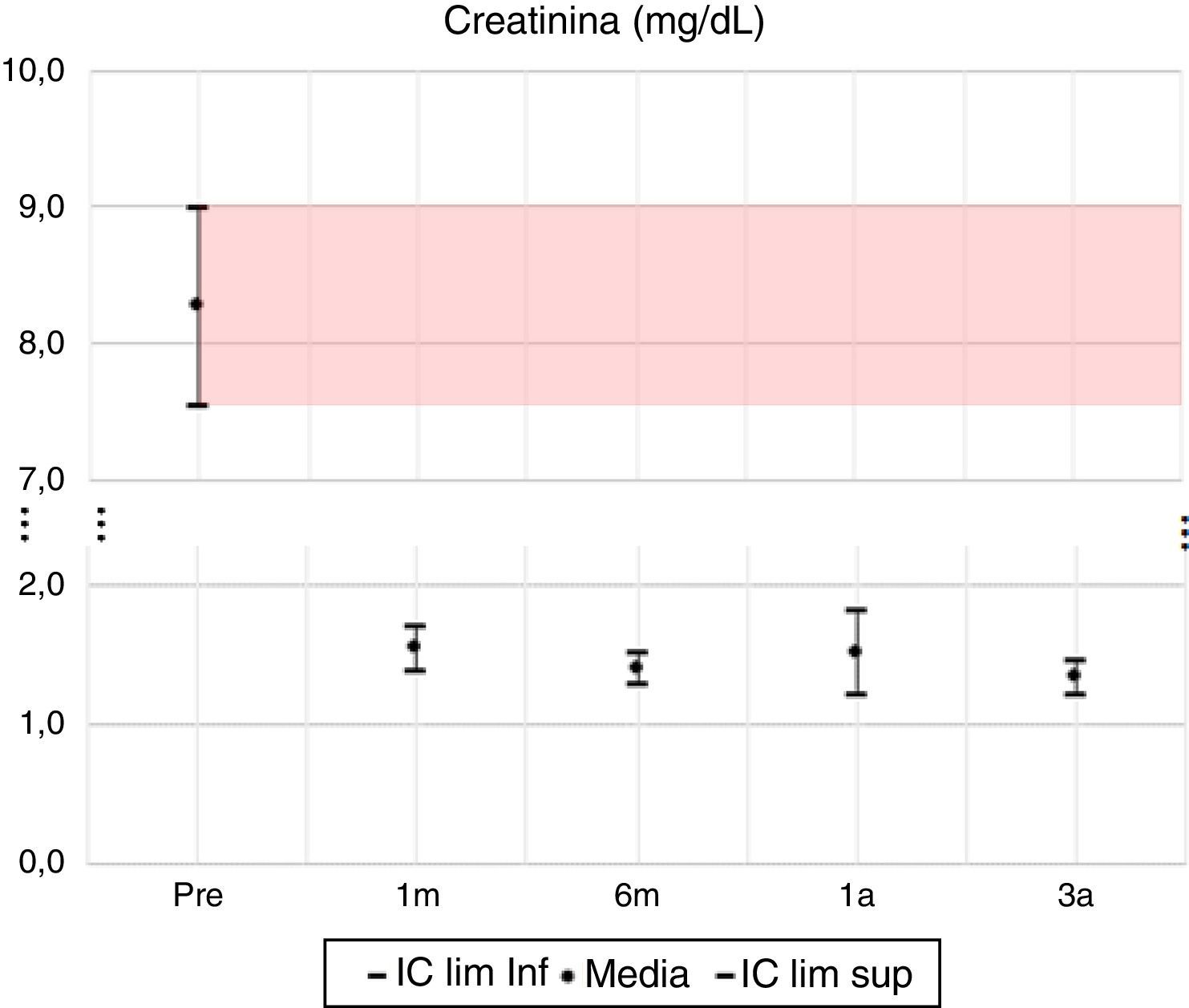
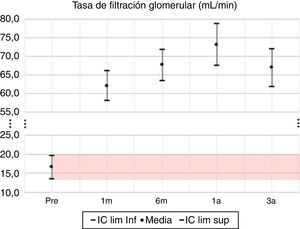
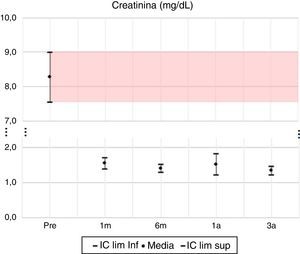
En las variables de evaluación de la función renal, creatinina y TFG, se observan las mayores diferencias porcentuales; el valor promedio de la creatinina al tercer año desciende en un 84% y la TFG promedio aumenta en un 304%.
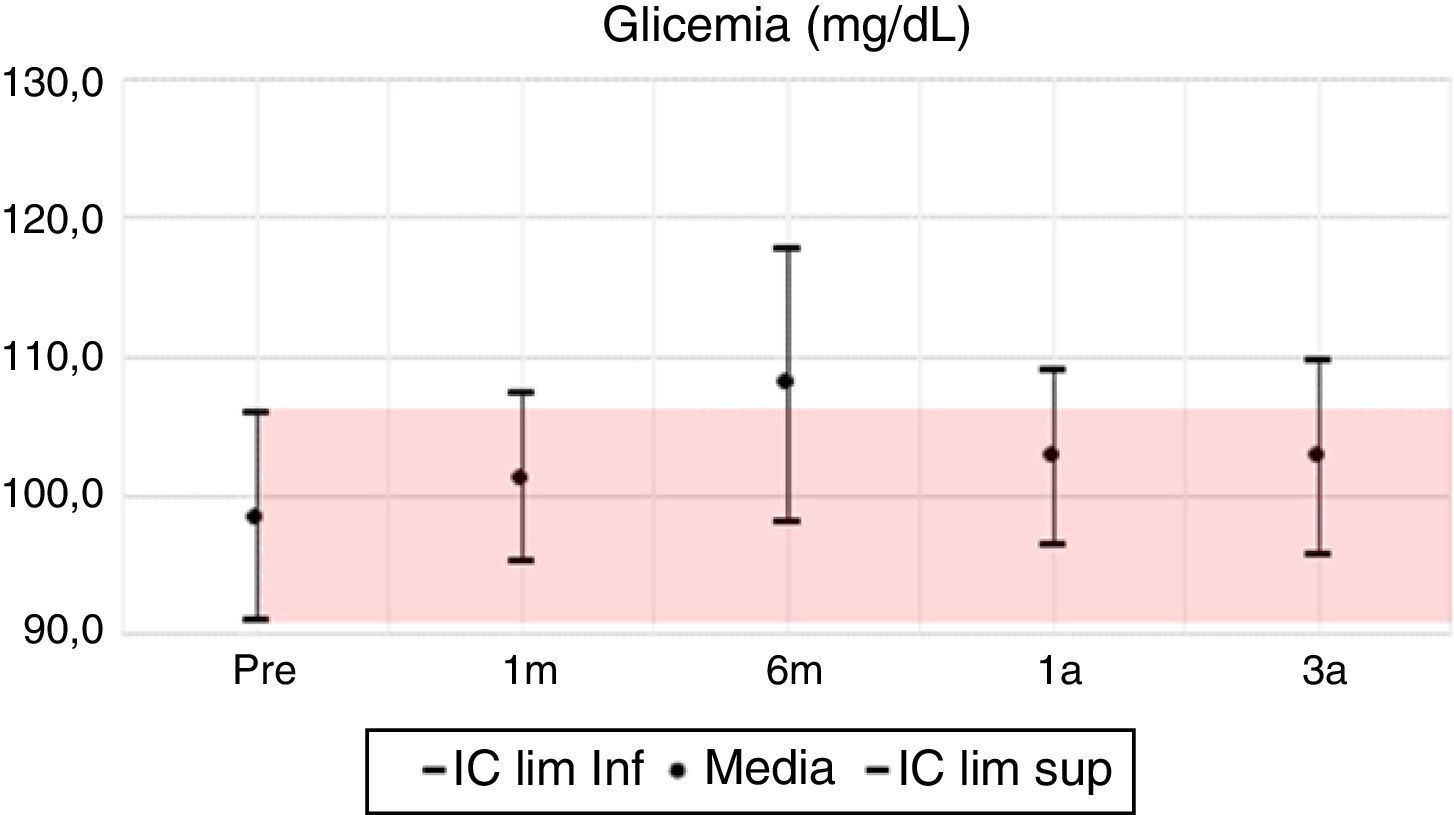
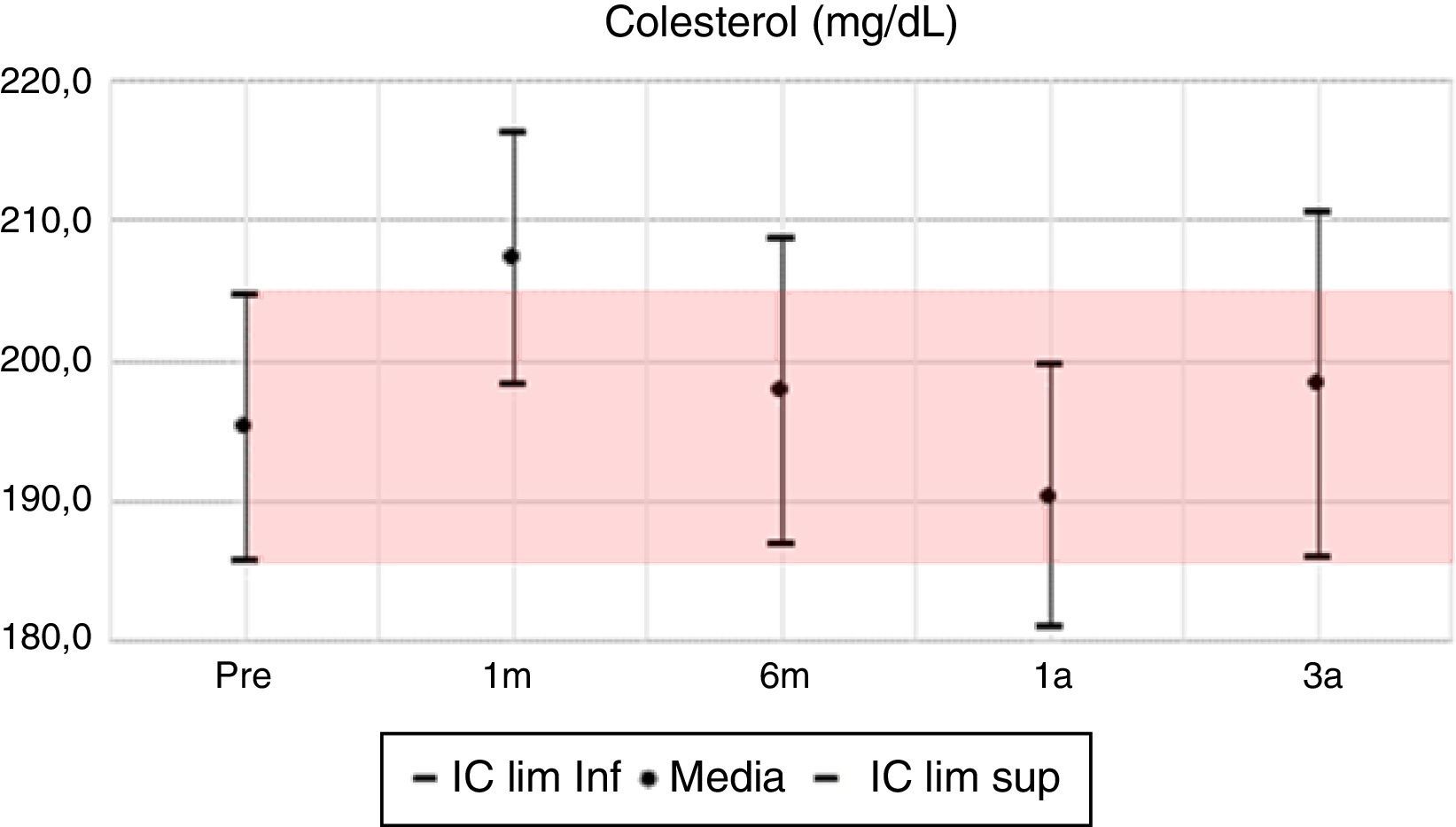
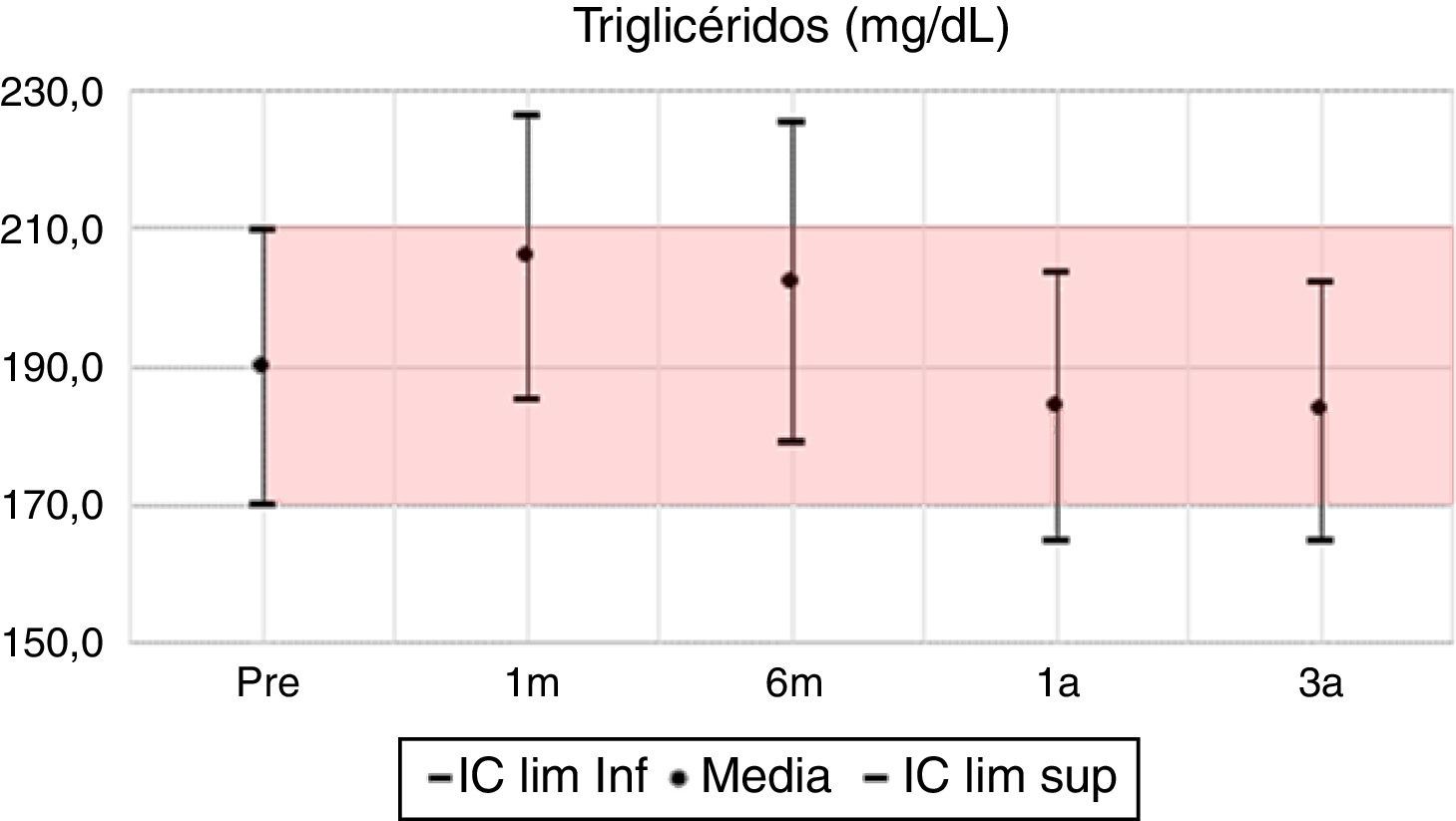
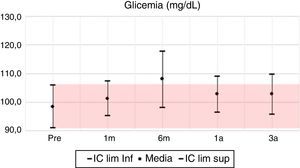
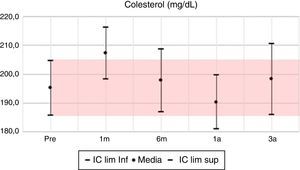
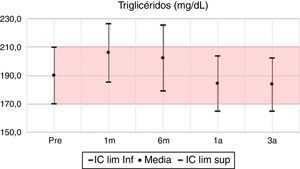
La glucosa y el colesterol tuvieron leves variaciones en los periodos de seguimiento fluctuantes en valores inferiores a un 10%, observando para el tercer año unas diferencias porcentuales positivas del 4 y 2% respectivamente. Por el contrario, los triglicéridos para el tercer año evidenciaron un descenso con una diferencia porcentual del 6,5%, pasando de 190mg/dl en el pretrasplante a 183mg/dl.
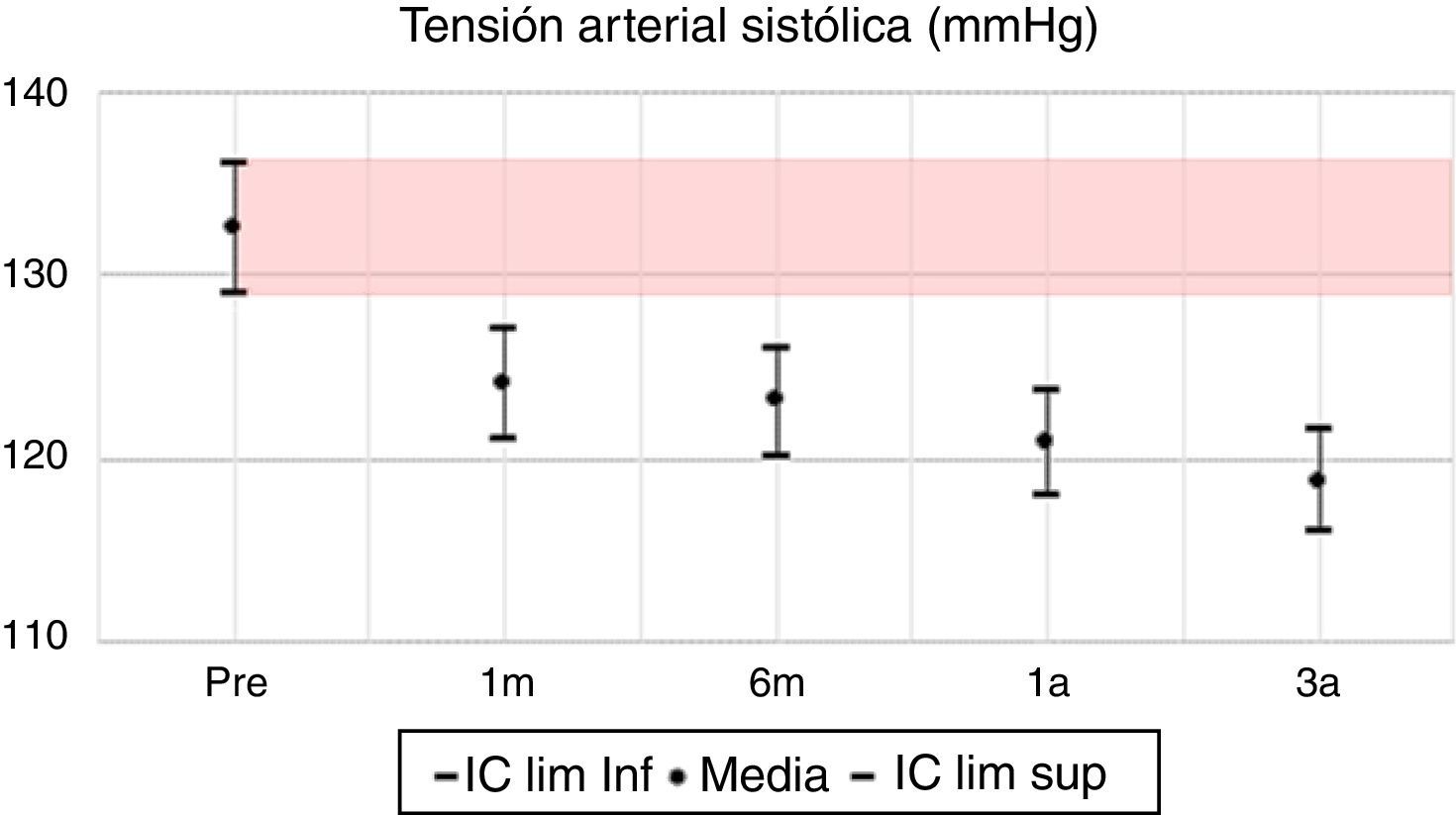
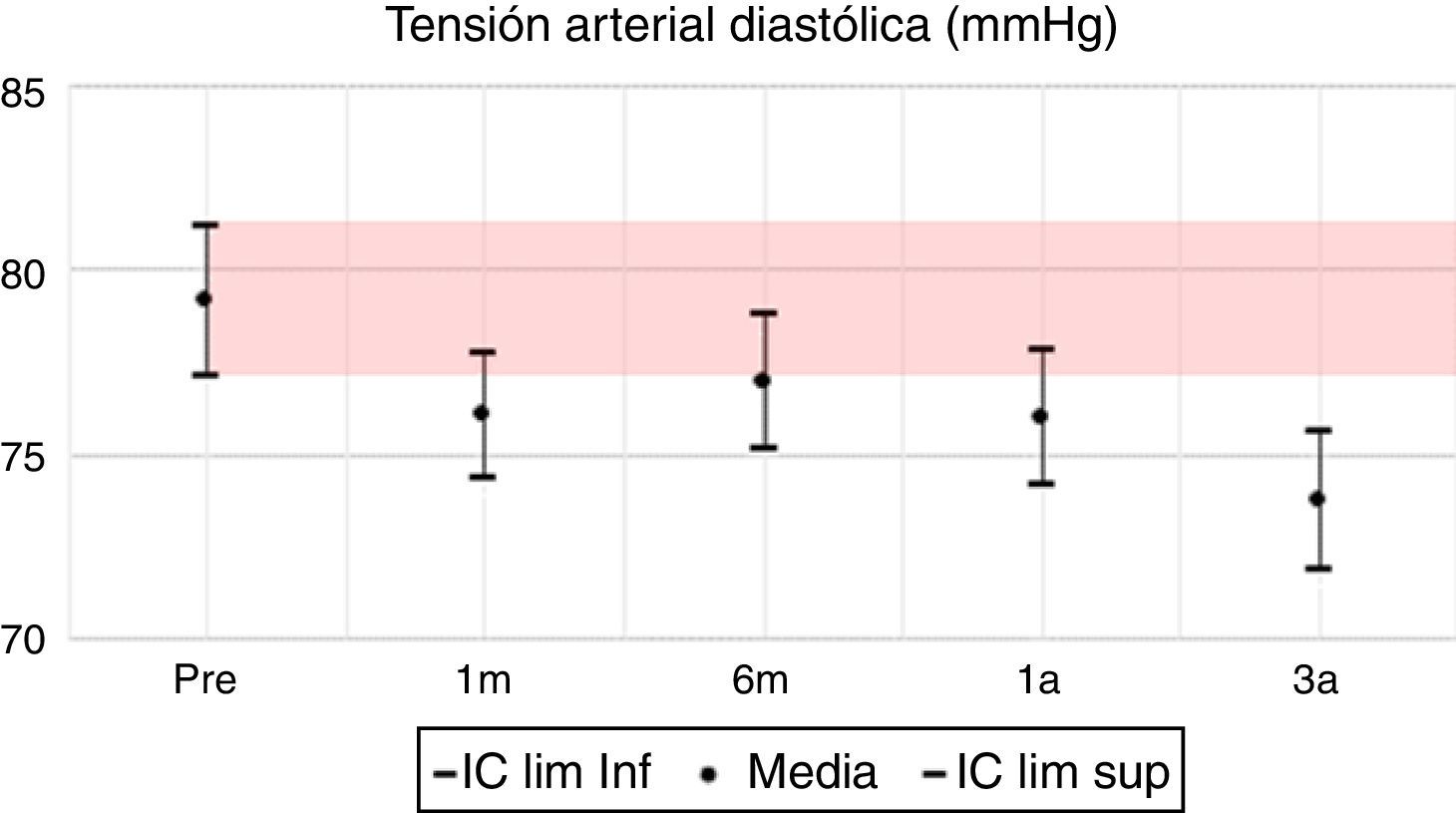
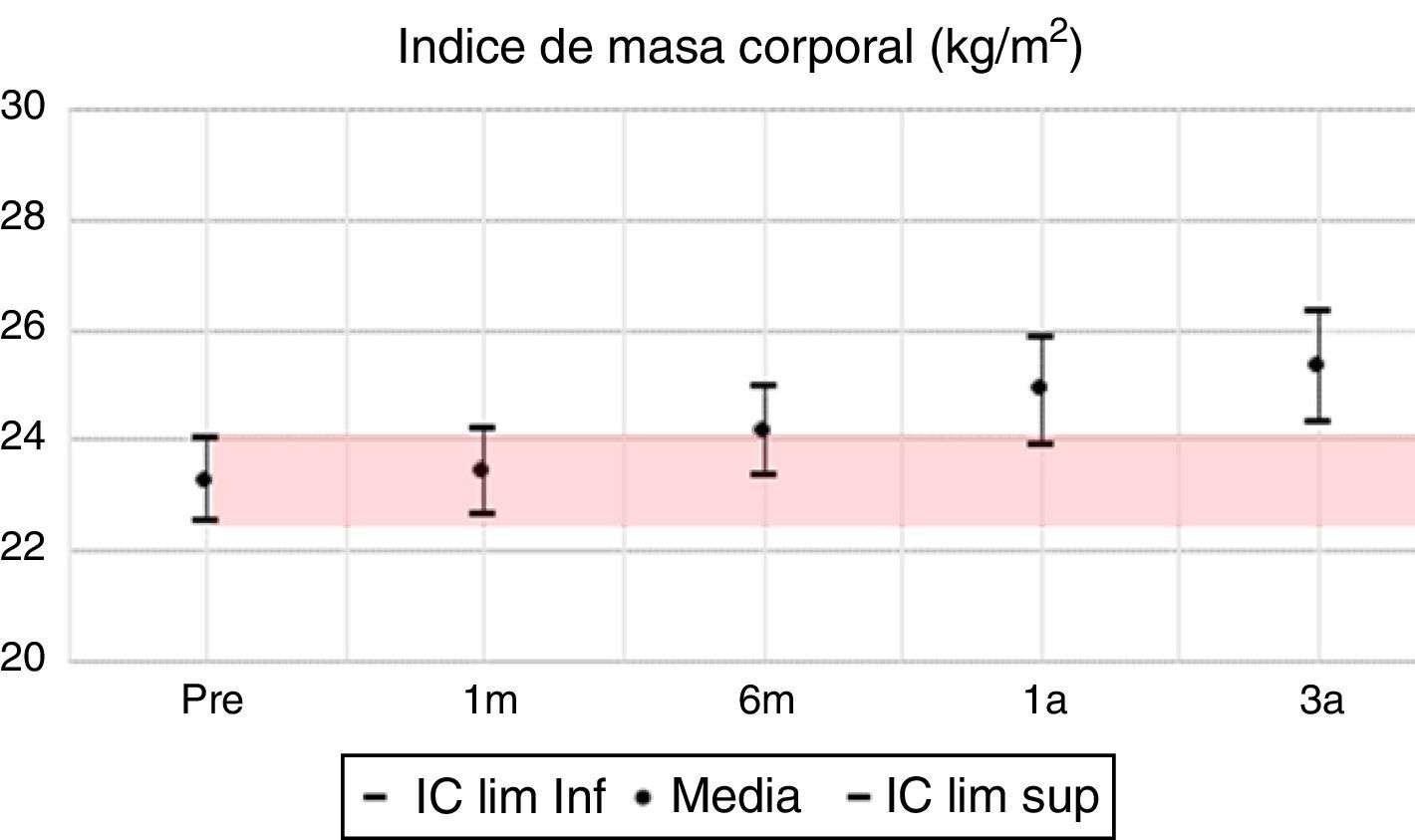
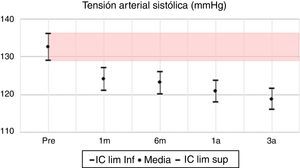
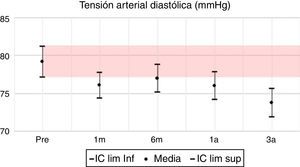
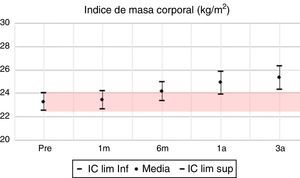
En las variables clínicas PAS, PAD e IMC, aun cuando las variaciones porcentuales y absolutas no son amplias, se evidencian diferencias estadísticamente significativas. La PAS tiene su mayor variación en el tercer año, alcanzando un 10% de descenso respecto al valor pretrasplante; la PAD desciende aproximadamente un 7% y el IMC incrementa en un 9%, pasando de una media de 22,7kg/m2 en el pretrasplante a 24,5kg/m2 a los 3 años. Todas las variables clínicas presentan diferencias estadísticamente significativas (tabla 7, figs. 1–13).
Porcentajes de diferencia y diferencias absolutas entre los valores pretrasplante y el seguimiento a 1 mes, 6 meses, 1 año y 3 años
| Variable | 1 mes | 6 meses | 1 año | 3 años | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| % Dif. | Dif. abs. | p | % Dif. | Dif. abs. | p | % Dif. | Dif. abs. | p | % Dif. | Dif. abs. | p | |
| Leucocitos | 3 | 193,0 | 0,737 | 12 | –865,3 | 0,000 | 2 | 156,9 | 0,505 | 2 | 128,5 | 0,505 |
| Neutrófilos | 29 | 18,9 | 0,000 | 2 | 1,6 | 0,039 | 3 | 2,0 | 0,048 | –2 | –1,3 | 0,048 |
| Linfocitos | –68 | –14,7 | 0,000 | –19 | –4,1 | 0,002 | –10 | –2,1 | 0,106 | 7 | 1,4 | 0,106 |
| Hb | 0 | 0,0 | 0,987 | 10 | 1,1 | 0,000 | 6 | 0,7 | 0,004 | 3 | 0,3 | 0,004 |
| Plaquetas | 16 | 43.831,0 | 0,000 | 3 | 8.788,8 | 0,209 | 2 | 4.799,7 | 0,584 | 1 | 2.505,6 | 0,584 |
| Creatinina | –81 | –6,7 | 0,000 | –83 | –6,9 | 0,000 | –82 | –6,8 | 0,000 | –84 | –6,9 | 0,000 |
| TFG | 275 | 45,5 | 0,000 | 309 | 51,1 | 0,000 | 341 | 56,5 | 0,000 | 304 | 50,4 | 0,000 |
| Glucosa | 3 | 2,8 | 0,031 | 10 | 9,5 | 0,005 | 4 | 4,3 | 0,132 | 4 | 4,3 | 0,132 |
| Colesterol | 6 | 12,1 | 0,009 | 1 | 2,5 | 0,226 | –3 | –5,0 | 0,924 | 2 | 3,0 | 0,924 |
| Triglicéridos | 8 | 15,7 | 0,120 | 6 | 12,0 | 0,157 | –3 | –5,9 | 1,000 | –3 | –6,5 | 1,000 |
| PAS | –6 | –8,6 | 0,000 | –7 | –9,5 | 0,000 | –9 | –11,8 | 0,000 | –10 | –13,8 | 0,000 |
| PAD | –4 | –3,1 | 0,013 | –3 | –2,2 | 0,049 | –4 | –3,2 | 0,003 | –7 | –5,4 | 0,003 |
| IMC | 1 | 0,2 | 0,728 | 4 | 0,9 | 0,000 | 7 | 1,6 | 0,000 | 9 | 2,1 | 0,000 |
Nota: Los valores en negrita corresponden a las diferencias estadísticamente significativas.
% Dif.: porcentaje de diferencia=(valor postrasplante–valor pretrasplante)/valor pretrasplante.
Dif. abs.: Diferencia absoluta: valor postrasplante–valor pretrasplante.
La p corresponde a la prueba no paramétrica para comparación de medias independientes U de Mann-Whitney.
Hb: hemoglobina; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAS: presión arterial sistólica; TFG: tasa de filtración glomerular.
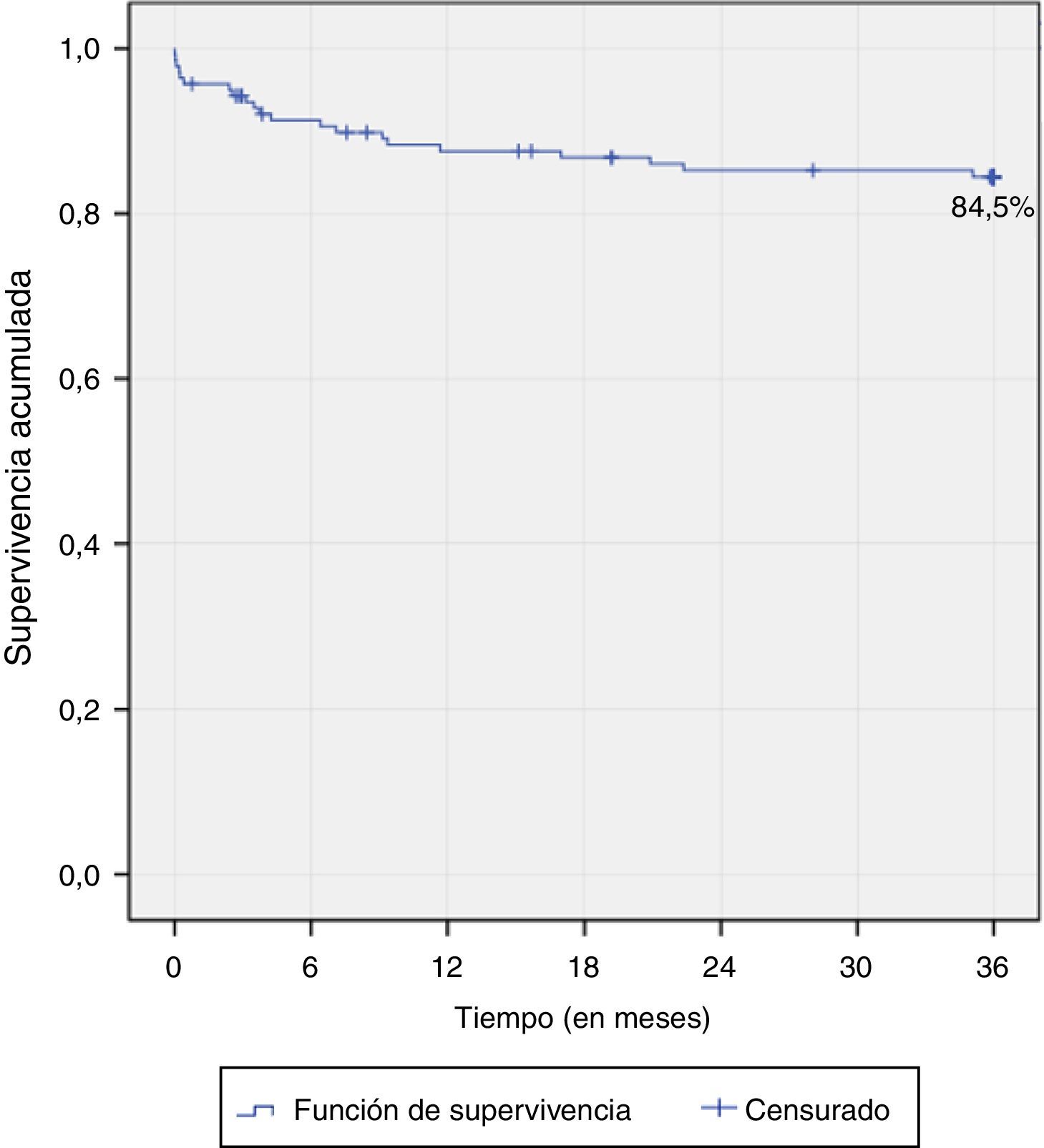
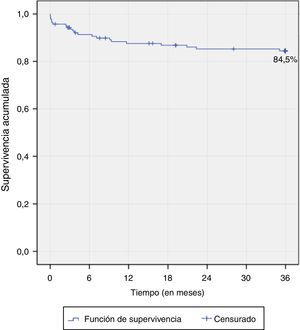
Supervivencia o sobrevida del injerto y del paciente. Para el cálculo de la supervivencia o sobrevida del injerto y del paciente con seguimiento a 3 años se utilizó el método de Kaplan-Meier.
Con un total de 21 pérdidas del injerto, este alcanzó una sobrevida a 3 años de seguimiento del 84,5%. En los primeros 6 meses la sobrevida del injerto fue del 91,3%, con 12 pérdidas durante el periodo. Para el primer año la sobrevida fue del 87,6%, con 5 pérdidas más, y para el segundo año se alcanzó una sobrevida del 85,2% (fig. 14). Durante el primer año postrasplante se presentaron cerca del 80% del total de pérdidas del injerto.
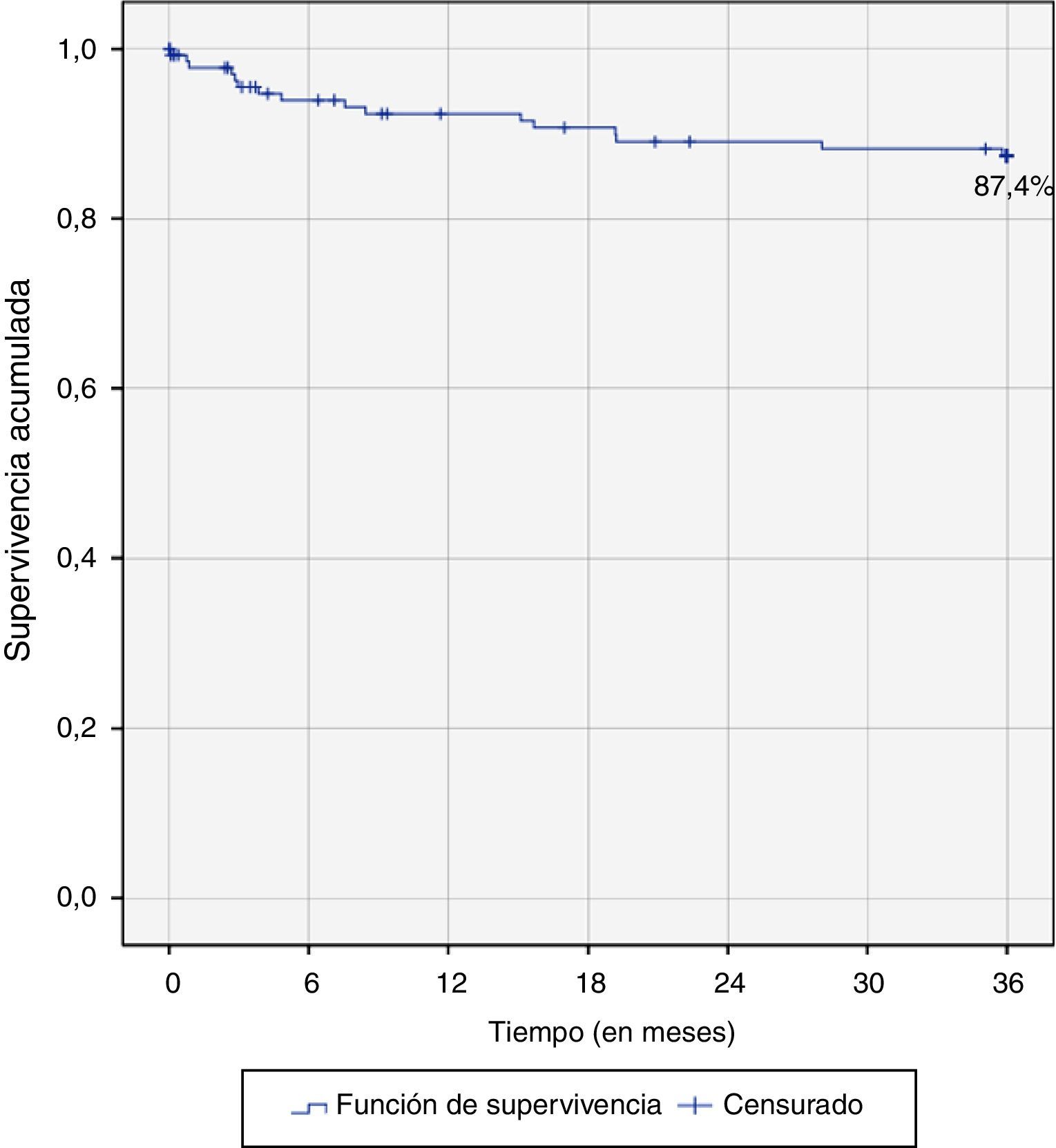
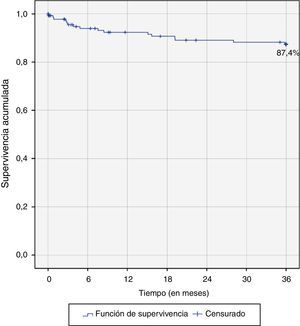
En el primer año se presentaron un total de 10 muertes, alcanzando una sobrevida acumulada de 92,4%. Para el segundo año, con 4 muertes más, se llegó a una sobrevida del 89,1% y para el tercer año, con 2 pacientes fallecidos, la sobrevida acumulada fue del 87,4% (fig. 15). En el periodo de seguimiento de 3 años, un total de 16 pacientes fallecieron.
DiscusiónEl trasplante renal se ha constituido en una alternativa considerada como la más costo-efectiva en el manejo de la enfermedad renal crónica3,5. El seguimiento paraclínico y clínico de los pacientes y la sobrevida del injerto renal y de los pacientes constituyen elementos fundamentales de observación en los pacientes trasplantados9.
Con relación a la celularidad sanguínea, el estudio evidenció un conteo de leucocitos y una distribución porcentual de neutrófilos y linfocitos en rangos considerados de normalidad para la población en general. El estudio de Weissenbacher et al.11 presenta resultados similares en un análisis retrospectivo comparativo entre el uso de alemtuzumab y basiliximab como manejo de inducción. Allí se presenta una media porcentual de linfocitos pretrasplante alrededor de 23%, con cambios significativos en el postrasplante, descendiendo a 2,61±3,11% entre el día 7 y la tercera semana, y acercándose a los niveles basales con media de 18,2±11,48% entre el tercer y el sexto mes, para el grupo de alemtuzumab.
En Turquía, Çankaya et al.12 compararon grupos de pacientes trasplantados con derecho preferente y sin derecho preferente, analizando la razón neutrófilos/linfocitos pretrasplante y al año postrasplante, con valores en leucocitos alrededor de 7.000 y entre 3,3 y 3,5 las razones neutrófilos/linfocitos. Respecto a la línea roja, el valor más alto de hemoglobina se evidenció al sexto mes postrasplante, con una media de 12,8g/dl, y el más bajo en el primer mes, con un valor igual al pretrasplante de 11,6g/dl. El gran estudio multicéntrico en 17 países europeos del año 200313, que involucró 4.263 pacientes, reveló un incremento en el promedio de hemoglobina entre 1,1 a 2g/dl en el seguimiento a los 6 meses, un año, 3 años y 5 años, mayor a la experiencia local, en donde el incremento observado fue entre 0,3 y 1,1g/dl. El estudio europeo identificó una prevalencia de anemia del 38%, doblando la prevalencia encontrada en Turquía14 con un 19% de pacientes anémicos, y en donde se señala un promedio de Hb de 13,2g/dl, con una media de tiempo postrasplante de 79 meses. El estudio de Radoui et al.15 relaciona una serie de trabajos con prevalencias de anemia (con base en el nivel de Hb <12g/dl) entre 31,85 y 44,8, valores entre los que se encuentra la serie del presente estudio.
Durante el seguimiento de los pacientes trasplantados el perfil lipídico presenta leve variabilidad en sus valores y no se evidencian diferencias con significación estadística, destacando la limitación de la ausencia de categorización de los valores de colesterol y triglicéridos en los rangos de normalidad y dislipidemia. El estudio español de Fernández Castillo et al.16, por el contrario, categoriza los resultados del perfil lipídico señalando el porcentaje de pacientes que año a año cumplen criterio de dislipidemia, pasando de un 35% a un promedio de 55% durante los años posteriores. Sin embargo, el estudio no señala la evaluación de la significación estadística de las diferencias encontradas. Adicionalmente, presenta los valores medios con resultados muy similares al primer y al tercer año para el colesterol (202,6mg/dl y 189,9mg/dl vs. 190,2mg/dl y 198mg/dl del estudio presente), y con una diferencia significativa en los valores de triglicéridos incluso desde el pretrasplante (143mg/dl), con incremento en los años de seguimiento, alcanzando una media de 150mg/dl para el tercer año; el estudio actual describe medias de los triglicéridos en un rango de 210 y 180mg/dl, con el mayor valor al primer mes y el menor en el tercer año. Para el grupo de Kisielnicka et al.17, las diferencias en colesterol y los valores del estudio fueron mayores y más adversos, señalando la tendencia a la hipercolesterolemia de los pacientes trasplantados, pero compartiendo resultados similares frente al comportamiento de los triglicéridos, en los cuales se observó una estabilidad en sus valores postrasplante.
La presión arterial presenta una evolución favorable en el seguimiento, observando diferencias estadísticamente significativas en las cifras sistólicas y diastólicas frente a los valores pretrasplante, similar a lo observado en la literatura mundial18.
Frente al IMC, la tendencia de los pacientes trasplantados es a aumentar de peso. Fernández Castillo et al. documentan en España un incremento cercano a 2kg/m2 en el primer año y cerca de 0,5kg/m2 hasta el quinto año, señalando que desde el pretrasplante se parte de un IMC mayor a 2519; en la serie de Vega20, estudio chileno que evalúa la influencia de la ganancia de peso en los desenlaces comparando ganancias menores y mayores al 15%, se señala que el mayor incremento se presenta durante los primeros 6 meses y el promedio de aumento de peso a los 6 meses es de 6,6kg. En Medellín, Nieto-Ríos et al.21 describen una media de incremento en el IMC al año de 1,5±2,9kg/m2, con diferencia estadísticamente significativa frente al valor pretrasplante. Esta situación es advertida en el presente estudio, en donde el incremento al tercer año alcanzó cerca del 10% en el IMC y la diferencia frente al pretrasplante fue significativa. Sasaki et al. en Japón22, en una evaluación realizada a 31 pacientes con un promedio de tiempo postrasplante de 16 años, identificaron un IMC promedio de 20kg/m2, sin advertir el IMC pretrasplante. En Brasil, el trabajo de Alencastro et al.23, que caracteriza el síndrome metabólico en los pacientes trasplantados y su relación con la función del injerto e inflamación, identifica que el 59% de los pacientes tienen sobrepeso (41,5%) u obesidad (17,5%). Es importante señalar que existen diferencias por regiones del mundo en el IMC24, sin embargo, lo observado en la literatura con más frecuencia es el reporte del incremento en el peso y su consiguiente aumento en el IMC.
La supervivencia del injerto y del paciente son quizá los resultados más relevantes en el seguimiento del paciente trasplantado. La literatura reporta mejores resultados en sobrevida del paciente en el trasplante de donantes vivos25, aunque en otros estudios estos hallazgos no se respaldan26. Sin embargo, los resultados de la serie del presente estudio presentan un comportamiento similar a lo reportado por los anteriores estudios citados. Se reportan diferentes factores asociados a la sobrevida del paciente y del injerto, como las complicaciones posquirúrgicas, las infecciones, la edad del donante, el tiempo de isquemia fría, entre otros27, señalando que el presente estudio no se planteó como objetivo la identificación de factores asociados a los desenlaces de mortalidad o pérdida del injerto.
ConclusionesEl trasplante renal se ha consolidado como la alternativa más costo-efectiva para el manejo de la enfermedad renal crónica en estadio avanzado (estadio 5). La serie actual evidencia el comportamiento clínico y paraclínico de las variables de mayor relevancia, junto con la evaluación de la sobrevida. Los resultados de la experiencia de la Unidad de Trasplante Renal del Hospital Universitario de Neiva tienen un comportamiento muy similar a lo reportado en la literatura, tanto en países con condiciones socioeconómicas similares como en países con mayor desarrollo. Este estudio pretende dar pie a nuevos interrogantes frente al trasplante renal en la búsqueda de la generación del mayor beneficio para los pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos que permitan identificaciones individuales de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.