El ronquido es un problema altamente prevalente, que afecta a millones de personas a nivel mundial. Impacta negativamente en la calidad de vida al afectar la relación de pareja y la calidad de sueño, además de constituir un factor de riesgo cardiovascular. El objetivo de esta revisión es analizar y discutir los aspectos más relevantes de esta condición, desde su etiopatogenia hasta las diferentes alternativas terapéuticas disponibles. En la evaluación del paciente roncador se debe realizar un minucioso examen de nariz, boca, faringe, cuello y esqueleto facial, además de estimar el riesgo de que exista una apnea obstructiva del sueño asociada. Son de utilidad una serie de cuestionarios que permiten asignar puntaje a la sintomatología del paciente y evaluar su impacto en la vida diaria. En general, el estudio deberá incluir exámenes radiológicos, endoscopías de la vía aérea superior (con el paciente despierto y bajo sueño inducido por medicamentos) y estudios del sueño, que se pueden realizar tanto en forma ambulatoria como hospitalizado. Existe una amplia gama de tratamientos disponibles para el ronquido, los que han demostrado una alta efectividad en diferentes subgrupos de pacientes: bajar de peso, dejar de fumar, medicamentos antialérgicos, terapia postural, ejercicios faríngeos, dispositivos de avance mandibular y procedimientos quirúrgicos que van desde intervenciones mínimamente invasivas hasta procedimientos avanzados como cirugía robótica, avances máxilo-mandibulares y la estimulación del nervio hipogloso. Es clave para manejar exitosamente el ronquido el realizar una evaluación detallada del paciente y establecer un plan terapéutico personalizado.
Snoring is a highly prevalent problem, affecting millions of people worldwide. It negatively impacts quality of life by affecting couple relationships and sleep quality, as well as being a cardiovascular risk factor. The aim of this review article is to analyze and discuss the most relevant aspects of this condition, ranging from its etiology and pathogenesis to the different available therapeutic options. When evaluating a snoring patient, a thorough examination of the nose, mouth, pharynx, neck and facial skeleton should be performed, and the risk of having an associated obstructive sleep apnea must be estimated. A series of questionnaires are useful to assign scores to the patient's symptoms and assess their impact on daily life. In general terms, patient evaluation should include radiological examinations, upper airway endoscopies (awake and under drug-induced sleep) and sleep studies, which can be performed both on an outpatient or inpatient basis. There is a wide range of treatments available for snoring, which have shown high effectiveness in different patient subgroups: weight loss, quitting smoking, anti-allergic medications, postural therapy, pharyngeal exercises, mandibular-advancement devices and surgical procedures ranging from minimally invasive interventions to advanced procedures such as robotic surgery, maxillomandibular advancement and hypoglossal nerve stimulation. The cornerstone for a successful snoring management is to perform a detailed patient evaluation and to establish a personalized therapeutic plan.
El ronquido es un fenómeno acústico, consecuencia de la vibración y el colapso de las estructuras de la vía aérea superior (VAS) que ocurre durante el sueño. Esto se produce por la hipotonía muscular y la presión inspiratoria negativa al dormir, lo que puede o no asociarse a apnea del sueño. La hipotonía es característica del sueño profundo, llegando a su máximo en el sueño REM1. Aunque su prevalencia en la población general es difícil de estimar, puede llegar a presentarse en más del 50% de los individuos adultos, siendo más frecuente en hombres que en mujeres2. La prevalencia del ronquido aumenta con la edad y con el índice de masa corporal, aunque algunos autores consideran más específica su relación con el diámetro del cuello. La posición al dormir es otra variable relevante: el ronquido aumenta en decúbito supino, y se atenúa en decúbito lateral, por el efecto de la gravedad sobre las partes blandas de la VAS. Este problema aumenta con el consumo de relajantes musculares, benzodiacepinas y alcohol, al producir hipotonía en la musculatura orofaríngea. El ronquido también se asocia a ciertas patologías, tales como el reflujo gastroesofágico y el hipotiroidismo3,4, a hábitos como el tabaquismo y a condiciones fisiológicas como el embarazo5.
La presencia de ronquido como factor de riesgo cardiovascular ha sido investigada en múltiples estudios, y en la mayoría de ellos se ha encontrado que la prevalencia de enfermedades cardiovasculares en pacientes roncadores es superior que en los sujetos no roncadores. Sin embargo, esta asociación está más claramente establecida con el síndrome de apnea-hipoapnea obstructiva del sueño (SAHOS), considerado como la culminación de un proceso que comienza con el ronquido simple y que, de acuerdo con el momento evolutivo en que sea diagnosticado, tendrá diferentes manifestaciones clínicas y gravedad6.
El ronquido es una causa relevante de problemas de pareja, alterando la calidad de sueño del compañero de cama: se estima que la mitad de las parejas de roncadores prefieren dormir en cuartos separados7.
EtiopatogeniaEl ronquido ocurre tanto por la presencia de una VAS estrecha, como por la ineficacia de los músculos dilatadores de ésta que no logran contrarrestar su tendencia al colapso inspiratorio3,8. La presión crítica (PCrit) es una variable que representa la colapsabilidad de la vía aérea superior: su valor es más alto en los pacientes con SAHOS, es francamente menor en los roncadores simples y suele tener valores negativos en pacientes sin trastornos del sueño.
Dentro de los factores que determinan una mayor colapsabilidad, destaca el sobrepeso y la obesidad: con el aumento de peso se generan depósitos grasos en las paredes faríngeas laterales y en el espesor de la lengua, estrechando el lumen de la VAS. Junto a esto, se produce una elevación del diafragma y una disminución del volumen pulmonar, lo que desestabiliza la vía aérea superior y aumenta la PCrit.
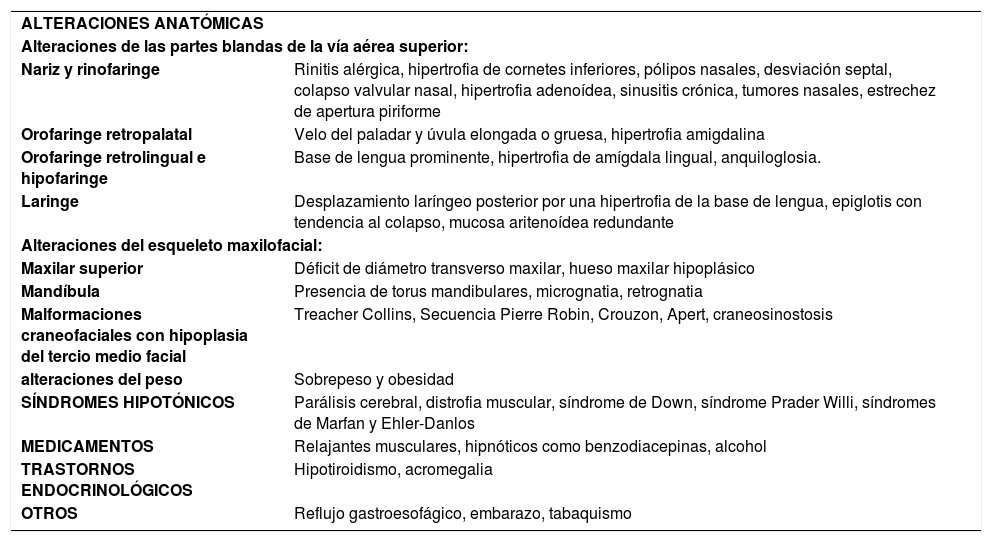
También son causa de una mayor colapsabilidad de la VAS las alteraciones anatómicas que provocan una obstrucción a nivel nasal, faríngeo, laríngeo y del esqueleto maxilofacial. Asimismo, son relevantes también las alteraciones hormonales, los efectos farmacológicos y factores irritantes locales como el reflujo gastroesofágico y el tabaco. Es importante tener en cuenta que, en la mayoría de los pacientes, el ronquido es un problema multifactorial (Tabla 1).
Factores que predisponen al ronquido en niños y adultos
| ALTERACIONES ANATÓMICAS | |
| Alteraciones de las partes blandas de la vía aérea superior: | |
| Nariz y rinofaringe | Rinitis alérgica, hipertrofia de cornetes inferiores, pólipos nasales, desviación septal, colapso valvular nasal, hipertrofia adenoídea, sinusitis crónica, tumores nasales, estrechez de apertura piriforme |
| Orofaringe retropalatal | Velo del paladar y úvula elongada o gruesa, hipertrofia amigdalina |
| Orofaringe retrolingual e hipofaringe | Base de lengua prominente, hipertrofia de amígdala lingual, anquiloglosia. |
| Laringe | Desplazamiento laríngeo posterior por una hipertrofia de la base de lengua, epiglotis con tendencia al colapso, mucosa aritenoídea redundante |
| Alteraciones del esqueleto maxilofacial: | |
| Maxilar superior | Déficit de diámetro transverso maxilar, hueso maxilar hipoplásico |
| Mandíbula | Presencia de torus mandibulares, micrognatia, retrognatia |
| Malformaciones craneofaciales con hipoplasia del tercio medio facial | Treacher Collins, Secuencia Pierre Robin, Crouzon, Apert, craneosinostosis |
| alteraciones del peso | Sobrepeso y obesidad |
| SÍNDROMES HIPOTÓNICOS | Parálisis cerebral, distrofia muscular, síndrome de Down, síndrome Prader Willi, síndromes de Marfan y Ehler-Danlos |
| MEDICAMENTOS | Relajantes musculares, hipnóticos como benzodiacepinas, alcohol |
| TRASTORNOS ENDOCRINOLÓGICOS | Hipotiroidismo, acromegalia |
| OTROS | Reflujo gastroesofágico, embarazo, tabaquismo |
La anamnesis del paciente roncador deberá investigar la severidad de este síntoma, su frecuencia (ocasional o todas las noches), la presencia de pausas respiratorias y la asociación a otras alteraciones del sueño como reflujo nocturno, insomnio, nicturia y pesadillas. En general, para realizar una completa historia clínica sobre el ronquido se debe consultar a la pareja del paciente9. También se debe preguntar si el paciente presenta una obstrucción nasal crónica e investigar sus posibles causas: inflamatorias (rinitis alérgica y no alérgica), infecciosas (rinosinusitis crónica) y alteraciones anatómicas (desviación septal, hipertrofia de cornetes)10. Es importante también documentar el uso de medicamentos como ansiolíticos y relajantes musculares.
Es muy importante preguntar por síntomas sugerentes de SAHOS, ya que su presencia se asocia a una mayor morbimortalidad y afectará el plan terapéutico: apneas observadas, sudoración nocturna, eventos asfícticos, cansancio crónico, somnolencia diurna excesiva, cefalea matinal y síntomas neurocognitivos como deficit de concentración, fallas en la memoria, cambios de humor, ansiedad y depresión.
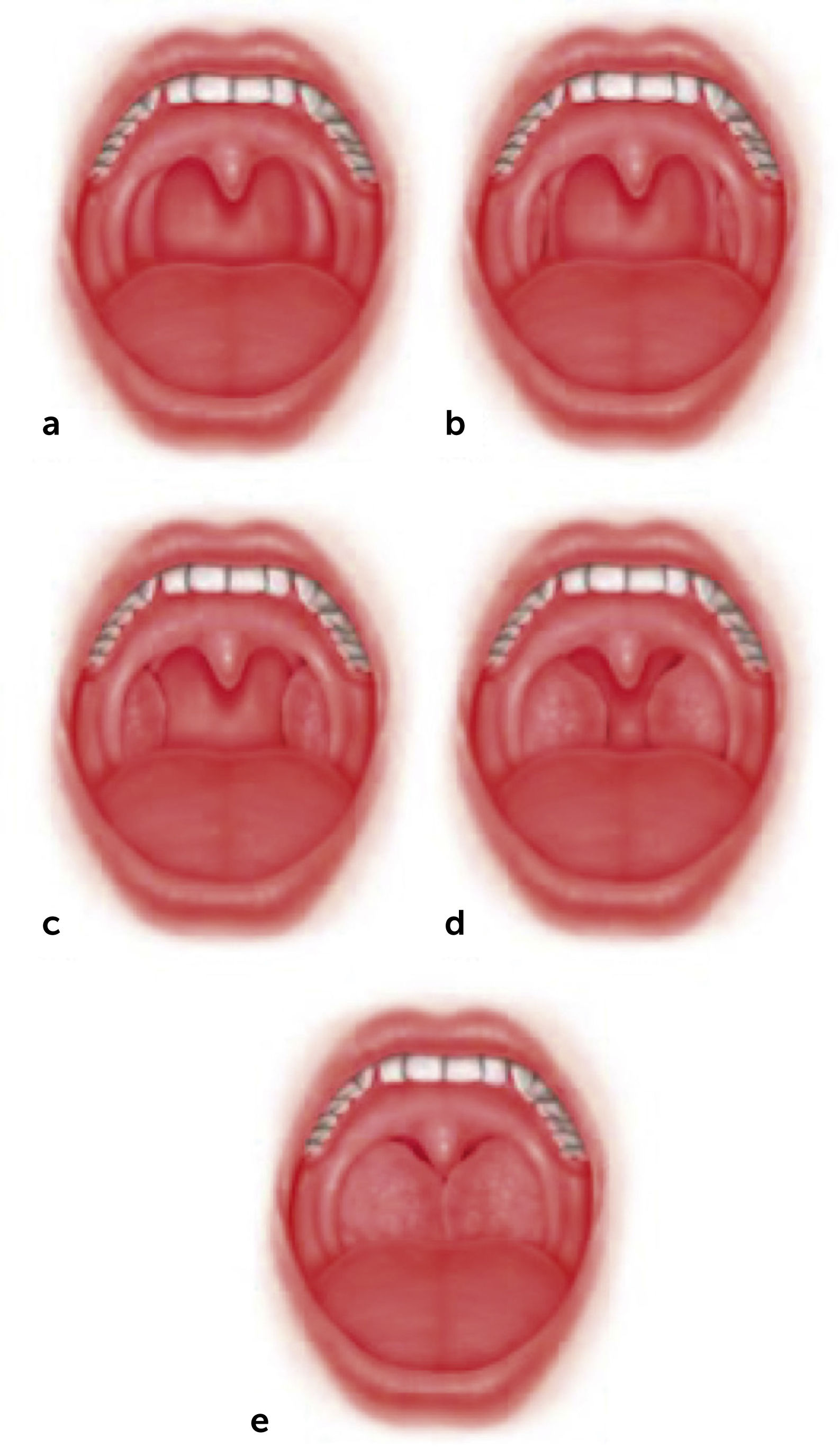
El examen físico permite detectar los factores anatómicos que producen una obstrucción de la VAS y que predisponen a la aparición del ronquido. Este debe incluir una completa exploración nasal, mediante rinoscopía anterior que puede ser complementada con una endoscopía nasal rígida o flexible, evaluando la posición del tabique nasal, el tamaño de los cornetes, signos inflamatorios de la mucosa nasal y la presencia de lesiones o anomalías anatómicas obstructivas. A nivel faríngeo, se debe realizar un detallado examen ayudado con un bajalenguas y una luz frontal. Las amígdalas se evalúan con boca abierta y la lengua en posición neutra, determinándose su tamaño según la escala de Brodsky, que va del 0 a 4: se considera grado 0 a un paciente amigdalectomizado, en el grado 1 las amígdalas están escondidas detrás del pilar anterior y en el grado 4 en que las amígdalas ocupan más del 75% del espacio faríngeo11. La relación del paladar con la lengua se describe según el test modificado de Mallampati12, el que tiene una correlación positiva con la presencia y severidad del ronquido13. Friedman popularizó unas versiones modificadas de las escalas que determinan el tamaño amigdalino (Figura 1) y la relación del paladar con la lengua (Figura 2)14. Adicionalmente, describió un sistema de etapificación de la anatomía faríngea que considera tanto esas variables como el índice de masa corporal (IMC) (Tabla 2), que tiene un potente rol predictor sobre el éxito quirúrgico en estos pacientes: a menor etapa, mayor tasa de curación con una uvulopalatofaringoplastía15.
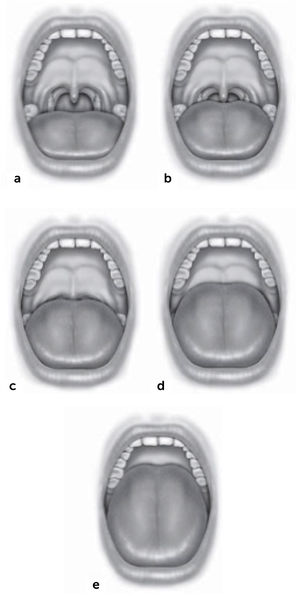
Escala de tamaño amigdalino
a. Tamaño 0, ausencia de tejido amigdalino. b. Tamaño 1, limitadas dentro de los pilares fauciales. c. Tamaño 2, alcanzan o sobrepasan ligeramente los pilares fauciales. d. Tamaño 3, se extienden más allá de los pilares. e. Tamaño 4, alcanzan la línea media.
Fuente: Friedman M, Salapatas AM, Bonzelaar LB. Updated Friedman Staging System for Obstructive Sleep Apnea. Adv Otorhinolaryngol. 2017;80:41-48. doi: 10.1159/000470859. (Ref.14).
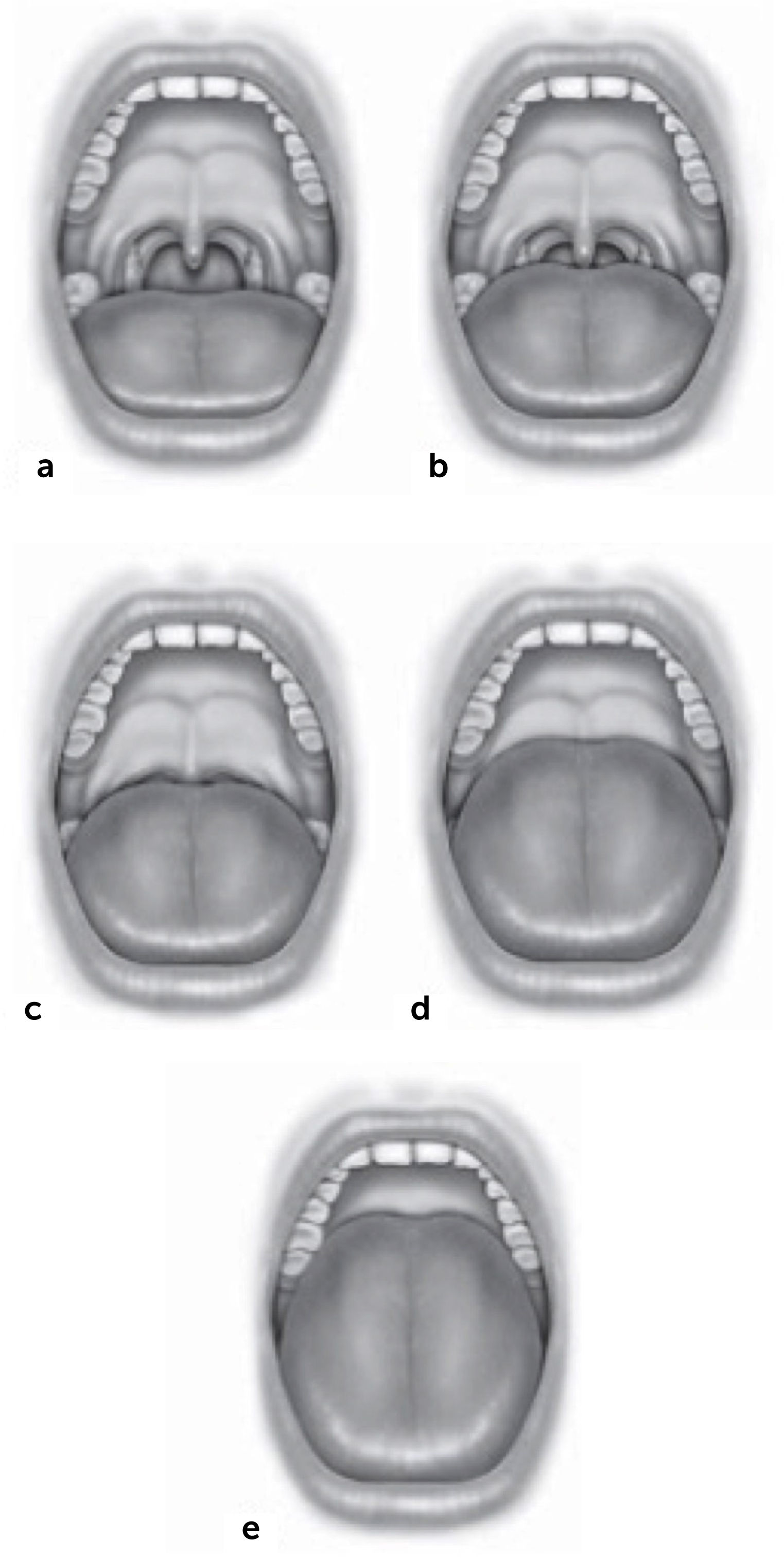
Escala modificada de Mallampati (también conocida como escala de Friedman de posición lingual) para evaluación de la relación entre paladar y lengua
a. Posición I: Se visualiza la úvula y amígdalas/pilares. b. Posición IIa: Se visualiza la mayor parte de la úvula pero no las amígdalas/pilares. c. Posición IIb: Se visualiza todo el paladar blando hasta la base uvular. d. Posición III: Muestra parte del paladar blando con su extremo distal ausente. e. Posición IV: Sólo se visualiza el paladar duro.
Fuente: Friedman M, Salapatas AM, Bonzelaar LB. Updated Friedman Staging System for Obstructive Sleep Apnea. Adv Otorhinolaryngol. 2017;80:41-48. doi: 10.1159/000470859. (Ref.14).
Se deben evaluar alteraciones craneofaciales que estrechen la VAS: retrognatia-micrognatia y baja posición del hioides en relación con el plano mandibular, entre otras16.
El análisis antropométrico es fundamental, por el rol que tiene el sobrepeso y la obesidad en el ronquido. Se debe documentar el IMC del paciente: valores sobre 30kg/m2 se asocian a un mayor riesgo de SAHOS. La circunferencia cervical (CC) debe ser medida en todos estos pacientes, dado que se correlaciona fuertemente con la permeabilidad de la VAS y la presencia de trastornos respiratorios del sueño. La CC suele ser mayor en pacientes roncadores que en controles sanos, y se asocia a un riesgo elevado de SAHOS cuando supera los 43cm. en hombres y los 40cm. en mujeres.
Exámenes complementariosDependiendo de los hallazgos de la evaluación clínica inicial, se podrán solicitar exámenes que permitan profundizar el análisis anatómico de la vía aérea del paciente.
Tomografía de cavidades paranasales: Permite confirmar y determinar la severidad de las alteraciones anatómicas detectadas al examen físico, además de definir si existen procesos inflamatorios-infecciosos rinosinusales asociados.
Cefalometría: Examen radiológico que permite la medición de una serie de parámetros craneofaciales y de permeabilidad de la VAS que se relacionan con la existencia de ronquido y SAHOS, especialmente en pacientes no obesos.
Medición del flujo nasal: Puede realizarse en forma simple, no invasiva mediante una rinomanometría anterior o una rinometría acústica. La rinomanometría anterior permite medir la resistencia nasal (rango normal entre 0,10 a 0,3Pa/cm3/s). La rinometría acústica se basa en el análisis de ondas sonoras reflejadas en la cavidad nasal, determinando las áreas de sección transversal y volumen nasal17. Sin embargo, existe poca evidencia de que estos métodos objetivos sean superiores a los métodos subjetivos (anamnesis, escalas sintomáticas) para evaluar la obstrucción nasal.
Nasofaringolaringoscopía flexible: Examen endoscópico que evalúa, en el paciente despierto, la permeabilidad de la VAS desde la nariz hasta la hipofaringe y laringe. Mediante este procedimiento se puede visualizar la longitud y grosor del paladar, la úvula, el lumen faríngeo, el tamaño amigdalino, el volumen de la base de la lengua y la posición laríngea. La maniobra de Muller permite evaluar, en forma dinámica, la tendencia al colapso de la faringe, solicitándole al paciente que realice una inspiración forzada con la boca cerrada y nariz tapada18. La exploración endoscópica de la VAS en el paciente despierto tiene una alta sensibilidad en determinar la presencia de obstrucción a nivel alto (orofaringe y velo del paladar).
Endoscopía del sueño inducida por fármacos: Más conocida como DISE por su sigla en inglés (Drug Induced Sleep Endosocopy), este examen ofrece una evaluación dinámica del tamaño y colapsabilidad de la vía aérea en un estado que imita el sueño natural del paciente, mediante el uso de medicamentos endovenosos (habitualmente midazolam, dexmedetomidina o propofol). Se determina mediante un puntaje el grado de obstrucción y la configuración de dicha obstrucción, en los diferentes sitios de la VAS. Permite determinar el colapso a nivel bajo (base de la lengua y epiglotis), el que habitualmente no se visualiza en los estudios con el paciente despierto19.
Escalas sintomáticasSe han diseñado diferentes escalas que permiten evaluar la intensidad de los síntomas asociados a los trastornos respiratorios del sueño y su impacto en la calidad de vida de los pacientes. Algunos de estos instrumentos, que incluyen tanto síntomas como variables antropométricas, permiten realizar un tamizaje para detectar, dentro del grupo de los sujetos roncadores, a los que presentan un mayor riesgo de tener SAHOS20.
Escala NOSE (Nasal Obstructive Symptom Evaluation)21: Es una herramienta para objetivar el grado de obstrucción nasal que presenta el paciente. Es un cuestionario breve, con 5 preguntas que se valoran de 0 a 4 y luego se multiplican por 5, correspondiendo un valor de 100 a la máxima obstrucción nasal posible. Existe una correlación entre la presencia de obstrucción nasal y la calidad del sueño, el nivel de ronquido y la somnolencia diurna excesiva13.
Escala de somnolencia de Epworth: Es un cuestionario autocompletado compuesto por 8 preguntas que evalúan la somnolencia diurna en 8 situaciones o actividades de la vida diaria. Se asigna un valor de 0 a 3 para cada pregunta y la puntuación total puede oscilar entre 0 y 24. Un puntaje bajo 11 se considera normal (bajo riesgo de somnolencia), mientras que valores entre 11 y 24 orientan a un alto riesgo de somnolencia22.
stop-bang: Instrumento que incluye ocho preguntas que se responden en modo binario, sí/no, acerca de la existencia de ronquido intenso, somnolencia diurna o fatigabilidad, apneas presenciadas durante el sueño, diagnóstico de hipertensión arterial (HTA), edad, género, índice de masa corporal y circunferencia cervical. Los trabajos muestran que tiene alta sensibilidad, pero baja especificidad, para la detección de SAHOS23.
Índice de Flemons: Corresponde a la medición de la circunferencia cervical (CC) ajustada. A la medición de la CC en cm. se le suma un puntaje por la presencia de HTA (4 puntos), presencia de ronquido habitual (3 puntos) y apneas presenciadas (3 puntos). El riesgo de que exista un SAHOS asociado es bajo con puntajes bajo 43, pero es alto con valores sobre 4824.
Escala de Thornton: Cuestionario con 5 preguntas que se puntúan entre 0 (nunca) y 3 (la mayoría de las veces) y que evalúa el impacto del ronquido en las relaciones interpersonales del paciente.
Estudios del sueñoEn aquellos pacientes roncadores con riesgo al menos moderado de presentar SAHOS, se deben solicitar estudios objetivos del sueño. En la actualidad existen diferentes tipos de estudios del sueño, cada uno con sus ventajas y limitaciones (Tabla 3).
Tipos de estudios del sueño
| Tipo de estudio | Descripción |
|---|---|
| Estudio tipo I: polisomnograma (PSG) convencional | Aún considerado el gold standard de los estudios del sueño. Cuenta con al menos siete canales, incluyendo electroencefalograma (EEG), electro-oculografía (EOG), electromiografía de mentón, electrocardiograma, flujo aéreo vía cánula nasal, esfuerzo respiratorio (tórax y abdomen) y oximetría de pulso. Es realizado en laboratorio y con la supervisión de un técnico especializado. |
| Estudio tipo II: PSG ambulatorio | PSG completa, pero realizada con equipo portátil en el domicilio del paciente, sin supervisión técnica. |
| Estudio tipo III: poligrafía respiratoria ambulatoria | Estudio ambulatorio con menos canales. Incluye dos variables respiratorias (movimiento respiratorio, flujo aéreo), variable cardíaca (ritmo cardíaco o electrocardiograma) y saturación arterial de oxígeno. Puede incluir adicionalmente registro de ronquido y de posición corporal. |
| Estudio tipo IV: análisis simple o dual | Equipos continuos simples o de canal dual que incluye registro de flujo aéreo y saturación de O2. |
En el Centro del Sueño de Clínica Las Condes se realizan regularmente estudios tipo I y III. En general, se solicita un PSG en laboratorio a los pacientes roncadores con baja probabilidad de SAHOS (Flemons <43, STOP-BANG <3), dado que es un examen con mayor sensibilidad, o bien cuando se sospecha la presencia de algún otro trastorno del sueño. En cambio, aquellos pacientes con moderado y alto riesgo de SAHOS (Flemons ≥43, STOP - BANG ≥3) se estudian con una poligrafía respiratoria ambulatoria, que suele ser suficiente para confirmar el diagnóstico.
TratamientoEl ronquido puede ser manejado mediante distintas estrategias. Muchas de ellas serán complementarias entre sí, y dependerán de las causas del problema que se hayan logrado establecer durante la evaluación del paciente.
Baja de peso: En aquellos pacientes con sobrepeso y obesidad, en especial si este factor se ha relacionado con la aparición o agravamiento de los ronquidos, establecer un plan de control del peso es fundamental. Se deberá implementar una dieta hipocalórica, un plan de aumento de actividad física y, en muchos casos, el apoyo con tratamiento farmacológico, bajo la supervisión de un médico nutriólogo. La cirugía bariátrica deberá ser considerada en pacientes con obesidad mórbida y/o con comorbilidades25. Se ha establecido una correlación entre la baja de peso, una reducción del tamaño de la lengua y una mayor permeabilidad de la vía respiratoria alta, aliviando el ronquido y la apnea del sueño26.
Cesación de tabaquismo: La inflamación producida en la vía aérea superior por el hábito de fumar agudiza la intensidad y frecuencia del ronquido27. Estudios han demostrado que dejando de fumar, el ronquido se atenúa en forma significativa28. El paciente puede ser derivado a un programa multidisciplinario que le ayude a abandonar este hábito.
Tratamiento antialérgico: La rinitis alérgica produce edema de la mucosa nasal, acumulación de secreciones y obstrucción nasal, todo lo cual puede producir o exacerbar el ronquido29. En pacientes riníticos que consultan por ronquido, se debe iniciar un tratamiento antialérgico consistente en la asociación de antihistamínicos y corticoides tópicos nasales. En pacientes atópicos, el tratamiento antialérgico suele atenuar el ronquido, mejorar la calidad de sueño, la somnolencia diurna e incluso reducir el índice de apnea-hipoapnea30, aunque rara vez será curativo, por sí solo, de una apnea obstructiva del sueño. Adicionalmente, el manejo de la alergia nasal constituye una terapia coadyuvante a otros tratamientos que se deban implementar.
Maniobras posturales: En la mayoría de los casos, el ronquido empeora en decúbito supino y se atenúa en decúbito lateral o prono. Este fenómeno puede ser corroborado por la pareja, y en algunos casos el estudio del sueño puede confirmar un predominio de las apneas al dormir de espalda. Para manejar este problema, tradicionalmente se han utilizado diferentes dispositivos para dormir que hagan incómodo el estar en decúbito supino y así habitúen al paciente a dormir de costado, como son algunas mochilas modificadas o poleras con un bolsillo en la espalda, donde se ubica una pelota de tenis31. Más recientemente se han desarrollado sistemas electrónicos que detectan cuando el paciente duerme en decúbito supino, enviando señales vibro-táctiles para que cambie su posición sin despertarlo32.
Terapia miofuncional: Este tratamiento realizado por fonoaudiólogos consiste en una serie de ejercicios que permiten tonificar la musculatura orofaríngea y con ello prevenir el colapso de la vía aérea a este nivel al dormir. Está indicado en pacientes roncadores sin apneas, o en apnea del sueño leve y moderada, y diversos estudios han demostrado una significativa reducción de la intensidad y frecuencia del ronquido33,34.
Dispositivo de avance mandibular (DAM): Semejantes a los planos de relajación que se indican para el bruxismo, los DAM son diseñados y adaptados por odontólogos y cirujanos máxilo-faciales especialistas, con el propósito de desplazar hacia adelante la mandíbula durante el sueño, previniendo el colapso hacia posterior de la lengua y ampliando las dimensiones faríngeas. Está indicado en pacientes roncadores sin apneas, o en apnea del sueño leve a moderada, sin patología nasal asociada35,36.
Presión positiva continua de vía aérea: Conocido como CPAP por su sigla en inglés, es un tratamiento que proporciona un soporte neumático a la VAS a través de un flujo continuo de aire que se aplica a través de interfaces nasales (nariceras) o máscaras oronasales. En general se reserva para pacientes con SAHOS moderado a severo, tiene una alta eficacia en reducir los eventos obstructivos y la somnolencia diurna37, pero su adherencia a largo plazo no supera el 60-70%38.
Cirugía del Sueño: Se agrupan bajo este concepto todas las intervenciones quirúrgicas que pueden realizarse en la vía aérea superior que tengan por objetivo aumentar su permeabilidad, prevenir su colapso nocturno y así manejar el ronquido y la apnea del sueño. En general, valores menores de IMC, del índice de apnea-hipoapnea (IAH) y de somnolencia diurna, así como la presencia de alteraciones anatómicas fácilmente corregibles, son predictores de éxito quirúrgico39. Cuando se realizan procedimientos en diferentes niveles de la vía respiratoria (nariz, orofaringe, hipofaringe y/o laringe) para tratar el ronquido y la apnea del sueño, se habla de la cirugía multinivel del sueño, la que ha demostrado altos niveles de efectividad y seguridad cuando se indica en pacientes bien seleccionados40. A continuación detallaremos algunos de estas intervenciones:
1) Septoplastía: La septoplastía es la cirugía indicada para tratar una obstrucción nasal crónica secundaria a una desviación del tabique nasal. En la actualidad, el apoyo endoscópico permite una muy buena visión durante la cirugía, mejorando el control de las regiones más posteriores del tabique. Es un procedimiento altamente efectivo, describiéndose tasas de éxito cercanas al 95%41. Sin embargo, su impacto en el tratamiento de la apnea del sueño es mucho menor, describiéndose tasas de curación inferiores al 20%42. No obstante lo anterior, la mayoría de los pacientes operados de septoplastía refieren presentar una mejoría significativa en la percepción de su calidad de sueño43, y este procedimiento habitualmente forma parte de la cirugía multinivel del sueño.
2) Turbinoplastía: La turbinoplastía consiste en la remodelación de los cornetes nasales, en particular los inferiores, para reducirlos de tamaño y lograr un mayor flujo de aire nasal. Suele realizarse como un procedimiento complementario a la septoplastía en pacientes con obstrucción nasal crónica y ronquido, mejorando en forma significativa su respiración nasal y calidad de vida44. En la actualidad, las dos técnicas más utilizadas son la cauterización submucosa con radiofrecuencia y la remodelación con microdebridador. La primera es más rápida y se asocia a un menor riesgo de sangrado nasal post-operatorio, mientras que algunos estudios sugieren que la segunda tendría una mayor efectividad y perdurabilidad en el aumento del flujo aéreo45.
En algunos pacientes con SAHOS moderado a severo, portadores de una desviación septal obstructiva, puede plantearse hacer una septoplastía y turbinoplastía para permitir posteriormente una mejor adaptación a un equipo de CPAP.
3) Adenoidectomía y amigdalectomía: En niños, la hipertrofia de amígdalas y de adenoides es la principal causa de ronquido y apnea del sueño. La adenoamigdalectomía es una de las cirugías más frecuentes que se realiza en la edad pediátrica, es un procedimiento seguro y de rápida recuperación, que alivia significativamente la calidad de vida de niños con trastornos respiratorios del sueño, ronquido y apnea obstructiva46. Sin embargo, condiciones asociadas como la obesidad, síndrome de Down, anomalías craniofaciales, trastornos neuromusculares, rinitis alérgica y mucopolisacaridosis se asocian a un riesgo elevado de roncopatía y apnea obstructiva residual post-adenoamigdalectomía47,48.
4) Faringoplastía: Esta cirugía, llamada inicialmente uvulo-palato-faringoplastía y abreviada como UPPP por su sigla en inglés, fue descrita por primera vez por Fujita en 198149. En los 40 años que han pasado desde entonces, esta cirugía ha evolucionado desde una técnica resectiva y con elevada morbilidad a una serie de intervenciones mucho más conservadoras, que respetan la funcionalidad faríngea50. En pacientes con una anatomía favorable (etapa I de Friedman), la UPPP tiene una tasa de éxito cercana al 80% en tratar el ronquido y la apnea del sueño15,51. Las faringoplastías actuales se centran en reposicionar (no remover) grupos musculares y en disminuir el bulto de tejido en la pared lateral de la faringe, estabilizando esta parte de la vía aérea y previniendo su colapso. Entre las técnicas más utilizadas en la actualidad están la faringoplastía de expansión de esfínter (descrita por Pang y Woodson)52, la faringoplastía barbada (descrita por Mantovani y popularizada por Vicini)53,54, la faringoplastía lateral (en las múltiples versiones desarrolladas por Cahali)55 y la UPPP australiana (técnica de Robinson)56. La selección de una técnica en particular dependerá de la anatomía faríngea de cada paciente, así como de la experiencia del cirujano. Su efectividad es alta en pacientes bien seleccionados, y además suele ser parte de la cirugía multinivel para ronquido y apnea del sueño.
5) Palatoplastía con radiofrecuencia: Es un procedimiento mínimamente invasivo que busca reducir la vibración del paladar y evitar el colapso de la región retropalatina durante el sueño. Se aplica en forma submucosa, ya sea con anestesia local o general, una sonda que produce calor local limitado mediante radiofrecuencia. Esto produce una cauterización y posterior fibrosis del tejido, reduciendo su volumen y dándole mayor firmeza y estabilidad57. Tiene una demostrada eficacia en el manejo del ronquido originado a nivel del paladar blando58, pero su efecto en la apnea del sueño es limitado59.
7) Procedimientos para reducción de base de lengua: Una base de lengua prominente o una hipertrofia de la amígdala lingual pueden estrechar en forma significativa la hipofaringe y provocar un colapso a este nivel durante el sueño. La amigdalectomía lingual se puede realizar con radiofrecuencia vía laringoscopía directa60 o bajo visión endoscópica61, con mínima morbilidad. Cuando la obstrucción se debe a una hipertrofia de la base de la lengua, se han descrito una serie de procedimientos que pueden ayudar a resolver este problema: reducción volumétrica de la base de la lengua con radiofrecuencia62, glosectomía parcial de línea media63 y glosectomías endoscópicas submucosas como la técnica SMILE64. La cirugía robótica para remover parte de la base de la lengua (TORS por trans-oral robotic surgery) se reserva para casos de apnea del sueño moderada a severa65.
8) Procedimientos laríngeos: En algunos casos de roncopatía y apnea del sueño, la obstrucción se genera a nivel hipofaríngeo y laríngeo por un desplazamiento hacia posterior de la epiglotis al dormir. La suspensión del hioides (hiotiroidopexia), realizada a través de una cervicotomía, permite estabilizar la vía aérea hipofaríngea66. Sin embargo, en la actualidad esta intervención está siendo reemplazada por técnicas menos invasivas y más efectivas. En este sentido, se pueden efectuar procedimientos endoscópicos de fijación de la epiglotis hacia la base de la lengua (epiglotopexia)67 o resecciones parciales de la epiglotis (epiglotoplastía), habitualmente en asociación a procedimientos de reducción de la base de la lengua63,68.
9) Avance máxilo-mandibular: Esta cirugía remodela el esqueleto facial, adelantando el hueso maxilar y la mandíbula mediante una serie de osteotomías cuidadosamente planificadas y ejecutadas. Es una cirugía altamente efectiva en aumentar la permeabilidad de la vía aérea, con una de las mayores tasas de éxito quirúrgico en apnea del sueño69. Entre sus limitantes está una recuperación compleja y el hecho de que se modifica el perfil facial y la expresión del paciente. Está reservado para pacientes con apnea del sueño severa con importante colapso retrolingual que no toleran el CPAP o que tienen una falta de desarrollo del tercio medio facial y retrognatia.
10) Estimulador del hipogloso: Esta técnica consiste en instalar quirúrgicamente un sistema similar a un marcapasos, que estimula el nervio hipogloso (XII° par craneal) de un lado, en sincronización con la respiración del paciente. La activación del hipogloso produce una contracción del músculo geniogloso, uno de los principales músculos de la lengua, lo que permeabiliza la vía aérea hipofaríngea. Esta técnica está reservada en pacientes con apnea del sueño moderada a severa, como alternativa al CPAP, con altas tasas de éxito y baja morbilidad70.
Es evidente que esta multiplicidad de alternativas de tratamiento nos indica que no existe una única terapia que pueda resolver el problema del ronquido y la apnea del sueño en todos los pacientes. La selección de un tratamiento específico (o un esquema de tratamiento multimodal) dependerá de las características particulares de cada paciente.
ConclusiónEl ronquido es una patología muy prevalente, que afecta la calidad de vida de millones de personas a nivel global. Actualmente existen múltiples alternativas de tratamiento, cada una de las cuales ha demostrado tener una alta eficacia en subgrupos seleccionados de pacientes. Por lo tanto, para tener éxito en el manejo de este trastorno respiratorio del sueño, es fundamental realizar una acuciosa evaluación de cada paciente, para determinar los factores etiopatogénicos que desempeñan un papel relevante en su patología. De esta forma se puede elaborar un plan terapéutico específico para ese individuo, el cual puede consistir en una terapia única o en una combinación de diferentes estrategias. Con este enfoque personalizado se obtendrán los buenos resultados esperados, atenuando el ronquido, reestableciendo un sueño reparador y, con ello, mejorando la calidad de vida de nuestros pacientes.
Declaración de conflicto de interésLos autores declaran no tener ningún conflicto de interés respecto del tema tratado en este artículo.