Analizamos el perfil de pacientes candidatos a quimioterapia neoadyuvante (QTn) en estadio pT2-4aN0M0, la tolerabilidad y adherencia de nuestro protocolo basado en cisplatino y los resultados oncológicos.
Material y métodosEstudio observacional de cohortes retrospectivo que incluye a pacientes con diagnóstico de carcinoma vesical músculo infiltrante tratados con QTn. Se analizaron las características clínicas, histopatológicas, terapéuticas y evolutivas de los pacientes. El uso de la QTn se evaluó mediante la respuesta completa en la pieza quirúrgica (pT0). Este y otros factores anatomopatológicos se relacionaron con la supervivencia global y el tiempo libre de progresión.
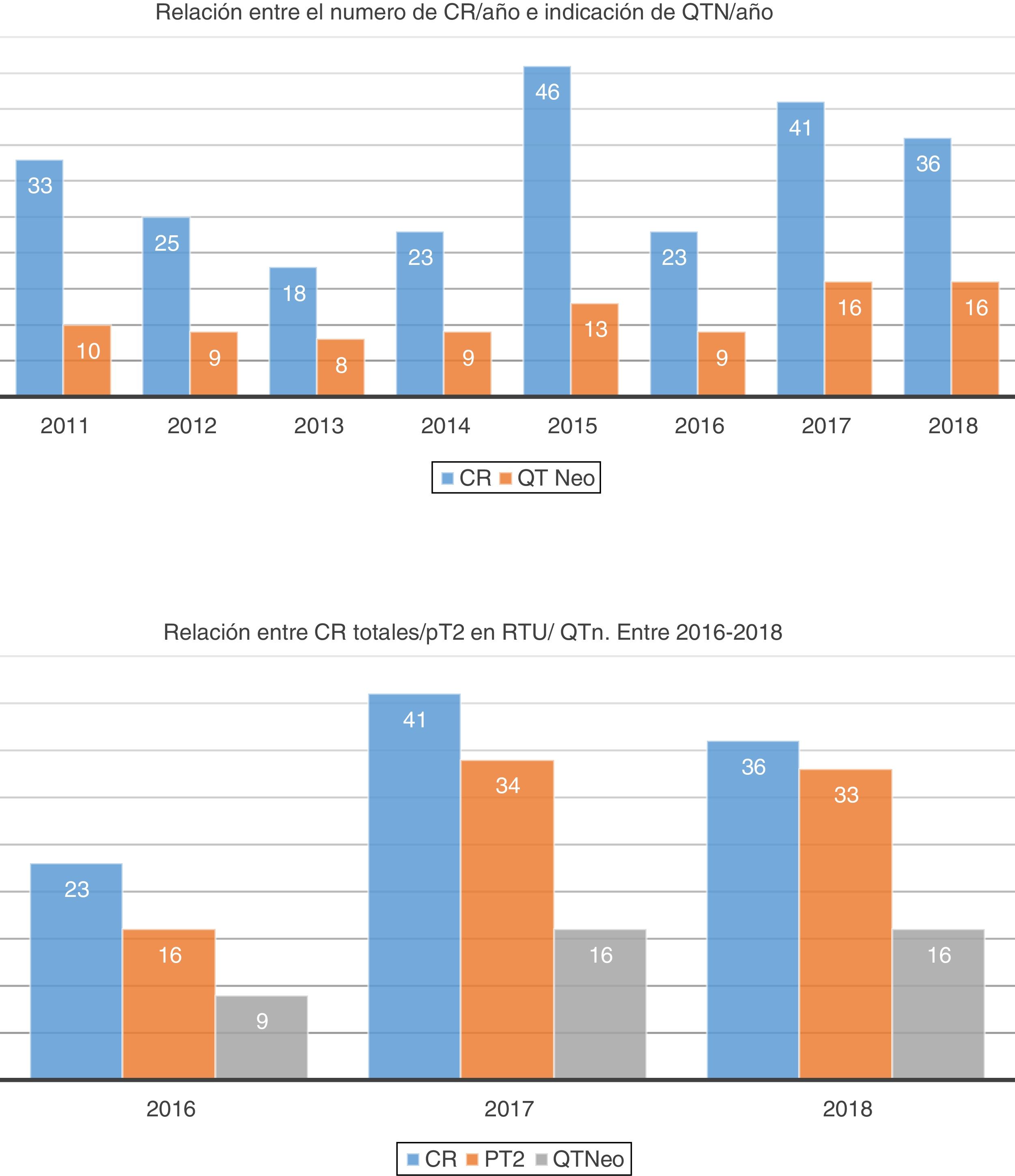
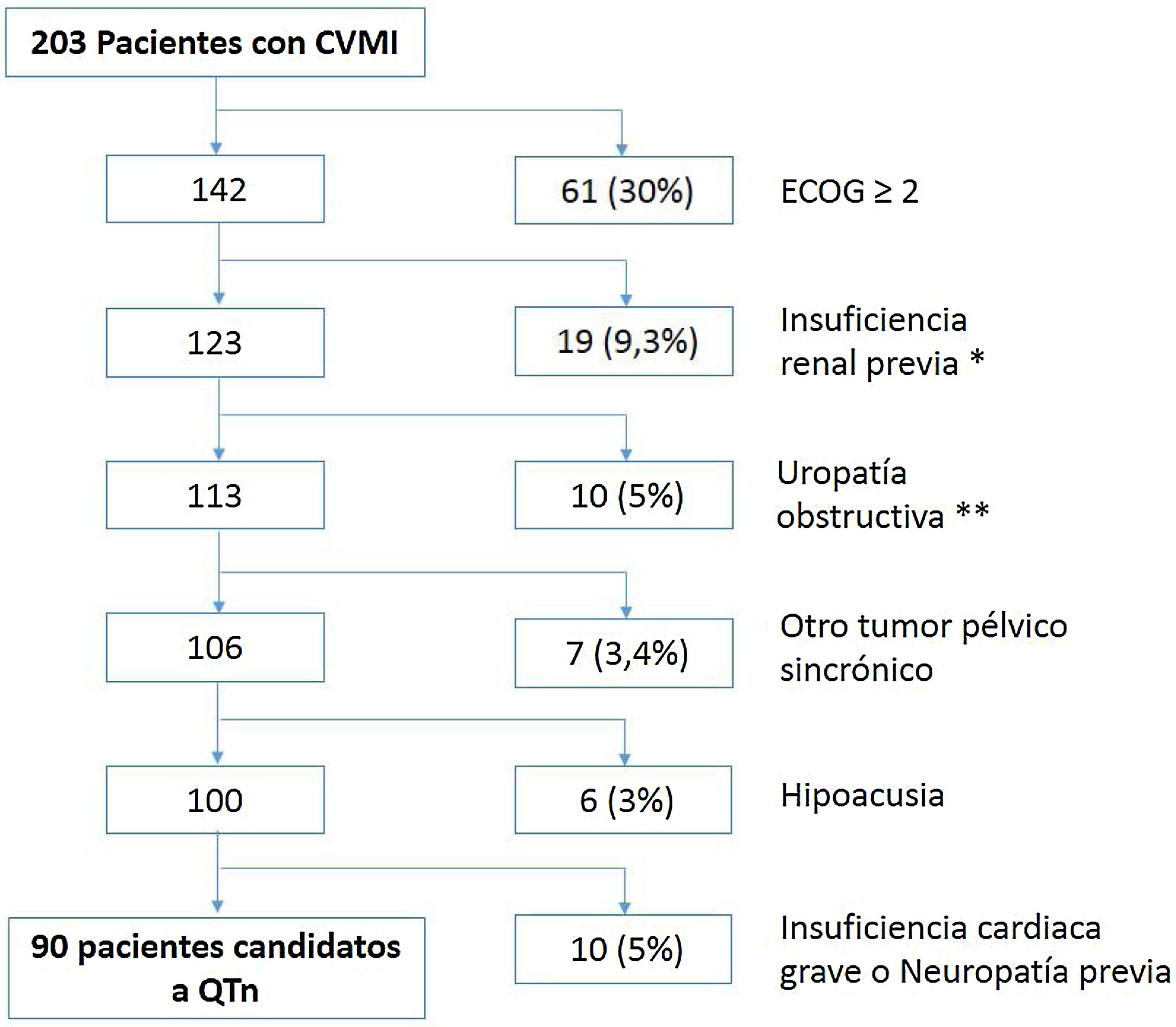
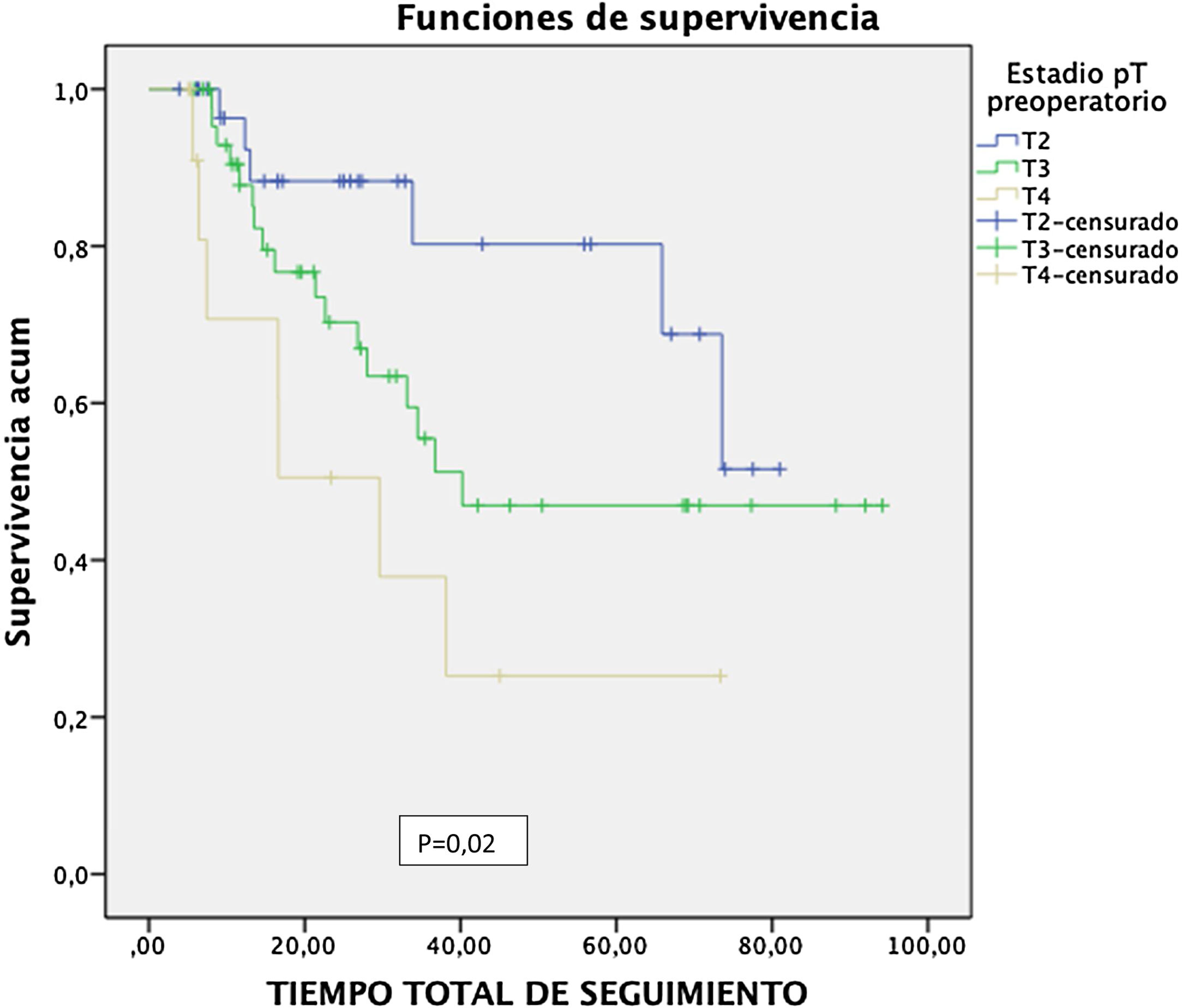
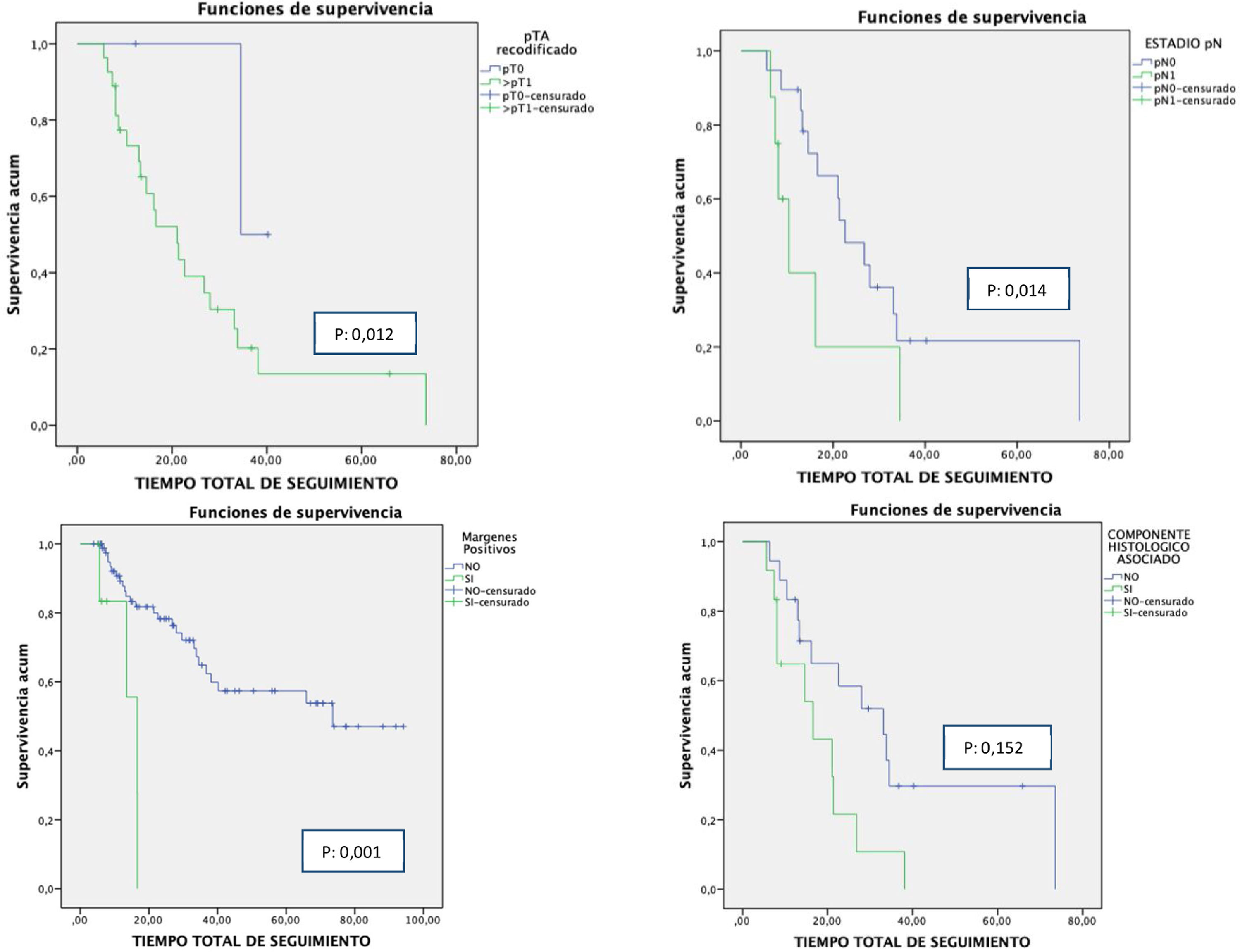
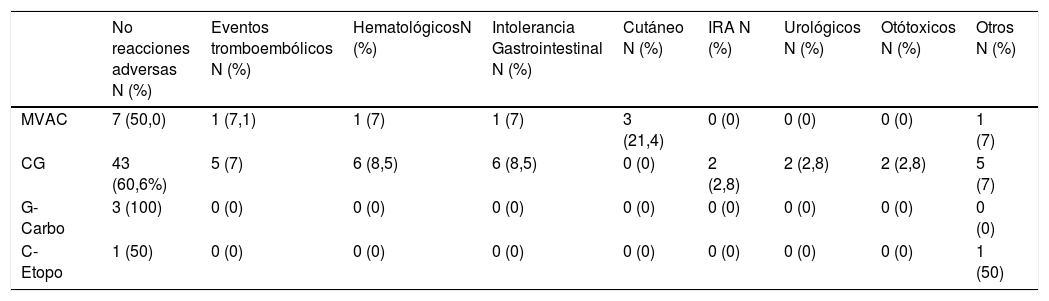
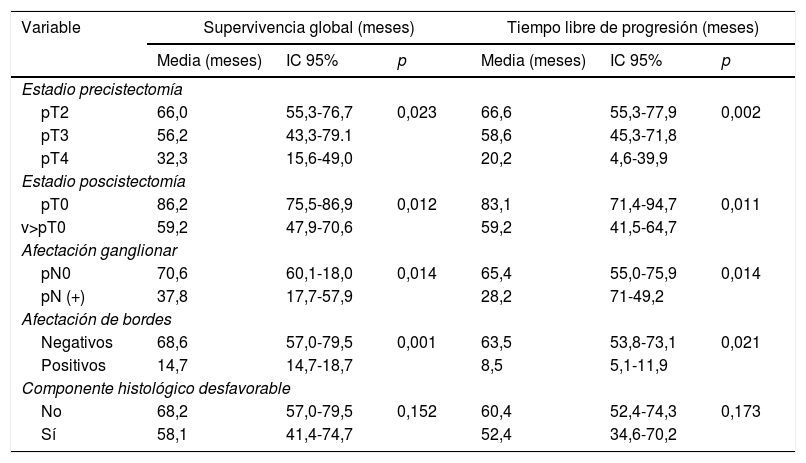
ResultadosIncluimos a 90 pacientes con carcinoma vesical músculo invasivo (estadio clínico T2a-T4aN0M0) que recibieron algún esquema de QTn basado en cisplatino, entre enero de 2011 y diciembre de 2018, antes del tratamiento quirúrgico radical. El 40% de los pacientes presentaron alguna reacción adversa al tratamiento, con un cumplimiento del protocolo de QTn del 92,2%. No se presentaron muertes relacionadas con el tratamiento sistémico y ninguna reacción adversa al tratamiento imposibilitó la realización de la cistectomía radical. Tras la cistectomía radical, se objetivó la presencia de respuesta completa (pT0) en 20 pacientes (21%), un estadio inferior en pieza quirúrgica ( p = 0,012), en enfermos con afectación ganglionar respecto a pN0 (65,4 vs. 28,2 meses; p=0,014) y en aquellos con bordes quirúrgicos afectos respecto a los que presentaban márgenes libres de tumor (63,5 vs. 8,5 meses; p=0,021).
ConclusiónLa selección adecuada de los pacientes con carcinoma vesical músculo infiltrante ha mostrado una buena tolerancia a la QTn, con una alta tasa de cumplimiento previo a la CR. La mejoría en la tasa de respuesta completa implica una mayor supervivencia en este grupo de pacientes. La afectación ganglionar y los bordes quirúrgicos positivos son factores pronósticos importantes.
We analyzed the profile of patients who were candidates for neoadjuvant chemotherapy (NACT) in stage pT2-4aN0M0, the tolerability and adherence of our cisplatin-based protocol and oncological outcomes.
Material and methodsRetrospective observational cohort study including patients diagnosed with muscle-invasive bladder carcinoma treated with NACT. Clinical, histopathological, therapeutic and evolutionary characteristics of the patients were analyzed. The use of NACT was evaluated by the complete response in the surgical specimen (pT0). This and other pathological factors were related to overall survival and progression-free survival.
ResultsWe included 90 patients with muscle-invasive bladder carcinoma (clinical stage T2a-T4aN0M0) who received a cisplatin-based NACT regimen between January 2011 and December 2018, prior to radical surgery. Forty percent of patients presented an adverse reaction, with a compliance with the NACT regimen of 92.2%. There were no deaths related to systemic treatment and no adverse reaction to treatment made radical cystectomy impracticable. After performing radical cystectomy, the presence of complete response (pT0) was observed in 20 patients (21%), lower stage in the surgical specimen ( P=0.012), in patients with lymph node involvement compared to pN0 (65.4 vs. 28, 2 months, P=0.014) and in those with positive surgical margins compared to those with tumor-free margins (63.5 vs. 8.5 months, P=0.021).
ConclusionThe adequate selection of patients with muscle-invasive bladder carcinoma has shown a good tolerance to NACT, with a high compliance rate prior to RC. The improvement in the complete response rate implies a greater survival in this group of patients, with lymph node involvement and positive surgical margins being important prognostic factors.