Edited by: Domingo Orozco-Beltran - Miguel Hernandez University of Elche Department of Clinical Medicine
Antonio Pérez Pérez - Hospital of the Holy Cross and Saint Paul
El tratamiento de la diabetes mellitus tipo 2 (DM2) se basa en cuatro pilares básicos que son la alimentación, el ejercicio, la educación terapéutica y la terapia farmacológica.
Existen 10 grupos de antidiabéticos que se pueden clasificar de acuerdo con su mecanismo de acción, efectos sobre el peso corporal, riesgo de hipoglucemias y capacidad de reducir el desarrollo de complicaciones.
La elección de la medicación se hará de forma individualizada según las preferencias y las características del individuo, tomando en consideración la presencia de enfermedad cardiovascular (ECV), insuficiencia cardiaca (IC), enfermedad renal crónica (ERC), obesidad o esteatosis hepática no alcohólica.
El algoritmo de tratamiento de la DM2 de la Fundación red de grupos para el estudio de la diabetes en atención primaria de salud (RedGDPS) es una herramienta basada en la evidencia, que nos puede ayudar a seleccionar la terapia farmacológica más adecuada, dependiendo de las características de cada paciente.
The treatment of type 2 diabetes is based on four fundamental pillars: diet, exercise, therapeutic education, and pharmacological therapy.
There are ten groups of antidiabetic drugs that can be classified according to their mechanism of action, effects on body weight, risk of hypoglycemia, and ability to reduce the development of complications.
The choice of medication will be individualized based on the preferences and characteristics of the individual, taking into consideration the presence of cardiovascular disease, heart failure, chronic kidney disease, obesity, or non-alcoholic fatty liver disease.
The type 2 diabetes mellitus treatment algorithm from the RedGDPS Foundation is an evidence-based tool that can help us select the most appropriate pharmacological therapy depending on the characteristics of each patient.
El tratamiento de la diabetes mellitus tipo 2 (DM2) se basa en cuatro pilares básicos que son la alimentación, el ejercicio, la educación terapéutica y la terapia farmacológica, todos ellos son necesarios para alcanzar los objetivos de buen control y reducción del desarrollo de complicaciones agudas y crónicas, que son las causantes del aumento de la morbilidad, mortalidad y deterioro de la calidad de vida de las personas con diabetes. Por ello se debe realizar un abordaje holístico, multifactorial e individualizado en cada persona según su estado vital1. En este apartado nos centraremos en la revisión del tratamiento farmacológico de la DM2.
Clasificación de los antidiabéticosExisten 10 grupos de antidiabéticos que los podemos clasificar de acuerdo con su mecanismo de acción:
- •
Estimulan la secreción de insulina: sulfonilureas, secretagogos de acción rápida (glinidas), inhibidores de la dipeptidil-peptidasa-4 (iDPP4), agonistas del receptor del péptido similar al glucagón tipo 1 (arGLP1) y péptido similar al glucagón tipo 1 (GLP1) y polipéptido inhibidor gástrico (GIP) (arGLP1/GIP).
- •
Disminuyen la resistencia a la insulina: biguanidas y glitazonas.
- •
Reducen o enlentecen la absorción de la glucosa: inhibidores de las α-glucosidasas.
- •
Inhiben la reabsorción de glucosa a nivel renal: inhibidores del cotransportador de sodio-glucosa tipo 2 (iSGLT2).
- •
Tratamiento sustitutivo mediante insulina exógena humana y análogos de insulina que podemos administrar por vía parenteral para complementar el déficit de insulina.
También podemos clasificar los antidiabéticos de acuerdo con sus principales efectos indeseables como son las hipoglucemias o el aumento de peso (tabla 1 y tabla 2).
Clasificación de los antidiabéticos de acuerdo con su efecto sobre el peso corporal
| Reducen peso corporal | No modifican peso corporal | Incrementan peso corporal |
|---|---|---|
| arGLP1 | Metformina | Sulfonilureas |
| iSGLT2 | iDPP4 | Glinidas |
| arGLP1/GIP | Inh α gluco | Pioglitazona |
| Insulina |
arGLP1: análogo de los receptores del péptido similar al glucagón tipo 1; GIP: polipéptido inhibidor gástrico; iDPP4: inhibidor de la dipeptidil peptidasa tipo 4; Inh α gluco: inhibidores de la alfa glucosidasa; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2.
Clasificación de los antidiabéticos de acuerdo con su riesgo de provocar hipoglucemias
| Bajo riesgo de provocar hipoglucemias | Alto riesgo de provocar hipoglucemias |
|---|---|
| Metformina | Sulfonilureas |
| iDPP4 | Glinidas |
| Inh α gluco | Insulina |
| Pioglitazona | |
| iSGLT2 | |
| arGLP1 | |
| arGLP1/GIP |
arGLP1: análogo de los receptores del péptido similar al glucagón tipo 1; GIP: polipéptido inhibidor gástrico; iDPP4: inhibidor de la dipeptidil peptidasa tipo 4; Inh α gluco: inhibidores de la alfa glucosidasa; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2.
La elección de la medicación se hará de forma individualizada según las preferencias y las características del individuo, tomando en consideración la presencia de enfermedad cardiovascular (ECV), insuficiencia cardiaca (IC), enfermedad renal crónica (ERC), obesidad o esteatosis hepática no alcohólica.
Principales características de los antidiabéticosA continuación haremos una breve descripción de las principales características de cada una de las familias de antidiabéticos disponibles en la actualidad:
- 1.
Biguanidas (metformina). Inhibe la neoglucogénesis hepática, disminuye la absorción de glucosa y mejora la sensibilidad a la insulina. Es el fármaco inicial de elección en todos los pacientes con DM2, sola o en combinación (salvo intolerancia o contraindicación). Tiene potencia elevada. No produce aumento de peso, reduce de manera significativa las complicaciones macrovasculares y ha demostrado la reducción de la mortalidad2. Su efecto secundario más frecuente es la diarrea que se produce en torno a un 30% de los pacientes, la cual es dosis-dependiente y suele ser transitoria al inicio del tratamiento, por lo que se recomienda iniciarla titulando progresivamente la dosis. Otros efectos secundarios menos frecuentes son náuseas, vómitos, dolor abdominal y pérdida de apetito. Disminuye absorción de la vitamina B12 en tratamientos a largo plazo por lo que puede ser aconsejable su monitorización en tratamientos prolongados. No produce hipoglucemia en monoterapia, aunque puede agravar la producida por otros hipoglucemiantes. Contraindicaciones: Insuficiencia renal grave: no iniciar con filtrado glomerular estimado (FGe) <30mL/min y con un FGe entre 30-45mL/min se debe reducir su dosis a la mitad (máximo 1.000mg/día). Insuficiencia hepática, respiratoria y/o cardiaca grave. Embarazo o lactancia, cirugía mayor o enfermedad aguda grave. Alcoholismo. Durante 24 horas anteriores y posteriores al uso de contrastes yodados. Situación de deshidratación.
- 2.
Sulfonilureas. Estimulan la secreción de la insulina preformada en el páncreas. Reducen el riesgo de complicaciones microvasculares y a largo plazo también las macrovasculares3. En el estudio Action in Diabetes and Vascular disease; preterAx and diamicroN-MR Controlled Evaluation (ADVANCE)4, la estrategia intensiva basada en gliclazida se asoció con un riesgo muy bajo de hipoglucemia severa y de ganancia de peso, por lo que es la sulfonilurea de elección. En el estudio CARdiovascular Outcome study of LINAgliptin (CAROLINA)5 la glimepirida demostró no inferioridad con respecto a linagliptina con relación a su seguridad cardiovascular. Sus efectos secundarios más frecuentes son el aumento de peso y las hipoglucemias (menor riesgo de hipoglucemia con gliclazida de liberación retardada y glimepirida). Potencian el efecto de los antagonistas de la vitamina K. Contraindicaciones: diabetes mellitus tipo 1. Embarazo, cirugía mayor o enfermedad grave. Antecedentes de reacciones adversas a sulfamidas y tiazidas. Cetoacidosis diabética. Insuficiencia hepática grave Child-Pugh C (si es leve puede utilizarse glipizida). Enfermedad renal con FGe<30mL/min (si FGe entre 30-60mL/min pueden utilizarse gliclazida y glimepirida).
- 3.
Glitazonas (pioglitazona). En España actualmente solo se comercializa la pioglitazona.
Reduce la resistencia a la insulina en tejidos periféricos (músculo esquelético y tejido graso) por lo que aumenta la utilización periférica de la glucosa. Su potencia de acción es similar a la metformina. Se suele emplear en combinación con metformina, sulfonilureas, iDPP4, arGLP1 o insulinas.
La pioglitazona reduce eventos cardiovasculares y ateroescleróticos6,7, especialmente en pacientes con ictus previo/recurrente. Produce retención hidrosalina, lo que puede descompensar una IC por lo que está contraindicado en esta patología.
Entre sus contraindicaciones se encuentran la diabetes mellitus tipo 1, cáncer de vejiga activo o previo, embarazo o lactancia, cetoacidosis diabética, IC o hepatopatía grave (realizar controles de enzimas hepáticos).
- 4.
Inhibidores de alfa glucosidasas (acarbosa y miglitol). Actúan ralentizando la absorción de hidratos de carbono a nivel intestinal, disminuyendo los picos de glucemia posprandial. La acarbosa ha demostrado una reducción de la aparición de eventos cardiovasculares en un metaanálisis8. No producen hipoglucemias en monoterapia. Cuando se utilizan en combinación con sulfonilureas, glinidas o insulina pueden producirse hipoglucemias que se tratarán con glucosa pura oral, pero no con sacarosa (azúcar), debido a que está retardada su absorción. Su efecto secundario más frecuente es la flatulencia que se produce hasta en un 77% de los casos, que se ve agravada si se asocia a metformina. Entre sus contraindicaciones figuran el embarazo o lactancia, trastornos gastrointestinales (trastornos de absorción y digestión, enfermedad de Crohn, colitis ulcerosa), insuficiencia renal severa o cirrosis.
- 5.
Secretagogos de acción rápida: glinidas (repaglinida y nateglinida). Producen una liberación rápida y de corta duración de insulina a través de un mecanismo de acción similar al de las sulfonilureas. Se administran en función de las comidas, y su principal efecto es la reducción de las hiperglucemias posprandiales. Producen menos hipoglucemias que las sulfonilureas. Son útiles en pacientes ancianos y con insuficiencia renal, así como en pacientes con un horario y distribución irregular de las comidas. La repaglinida es más potente que la nateglinida.
Carecen de estudios a largo plazo sobre reducción de complicaciones y mortalidad, aunque un estudio demostró un probable efecto cardiovascular protector similar a la metformina9. Sus efectos secundarios más frecuentes son la hipoglucemia y ligero aumento de peso. Se debe advertir a los pacientes que omitan la dosis si se saltan una comida ya que podría desencadenar una hipoglucemia.
Sus contraindicaciones son la diabetes mellitus tipo 1 o secundaria a enfermedad pancreática, embarazo o lactancia e insuficiencia hepática. Está contraindicada su asociación con gemfibrozilo, debido al gran aumento de la concentración de los niveles plasmáticos de repaglinida que provoca.
- 6.
iDPP4 (sitagliptina, vildagliptina, saxagliptina, linagliptina y alogliptina). Actúan inhibiendo la enzima DPP4, la cual tiene como función degradar a la incretina GLP1, que se libera en el intestino ante la llegada de los alimentos, produciendo la liberación de insulina pancreática e inhibiendo la de glucagón de manera glucosa-dependiente. Poseen como principal característica el control de la hiperglucemia sin producir incremento de peso y con una incidencia de hipoglucemias muy baja. Tienen una potencia hipoglucemiante moderada. Están indicadas en tratamiento combinado con cualquier antidiabético, excepto arGLP1 o arGLP1/GIP.
En cuatro ensayos clínicos con saxagliptina10, alogliptina11, sitagliptina12 y linagliptina13, en pacientes con DM2 y presencia de al menos un evento cardiovascular se demostró que no aumentan el riesgo cardiovascular (RCV), excepto en el estudio con saxagliptina en el que se observó un incremento en el número de ingresos por IC.
Entre sus contraindicaciones figuran la diabetes mellitus tipo 1 o secundaria a enfermedad pancreática, embarazo o lactancia. La vildagliptina también está contraindicada en caso de insuficiencia hepática o elevación de transaminasas. En caso de insuficiencia renal moderada y grave se debe reducir su dosis excepto con linagliptina. No se deben utilizar concomitantemente con arGLP1.
- 7.
Análogos de GLP1 (exenatida, exenatida de liberación prolongada [exenatida long-acting release [LAR]] lixisenatida, liraglutida, semaglutida [sc u oral] y dulaglutida).
Son polipéptidos con una estructura similar al GLP1, que no pueden ser degradados por la enzima DPP4, debido a que se ha modificado su estructura, lo que hace que su vida media sea prolongada. Actúan estimulando la secreción de insulina pancreática e inhibiendo la de glucagón de manera glucosa-dependiente. Poseen otros efectos como el enlentecimiento del vaciado gástrico, la disminución del apetito y la inapetencia por alimentos grasos, características que lo convierten en un fármaco excelente para los pacientes con obesidad, puesto que les ayuda a perder peso. Reducen la glucemia de una manera eficaz con bajo riesgo de hipoglucemias ya que dejan de actuar con niveles normales de glucemia.
Exenatida y lixisenatida tiene una acción posprandial mientras que liraglutida, exenatida semanal, semaglutida y dulaglutida tienen una acción tanto basal como posprandial.
Liraglutida y semaglutida han demostrado la reducción de eventos cardiovasculares, disminución de lípidos, disminución de presión arterial sistólica y reducción de la progresión de la placa ateroesclerótica en pacientes en prevención secundaria14,15, mientras que dulaglutida redujo los eventos cardiovasculares tanto en prevención primaria como secundaria16, y exenatida LAR redujo la mortalidad total en pacientes en prevención secundaria17.
Existe evidencia que apoya un papel protector a nivel renal, con reducción de la albuminuria y retraso de la progresión de la enfermedad renal diabética. Semaglutida subcutánea a dosis de 1mg consiguió reducir la aparición de un compuesto de eventos renales y la mortalidad cardiovascular en el estudio Evaluate Renal Function with Semaglutide Once Weekly (FLOW)18. Para su financiación por el Sistema Nacional de Salud se requiere su uso en terapia combinada con otros fármacos y en pacientes que tengan un Índice de masa corporal (IMC) ≥ 30kg/m2. Se pueden administrar en combinación con otros antidiabéticos (excepto iDPP4 o ar GLP1/GIP), y en monoterapia si no se tolera metformina.
Sus contraindicaciones son la diabetes mellitus tipo 1 o secundaria a insuficiencia pancreática, embarazo, lactancia, pancreatitis aguda o crónica e insuficiencia renal grave (liraglutida, semaglutida y dulaglutida pueden utilizarse si FGe> 15mL/min), así como la presencia de carcinoma medular de tiroides o neoplasia endocrina múltiple Multiple endocrine neoplasia, type 2 (MEN2).
- 8.
iSGLT2 (dapagliflozina, empagliflozina, canagliflozina y ertugliflozina). Actúan como inhibidores selectivos y reversibles del cotransportador renal de sodio y glucosa, responsable de la reabsorción de glucosa en el túbulo proximal, lo que provoca aumento de excreción urinaria de glucosa y una diuresis osmótica que provoca una reducción de la presión intraglomerular. Además, produce reducción de sobrecarga de volumen, disminución de presión sanguínea y de la pre/poscarga con un efecto beneficioso en la función diastólica y en la preservación de la función renal.
Pueden utilizarse en monoterapia (en caso de intolerancia o contraindicación a metformina) o añadido a otros antidiabéticos. Presentan un bajo riesgo de hipoglucemias. Son de elección en pacientes con enfermedad cardiaca, renal o eventos cardiovasculares.
En pacientes con diabetes han demostrado una reducción significativa de eventos cardiovasculares, así como disminución de hospitalización por IC y un enlentecimiento de la progresión de la enfermedad renal19,20.
No precisan ajuste dosis, pero no se recomienda iniciarlos si el FGe es menor de 30mL/min. Su efecto hipoglucemiante es mínimo cuando el FGe es menor de 45mL/min, por lo que se recomienda valorar la adición de otro antidiabético para mejorar el control glucémico.
Sus efectos adversos más frecuentes son las infecciones genitourinarias, y la depleción de volumen. Pueden facilitar la aparición de cetoacidosis diabética en pacientes insulinopénicos (sospechar ante rápida progresión de diabetes, mal control con hemoglobina glucosilada (HbA1c)> 10% o con clínica cardinal e importante pérdida de peso); en estos casos parece prudente iniciar insulina basal antes de comenzar con un iSGLT2. Sus contraindicaciones son embarazo, lactancia y situaciones de riesgo de cetoacidosis.
- 9.
Agonista dual GLP1/GIP (tirzepatida). Tirzepatida es un agonista dual de los receptores GIP y GLP1. Ambos receptores están en las células endocrinas (alfa y beta) del páncreas, cerebro, corazón, intestino, adipocito y leucocitos. Tirzepatida mejora el control glucémico al reducir las concentraciones de glucosa en ayunas y posprandiales en pacientes con DM2 a través de múltiples mecanismos: aumenta la secreción pancreática de insulina, reduce el apetito y consecuentemente el peso corporal, mejorando la sensibilidad a la insulina, reduce las concentraciones de glucagón y retrasa el vaciamiento gástrico.
Se administra por vía subcutánea semanalmente y está indicado sobre todo en pacientes con DM2 mal controlada y obesidad. Puede utilizarse en monoterapia (si la metformina no se tolera o está contraindicada), o en combinación con otros antidiabéticos, excepto arGLP1 o iDPP4.
Presenta una potencia superior en disminución de peso y HbA1c frente a otras terapias inyectables como son insulina y arGLP121.
Sus principales efectos adversos son náuseas, vómitos y diarrea, así como eczema y prurito en la zona de inyección.
- 10.
Insulina. La insulina humana o los análogos de insulina permiten realizar un tratamiento sustitutivo en pacientes con déficit de insulina. Se administran por vía parenteral y se dividen en insulinas basales, con efecto a lo largo de todo el día, intermedias, con duración prolongada pero que no alcanza a cubrir 24 horas, insulinas rápidas o prandiales, con efecto de pocas horas de duración e insulinas premezcladas que contienen una combinación de una insulina intermedia con una prandial. En pacientes con DM2 habitualmente se inicia la insulinoterapia con una dosis de insulina basal al día, junto con otros antidiabéticos, cuando estos no consiguen un buen control glucémico del paciente. En algunos casos es necesaria la adición de insulina prandial para controlar las hiperglucemias posprandiales.
Las evidencias de los beneficios a largo plazo del tratamiento con insulina en pacientes con DM2 se han obtenido del estudio United Kingdom Prospective Diabetes Study (UKPDS)3 y de su prolongación durante 10 años más22. En ellos se ha visto que el tratamiento intensivo con insulina reducía las complicaciones microvasculares en un 25% ya en los primeros 10 años, mientras que la reducción de la mortalidad y de las complicaciones macrovasculares no fue estadísticamente significativa hasta pasados 20 años del inicio del estudio. Más recientemente se ha publicado el estudio Outcome Reduction with an Initial Glargine Intervention (ORIGIN), en el que se ha podido observar que en la rama de tratamiento intensivo de pacientes con DM2 de reciente diagnóstico con una dosis de insulina glargina durante seis años, no mostraba diferencias significativas en reducción de complicaciones, mortalidad o desarrollo de cáncer con respecto al tratamiento convencional23. Sus principales efectos adversos son el aumento de peso y del riesgo de hipoglucemias.
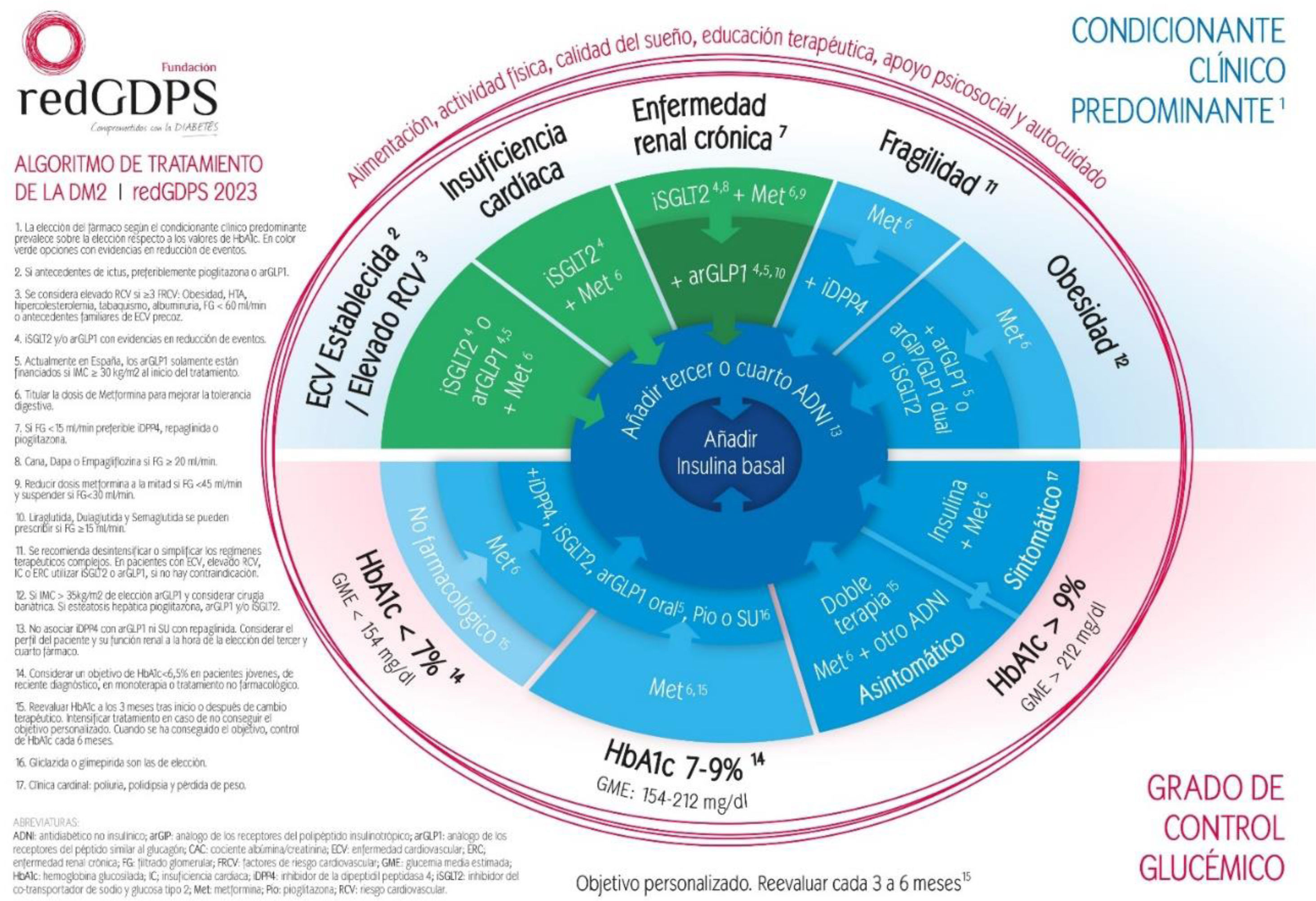
Como se ha comentado al inicio, el abordaje terapéutico de la DM2 precisa de una valoración individualizada. En la toma de decisiones, los clínicos han de considerar las comorbilidades, complicaciones, objetivo de control y preferencias del paciente, así como los beneficios y riesgos de cada grupo farmacológico. Utilizaremos el algoritmo de tratamiento de la DM2 de la RedGDPS para ilustrar estos aspectos (fig. 1).
Manejo del algoritmo24- 1.
Valoración e intervención en estilo de vida: alimentación y actividad física, calidad del sueño, educación terapéutica, apoyo psicosocial y autocuidado.
- 2.
Considerar si el paciente presenta algún condicionante clínico (ECV establecida, elevado RCV, IC, ERC, fragilidad u obesidad). En caso de presentar más de un condicionante priorizar la elección de los fármacos para el tratamiento de izquierda a derecha, ya que los supuestos con fondo verde han demostrado evidencia en reducción de eventos. La elección del fármaco según condicionante prevalece sobre los valores de HbA1c.
En pacientes con ECV establecida o con RCV elevado, el tratamiento de elección será la metformina en combinación con un iSGLT2 o un arGLP119,25.
En pacientes con IC el tratamiento de elección es la metformina en combinación con un iSGLT220.
En pacientes con ERC con un FG entre 20 y 59mL/min y/o albuminuria, se recomienda metformina conjuntamente con un iSGLT2 (reducir la dosis de metformina a la mitad si FG <de 45mL/min)26, en caso de no cumplirse el objetivo de control podría añadirse un arGLP118,27.
En pacientes con fragilidad, la metformina es el fármaco de elección tras valoración de la función renal y con monitorización periódica de la misma. Debido a que en este grupo de pacientes existe un riesgo elevado de hipoglucemia, y de intolerancia e interacciones farmacológicas es preferible utilizar un inhibidor de la DPP4 en el segundo escalón. Reevaluar periódicamente la posibilidad de deprescribir o simplificar el tratamiento para minimizar el riesgo de hipoglucemias y facilitar el cumplimiento28.
En los pacientes con obesidad se ha optado en el segundo escalón por la asociación de la metformina con un arGLP1, un agonista dual arGLP1/GIP o un iSGLT2, porque se asocian a pérdida de peso29. En caso de obesidad de grado 2 (índice de masa corporal>35kg/m2) por su efecto sobre el control del apetito es preferible un arGLP1 o unos dual arGLP1/GIP y valorar además la posibilidad de cirugía bariátrica. Se recomienda valorar la efectividad del tratamiento con arGLP1 a los tres a seis meses y suspenderlo si no ha sido efectivo (reducción de al menos el 1% en la HbA1c y del 3% del peso corporal).
- 3.
Cuando el paciente no presente ningún condicionante, la elección del tratamiento se realizará dependiendo de las cifras de HbA1c. Se recomienda actuar de forma diferente si su valor inicial es menor del 7%, está entre el 7 y el 9% o si es mayor del 9%.
Si la HbA1c es menor del 7%, se comenzará el tratamiento solo con modificaciones en el estilo de vida (dieta y ejercicio). Si en tres a seis meses no se consigue alcanzar el objetivo terapéutico propuesto, se recomienda la introducción de la metformina comenzando con 500mg/día, aumentando su dosis semanalmente en 500mg/día, hasta alcanzar los 1.000mg/12h o la máxima dosis tolerada. En caso de intolerancia gastrointestinal a la metformina, titular más lentamente y asegurarse de que el paciente esté tomando el medicamento con alimentos para mejorar la tolerabilidad.
Si con la monoterapia no se consigue el objetivo, se combinará la metformina con otro fármaco oral, añadiendo iDPP4, iSGLT2, arGLP1 oral, pioglitazona o una sulfonilurea (gliclazida o glimepirida). Para elegir el segundo fármaco se deben considerar las características del paciente.
Si con la doble terapia oral tampoco se alcanza el objetivo, se añadirá un tercer fármaco oral, insulina basal o un agonista de los receptores del GLP1. No asociar sulfonilurea con repaglinida, ni iDPP4 con arGLP1 o arGLP1/GIP ya que al compartir mecanismo de acción no aumenta la eficacia y si el coste y la posibilidad de efectos adversos.
Tras el fracaso con triple o cuádruple terapia con antidiabéticos no insulínicos se debe iniciar tratamiento con una dosis de insulina basal. Se pueden mantener los otros antidiabéticos no insulínicos salvo las sulfonilureas, por el riesgo de hipoglucemia que comporta el uso conjunto con insulina.
Si la HbA1c está entre el 7 y el 9%, procederemos igual que en el caso anterior, iniciando el tratamiento con metformina y progresando en el algoritmo a la terapia doble, triple o cuádruple y, finalmente a la insulinización con insulina basal si fuese necesario. La única diferencia es que en este grupo las medidas no farmacológicas se iniciarán a la vez que el tratamiento farmacológico.
Si la HbA1c es mayor del 9% o el paciente está muy sintomático y hay pérdida de peso reciente, es preferible comenzar con una dosis de insulina basal asociada a metformina. Se deben titular ambos fármacos de forma rápida y progresiva, y unas semanas después de alcanzar el control glucémico se podría intentar introducir un segundo antidiabético no insulínico y descender progresivamente la dosis de insulina hasta suspenderla. En pacientes con pocos síntomas, se recomienda desde el inicio biterapia con metformina y otro antidiabético no insulínico. Si persiste el mal control deberíamos pasar a triple o cuádruple terapia y, finalmente a la insulinización con insulina basal.
Dado que la DM2 es una enfermedad crónica y progresiva, será precisa una reevaluación periódica tanto de los objetivos como de la posible aparición de complicaciones, para modificar el tratamiento de los pacientes, ajustándolo a la evolución de la enfermedad.
Es bien conocido que el tratamiento farmacológico de la diabetes reduce el desarrollo de complicaciones microvasculares, sin embargo, la reducción de las complicaciones macrovasculares tan solo se consigue con el uso de algunos fármacos.
¿Qué aporta este estudio?- -
En esta revisión hemos descrito los beneficios y efectos adversos de cada una de las opciones terapéuticas en el tratamiento farmacológico de la diabetes tipo 2.
- -
Destacamos la necesidad de realizar una individualización a la hora de elegir los fármacos, de acuerdo con las características de cada paciente.
- -
Se prioriza la capacidad de cada opción terapéutica en la reducción del desarrollo de complicaciones a largo plazo y en la mejoría en la calidad de vida de las personas con diabetes tipo 2.
El contenido del trabajo no ha sido publicado con anterioridad y el mismo artículo, o una parte de él, no ha sido enviado simultáneamente a otra revista.
No precisa consentimiento informado al no incluir pacientes, pues se trata de una revisión de la literatura.
Hacemos constar la aceptación explícita, por todos los autores, del contenido de la versión enviada. Cada uno de los autores manifiesta haber contribuido sustancialmente a la concepción y diseño, o a la adquisición de datos, o al análisis e interpretación de los datos; haber escrito el borrador del artículo o haber revisado de manera crítica su contenido intelectual, y haber aprobado la versión que finalmente va a ser publicada.
Contribución de los autores- 1.
Concepción y diseño del estudio, búsqueda bibliográfica y adquisición de datos, análisis e interpretación de los datos, FJGS.
- 2.
Borrador del artículo y revisión crítica del contenido intelectual, FJGS, JRV.
- 3.
Aprobación definitiva de la versión que se presenta, FJGS, JRV.
- 4.
FJGS, Francisco Javier García Soidán; JRV, Javier Riveiro Villanueva.
Este estudio no ha recibido ninguna fuente de financiación y ha sido realizado íntegramente por los autores.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses en relación a la elaboración de este artículo.