De acuerdo con los últimos estudios, la tasa de intervención quirúrgica de la válvula tricúspide es muy baja, pese al gran número de pacientes con insuficiencia tricuspídea severa con indicación de cirugía, según las guías de práctica clínica. Asimismo, datos recientes demuestran que la cirugía aislada de la válvula tricúspide se asocia de manera significativa e independiente con una elevada mortalidad. Las nuevas terapias transcatéter surgen para dar solución a estos problemas. En el presente trabajo, se realiza una revisión no sistemática del estado del arte de los diferentes dispositivos percutáneos existentes en el mercado, organizados en tres grupos: válvula con implante en posición ortotópica o heterotópica, sistemas de anuloplastia y sistemas de coaptación. Así, este documento pretende ofrecer una visión global sobre el panorama actual y las perspectivas futuras del tratamiento endovascular de la enfermedad valvular tricuspídea, un campo de gran interés en plena expansión.
According to the latest studies, the surgical intervention rate of the tricuspid valve is very low, despite the large number of patients with severe tricuspid regurgitation withindication for surgery according to clinical practice guidelines. Likewise, recent data demonstrate that isolated tricuspid valve surgery is significantly and independently associated withhigh mortality. New transcatheter therapies are emerging to solve these issues. In the present work, a non-systematic review of the state of the art of the different percutaneous devices currently on the market was carried out, organized into three groups: valve with implant in orthotopic or heterotopic position, annuloplasty systems and coaptation systems. Thus, this document aims to offer a global vision of the current landscape and future perspectives of endovascular treatments of tricuspid valve disease, a field of great interest in full expansion.
La insuficiencia tricuspídea (IT) es una enfermedad prevalente, se estima que afecta del 65 al 85% de la población, pero aún es infratratada1. En ausencia de otra valvulopatía concomitante, son pocos los pacientes que se someten a una intervención quirúrgica aislada sobre la válvula tricúspide (VT). De hecho, la mayoría de los pacientes con IT significativa reciben tratamiento médico y solo en un 0,5% de los casos se realiza una reparación o sustitución de la VT. Además, esta cirugía se asocia con un mal pronóstico2, especialmente en pacientes con antecedentes de cirugía cardiaca previa, en quienes la tasa de mortalidad hospitalaria oscila entre el 10 y el 35%3. Una de las causas principales de estos malos resultados es la remisión tardía de los pacientes quienes, habitualmente, ya presentan una disfunción grave del ventrículo derecho (VD) o daño de órganos diana.
Como consecuencia de todo ello, y dada la creciente popularidad de las estrategias transcatéter sobre la válvula aórtica y mitral, se ha abogado por el desarrollo de alternativas menos invasivas para el manejo de la IT. No obstante, ninguna de las guías sobre valvulopatías4,5 incluye recomendaciones sobre el tratamiento percutáneo de la VT. Un potencial nicho para esta terapia son los pacientes con IT funcional severa, signos o síntomas de insuficiencia cardiaca derecha refractarios a tratamiento médico óptimo, sin hipertensión pulmonar irreversible y riesgo quirúrgico alto o prohibitivo basado en la decisión de un equipo multidisciplinario del corazón. También se puede emplear de forma combinada en pacientes subsidiarios de intervencionismo sobre otra válvula.
Tratamiento percutáneo de la insuficiencia tricuspídeaInicialmente, los sistemas diseñados para la enfermedad valvular aórtica o mitral, tales como la prótesis Edwards SAPIEN (Edwards Lifesciences; Irvine, California, EE. UU.) o la técnica de reparación edge-to-edge con MitraClip® (Abbot Vascular; Santa Clara, California, EE. UU.) se utilizaron off-label y con uso compasivo en posición tricuspídea. Sin embargo, en los últimos años, han emergido varios dispositivos percutáneos para el tratamiento exclusivo de la VT.
Se han identificado tres grupos según la diana terapéutica: implante (ortotópico o heterotópico) de una válvula cardiaca percutánea (VCP), dispositivos de anuloplastia y dispositivos de coaptación.
Implante (ortotópico o heterotópico) de una VCPA.1. Implante ortotópico de una VCP:
Son muchas las empresas que trabajan en el diseño de prótesis transcatéter tricuspídea, teniendo que esforzarse en superar una serie de dificultades: gran tamaño (>40 mm) y forma elíptica del anillo tricuspídeo (AT), estructura trabeculada y pared fina del VD, así como proximidad de otras estructuras anatómicas (arteria coronaria derecha, seno coronario, vena cava o nódulo aurículo-ventricular). Sin embargo, hasta la fecha, solo una se ha implantado con éxito en humanos y varias continúan en desarrollo. A pesar de que la experiencia acumulada hasta el momento es escasa, los resultados preliminares son prometedores, siendo importante conocer las particularidades de las diferentes VCP ortotópicas (tabla 1):
Válvulas cardiacas percutáneas para el tratamiento de la IT
AD: aurícula derecha; IT: insuficiencia tricuspídea; VCI: vena cava inferior; VCS: vena cava superior.
NaviGate: imagen reproducida con permiso de Moñivas Palomero V et al. 64 TriSol, Lux y TriCares: imágenes reproducidas con permiso de Demir OM et al. 65 TricValve: imagen reproducida con permiso de Lauten12. Tricento: imagen reproducida con permiso de Agricola E et al. 66
El sistema NaviGate (NaviGate Cardiac Structures Inc.; Lake Forest, California, EE. UU.) fue el primero en conseguir un reemplazo valvular tricuspídeo transcatéter (TTVR) completamente ortotópico. Se trata de una bioprótesis con velos de pericardio equino insertados en un stent de nitinol autoexpandible con forma troncocónica, lo que permite reducir el gradiente transvalvular y minimizar la obstrucción del tracto de salida del VD. Actualmente, se puede implantar por vía yugular o a través de la aurícula derecha (AD) mediante minitoracotomía. El diámetro de la vena yugular debe ser ≥ 14 mm, ya que la vaina del introductor es de 42 Fr. Se requieren al menos 7 cm desde el punto de entrada al AT para poder dirigir el dispositivo y colocarlo coaxial al plano anular. Existen cinco tamaños disponibles (36, 40, 44, 48 y 52 mm) y se recomienda un sobredimensionamiento del 5 al 10% con respecto a la medida del AT. Desde el primer implante en humanos6 en 2017 hasta ahora, solo se ha reportado una treintena de casos en todo el mundo y siempre con uso compasivo. Recientemente, se han publicado los resultados iniciales de un único centro con cinco pacientes consecutivos7. Solo un individuo falleció en los primeros 30 días después del procedimiento. El implante exitoso se asoció con una reducción de la IT severa o torrencial, remodelado inverso del VD, aumento del gasto cardiaco y mejoría de la clase funcional New York Heart Association (NYHA). Son necesarios más estudios con un tamaño muestral mayor y un seguimiento a más largo plazo para corroborar estos resultados.
Próximas VCP ortotópicasLa válvula TriSol (TriSol Medical Ltd., Inc.; Yokneam, Israel) se ensambla como una malla de nitinol sobre un faldón exterior de poliéster y una válvula de pericardio bovino en su interior. La malla de nitinol tiene forma cónica y anclaje al AT mediante fuerzas axiales, lo que le proporciona estabilidad sin afectar al sistema de conducción. El faldón exterior previene la fuga paravalvular. La válvula consiste en una única valva que está unida en dos comisuras centrales opuestas. Durante la diástole, las hojas se mueven hacia el centro, creando dos orificios laterales para el llenado ventricular. Durante la sístole, se cierran en forma de cúpula, lo que aumenta el volumen del VD. Se espera que esto reduzca la presión en el VD y preserve la función del mismo, ya que el aumento repentino de la precarga tras el reemplazo de la VT puede conducir a un fallo del VD. Hasta ahora, solo se ha utilizado en modelos con cerdos8, estando prevista su implantación en humanos a partir del 2020.
La válvula Lux (Jenscare Biotechnology; Ningbo, China)9 y la TriCares (TriCares GmbH; Aschheim, Alemania) son otras prótesis transcatéter tricuspídeas en desarrollo que, tras ser testadas en estudios experimentales con animales, están pendientes de ensayos clínicos para comprobar la viabilidad y seguridad en humanos.
A.2. Implante heterotópico de una VCP:
En este caso, el objetivo principal consiste en reducir el volumen y la presión de regurgitación hacia la vena cava, mejorando así los síntomas de insuficiencia cardiaca derecha10. Sin embargo, al no tratar directamente la IT, se produce una sobrecarga crónica de la AD y, por consiguiente, un aumento de la precarga en el VD, por lo que el implante de una válvula en vena cava (CAVI) se reserva para estadios avanzados de la IT. Otro inconveniente es la necesidad de anticoagulación, ya que el flujo lento en la vena cava podría favorecer la trombosis valvular. Algunas de las válvulas específicamente diseñadas para este fin se describen a continuación (tabla 1):
Prótesis TricValveEl sistema TricValve (P + F Products + Features GmbH; Viena, Austria), consta de dos válvulas autoexpandibles de pericardio bovino montadas sobre un stent de nitinol, una disponible en tamaños 25 y 29 mm para la vena cava superior (VCS) y otra en 31 y 35 mm para la vena cava inferior (VCI). Ambas se despliegan mediante abordaje transfemoral en un catéter de 27 Fr. Hay tres dificultades que es necesario tener en cuenta: la proximidad de las venas hepáticas, la distensibilidad y grado de dilatación de las venas cavas y la importante variabilidad anatómica de la VCS. Por todo ello, el doble implante en las venas cavas es una intervención técnicamente exigente, siendo imprescindible un estudio preoperatorio exhaustivo. La experiencia inicial en humanos describe una abolición inmediata del reflujo hacia ambas venas cavas y una mejoría clínica a los 12 meses de seguimiento evaluada con la clase funcional NYHA, la función hepática y la prueba de la marcha a los seis minutos11,12. No obstante, aún no se disponen de datos a largo plazo sobre el impacto de la ventricularización de la AD y el efecto de la disfunción del VD. Del mismo modo, las consecuencias derivadas de las complicaciones trombóticas son desconocidas. El estudio TRICUS Euro (NCT04141137) se diseñó con el objetivo de conseguir la marca Conformité Européenne (CE) y evaluar la seguridad y eficacia del sistema TricValve en 35 pacientes a los 30 días y hasta los cinco años.
Prótesis TricentoEl dispositivo Tricento (NVT AG; Muri, Suiza) es una sofisticación del concepto CAVI. Está compuesto por un stent de nitinol con anclaje bicava y una válvula bicúspide de pericardio porcino en el lateral. Mediante acceso transfemoral, el dispositivo se libera desde la VCS hacia la VCI a través de un catéter 24 Fr. Es totalmente reposicionable y recuperable hasta su despliegue final. Debe ser personalizado para cada paciente, por lo que tiene un alto coste. Ya que, nuevamente, la idea es evitar el flujo de retorno de la IT hacia las venas cavas, todos los inconvenientes asociados al CAVI se aplican a este dispositivo. Desde el primer implante en un ser humano en 201813, solo se han reportado series de casos pequeñas y con seguimiento a corto plazo. El más reciente, se trata de un estudio multicéntrico en el que participan cuatro centros españoles e incluye un total de seis pacientes. La tasa de éxito del implante del dispositivo Tricento fue del 100%. En todos los sujetos se observó una mejoría de la clase funcional NYHA a los cuatro meses de seguimiento. En el ecocardiograma de control a los seis meses se objetivó una reducción de la IT ≥ 1 grado en cuatro de los seis pacientes reclutados14.
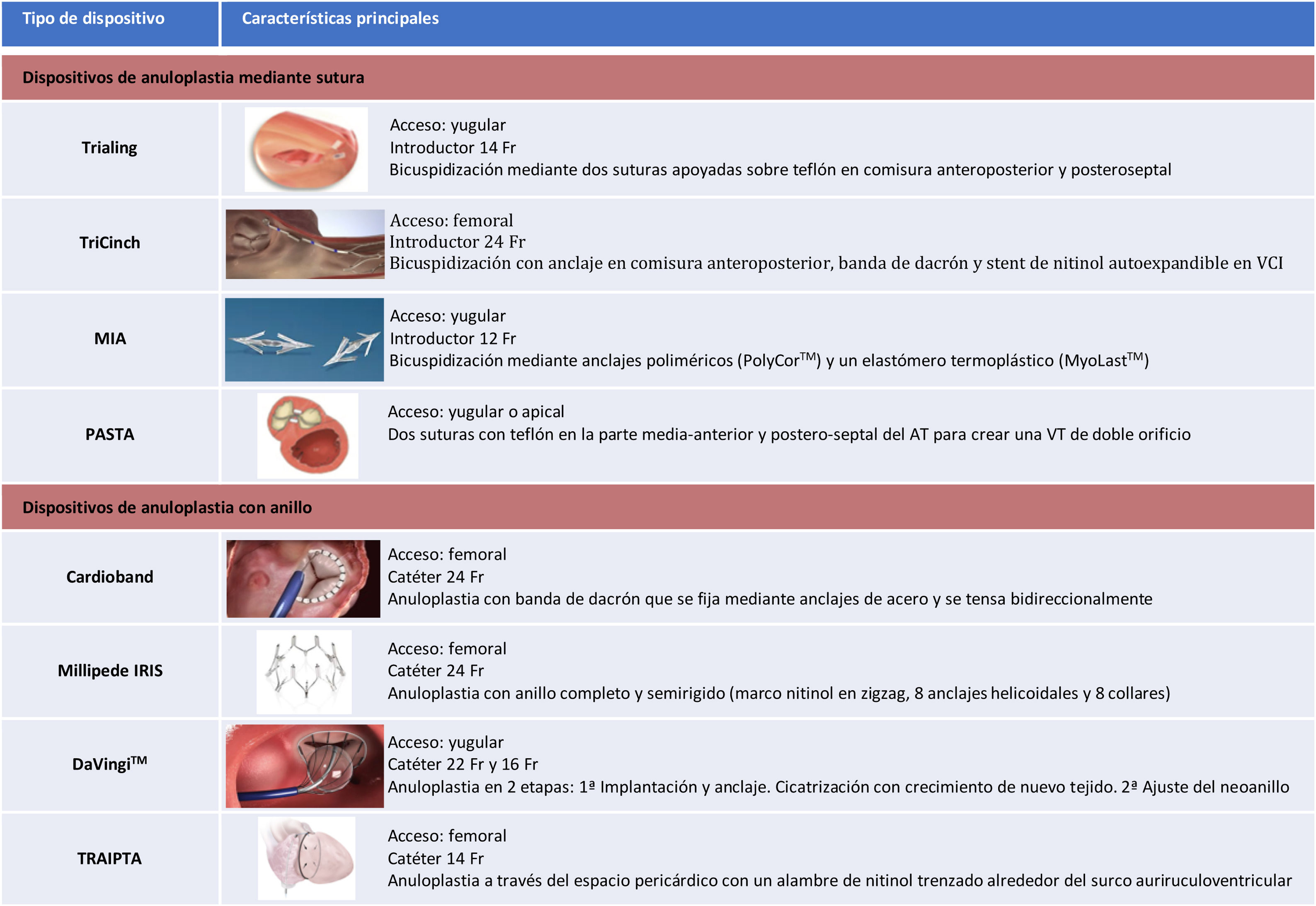
Dispositivos de anuloplastiaLa principal ventaja de los dispositivos de anuloplastia percutánea es que reproducen técnicas quirúrgicas ampliamente demostradas15. Adicionalmente, preservan la anatomía de la VT, permitiendo futuras opciones de tratamiento como el uso de VCP o dispositivos de coaptación, si fuera necesario. Se pueden clasificar en dos grupos según el mecanismo de acción, dispositivos de anuloplastia mediante sutura o con anillo, siendo los más destacados los siguientes (tabla 2):
Dispositivos de anuloplastia tricuspídea percutánea
AT: anillo tricuspídeo; VCI: vena cava inferior; VT: válvula tricúspide.
Trialing y PASTA: imágenes reproducidas con permiso de Curio. TriCinch63: imagen reproducida con permiso de Latib A et al.67 MIA: imagen reproducida con permiso de Micro Interventional Devices, IncTM. Cardioband: imagen reproducida con permiso de Edwards Lifesciences. Millipede IRIS: imagen reproducida con permiso de Boston Scientific Corporation. DaVingiTM: imagen reproducida con permiso de Cardiac Implants LLC. TRAIPTA: imagen reproducida con permiso de Rogers36.
El dispositivo Trialing (Mitraling Inc.; Tewksbury, Massachusetts, EE. UU.) imita la cirugía de bicuspidización de Kay-Cross16. Mediante acceso transyugular, se introduce un catéter articulado que atraviesa la VT hasta el VD. Se avanza una guía de radiofrecuencia que se dirige retrógradamente hacia el AT bajo control por ecocardiograma transesofágico (ETE). A continuación, se liberan dos suturas apoyadas sobre teflón a nivel de la comisura anteroposterior y posteroseptal, respectivamente. Se aproximan para aplicar el velo posterior y se fijan en cara auricular. En el ensayo clínico SCOUT (NCT02574650) se evaluó la viabilidad y seguridad del sistema Trialing en 15 pacientes. El implante del dispositivo se logró en todos los sujetos, sin embargo, un paciente requirió la colocación de un stent en la arteria coronaria derecha por compresión extrínseca de la misma. A los 30 días del procedimiento, tres personas presentaron dehiscencia de una o más suturas. En los restantes 12 pacientes, se observó una reducción significativa del diámetro del AT y del área del orificio regurgitante efectivo, así como un aumento del volumen sistólico del ventrículo izquierdo y una mejoría de la clase funcional NYHA, la prueba de la marcha a los seis minutos y la calidad de vida con el Minnesota Living Heart Failure Questionnaire (MLHFQ)17. A los 12 meses, se registró una muerte no relacionada con el dispositivo ni el procedimiento y un paciente requirió reintervención electiva. Las mejoras en la clase funcional NYHA y en la calidad de vida se mantuvieron durante el seguimiento18,19. Está en curso el ensayo clínico SCOUT-II (NCT03225612) que incluirá a 60 pacientes de 15 centros de EE. UU. y Europa con un seguimiento hasta por cinco años.
TriCinchEl dispositivo TriCinch (4 Tech Cardio; Galway, Irlanda) simula igualmente la bicuspidización quirúrgica. En esta ocasión, el dispositivo TriCinch de primera generación, cuenta para ello con los siguientes elementos: un anclaje de acero inoxidable en forma de sacacorchos, una banda de dacrón y un stent de nitinol autoexpandible disponible en cuatro tamaños entre 27 y 43 mm. La intervención se lleva a cabo guiada con fluoroscopia, ETE y ecocardiografía intracardiaca. Durante el procedimiento, se coloca una guía en la arteria coronaria derecha para prevenir la lesión de la misma. Se inserta un introductor de 24 Fr en la vena femoral derecha y se avanza un catéter deflectable que permite liberar el anclaje en el AT, cerca de la comisura anteroposterior. Se tracciona de la banda de dacrón para cinchar el AT y reducir así el diámetro septolateral de este. Por último, se despliega el stent en la VCI para asegurar el sistema y mantener la tensión aplicada. En el ensayo clínico PREVENT (NCT02098200), un estudio multicéntrico de 24 pacientes, el porcentaje de implantes exitosos fue del 75%, con reducción de la IT ≥ 1 grado en el 94% de los casos. Se registraron dos casos de hemopericardio y cuatro de desprendimiento del sistema de anclaje. En el seguimiento a seis meses, se observó una mejoría significativa de la distancia recorrida en la prueba de la marcha a los seis minutos y de la calidad de vida, con un 75% de los pacientes en clase I o II de la NYHA20.
En la segunda generación del dispositivo TriCinch, el sistema de anclaje tiene forma hemiespiral y se fija en el espacio pericárdico. La experiencia preliminar en humanos reveló una reducción significativa de la IT, así como mejoras en la clase funcional NYHA y en la calidad de vida medida con el Kansas City Cardiomyopathy Questionnaire (KCCQ) a los 30 días21,22. Estos resultados se evaluarán más a fondo en dos nuevos ensayos clínicos; Clinical Trial Evaluation of the Percutaneous 4 Tech TriCinch Coil Tricuspid Valve Repair System (NCT03294200) y Early Feasibility Study of the Percutaneous 4 Tech TriCinch Coil Tricuspid Valve Repair System (NCT03632967).
Minimally Invasive Annuloplasty (MIA)La anuloplastia mínimamente invasiva (MIA, Micro Interventional Devices, IncTM; Newtown, Pennsylvania, EE. UU.) se trata del primer sistema en el mundo en incorporar anclajes poliméricos de baja masa (PolyCorTM) y un elastómero termoplástico (MyoLastTM) para reproducir la bicuspidización quirúrgica de la VT23. El procedimiento se realiza guiado por fluoroscopia y ETE 3 D. Utilizando un sistema de liberación de 12 Fr se despliegan múltiples anclajes en la región entre las comisuras anteroposterior y posteroseptal que, seguidamente, se tensan con el elastómero provocando así la obliteración del velo posterior. Está en marcha el estudio STTAR que incluye 40 pacientes en el brazo de tratamiento percutáneo. En los primeros cuatro pacientes inscritos, se ha observado una reducción significativa de la IT y una disminución del área del AT del 48%, en ausencia de eventos adversos mayores24.
Pledget-Assisted Suture Transcatheter Annuloplasty (PASTA)La anuloplastia transcatéter con sutura asistida con teflón emula la técnica de doble orificio de Hetzer. Mediante un abordaje transyugular o transapical se colocan secuencialmente dos suturas con teflón en la parte media-anterior y posteroseptal del AT y se anudan con un dispositivo Cor-Knot (LSI Solutions; New York, New York, EE. UU.), creando así una VT de doble orificio. En un estudio con 22 cerdos, PASTA redujo las dimensiones del AT y el grado de IT. No obstante, cuatro animales tuvieron complicaciones relacionadas con el dispositivo (desgarro y atrapamiento de valvas, atrapamiento de cuerdas, bloqueo transitorio del nodo auriculoventricular y fibrilación ventricular) y otros cuatro presentaron complicaciones relacionadas con el abordaje transapical (neumotórax, hemotórax y derrame pericárdico)25. Poco después, se comunicaron los resultados de los primeros casos en humanos con uso compasivo26.
CardiobandEl sistema Cardioband (Edwards Lifesciences; Irvine, California, EE. UU.) consiste en una banda de dacrón ajustable que se fija en posición supraanular, de manera similar a la anuloplastia quirúrgica. Se inserta a través de un introductor transfemoral de 24 Fr. Requiere control por fluoroscopia y ETE. La banda se fija al AT mediante 17 anclajes de acero inoxidable de 6 mm de longitud colocados en la cara auricular del AT respetando el velo septal. Una vez fijada, se tensa bidireccionalmente para reducir proporcionalmente las dimensiones del AT. Obtuvo la marca CE en abril de 2018 tras conocerse los resultados del estudio TRI-REPAIR (NCT02981953). Según los datos publicados en este estudio con 30 pacientes, el éxito técnico del procedimiento fue del 100% y se objetivó una reducción significativa del diámetro anular septolateral (9%), del área efectiva del orificio regurgitante (50%) y del ancho de la vena contracta (28%) a los seis meses. Además, aumentó la distancia en la prueba de marcha a los seis minutos (60 m) y la puntuación promedio del KCCQ (24 puntos). El 76% de los pacientes mejoraron en al menos una clase funcional de la NYHA, con 88% de los pacientes clase funcional I o II de la NYHA a los seis meses27. Las mejorías ecocardiográficas y clínicas se mantuvieron al año de seguimiento28. La incidencia de eventos adversos mayores (muerte, infarto agudo de miocardio, accidente cerebrovascular, taponamiento cardiaco y cirugía cardiaca relacionada con el dispositivo) fue del 13% a los 30 días29. La tasa de mortalidad por todas las causas fue del 10% a los seis meses y del 17% al año27,28. Actualmente, está en curso el ensayo TriBAND (NCT03779490), un estudio de poscomercialización para evaluar el rendimiento y seguridad de la reparación transcatéter tricuspídea con el sistema Cardioband. Se espera que se recluten un total de 150 pacientes con seguimiento a los 30 días, seis meses y anual hasta llegar a los cinco años.
En enero del 2021, consiguió la aprobación por la Administración de Drogas y Alimentos (FDA) de EE. UU., tras conocerse los resultados del estudio Edwards Cardioband Tricuspid Valve Reconstruction System Early Feasibility (NCT03382457)30. Según dicho estudio, que incluyó 30 pacientes con IT funcional crónica sintomática severa, el éxito técnico fue del 93%. A los 30 días, el diámetro septolateral del AT se redujo en un 13% y el 85% de los pacientes presentó una disminución de la IT ≥ 1 grado, con un 75% de los pacientes en clase I o II de la NYHA y una puntuación media del KCCQ 16 puntos por encima de la basal. No hubo ninguna muerte relacionada con el dispositivo o el procedimiento. El estudio ACTIVE TR US Pivotal Trial (NCT03016975) es un ensayo clínico aleatorizado y multicéntrico que incluirá 375 pacientes con un período de seguimiento de hasta cinco años. La fecha estimada de finalización del estudio es 2024.
Millipede IRISEl dispositivo Millipede IRIS (Boston Scientific; Marlborough, Massachusetts, EE. UU.) es un anillo completo y semirrígido que consta de un marco plegable de nitinol en forma zigzag, ocho anclajes helicoidales en la base para su fijación al AT y ocho collares en cada punta que se ajustan de forma individual para reducir así las porciones más dilatadas del AT. Es totalmente reposicionable y recuperable, el anclaje cerca del nódulo auriculoventricular se puede retirar para minimizar el riesgo de alteraciones de la conducción, y no requiere anticoagulación oral. Se ha implantado quirúrgicamente en dos pacientes sometidos a reparación conjunta de la válvula mitral, mostrando una reducción significativa del AT (40%) y del grado de IT que se mantuvo estable a los seis y 12 meses31,32. Se está desarrollando un sistema de liberación transcatéter dedicado a la VT. Aunque la experiencia inicial presagia resultados halagüeños, hacen falta cohortes de pacientes más grandes para demostrarlos.
DaVingiTMEl sistema DaVingiTM (Cardiac Implants LLC; Wilmington, Delaware, EE. UU.) consiste en un anillo completo y flexible conformado por los siguientes elementos: una capa exterior de tela, una matriz de anclajes preestablecidos y un cordón de ajuste interno. El procedimiento se desarrolla en dos etapas. En la primera fase, se coloca el anillo en el lado auricular del AT, utilizando un dispositivo de liberación de 22 Fr con un balón distal que apoya la estabilización del anillo. Una vez implantado, se disparan simultáneamente todos los anclajes. Se desencadena así un proceso de cicatrización que promueve el crecimiento de nuevo tejido alrededor del AT nativo. En la segunda fase, se constriñe el neoanillo fibroso tirando del cordón alojado en la vena yugular con ayuda de un dispositivo de ajuste de 16 Fr creado para tal finalidad33. La viabilidad y seguridad del sistema DaVingiTM se están evaluando actualmente en 15 pacientes con IT secundaria34.
TRansAtrial IntraPericardial Tricuspid Annuloplasty (TRAIPTA)La anuloplastia tricuspídea intrapericárdica transauricular es un sistema de anuloplastia indirecta. A través de una vena femoral y, tras la punción de la orejuela de la AD, se accede al espacio pericárdico para colocar alrededor del surco auriculoventricular el dispositivo consistente en un alambre de nitinol trenzado capaz de ejercer una compresión externa controlada sobre el AT. Una vez apretado y obtenida la reducción deseada del AT, se recupera el sistema de administración y se sella la punción de la orejuela de la AD con un oclusor de nitinol o biorreabsorbible. Esta técnica requiere que el espacio pericárdico esté libre de adherencias, lo que excluye su uso en pacientes con antecedentes personales de pericarditis o pericardiectomía previa35. En nueve cerdos sanos, se logró una reducción significativa de los diámetros anteroposterior y septolateral, así como del área y del perímetro del AT. Se observaron pequeños derrames pericárdicos inmediatamente después del procedimiento, con resolución espontánea y sin secuelas durante el seguimiento. En otros cuatro cerdos con IT funcional, mostró una disminución del grado de IT36. Hay planes para una primera evaluación en humanos37.
Dispositivos de coaptaciónEl número de dispositivos transcatéter dirigidos a la restauración de la coaptación de los velos ha ido creciendo exponencialmente. Algunos de los sistemas que despiertan más interés se resumen a continuación (tabla 3):
TriClipTMLa reparación percutánea edge-to-edge con dispositivo MitraClip® comenzó a utilizarse en posición tricuspídea en 201638. La familiaridad del operador con este sistema, ha propiciado que se haya convertido en el tratamiento endovascular más extendido en la actualidad, representando el 66% de todas las terapias transcatéter dirigidas al manejo de la IT severa, según datos del registro internacional TriValve39. Basándose en la técnica quirúrgica de Clover40, esta estrategia consigue la aproximación de los velos tricuspídeos mediante la colocación de clips de cromo-cobalto recubiertos de poliéster que se introducen por acceso yugular o femoral. En un estudio multicéntrico con 64 pacientes consecutivos, se describió una tasa de éxito en el implante del dispositivo del 97%, con una reducción de la gravedad de la IT en al menos un grado en el 91%, acompañada de una disminución significativa del área del orificio regurgitante efectivo, del ancho de la vena contracta y del volumen de regurgitación, así como una mejoría significativa de la clase funcional NYHA y de la prueba de la marcha a los seis minutos a los 30 días41. Otros dos estudios demostraron que dichas mejorías ecocardiográficas y clínicas se mantenían constantes en el seguimiento a seis y 12 meses42,43. La tasa de mortalidad por todas las causas fue del 5, 16 y 38%, a los 30 días, seis meses y 12 meses de seguimiento, respectivamente41–43. La presencia de jets predominantemente centrales o anteroseptales se identificó como factor predictor del éxito del procedimiento44,45.
La reparación percutánea borde a borde con MitraClip® de la VT supone un desafío. Una de las principales dificultades es la variabilidad anatómica y grandes defectos de coaptación, con mayor complejidad para la fijación del sistema a las valvas, que hace que, a menudo, se necesiten múltiples clips. Una nueva generación, el MitraClip XT®, con brazos 5 mm más largos que su predecesor, destinados a facilitar el alcance y el agarre, aparecería poco después para tratar de dar solución a este problema. Sin embargo, la experiencia inicial en 31 pacientes tratados únicamente con el dispositivo MitraClip XT®, reveló que el 25% de los sujetos con una distancia de coaptación ≥ 7 mm experimentaron el desprendimiento de algún clip46. Otros retos que plantea son la laboriosidad para dirigir el sistema en el interior de la AD, perpendicular al plano del AT, y en el VD, sin quedar atrapado en el aparato subvalvular, y para visualizar las valvas con ETE, ya que, a diferencia de lo que ocurre con la válvula mitral, la calidad de la imagen suele ser subóptima. El TriClipTM es una adaptación del MitraClip XT®, con el que comparte la misma tecnología de clip, pero con un sistema de liberación creado para su uso exclusivo en el corazón derecho. El estudio TRILUMINATE (NCT03227757) es un ensayo clínico multicéntrico, prospectivo y de un solo brazo de tratamiento, diseñado para evaluar la seguridad y eficacia del dispositivo TriClipTM en 85 pacientes con IT ≥ 2 sintomática. A los 30 días, la IT se redujo al menos en un grado en el 86% de los pacientes reclutados. A los seis meses, tres pacientes (4%) presentaron algún evento mayor adverso y cuatro (5%) fallecieron47. A principios de año salieron a la luz los resultados a los 12 meses de seguimiento. La gravedad de la IT se redujo a moderada o ligera en el 71% de los individuos. Se apreció un remodelado inverso del VD, con mejoría de su tamaño y función. Además, los pacientes tuvieron una mejoría clínica significativa, valorada con la clase funcional NYHA, en la prueba de la marcha de seis minutos y en el KCCQ. La tasa de eventos mayores adversos y mortalidad por todas las causas fueron, en ambos casos, del 7,1% al año de seguimiento48. Aún se necesita conocer los resultados a dos, tres y cinco años para poder llegar a conclusiones firmes. El estudio TRILUMINATE Pivotal Trial (NCT03904147) es un ensayo clínico aleatorizado que pretende reclutar 700 pacientes con IT severa sintomática y riesgo quirúrgico intermedio o alto y comparar los resultados del TriClipTM frente al tratamiento médico óptimo.
FORMAEl dispositivo FORMA (Edwards Lifesciences; Irvine, California, EE. UU.) aumenta la superficie de coaptación de los velos ocupando el orificio regurgitante. A través de la vena axilar o subclavia izquierda, se introduce un riel que se ancla distalmente en el ápex del VD. Dicho riel sirve para guiar la colocación de un espaciador, que no es más que un balón cilíndrico relleno de espuma y expansible pasivamente que se posiciona en el orificio regurgitante. El espaciador está disponible en tres tamaños (12, 15 y 18 mm), requiriendo en cada caso un introductor de calibre diferente (20 o 24 Fr). El dispositivo es totalmente recuperable y reposicionable. Una vez se comprueba que está en una posición óptima por fluoroscopia y ETE 3 D, se fija proximalmente en plano subcutáneo49. En un estudio multicéntrico con 18 pacientes tratados en un programa de uso compasivo, la implantación del dispositivo fue exitosa en el 89%, con una reducción de la IT a moderada-severa o menos en el 69% a los 30 días y en el 46% al año de seguimiento50. Curiosamente, a los dos a tres años de seguimiento, el porcentaje de pacientes con IT moderada-severa o menor fue del 67%51. Probablemente, este hecho se deba a que la evaluación ecocardiográfica de la IT residual es especialmente compleja dada la presencia de múltiples chorros pequeños. Posteriormente, en un estudio inicial de viabilidad de EE. UU. con 29 pacientes y seguimiento a 30 días52, hubo dos muertes debido a la perforación del VD y otros nueve pacientes presentaron algún evento mayor adverso (muerte, lesión vascular grave, sangrado amenazante o migración del dispositivo, entre otras). Todo ello condujo a mejoras en el dispositivo53. Aunque se utilizó satisfactoriamente en pacientes portadores de marcapasos definitivo u otros dispositivos de estimulación cardiaca, esta población suele tener un orificio de regurgitación asimétrico, por lo que la reducción de la IT es menos efectiva. En la actualidad, están en marcha un nuevo estudio de viabilidad temprana, con las mejoras del dispositivo ya adoptadas, y el ensayo clínico SPACER (NCT02787408) que, previsiblemente, ampliarán sustancialmente nuestra compresión sobre el rendimiento de este sistema.
PascalEl sistema Pascal (Edwards Lifesciences; Irvine, California, EE. UU.) integra aspectos técnicos de los dispositivos MitraClip® y FORMA al combinar un espaciador central de 10 mm y dos brazos y palas metálicas para aproximar los velos y sujetar el espaciador a los mismos, superando así posibles limitaciones de los sistemas anteriores por separado. El procedimiento se lleva a cabo mediante abordaje transfemoral, a través de un introductor de 22 Fr y guiado por ETE. Tras informarse la primera experiencia en humanos54, se han presentado los resultados de 28 pacientes tratados con uso compasivo, observándose una reducción de al menos un grado de la IT en el 86% y una mejoría significativa de la clase funcional NYHA, con el 88% en clase funcional NYHA ≤ II55. Se necesitan más datos para extender su uso, habiéndose propuesto dos ensayos clínicos: CLASP TR EFS (NCT037455313) y CLASP II TR (NCT04097145).
DiscusiónMás frecuentemente, la regurgitación tricuspídea es funcional, debido a la dilatación y disfunción del VD por sobrecarga de presión y/o volumen del mismo en ausencia de velos estructuralmente patológicos. Posibles causas de IT orgánica son; endocarditis infecciosa (especialmente en adictos a drogas por vía parenteral), enfermedad reumática, síndrome carcinoide, degeneración mixomatosa, enfermedad congénita (anomalía de Ebstein), toxicidad, traumatismos, etc. Tradicionalmente, la cirugía ha sido el tratamiento gold standard de la IT. No obstante, establecer el momento idóneo para llevar a cabo una intervención quirúrgica en estos pacientes sigue siendo controvertido, en consonancia con la escasez de datos publicados y la heterogeneidad de su naturaleza. Las guías de práctica clínica vigentes recomiendan la reparación precoz de la VT en pacientes con dilatación del AT sometidos a cirugía cardiaca izquierda, incluso en presencia de IT leve56–58, así como en individuos con IT aislada severa sintomática o asintomática, pero con dilatación/disfunción progresiva del VD. Pese a ello, solo una minoría de estos sujetos se someten a una cirugía aislada de la VT. Muy probablemente, esta reticencia se deba a la alta mortalidad asociada. Dos registros contemporáneos de EE. UU. informaron una mortalidad hospitalaria entre el 8 al 10%59,60 y una mortalidad al año del 24%60. Según el registro de intervenciones de la Sociedad Española de Cirugía Cardiovascular y Endovascular de 2019, la cirugía aislada de la VT representa tan solo un 1,95% del total de las cirugías univalvulares aisladas, con una mortalidad observada del 13,92% para la sustitución valvular aislada y del 5,77% para la reparación valvular aislada61.
Este escenario tan hostil ha permitido el desarrollo de numerosas terapias percutáneas que tienen como objetivo un cambio de paradigma en el tratamiento de la IT. Es por ello que este grupo considera de vital importancia analizar este tipo de procedimientos dentro de un foro quirúrgico. Desde nuestro punto de vista, este hito de la medicina moderna no debe ser privativo de la cardiología intervencionista, sino que debe incorporarse al armamento terapéutico de cualquier servicio de cirugía cardiovascular. Vale la pena recalcar que, dentro del territorio nacional, el único grupo quirúrgico en publicar su experiencia inicial, ha sido el del Hospital Puerta del Mar de Cádiz, que presentó un caso de implante de VT transcatéter en un paciente con disfunción de bioprótesis62.
La aplicación clínica del tratamiento percutáneo de la IT con los diferentes dispositivos disponibles en la actualidad, se está evaluando en el Registro TriValve39, un registro internacional en el que participan 18 centros de Europa y EE. UU. La última actualización reunió un total de 312 pacientes. El espectro clínico de la población estudiada mostró un riesgo quirúrgico alto (EuroSCORE II 9 ± 8%), con síntomas graves al ingreso (95% en clase funcional NYHA III-IV) y antecedentes personales de cirugía cardiaca izquierda previa en el 35%. En el 93% de los sujetos la IT fue de etiología funcional y, mayoritariamente, de grado severo o torrencial (vena contracta 1,1 ± 0,5 cm, orificio regurgitante efectivo 0,78 ± 0,6 cm2, volumen regurgitante 54 ± 34 mL/latido). Los dispositivos empleados fueron, por orden decreciente de frecuencia: MitraClip® (66%), CAVI (9%), FORMA (8%), Trialing (6%), Cardioband (4%), TriCinch (4%) y, por último, otros como NaviGate o Pascal (3%). El éxito del procedimiento (definido por una IT residual ≤ 2) se obtuvo en el 72,8%, identificándose la profundidad de coaptación > 1 cm como predictor independiente de fracaso en el procedimiento. La mortalidad global a los 30 días fue del 3,6%, siendo significativamente menor entre los pacientes en quienes el procedimiento resultó exitoso (1,9 vs. 6,9%, p = 0,04). Se observó una mejoría clínica mantenida a los seis meses de seguimiento, con el 54% de los pacientes en clase funcional NYHA I-II. La supervivencia global fue del 77,2 ± 5,9% a los 1,5 años, observándose nuevamente una supervivencia mayor en aquellos sujetos en los que el procedimiento se logró con éxito (70,3 ± 8% vs. 90,8 ± 4% al año, p = 0,0037).
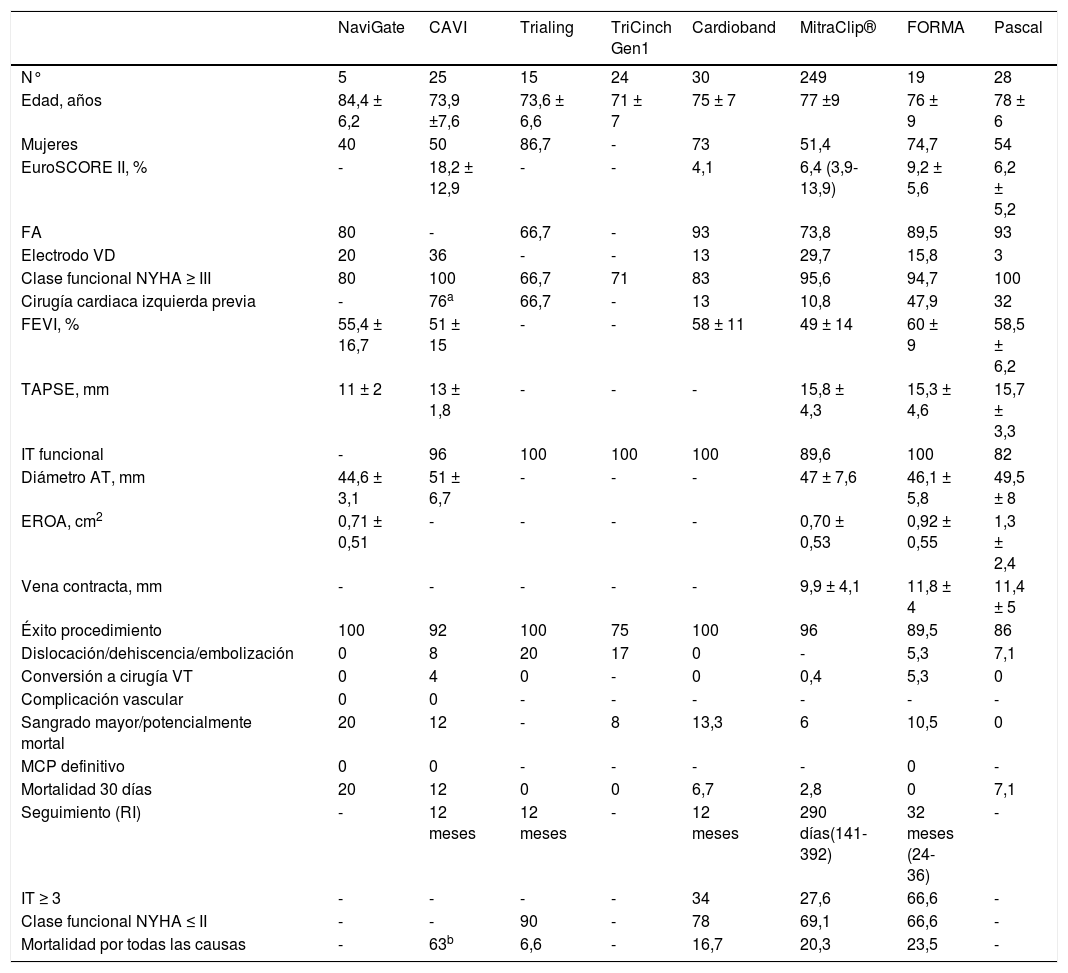
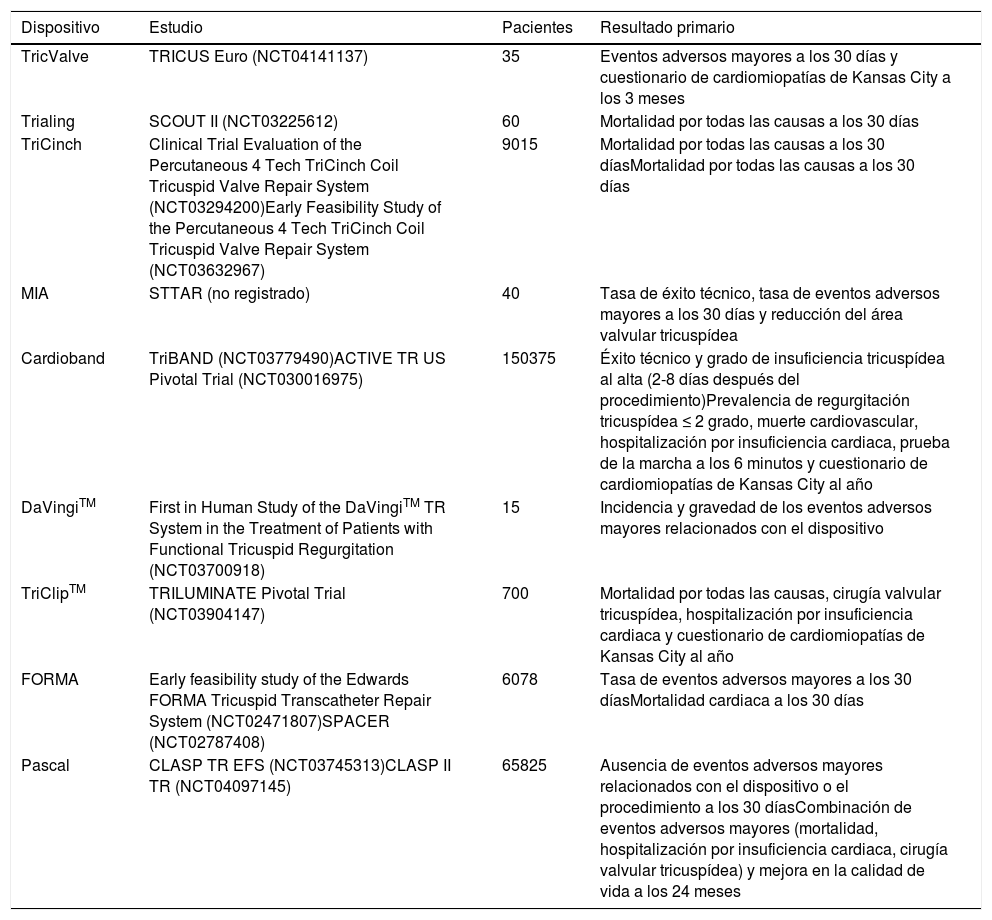
La experiencia global, así como los estudios en marcha sobre el tratamiento transcatéter de la regurgitación tricuspídea se resumen en las tablas 4 y 5. Con base en el análisis crítico de estos datos, aún es demasiado pronto para predecir qué dispositivo será más popular en el futuro. Hoy por hoy, los dispositivos de coaptación y, particularmente, la reparación edge-to-edge con el sistema MitraClip®, lideran este campo (resultados demostrados a corto y medio plazo, mayor experiencia del operador y preservación de la anatomía de la VT nativa). Sin embargo, este escenario puede cambiar radicalmente tras la obtención de la marca CE y la aprobación por la FDA por parte del dispositivo Cardioband. Asimismo, aún debemos asistir al desarrollo de las VCP en posición ortotópica ya que, en manos experimentadas, podrían ofrecer potenciales ventajas (plataforma de tratamiento tanto de la IT funcional como orgánica, reproducibilidad, curva de aprendizaje fácil y eliminación completa de la IT).
Experiencia global con el Tratamiento Transcatéter de la Regurgitación Tricuspídea*
| NaviGate | CAVI | Trialing | TriCinch Gen1 | Cardioband | MitraClip® | FORMA | Pascal | |
|---|---|---|---|---|---|---|---|---|
| N° | 5 | 25 | 15 | 24 | 30 | 249 | 19 | 28 |
| Edad, años | 84,4 ± 6,2 | 73,9 ±7,6 | 73,6 ± 6,6 | 71 ± 7 | 75 ± 7 | 77 ±9 | 76 ± 9 | 78 ± 6 |
| Mujeres | 40 | 50 | 86,7 | - | 73 | 51,4 | 74,7 | 54 |
| EuroSCORE II, % | - | 18,2 ± 12,9 | - | - | 4,1 | 6,4 (3,9-13,9) | 9,2 ± 5,6 | 6,2 ± 5,2 |
| FA | 80 | - | 66,7 | - | 93 | 73,8 | 89,5 | 93 |
| Electrodo VD | 20 | 36 | - | - | 13 | 29,7 | 15,8 | 3 |
| Clase funcional NYHA ≥ III | 80 | 100 | 66,7 | 71 | 83 | 95,6 | 94,7 | 100 |
| Cirugía cardiaca izquierda previa | - | 76a | 66,7 | - | 13 | 10,8 | 47,9 | 32 |
| FEVI, % | 55,4 ± 16,7 | 51 ± 15 | - | - | 58 ± 11 | 49 ± 14 | 60 ± 9 | 58,5 ± 6,2 |
| TAPSE, mm | 11 ± 2 | 13 ± 1,8 | - | - | - | 15,8 ± 4,3 | 15,3 ± 4,6 | 15,7 ± 3,3 |
| IT funcional | - | 96 | 100 | 100 | 100 | 89,6 | 100 | 82 |
| Diámetro AT, mm | 44,6 ± 3,1 | 51 ± 6,7 | - | - | - | 47 ± 7,6 | 46,1 ± 5,8 | 49,5 ± 8 |
| EROA, cm2 | 0,71 ± 0,51 | - | - | - | - | 0,70 ± 0,53 | 0,92 ± 0,55 | 1,3 ± 2,4 |
| Vena contracta, mm | - | - | - | - | - | 9,9 ± 4,1 | 11,8 ± 4 | 11,4 ± 5 |
| Éxito procedimiento | 100 | 92 | 100 | 75 | 100 | 96 | 89,5 | 86 |
| Dislocación/dehiscencia/embolización | 0 | 8 | 20 | 17 | 0 | - | 5,3 | 7,1 |
| Conversión a cirugía VT | 0 | 4 | 0 | - | 0 | 0,4 | 5,3 | 0 |
| Complicación vascular | 0 | 0 | - | - | - | - | - | - |
| Sangrado mayor/potencialmente mortal | 20 | 12 | - | 8 | 13,3 | 6 | 10,5 | 0 |
| MCP definitivo | 0 | 0 | - | - | - | - | 0 | - |
| Mortalidad 30 días | 20 | 12 | 0 | 0 | 6,7 | 2,8 | 0 | 7,1 |
| Seguimiento (RI) | - | 12 meses | 12 meses | - | 12 meses | 290 días(141-392) | 32 meses (24-36) | - |
| IT ≥ 3 | - | - | - | - | 34 | 27,6 | 66,6 | - |
| Clase funcional NYHA ≤ II | - | - | 90 | - | 78 | 69,1 | 66,6 | - |
| Mortalidad por todas las causas | - | 63b | 6,6 | - | 16,7 | 20,3 | 23,5 | - |
AT: anillo tricuspídeo; EROA: área del orificio regurgitante efectivo; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; IT: insuficiencia tricuspídea; MCP: marcapasos; N°: número de pacientes; NYHA: New York Heart Association; RI: rango intercuartílico; TAPSE: excursión sistólica del plano lateral del anillo tricuspídeo; VD: ventrículo derecho; VT: válvula tricúspide.
Estudios en marcha sobre el Tratamiento Transcatéter de la Regurgitación Tricuspídea
| Dispositivo | Estudio | Pacientes | Resultado primario |
|---|---|---|---|
| TricValve | TRICUS Euro (NCT04141137) | 35 | Eventos adversos mayores a los 30 días y cuestionario de cardiomiopatías de Kansas City a los 3 meses |
| Trialing | SCOUT II (NCT03225612) | 60 | Mortalidad por todas las causas a los 30 días |
| TriCinch | Clinical Trial Evaluation of the Percutaneous 4 Tech TriCinch Coil Tricuspid Valve Repair System (NCT03294200)Early Feasibility Study of the Percutaneous 4 Tech TriCinch Coil Tricuspid Valve Repair System (NCT03632967) | 9015 | Mortalidad por todas las causas a los 30 díasMortalidad por todas las causas a los 30 días |
| MIA | STTAR (no registrado) | 40 | Tasa de éxito técnico, tasa de eventos adversos mayores a los 30 días y reducción del área valvular tricuspídea |
| Cardioband | TriBAND (NCT03779490)ACTIVE TR US Pivotal Trial (NCT030016975) | 150375 | Éxito técnico y grado de insuficiencia tricuspídea al alta (2-8 días después del procedimiento)Prevalencia de regurgitación tricuspídea ≤ 2 grado, muerte cardiovascular, hospitalización por insuficiencia cardiaca, prueba de la marcha a los 6 minutos y cuestionario de cardiomiopatías de Kansas City al año |
| DaVingiTM | First in Human Study of the DaVingiTM TR System in the Treatment of Patients with Functional Tricuspid Regurgitation (NCT03700918) | 15 | Incidencia y gravedad de los eventos adversos mayores relacionados con el dispositivo |
| TriClipTM | TRILUMINATE Pivotal Trial (NCT03904147) | 700 | Mortalidad por todas las causas, cirugía valvular tricuspídea, hospitalización por insuficiencia cardiaca y cuestionario de cardiomiopatías de Kansas City al año |
| FORMA | Early feasibility study of the Edwards FORMA Tricuspid Transcatheter Repair System (NCT02471807)SPACER (NCT02787408) | 6078 | Tasa de eventos adversos mayores a los 30 díasMortalidad cardiaca a los 30 días |
| Pascal | CLASP TR EFS (NCT03745313)CLASP II TR (NCT04097145) | 65825 | Ausencia de eventos adversos mayores relacionados con el dispositivo o el procedimiento a los 30 díasCombinación de eventos adversos mayores (mortalidad, hospitalización por insuficiencia cardiaca, cirugía valvular tricuspídea) y mejora en la calidad de vida a los 24 meses |
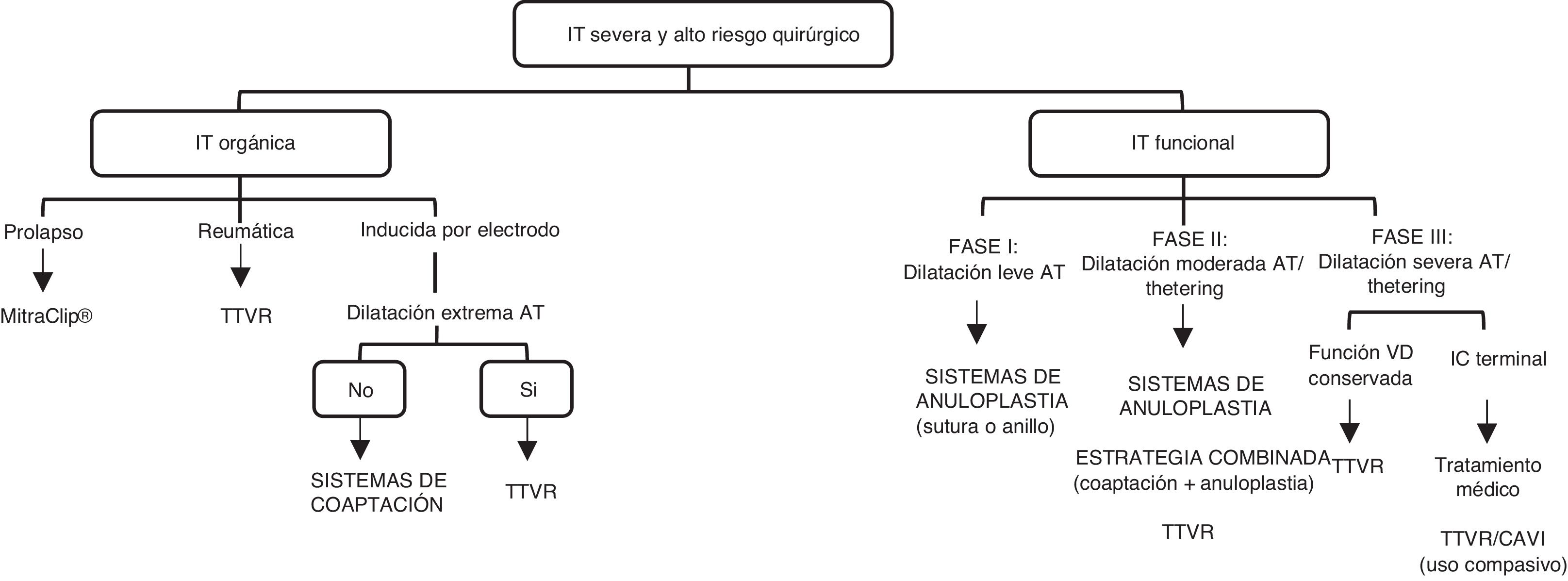
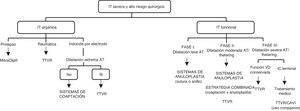
Se ha propuesto un algoritmo para la selección del dispositivo más adecuado con base en el mecanismo e historia natural de la IT (fig. 1)23. Si nos centramos en la IT funcional, en la fase inicial de la IT funcional, un sistema de anuloplastia podría ser suficiente. Una vez que progresa la dilatación del AT hacia moderada y se asocia a tethering de los velos, se puede elegir entre utilizar sistemas de coaptación o una estrategia combinada (dispositivos de coaptación + dispositivos de anuloplastia). Se han descrito combinaciones de MitraClip® con Cardioband63, MitraClip® con Trialing y MitraClip® con TriCinch39. En este punto, el TTVR también podría resultar útil. En la etapa final de la enfermedad, donde sobreviene una disfunción y remodelación progresivas del VD, se puede considerar el TTVR, reservando el CAVI para su uso compasivo en aquellos pacientes con signos o síntomas de insuficiencia cardiaca derecha en estado terminal.
Algoritmo para la selección del Tratamiento Transcáteter de la Regurgitación Tricuspídea*
* Adaptada con permiso de Asmarats et al.23
AT: anillo tricuspídeo; CAVI: implante de una válvula en vena cava; IC: insuficiencia cardiaca; IT: insuficiencia tricuspídea; TTVR: reemplazo valvular tricuspídeo transcatéter.
En la última década, hemos sido testigos del advenimiento y de la adopción generalizada de un sinfín de tratamientos endovasculares, motivados por los resultados insatisfactorios de la cirugía aislada de la IT. La experiencia inicial con el tratamiento transcatéter de la regurgitación tricuspídea con uso compasivo o en pacientes de riesgo quirúrgico alto/prohibitivo es alentadora, habiéndose asociado a mejoras clínicas y ecocardiográficas significativas. No obstante, estas técnicas no están exentas de complicaciones y los resultados a largo plazo continúan siendo inciertos. En los próximos años, los diferentes dispositivos percutáneos diseñados para el manejo de la IT deberán demostrar su viabilidad, seguridad y eficacia, siendo necesario para ello ensayos clínicos aleatorizados que confirmen su superioridad con respecto al tratamiento estándar, especialmente si se pretende extender su uso a un espectro más amplio de pacientes. Asimismo, es mandatorio que los futuros estudios arrojen luz sobre la estrategia más idónea en función de las peculiaridades de cada sujeto, como la disfunción del VD, tamaño del AT y características anatómicas.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.