Obesidad y Reflujo Gastro Esofágico
More infoLa persistencia de obesidad favorece el fracaso de la funduplicatura (FP) en el tratamiento del reflujo gastroesofágico (RGE). Sin embargo, la pérdida de peso obtenida con la realización de un bypass gástrico (BPG) permite una buena resolución de síntomas, sin incrementar la incidencia de complicaciones postoperatorias. Todo ello lleva a considerar que mientras la FP es la indicación en el paciente con IMC<30, en aquellos pacientes con IMC>35 el BPG se muestra como el procedimiento de elección. Pero todavía no existe un posicionamiento en el caso de pacientes con IMC entre 30 y 35, si bien deberemos tener en consideración que se ha descrito un aumento de recurrencia del RGE tras FP en pacientes con un IMC>30. Aunque la gastrectomía vertical (GV) es uno de los procedimientos bariátricos más frecuentemente utilizado en los últimos años, su asociación a una tasa elevada de RGE postoperatorio ha llevado a varios autores a proponer su realización asociada a un procedimiento antirreflujo en aquellos pacientes con síntomas de RGE.
Así mismo, en caso de constatarse la existencia de una hernia de hiato, esta debe ser tratada mediante hiatoplastia, tanto durante la realización de un BPG como de una GV. Este tratamiento simultáneo no se asocia con un incremento de complicaciones.
The persistence of obesity favors the failure of the fundoplication (FP) in the treatment of gastroesophageal reflux (GER). However, the weight loss obtained with the performance of a gastric bypass (GBP) allows a good resolution of symptoms, without increasing the incidence of post-operative complications. All of this leads us to consider that while FP is the indication in patients with BMI<30, in those patients with BMI>35, GBP appears to be the procedure of choice. But there is still no position in the case of patients with a BMI between 30 and 35, although we must take into account that an increase in GER recurrence has been described after FP in patients with a BMI>30. Although sleeve gastrectomy (SG) is one of the most frequently used bariatric procedures in recent years, its association with a high rate of post-operative GER has led several authors to propose its performance associated with an anti-reflux procedure in patients with GER symptoms.Likewise, if the existence of an hiatal hernia is verified, it must be treated by hiatoplasty, both during the performance of a GBP and a SG. This simultaneous treatment is not associated with an increase in complications.
Como se ha referido en capítulos anteriores, son varios los mecanismos fisiopatológicos que juegan un papel en el desarrollo del reflujo gastroesofágico (RGE) en pacientes obesos, incluyendo un esfínter esofágico inferior hipotónico, alteraciones motoras del esófago, o la disrupción anatómica o fisiológica de la unión esofagogástrica secundaria al incremento de la presión intraabdominal1. Independientemente de ello, diferentes estudios han demostrado la existencia de correlación entre la elevación del índice de masa corporal (IMC) y el grado de RGE2. La prevalencia de síntomas de RGE se sitúa en el 23%, el 27% y el 50% de pacientes según el IMC sea <25, 25-30, o >30kg/m2, y de hasta el 55% en pacientes candidatos a cirugía bariátrica3.
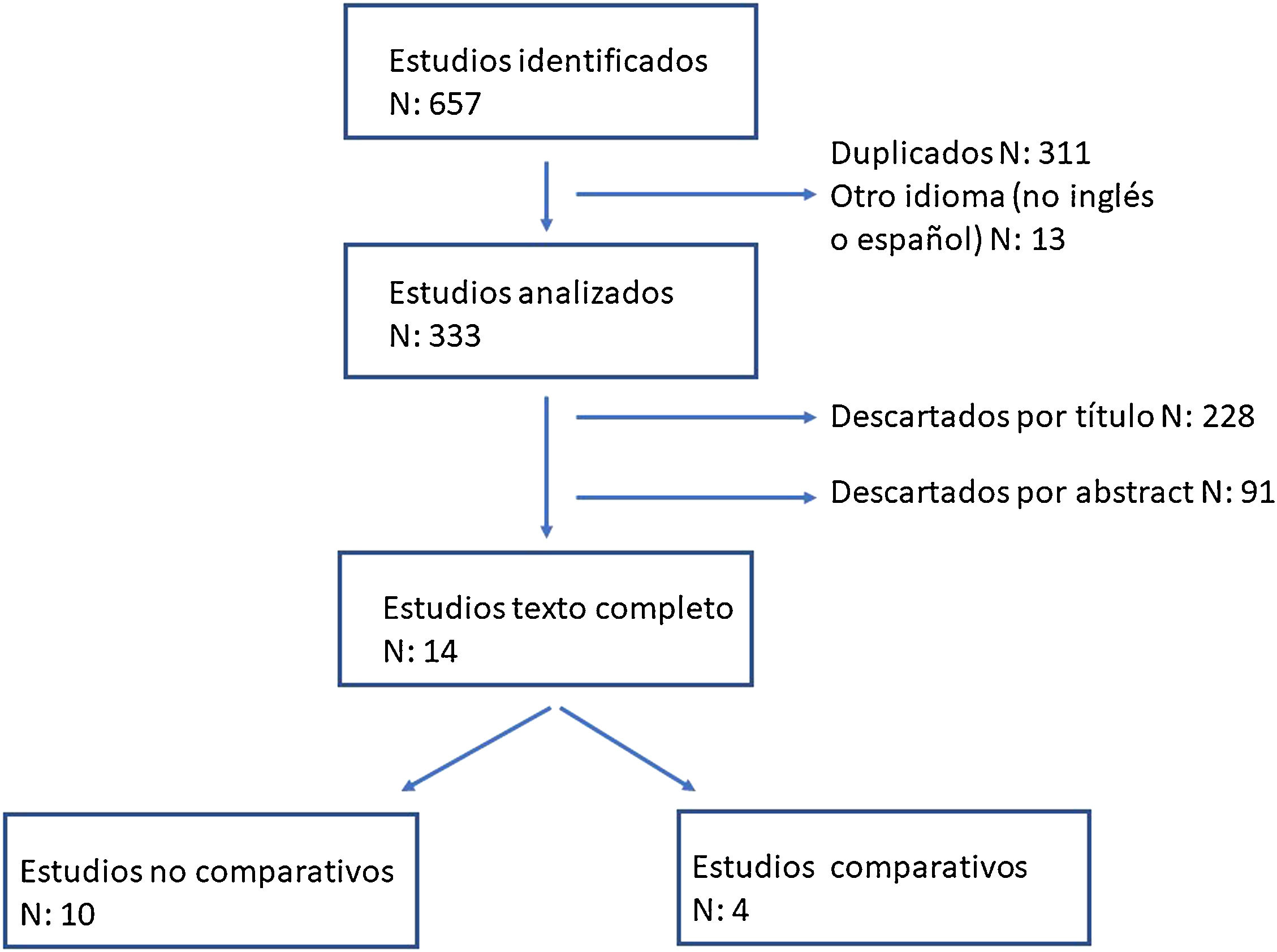
Cirugía antirreflujo vs cirugía bariátrica como tratamiento anti-RGE en el paciente con obesidadPara dar respuesta a esta cuestión mediante la cirugía basada en la evidencia hemos realizado una revisión sistemática de la literatura hasta septiembre de 2022 y hemos seleccionado aquellos estudios que informan de los resultados clínicos obtenidos comparando el bypass gástrico (BPG) y la funduplicatura (FP) en pacientes obesos con RGE. Para identificar los estudios hemos utilizado los siguientes términos: «obesity», «obese patient», «antireflux», «bariatric surgery», «gastric bypass», «fundoplication», «Nissen», «Toupet», «Dor». Las referencias de los artículos seleccionados se utilizaron para identificar otros artículos potencialmente relevantes. De los 657 artículos obtenidos, se descartaron 324 entre duplicados y escritos en un idioma diferente a español o inglés. A partir del título y el abstract-resumen de las publicaciones se excluyeron otros 319 artículos, quedándonos con 14 estudios clínicos que analizan resultados de la realización de FP o BPG en pacientes obesos con RGE (ver diagrama de flujo en la fig. 1). De esos 14 estudios, únicamente 4 comparan la realización de cirugía antirreflujo con el BPG (tabla 1) y su heterogeneidad y características no permite realizar un análisis cuantitativo.
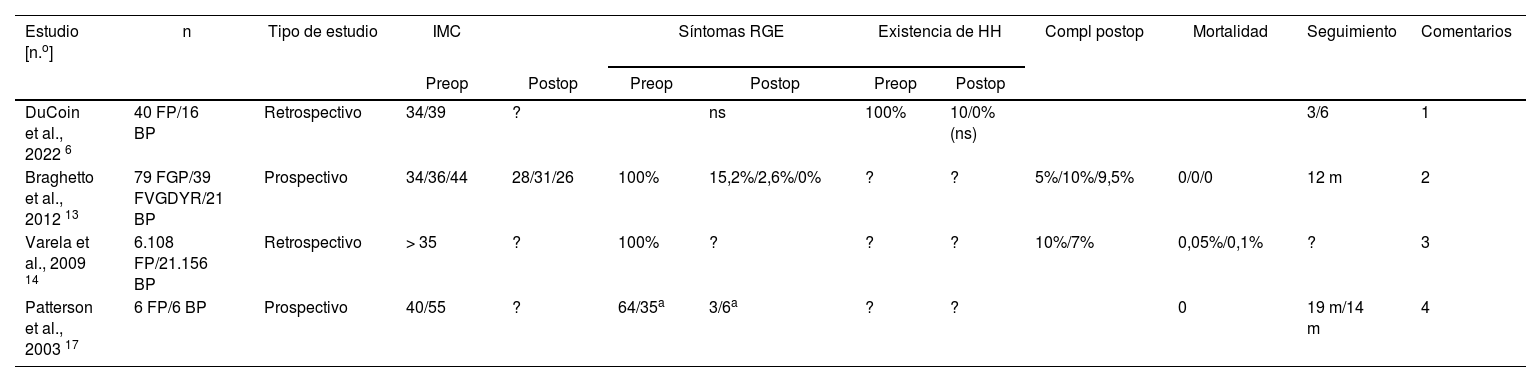
Resultados de los estudios comparativos bypass vs funduplicatura
| Estudio [n.o] | n | Tipo de estudio | IMC | Síntomas RGE | Existencia de HH | Compl postop | Mortalidad | Seguimiento | Comentarios | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Preop | Postop | Preop | Postop | Preop | Postop | |||||||
| DuCoin et al., 2022 6 | 40 FP/16 BP | Retrospectivo | 34/39 | ? | ns | 100% | 10/0% (ns) | 3/6 | 1 | |||
| Braghetto et al., 2012 13 | 79 FGP/39 FVGDYR/21 BP | Prospectivo | 34/36/44 | 28/31/26 | 100% | 15,2%/2,6%/0% | ? | ? | 5%/10%/9,5% | 0/0/0 | 12 m | 2 |
| Varela et al., 2009 14 | 6.108 FP/21.156 BP | Retrospectivo | > 35 | ? | 100% | ? | ? | ? | 10%/7% | 0,05%/0,1% | ? | 3 |
| Patterson et al., 2003 17 | 6 FP/6 BP | Prospectivo | 40/55 | ? | 64/35a | 3/6a | ? | ? | 0 | 19 m/14 m | 4 | |
BPG: bypass gástrico; FGP: funduplicatura +gastropexia posterior; FP: funduplicatura; FVGDYR: funduplicatura +vagotomia +gastrectomía con Y-Roux.
Puntuación de DeMeester.
Comentarios:
1. Mayor reducción de recurrencia de HH tras bypass gástrico sin significación estadística.
2. Similar regresión de la metaplasia intestinal (favoreciendo el BPG) pero la funduplicatura solo en Barrett corto y las otras dos técnicas en Barrett largo.
3. Pacientes del grupo baypass presentaban más comorbilidades.
4. pHmetrías postoperatorias normalizadas en todos los casos. No suficientemente comparables ambos grupos.
Uno de estos 4 estudios4 analiza el postoperatorio inmediato de una serie de 27.264 pacientes con obesidad mórbida sometidos a FP laparoscópica (n=6.108) o a BPG laparoscópico (n=21.156), objetivando una incidencia de complicaciones postoperatorias significativamente menor en el grupo de BPG, sin diferencias en cuanto a la estancia hospitalaria, la mortalidad o los costes hospitalarios. Pero, como los autores reconocen, la información postoperatoria es muy limitada en el tiempo y no permite obtener información en cuanto a la efectividad en el tratamiento del RGE así como la evolución del IMC. Por su parte, el estudio de Braghetto et al.5 se centra en el análisis de pacientes obesos que, además del RGE, presentan esófago de Barrett (EB) y compara fundamentalmente los resultados de tres procedimientos quirúrgicos sobre la evolución de la metaplasia intestinal: grupoI: FP con gastropexia posterior (n=79), grupoII: FP con vagotomía +gastrectomía distal y reconstrucción en Y de Roux (n=39) y grupoIII: BPG (n=21). En este estudio, la longitud del segmento de EB determinó la decisión de realizar una u otra intervención, indicando la FP con gastropexia en pacientes con segmento corto de EB, mientras que las otras dos técnicas se realizaron en los pacientes con segmento largo de EB. Los tres procedimientos obtuvieron buenos resultados en cuanto a la reducción postoperatoria de la sintomatología del RGE, así como regresión de la metaplasia intestinal (grupoI: 51,9%, grupoII: 51,3%, grupoIII: 61,9%). Los otros dos estudios2,6 comparan la efectividad antirreflujo de la FP y el BPG, constatando una mejora evidente de la clínica de RGE en el postoperatorio, sin diferencia significativa entre ambos procedimientos. Sin embargo, existen importantes sesgos, como diferencias en el IMC, o las puntuaciones de RGE de los pacientes de uno y otro grupo, que hacen difícil establecer conclusiones definitivas.
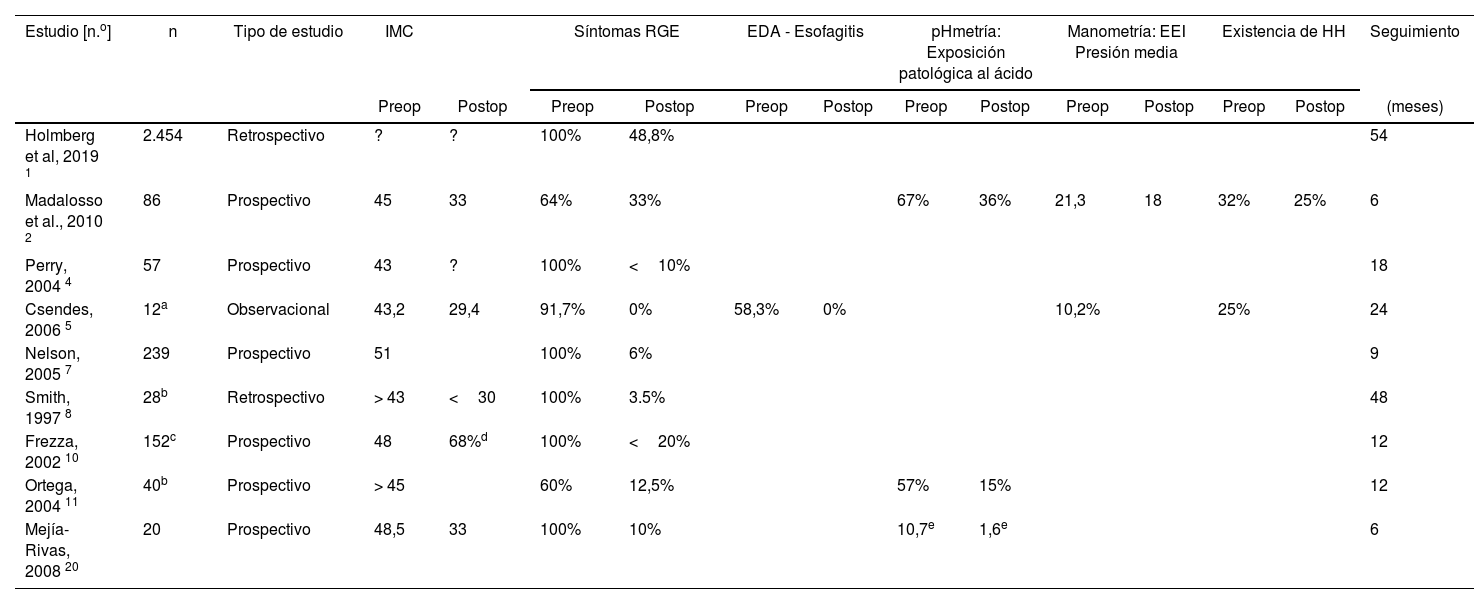
De los restantes 10 estudios, 9 analizan la aplicación del BPG en pacientes obesos con RGE (tabla 2) y el último es un metaanálisis de los resultados de la cirugía antirreflujo en pacientes obesos7. Las 9 publicaciones que analizan la aplicación del BPG coinciden en detectar una desaparición de síntomas en más del 50% de los pacientes (en algunos hasta el 90%) tras la realización del BPG. Aunque el seguimiento es escaso en la mayoría de los estudios, los buenos resultados se mantienen en aquellos que presentan un seguimiento superior a 4años8,9. En cuanto al estudio funcional de estos pacientes, los escasos datos existentes confirman una reducción significativa del porcentaje de pacientes con pHmetría patológica tras la cirugía. Este dato coincide con los observados por el estudio comparativo de Patterson et al.2, donde ambos grupos (FP y BPG), en el postoperatorio, presentan una pHmetría y una manometría con resultados dentro de la normalidad, aunque los datos preoperatorios estaban más alterados en los pacientes sometidos a una FP, dando lugar a unos cambios más significativos que los observados en pacientes sometidos a BPG. Por este motivo, los autores reconocen que no pueden concluir que los dos procedimientos consigan iguales resultados, aunque ambos son efectivos, sobre todo en el control de síntomas.
Pacientes sometidos a bypass gástrico. Resultados de los estudios publicados
| Estudio [n.o] | n | Tipo de estudio | IMC | Síntomas RGE | EDA - Esofagitis | pHmetría: Exposición patológica al ácido | Manometría: EEI Presión media | Existencia de HH | Seguimiento | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Preop | Postop | Preop | Postop | Preop | Postop | Preop | Postop | Preop | Postop | Preop | Postop | (meses) | |||
| Holmberg et al, 2019 1 | 2.454 | Retrospectivo | ? | ? | 100% | 48,8% | 54 | ||||||||
| Madalosso et al., 2010 2 | 86 | Prospectivo | 45 | 33 | 64% | 33% | 67% | 36% | 21,3 | 18 | 32% | 25% | 6 | ||
| Perry, 2004 4 | 57 | Prospectivo | 43 | ? | 100% | <10% | 18 | ||||||||
| Csendes, 2006 5 | 12a | Observacional | 43,2 | 29,4 | 91,7% | 0% | 58,3% | 0% | 10,2% | 25% | 24 | ||||
| Nelson, 2005 7 | 239 | Prospectivo | 51 | 100% | 6% | 9 | |||||||||
| Smith, 1997 8 | 28b | Retrospectivo | > 43 | <30 | 100% | 3.5% | 48 | ||||||||
| Frezza, 2002 10 | 152c | Prospectivo | 48 | 68%d | 100% | <20% | 12 | ||||||||
| Ortega, 2004 11 | 40b | Prospectivo | > 45 | 60% | 12,5% | 57% | 15% | 12 | |||||||
| Mejía-Rivas, 2008 20 | 20 | Prospectivo | 48,5 | 33 | 100% | 10% | 10,7e | 1,6e | 6 | ||||||
EDA: endoscopia digestiva alta; EEI: esfínter esofágico inferior; HH: hernia de hiato; IMC: índice de masa corporal; RGE: reflujo gastroesofágico.
Se considera que la pérdida de peso, que permitirá reducir el gradiente de presión toracoabdominal, es uno de los factores que influyen en la resolución de síntomas de RGE tras la realización de un BPG. Otros factores considerados son la reducción de producción ácida del reservorio o la reducción del posible reflujo biliar a través de un asa alimentaria de suficiente longitud.
Diferentes estudios han demostrado correlación entre la elevación del IMC y el grado de RGE2. Esta correlación también se observa tras cirugía antirreflujo, como lo objetiva el metaanálisis de Abdelrahman et al.7, donde se confirma que tras la realización de una FP existe una mayor recurrencia de los síntomas de RGE en aquellos pacientes con IMC>30 respecto a los que tienen un IMC<30. A este respecto, el IMC>35 preoperatorio fue un factor predictor de recidiva tras la realización de una FP en una serie de 174 pacientes con un seguimiento a 10años10. Algunas series con inclusión de pacientes obesos sometidos a cirugía antirreflujo de revisión por fracaso de la FP previa refieren que la causa más frecuente de recidiva se relacionó con una disrupción de la FP, sugiriendo la obesidad como posible factor causal por la mayor presión intraabdominal ejercida11.
En cambio, tras la realización de un BPG, Nelson et al.12 no observaron que la mejora de la sintomatología de RGE se relacionara con la pérdida de peso, probablemente porque en este caso jueguen un papel suficientemente importante los otros factores mencionados (menor producción de ácido y control del posible reflujo biliar) que permitan obviar en gran parte el efecto de la pérdida de peso.
A la vista de la los datos que aporta la literatura, la FP se mantiene como el tratamiento preferido en pacientes con RGE y un IMC inferior a 30kg/m2. Por otra parte, la persistencia de obesidad favorecerá el fracaso de la cirugía en el caso de la FP. Al mismo tiempo, el BPG se ha mostrado muy efectivo en la remisión del RGE en pacientes con IMC>35kg/m2, con bajos índices de recurrencia. Ello lo consigue, además, sin incrementar la incidencia de complicaciones postoperatorias y añadiendo los beneficios sobre la salud de la pérdida de peso obtenida con este procedimiento4,13. Todo ello lleva a considerar al BPG como el procedimiento de elección en el paciente obeso mórbido con RGE2.
Pero deberemos tener en consideración aspectos técnicos en la realización de este BPG, como el tamaño del reservorio. Si realizamos un reservorio más largo, podremos favorecer que persista una mayor producción de ácido, y ello influiría negativamente en los resultados, ya que la presión del esfínter esofágico inferior (EEI) tras la realización de un BPG no presenta cambios significativos respecto a los valores preoperatorios14, a diferencia de lo que ocurre tras la FP. Madalosso et al.14 objetivaron, a través de la pHmetría, que el reservorio gástrico ácido en el postoperatorio correlacionaba con una mayor exposición del esófago al ácido respecto a los pacientes sin acidez en el reservorio gástrico (47% vs 17%), así como también presentaban más frecuentemente esofagitis (26% vs 0%).
Pocos son los estudios que analizan la resolución del RGE y dan suficiente información sobre la existencia y características de una posible hernia de hiato (HH) asociada. En caso de constatarse la existencia de una HH, esta debe ser tratada mediante hiatoplastia durante la realización del BPG. Este tratamiento simultáneo no se asocia con un incremento de complicaciones, como han publicado recientemente Lewis et al.15.
Otro aspecto a considerar es la actitud a tomar frente al paciente obeso con EB, cuya incidencia se sitúa entre el 1,3 y el 3,8%, más del doble de la prevalencia en la población general16. Además, aproximadamente el 50% de estos pacientes no presentan síntomas. Una revisión sistemática llevada a cabo recientemente17 muestra que el BPG se asocia con una regresión del EB y la displasia en el 36 al 62% de los pacientes con EB confirmado preoperatoriamente.
En 2014, Pagé et al.18 publicaron los resultados de una encuesta realizada a miembros de la Society of American Gastrointestinal and Endoscopic Surgeons (SAGES) con el objetivo de conocer el posicionamiento de los cirujanos en el tratamiento quirúrgico del RGE en el paciente obeso, según el IMC. Mientras que en los pacientes con IMC>30 el 94% realizarían FP, este porcentaje desciende al 57,8% cuando el IMC se sitúa en >35, y con IMC>40 el BPG era la técnica de elección para el 80% de cirujanos. Actualmente, a la vista de los datos publicados, no sorprende que sociedades científicas como el American College of Gastroenterology (ACG) o la SAGES recomienden el BPG como gold standard en la población con RGE e IMC>35; es probable que otras sociedades científicas, en próximas puestas al día de sus guidelines, adopten también este posicionamiento.
Pero todavía no existe un posicionamiento en el caso de pacientes con IMC entre 30 y 35, si bien deberemos tener en consideración que el metaanálisis de Abdelrahman et al.7 refiere el aumento de recurrencia tras FP en pacientes obesos, colocando el punto de corte en un IMC>30.
Nuevas propuestas quirúrgicasAunque el BPG parece ser la cirugía bariátrica más recomendada en pacientes obesos con RGE, en los últimos años se han propuesto nuevos procedimientos que permitan abrir el abanico de posibilidades terapéuticas.
Uno de los procedimientos bariátricos más frecuentemente utilizado es la gastrectomía vertical (GV), y diferentes estudios han evaluado su factibilidad, su seguridad y su reproducibilidad en términos de pérdida de peso y reducción de comorbilidades, comparado con el BPG. A pesar de las ventajas, la GV se asocia con una elevada tasa de RGE postoperatorio, independientemente del diagnóstico preoperatorio19. Es por ello que en los últimos años se ha propuesto la realización de GV asociada a un procedimiento preventivo del RGE. Uno de los mecanismos implicados en la etiología del RGE es la presencia de HH, y diferentes autores han descrito una mayor resolución de la sintomatología si la GV se asocia con la reparación concurrente de la HH (GV +HHR). Soricelli et al.20 realizan un análisis retrospectivo de 97 pacientes a los que se realizó GV +HHR. Cuarenta y uno de estos pacientes presentaban síntomas preoperatorios de RGE, y tras un seguimiento postoperatorio de 18meses, 33 de ellos (80,4%) presentaban remisión de la sintomatología, sin casos con RGE de novo. Estos resultados también son corroborados por Sucandy et al.21 en su serie retrospectiva de 131 pacientes: de los 35 casos con HH y sintomatología preoperatoria de RGE a los que se realizó GV +HHR, 32 casos (91%) presentaron resolución completa de la sintomatología, y mejoría de la misma en los otros 3 pacientes. Pero otros estudios no presentan resultados tan óptimos, con una persistencia de la clínica de RGE en casi el 50% de casos y el desarrollo de RGE de novo en más del 20% de pacientes, tras la realización de GV +HHR22.
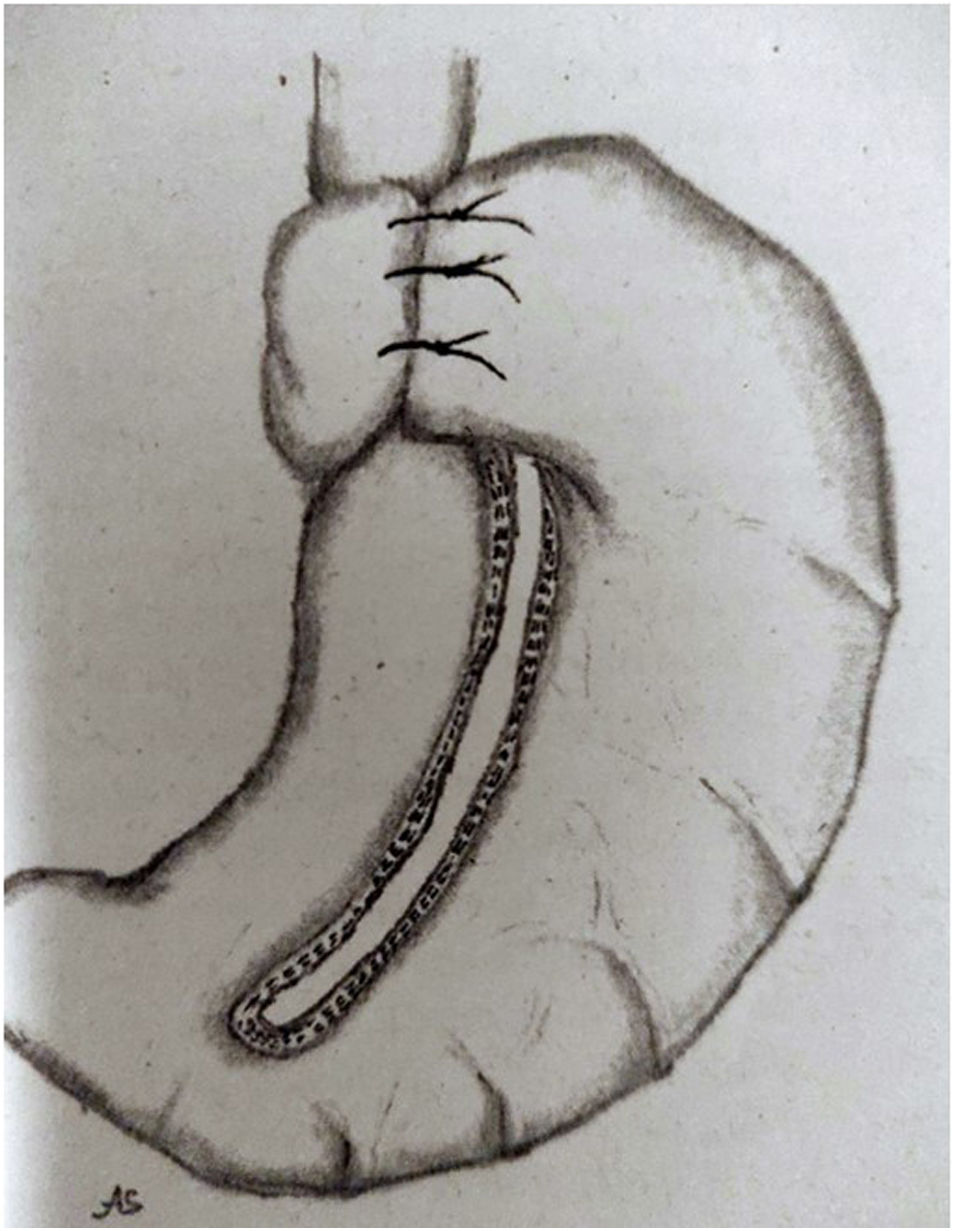
Desde aproximadamente 2015 son varios los grupos que han comenzado a utilizar la combinación de GV con diferentes sistemas antirreflujo, con resultados preliminares prometedores. Una de ellas es la asociación de GV con la operación de Magenstrasse-Mill y una FP Nissen. La operación de Magenstrasse-Mill consiste en realizar una sección longitudinal de la curvatura mayor gástrica desde 5cm proximal al píloro hasta el ángulo de His y sin resección del estómago seccionado, ya que el fundus se utiliza para llevar a cabo una FP de 360° (fig. 2)23. Por su parte, Le Page y Martin24 proponen otro tipo de FP asociada a la GV, consistente en una resección parcial del fundus gástrico para disponer de una parte del mismo que permita realizar una FP anterior de 120° alrededor de la base del esófago. Así mismo, Sanchez-Pernaute et al.25 describen como posibilidad la asociación de la GV con la gastropexia de Hill. Pero se trata de propuestas que refieren buenos resultados en casos aislados, sin ofrecer análisis de resultados en series suficientemente amplias que permitan considerar estas opciones más allá de posibilidades por el momento.
Operación de Magenstrasse-Mill con FP Nissen.
Fuente: Fedenko y Evdoshenko23.
Del procedimiento que más información disponemos en los últimos años es la combinación de GV con FP 360° (Rossetti, Nissen)26,27. Este tipo de procedimiento se basa en la realización inicial de la FP utilizando la menor parte posible del fundus para poder llevar a cabo la mayor resección del mismo durante el siguiente paso, que consiste en la GV. Los datos presentados ofrecen resultados favorables a su utilización, con desaparición de los síntomas de RGE en un elevado porcentaje de pacientes. Uccelli et al.28 presentan los resultados a 5años de una serie de 127 pacientes a los que se realizó una GV asociada a FP de 360° tipo Rossetti (R-GV). Del 74,8% de pacientes con síntomas de RGE preoperatorio sometidos a R-GV, ese porcentaje se redujo al 4,2% tras un seguimiento de 60meses, al tiempo que describen una pérdida de peso y una resolución de comorbilidades comparable a aquellos pacientes sometidos a GV estándar; también objetivaron la resolución de los dos casos con EB previos a la cirugía.
No debemos perder de vista que en todos los casos con HH deberá asociarse la reducción de la misma con cierre de pilares, independientemente del procedimiento antirreflujo que se vaya a aplicar asociado a la GV.
Otros procedimientos propuestos consisten en la aplicación de radiofrecuencia en la unión esofagogástrica por vía endoscópica (Stretta®)29 o la colocación a ese nivel de un anillo de cuentas de titanio con un núcleo magnético que actúe como esfínter (LINX®)30, considerados como opciones terapéuticas para pacientes con síntomas de RGE tras una GV. Pero todavía precisamos más resultados y un seguimiento a más largo plazo para establecerlos como procedimientos ampliamente aceptados.
ConclusionesMientras la FP es el tratamiento preferido en pacientes con RGE y un IMC inferior a 30kg/m2, el BPG es el procedimiento de elección en pacientes con IMC >35kg/m2. Quedan aspectos a considerar, como la estrategia en aquellos pacientes con IMC entre 30 y 35kg/m2 con RGE severo, o que, a pesar de tener indicación para la cirugía bariátrica, no están interesados en dicha opción quirúrgica31.
Se ha objetivado que el BPG se asocia con una regresión del EB y la displasia en el 36 al 62% de los pacientes con EB confirmado preoperatoriamente17.
La mayoría de nuevas propuestas quirúrgicas para el tratamiento de estos pacientes se han basado en asociar un tratamiento antirreflujo a la realización de una GV, con resultados preliminares que parecen reducir el RGE pero no suficientemente concluyentes por el momento.
La existencia de una HH precisa su resolución en el acto operatorio tanto si vamos a realizar un BPG como una GV, sin que se incremente la incidencia de complicaciones.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.