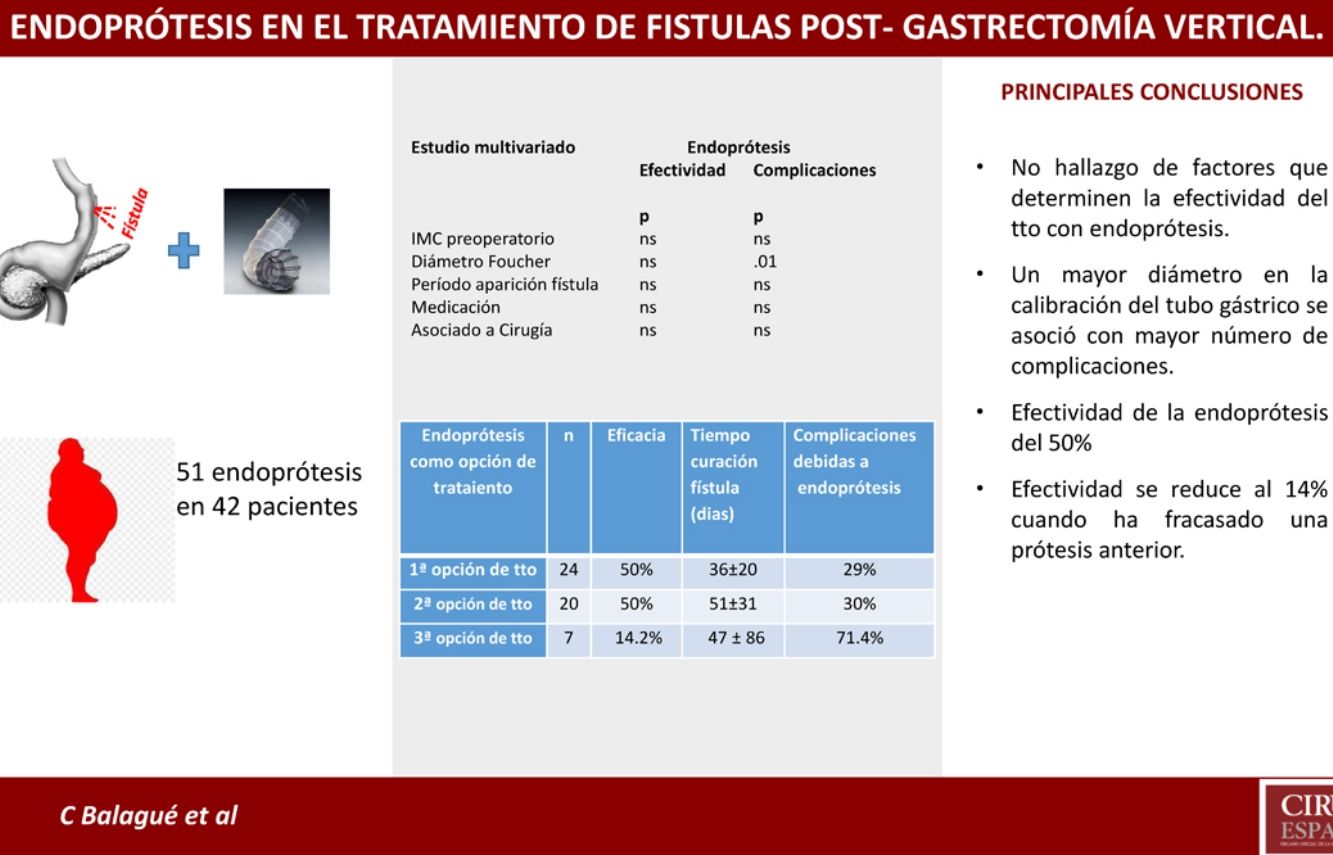
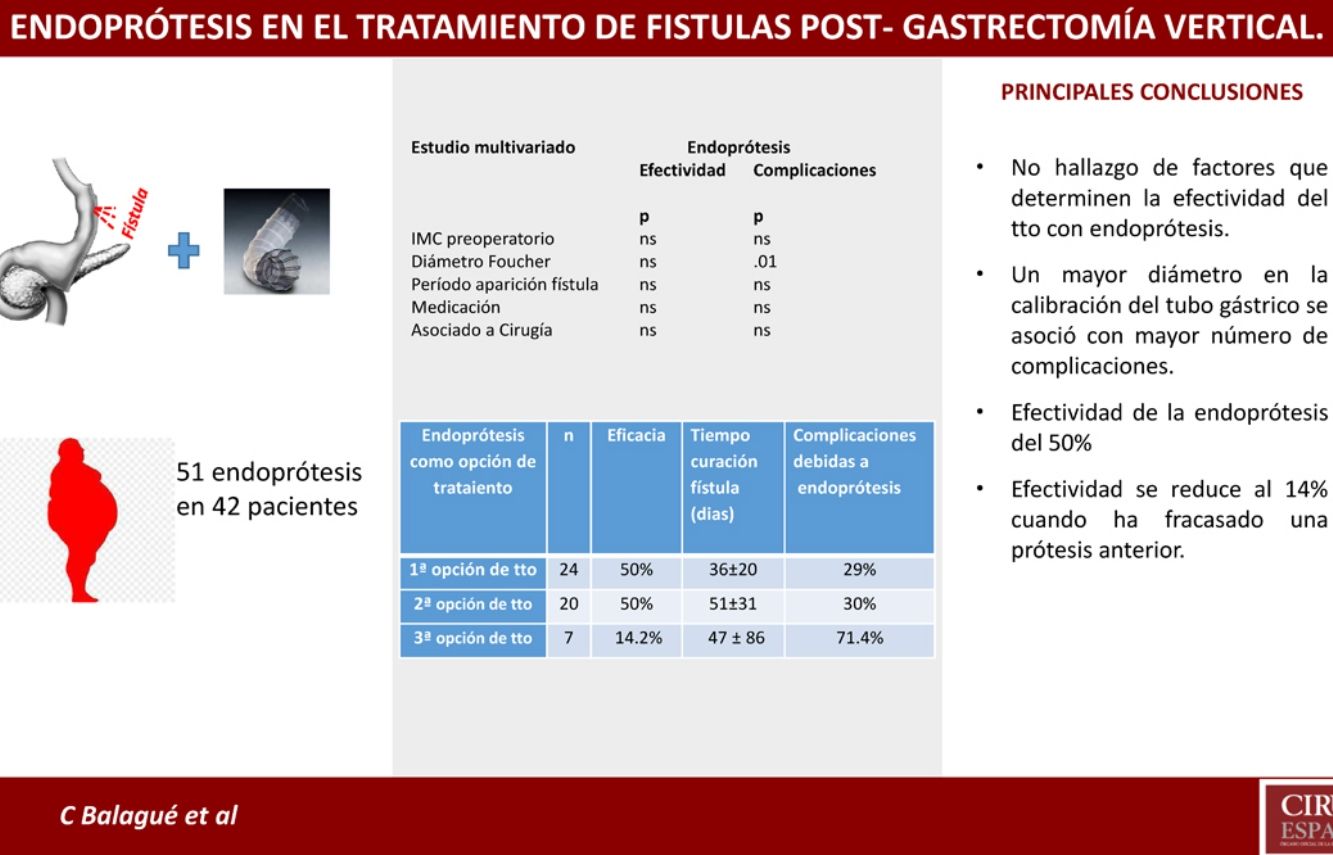
Se ha propuesto la endoprótesis como tratamiento eficaz de la fístula tras gastrectomía vertical, pero existe variabilidad en los resultados publicados. Para evaluar la efectividad de la endoprótesis como tratamiento de la fuga posgastrectomía vertical, La Sociedad Española de Cirugía de la Obesidad (SECO) y la Sección de Obesidad de la Asociación Española de Cirujanos (AEC) propusieron a sus miembros participar en un registro nacional donde incluir a pacientes con fístula posgastrectomía vertical. Analizamos los tratados con endoprótesis. Diecinueve centros han utilizado endoprótesis. Se colocaron 51 endoprótesis en 42 pacientes, 34 M/8 H, edad media: 43,8 años, IMC: 47,6. Efectividad global: 45%, con 35% de complicaciones. El estudio uni- y multivariado no objetivó factores determinantes de la eficacia del tratamiento. Un mayor diámetro del tubo gástrico se relacionó con una mayor incidencia de complicaciones. No hemos encontrado factores implicados en la efectividad de la endoprótesis. Apenas es efectiva una segunda endoprótesis si la primera no lo fue.
It has been suggested that endoprostheses are an effective treatment for fistulae after sleeve gastrectomy, but the results published are very variable. To analyze the effectiveness of stents as treatment of leakage after sleeve gastrectomy, the Spanish Society of Obesity Surgery (SECO) and the Obesity Division of the Spanish Association of Surgeons (AEC) set up a National Registry to record treatments of leaks after sleeve gastrectomy. We have analyzed patients with leaks after sleeve gastrectomy and treated with endoprostheses: 19 medical centers reported the use of endoprostheses, where 51 endoprostheses were used in 42 patients (34 women/8 men, mean age: 43.8 years, BMI: 47.6). Global effectiveness was 45%, with a complication rate of 35%. Uni- and multivariate analyses detected no factors influencing the efficacy of treatment. A larger diameter bouggie used to calibrate the stomach was related to a higher incidence of complications. No factors were found related with better stent efficacy. The effectiveness of a second stent was very low when the previous one had not been effective.
Los excelentes resultados obtenidos por la gastrectomía vertical (GV), no solo a nivel de pérdida de peso, sino también con relación al control de las comorbilidades asociadas, la han posicionado como una de las técnicas bariátricas más populares1–3.
Pero no está exenta de complicaciones, y la fístula a lo largo de la línea de sutura, a pesar de su baja incidencia, es la más temida. Ello se debe a la morbimortalidad que implica4,5 y a la dificultad en conseguir un tratamiento efectivo en muchos casos.
El tratamiento de las fístulas post-GV abarca distintas alternativas, desde la antibioticoterapia hasta la cirugía. En los últimos años los procedimientos endoluminales han demostrado ser una buena opción en el tratamiento de estas complicaciones. Estos procedimientos incluyen la utilización de endoprótesis, materiales sellantes o endoclips. La progresiva experiencia conseguida con estas técnicas permite obtener resultados clínicos cada vez más satisfactorios6–9.
La colocación de endoprótesis es el procedimiento endoluminal más frecuentemente utilizado. Inicialmente su uso se destinó al tratamiento de estenosis intestinales malignas, extendiéndose su aplicación a estenosis benignas y a dehiscencias de suturas. Su objetivo consiste en aislar la fístula del tránsito gastrointestinal mientras se lleva a cabo el proceso de curación de la misma.
En este trabajo analizamos una cohorte de pacientes diagnosticados de fístula post-GV y a los que se colocó una endoprótesis en algún momento del proceso de tratamiento, con el objetivo de evaluar la efectividad de la endoprótesis y las posibles complicaciones asociadas, así como analizar si existen factores que permitan considerar una mayor efectividad de estos dispositivos.
MétodosDesde la Sociedad Española de Cirugía de la Obesidad (SECO) y la Sección de Obesidad de la Asociación Española de Cirujanos (AEC), se propuso a sus miembros la participación en un registro nacional donde se incluyeron retrospectivamente aquellos pacientes diagnosticados de fístula post-GV. La información se recopiló en una base de datos online (www.survio.com/survey/d/registro-fistula-seco) entre enero de 2016 y diciembre de 2017, con preservación de la confidencialidad de los pacientes, cumpliendo con los requisitos de anonimización de los datos, según establece la Agencia Española de Protección de Datos (AEPD).
Un porcentaje importante de pacientes recibieron más de un tratamiento. Es por ello que se recogieron los resultados en función del orden de intentos de tratamientos realizados: primera, segunda o tercera opción de tratamiento.
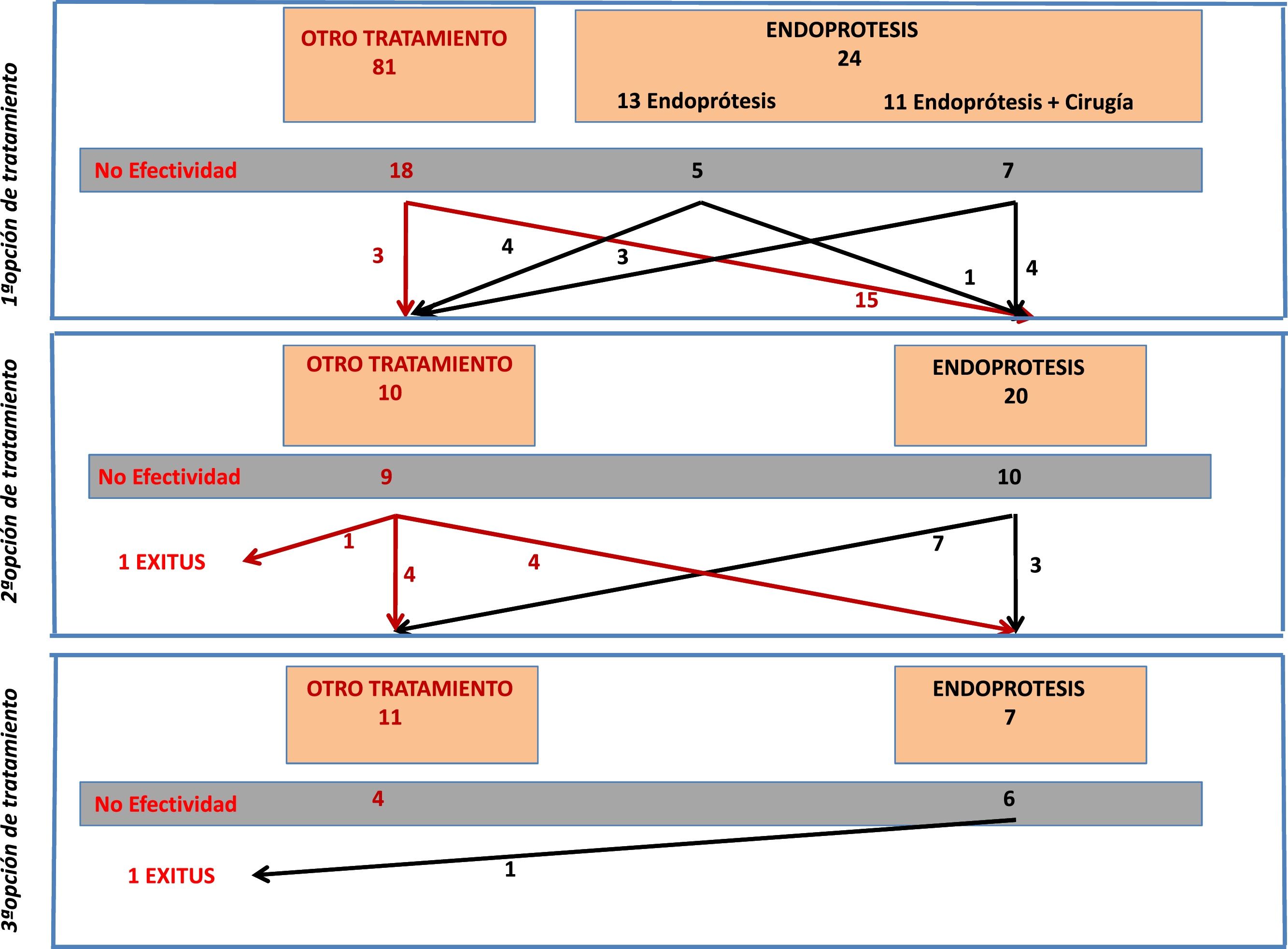
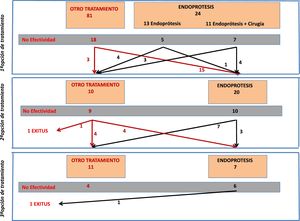
Del global de pacientes incluidos en el registro, en este estudio analizamos aquellos pacientes a los que se colocó una endoprótesis como opción terapéutica en alguno de los intentos de tratamiento. En la figura 1 se indica el flujo de tratamientos que se realizaron en los pacientes incluidos en este estudio.
Se registraron las diferentes variables epidemiológicas así como el tiempo transcurrido hasta el diagnóstico de la fístula, la forma principal de presentación clínica, la sonda Foucher utilizada, la localización de la fístula, el número de tratamientos recibidos, las características de la prótesis, la efectividad del tratamiento así como las complicaciones derivadas de su colocación.
Análisis estadísticoLos datos se expresan como media±desviación estándar. Para la evaluación estadística, se ha utilizado el test Chi-cuadrado o el test de Fisher para las variables cualitativas y ANOVA o test de Mann-Whitney para las variables cuantitativas. Asimismo, en el subgrupo de 24 pacientes sometidos a colocación de endoprótesis como primera opción del tratamiento, se ha utilizado el modelo de regresión de Cox para analizar posibles factores de riesgo de fracaso del tratamiento con endoprótesis, estableciendo como variable dependiente la resolución de la fístula. El mismo modelo y en el mismo grupo de pacientes se ha llevado a cabo para analizar la posible influencia de algún factor sobre la incidencia de complicaciones, tomando este último dato como variable dependiente. Se ha utilizado el paquete estadístico IBM SPSS Statistics 25.0 Inc., Chicago, IL., EE: UU.
ResultadosEn el registro global han participado 27 centros con la inclusión de 105 casos de fístula post-GV. Se colocó un total de 51 endoprótesis en 42 pacientes durante las diferentes opciones de tratamiento. Este grupo es el que analizamos. El número de centros que han referido la utilización de endoprótesis para tratamiento de la fístula post-GV han sido 19.
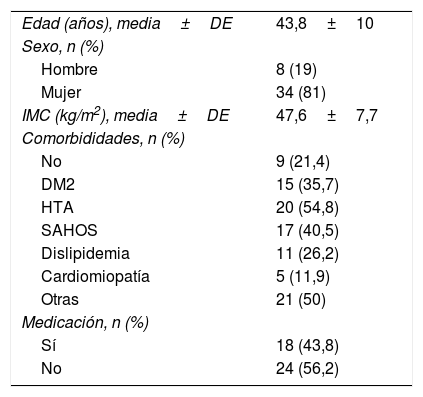
De estos 42 pacientes, 34 eran mujeres (81%) y 8 eran hombres (19%). La edad media fue de 43,8±10 años, con un IMC preoperatorio de 47,6±7,7kg/m2. En la tabla 1 se presentan los datos epidemiológicos de la serie.
Datos epidemiológicos
| Edad (años), media±DE | 43,8±10 |
| Sexo, n (%) | |
| Hombre | 8 (19) |
| Mujer | 34 (81) |
| IMC (kg/m2), media±DE | 47,6±7,7 |
| Comorbididades, n (%) | |
| No | 9 (21,4) |
| DM2 | 15 (35,7) |
| HTA | 20 (54,8) |
| SAHOS | 17 (40,5) |
| Dislipidemia | 11 (26,2) |
| Cardiomiopatía | 5 (11,9) |
| Otras | 21 (50) |
| Medicación, n (%) | |
| Sí | 18 (43,8) |
| No | 24 (56,2) |
DE: desviación estándar; DM2: diabetes mellitus tipo 2; HTA: hipertensión arterial; IMC: índice de masa corporal; SAHOS: síndrome de apnea-hipopnea obstructiva del sueño.
El período de tiempo medio transcurrido entre la realización de la GV y la aparición de la fístula fue de 11±13 días.
En 39 de las 51 endoprótesis colocadas se han referenciado las características de las mismas. Aunque se describen una amplia variabilidad de modelos utilizados, la mayoría de los cirujanos optan por prótesis total o parcialmente cubiertas, con longitudes entre los 10 y 20cm y un diámetro aproximado de 25mm. La composición de la endoprótesis se indica únicamente en 19 casos: 8 dispositivos de silicona, 8 metálicos y 3 de nitinol (níquel-titanio).
Colocación de endoprótesis como primera opción de tratamientoDe la serie global de fístula post-GV (n: 105) se colocó una endoprótesis como primera opción de tratamiento en 24 pacientes (el 23% de la serie). Solo en un paciente no fue posible su colocación, con una efectividad técnica del 96%.
De estos 24 pacientes, la endoprótesis fue tratamiento único en 13 mientras que en 11 casos se asoció cirugía para lavados de la cavidad abdominal y colocación de drenaje. Se consiguió la resolución de la fístula en 12 de los 24 casos (50%), sin diferencia significativa en la efectividad en función de haberse asociado o no a cirugía (36 vs. 61% respectivamente). Se debe tener en consideración que las cirugías asociadas a la colocación de endoprótesis consistieron en lavado y colocación de drenaje y que 9 de los 13 pacientes en los que la endoprótesis no se asoció a cirugía ya eran portadores de drenaje desde la primera intervención o bien se les colocó de forma percutánea.
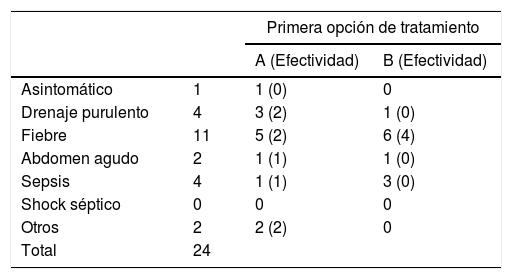
La forma de presentación de la fístula post-GV en 16 de los 24 pacientes fue un síndrome febril o salida de contenido purulento por el drenaje, mientras que los 8 pacientes restantes presentaron cuadro de sepsis o abdomen agudo; pero la forma de presentación no determinó una significativa mayor realización de cirugías asociadas a la colocación de endoprótesis (tabla 2).
Forma principal de presentación en los pacientes tratados con endoprótesis como primera opción de tratamiento
| Primera opción de tratamiento | |||
|---|---|---|---|
| A (Efectividad) | B (Efectividad) | ||
| Asintomático | 1 | 1 (0) | 0 |
| Drenaje purulento | 4 | 3 (2) | 1 (0) |
| Fiebre | 11 | 5 (2) | 6 (4) |
| Abdomen agudo | 2 | 1 (1) | 1 (0) |
| Sepsis | 4 | 1 (1) | 3 (0) |
| Shock séptico | 0 | 0 | 0 |
| Otros | 2 | 2 (2) | 0 |
| Total | 24 | ||
A: endoprótesis; B: endoprótesis+cirugía.
El tiempo medio de curación en los pacientes en los que ha sido efectiva la prótesis como primer tratamiento fue de 36±20 días.
Por otra parte, 7 pacientes (29%) presentaron complicaciones relacionadas con la endoprótesis: un caso de acodamiento de la endoprótesis, 2 desplazamientos (que obligó a su recolocación en un caso y a retirarla en el otro), 2 casos presentaron intolerancia con vómitos, una erosión esofágica y una úlcera gástrica. En 3 de estos casos se resolvió la fístula a pesar de la complicación (el paciente con la erosión esofágica, el caso de la úlcera gástrica y uno de los pacientes que presentaron intolerancia con vómitos).
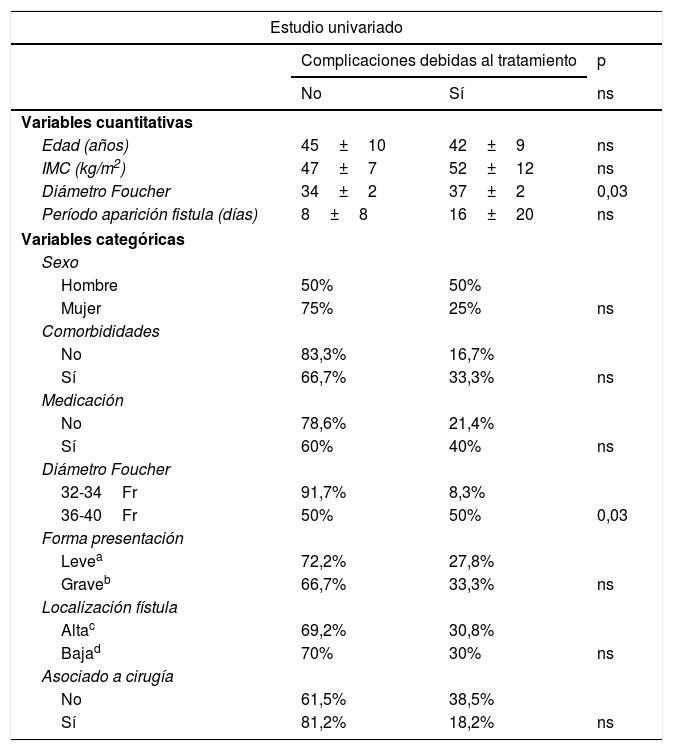
Se realizó estudio uni- y multivariado con el objetivo de analizar si existía algún factor que influyera sobre la aparición de complicaciones y también sobre la efectividad del tratamiento. Este análisis se realizó con el grupo de pacientes sometidos a endoprótesis como primera opción de tratamiento (n: 24) porque una parte de los factores a analizar correspondían a datos del diagnóstico inicial de la fístula, como el período de aparición de la fístula desde la realización de la GV, la forma principal de presentación, o la asociación o no de cirugía a la colocación de la endoprótesis. Este grupo de pacientes no está influido por cambios introducidos por otros tratamientos previos de la fístula y que podían provocar un sesgo. También se analizó la existencia de comorbididades asociadas, ingesta o no de medicaciones, la localización de la fístula como variable cuantitativa y como variable categórica (unión esofagogástrica y tercio superior vs. tercio medio e inferior) y el diámetro de la sonda Foucher utilizada para realización de la GV (como variable cuantitativa y como variable categórica dividiendo por encima y por debajo de 36Fr). Además de las variables mencionadas, también se incluyeron variables demográficas (edad, sexo, IMC preoperatorio). Ninguna de las variables analizadas demostraron influencia significativa sobre la eficacia del tratamiento y únicamente un mayor tamaño de la sonda Foucher mostró un mayor número de complicaciones tras la primera opción de tratamiento (ver análisis univariado y multivariado en tabla 3 para complicaciones y tabla 4 para efectividad del tratamiento).
Estudio univariado y multivariado para complicaciones
| Estudio univariado | |||
|---|---|---|---|
| Complicaciones debidas al tratamiento | p | ||
| No | Sí | ns | |
| Variables cuantitativas | |||
| Edad (años) | 45±10 | 42±9 | ns |
| IMC (kg/m2) | 47±7 | 52±12 | ns |
| Diámetro Foucher | 34±2 | 37±2 | 0,03 |
| Período aparición fistula (días) | 8±8 | 16±20 | ns |
| Variables categóricas | |||
| Sexo | |||
| Hombre | 50% | 50% | |
| Mujer | 75% | 25% | ns |
| Comorbididades | |||
| No | 83,3% | 16,7% | |
| Sí | 66,7% | 33,3% | ns |
| Medicación | |||
| No | 78,6% | 21,4% | |
| Sí | 60% | 40% | ns |
| Diámetro Foucher | |||
| 32-34Fr | 91,7% | 8,3% | |
| 36-40Fr | 50% | 50% | 0,03 |
| Forma presentación | |||
| Levea | 72,2% | 27,8% | |
| Graveb | 66,7% | 33,3% | ns |
| Localización fístula | |||
| Altac | 69,2% | 30,8% | |
| Bajad | 70% | 30% | ns |
| Asociado a cirugía | |||
| No | 61,5% | 38,5% | |
| Sí | 81,2% | 18,2% | ns |
| Estudio multivariado | |
|---|---|
| IMC preoperatorio (kg/m2) | ns |
| Diámetro Foucher | 0,01 |
| Período aparición fistula (días) | ns |
| Medicación | ns |
| Asociado a cirugía | ns |
IMC: índice de masa corporal.
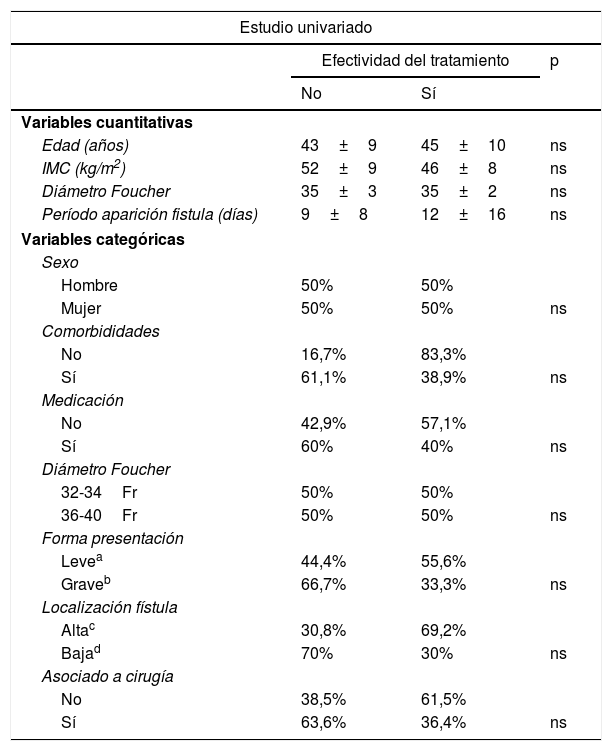
Estudio univariado y multivariado para efectividad del tratamiento
| Estudio univariado | |||
|---|---|---|---|
| Efectividad del tratamiento | p | ||
| No | Sí | ||
| Variables cuantitativas | |||
| Edad (años) | 43±9 | 45±10 | ns |
| IMC (kg/m2) | 52±9 | 46±8 | ns |
| Diámetro Foucher | 35±3 | 35±2 | ns |
| Período aparición fistula (días) | 9±8 | 12±16 | ns |
| Variables categóricas | |||
| Sexo | |||
| Hombre | 50% | 50% | |
| Mujer | 50% | 50% | ns |
| Comorbididades | |||
| No | 16,7% | 83,3% | |
| Sí | 61,1% | 38,9% | ns |
| Medicación | |||
| No | 42,9% | 57,1% | |
| Sí | 60% | 40% | ns |
| Diámetro Foucher | |||
| 32-34Fr | 50% | 50% | |
| 36-40Fr | 50% | 50% | ns |
| Forma presentación | |||
| Levea | 44,4% | 55,6% | |
| Graveb | 66,7% | 33,3% | ns |
| Localización fístula | |||
| Altac | 30,8% | 69,2% | |
| Bajad | 70% | 30% | ns |
| Asociado a cirugía | |||
| No | 38,5% | 61,5% | |
| Sí | 63,6% | 36,4% | ns |
| Estudio multivariado | |
|---|---|
| IMC preoperatorio (kg/m2) | ns |
| Diámetro Foucher | ns |
| Período aparición fistula (días) | ns |
| Medicación | ns |
| Asociado a cirugía | ns |
IMC: índice de masa corporal.
En 20 pacientes se colocó una endoprótesis como segunda opción de tratamiento, es decir, tras el fracaso de un primer tratamiento. La efectividad de la endoprótesis en estos 20 casos fue del 50% (n=10). En 4 casos, el tratamiento que había fracasado anteriormente ya fue la colocación de una endoprótesis. De estos 4 casos, la colocación de otro segundo dispositivo solo fue efectiva en un paciente (25%). En cambio, la efectividad en los otros 16 pacientes a los que se colocó una endoprótesis por primera vez, tras otro tratamiento previo, fue del 56% (9/16).
En los pacientes en los que la colocación de endoprótesis fue efectiva como segunda opción de tratamiento, se precisó una media de 51±31 días desde la colocación de la endoprótesis.
La incidencia de complicaciones relacionadas con la endoprótesis fue del 30% (6 casos) y las causas fueron: 3 casos de migración y un caso de enclavamiento de la endoprótesis que requirieron recolocación de la misma, una estenosis distal por tejido hiperplásico y una úlcera antral que se objetivó a la retirada de la endoprótesis. De estos 6 casos, la endoprótesis no fue efectiva en 2 de ellos (un caso de prótesis desplazada y el paciente con la estenosis distal).
Colocación de endoprótesis como tercera opción de tratamientoSe colocó una endoprótesis como tercera opción de tratamiento únicamente en 7 pacientes. En este pequeño grupo de pacientes la efectividad fue del 14% (solo en un paciente) con una tasa de complicaciones de hasta el 71,4% (5 pacientes): 4 de estos casos se solucionaron con la retirada del dispositivo (2 casos de migración de la endoprótesis, un caso de hemorragia severa y un caso de estenosis distal por hiperplasia del tejido). En el quinto caso hubo un desplazamiento de la endoprótesis pero no precisó recolocación y la fístula se solucionó.
En 3 de los 7 casos a los que se colocó una endoprótesis como tercera opción de tratamiento, se trataba de un segundo dispositivo tras fracaso del primero y en ninguno de ellos resolvió el cuadro.
Si valoramos toda la serie de 42 paciente a los que se colocó una endoprótesis en alguna fase del tratamiento, vemos que en 7 pacientes se colocó una segunda endoprótesis tras fallo de la primera; la efectividad en este grupo de pacientes se sitúa en el 14% (únicamente se resolvió en un caso).
La mortalidad de este grupo de 42 pacientes se situó en el 4,7% (n=2). De estos 2 pacientes que fallecieron, la endoprótesis se colocó como primera opción de tratamiento en un caso y como segunda opción en el otro; en ambos casos, la causa de la muerte se debió a evolución del cuadro séptico que no respondió al tratamiento y en ninguno se relacionó con el dispositivo.
En la tabla 5 se indica los diferentes resultados obtenidos con la colocación de endoprótesis según fuera la primera, segunda o tercera opción de tratamiento.
Resultados de las endoprótesis según el momento de su utilización
| Endoprótesis como opción de tratamiento | n | Eficacia | Consideraciones | Tiempo curación fístula (días) | Complicaciones debidas a endoprótesis |
|---|---|---|---|---|---|
| Primeraa | 24 | 50% | - Tratamiento combinado con cirugía: 13- Tratamiento único: 11 | 36±20 | 29% |
| Segundab | 20 | 50% | 4 casos: segunda endoprótesisb | 51±31 | 30% |
| Tercerac | 7 | 14,2% | 3 casos: segunda endoprótesisc | 47±86 | 71,4% |
Las complicaciones más importantes que se derivan de la GV son el sangrado de la línea de sutura (2%), la estenosis de la del tubo gástrico (1%) y la aparición de fístulas (<2%), siendo esta última la más temida por la morbimortalidad que supone y la complejidad que puede entrañar su tratamiento. Su prevalencia varía según las series, desde el 0,7% hasta un 7%, y la mortalidad puede alcanzar el 35%10.
Una vez esta complicación aparece, su tratamiento puede incluir múltiples opciones terapéuticas11, pero la heterogeneidad de los estudios publicados y la ausencia de estudios aleatorizados dificultan la posibilidad de estandarización de su tratamiento.
Si bien, clásicamente, la cirugía había sido el tratamiento de referencia para las fístulas desarrolladas tras una cirugía bariátrica12, diversos artículos han puesto de manifiesto los buenos resultados obtenidos con tratamientos menos invasivos. Diferentes técnicas endoluminales, como la colocación de endoclips, endoprótesis o sellantes de fibrina, son cada vez más utilizados13–15.
En el momento actual, el empleo de endoprótesis tiene un papel destacado. Las guías de la Sociedad Europea de Endoscopia Gastrointestinal aprueban su utilización temporal en el tratamiento de fístulas y perforaciones esofágicas de causa benigna16. Asimismo, la Sociedad Americana de Cirugía Bariátrica y Metabólica (ASMBS) recomienda la colocación de endoprótesis para este tipo de complicaciones, frente a otras alternativas endoluminales17.
Cabe destacar que, en nuestro medio, la aplicación de endoprótesis en este tipo de complicaciones se está incrementando progresivamente. En el presente registro se consideró la endoprótesis como primera opción de tratamiento en 24 pacientes, lo que representa un 23% de la serie global de 105 pacientes tratados por fístula post-GV. Al final, hasta el 40% (n=42) de los casos fueron tratados con prótesis en algún momento del proceso. Pero no hemos evidenciado ningún factor que orientara a la obtención de mejores resultados con la colocación de endoprótesis como tratamiento inicial de la fístula post-GV.
Por otra parte, la heterogeneidad de datos publicados en la literatura actual con relación al momento de la colocación y extracción de la endoprótesis, así como sus dimensiones o materiales, no permite llegar a definir el modelo óptimo. En nuestra serie, la mayoría apuntan a prótesis cubiertas total o parcialmente, con longitudes superiores a los 10cm y diámetro inferior a los 3cm. Probablemente, las nuevas prótesis disponibles en el mercado, flexibles y anguladas para adaptarse a la morfología del tubo gástrico, de mayor longitud (hasta 240mm) y recubiertas de silicona, permitan una mayor estanqueidad y, en consecuencia, un mejor sellado de las fístulas, aunque por el momento la experiencia es escasa y en la literatura solo disponemos de casos clínicos aislados18.
Sin duda, una de las ventajas que aportan las endoprótesis sobre otro tipo de tratamientos, es que permite mantener incomunicada la fístula del tránsito de saliva y alimentos. El aislamiento que la endoprótesis proporciona permite al paciente beneficiarse de la alimentación oral, con reducción de la estancia hospitalaria e incluso los costes, según algunos autores19, al tiempo que la cobertura de la prótesis permite suponer que existirá un control inmediato de la fuga, contribuyendo a una menor contaminación peritoneal, con reducción de la sepsis. Asimismo, se considera que su colocación permite disminuir la presión endoluminal del tubo gástrico, uno de los posibles factores favorecedores de la aparición de esta complicación20,21, además de proporcionar la posibilidad de tratar una posible estenosis del tubo gástrico, en caso de haberse evidenciado.
Por otra parte, el uso de estos dispositivos no está exento de complicaciones, tal y como se refleja en nuestra serie, donde alcanzó el 35% (18/51). El mayor diámetro de la sonda utilizada para la elaboración del tubo gástrico ha sido el único factor asociado a una mayor incidencia de complicaciones tras la colocación de endoprótesis como primera opción de tratamiento, con significación estadística tanto en el estudio univariado como en el multivariado. Cabría considerar que pueda deberse a una peor adaptación de la endoprótesis al tubo gástrico puesto que en 4 de los 7 casos las complicaciones consistieron en migración, acodamiento o una incorrecta cobertura de la fuga.
La migración de la endoprótesis es una de las mayores limitaciones, pudiendo ocasionar serios problemas y precisar su retirada, incluso por vía laparoscópica. En nuestra serie representó el 44% de las complicaciones (8/18), sin poder establecer su relación con un tipo de endoprótesis u otro. Otros autores han publicado una mayor tasa de migración en las endoprótesis de poliéster (60 vs. 54%)19. De forma global, las prótesis de poliéster presentan mayor riesgo de migración que las metálicas totalmente recubiertas, y estas últimas más que las parcialmente recubiertas22,23. Con la finalidad de prevenir dicho fenómeno, se han ideado diversas estrategias como la fijación con suturas, la superposición de 2 endoprótesis incrementando así la superficie de anclaje de la mucosa, la utilización de endoprótesis de mayor longitud o ajustadas al tamaño y morfología del tubo gástrico. Pero aunque estos mecanismos pueden reducir la incidencia de migración de la endoprótesis, también se han descrito otros efectos adversos como la aparición de úlceras, sangrados o, incluso, perforación duodenal18; todo ello principalmente relacionado con el anclaje del extremo distal de la endoprótesis. Actualmente se dispone en el mercado de prótesis específicamente diseñadas para cirugía bariátrica con los extremos redondeados y de mayor amplitud para facilitar su anclaje al antro o al bulbo duodenal. De esta forma permite reducir el porcentaje de migraciones al tiempo que minimiza los otros posibles efectos adversos18.
La experiencia acumulada de nuestra cohorte es baja, lo que dificulta el desarrollo de conclusiones. Además, existen aspectos a tener en consideración: por una parte no podemos analizar de forma global a los 42 pacientes puesto que no son comparables los resultados obtenidos con la endoprótesis como primera opción de tratamiento con aquellos pacientes que habían recibido algún otro tratamiento antes de optar por la endoprótesis. Ello ha limitado el estudio uni- y multivariado a los 24 pacientes en que la endoprótesis fue el primer tratamiento. Otro aspecto a considerar es que un 21,5% (11/51) de las endoprótesis colocadas forman parte de un tratamiento combinado con cirugía para colocación de drenaje. Este hecho aumenta todavía más la dificultad de análisis de resultados, si bien ha sido uno de los factores analizados.
De los 27 centros que participaron en la inclusión de pacientes con fístula post-GV, han sido 19 los que han referenciado los casos de utilización de endoprótesis como tratamiento, con importante variabilidad no solo en cuanto a los diferentes tipos de dispositivos, sino también en cuanto a los criterios para su utilización. Este hecho supone una limitación para nuestro estudio, dificultando la obtención de conclusiones definitivas. Pero debemos asumir la realidad de cada centro, ya que la decisión de las maniobras a realizar para el tratamiento de esta complicación dependerá principalmente del cirujano, y su grado de familiarización con los diferentes tratamientos endoluminales, así como de la experiencia de los endoscopistas y/o radiólogos de cada centro.
Pero a pesar de las limitaciones del presente estudio, cabe destacar la reducción de efectividad de la endoprótesis tras el fracaso de una endoprótesis previa. En nuestra serie esta efectividad cae al 14% (1/7) cuando una endoprótesis previa ha fracaso, frente a una efectividad del 50% (22/44) cuando se coloca por primera vez.
En conclusión, el desarrollo de fístulas post-GV es una complicación poco frecuente pero suficientemente trascendental para preocupar al cirujano. Aunque la heterogeneidad de los datos publicados dificultan la estandarización del tratamiento, la utilización de endoprótesis como tratamiento de la fístula post-GV es una opción a tener en cuenta en aquellos pacientes con un estado general conservado y si contamos con endoscopistas experimentados. Según nuestros resultados, la decisión de su utilización sería independiente del tiempo transcurrido desde la cirugía. Por otra parte, el diámetro del tubo gástrico será un factor a tener en consideración en el momento de colocar la endoprótesis, así como la decisión de colocar o no un drenaje. Al margen del tipo de endoprótesis utilizada, es importante mantener un control radiológico y endoscópico durante el período en que el dispositivo se mantenga implantado, para minimizar la repercusión de las complicaciones que puedan producirse, como hemorragias o desplazamientos de las mismas.
FinanciaciónEl presente trabajo ha sido financiado por la Fundación de la Sociedad Española de Cirugía de Obesidad (Funseco) (Beca n.o SECO-2018-9).
Conflicto de interesesLos autores declaramos no tener ningún tipo de conflicto de intereses, ni ninguna relación económica, personal, política, interés financiero ni académico que pueda influir en la preparación del manuscrito.