El comienzo insidioso de la diabetes mellitus tipo 2 (DM2) hace que muchas veces los pacientes ya presenten complicaciones al momento del diagnóstico. Actualmente, se insiste en el diagnóstico temprano de la enfermedad para evitar o retrasar la progresión de las complicaciones crónicas, pero no se pone el mismo énfasis en la necesidad de identificarlas una vez confirmada la DM2. El problema de las complicaciones crónicas al momento del diagnóstico de la DM2 merece una especial consideración que se magnifica si se estima que aproximadamente el 30-50% de los pacientes no están diagnosticados.
ObjetivoEl presente estudio fue diseñado con el objetivo de evaluar las complicaciones crónicas y su estadio evolutivo en personas con DM2 de reciente diagnóstico (DMRD).
Pacientes y métodoSe evaluó a 302 pacientes sucesivos con DMRD. Éstos fueron sometidos a examen clínico y de laboratorio, estandarizados para cada complicación, dentro de los 30 días siguientes al diagnóstico.
ResultadosLa media de edad de la muestra fue 53 ± 10 (intervalo, 24- 77) años, sin diferencia entre sexos. Tenían complicaciones crónicas 156 (51,7%) pacientes; 70 (44,9%), sólo una complicación y 86 (55,1%), dos o más. Se halló hipertensión arterial en 192 (63,6%) de los DMRD y el 38,6% tenía enfermedad coronaria (clasificada por el Código de Minnesota). Entre las alteraciones lipídicas, la más frecuente fue las concentraciones bajas de colesterol ligado a lipoproteínas de alta densidad (34,6%). Las complicaciones microvasculares fueron prevalentes tanto en varones como en mujeres y en este orden decreciente: neuropatía (27,5%), nefropatía (20,2%), retinopatía (17,9%); proporcionalmente, la retinopatía fue más severa. El hallazgo de infarto silente de miocardio fue más frecuente de lo esperado (17,7%).
ConclusionesDebe enfatizarse la necesidad de identificar las complicaciones crónicas de la diabetes al hacer el diagnóstico de la enfermedad.
The sly start of type 2 diabetes (DM2) very often complicates the patient before diagnosis. An early diagnosis of diabetes is strongly stressed nowadays so as to avoid or retard the progression of chronic complications. But the same emphasis is not put on the urgency of the diagnosis of these complications, at the same time as diabetes is diagnosed. If we consider that around 50% of type 2 diabetics are not aware of their condition, the problem of chronic complications of varied severity in them needs special consideration.
ObjectiveThe present study was designed in order to evaluate the presence of chronic complications and their evolutive stage in our population.
Patients and methodThree hundred and two newly diagnosed diabetic patients (NDD) underwent full clinical examination and laboratory evaluation within 30 days of diagnosis. Diagnostic procedures and tests were standardized for each complication.
ResultsThe mean age of the sample was 53±10 years (range, 24-77), with no difference between sexes. Complications were present in 156 patients (51.7%); 70 (44.9%) had one complication and 86 (55.1%) had 2 or more. Hypertension (HTA) was present in 192 (63.6%) NDD, 38.6% had coronary heart disease (by Minnesota Code). Among lipid alterations, low high-density lipoprotein cholesterol was the most frequent (34.6%). Microvascular complications were prevalent both in women and men, in decreasing order: neuropathy (27.5%), nephropathy (20.2%), retinopathy (17.9%). Taking into account the severity of complications, retinopathy showed preponderance in evolutive stage. The silent myocardial infraction seems to be a more frequent pathology than expected (17.7%).
ConclusionsIt must be stressed the need for identification of chronic complications immediately after the diagnosis of DM2.
El prolongado período preclínico de la diabetes mellitus tipo 2 (DM2) hace que muchas veces los pacientes lleguen al diagnóstico con complicaciones crónicas de variada gravedad.
Actualmente, se insiste en la necesidad del diagnóstico temprano de la enfermedad para evitar o retrasar la progresión de las complicaciones crónicas (CC), pero no se pone el mismo énfasis en la necesidad de identificarlas una vez confirmada la DM2.
Es necesario concienciar a los médicos de atención primaria, que son los que identifican con mayor frecuencia a las personas con DM, que el inicio de las CC precede en varios años al diagnóstico de la enfermedad1.
Las Clinical Practice Recommendations 2005 de la American Diabetes Association (ADA)2 no mencionan la detección de las complicaciones ni en el capítulo sobre diagnóstico ni en el de cribado. En la sección de evaluación inicial dedica sólo unas pocas palabras al problema: "detectar la presencia o ausencia de complicaciones de la DM2, consensuar un plan de atención y establecer las bases para el cuidado permanente", y aunque en "Componentes de la visita inicial" de su tabla 5 se refiere a síntomas y tratamiento de las complicaciones crónicas en ojos, pies, riñones, etc., no es esta visita inicial necesariamente la del diagnóstico de la DM2. El problema recién se analiza en el capítulo de prevención y manejo de las complicaciones.
Existen muy pocas publicaciones sobre complicaciones crónicas en el paciente diabético de reciente diagnóstico (la mayoría con el criterio de glucemia en ayunas ≥ 140 mg/dl) y se refieren a afecciones específicas aisladas: enfermedad cardiovascular3–5, retinopatía6, neuropatía7,8, etc.
La única excepción ha sido el United Kingdom Prospective Diabetes Study (UKPDS), que dedicó 7 publicaciones a diferentes aspectos de la DM2 de reciente diagnóstico9–15, entre ellos las complicaciones crónicas12.
El problema de las complicaciones crónicas al momento del diagnóstico de la DM2 merece una especial consideración, que se magnifica si se estima que aproximadamente un 30-50% de los pacientes no están diagnosticados a pesar de tener signos clínicos de larga data que no fueron jerarquizados oportunamente.
El presente estudio ha sido diseñado con el objetivo de evaluar las complicaciones crónicas y su grado de gravedad en nuestra población de pacientes con DM2 de reciente diagnóstico (DMRD).
PACIENTES Y MÉTODOSe estudió la presencia de complicaciones crónicas y su estadio evolutivo en 302 pacientes con DM2 al momento del diagnóstico. Los pacientes fueron reclutados en forma sucesiva, a medida que se los diagnosticaba, en los consultorios de médicos clínicos y generalistas de instituciones públicas y privadas de 6 diferentes regiones del país.
Se consideró criterio de exclusión que tuvieran enfermedades endocrinas o sistémicas y cáncer.
Se registró la historia familiar DM, historia clínica personal, forma de presentación y síntomas de DM al diagnóstico: poliuria, polidipsia, polifagia, pérdida de peso y prurito genital, y su tiempo de evolución.
Los pacientes fueron sometidos al correspondiente examen clínico y de laboratorio dentro de los 30 días siguientes al diagnóstico.
Las determinaciones bioquímicas incluyeron: glucemia plasmática en ayunas, hemoglobina glucosidada (HbA1c), colesterol total, ligado a lipoproteínas de alta densidad (cHDL) y ligado a lipoproteínas de baja densidad (cLDL), triglicéridos, uremia, creatininemia, microalbuminuria, proteinuria y aclaramiento de creatinina. Los valores de corte para cada variable se establecieron de acuerdo con los últimos estudios internacionales.
El criterio diagnóstico de DM16 fue la glucemia en ayunas ≥ 126 mg/dl (7,8 mmol/l) o prueba oral de tolerancia a la glucosa (POTG) a las 2 h ≥ 200 mg/dl (11,1 mmol/l). Se consideró dislipemia los valores elevados de colesterol y/o triglicéridos y/o de HDL bajos y/o de LDL elevados, según el Adult Treatment Panel (ATP III)17: colesterol > 200 mg/dl; triglicéridos > 150 mg/dl; cHDL < 40 mg/dl; cLDL > 130 mg/dl, en los pacientes no medicados, o por antecedente en los que se encontraban en medicación hipolipemiante. Urea > 50 mg/dl; creatininemia > 1,3 en mujeres y > 1,4 en varones; microalbuminuria en 30-300 mg/24 h y proteinuria > 500 mg/24 h. La insuficiencia renal crónica (IRC) se definió como aclaramiento de creatinina < 50 ml/min.
Se consideró hipertensos a los pacientes con valores de presión arterial (PA) ≥ 140/90 mmHg según el criterio del JNC-718 o con valores < 140/90 mmHg con medicación antihipertensiva.
Para la HbA1c se consensuó entre los investigadores participantes un valor de corte arbitrario del 7,5% (debido a la falta de uniformidad de los métodos empleados y de información sobre la media de la población no diabética).
Las categorías ponderales19 se clasificaron según el índice de masa corporal (IMC): normal, 18,5-24,9; sobrepeso, 25-26,9, y obesidad, > 27.
Se estandarizaron los procedimientos y exámenes complementarios para el estudio de cada complicación. Retinopatía: diagnosticada por fondo de ojo con dilatación pupilar realizado por oftalmólogo. Neuropatía periférica: evaluación de la sintomatología subjetiva de dolor, parestesia, examen de sensibilidad con monofilamento 10 puntos en cada pie, sensibilidad térmica frío-calor con tubos de agua fría y caliente o lápiz de dos metales, sensibilidad vibratoria con diapasón, alteración del reflejo aquiliano, sensibilidad dolorosa con aguja. Se diagnosticó neuropatía con 2 o más signos positivos. La neuropatía autonómica se investigó por hipotensión ortostática como la diferencia ≥ 30 mmHg entre la PA sistólica en supinación y la PA sistólica en sedestación con una diferencia de 2 min entre ambas tomas. Nefropatía: de acuerdo con los valores de microalbuminuria, proteinuria, creatininemia, uremia y aclaramiento de creatinina.
Se diagnosticó enfermedad vascular periférica por la presencia de 2 o más signos o síntomas positivos: ausencia de pulsos periféricos, alteración de la auscultación arterial periférica, diferencia de PA tobillo/brazo > 0,9 y sintomatología de claudicación intermitente. Los registros electrocardiográficos (ECG) fueron clasificados según el Código de Minnesota20 por el mismo operador.
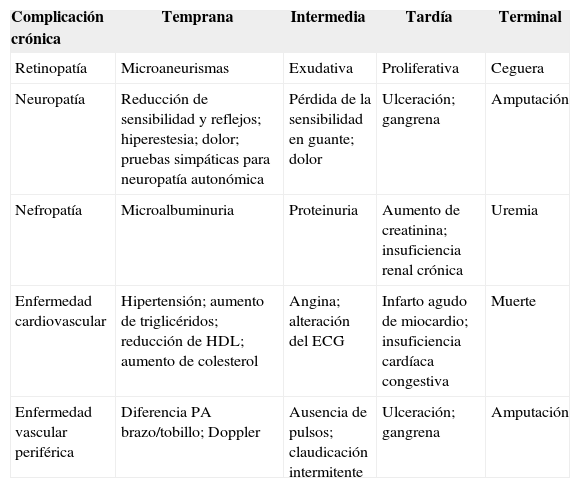
Las complicaciones fueron clasificadas por su estadio evolutivo en tempranas, intermedias, tardías y terminales (tabla 1)21.
Estadio evolutivo de las complicaciones crónicas
| Complicación crónica | Temprana | Intermedia | Tardía | Terminal |
| Retinopatía | Microaneurismas | Exudativa | Proliferativa | Ceguera |
| Neuropatía | Reducción de sensibilidad y reflejos; hiperestesia; dolor; pruebas simpáticas para neuropatía autonómica | Pérdida de la sensibilidad en guante; dolor | Ulceración; gangrena | Amputación |
| Nefropatía | Microalbuminuria | Proteinuria | Aumento de creatinina; insuficiencia renal crónica | Uremia |
| Enfermedad cardiovascular | Hipertensión; aumento de triglicéridos; reducción de HDL; aumento de colesterol | Angina; alteración del ECG | Infarto agudo de miocardio; insuficiencia cardíaca congestiva | Muerte |
| Enfermedad vascular periférica | Diferencia PA brazo/tobillo; Doppler | Ausencia de pulsos; claudicación intermitente | Ulceración; gangrena | Amputación |
ECG: electrocardiograma; HDL: lipoproteínas de alta densidad. PA: presión arterial.
Análisis estadístico: los datos fueron analizados usando los tests de Student, Mantel-Haenszel y Fisher.
Las causas más frecuentes que condujeron al diagnóstico fueron los síntomas de DM referidos (2 o más) en el 53% de los casos y fue un hallazgo accidental en el resto (37,4%). La media de edad de la muestra fue de 53 ± 10 (24-77) años, sin diferencia entre sexos.
El antecedente de DM en familiares de primer grado estuvo presente en 153 (50,7%) pacientes, de los que 143 (47,7%) eran DM2. De las mujeres, 164 (37,2%) registraban el antecedente de hijos nacidos con un peso ≥ 4.000 g.
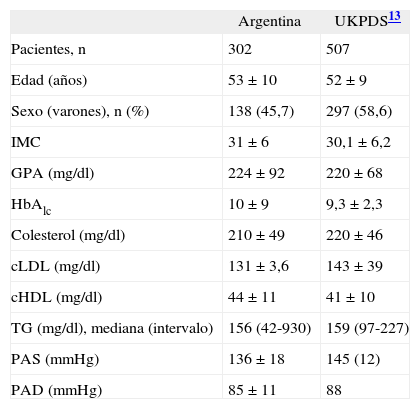
El IMC, las variables bioquímicas y los valores de PA se describen en la tabla 2.
Variables biométricas y bioquímicas en los pacientes con diabetes mellitus tipo 2 al diagnóstico en el estudio argentino y en el UKPDS
| Argentina | UKPDS13 | |
| Pacientes, n | 302 | 507 |
| Edad (años) | 53 ± 10 | 52 ± 9 |
| Sexo (varones), n (%) | 138 (45,7) | 297 (58,6) |
| IMC | 31 ±6 | 30,1 ±6,2 |
| GPA (mg/dl) | 224 ±92 | 220 ± 68 |
| HbAlc | 10 ±9 | 9,3 ±2,3 |
| Colesterol (mg/dl) | 210 ± 49 | 220 ± 46 |
| cLDL (mg/dl) | 131 ±3,6 | 143 ±39 |
| cHDL (mg/dl) | 44 ± 11 | 41 ± 10 |
| TG (mg/dl), mediana (intervalo) | 156 (42-930) | 159 (97-227) |
| PAS (mmHg) | 136 ± 18 | 145 (12) |
| PAD (mmHg) | 85 ± 11 | 88 |
Las variables están expresadas en media ± desviación estándar, salvo excepciones especificadas.
IMC: índice de masa corporal; cHDL: colesterol ligado a lipoproteínas de alta densidad; cLDL: colesterol ligado a lipoproteínas de baja densidad; GPA: glucosa plasmática en ayunas; HbA1c: hemoglobina glucosilada; TG: triglicéridos; PAS: presión arterial sistólica; PAD: presión arterial diastólica; UKPDS: United Kingdom Prospective Diabetes Study.
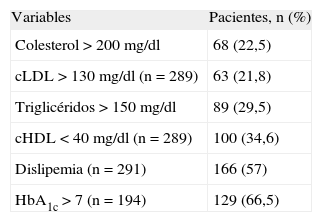
Se debe destacar que el 50% eran obesos. De las alteraciones lipídicas, las bajas concentraciones de cHDL fueron las más frecuentes (34,6%) (tabla 3).
Frecuencia de las alteraciones bioquímicas
| Variables | Pacientes, n (%) |
| Colesterol > 200 mg/dl | 68 (22,5) |
| cLDL > 130 mg/dl (n = 289) | 63 (21,8) |
| Triglicéridos > 150 mg/dl | 89 (29,5) |
| cHDL < 40 mg/dl (n = 289) | 100 (34,6) |
| Dislipemia (n = 291) | 166 (57) |
| HbA1c > 7 (n = 194) | 129 (66,5) |
cHDL: colesterol ligado lipoproteínas de alta densidad; cLDL: colesterol ligado a lipoproteínas de baja densidad; HbA1c: hemoglobina a glucosilada.
La hipertensión arterial estuvo presente en 192 (63,6%) de los DMRD; 47 (24,5%) no sabían que la tenían y 145 (75,5%) habían sido previamente diagnosticados y medicados (excepto 2 de ellos), pero sólo 44 (30,8%) tenían registro de PA < 140/90 mmHg.
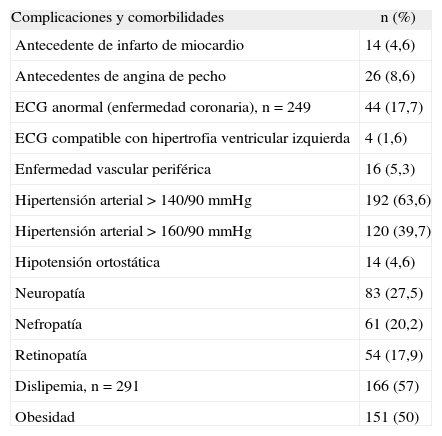
El análisis de los 249 (82,5%) ECG, según el Código de Minnesota, evidenció 79 con alteraciones; de éstos, 44 (17,7%) tenían alteraciones compatibles con enfermedad coronaria (EC): 8 de ellos presentaban antecedente de EC y 9, de angina; en total, 17 (38,6%), lo que nos permite asumir que 27 (61,4%) sufrieron infarto silente de miocardio. La enfermedad vascular periférica fue poco frecuente en nuestra muestra. Hubo complicaciones en 156 (51,7%) pacientes: 70 (44,9%) tuvieron una sola complicación y 86 (55,1%), 2 o más (tabla 4). Las complicaciones microvasculares fueron prevalentes tanto en varones como en mujeres; en orden decreciente: neuropatía, nefropatía y retinopatía.
Complicaciones y comorbilidades en los pacientes con diabetes tipo 2 al diagnóstico
| Complicaciones y comorbilidades | n (%) |
| Antecedente de infarto de miocardio | 14 (4,6) |
| Antecedentes de angina de pecho | 26 (8,6) |
| ECG anormal (enfermedad coronaria), n = 249 | 44 (17,7) |
| ECG compatible con hipertrofia ventricular izquierda | 4 (1,6) |
| Enfermedad vascular periférica | 16 (5,3) |
| Hipertensión arterial > 140/90 mmHg | 192 (63,6) |
| Hipertensión arterial > 160/90 mmHg | 120 (39,7) |
| Hipotensión ortostática | 14 (4,6) |
| Neuropatía | 83 (27,5) |
| Nefropatía | 61 (20,2) |
| Retinopatía | 54 (17,9) |
| Dislipemia, n = 291 | 166 (57) |
| Obesidad | 151 (50) |
ECG: electrocardiograma.
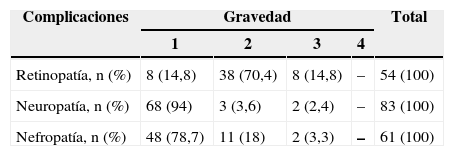
Las complicaciones presentaron diferentes niveles de gravedad de acuerdo con la clasificación descrita en "Pacientes y método" (tabla 5). Neuropatía, nefropatía y enfermedad vascular periférica fueron más frecuentes en el estadio temprano (grado 1). Ninguno de los DMRD presentó complicaciones en el cuarto grado de gravedad (representado por ceguera, amputaciones o estadio terminal de insuficiencia renal).
DISCUSIÓNNuestros resultados confirman la reputación de la DM2 como una enfermedad insidiosa y destructiva. Más de la mitad de los DMRD incluidos en el estudio tenían una o más complicaciones, y la neuropatía y la nefropatía fueron las más frecuentes.
Se hace dificultoso comparar frecuencia y grado de gravedad de las complicaciones en las distintas publicaciones: en primer lugar por los sucesivos cambios en el criterio diagnóstico de DM, de las enfermedades asociadas (hipertensión, obesidad) y de otros trastornos metabólicos (dislipemia); y en segundo lugar, por la falta de uniformidad en la metodología de estudio de las diferentes CC.
Se pudo comparar, por ejemplo, nuestros datos sobre anormalidades en el ECG con los del UKPDS12 porque en ambos estudios se los clasificó por el Código de Minnesota, y se encontró una total coincidencia (el 17,7 frente al 18%, respectivamente) en lo referente a EC.
Si aplicáramos el criterio diagnóstico del UKPDS (> 160/> 90 mmHg), nuestra población presentaría una frecuencia de hipertensión arterial mayor que la del UKPDS (el 46 frente al 29,3%)13, pero con valores promedio menores (136/85 y 145/88 mmHg)14.
Por otro lado, la retinopatía fue diagnosticada por el oftalmólogo, y en el UKPDS se usó la fotografía en color de la retina tomada con cámara de 30°; en consecuencia, los resultados no son comparables. El mismo problema plantearon Lehtinen et al8 en cuanto a prevalencia de la neuropatía en DMRD usando criterios clínicos (5,3%) frente a los electrofisiológicos (15,2%).
Es de destacar la falta de buen control de la PA en nuestra población de DMRD: menos de la mitad de los medicados alcanzaban el objetivo de < 140/90 mmHg.
La obesidad en nuestra muestra (50%) fue mucho mayor que la esperada en la población general (26,9%)22.
Dado que el reclutamiento de los pacientes con DMRD participantes en el estudio se realizó de la misma forma que en el UKPDS23, comparamos las características de ambos grupos, y muestran una curiosa similitud. En nuestro grupo hubo menos varones, fueron levemente más obesos y más hiperglucémicos, pero tenían un mejor perfil lipídico (colesterol total, cLDL y triglicéridos más bajos y cHDL más alto).
Comparando ambos sexos, las mujeres tuvieron menos antecedente de infarto de miocardio y de anormalidades compatibles con EC en el ECG; también presentaron menos retinopatía, enfermedad vascular periférica e hipertensión, pero fueron más obesas y presentaron más nefropatía.
Si se evalúa desde la gravedad de las complicaciones, nuestro estudio mostró que la retinopatía aparecía como la más grave: ¿esto se debe a que es una complicación temprana, a que evoluciona más rápidamente o a que se la estudia más específicamente?
El infarto silente de miocardio se mostró como un proceso más frecuente de lo esperado.
La frecuencia y la severidad de las complicaciones al momento del diagnóstico ponen en evidencia la gravedad del problema.
En conclusión, se debe enfatizar ante la comunidad médica la necesidad de estudiar la presencia de las CC en el paciente con DM2 al momento del diagnóstico. Asimismo sería interesante realizar en el futuro estudios semejantes al presente incluyendo variables que pudiesen modificar la frecuencia y la gravedad de las CC: nivel socioeconómico y educativo, características étnicas y ambientales y acceso a los distintos niveles de atención médica de la población diana.
A los centros participantes: Hospital Vidal, Corrientes (Corrientes): Dra. Silvia Lapertosa; Hospital Fiorito, Avellaneda (Buenos Aires): Dra. Mónica Damiano; Hospital Británico, Ciudad Autónoma de Buenos Aires: Dra. Ángela Conejero; Hospital Piñeiro, Ciudad Autónoma de Buenos Aires: Dra. Marcela Moser; Hospital Privado de la Comunidad, Mar del Plata (Buenos Aires): Dra. Gloria Viñes; Hospital Bouquet Roldán, Neuquén (Neuquén): Dra. María Cristina Luaces; Hospital Central, Mendoza (Mendoza): Dr. José E. Minoprio (†).