Los múltiples intentos durante la canalización periférica pueden producir importantes consecuencias que afectan a pacientes, familiares y profesionales, por ello se planteó la necesidad de conocer la dimensión de este problema en una unidad de cuidados intensivos pediátricos (UCIP).
ObjetivosEl objetivo principal fue describir la canalización de catéter venoso periférico y catéter central de inserción periférica en niños de UCIP. Como objetivos secundarios se propuso determinar la proporción de éxito en el primer intento de canalización, cuantificar los pacientes que presentan vía venosa difícil (VVD), así como explorar la asociación entre la aparición de la VVD y las características sociodemográficas, las relativas a la técnica y a las enfermeras.
MétodoEstudio descriptivo transversal. Mediante muestreo consecutivo se reclutaron pacientes entre 0 y 18 años ingresados en UCIP que precisaron canalización de acceso venoso periférico. Para ello se utilizó un cuestionario ad hoc incluyendo la presencia de VVD como variable independiente.
ResultadosSe recogieron 163 canalizaciones venosas. El 55,8% (91) se realizaron en pacientes menores de 1 año. El 38,7% (63) acertó en el primer intento y el 36,8% (60) presentaron VVD. Cuando aparecía VVD el 85% (51) de los pacientes tuvieron complicaciones, la mediana de tiempo para la canalización mediante catéter venoso periférico corto fue de 30minutos [15-53] y se precisaron 2 o más enfermeras en el 80% (48) de las ocasiones.
ConclusionesSe encontró un bajo porcentaje de acierto al primer intento y una proporción elevada de VVD. Aparecía un mayor número de enfermeras y de tiempo empleado durante la canalización y un aumento de las complicaciones si el paciente presentaba VVD. Se encontró asociación estadísticamente significativa entre VVD y edad, peso, mala perfusión, vena no visible ni palpable, puntuación en la escala DIVA≥4, historia de VVD, complicaciones, número de enfermeras y tiempo empleado.
Multiple attempts during peripheral cannulation can have major consequences for patients, relatives, and healthcare professionals, therefore we set out to determine the extent of this problem in a paediatric intensive care unit (PICU).
ObjectivesThe main aim was to describe peripheral venous catheter (PVC) and peripherally inserted central catheter (PICC) cannulation in children in the PICU. Secondary objectives were to determine the success rate of the first cannulation attempt, to quantify patients with difficult venous access (DVA), and to explore the association between DVA and sociodemographic, technique and nursing-related characteristics.
MethodA cross-sectional descriptive study. Consecutive sampling was used to recruit patients aged 0-18 years admitted to the PICU who required peripheral venous cannulation. An ad hoc questionnaire was used for this purpose, including the presence of DVA as an independent variable.
ResultsA total of 163 venous cannulations were reported. A total of 55.8% (91) were performed in patients under 1 year of age. Of these, 38.7% (63) were successful on the first attempt and 36.8% (60) had DVA. When there was DVA, 85% (51) of patients had complications, median time to cannulation by short CVP was 30minutes [15-53] and 2 or more nurses were required on 80% (48) of occasions.
ConclusionsWe found a low success rate at first attempt and a high proportion of DVA. More nurses and time were employed during cannulation and complications increased if the patient had DVA. A statistically significant association was found between DVA and age, weight, poor perfusion, veins that were neither visible nor palpable, DIVA score≥4, history of difficult intravenous access, complications, number of nurses and time spent.
Se ha descrito por diferentes autores entre un 46% y un 76% de éxito al primer intento en la canalización de accesos periféricos en pacientes pediátricos que pertenecían a servicios de urgencias o de plantas de pediatría. En la literatura se define la vía venosa difícil cuando se producen varios fallos durante la canalización; Gónzalez en 2004 concreta más, estableciendo en 2 los fallos.
El presente estudio propone identificar la vía venosa difícil en los pacientes de una unidad pediátrica de cuidados intensivos basándose en esta definición más concreta, explorando además su asociación con diferentes factores y determinando el éxito en el primer intento. El área en donde se enmarca este estudio ha sido poco investigada, y por lo tanto su aportación es original y relevante.
Implicaciones del estudioEl objetivo en los pacientes pediátricos es conseguir una canalización exitosa en el primer intento para evitar múltiples consecuencias negativas. El punto de partida para disminuir el número de punciones es cuantificar la dimensión del problema de la vía venosa difícil. Esto permitirá evaluar, si es preciso, la implementación de intervenciones que ayuden en este sentido, tales como el empleo de tecnologías facilitadoras, algoritmos de decisión y herramientas predictivas que faciliten la identificación de pacientes con vía venosa difícil.
La canalización de accesos venosos es una de las técnicas más usadas en los centros hospitalarios para la administración de terapia intravenosa y extracción de muestras sanguíneas1,2. Se define el acceso venoso como el procedimiento que comunica una vena con el exterior mediante un catéter3. En las unidades de cuidados intensivos (UCI) todos los pacientes cuentan con algún tipo de catéter venoso debido a la necesidad de tratamiento de efecto inmediato ante situaciones de emergencia o la extracción de muestras sanguíneas frecuentes4.
En pediatría pueden utilizarse distintos tipos de catéteres según las necesidades diagnósticas y terapéuticas del paciente, así como el tiempo de tratamiento y las características de la solución a infundir: catéter venoso periférico (CVP) corto o de longitud media, catéter central de inserción periférica (PICC) y catéter venoso central (CVC). Pueden aparecer complicaciones tanto durante la inserción como durante su uso (dolor, hematoma, punción arterial, lesión de un nervio, extravasación, flebitis, trombosis, infección u obstrucción del catéter). Las complicaciones relacionadas con los catéteres venosos centrales son más graves y ponen en riesgo la vida del paciente, como la embolia aérea, el neumotórax o las arritmias5–7.
Los CVP y los PICC, cuya punción venosa se realiza principalmente en las extremidades, son una competencia técnica de las enfermeras, pero habitualmente la canalización de accesos venosos en niños es más complicada que en adultos debido a las características del paciente pediátrico. Los niños poseen venas de menor calibre, una vasculatura superficial poco desarrollada, en ocasiones anómala, y un grueso tejido subcutáneo, lo que dificulta la palpación y visualización de vasos sanguíneos8. Otro inconveniente añadido es que los niños no suelen cooperar si no están sedados, lo que aumenta la dificultad de canalización de accesos venosos8. También existen diversos factores de riesgo que pueden dificultar el éxito en su inserción como son: edad menor de 3 años, peso menor de 5kg, prematuridad, obesidad, color de la piel, deshidratación o sepsis, vasoconstricción, padecer una enfermedad crónica, necesidad de tratamientos intravenosos previos y experiencia de la enfermera que intenta la inserción8. En 2012 De Negri et al.9 describieron otros factores como la desnutrición, el uso previo de CVC, poseer antecedentes de flebitis o una historia previa de canalización difícil.
Se describe en la literatura que un paciente presenta vía venosa difícil (VVD) cuando una enfermera experimentada tras 2 intentos, usando los métodos convencionales, no logra canalizar un CVP10. Estos métodos convencionales consisten en la aplicación de un torniquete, la colocación en declive del miembro y la visualización y palpación de la vena que se va a puncionar11. Aunque esta definición de VVD no determina cuáles son los criterios para considerar a una enfermera experimentada, el estudio de Larsen et al.12 describía que las enfermeras con más de un año de experiencia laboral presentaban un mayor porcentaje de éxito en la canalización de un CVP. El 8-16% de los pacientes adultos a los que se les intenta canalizar un CVP presentan VVD, aumentando hasta el 37% en la edad pediátrica13. Incluso en condiciones ideales en el 20-30% de los niños se precisa más de un intento, incrementándose hasta en el 50% en menores de un año8. Kuensting et al., en 20098, estimaron una media de 2,2 en el número de intentos necesarios para conseguir canalizar un CVP, un tiempo de media hora para lograrlo y no se consiguió colocar el CVP en el 5% de los pacientes.
Para detectar pacientes que presentan VVD en 2008 Yen et al.14 diseñaron la escala Difficult Intravenous Access Score (DIVA score) para población pediátrica. Esta escala consta de 4 ítems: vena visible y vena palpable tras aplicar un torniquete, edad y antecedentes de prematuridad. Posteriormente se realizó la validación y adaptación de la escala para su aplicación en urgencias pediátricas y pacientes adultos en entornos quirúrgicos15,16.
Estos instrumentos se diseñaron para predecir la probabilidad de fallo de la canalización venosa al primer intento y valorar la necesidad de técnicas facilitadoras no convencionales, como los dispositivos de transiluminación, de luz infrarroja o de ultrasonidos (US)11. Los dispositivos de transiluminación se encargan de iluminar y localizar venas subcutáneas mediante luz fría11. Diversos estudios en los que se utilizaba este dispositivo en la canalización de CVP en niños mostraron una disminución en el riesgo de fallo en menores de 2-3 años y en el tiempo de canalización17–19. La luz infrarroja usada para contrastar los vasos sanguíneos con el resto de la piel también se ha empleado durante la canalización de CVP en pacientes pediátricos, donde únicamente los pacientes con VVD obtuvieron mayor éxito en la canalización al primer intento8,20. El uso del US es el recurso más utilizado en los últimos años, y consiste en un transductor que emite ondas de ultrasonido devolviendo una imagen bidimensional que permite visualizar los vasos, las estructuras cercanas y guiar la punta del catéter16,21. El uso del US para la canalización de PICC también demuestra un menor número de intentos fallidos13, disminuyendo la aparición de complicaciones como hematomas y trombosis22. En pediatría la evidencia sobre la utilización de US para la canalización de CVP es débil, aunque algunos resultados indican que aumenta el porcentaje de éxito y disminuye el tiempo de la técnica, con un menor número de intentos y de redireccionamientos del catéter2,23.
En definitiva, los múltiples intentos de canalización de los accesos venosos periféricos disminuyen la disponibilidad vascular del paciente, aumentan el riesgo de aparición de complicaciones y retrasan el inicio del tratamiento8. Además, en ocasiones, la inserción o retraso en la retirada de CVC es la única alternativa de mantener algún tipo de acceso venoso. Debido a ello las bacteriemias asociadas a CVC son las infecciones nosocomiales más frecuentes en la población pediátrica, lo que conlleva un aumento de la estancia hospitalaria, los costes y la tasa de mortalidad24. La presencia de CVC también es un factor predisponente de tromboembolismo en niños, desarrollando trombosis hasta un 20% de los pacientes con este tipo de catéteres25. Asimismo, los intentos repetidos de canalización provocan preocupación e insatisfacción en sus padres y frustración en las enfermeras, así como dolor y ansiedad en el niño8. Se debe tener en cuenta que los niños pequeños, incluso los recién nacidos, sienten dolor y que estos recuerdos dolorosos pueden tener consecuencias futuras tanto a nivel fisiológico como psicológico, provocando respuestas inadaptadas al dolor en la edad adulta26.
Se planteó como objetivo principal del estudio describir la canalización de CVP y PICC en niños de una UCIP. Como objetivos secundarios se propuso determinar la proporción de éxito en el primer intento de canalización, cuantificar los pacientes que presentan VVD, así como explorar la asociación entre la aparición de la VVD y las características sociodemográficas, las relativas a la técnica y a las enfermeras.
MetodologíaDiseño y población del estudioSe diseñó un estudio descriptivo transversal en el que fueron incluidos desde el 1 de abril hasta el 31 de octubre del 2019 pacientes con una edad entre 0 y 18 años, que permanecieron ingresados en la UCIP de un hospital de tercer nivel con 16 camas y que precisaron CVP corto (angiocatéter) o largo (técnica de Seldinger), así como PICC.
Los criterios de inclusión consistieron en la necesidad de canalización de CVP corto, largo o PICC y en el consentimiento de los tutores legales y/o el menor. Los criterios de exclusión establecidos fueron precisar el acceso venoso durante una situación de urgencia (entendiendo como tal una situación crítica de peligro evidente para la vida del paciente y que requería de una actuación inmediata), así como no rellenar la parte del cuestionario destinada a indicar el número de intentos necesarios para conseguir la canalización venosa.
Proceso de recogida de datosTras una revisión bibliográfica se diseñó un cuestionario ad hoc entre todo el equipo investigador que abordó la presencia de VVD como variable independiente y las siguientes variables dependientes:
- •
Datos sociodemográficos y clínicos: edad, sexo, peso, diagnóstico médico al ingreso e historia de prematuridad.
- •
Datos relacionados con la técnica y canalización: tipo de catéter, zona de acceso, uso de sedación, alteración de la perfusión periférica (presencia de vasoconstricción, hipovolemia o hipoventilación) y en los miembros (presencia de cualquier deformidad, rigidez, edema, falta de integridad cutánea u otras alteraciones físicas visibles que pudieran afectar a la canalización de la vía), historia de VVD, intentos previos de canalización recientes, vena visible y/o palpable tras aplicar el torniquete, puntuación DIVA score, aparición de complicaciones, desestimación de la técnica, técnicas alternativas, tiempo que dura la técnica, canalización exitosa al primer intento y número de punciones totales.
- •
Datos relacionados con las enfermeras: experiencia profesional, experiencia en pediatría y número de enfermeras que intentan la canalización del acceso venoso.
- •
Presencia de vía venosa difícil: según Gónzalez10 se define VVD cuando una enfermera experimentada tras 2 intentos usando los métodos convencionales no logra canalizar un CVP. También se consideró VVD cuando se desestimó la técnica en cualquier momento del procedimiento, a pesar del número de punciones, debido a una falta de disponibilidad de vasos o por una alta probabilidad de fallo percibida por la enfermera.
En dicho documento ad hoc se incluyó la DIVA score14. Este instrumento, tal y como se ha descrito previamente, está compuesto de 4 ítems: venas visibles después de torniquete, venas palpables después de torniquete, edad del paciente e historia de prematuridad. A cada variable se le otorga un valor y cuando la puntuación final es mayor o igual de 4 existe un 50% de posibilidades de fallar en el primer intento. Sus ítems se incluyeron por separado dentro de las características de la técnica para poder valorar su posible relación con la aparición de VVD. Es decir, una vez completados los cuestionarios, se emplearon los ítems para obtener una puntuación de la DIVA score.
Yen et al.14 reportaron que el área bajo la curva de ROC de la DIVA score era de 0,67, el valor aceptable sería de 0,7; sin embargo, refirió no ser tan importante una alta capacidad de discriminación en esta regla de predicción, ya que las consecuencias serían mínimas. Posteriormente, en la validación que realizaron Riker et al.15 mostraron un área bajo la curva de 0,72 (IC 95% [0,67, 0,78]) y en la validación de O’Neill et al.27 se mostró un área bajo la curva de 0,67; la sensibilidad cuando había una puntuación de 4 fue del 75,9%, la especificidad fue del 51,8%, el valor predictivo positivo fue 84,4%, el valor predictivo negativo fue 37,7%, y la razón de probabilidad fue 1,6. Esta escala todavía no ha sido adaptada transculturalmente y validada al español.
Al cuestionario se adjuntó una guía de apoyo para resolver dudas sobre el registro de las variables. Se realizó un pilotaje del contenido del cuestionario en 8 enfermeras de la unidad. Al finalizar la fase de diseño se formó para una adecuada cumplimentación a las enfermeras de la unidad mediante una sesión formativa en la que se les explicó los criterios de inclusión y exclusión, la definición de cada una de las variables, cómo efectuar la recogida del tiempo de canalización, el procedimiento de la firma del consentimiento informado, así como el método de archivado de los cuestionarios cumplimentados.
Los cuestionarios se recogieron de forma consecutiva cuando un paciente precisaba una canalización venosa de acceso periférico, incluyendo todos los intentos que fuesen necesarios hasta la canalización exitosa o la desestimación.
Tras la canalización de la vía la enfermera responsable del paciente se encargó de cumplimentar el cuestionario y archivarlo. Los datos sociodemográficos y clínicos fueron extraídos de la historia del paciente por dichas enfermeras, que también midieron el tiempo de canalización a través de los monitores de cabecera o de sus dispositivos móviles.
Consideraciones éticasEl proyecto fue aprobado por la Comisión de investigación y el Comité de ética del Hospital Universitario 12 de Octubre. En todo momento se respetaron las normas de buena práctica clínica que garantizan el cumplimiento de los principios de la Declaración de Helsinki de investigación con seres humanos (Asociación Médica Mundial, Declaración de Helsinki, 2013). También se garantizó el anonimato de los participantes, así como la confidencialidad de la información según lo dispuesto en la Ley Orgánica 3/2018, del 6 de diciembre de Protección de datos personales y garantía de los derechos digitales.
Los tutores de los menores ingresados fueron informados verbalmente con anterioridad a la realización de la técnica, y posteriormente se les entregó por escrito el consentimiento informado. Cuando los tutores presentaban dificultad para comprender el idioma español se recurrió a un intérprete, principalmente algún familiar que por su adecuado conocimiento del idioma les podía hacer llegar nuestra información correctamente. A los menores entre 12 y 16 años se les hizo también entrega de un consentimiento informado adaptado, tomando su opinión en cuenta en función de su edad y su grado de madurez, así como su situación clínica (Convenio de Oviedo, 1997).
Análisis de datosSe revisaron y depuraron los datos para tratarlos estadísticamente con el paquete de programas SPSS v25 de IBM®. Se describieron las variables cualitativas por medio de frecuencias y porcentajes, y las cuantitativas con media y desviación estándar o mediana y rango intercuartílico, dependiendo de si seguían una distribución normal o no. La prueba de normalidad se realizó mediante el test de Kolmogorov-Smirnov. Para el análisis bivariante entre la variable independiente VVD y las variables dependientes relevantes (características sociodemográficas, las relativas a la técnica y a las enfermeras) se utilizaron los siguientes test estadísticos no paramétricos: Chi cuadrado, U de Mann-Whitney y correlación de Spearman. El análisis estadístico e inferencial se realizó estableciendo un intervalo de confianza del 95% y un nivel de significación estadística de p<0,05.
ResultadosSe recogieron 163 intervenciones de canalización venosa de acceso periférico durante el periodo estudiado, de las cuales 16 fueron PICC. Los datos demográficos por sexo mostraron que el 68,7% de la muestra eran varones (112) y el 55,8% (91) menores de 1 año. El diagnóstico de ingreso, el peso y los antecedentes de prematuridad se encuentran recogidos en la tabla 1.
Características sociodemográficas y clínicas de la muestra
| Variables | N=163 (100%) |
|---|---|
| Edad en añosa | |
| <1 año | 91 (55,8) |
| 1-3 años | 18 (11) |
| >3 años | 54 (33,1) |
| Sexoa | |
| Femenino | 51 (31,3) |
| Masculino | 112 (68,7) |
| Peso en kilogramosb | 6,4 [4-18] |
| Tipo de enfermedada | |
| Polidiagnóstica | 29 (17,8) |
| Cirugía cardiaca | 25 (15,3) |
| Respiratoria | 23 (14,1) |
| Cirugía de vía aérea | 21 (12,9) |
| Cirugía digestiva | 14 (8,6) |
| Neurológica | 13 (8) |
| Cardiovascular | 13 (8) |
| Infecciosa | 7 (4,3) |
| Cirugía traumatológica | 7 (4,3) |
| Metabólica | 5 (3,1) |
| Neurocirugía | 2 (1,2) |
| Cirugía renal | 2 (1,2) |
| No registrado | 2 (1,2) |
| Historia de prematuridada | |
| Sí | 35 (21,5) |
| No | 128 (78,5) |
Respecto a las variables relacionadas con la técnica de canalización venosa, el tipo de dispositivo fundamentalmente utilizado fue un CVP corto en el 89,6% (146) de las canalizaciones. La zona de canalización venosa más frecuente fue en los miembros superiores en el 69,5% (98) de las ocasiones, en los miembros inferiores en el 20,6% (29), en la zona epicraneal en el 6,4% (9) y en el 3,5% (5) en otras localizaciones, como la yugular externa. Se utilizó sedación previa a la técnica en el 39,9% (65) de los pacientes, presentando alteración de la perfusión el 38% (62) o de los miembros en el 21,5% (35). El 83,5% (136) de los pacientes ya había recibido intentos previos de canalización recientemente. Durante la canalización del acceso venoso periférico presentaron alguna vena visible el 73,6% (120) y una vena palpable el 61,3% (100).
El porcentaje de acierto al primer intento fue de 38,7% (63). Cuando este intento inicial fracasaba se intentó la canalización 2 veces en el 27% (44), 3 en el 12,9% (21), el 9,2% (15) precisó 4 intentos y el 12,2% (20) necesitó 5 o más intentos. La mediana de punciones totales fue 2 [1-3]. El 36,8% (60) de la muestra presentó VVD con 2 intentos fallidos o desestimación de la técnica. En el caso de los PICC el 74,3% (12) de las punciones precisó la canalización en más de una ocasión.
La técnica se desestimó en el 13,5% de la totalidad de la muestra (22). Las alternativas que se utilizaron al desestimar la técnica fueron: canalización guiada mediante US en el 18,2% (4), canalización de un CVC en el 9,1% (2) y en el 13,6% (3) se procedió a cambiar la pauta a medicación por vía oral. En el 59,1% (13) de los pacientes en los que se desestimó la canalización venosa periférica se recurrió a otras opciones, como administrar la medicación intravenosa de forma intermitente y no en perfusión continua.
Durante los intentos de canalización de acceso venoso periférico aparecieron diversas complicaciones, como son la rotura del vaso o hematoma en el 46% (75), la extravasación en el 8,6% (14) y la punción de un vaso arterial en el 1,8% (3). Sin embargo, al diferenciar entre los pacientes que presentaban VVD y los que no presentaban VVD, el grupo de VVD tuvo complicaciones en el 85% (51) de las punciones, frente al 28,2% (29) en el grupo de vía venosa no difícil (VVND). Se encontró asociación estadísticamente significativa (p<0,01) entre la presencia de complicaciones y la VVD.
Respecto al tiempo necesario para la canalización de un CVP cuando se fallaba en el primer intento la mediana fue de 16minutos [10-39], mientras que si se acertaba en el primer intento la mediana fue de 5minutos [2-10]. En cambio, para la canalización de un PICC cuando se fallaba en el primer intento la mediana fue de 32,5minutos [12,5-53,75].
La mediana de tiempo para la canalización de un CVP en el grupo de VVD fue de 30minutos [15-53], frente a 5minutos [3-14,5] en el grupo de VVND, existiendo asociación estadísticamente significativa (Z=7,08; p<0,01). Sin embargo, se precisó mayor tiempo para la canalización de un PICC tanto en el grupo de VVD (5) cuya mediana fue de 50minutos [27,5-70], como en el grupo de VVND (11) que fue de 30minutos [10-30].
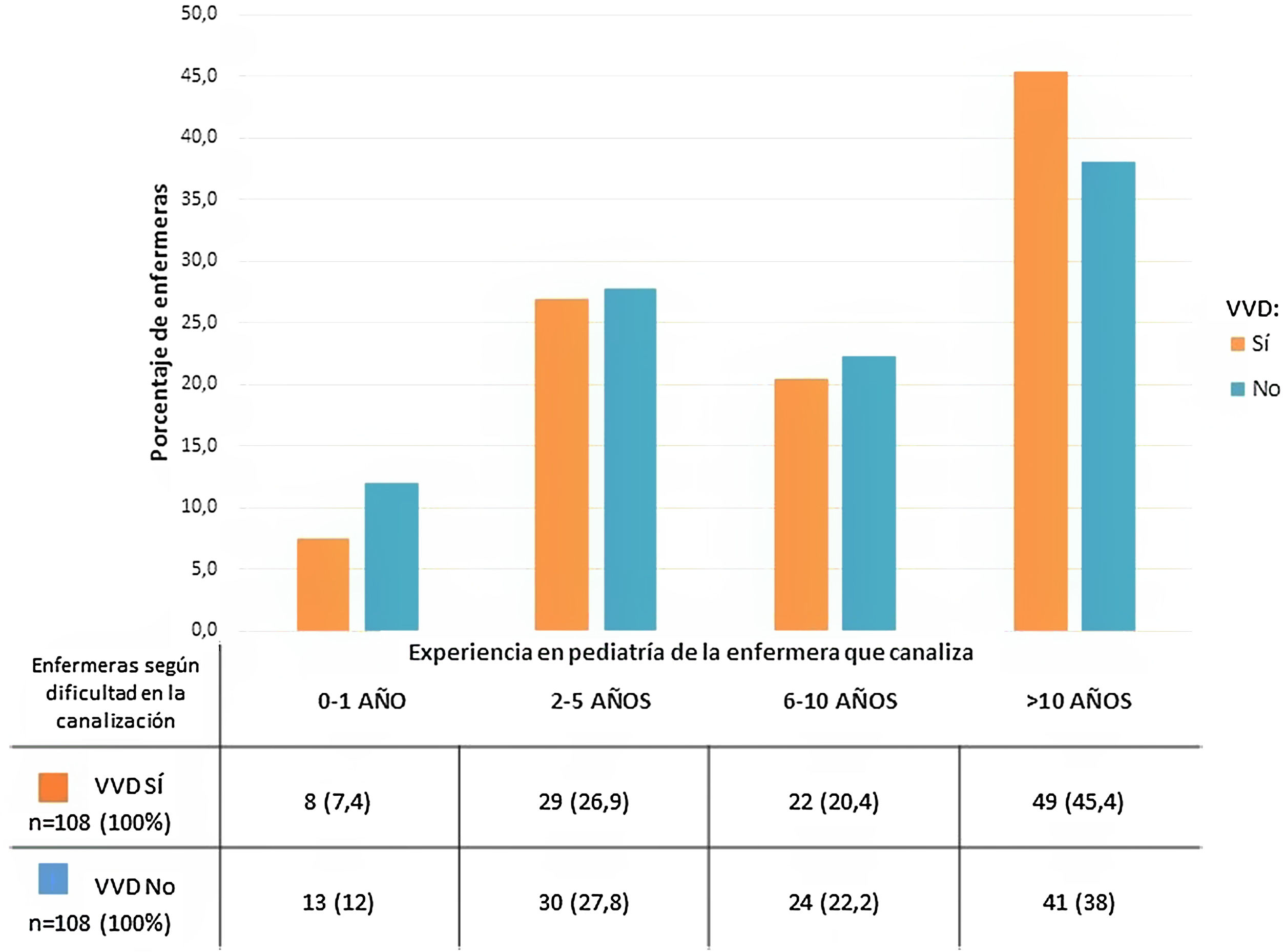
Respecto al número de enfermeras que se precisaron en cada técnica realizó la canalización una única enfermera en el 95% (98) de las veces cuando el paciente presentó VVND y solo el 20% (12) cuando el paciente presentó VVD. Por tanto, la mediana de enfermeras en el grupo de VVD fue de 2 [2-3]. Al comparar la experiencia en pediatría se obtuvo una mediana de 9,5 años [3-13] en el grupo de VVD, similar a los 9 años [4,5-24] del grupo de VVND, no apreciándose diferencias estadísticamente significativas (fig. 1). También se relacionó el número de punciones totales con la experiencia en pediatría, no encontrando asociación estadísticamente significativa (r=0,2; p=0,16).
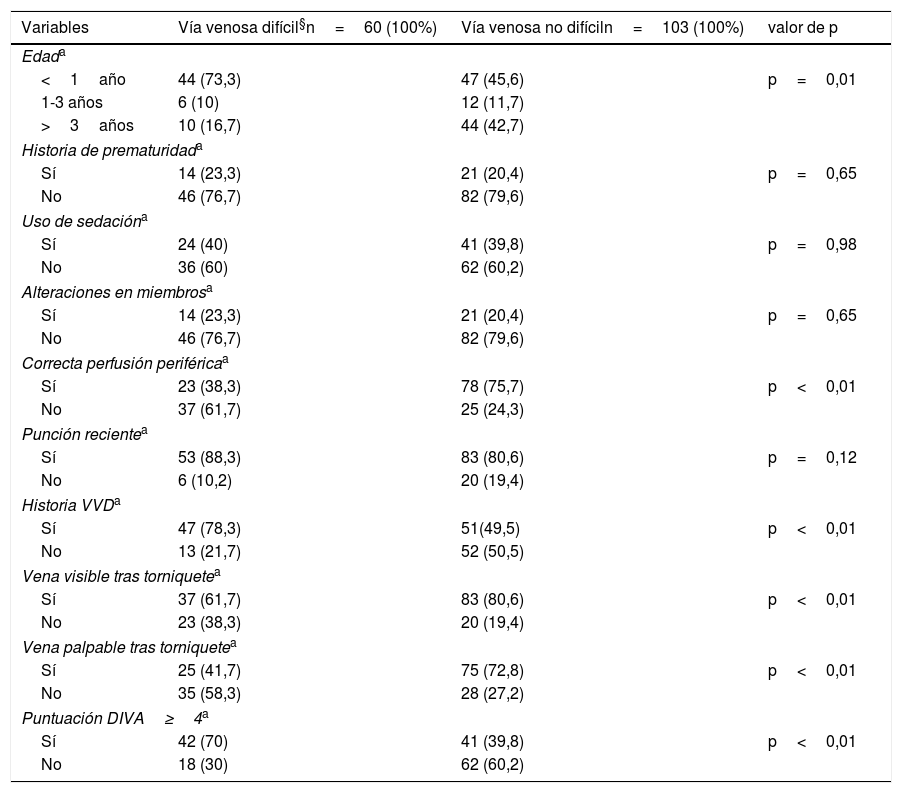
Por último, se halló asociación estadísticamente significativa entre la presencia de VVD y las siguientes variables: edad, correcta perfusión periférica, historia de VVD, vena visible tras torniquete, vena palpable tras torniquetes y puntuación DIVA (tabla 2). También se encontró asociación estadísticamente significativa entre el peso del paciente pediátrico y el número de punciones totales necesarias, precisando menos punciones a mayor peso (r=–0,33; p<0,01).
Asociación bivariante entre vía venosa difícil y variables dependientes
| Variables | Vía venosa difícil§n=60 (100%) | Vía venosa no difíciln=103 (100%) | valor de p |
|---|---|---|---|
| Edada | |||
| <1año | 44 (73,3) | 47 (45,6) | p=0,01 |
| 1-3 años | 6 (10) | 12 (11,7) | |
| >3años | 10 (16,7) | 44 (42,7) | |
| Historia de prematuridada | |||
| Sí | 14 (23,3) | 21 (20,4) | p=0,65 |
| No | 46 (76,7) | 82 (79,6) | |
| Uso de sedacióna | |||
| Sí | 24 (40) | 41 (39,8) | p=0,98 |
| No | 36 (60) | 62 (60,2) | |
| Alteraciones en miembrosa | |||
| Sí | 14 (23,3) | 21 (20,4) | p=0,65 |
| No | 46 (76,7) | 82 (79,6) | |
| Correcta perfusión periféricaa | |||
| Sí | 23 (38,3) | 78 (75,7) | p<0,01 |
| No | 37 (61,7) | 25 (24,3) | |
| Punción recientea | |||
| Sí | 53 (88,3) | 83 (80,6) | p=0,12 |
| No | 6 (10,2) | 20 (19,4) | |
| Historia VVDa | |||
| Sí | 47 (78,3) | 51(49,5) | p<0,01 |
| No | 13 (21,7) | 52 (50,5) | |
| Vena visible tras torniquetea | |||
| Sí | 37 (61,7) | 83 (80,6) | p<0,01 |
| No | 23 (38,3) | 20 (19,4) | |
| Vena palpable tras torniquetea | |||
| Sí | 25 (41,7) | 75 (72,8) | p<0,01 |
| No | 35 (58,3) | 28 (27,2) | |
| Puntuación DIVA≥4a | |||
| Sí | 42 (70) | 41 (39,8) | p<0,01 |
| No | 18 (30) | 62 (60,2) | |
DIVA: Difficult Intravenous Access Score; VVD: vía venosa difícil (cuando una enfermera experimentada, mediante la técnica tradicional, no consigue acceso venoso tras 2 intentos).
Se ha determinado un porcentaje de éxito en el primer intento durante la canalización de acceso venoso periférico muy bajo, de tan solo el 38%, con un promedio de 2 intentos. Este hecho contrasta con las publicaciones previas que muestran porcentajes de éxito al primer intento más favorecedoras, entre un 46-76%. Sin embargo, el promedio de intentos en el total de la muestra y el tiempo estimado es parecido al de los estudios realizados por dichos autores, que reportan entre 1,75 a 2,3 intentos8,14,28–30.
Esta diferencia puede deberse a que la muestra del presente estudio pertenece en su totalidad a una UCIP en la que los pacientes presentan enfermedades de alta complejidad y cronicidad que implican estancias de larga duración y varios reingresos, por lo que su capital venoso suele estar deteriorado. Sin embargo, en los estudios citados la muestra pertenecía a servicios de urgencias o servicios de pediatría general. Rauch et al.17 afirman que en ciertos entornos clínicos con un alto volumen de niños con condiciones médicas frágiles y/o crónicas puede aumentar la frecuencia de VVD. Además, si atendemos a la distribución por edad, casi la mitad de la muestra eran lactantes menores de un año, que debido a sus características anatómicas, el bajo peso y la falta de colaboración aumentan la probabilidad de fallo considerablemente8,9. Lininger et al.28 y Black et al.29 reportan que la proporción de éxito en el primer intento para lactantes podría ser de tan solo el 33%, más aproximado a nuestros resultados.
Al basarnos en la definición de Gónzalez10 encontramos que un 36,8% de la muestra presentó VVD con 2 o más intentos fallidos, o fue imposible la canalización. Esto significa que 4 de cada 10 niños precisaron más de 2 punciones para la canalización de un acceso venoso.
Esta proporción tan elevada de punciones supone numerosos eventos adversos que han sido descritos por diferentes autores y que viven nuestros pacientes cada vez que es necesaria la canalización de un acceso venoso periférico8,17. A esto le sumamos que los ingresos de estos pacientes con enfermedades complejas (polidiagnóstico, cirugía cardiaca y de vía aérea) generalmente son largos, por lo que al presentarse una proporción de punciones tan alta y darse esta misma condición repetidamente se termina produciendo una disminución en la disponibilidad vascular, haciendo imposible la canalización y agravando consecuentemente esta situación31,32. En este estudio también queda patente que la VVD supone un aumento de las complicaciones tal y como reflejan diferentes autores8,17. Los hematomas fueron la complicación más frecuente, lo que coincide con lo referenciado por De Negri et al. en 20129.
Además, el tiempo que se estimó para la canalización de un acceso venoso se incrementa hasta seis veces más cuando existe una VVD. Larsen et al.12 estiman el tiempo requerido para la canalización en los pacientes que precisaron 2 o más punciones de 28,43minutos (SD 28,06), con una mediana de 20minutos, tiempos muy similares a los de este estudio. Esto supone un retraso en los tratamientos8,10,17, y si a esto le sumamos que en un 13,5% de la muestra no se logró CVP, puede que sea necesario buscar diferentes alternativas a esta, tales como el paso de determinada medicación precipitadamente a vía oral o la canalización de CVC para garantizar el acceso venoso en caso de una urgencia, lo que conlleva a un aumento de la probabilidad de bacteriemia.
En la UCIP donde se enmarca el estudio la ratio enfermera-paciente es de 1:2, sin embargo su nivel asistencial es de nivel iii y la complejidad de sus pacientes en su mayoría son nivel iv (según la escala de medición Therapeutic Intervention Scoring System-28 [TISS-28])33,34. Por tanto, la ratio enfermera-paciente debería ser 1:1, e incluso 2:135,36. Esto se traduce en una gran sobrecarga de trabajo, que aumenta considerablemente cuando se presenta una VVD, ya que si tenemos en cuenta los resultados se incrementa en un 75% la necesidad de intervención de 2 o más enfermeras, precisándose hasta 3 y 4 enfermeras en un 26,4% de las ocasiones. Además, el tiempo estimado para canalizar un acceso venoso es de 30 minutos, por lo que los cuidados llevados a cabo por las enfermeras implicadas en la técnica se retrasarán este tiempo, multiplicándose por 2 debido a una ratio enfermera-paciente 1:2.
Según Kalish37 esta situación se define como cuidados enfermeros perdidos (missed nursing care), es decir, «cualquier aspecto de la atención que requiere el paciente y que se omite (en parte o en su totalidad) o se demora». Este concepto está estrechamente ligado con la calidad asistencial y la seguridad del paciente. Por ello, el retraso en la administración de los cuidados, anteriormente citado, como consecuencia de la dificultad en la realización de la técnica afectaría directamente a la calidad asistencial, a la seguridad del paciente, así como a la satisfacción tanto del paciente como de sus familiares y de los profesionales38-41.
Respecto a la asociación de determinados factores con la aparición de VVD, a pesar de que en investigaciones previas se ha descrito una relación causal importante de la historia de prematuridad con el fallo en el primer intento, en este estudio no se ha encontrado relación estadísticamente significativa14. Esto se puede deber a que la muestra era pequeña y esta circunstancia se ha dado en escasas ocasiones.
En cuanto al uso de sedación tampoco se obtuvo relación estadística con la presencia de VVD. Encontramos la explicación en el hecho de que no se recogió el estado de sedación del individuo con escala validada, por lo que a pesar de su uso es posible que el niño no estuviese bien sedado y, por tanto, al no colaborar, dificultase la realización de la técnica, tal y como referencian distintos autores8,30. Larsen et al.12 definieron la colaboración del paciente pediátrico como uno de los factores que más relación mantenía con canalizar el acceso venoso en el primer intento.
Tampoco encontramos relacionada la experiencia de la enfermera con la probabilidad de que se produjeran más de 2 punciones fallidas. La razón la encontramos en que las enfermeras de nuestro servicio tienen una amplia experiencia. Larsen et al.12 señalan que las enfermeras con menos de un año de experiencia son las que tienen más dificultades al realizar la técnica y no obtuvieron una relación significativa con el acierto en el primer intento, al igual que Black et al.29, que tampoco encontraron asociación entre el porcentaje de éxito y los años de experiencia de la enfermera.
En los pacientes que tengan una historia de VVD, que se haya fallado 2 veces en la canalización venosa mediante la técnica tradicional o que muestren predisposición para tener VVD, se deberían aplicar técnicas facilitadoras tales como infrarrojos, transiluminación o US8,17,22,42–44.
Respecto a las investigaciones realizadas sobre esta última técnica, Benkhadra et al.23, en su estudio con población menor de 3 años, evidenciaron un menor tiempo empleado (6 veces más rápido que con la técnica habitual) y mayor éxito en la primera canalización (85% vs. 35%), recomendando su uso en niños pequeños con VVD. Doniger et al.45, con una muestra escasa, obtuvieron como resultados un menor tiempo de canalización (de 14,4 a 6,3minutos), descenso en el número de intentos (de 3 a uno) y menos necesidades de redireccionar el catéter (de 10 a 2). Los resultados de Otani et al.46 avalaban un empeoramiento con el uso de US respecto al tiempo y tasa de éxito. Sin embargo, el reciente estudio de Vinograd et al. en 201947 arroja resultados esperanzadores con una mejoría del 30% frente a los métodos tradicionales.
Por tanto, la técnica de canalización intravenosa guiada por US podría ser una de estas alternativas para el problema encontrado. Sin embargo, en pediatría, aunque la literatura revela una tendencia en la mejoría del éxito al primer intento, e incluso las sociedades científicas emiten recomendaciones en torno al uso de US cuando existe VVD43, no existen resultados del todo concluyentes, por lo que este campo debe ser tratado en futuras líneas de investigación.
Por todo lo descrito es necesaria la disminución de este porcentaje tan alto de VVD. Para ello se deben crear herramientas predictivas, tales como la escala predictiva DIVA14, que nos ayude a evaluar qué pacientes pueden presentar VVD para plantearse previamente los métodos de ayuda anteriormente descritos. Esta escala no está validada en España, sin embargo encontramos relación entre la existencia de VVD y la escala DIVA cuando era mayor o igual a 4, por lo que podría ser útil su adaptación y validación transcultural para poder usarla como herramienta predictiva. Además, es necesario implementar algoritmos de decisión y protocolos en función de la dificultad de acceso venoso, así como guías de práctica clínica de canalización venosa en pediatría que emitan recomendaciones en este sentido.
Hartmant et al.48 refieren en su estudio pre-post que la implementación de algoritmo de decisión de VVD disminuyó los intentos generales para insertar un catéter periférico y la cantidad de personal que intentó la técnica por episodio. Sou et al.49 reportaron que la utilización de US junto con un algoritmo de decisión ha mejorado el tiempo empleado y el éxito en el primer intento: 9 de cada 10 catéteres son implantados en el primer intento.
Schults et al., en 201950, manifestaron que el objetivo en niños es conseguir una canalización periférica exitosa en el primer intento, y para ello se deben combinar el uso de tecnologías por personal entrenado junto con herramientas predictivas que faciliten la identificación de los pacientes con VVD, además de guías de práctica clínica que permitan una estrategia bien definida.
La limitación principal del presente estudio la encontramos en que la muestra fue recogida exclusivamente en la UCI pediátrica de un mismo hospital, por lo que los resultados son transferibles únicamente a una población similar. Por otro lado, no se puede evaluar la dificultad de la técnica en función del uso de sedación, ya que como se ha descrito anteriormente no se recogió el grado de sedación y por tanto no se conoce el nivel de colaboración del paciente. Respecto a la medición del tiempo que se tardaba en lograr la canalización puede ser variable debido a que su medición fue llevada a cabo por diferentes personas, y usando indistintamente los monitores de cabecera del paciente y sus dispositivos móviles personales. Por último, todavía no se ha realizado la adaptación transcultural y validación de DIVA score en nuestro idioma, por ello la variable DIVA fue recogida únicamente con la intención de sondear si guardaba relación con la presencia de VVD según la definición establecida y su posible utilidad futura.
ConclusionesEn el presente estudio se encontró un bajo porcentaje de acierto al primer intento y una proporción elevada de pacientes que disponían de VVD. Si el paciente presentaba VVD se producía un aumento de las complicaciones, se requería un mayor número de enfermeras y de tiempo para realizar la canalización. Además, se encontró asociación estadísticamente significativa entre la aparición de VVD y variables como la edad, el peso, la mala perfusión periférica, la vena no visible ni palpable, la puntuación escala DIVA≥4, la historia de vía venosa difícil, las complicaciones, el número de enfermeras y el tiempo empleado.
Conflicto de interesesLa autora María de la Vieja fue dotada con una beca del programa de intensificación para la actividad investigadora en el área de enfermería del Hospital 12 de Octubre durante el año 2019. Las autoras declaran que no existe ningún conflicto de intereses.
Nuestro más sincero agradecimiento a todo el equipo de enfermería de la UCIP del Hospital Universitario 12 de Octubre, ya que gracias a su colaboración y apoyo ha sido posible llevar a cabo este estudio.