El tratamiento con insulina en personas con diabetes mellitus tipo 2 (DM2) continúa siendo fundamental y su consumo ha aumentado en los últimos años. A pesar de ello, el grado de control para esta patología continúa siendo muy deficiente. El inicio del tratamiento con insulina se realiza con cifras muy por encima de las recomendaciones de las Guías de Práctica Clínica (GPC) y los pacientes están sometidos a cifras de glucemia muy elevadas durante largos periodos de tiempo.
En este artículo se revisa el papel de la insulina siguiendo las diferentes GPC, los criterios para el inicio y la intensificación con dicha terapia, los diferentes tipos de insulina comercializados en nuestro país, la insulinización en situaciones especiales (tratamiento con corticoides, en el anciano frágil, personas en situación de cuidados paliativos, enfermedad renal crónica y personas que cumplen el Ramadán) y finalmente se aborda el problema de la inercia terapéutica en la insulinización.
Insulin treatment in type 2 diabetes mellitus patients is still essential and its usage has increased during recent years. Despite this, the level of control continues to be very poor. Insulin treatment is initiated with control levels above the recommendations set by the Clinical Practice Guidelines (CPG) and patients are exposed to very high blood glucose levels during long periods of time.
This paper reviews the role of insulin in the different CPG, the criteria for therapy initiation and intensification, the beginning of the intensification and the different types of insulin which are commercialized in our country. Moreover, we discuss insulinization in special situations such as corticosteroid treatment, fragile elderly patients, palliative care situations, chronic kidney disease or during Ramadan. Finally, the problem of therapeutic inertia in insulinization is also addressed.
La diabetes mellitus tipo 2 (DM2) es una enfermedad crónica muy prevalente, con riesgo de desarrollar complicaciones micro y macrovasculares cuando el control glucémico es subóptimo. Actualmente disponemos de fármacos para su tratamiento que nos ofrecen seguridad y eficacia al mismo tiempo que pérdida de peso, reducción de riesgo de hipoglucemia y beneficios a nivel cardiovascular. Aun así, por la propia progresión de la enfermedad, muchos pacientes necesitarán tratamiento con insulina para conseguir un control óptimo.
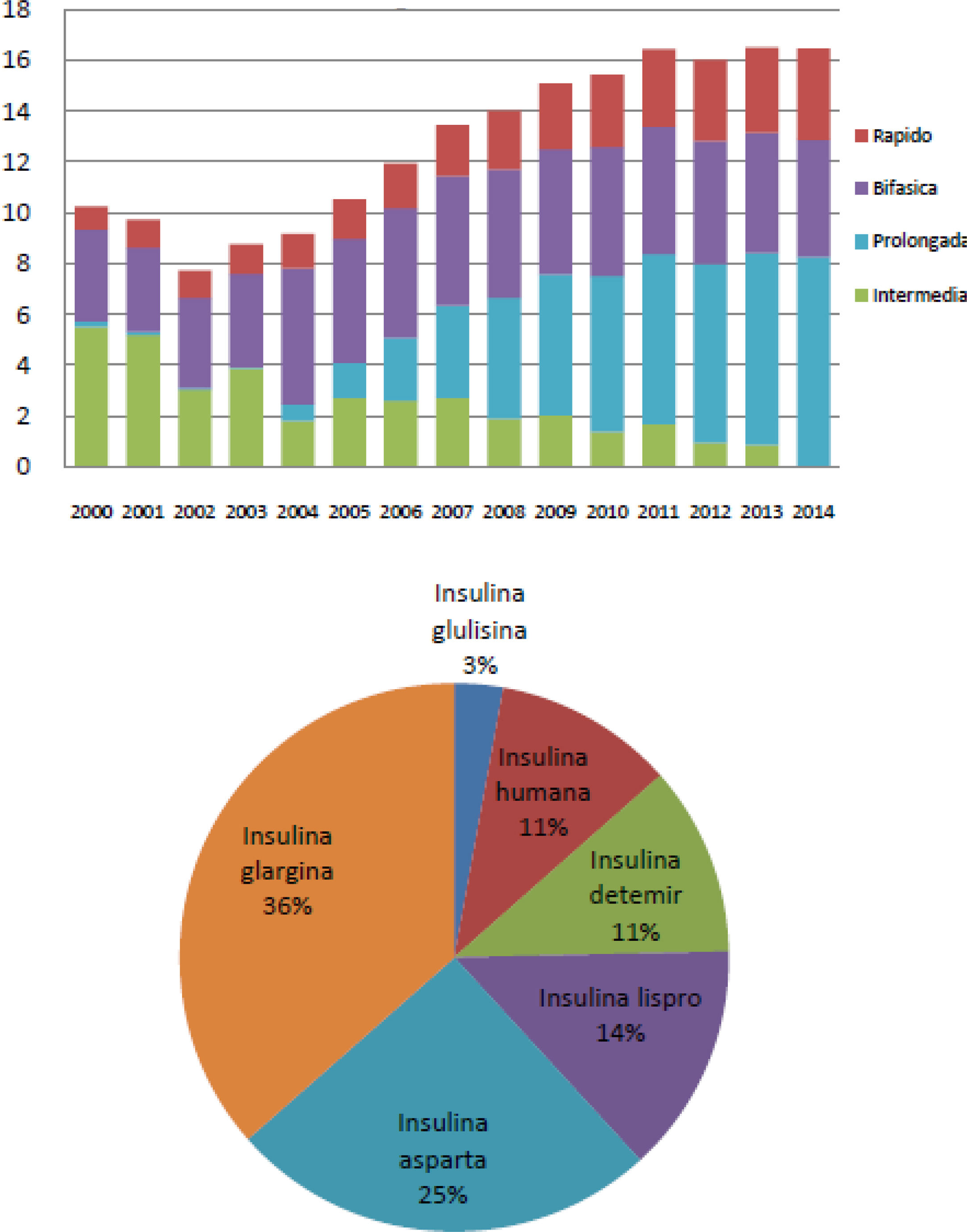
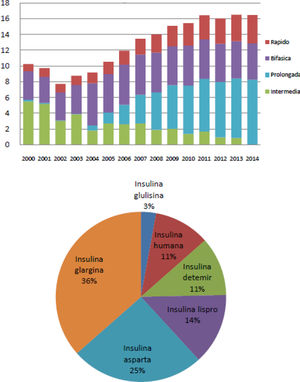
El uso de insulinas en el tratamiento de las personas con DM2 puede diferir ligeramente en los distintos países1. En el Reino Unido la prescripción se mantuvo estable alrededor del 20-24% durante el periodo del 2000 al 2013, observando la misma tendencia entre el periodo 2010-20172. En nuestro país, existen varios estudios donde se aprecia una tendencia similar. Según la base de datos de Cataluña, durante el periodo 2007-2013, se observó un ligero incremento en la utilización de insulina sola o en combinación, pasando del 17,5% en 2007 al 20% en 20133. Este porcentaje fue ligeramente superior en otro estudio realizado en Málaga entre los años 2008-2012, alcanzando cifras del 31% respecto al de otros antidiabéticos no insulínicos y además se observó un cambio de tendencia en el tipo de insulinas prescritas, pasando del empleo mayoritario de insulinas intermedias y mezclas en 2008 (38%) a insulinas prolongadas en 2012 (36%)4. Esta tendencia se observa también en el informe de uso de medicamentos del Ministerio de Sanidad del periodo 2000 a 2014, donde se plasma el cambio a un uso mayoritario de análogos de insulina5 (fig. 1).
Utilización de insulinas en España. A) Evolución de la utilización de insulina por tipo (DHD). B) Patrón de utilización de insulina según el tipo estructural en 20145.
A pesar del aumento de la utilización de insulina, el control de la DM2 sigue siendo subóptimo, consiguiendo un control de HbA1c < 7% en nuestro país, solo el 21,3% de las personas en tratamiento con la misma6.
A pesar de la mayor prescripción de insulinas de acción prolongada, más seguras por presentar menor riesgo de hipoglucemias5, el control de la enfermedad está muy lejos de lo deseado, probablemente porque la insulina sigue siendo el último paso en el tratamiento3.
Indicación del tratamiento con insulina en las Guías de Práctica ClínicaLa insulina es el pilar del tratamiento farmacológico de las personas con diabetes mellitus tipo 1 (DM1) y puede ser necesario en diversas ocasiones en personas con DM2.
Las Guías de Práctica Clínica (GPC) discrepan en cuanto al inicio de la insulinización y su utilización en terapia combinada. Así, la Asociación Americana de Diabetes (ADA)7 propone iniciar la terapia con insulina si la HbA1c es ≥ 10% o glucemia ≥ 300 mg/dL o si el paciente muestra síntomas de hiperglucemia (poliuria o polidipsia) o evidencia de catabolismo (pérdida de peso), pudiendo a medida que se resuelve la toxicidad de la glucosa simplificar el régimen y/o cambiar a agentes orales. También recomienda considerar el tratamiento con insulina en personas con DM2 como parte de cualquier régimen de combinación cuando la hiperglucemia es grave, especialmente si se presentan características catabólicas (pérdida de peso, hipertrigliceridemia, cetosis), o en general, cuando no se logre un control adecuado de la glucemia con tres o más fármacos no insulínicos. La Diabetes Canada Clinical Practice Guidelines8 recomienda insulinizar en el momento del diagnóstico, con o sin metformina si existe descompensación metabólica, siguiendo el mismo criterio a lo largo de la evolución de la diabetes. Ambas GPC en cuanto a la pauta a utilizar, recomiendan insulina basal (IB) como forma de inicio, priorizando si el objetivo es reducir hipoglucemias nocturnas sintomáticas, los análogos de acción prolongada (insulina glargina-100 U/mL, glargina-300 U/mL, detemir, degludec) sobre la insulina NPH. Asimismo aconsejan insulina degludec o insulina glargina-300 sobre glargina-100 para reducir hipoglucemias en general y nocturnas en aquellas personas con alto riesgo de presentarlas.
Por su parte, la American Association of Clinical Endocrinologists (AACE) y el American College of Endocrinology (ACE)9 recomiendan considerar diversos factores en el momento de decidir el comienzo del tratamiento insulínico debiendo tomar la decisión en colaboración con el paciente, dependiendo de su motivación, presencia de complicaciones, edad, bienestar general, riesgo de hipoglucemia, estado general de salud y coste del tratamiento. Serían candidatos a la insulinización los pacientes ya tratados con dos fármacos orales y que presenten una HbA1c > 8% y/o una diabetes de larga duración pues tienen menos probabilidades de alcanzar las cifras objetivo de HbA1c con un tercer antidiabético oral. La adición de un agonista del receptor GLP1 (arGLP1) como tercer agente puede reducir con éxito la hiperglucemia, pero con el tiempo muchos de estas personas necesitarán insulina. Igualmente recomienda insulinoterapia con cifras de HbA1c ≥ 9% junto con síntomas de hiperglucemia.
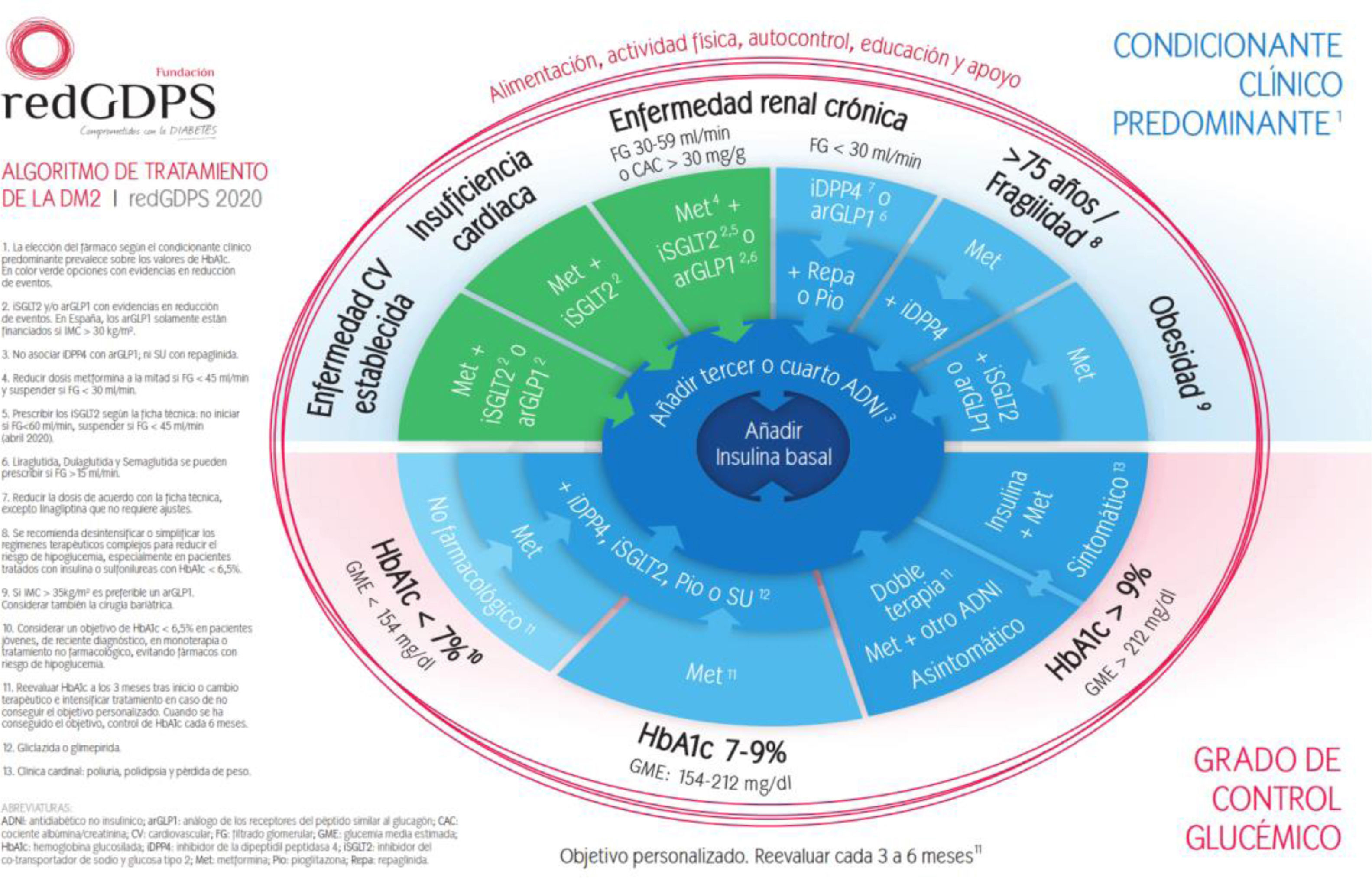
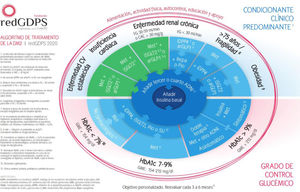
En nuestro país, la redGDPS propone el inicio del tratamiento con insulina en personas con DM2 que no alcanzan el control adecuado con tres o cuatro fármacos no insulínicos o en presencia de HbA1c > 9% y clínica cardinal10 (fig. 2).
Algoritmo de tratamiento de la DM2. redGDPS 202010.
Recientemente algunos autores han manifestado que las GPC deberían recomendar el inicio de tratamiento con insulina con cifras de HbA1c ≥ 9%, ya que los objetivos de control serán difíciles de conseguir con otros fármacos partiendo de HbA1c ≥10%, exponiendo a los pacientes a mayor carga hiperglucémica con aumento del riesgo de complicaciones11.
Criterios de insulinización y pautasLa insulinización precoz es importante para la intensificación del tratamiento, siendo necesario conocer cuáles son los criterios para iniciar esta terapia. Las recomendaciones varían dependiendo de las diferentes GPC7–10 y del momento de evolución de la diabetes.
Al diagnóstico de la enfermedad estaría indicado el tratamiento con insulina, si se observa pérdida de peso (síntomas de cetosis), síntomas de hiperglicemia (poliuria, polidipsia) o aparece cetonuria intensa, o con HbA1c mayores de 9-10%. Una vez resuelta la clínica, se pueden valorar tratamientos antidiabéticos no insulínicos o la simplificación del tratamiento.
Durante la evolución de la enfermedad, se puede precisar tratamiento con insulina en diferentes momentos, bien de forma transitoria o de forma definitiva12 (tabla 1).
Criterios de insulinización12
| Insulinización transitoria |
| Descompensaciones hiperglucémicas agudasDurante un ingreso: si el paciente anteriormente estaba en tratamiento con antidiabéticos oralesSi se precisa tratamiento con glucocorticoidesEn situaciones especiales:enfermedades febriles, traumatismos graves, embarazo y lactancia |
| Insulinización permanente |
| Control glucémico deficiente en pacientes tratados con otros antidiabéticos a dosis plenasCetonuria y pérdida espontánea de pesoEnfermedades crónicas que contraindiquen otros antidiabéticos: insuficiencia renal, hepática o pancreática |
Existen diferentes pautas de insulinización. El inicio del tratamiento se realizará con IB (NPH o análogos), valorando los riesgos de hipoglucemia y los costes. La dosis de inicio será de 0,1-0,2 UI/kg/día, realizando posteriormente una titulación individualizada hasta alcanzar la dosis necesaria.
Si la IB se ha titulado hasta alcanzar una glucemia basal aceptable o si la dosis es de 0,5 UI/kg/día y la HbA1c permanece por encima del objetivo, se considerará avanzar a la terapia inyectable combinada mediante el uso de un arGLP-1 agregado a la IB. Esta opción es recomendada por la mayor parte de las GPC, ya que consigue una reducción de la HbA1c y de la glucemia postprandial igual o ligeramente más eficaz que añadir bolos de insulina prandial, todo ello con una mejor evolución ponderal, menores tasas de hipoglucemia y reducción de las dosis de insulina. Esta pauta con arGLP1 añadida a insulina basal sería de elección en personas con DM tipo 2 y limitaciones para pautas con más dosis de insulina, tales como:
- •
Obesos en los que pautas con más dosis de insulina podrían incrementar el peso (índice de masa corporal > 35 kg/m2).
- •
Personas que han sufrido un evento macrovascular.
- •
Personas con antecedentes de hipoglucemias o alto riesgo de sufrirlas.
- •
Personas que no quieren o no pueden utilizar múltiples dosis de insulina.
Recientemente se han aprobado por las agencias reguladoras dos productos combinados a dosis fijas que mejorará la administración de esta terapia, ya que contienen insulina basal más un arGLP1: insulina glargina-100 más lixisenatida e insulina degludec más liraglutida, si bien aún no están comercializadas en nuestro país.
Otra opción en pacientes no controlados con IB, es añadir insulina prandial antes de la comida más copiosa a dosis de 4 unidades o 10% de la cantidad de IB. La insulina prandial se intensificará según las necesidades del paciente tanto añadiendo insulina antes de las otras ingestas como aumentando las unidades a administrar en cada una de ellas7.
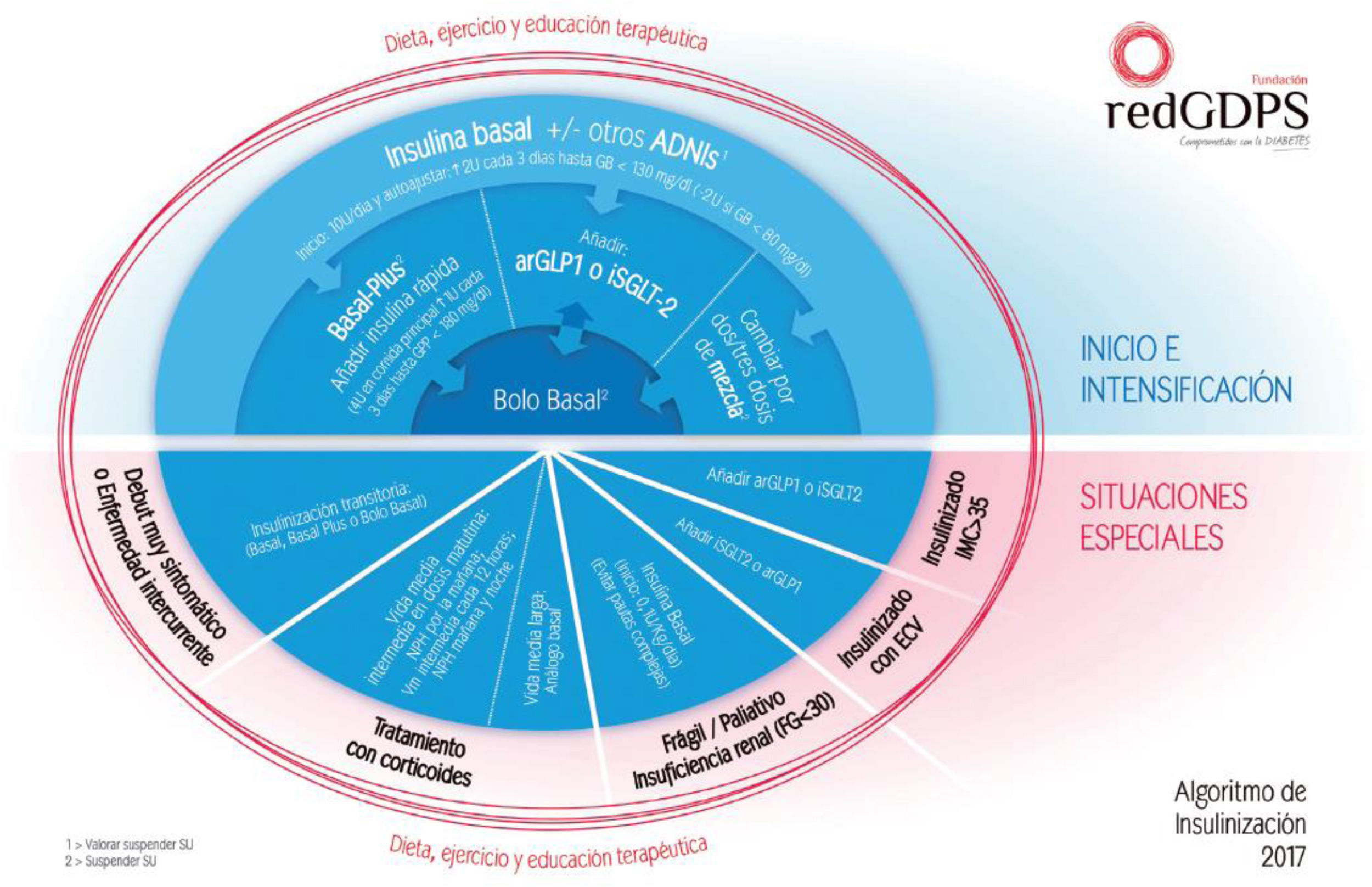
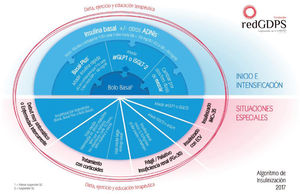
En 2017 se publicó el Consenso para la insulinización en DM2 de la redGDPS, incluyendo un algoritmo explicativo para el manejo de la insulinización basal, la intensificación y el manejo en situaciones especiales13 (fig. 3).
Algoritmo de insulinización13.
Existen diferentes tipos de insulinas que podríamos dividir en tres categorías atendiendo a su acción, inicio y duración. Las insulinas basales son insulinas estables que cubren los requerimientos continuos de insulina que los pacientes necesitan entre las comidas. Tienen una duración de entre 12 y 42 horas. En los últimos años se han comercializado nuevas insulinas basales (glargina-300 y degludec) que ofrecen un perfil mejorado, mayor cobertura y mayor seguridad respecto a las clásicas (NPH, detemir y glargina-100). Por otro lado, las insulinas prandiales son insulinas de acción corta, que constituyen un complemento de las basales a la hora de buscar un patrón fisiológico en respuesta a la ingesta de hidratos de carbono. Tienen un inicio de acción rápido o ultrarrápido y su duración oscila entre tres y seis horas. Por último, las insulinas mezcladas son aquellas que aportan una combinación fija de IB y prandial, todas ellas en concentración de 100 UI/mL13.
En los últimos años se han comercializado dos insulinas biosimilares de glargina-100. Una insulina biosimilar es un fármaco biológico similar a una insulina existente pero que no puede ser considerada una copia exacta de la insulina de marca original debido a los diferentes procesos de fabricación. Estas insulinas podrían contribuir a la sostenibilidad del sistema sanitario, debido a que de entrada se comercializaron a menor precio, si bien en la actualidad el coste es idéntico a la insulina de referencia. Biosimilitud no implica intercambiabilidad y una insulina no puede sustituirse por otra insulina biosimilar sin el permiso del médico prescriptor ya que se encuentran dentro de la lista de medicamentos no sustituibles por el farmacéutico14.
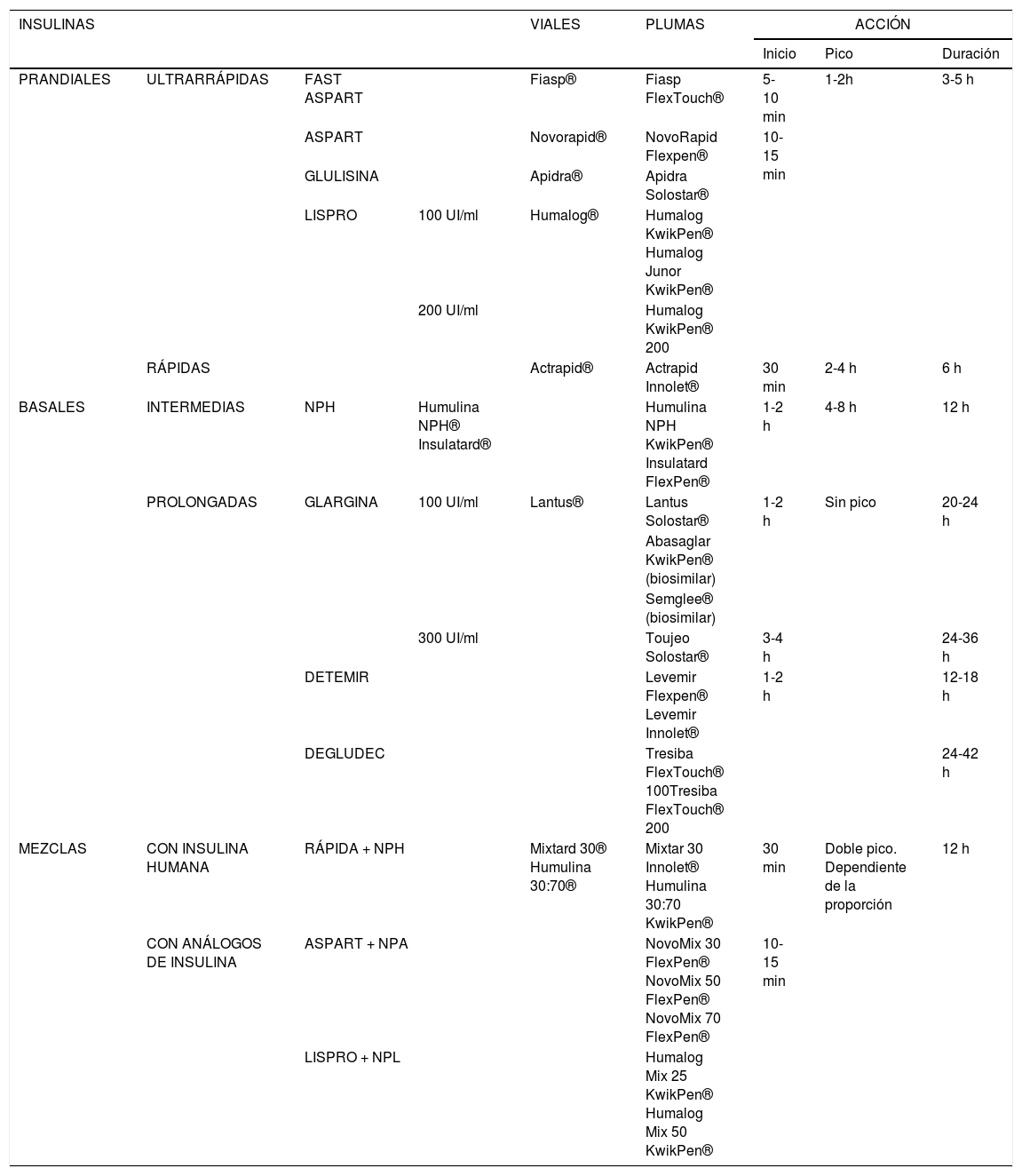
En la tabla 2, se pueden valorar los distintos tipos de insulina comercializados hasta la fecha, sus presentaciones y su acción.
Insulina comercializadas en España, presentaciones y mecanismo de acción
| INSULINAS | VIALES | PLUMAS | ACCIÓN | |||||
|---|---|---|---|---|---|---|---|---|
| Inicio | Pico | Duración | ||||||
| PRANDIALES | ULTRARRÁPIDAS | FAST ASPART | Fiasp® | Fiasp FlexTouch® | 5-10 min | 1-2h | 3-5 h | |
| ASPART | Novorapid® | NovoRapid Flexpen® | 10-15 min | |||||
| GLULISINA | Apidra® | Apidra Solostar® | ||||||
| LISPRO | 100 UI/ml | Humalog® | Humalog KwikPen® Humalog Junor KwikPen® | |||||
| 200 UI/ml | Humalog KwikPen® 200 | |||||||
| RÁPIDAS | Actrapid® | Actrapid Innolet® | 30 min | 2-4 h | 6 h | |||
| BASALES | INTERMEDIAS | NPH | Humulina NPH® Insulatard® | Humulina NPH KwikPen® Insulatard FlexPen® | 1-2 h | 4-8 h | 12 h | |
| PROLONGADAS | GLARGINA | 100 UI/ml | Lantus® | Lantus Solostar® | 1-2 h | Sin pico | 20-24 h | |
| Abasaglar KwikPen® (biosimilar) | ||||||||
| Semglee® (biosimilar) | ||||||||
| 300 UI/ml | Toujeo Solostar® | 3-4 h | 24-36 h | |||||
| DETEMIR | Levemir Flexpen® Levemir Innolet® | 1-2 h | 12-18 h | |||||
| DEGLUDEC | Tresiba FlexTouch® 100Tresiba FlexTouch® 200 | 24-42 h | ||||||
| MEZCLAS | CON INSULINA HUMANA | RÁPIDA + NPH | Mixtard 30® Humulina 30:70® | Mixtar 30 Innolet® Humulina 30:70 KwikPen® | 30 min | Doble pico. Dependiente de la proporción | 12 h | |
| CON ANÁLOGOS DE INSULINA | ASPART + NPA | NovoMix 30 FlexPen® NovoMix 50 FlexPen® NovoMix 70 FlexPen® | 10-15 min | |||||
| LISPRO + NPL | Humalog Mix 25 KwikPen® Humalog Mix 50 KwikPen® | |||||||
En el tratamiento de la DM2 es fundamental adaptar e individualizar el esquema terapéutico según las características de cada paciente teniendo en cuenta edad, enfermedades y/o comorbilidades, así como tratamientos asociados. Existen situaciones especiales que requieren iniciar o adecuar el tratamiento con insulina.
Tratamiento con corticoidesLa prevalencia de la diabetes esteroidea es muy variable (entre un 5 y un 50% en pacientes sin DM previa)15, estando probablemente infradiagnosticada. El criterio más útil para su diagnóstico es la presencia de glucemias > 200 mg/dL y la medida que ofrece mayor sensibilidad es la glucemia postprandial de la comida y preprandial de la cena.
Ante un valor de glucemia > 200 mg/dL la insulina es el fármaco de primera elección, ajustando la dosis en función del valor de glucemia de antes de la cena. En caso de tratamiento con corticoides de vida media intermedia, en monodosis matutina y sin tratamiento previo con insulina, se recomienda el uso de insulina de vida media intermedia en dosis única (NPH), asociada a hipoglucemiantes orales si fuera necesario, teniendo como objetivo mantener glucemias preprandiales < 140 mg/dL (ADA)16. En pacientes tratados con dos o más dosis de corticoides de acción intermedia se usará insulina NPH en dos dosis (2/3 de la dosis total antes del desayuno y 1/3 antes de la cena) y, en aquellos tratados con corticoides de vida media larga o intraarticular la opción será los análogos de insulina de larga duración (glargina o detemir) por su menor riesgo de hipoglucemia17. Ante hiperglucemias severas (> 300 mg/dL) se utilizará insulina regular, pudiéndose realizar pauta basal-plus o bolo-basal si fuera preciso.
Por último, en personas con DM ya insulinizadas se aumentará la dosis de insulina un 20-30%.
Paciente anciano frágilEn el paciente anciano existe mayor riesgo de hipoglucemia, por ello la insulinización se realiza a una dosis más baja (0,1 UI/kg/día), especialmente en ancianos frágiles. Se recomiendan por su menor tasa de hipoglucemias, los análogos de IB sobre la insulina NPH, y los análogos de insulina rápida sobre la insulina regular18. Las insulinas basales con menor riesgo de hipoglucemia son degludec y glargina-300 seguidas de glargina-100 y detemir respecto a NPH y mezclas de insulinas.
Otro aspecto para considerar son los diferentes dispositivos de administración de insulina, eligiendo aquel que mejor se adapte a las habilidades y capacidades del paciente.
Paciente en cuidados paliativosEl objetivo principal es evitar síntomas tanto de hipoglucemia como de hiperglucemia sostenida (mayor de 270 mg/dL)19. Por ello, se debe seguir la pauta de tratamiento más simple posible recomendándose, de inicio, una dosis única de IB, así como minimizar los controles de glucemia capilar.
Paciente con enfermedad renal crónicaLa insulina se puede usar sin precisar ajuste de dosis si el filtrado glomerular (FG) es mayor a 60 mL/min/1,73 m2, siendo necesario reducir la dosis un 25% si el FG es menor de 60 ml/min y, pudiendo llegar a reducir hasta un 50% la dosis si el FG es inferior a 5 mL/min20.
RamadánLas personas con diabetes de religión musulmana, aunque en principio están exentas de hacer el Ramadán, en la práctica frecuentemente desean cumplir el ayuno. Durante el Ramadán se realizan dos ingestas al día (iftar, tras ponerse el sol y suhur, antes del amanecer) predominando la toma de alimentos y bebidas ricas en hidratos de carbono de absorción rápida.
En pacientes previamente insulinizados existe mayor riesgo de hipoglucemia, particularmente si son de edad avanzada y/o larga evolución de la diabetes. Se recomienda utilizar insulinas con menor riesgo de hipoglucemia y ajustar la dosis establecida durante el Ramadán. Si no se consigue el control con IB, se aconseja utilizar insulinas de acción rápida con las dos comidas principales para cubrir el aporte calórico de las mismas. En la tabla 3 se presentan las recomendaciones para el ajuste de insulina durante el Ramadán. Es importante informar a los pacientes que las pruebas de glucosa en sangre durante el Ramadán no rompen el ayuno, ya que es un concepto erróneo frecuente en algunas partes del mundo21.
Ajuste de insulinas durante el Ramadán20
| Antes del Ramadán | Durante el Ramadán |
|---|---|
| Si insulina + sulfonilureas (SU) | Considere suspender SU. |
| Para cualquier insulina | Intente ajustar y establecer la dosis para lograr un control glucémico adecuado antes del inicio del Ramadán y luego ajuste la dosis durante el Ramadán si procede. |
| Insulina basal | |
| Una vez al día | Adminístrela con la comida de Iftaar, pero considere una reducción del 20% de la dosis habitual. |
| Dos veces al día | Ponga la dosis habitual de la mañana con la comida Iftaar y el 50% de la dosis habitual de la noche con la comida Suhoor. |
| Análogos de acción rápida | Ponga la dosis habitual de la mañana con la comida de Iftaar, omita la dosis habitual de la hora del almuerzo y administre el 50% de la dosis habitual de la noche para la comida de Suhoor si es necesario. |
| Insulinas premezcladas | Ponga la dosis habitual de la mañana con la comida Iftaar y el 50% de la dosis habitual de la noche con la comida Suhoor. Suspenda la insulina de la hora del almuerzo si la pone 3 veces al día |
Las GPC recomiendan la intensificación de la terapia mediante la adición de terapia con IB en personas con DM2 no controladas adecuadamente con antidiabéticos orales o arGLP1.
La inercia terapéutica de la terapia con insulina incluye inercia de inicio (inicio retardado de la IB), inercia de titulación (falta de ajuste de la dosis de la misma) e inercia de intensificación (retraso en intensificar la IB con otros fármacos adicionales).
Un estudio realizado en el Reino Unido encontró que las personas con diabetes persistían entre seis y siete años con cifras de HbA1c por encima del objetivo, independientemente de estar con uno, dos o tres antidiabéticos orales, antes de iniciar tratamiento con insulina y se tardaba 3,7 años en intensificar el tratamiento para aquellas personas que ya estaban con IB22. Mata-Cases et al. encontraron en nuestro país, en personas tratadas con dos antidiabéticos orales, que se intensificaba con insulina con HbA1c de 9,4%, siendo el fármaco de elección para intensificar con HbA1c ≥ 10%23.
En vida real la insulinización basal se realiza con cifras muy elevadas de HbA1c y las dosis utilizadas son mucho más bajas de las utilizadas en los ensayos clínicos. Un estudio en el que participaron 10 países, la proporción de personas con HbA1c ≥ 9% al inicio de la insulinización varió del 23-64%24.
Por lo general, las primeras 12 semanas después del inicio de la terapia con IB representan el periodo en el que se producen los mayores aumentos de dosis y las mayores reducciones glucémicas, si bien deben evitarse en lo posible las hipoglucemias para evitar la interrupción del tratamiento. En una revisión de 15 ensayos clínicos con insulina glargina-100, se apreció que el 89% del aumento de las dosis de IB se produjo en las primeras 12 semanas25. En la práctica clínica los resultados son diferentes. Un estudio observacional de personas europeas y estadounidenses con DM2 mostró que el 79,1% y el 72,2% de las personas que iniciaron la IB no lograron una HbA1c de ≤ 7,0% después de tres y 24 meses, respectivamente y los pacientes que no lograban los objetivos de control los primeros tres meses tenían menos probabilidades de presentar buen control a los dos años de la insulinización26.
El riesgo de hipoglucemias es menor cuando se utilizan análogos de insulina de segunda generación (glargina-300 y degludec) respecto a los de primera generación (glargina-100 y detemir) y NPH. Glargina-300 ha demostrado menos hipoglucemias durante el periodo de titulación respecto a insulina degludec27.
El beneficio obtenido en los ensayos clínicos, respecto a las hipoglucemias, no se ha encontrado en los estudios en la práctica clínica, probablemente debido al bajo registro que se realiza de los eventos hipoglucémicos en vida real.
La implicación del paciente es fundamental para reducir la inercia terapéutica en la insulinización. Se ha demostrado que las personas que realizan la autotitulación consiguen mejores cifras de HbA1c que cuando esta la realiza el profesional sin aumentar las hipoglucemias y mejorando la satisfacción de los pacientes28.
FinanciaciónSe recibió apoyo de Sanofi para el desarrollo del manuscrito, pero las opiniones representan las de los autores y no las de Sanofi.
Conflicto de interesesNo existe ningún conflicto de intereses de los autores con relación a la elaboración de este estudio.