Actualización en el tratamiento de la enfermedad renal crónica
More infoEl descubrimiento del papel nefroprotector de los fármacos inhibidores del cotransportador sodio-glucosa tipo 2 (iSGLT2) en las personas con diabetes mellitus tipo 2 (DM2) tras los resultados obtenidos en los respectivos ensayos de seguridad cardiovascular, supuso un cambio en el abordaje de la enfermedad renal diabética en los últimos años, posicionando a este grupo en el primer escalón de tratamiento de dicha comorbilidad.
La publicación de los resultados del estudio DAPA-CKD con dapagliflozina, en los que se demuestra su beneficio frenando la progresión de la enfermedad renal crónica (ERC) en pacientes con y sin DM ha abierto una nueva era en el manejo de esta enfermedad.
Se trata además de fármacos seguros y de fácil manejo para el clínico.
En este artículo se revisa el manejo de los iSGLT2 en los pacientes con ERC diabética y no diabética.
The discovery of the nephroprotective role of sodium-glucose cotransporter type 2 (iSGLT2) inhibitor drugs in people with type 2 diabetes mellitus (DM 2) following the results obtained in the respective cardiovascular safety trials led to a change in the approach to diabetic kidney disease in recent years, positioning this group in the first step in the treatment of this comorbidity.
The publication of the results of the DAPA-CKD study with dapagliflozin, demonstrating its benefit in slowing the progression of chronic kidney disease (CKD) in patients with and without DM, has opened a new age in the management of this pathology.
These drugs are also safe and easy to use for the clinician.
This article reviews the management of iSGLT2 in patients with diabetic and non-diabetic CKD.
La enfermedad renal crónica (ERC) es un importante problema de salud pública a nivel mundial, por lo que su detección y abordaje precoz debe considerarse una prioridad en la práctica clínica.
La ERC es definida por la organización internacional KDIGO1 por la presencia de alteraciones de estructura o función renal durante un periodo superior a 3 meses, con consecuencias para la salud independientemente de la causa puestas de manifiesto mediante distintos criterios, que se resumen en la tabla 1.
Criterios diagnósticos de ERC
| Criterios diagnósticos de ERC (cualquiera de los siguientes si persiste más allá de los 3 meses) | |
|---|---|
| Descenso del filtrado glomerular | • Filtrado glomerular <60ml/min/1,73m2 |
| Marcadores de lesión o daño renal | • Albuminuria (CAC>30mg/g; EAU>30mg/24h)• Proteinuria (PR/CR>50mg/g; EPU>150mg/24h)• Alteraciones histológicas en la biopsia renal, alteraciones en el sedimento urinario o alteraciones estructurales detectadas por técnicas de imagen• Trastornos hidroelectrolíticos o de otro tipo de origen tubular• Historia de trasplante renal |
CAC: cociente albúmina/creatinina en una muestra de orina al azar; EAU: excreción de albúmina en orina de 24h; EPU: excreción de proteína en orina de 24h; ERC: enfermedad renal crónica; PR/CR: cociente proteína/creatinina en una muestra de orina al azar.
Fuente: traducido y adaptado de García-Maset et al.2.
Los pacientes con ERC tienen en la mayoría de los casos múltiples factores de riesgo cardiovascular (FRCV) asociados, de forma que conforme aumenta el número de FRCV, se incrementa la presencia de ERC3.
Teniendo en cuenta la elevada prevalencia de ERC en la población en edad avanzada o con múltiples FRCV, es necesaria una correcta clasificación para evaluar el riesgo de los pacientes.
La clasificación de la ERC según las guías KDIGO se basa en 2 parámetros fundamentalmente: la tasa de filtrado glomerular (TFG) y la albuminuria o el cociente albúmina-creatinina1. En base a estos parámetros, se permite clasificar al paciente según el pronóstico en situaciones de riesgo bajo, moderado, alto o muy alto respecto al riesgo de referencia de pacientes sin ERC4.
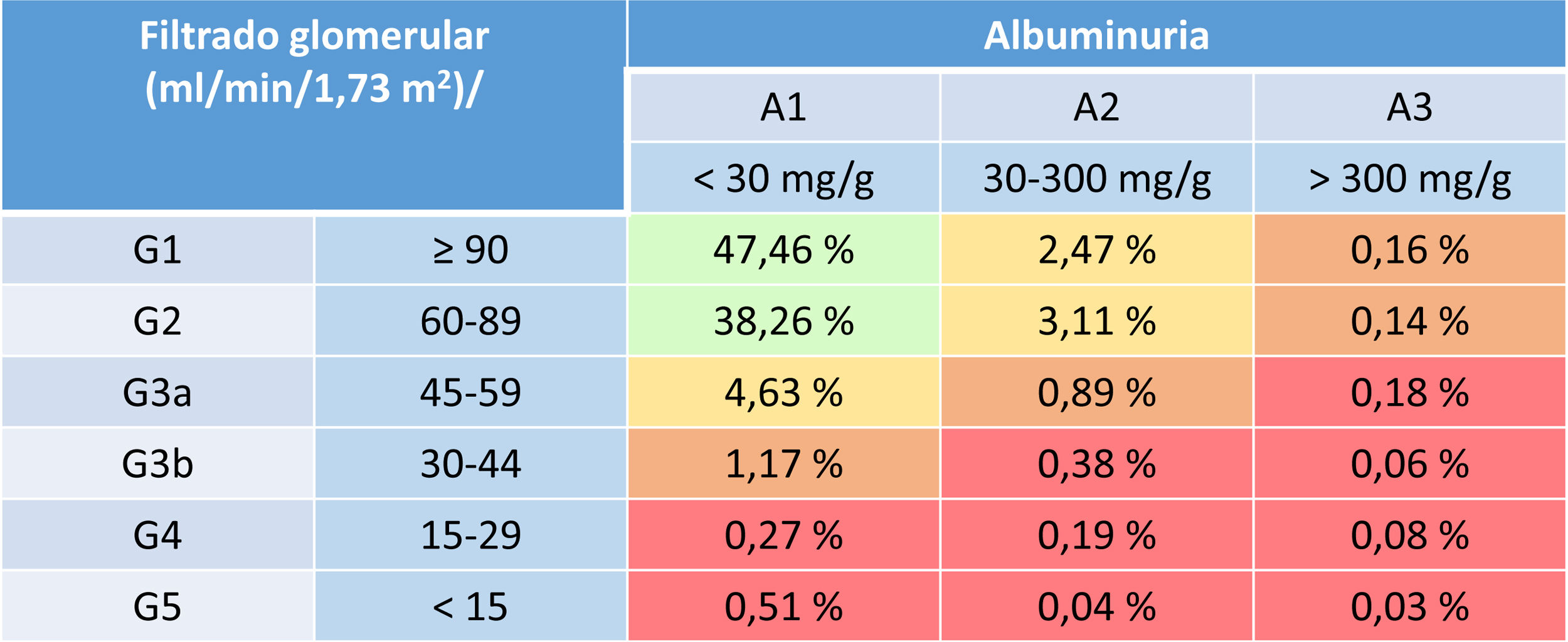
Atendiendo a esta clasificación y a este riesgo planteado por las guías KDIGO, según el estudio IBERICAN, la mayoría de la población española presenta un riesgo bajo de ERC (85,7%), mientras que menos del 5% tiene un riesgo alto o muy alto3 (tabla 2).
Clasificación, pronóstico y porcentaje de los pacientes con ERC incluidos en el estudio IBERICAN
Color verde: sin enfermedad renal crónica y riesgo de referencia.
Color amarillo: riesgo moderadamente aumentado.
Color gris: riesgo alto.
Color azul: riesgo muy alto.
Fuente: modificado de referencia Llisterri et al.3.
La diabetes mellitus tipo 2 (DM2) es la principal causa de ERC en todo el mundo (42%)5, y una de las comorbilidades que más condicionan el pronóstico en estos pacientes, aumentando el riesgo de progresión a enfermedad renal terminal y de muerte cardiovascular. Por ello, el abordaje precoz y el uso de terapias que han demostrado beneficios nefroprotectores cobra especial relevancia. La relación entre la DM2 y la ERC está claramente demostrada. Tanto es así, que la probabilidad de tener un evento renal en las personas con DM2 es superior al 50%, aproximadamente un 30% de los pacientes tendrán insuficiencia cardiaca y 4 de cada 5 personas con DM tipo tendrá un evento cardiovascular (ECV), renal o fallecerá debido a un ECV6. La ERC asociada a un mal control de la DM2 se inicia con una hiperglucemia crónica, que provoca un aumento en la reabsorción de sodio y glucosa a nivel del túbulo proximal y disminuye la captación de sodio en la mácula densa yuxtaglomerular, provocando un aumento de la presión intraglomerular y una hiperfiltración7.
Durante décadas han existido pocas alternativas terapéuticas a largo plazo para frenar la progresión de la ERC diabética, salvo el control estricto de la glucemia y de la presión arterial, que la ralentizaba, pero no la prevenía.
La ERC diabética puede presentarse como una pérdida de la función renal, demostrable como descenso del filtrado glomerular o bien como aparición de proteínas en la orina (albuminuria), o como ambas situaciones simultáneamente. Existe una gran variabilidad en la presentación y gravedad de la afectación renal en la DM, siendo posible encontrar casos en los que se presenta disminución del filtrado glomerular sin proteinuria en orina. En el estudio PERCEDIME2, realizado en consultas de atención primaria, se encontró una prevalencia de nefropatía del 27,9%; el 18% presentaba disminución del filtrado glomerular (FG) y, entre ellos, un 69% no presentaba proteinuria8.
El bloqueo del sistema renina-angiotensina-aldosterona con inhibidores de la enzima convertidora de angiotensina (IECA) o bloqueadores de los receptores de angiotensina II (ARA II) es más efectivo que otros antihipertensivos para la prevención de la ERC diabética. Su uso frente a placebo mejora todos los resultados renales (enfermedad renal crónica terminal, duplicación de creatinina sérica, complicaciones microvasculares, macroalbuminuria y regresión de albuminuria) excepto microalbuminuria en personas con ERC diabética9.
En el estudio RENAAL, losartán en comparación con placebo logró reducir un 25% el riesgo de duplicidad de creatinina sérica y un 28% el riesgo de enfermedad renal terminal, reduciendo también la proteinuria en un 35%10.
A medida que va evolucionando la enfermedad, la función renal se va deteriorando provocando disminución del filtrado glomerular y aumentando los niveles de albuminuria. Estos mecanismos provocan nefropatía incipiente y posteriormente establecida que deteriora la calidad de vida de los pacientes, aumentando su morbimortalidad a corto, medio y largo plazo.
Entre los factores que potencian y facilitan la progresión de la ERC diabética se encuentran aquellos que contribuyen a la hiperfiltración glomerular. Estos procesos están presentes desde las primeras etapas de la DM y se resumen a continuación11:
- -
Hormonales: hiperglucemia, insulinopenia, incremento en los niveles de glucagón y de hormona de crecimiento, etc.
- -
Metabólicos: aumento en las concentraciones de ácidos orgánicos (aminoácidos, lactatos, cetoácidos) y alteraciones en el funcionamiento de distintas vías metabólicas (poliol, calcio…).
- -
Otros: ingesta de proteínas elevada, expansión del volumen extracelular, etc.
Dada la elevada prevalencia de la ERC en las personas con DM2, se recomienda el cribado de esta complicación en el momento del diagnóstico en personas con DM2 y a los 5 años del diagnóstico en aquellas con DM tipo 112.
El control adecuado de la presión arterial y los niveles de lípidos, así como del resto de factores de riesgo cardiovascular son fundamentales para frenar la progresión de la ERC diabética.
El seguimiento de la ERC diabética precisa de un control estricto de los niveles de creatinina sérica, TFG y CAC. Se recomienda una medición de estos niveles de forma semestral para los estadios 1 y 2 de la ERC, cuatrimestral para pacientes en estadio 3 de la ERC y trimestral en pacientes a partir del estadio 4, aunque estas recomendaciones deben individualizarse en función de cada paciente13.
Las principales guías de práctica clínica12,13, recomiendan elegir el tratamiento antidiabético con un enfoque centrado en el paciente y con los fármacos que mejor se adapten a sus características y comorbilidades. En pacientes con enfermedad cardiovascular establecida o riesgo cardiovascular alto, enfermedad renal o insuficiencia cardiaca, se recomienda el uso de los iSGLT2 o los agonistas de los receptores del péptido similar al glucagón tipo 1 (arGLP1) con beneficios de protección cardiovascular demostrados, independientemente de los niveles glucémicos y lo más precozmente posible.
Papel de los inhibidores del cotransportador sodio-glucosa tipo 2 en la enfermedad renal crónica diabéticaLos iSGLT-2 desempeñan un papel esencial para frenar la progresión de la ERC diabética en fenotipos tanto albuminúricos como no albuminúricos. Estos fármacos actúan disminuyendo los niveles de glucemia mediante la inhibición del cotransportador sodio-glucosa, bloqueando la captación de sodio y glucosa en el túbulo proximal y promoviendo la glucosuria además de otros cambios a nivel renal. Los resultados de varios ensayos de seguridad cardiovascular de los iSGLT214–16 sugerían un beneficio renal al demostrase una reducción de riesgo comparado con placebo en los objetivos renales del 47% para dapagliflozina, 46% para empagliflozina y 40% para canagliflozina.
Posteriormente estos resultados han sido han sido confirmados en otros estudios específicos sobre población con ERC17.
En estos trabajos se ha demostrado la acción nefroprotectora de los iSGLT2 en diferentes niveles de filtrado glomerular y de albuminuria, incluso ante la ausencia de diabetes, suponiendo un importante avance en el manejo de la ERC en los últimos años18.
Manejo práctico de los inhibidores del cotransportador sodio-glucosa tipo 2 en la enfermedad renal crónica diabéticaLas guías KDIGO para el manejo de la ERC en la DM13 posicionan a los iSGLT2 como primera opción para el tratamiento junto a modificaciones de estilos de vida y metformina con un nivel de recomendación IA.
El inicio de estos fármacos debe considerarse de forma temprana por todos los beneficios sobre el continuo cardio-reno-metabólico demostrados.
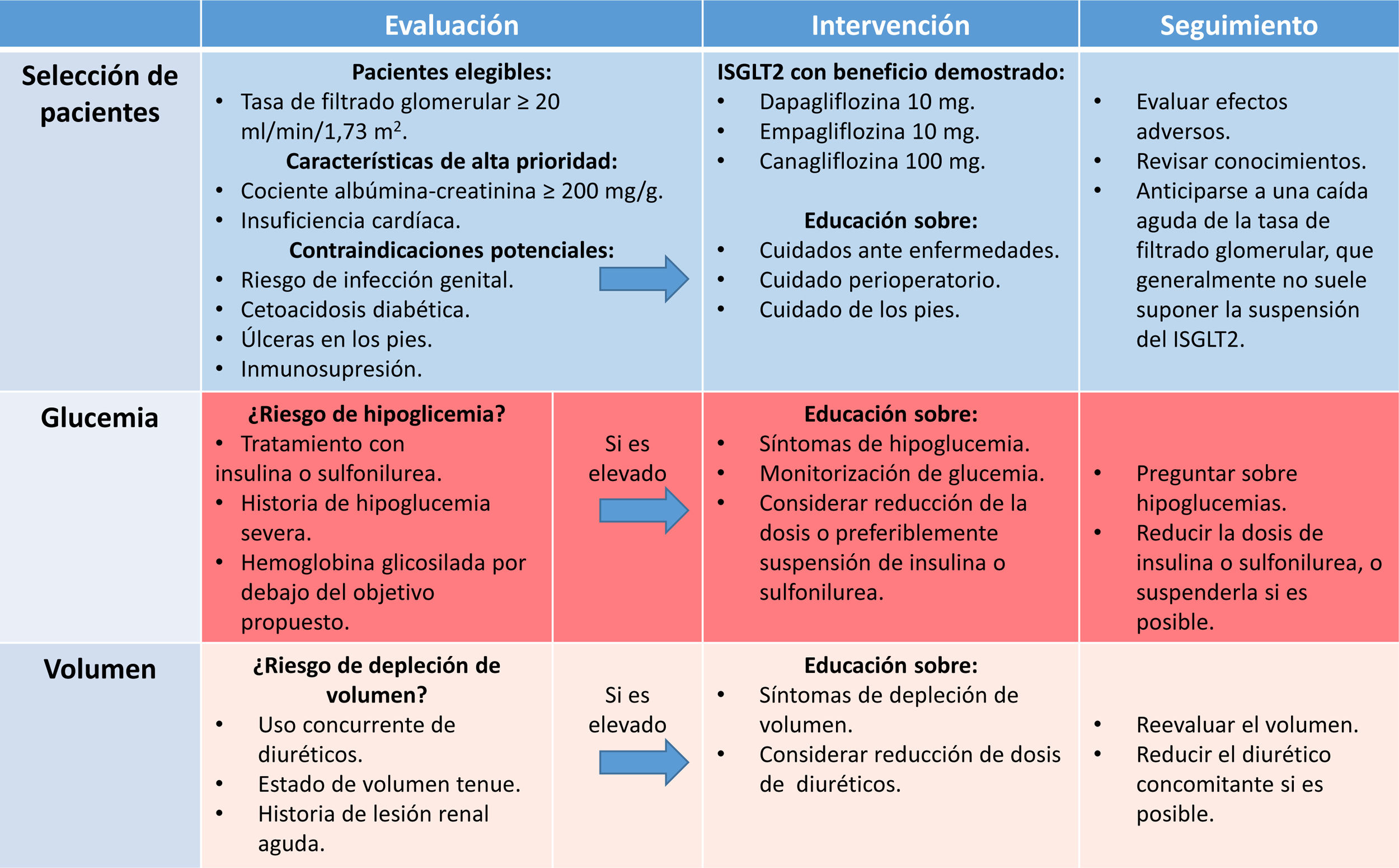
Las consideraciones a tener cuenta para el inicio y el seguimiento de iSGLT-2 en personas con ERC diabética se resumen en la tabla 3.
Manejo práctico de los iSGLT2 en pacientes con DM2 y ERC
DM2: diabetes mellitus 2; ERC: enfermedad renal crónica; iSGLT2: inhibidores del cotransportador sodio-glucosa tipo 2.
Fuente: traducida y modificada de Kidney Disease13.
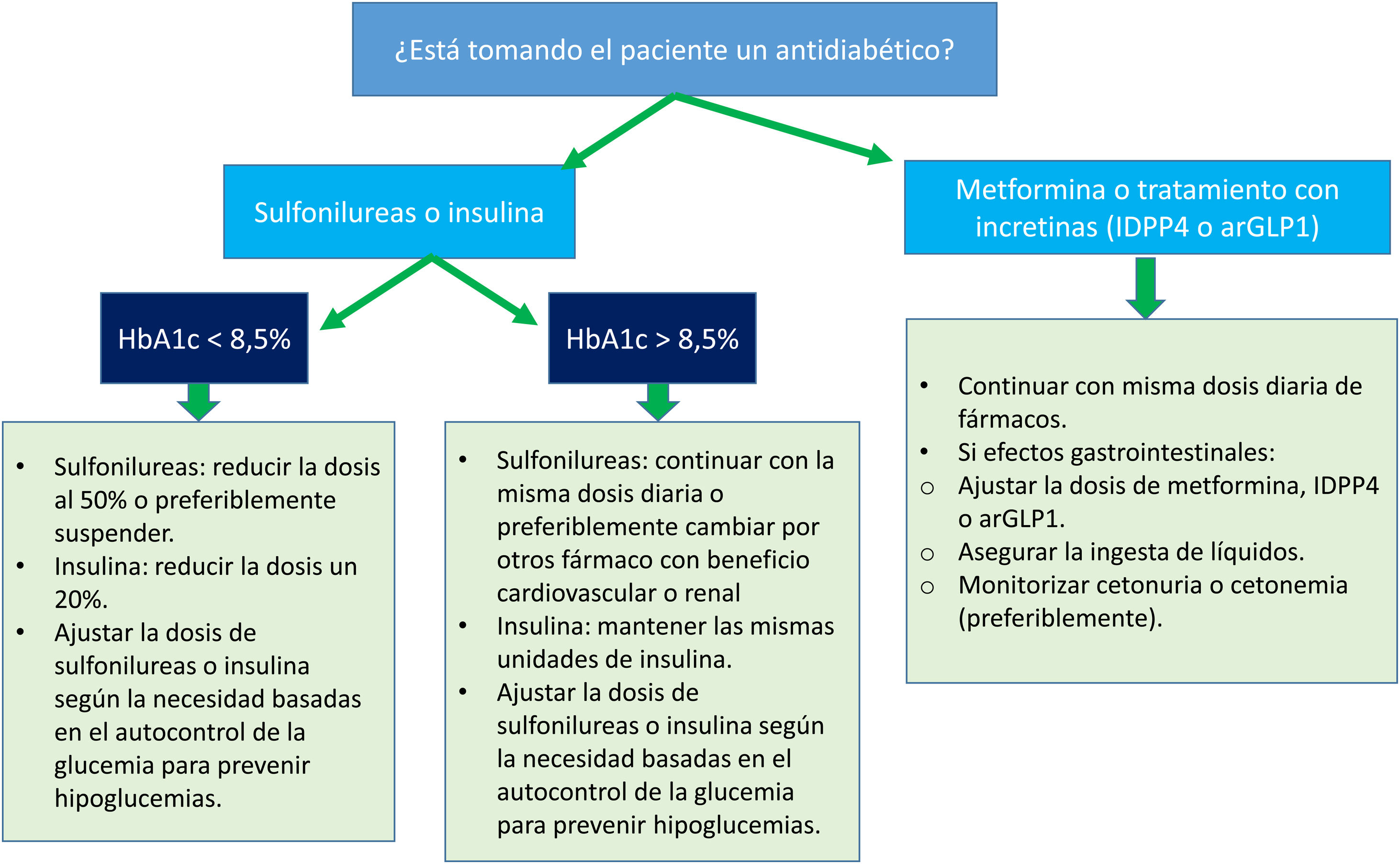
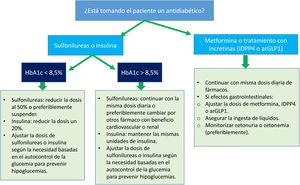
En aquellas personas con DM2 y ERC que previamente estuvieran tratadas con otros fármacos antidiabéticos, tanto no insulínicos como insulina, no debe retrasarse la introducción de un iSGLT2 por los beneficios nefroprotectores y cardiovasculares ya comentados19. El ajuste de dosis de otros fármacos en función del control glucémico de los pacientes se resume en la figura 1.
Manejo combinado de iSGLT2 y otros fármacos antidiabéticos. Fuente: adaptado de Gómez-Peralta et al.19.
Aunque la condición clínica que más contribuye a la prevalencia global de la ERC es la DM, existen otras causas de gran importancia como la hipertensión arterial (18%) o las glomerulonefritis (18%)5.
En España, el estudio ENRICA20 evaluó el impacto de los factores de riesgo de ECV en la prevalencia de ERC, concluyendo que ésta aumenta de forma marcada con la acumulación de FRCV. De hecho, la ERC se presenta en una cuarta parte de los pacientes mayores de 65 años y se incrementa exponencialmente con la presencian de varios FRCV3.
El estudio DAPA-CKD21 ha abierto una nueva era en el abordaje del paciente con ERC de etiología no diabética, ya que hasta su publicación no había habido ningún tratamiento que hubiera demostrado reducción de la mortalidad en estos pacientes. Dapagliflozina demostró una reducción del riesgo del 39% en el objetivo primario (disminución sostenida en la TFG estimada de al menos un 50%, enfermedad renal en etapa terminal o muerte por causas renales o cardiovasculares), con una disminución de la mortalidad por cualquier causa y demostrando el beneficio de los iSGLT2 independientemente de la presencia o la ausencia de la diabetes.
Este efecto nefroprotector de los iSGLT2 en pacientes sin DM se ha corroborado recientemente con empagliflozina en el estudio EMPA-KIDNEY22, que comparó empagliflozina con placebo en pacientes con ERC que tenían una TFG entre 20-45mil/min o un TFG entre 45-90mil/min con un CAC de al menos 200mg/g, evaluó el efecto renal de la empagliflozina en ese perfil de pacientes. En dicho estudio, la terapia con empagliflozina se asoció a un menor riesgo de progresión de la enfermedad renal o muerte por causas cardiovasculares frente a placebo (reducción del 28%), siendo estos resultados consistentes entre los pacientes con o sin diabetes e independientemente del subgrupo definido según la TFG. Por todo ello, podemos decir que los iSGLT2 constituyen un fármaco clave en el manejo de la ERC, independientemente de la presencia de diabetes, aunque sus potenciales beneficios aún se siguen investigando, debe constituir la piedra angular del tratamiento de la ERC.
Manejo de los inhibidores del cotransportador sodio-glucosa tipo 2 en la enfermedad renal crónica no diabéticaEn el momento actual, dapagliflozina es el único iSGLT2 con uso aprobado en ficha técnica en España en ERC de cualquier etiología23.
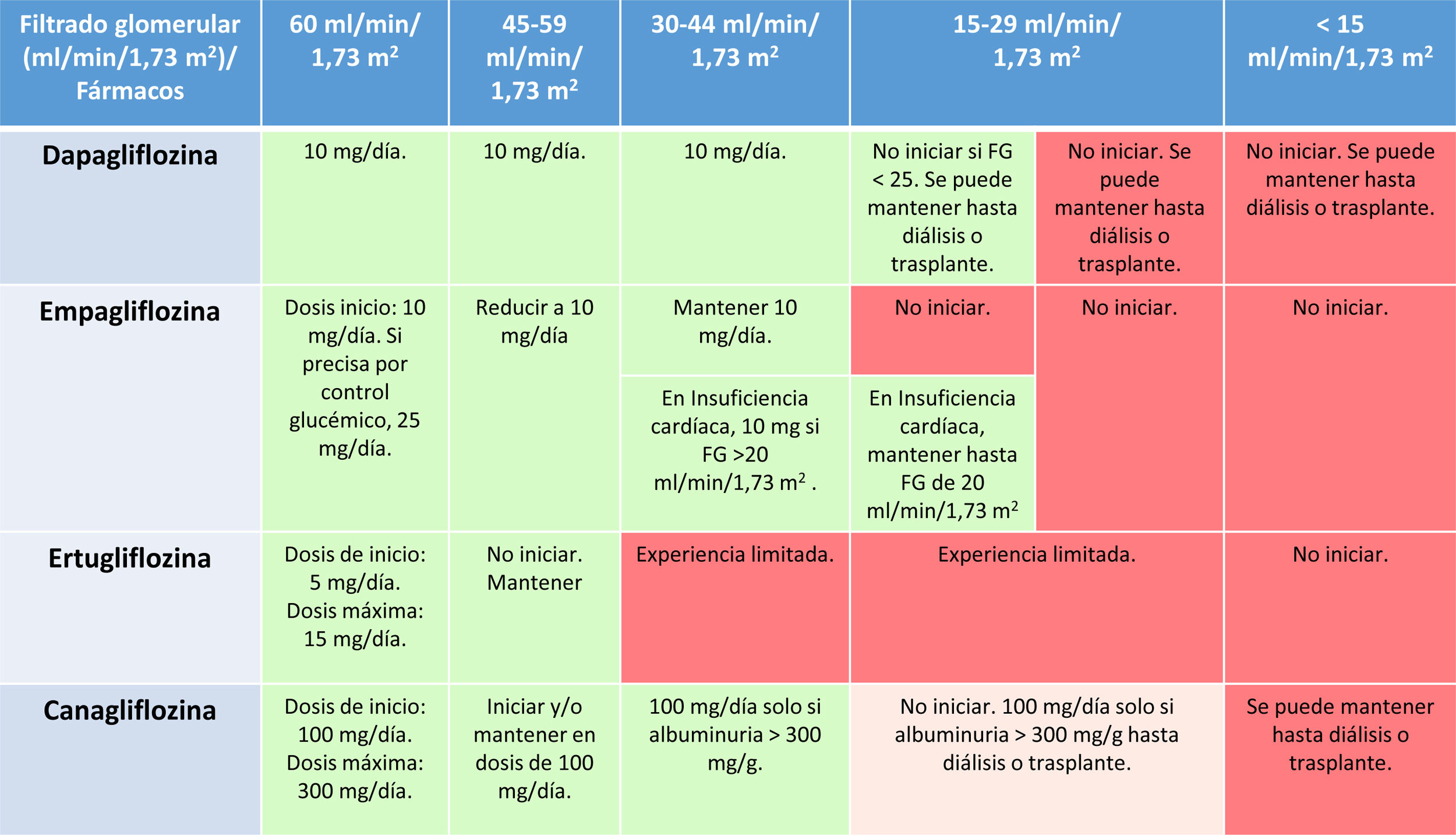
Su inicio está recomendado hasta una TFG de 25ml/min/1,73m2, pudiéndose mantener hasta el comienzo de la terapia renal sustitutiva o el trasplante. Este es un hecho diferencial de sapagliflozina con respecto al resto de iSGLT2, reflejando su seguridad en pacientes con ERC avanzada. La dosis de dapagliflozina es de 10mg, se mantiene constante durante todos los estadios de función renal y su manejo no difiere del ya comentado en el paciente con ERC diabética. El ajuste de dosis en función del filtrado glomerular de los iSGLT2 en personas con DM se detalla en la tabla 4.
Ajuste de iSGLT2 en función del filtrado glomerular en personas con DM
DM: diabetes mellitus; FG: filtrado glomerular; iSGLT2: inhibidores del cotransportador sodio-glucosa tipo 2.
Fuente: modificado de García-Maset et al.2.
A lo largo del desarrollo de los diferentes ensayos clínicos con iSGLT214,21,22,24-27 los resultados de seguridad tanto en pacientes con DM como en los que no lo son permiten afirmar que su uso es seguro en pacientes con ERC.
Las complicaciones derivadas de su uso que pueden presentarse23-29 se resumen a continuación:
FrecuentesInfecciones genitourinarias
Las infecciones genitourinarias son una complicación frecuente tanto en hombres como en mujeres con DM. La excreción urinaria de glucosa producida por los iSGLT2 favorece el desarrollo de vulvovaginitis y balanitis sobre todo de origen fúngico, siendo los microorganismos más comúnmente implicados Candida albicans y Candida glabrata30.
Generalmente estas infecciones responden a tratamiento convencional y no precisan de ninguna medida adicional. Es fundamental reforzar unas medidas de higiene e hidratación correctas. En general, no es necesario suspender el iSGLT2 durante el episodio de infección genital. La pauta de tratamiento farmacológico se resume en la tabla 5.
Recomendaciones para el tratamiento de infecciones genitourinarias provocadas por iSGLT2
| Recomendaciones ante infecciones genitourinarias provocadas por iSGLT2 | |
|---|---|
| Vulvovaginitis candidiásica no complicada | • Antifúngico tópico o• Fluconazol 150mg vía oral, dosis única |
| Vulvovaginitis candidiásica complicada | • Fluconazol 150mg vía oral cada 72h hasta completar 3 dosis |
| Vulvovaginitis por Candida glabrata que no responde a azoles | • Ácido bórico intravaginal 600mg/cada 24h/14 días o• Nistatina intravaginal 100.000U/día/durante 14 días |
| Vulvovaginitis candidiásica recurrente | • Antifúngico tópico 10-14 días y fluconazol 150mg/vía oral/semanal/durante 6 meses |
| Balanitis candidiásica | • Clotrimazol al 1% tópico/cada 12h/durante 10 días o• Miconazol al 2% tópico cada 12h/durante 10 días |
iSGLT2: inhibidores del cotransportador sodio-glucosa tipo 2.
Fuente: adaptado de Pappas31.
En cuanto a las infecciones de tracto urinario (ITU), se ha constatado en los diversos estudios un riesgo ligeramente mayor en pacientes con iSGLT2, aunque no significativo. Este riesgo es mayor en personas con DM21,22 frente a las no diabéticas. En general, las ITU asociadas al uso de iSGLT2 responden a tratamiento antibiótico habitual, por lo que no debe ser una limitación para el empleo de estos fármacos.
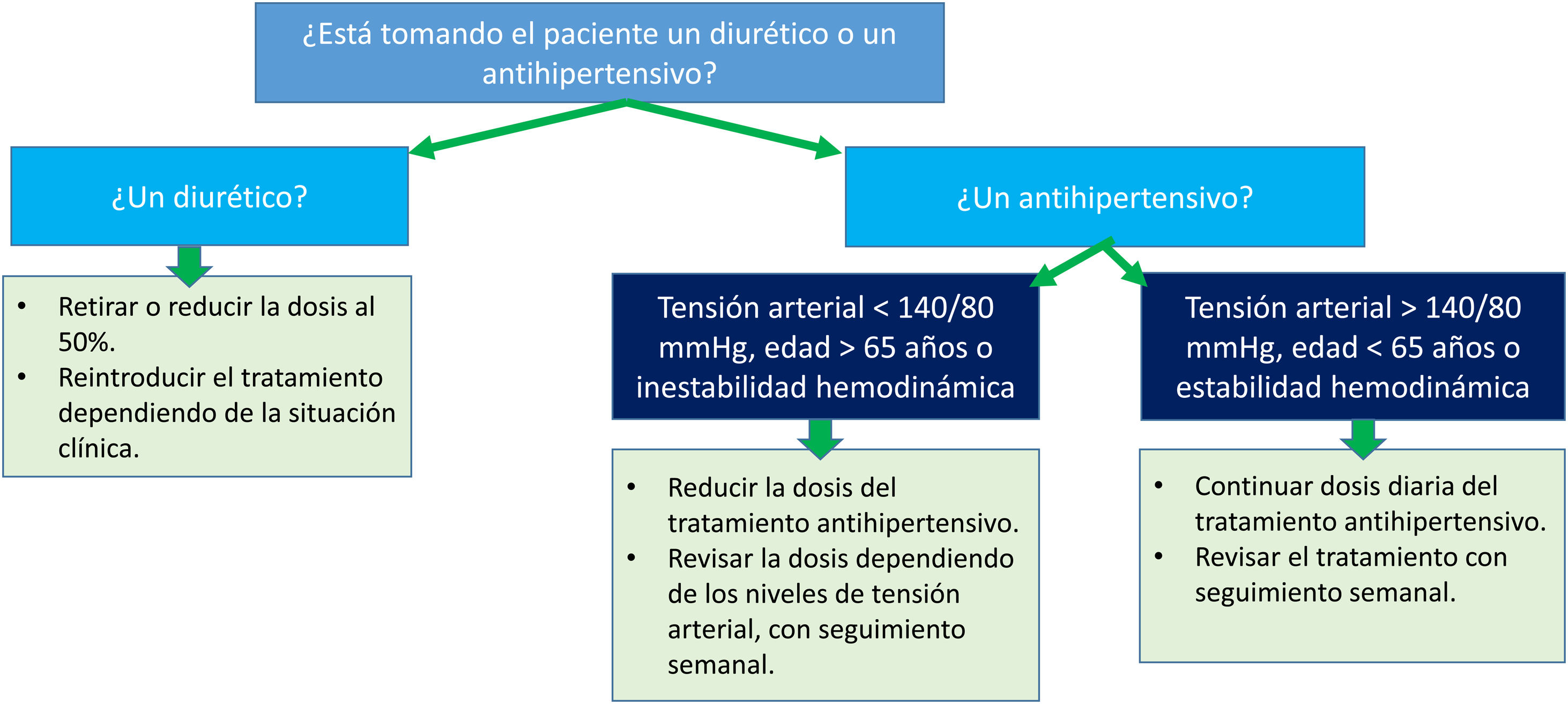
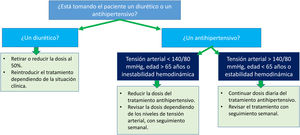
Deshidratación e hipotensiónEn general, el riesgo de hipovolemia en pacientes con iSGLT2 es mayor en aquellos con uso concomitante de diuréticos, sobre todo tiazídicos y de asa, respecto a los que no los toman. El ajuste de estos fármacos se resume en la figura 2.
Manejo combinado de iSGLT-2 y diuréticos. Fuente: adaptado de Gómez-Peralta et al.19.
Es aconsejable retirar transitoriamente el iSGLT2 en situaciones de riesgo de deshidratación, por ejemplo en el contexto de pérdidas agudas de volumen, infecciones o fiebre y reintroducirlo cuando se resuelva la situación26–28.
HipoglucemiaEn general los iSGLT2 cuando se utilizan en monoterapia se asocian a un riesgo muy bajo de hipoglucemia y la aparición de éstas suele relacionarse con el uso combinado con sulfonilureas o insulina, debiendo plantearse una reducción de dosis o incluso la suspensión de estos fármacos al añadir un iSGLT2. El uso concomitante con el resto de fármacos antidiabéticos no presenta ningún problema en este sentido.
Así mismo, no se ha detectado un riesgo significativo de hipoglucemia en personas no diabéticas en los estudios realizados con dapagliflozina y empagliflozina y ERC, demostrando ser fármacos seguros21,24–27.
Poco frecuentesCetoacidosis
Aunque a lo largo del desarrollo clínico de los iSGLT2 se han descrito casos de cetoacidosis euglucémica relacionados con su uso, las causas en personas con DM2 permanecen aún en estudio, y en la actualidad no hay evidencia para desaconsejar su utilización por este motivo al no haberse demostrado diferencias estadísticamente significativas en los principales estudios en comparación con placebo14–16. Tampoco se han encontrado diferencias en personas no diabéticas para dapagliflozina y empagliflozina21,22.
Antes de iniciar el tratamiento con iSGLT2 deben considerarse posibles factores que predispongan al desarrollo de cetoacidosis, como transgresiones dietéticas, emergencias quirúrgicas, estrés, deshidratación, etc.
Elevación de creatinina y disminución de la tasa de filtrado glomerularPor lo general, los aumentos iniciales en la creatinina y las disminuciones iniciales en la TFG estimada en los pacientes tratados con iSGLT2 son transitorios32 y no suponen un motivo para la retirada del fármaco23,28,29.
InfrecuentesFascitis necrosante del periné (gangrena de Fournier)
La relación entre el uso de iSGLT2 y la gangrena de Fournier es muy poco frecuente, aunque se han descrito casos tras la comercialización de canagliflozina29 y dapagliflozina23.
Aunque se trata de un acontecimiento bastante raro, puede resultar grave y potencialmente mortal, requiriendo una intervención quirúrgica urgente y tratamiento antibiótico.
Amputaciones
Tras la publicación de los datos del estudio CANVAS con canagliflozina14, el riesgo de amputaciones de miembro inferior con los iSGLT2 ha supuesto un motivo de controversia. En 2020, la Food and Drug Administration (FDA) retira la alerta al no haberse podido establecer una clara relación de este hecho con el uso de iSGLT2. En general, es aconsejable recomendar el cuidado rutinario de los pies en todas las personas con DM para evitar posibles complicaciones.
Manejo de iSGLT2 en situaciones especiales
Existen algunas situaciones concretas en las que los iSGLT2 tanto en personas diabéticas como no diabéticas deben emplearse con ciertas precauciones33,34:
- -
Enfermedades agudas intercurrentes (infecciones graves, síndrome coronario, etc.): se aconseja interrumpir su uso hasta la resolución de la situación clínica y la recuperación de la ingesta oral.
- -
Cirugía mayor: suspender entre 48 y 72h antes y reiniciar cuando el paciente esté clínicamente estable, euvolémico y con tolerancia oral adecuada.
- -
Cirugía bariátrica: suspender previamente en función del tratamiento dietético indicado al paciente, considerando especialmente la ingesta de carbohidratos.
- -
Situaciones con riesgo de depleción de volumen excesivo (realización de pruebas diagnósticas invasivas como colonoscopia, realización de ejercicio físico intenso programado, etc.): suspender entre 48 y 72h hasta recuperar un adecuado estado de hidratación.
Los iSGLT2 han demostrado ser fármacos nefroprotectores en personas con DM. Dapagliflozina y empagliflozina han demostrado frenar así mismo la progresión de la caída de filtrado glomerular y de la albuminuria en personas con ERC no diabética. El uso de estos fármacos es sencillo y seguro y abre una nueva era en el abordaje de la ERC de cualquier etiología, debiendo priorizarse su uso de forma precoz por sus beneficios metabólicos y cardiorrenales demostrados.
Información sobre el suplementoEste artículo forma parte del suplemento titulado «Actualización en el tratamiento de la enfermedad renal crónica», que ha sido patrocinado por AstraZeneca.
Conflicto de interesesÉste manuscrito forma parte del suplemento de Enfermedad Renal Crónica de la revista Medicina de Familia SEMERGEN con el patrocinio no condicionado de AstraZeneca.
La Dra. María José Castillo Moraga declara haber recibido honorarios por consultorías/ponencias de laboratorios Servier, Daiichi-Sankyo, Novartis, Almirall, Sanofi, Boehringer-Ingelheim, GSK, AstraZeneca, Lilly, Novartis, Novo Nordisk, Organon, Sanofi, Esteve, TEVA, Ferrer, Rovi y Vifor Pharma.
El Dr. Miguel Turégano Yedro declara haber recibido honorarios por consultorías/ponencias de laboratorios Servier, Daiichi-Sankyo, Novartis, Almirall, Astellas, Bayer, Bristol-Myers Squibb, Janssen, MSD, Lilly, Sanofi, Boehringer-Ingelheim, GSK, AstraZeneca, Novartis, Novo Nordisk, Sanofi, Esteve, Ferrer y Viatris.
El Dr. Vicente Pallarés Carratalá refiere haber recibido subvenciones y apoyo a la investigación (2018-2024): FIS ISCIII-AES-2018/003116 (ESCARVAL-Genero); Grant AZ Agora-AP Study, ESR-17-12871 (fundación SEMERGEN). Así mismo declara haber recibido honorarios por consultorías/ponencias de laboratorios Servier, MSD, DaiichiSankyo, Novartis, Almirall, Sanofi, Pfizer, Viatris, Bial, Boehringer-Ingelheim, Recordati, GSK, Rubió, AstraZeneca, Novartis, Organon, Sanofi, Esteve, Menarini, TEVA, Ferrer, Rovi, Vifor Pharma y VISO.