La brucelosis es una enfermedad zoonótica de distribución mundial que genera importantes pérdidas productivas e impactos negativos sobre la salud pública. El objetivo de este trabajo fue identificar factores de riesgo asociados a la presencia de brucelosis en explotaciones mixtas, con bovinos y caprinos, en la región centro-oeste de la provincia de Formosa. Se muestrearon de manera aleatoria 67 establecimientos mixtos con un total de 7.855 animales (2.943 bovinos y 4.912 caprinos) durante 2022 y el primer semestre de 2023. Las muestras fueron analizadas serológicamente (antígeno tamponado [BPA] + prueba de fluorescencia polarizada [FPA]) para determinar el número de animales positivos. Asimismo, en cada establecimiento se realizó una encuesta confidencial al productor para detectar potenciales variables asociadas a la presencia de la enfermedad. El análisis estadístico se realizó empleando modelos lineales generalizados mixtos (MLGM) con distribución binomial, función de enlace logarítmico y rodeo como variable aleatoria. La prevalencia estimada de brucelosis en establecimientos mixtos fue del 9% y por animal del 2,75% de manera conjunta (caprinos-bovinos). La prevalencia de brucelosis en bovinos y caprinos estuvo explicada por la presencia de animales con signología reproductiva (odds ratio [OR]=40), presencia de abortos de edades gestacionales avanzadas o nacimiento de crías débiles (OR=5,3), el tratamiento incorrecto de los abortos (OR=8) y el ingreso de animales desde otras explotaciones (OR=5,9), sin certificado negativo de brucelosis (OR=9,6). Es importante el manejo que se lleva a cabo en cada establecimiento para el control de la brucelosis, lo que debería abarcar medidas preventivas, prácticas de sanitización en los corrales y la protección de los operarios.
Brucellosis is a zoonotic disease with a worldwide distribution that causes significant productive losses and negative impacts on public health. The aim of this work was to identify the risk factors associated with the presence of brucellosis in mixed farms (cattle/goats) in the central-western region of the province of Formosa. Sixty seven mixed farms with 7,855 animals (2,943 cattle and 4,912 goats) were randomly sampled during 2022/2023. The samples were serologically analyzed (BPA + FPA) to determine which animals were positive. Likewise, in each farm, a confidential survey was carried out to evaluate potential associated variables. The statistical analysis was performed using Generalized Linear Mixed Models (GLMM) with binomial distribution, logarithmic link function, and farm as a random variable. The estimated prevalence of brucellosis in mixed farms was 9%, while the joint prevalence per animal (cattle and goats) was 2.75%. The prevalence of brucellosis in cattle and goats was explained by the presence of animals with reproductive signs (odds ratio, OR=40), the occurrence of abortions in the last term of gestation and the birth of weak offspring (OR=5.3), incorrect treatment of abortions (OR=8), the introduction of animals from other farms (OR=5.9), and not having a negative brucellosis certificate (OR=9.6). The management practices conducted in each farm such as preventive measures, sanitation practices for the pens, and prevention measures for the workers, are important for the control of brucellosis.
La brucelosis es una patología zoonótica de distribución mundial conocida desde hace muchos años; sin embargo, continúa siendo un problema sanitario y económico de envergadura. Es una enfermedad infectocontagiosa producida por bacterias intracelulares del género Brucella8,43.
Algunas especies como Brucella abortus, Brucella melitensis, Brucella suis, Brucella ovis, Brucella canis, Brucella neotomae, Brucella microti, Brucella vulpis, Brucella inopinata y Brucella papionis afectan a animales terrestres; otras especies afectan a mamíferos marinos (Brucella ceti y Brucella pinnipedialis). B. abortus, B. melitensis, B. suis y B. canis son patógenas para los humanos; como zoonosis, esta enfermedad está muy extendida en todo el mundo, ubicándose como una de las siete enfermedades más desatendidas según la Organización Mundial de la Salud (OMS)20,22. El riesgo de contraerla es más elevado para quienes trabajan con animales susceptibles de padecer la enfermedad, lo que abarca productores agropecuarios, veterinarios, trabajadores rurales y personal de frigoríficos27,29,43.
Las principales vías de transmisión de Brucella en los animales son la placenta, los líquidos fetales y las secreciones vaginales expulsadas por las hembras infectadas, ya sea al abortar o varios meses después del aborto o el parto. Una vez que esta bacteria ingresa al organismo, aquellas células que logran escapar del sistema inmune pueden llegar hasta los ganglios linfáticos de la cabeza y el cuello debido a que la vía de entrada más común es la oral/digestiva. Si la bacteria no es detenida, se establece una infección persistente con la posibilidad de producir una bacteriemia al dispersarse por todo el organismo. La bacteria puede llegar al bazo y órganos asociados a la reproducción (útero, epidídimo y testículos), así como a las articulaciones14,22,28.
El reservorio de estos microrganismos son especies domésticas de ganado vacuno, porcino, caprino y ovino, así como bisontes, camélidos americanos, alces y algunas especies de ciervos y de animales silvestres (liebre, zorro, comadreja, etc.)26.
La infección por Brucella en ganado bovino suele estar causada por biovariedades de B. abortus. Sin embargo, en algunos países del sur de Europa, África y Asia occidental, en los que el ganado bovino se suele criar en estrecha relación con ganado ovino o caprino, la infección también puede deberse a B. melitensis. En ocasiones, B. suis puede causar infecciones en ganado bovino2,22,27.
Esta patología está muy difundida a nivel mundial; sin embargo, y a pesar de ser la brucelosis una de las enfermedades más importantes del ganado bovino en América Latina y otras zonas de desarrollo preindustrial, muchos países carecen de programas de control43.
En la Argentina, rige el Plan de Control y Erradicación de la brucelosis (Resolución 67/2019 y sus modificatorias)41 y, como medida preventiva, se indica la vacunación antibrucélica obligatoria de todas las terneras de tres a ocho meses de edad con vacuna B. abortus cepa 19, controlada y aprobada por el Servicio Nacional de Sanidad Animal y Calidad Agroalimentaria (SENASA) e identificada con estampilla oficial, con su número de serie y fecha de vencimiento40.
Si bien el plan continúa vigente, existe una prevalencia predial de brucelosis bovina en el país del 12,4%38. En la provincia de Formosa, la cifra es del 13,55%. Estudios previos citan una prevalencia del 22%33 y, para el periodo 2018-2021, se estimó una prevalencia predial del 17,1%, mientras que la prevalencia por animal fue del 0,88% en la provincia16.
Con respecto a la especie caprina, en particular, la distribución de la enfermedad dentro del país no es homogénea32. Se identificaron áreas con alta prevalencia, como la provincia de Mendoza, sur de San Juan, este de Salta, oeste de Formosa y parte de La Rioja y Catamarca, y también áreas con prevalencias bajas en determinadas zonas de las provincias de San Luis, Córdoba, Tucumán, Santiago del Estero y oeste de Chaco. Incluso hay áreas donde no hay indicios de la enfermedad, como en la Quebrada de Humahuaca, los valles áridos de Salta y algunos departamentos de Catamarca y Tucumán. Tampoco en las provincias de Buenos Aires, La Pampa, Corrientes, Misiones, Entre Ríos y Santa Fe. Finalmente, la Patagonia fue declarada región libre de B. melitensis31. En la provincia de Formosa, se estimó una prevalencia global del 2%, con un incremento de este a oeste (0,22%, 1,22%y 3,76% en las zonas este, centro y oeste, respectivamente). La prevalencia de majadas positivas fue del 3,6% en la región este, del 12% en la región centro y del 36% en la región oeste34. Dichos valores son elevados y cabe mencionar que mediante la Resolución n.° 372/2017 se aprobó el Plan Nacional de Control de brucelosis caprina; sin embargo, dicho plan no se lleva a cabo hasta el día de la fecha en la provincia.
Por lo mencionado, es importante diseñar estrategias de control y erradicación de la enfermedad en sistemas mixtos de zonas con crianza familiar o de baja escala. Y para ello, es necesario identificar los factores de riesgo que modulan la presencia y difusión de la brucelosis. El presente trabajo tuvo como objetivo contribuir al conocimiento de la epidemiología de la brucelosis, identificando los factores de riesgo que modifican la prevalencia de la enfermedad en explotaciones mixtas compuestas de bovinos y caprinos, ubicadas en la región centro-oeste de la provincia de Formosa.
Materiales y métodosÁrea de estudio y muestreoSe realizó un estudio observacional transversal en establecimientos pecuarios mixtos (bovinos y caprinos) en los departamentos Patiño y Bermejo, provincia de Formosa. Estos tienen la particularidad de incluir rodeos de tamaño mediano a pequeño (hasta 500 animales), excepcionalmente los rodeos son más grandes (más de 500 cabezas). La mayoría de los propietarios son familias que utilizan sus animales para consumo propio, con bajo número de ventas.
El número de establecimientos para ser muestreados se determinó empleando la ecuación general del tamaño muestral para estimar una proporción (prevalencia), con una prevalencia esperada del 22% (considerando datos reportados en 201333), un intervalo de confianza del 95% (IC 95%) y un error aceptable <10%. De tal forma, se muestrearon de manera aleatoria 67 establecimientos ubicados en el centro-oeste de la provincia de Formosa, con un total de 7.855 animales (2.943 bovinos y 4.912 caprinos) durante el año 2022 y el primer semestre de 2023.
Dentro de cada establecimiento, se tomaron muestras de sangre de al menos un 25% de la totalidad de los animales de cada especie (bovinos: hembras mayores de 18 meses y machos mayores de seis meses; caprinos: hembras y machos mayores de seis meses, según recomendaciones del SENASA). Las muestras de sangre se recolectaron por venopunción de la vena yugular sin anticoagulante. Luego de la extracción e identificación, fueron trasladadas inmediatamente (<6h) hasta el laboratorio bajo refrigeración e identificadas para su posterior procesamiento.
En cada establecimiento, el investigador también realizó una encuesta confidencial a cada productor. El objetivo de esta encuesta fue evaluar el efecto de potenciales variables explicativas sobre la prevalencia de brucelosis. La encuesta incluyó los siguientes aspectos generales: ubicación geográfica, número de animales, condiciones ecológicas, prácticas pecuarias cotidianas y antecedentes de la enfermedad, en el caso de que hubiera.
Identificación de los animales serológicamente positivos a Brucella spp.Las muestras de sangre fueron centrifugadas para lograr la correcta separación del suero, en el que se efectuó la prueba de aglutinación en placa con antígeno tamponado (BPA) como prueba tamiz1 y luego la prueba de fluorescencia polarizada (FPA) como prueba confirmatoria. Los resultados de la FPA se obtuvieron en unidades de milipolarización (UmP)39. De acuerdo con los datos reportados por SENASA39, los bovinos se diagnosticaron como negativos cuando los valores fueron <94 UmP, sospechosos con valores entre 94 y 104 UmP y positivos con valores iguales o mayores de 105 UmP. Por otro lado, las muestras tomadas de caprinos fueron consideradas positivas cuando la prueba arrojó un valor igual o mayor de 85 UmP. De esta forma, una muestra se consideró positiva cuando ambas pruebas aplicadas en serie arrojaron resultados positivos.
Análisis estadístico e identificación de factores de riesgoLa cuantificación del grado de asociación entre los factores de riesgo identificados en la encuesta y la prevalencia de brucelosis en los rodeos (número de animales positivos/número total de animales muestreados) se realizó siguiendo la metodología epidemiológica clásica y ya aplicada en otros estudios epidemiológicos similares25. En una primera etapa, todas las variables independientes fueron comparadas con la presencia de brucelosis de manera individual empleando modelos lineales generalizados mixtos (MLGM) con distribución binomial, función de enlace logarítmico y rodeo como variable aleatoria15. Solo las variables asociadas con la variable dependiente luego del análisis univariado con un p <0,15 fueron ofrecidas, en una segunda etapa al MLGM con distribución binomial, función de enlace logarítmico y rodeo como variable aleatoria. Antes de realizar el análisis multivariado, se analizó la existencia de colinealidad, calculando la correlación entre pares de variables que expliquen situaciones similares, usando el coeficiente de correlación de Spearman o X2, dependiendo el tipo de variables. Cuando dos potenciales factores de riesgo se encontraron altamente correlacionados (coeficientes de correlación >0,6), solamente se ofreció al modelo multivariado aquella variable con menor valor de p en el modelo univariado. Se efectuó una selección de modelos tipo backward para seleccionar el más explicativo, quitando una por una las variables con mayor valor de significancia hasta que los coeficientes de regresión estimados para todas las variables del modelo tuvieran un p<0,05. Finalmente, las variables que fueron eliminadas al inicio del proceso fueron reintroducidas en el modelo y se eliminaron si el valor de significancia era >0,05 o la variación en los coeficientes estimados era menor del 20%9. Todos los análisis estadísticos fueron realizados empleando el programa Infostat (Universidad Nacional de Córdoba, Córdoba, Argentina).
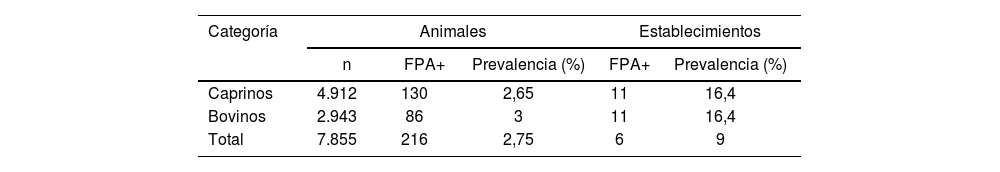
ResultadosSeroprevalencia de la enfermedadEn los establecimientos mixtos muestreados de Patiño y Bermejo, la prevalencia de brucelosis fue del 9% (IC 95%: 4-17%), considerando establecimiento positivo a todo aquel con al menos un bovino y un caprino positivo. Sin embargo, discriminando por especie, se obtuvo una prevalencia a nivel de rodeo del 16,4% (IC 95%: 9-25%), tanto para caprinos como para bovinos. Evaluando la prevalencia por animal, se obtuvo un 2,75% (IC 95%: 2,3-3,1%) de positividad de manera conjunta (caprinos-bovinos), 3% en bovinos (IC 95%: 2,3-3,5%) y 2,65% (IC 95%: 2,2-3,0%) en caprinos (tabla 1).
Prevalencia de brucelosis en bovinos y caprinos en sistemas productivos mixtos (n=67). Departamentos Patiño y Bermejo, provincia de Formosa (Argentina)*
| Categoría | Animales | Establecimientos | |||
|---|---|---|---|---|---|
| n | FPA+ | Prevalencia (%) | FPA+ | Prevalencia (%) | |
| Caprinos | 4.912 | 130 | 2,65 | 11 | 16,4 |
| Bovinos | 2.943 | 86 | 3 | 11 | 16,4 |
| Total | 7.855 | 216 | 2,75 | 6 | 9 |
FPA: prueba de fluorescencia polarizada.
A partir de la encuesta realizada a cada productor, surgieron 39 variables que fueron incluidas en el análisis univariado con el establecimiento como factor aleatorio (tabla 2). De acuerdo con el análisis univariado, la prevalencia de brucelosis se incrementa conforme aumenta la cantidad de animales existentes en los establecimientos, los cuales comparten fuentes de agua y pastorean frecuentemente de manera conjunta.
Resultados del análisis univariado (p <0,15)
| Variable | Niveles | Media | valor p |
|---|---|---|---|
| Tamaño del establecimiento | Mediano-grande | 0,06 | <0,001 |
| Pequeño | 0,01 | ||
| Producción simple | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Producción mixta | No | 0,03 | 0,212 |
| Sí | 0,02 | ||
| Pastoreo en conjunto | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Frecuencia de pastoreo | A veces | 0,01 | <0,001 |
| Nunca | 0,001 | ||
| Siempre | 0,05 | ||
| Comparten puntos de agua | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Tipo de bebedero | Estanque | 0,03 | <0,001 |
| Pozo | 0,01 | ||
| Río | 0,08 | ||
| Presencia de perros/gatos en el lugar | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Alambrado perimetral completo | No | 0,04 | <0,001 |
| Sí | 0,02 | ||
| Presencia de montes | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Acceso de animales silvestres al alimento | No | 0,03 | 0,364 |
| Sí | 0,03 | ||
| Acceso de animales silvestres al agua | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Ha realizado muestreo en caprinos | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Ha realizado muestreo en bovinos | No | 0,01 | <0,001 |
| Sí | 0,03 | ||
| Realiza vacunación | No | 0,05 | <0,001 |
| Sí | 0,02 | ||
| Animales positivos/sospechosos con signos reproductivos | No | 0,001 | <0,001 |
| Sí | 0,1 | ||
| Usa servicios veterinarios | No | 0,02 | 0,010 |
| Sí | 0,03 | ||
| Existen puntos de agua estancada | No | 0,03 | 0,549 |
| Sí | 0,03 | ||
| Bebederos/comederos con materia fecal | No | 0,03 | <0,001 |
| Sí | 0,001 | ||
| Drena la explotación a otra | No | 0,01 | <0,001 |
| Sí | 0,05 | ||
| Recibe drenaje de otra explotación | No | 0,01 | <0,001 |
| Sí | 0,05 | ||
| Usa estiércol como abono | No | 0,03 | <0,001 |
| Sí | 0,001 | ||
| Divide las cabras por categoría | No | 0,03 | <0,001 |
| Sí | 0,02 | ||
| Horas cabra/corral | 1 a 5 | 0,04 | <0,001 |
| 6 a 10 | 0,03 | ||
| más de 10 | 0,01 | ||
| Encontró abortos a término o nacidos débiles | No | 0,001 | <0,001 |
| Sí | 0,06 | ||
| Encontró restos de abortos/secundinas | No | 0,03 | <0,001 |
| Sí | 0,001 | ||
| Presencia de retención de placenta | No | 0,01 | <0,001 |
| Sí | 0,04 | ||
| Extraen la placenta | No | 0,02 | <0,001 |
| Sí | 0,05 | ||
| Destino de los abortos | Deja en el lugar | 0,06 | <0,001 |
| Lleva lejos | 0,03 | ||
| Aplica tratamientos previos, entierra o quema | 0,01 | ||
| Aíslan hembras próximas al parto | No | 0,02 | 0,074 |
| Sí | 0,03 | ||
| Intercambia reproductores | No | 0,03 | 0,689 |
| Sí | 0,03 | ||
| Ingresan animales de otra explotación | No | 0,01 | <0,001 |
| Sí | 0,04 | ||
| Ingresaron bovinos | No | 0,02 | <0,001 |
| Sí | 0,05 | ||
| Ingresaron caprinos | No | 0,04 | <0,001 |
| Sí | 0,001 | ||
| Realiza cuarentena (animales nuevos) | No | 0,04 | <0,001 |
| Sí | 0,001 | ||
| Los animales nuevos tenían certificado negativo a brucelosis | No | 0,04 | <0,001 |
| Sí | 0,001 | ||
| Elimina de inmediato animales positivos | No | 0,04 | <0,001 |
| Sí | 0,001 | ||
| Realiza reposición propia | No | 0,001 | <0,001 |
| Sí | 0,03 | ||
| Realiza controles al personal | No | 0,03 | <0,001 |
| Sí | 0,001 |
De igual manera, se refuerza la presencia de brucelosis cuando en los establecimientos no se desarrollan determinadas prácticas diarias como la recorrida de los potreros, lo que permite encontrar abortos o restos de ellos, placenta retenida o animales nacidos débiles; no se tienen presentes ciertas precauciones cuando ingresan animales, como solicitud de comprobante de seronegatividad y realización de la cuarentena correspondiente; o no se mantienen las medidas sanitarias como vacunar, tomar muestras periódicamente para el diagnóstico serológico, incluso aquellas referidas a movimientos o compra/venta de animales.
Otros puntos destacados son aquellos relacionados con las instalaciones y la geografía del establecimiento. A partir de estos resultados, se observa que la probabilidad de tener la enfermedad se incrementa cuando no es factible mantener el predio cerrado en su totalidad, lo que acarrea la posible circulación sin restricciones de animales domésticos de otros rodeos, así como la de animales silvestres cuya situación sanitaria se desconoce y quienes actúan como potenciales difusores del microorganismo. Adicionalmente, se incrementa la propagación del agente a través del curso que toman las aguas, ya sea porque se recibe el drenaje de predios vecinos o se drena hacia estos. Dado que el microorganismo tiene la particularidad de poder sobrevivir por periodos relativamente largos en el medio ambiente, esta situación sería preocupante cuando los rodeos vecinos son positivos a la enfermedad.
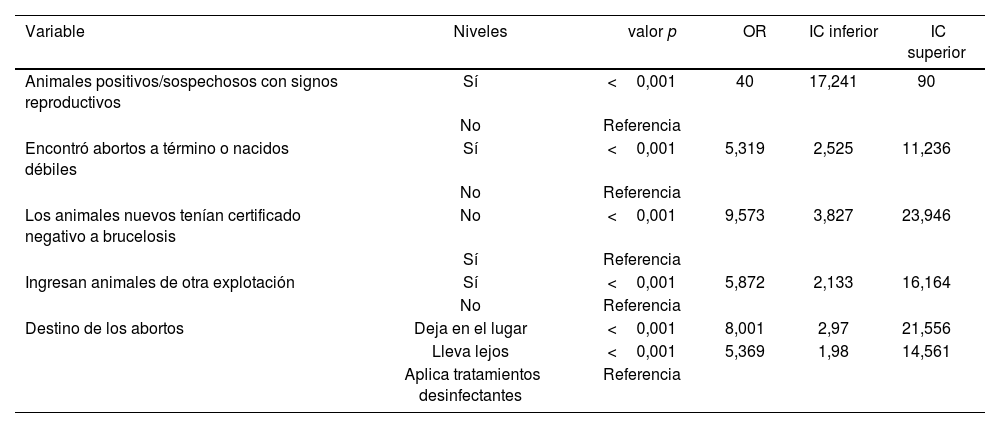
El modelo multivariado indica que la prevalencia de brucelosis en bovinos y caprinos está influenciada por la presencia de animales con signos reproductivos, presencia de abortos de edades gestacionales avanzadas o nacimiento de crías débiles, el tratamiento incorrecto de los abortos y el ingreso de animales desde otras explotaciones y sin certificado negativo de brucelosis (tabla 3).
Resultados del análisis multivariado (MLGM) p <0,05
| Variable | Niveles | valor p | OR | IC inferior | IC superior |
|---|---|---|---|---|---|
| Animales positivos/sospechosos con signos reproductivos | Sí | <0,001 | 40 | 17,241 | 90 |
| No | Referencia | ||||
| Encontró abortos a término o nacidos débiles | Sí | <0,001 | 5,319 | 2,525 | 11,236 |
| No | Referencia | ||||
| Los animales nuevos tenían certificado negativo a brucelosis | No | <0,001 | 9,573 | 3,827 | 23,946 |
| Sí | Referencia | ||||
| Ingresan animales de otra explotación | Sí | <0,001 | 5,872 | 2,133 | 16,164 |
| No | Referencia | ||||
| Destino de los abortos | Deja en el lugar | <0,001 | 8,001 | 2,97 | 21,556 |
| Lleva lejos | <0,001 | 5,369 | 1,98 | 14,561 | |
| Aplica tratamientos desinfectantes | Referencia |
IC: intervalo de confianza; MLGM: modelos lineales generalizados mixtos; OR: odds ratio.
Aquellos establecimientos que manifestaron tener problemas reproductivos tuvieron una probabilidad 40 veces mayor de tener brucelosis en su rodeo que aquellos donde no se reportó la presencia de animales con signos reproductivos. Además, el hecho de encontrar abortos o restos de estos, así como animales nacidos débiles, supone una probabilidad 5,3 veces mayor de tener brucelosis respecto de aquellos establecimientos en los que no se ha dado esta situación.
Es importante destacar que el destino que se les asigna a los abortos encontrados desempeñaría un papel importante, con mayor probabilidad de tener la enfermedad en aquellos predios en donde los dejan en el lugar (ocho veces mayor) o los llevan a un lugar alejado (5,4 veces mayor) que en los establecimientos que realizan algún tipo de práctica, como la quema, la desinfección o el enterrado de los abortos o secundinas encontrados.
Por otro lado, el ingreso de animales nuevos sin certificado negativo de brucelosis tuvo una probabilidad 9,6 veces mayor de tener la enfermedad en comparación con aquellos predios en los que sí se exige una certificación negativa de la enfermedad con los ingresos de animales. Además, existe una probabilidad 5,9 veces mayor de tener brucelosis cuando se permite el ingreso al predio de animales externos o no se refuerzan los controles para evitar esta situación.
DiscusiónLa producción pecuaria se ve afectada permanentemente por enfermedades de origen infeccioso que influyen negativamente en la reproducción, algunas de ellas son zoonóticas y provocan, además, problemas de salud pública12. Estas enfermedades interfieren en el buen desempeño productivo y reproductivo del ganado, lo que ocasiona enormes pérdidas económicas. En determinadas situaciones, incluso actúan como una barrera potencial para el comercio internacional de animales y de sus productos3,18,44. La brucelosis, en particular, lleva años siendo estudiada y se han establecido programas para su control y erradicación. No obstante, en muchas regiones la frecuencia de presentación se mantiene constante, constituyéndose en una endemia11,42.
En este estudio, la prevalencia estimada de brucelosis en rodeos mixtos de dos departamentos de Formosa fue inferior a la reportada en estudios previos efectuados en la misma zona16,33,38, probablemente por la condición de tener que presentar al menos un individuo positivo de cada especie para que el establecimiento fuese considerado positivo. Cabe destacar que los estudios citados fueron realizados en establecimientos bovinos y caprinos en forma separada, y que no hay datos de prevalencia de brucelosis de manera conjunta, tal como se describe en el presente trabajo. A pesar de ello, al determinar la prevalencia por especie, se observaron valores superiores a los reportados anteriormente. Esto podría deberse a la falta de controles periódicos en la zona (a pesar de la obligatoriedad de muestrear bovinos impuesta por entes nacionales), lo que lleva a que animales positivos permanezcan en los predios por tiempo indeterminado, constituyéndose en una fuente de infección tanto en rodeos mixtos como en aquellos de una sola especie.
La presencia de animales con signos reproductivos incrementa el riesgo de que los rodeos presenten bovinos y caprinos positivos a brucelosis. Esto es esperable, ya que las hembras, luego de abortar o incluso en ausencia de abortos, eliminan masivamente microorganismos a partir de la placenta, los líquidos o las membranas fetales, las secreciones vaginales y a través de la glándula mamaria6,28. De esa forma, estarían eliminando constantemente el agente responsable al medio, lo que predispondría al contagio de animales negativos, por lo que es imprescindible eliminar de manera inmediata todo bovino o caprino afectado para así poder disminuir el riesgo de infección7,24.
Asociado a lo anterior, encontrar abortos o animales nacidos débiles incrementa el riesgo de brucelosis en los rodeos mixtos, dado que, posiblemente, estos se constituyen en un foco de infección continuo. La presencia de estos signos nos demuestra que la enfermedad se perpetúa y que la infección uterina y mamaria permanecen. Adicionalmente, los productos del parto y la leche también contienen microorganismos que son eliminados al ambiente y se mantienen por largos periodos en el suelo y la materia fecal (80 días), e incluso mucho más tiempo (seis a ocho meses) en los productos del aborto14,23. En definitiva, a pesar de tratarse de una bacteria no esporulada, la resistencia de Brucella a los agentes físicoquímicos y su viabilidad en el medio ambiente pueden calificarse como considerables, si bien estas dependen de factores tales como la temperatura, la humedad y la presencia de materia orgánica13.
Ligado con lo anterior, dejar el feto y las membranas fetales en el mismo lugar donde se produjo el aborto o incluso transportarlos a un lugar más alejado incrementan el riesgo de que los establecimientos sean positivos a brucelosis. No aplicar algún tratamiento desinfectante en los productos del aborto o no eliminarlos de manera segura predispone aún más a la diseminación de microorganismos en el ambiente y, consecuentemente, incrementa el riesgo de transmisión hacia individuos susceptibles36.
Se ha documentado que los perros, los gatos y otros carnívoros salvajes, como los zorros, pueden ser importantes diseminadores mecánicos de la infección, transportando material infectado (fetos o restos de placenta procedentes de abortos) por diferentes zonas del establecimiento, esparciendo eficientemente el agente causal y con ello incrementando la tasa de diseminación del patógeno11. Si no existen medidas de protección, la presencia de estos animales en las proximidades de los rodeos afectados por la enfermedad o de las zonas de enterramiento de animales enfermos sacrificados puede incrementar los riesgos de transmisión del agente patógeno13.
En coincidencia con Vanzini et al.43, consideramos que la vigilancia epidemiológica de los rodeos debería reforzarse, no solo realizando muestreos sistemáticos para identificar posibles focos, sino también asegurando que los animales que ingresan al rodeo sean negativos o, si no cumplen esta condición, que permanezcan en cuarentena hasta la obtención de los resultados de sus respectivos análisis. Estas consideraciones se encuentran descritas en el Plan Nacional de Control y Erradicación de la Brucelosis, donde, a su vez, se nombra la Determinación Obligatoria del Estatus Sanitario (DOES)40.
Sin embargo, gran parte de los establecimientos no llevan a cabo las pautas establecidas. En ocasiones, se adjudica este comportamiento a cuestiones económicas. En este sentido, cabe advertir que probablemente debido al desconocimiento, los productores no notan los beneficios que conlleva lograr un rodeo libre y, por el contrario, las pérdidas que ocasiona el continuar con animales positivos o de situación desconocida frente a la enfermedad5. Todo propietario debería exigir animales serológicamente negativos o evitar el ingreso de animales con serología desconocida, ya que solo de esta manera podría proteger a su rodeo de posibles brotes y evitaría el ingreso de la enfermedad a su establecimiento. Frente a los brotes, no solo se afecta la producción, sino que también quedan expuestas las poblaciones de riesgo32,35,43.
Similar situación se produce con el ingreso no intencional de animales de otra explotación, al desconocerse su estatus sanitario. Como se pudo observar en este estudio, en predios donde la cría es extensiva, los alambrados perimetrales muchas veces no se encuentran en condiciones adecuadas, lo que hace que los animales recorran no solo el predio de su propietario sino también los predios vecinos, y esto es difícil de controlar. Tal como afirma Díaz14, es común que se compartan pasturas y aguadas entre animales de distintos rodeos, que luego regresan a sus potreros o corrales. Esta mezcla podría influir en los rodeos libres complicando el control de la enfermedad.
Franc et al.19 han señalado que la enfermedad tiende a permanecer en un rodeo por las prácticas de cría de diferentes especies animales compartiendo pasturas y bebederos. Sin embargo, en este estudio, las variables que hacen referencia a ese tipo de manejo no arrojaron resultados significativos. Probablemente esto se deba a que la mayoría de los animales bovinos no permanecen en un predio determinado, no se presenta la convivencia de manera constante ni existe hacinamiento en esta especie. Lo contrario ocurre en las cabras, que a menudo son contenidas durante toda la noche en corrales de dimensiones pequeñas, es decir, es común que en un mismo predio estas especies sean criadas de manera muy distinta y en estrecho contacto con sus propietarios.
Lo anterior acarrea un gran riesgo para la salud de los productores debido a su condición de enfermedad zoonótica. La brucelosis es un problema de salud común entre las personas que de forma constante están en relación estrecha con el ganado o incluso en aquellas que viven en zonas rurales45,46. La infección en humanos podría presentarse por el contacto con secreciones de animales infectados, traslado de fetos abortados o consumo de leche cruda o queso contaminado. Estas actividades son habituales en la zona bajo estudio, ya que son las familias las encargadas del manejo de los animales y suelen estar en estrecho contacto con ellos todo el tiempo, criándolos en condiciones de subsistencia, en su mayoría10,34. La bacteria podría ingresar al organismo a través de las vías respiratorias o de lesiones en la piel mientras se manipulan animales infectados o sus desechos30,37. De esa forma, la enfermedad puede ser adquirida por los propietarios de los animales cuando realizan prácticas diarias o durante la exposición ocupacional de los trabajadores de mataderos, carniceros y veterinarios4,17.
Sumado a lo anterior, los propietarios dedicados a la cría de animales a pequeña escala presentan el hábito de comercializar productos artesanales derivados de la leche (quesillos) sin tener en cuenta la práctica de pasteurización. Además, suelen faenar los animales sin los debidos controles sanitarios siendo esta una de las rutas más comunes de transmisión21.
ConclusiónA través de este estudio fue posible identificar factores involucrados en la permanencia de la enfermedad en los rodeos, y son estos factores una pieza fundamental en la elaboración de estrategias de manejo del riesgo basadas en ciencia. Se pudo demostrar la importancia que reviste el manejo de los animales en cada establecimiento, en especial, la toma de medidas preventivas con respecto a los ingresos o movimientos de animales, así como también en lo referido a prácticas de sanitización de los corrales y medidas de prevención por parte de los operarios. Uno de los puntos fundamentales es la eliminación inmediata de todo animal positivo a brucelosis, así como el control epidemiológico continuo.
Es necesario reforzar el compromiso constante de los entes sanitarios nacionales y provinciales para incentivar el control de la brucelosis, ya que existe un gran desconocimiento por parte de los productores debido a la falta de información y asesoramiento. Sin dudas, esto es un trabajo que necesita del compromiso de todos los ejes involucrados para lograr resultados reales y visibles, cuidando no solo de la ganadería, sino también de la salud pública.
FinanciaciónLos análisis de laboratorio realizados en este estudio fueron financiados con fondos provenientes del Centro de Investigaciones y Transferencia (CIT Formosa).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.