El número y la complejidad de los procedimientos de diagnóstico e intervencionismo cardiovascular han incrementado de manera significativa, hecho que genera mayor exposición a dosis bajas de radiación ionizante debido a la radiación dispersa por el paciente. El cristalino es una de las estructuras más sensibles a la radiación y las cataratas son la enfermedad ocular más estudiada y frecuente en el personal de la salud ocupacionalmente expuesto a dosis bajas de radiación.
La formación de cataratas es un proceso multifactorial y la exposición a la radiación ionizante se ha asociado a opacidades subcapsulares posteriores, que es la forma más común de lesión, seguida por las cataratas corticales.
Existen varios estudios que han evaluado los efectos de la exposición ocupacional por radiación ionizante en el cristalino en cardiólogos intervencionistas, comparándolos con controles no expuestos. Concluyen que hay mayor prevalencia de opacidades subcapsulares posteriores en el personal expuesto a radiación ionizante, especialmente en los cardiólogos intervencionistas (por trabajar muy cerca del generador de rayos X), las cuales están relacionadas con la duración de la práctica del intervencionismo cardíaco y disminuyen con el uso regular de los lentes plomados.
Lo llamativo de muchos estudios es el bajo uso por parte de los cardiólogos intervencionistas de los elementos de protección radiológica, especialmente gafas y mampara plomada, las cuales han demostrado efectividad en la reducción de la radiación ionizante recibida por el personal de la sala de cateterismo cardiaco.
As the number and complexity of diagnostic and cardiovascular intervention procedures has increased significantly, this has led to a greater exposure to low doses of ionising radiation due to the radiation dispersal by the patient. The crystalline lens is one of the structures most sensitive to radiation, and cataracts are the most studied eye disease, and are common in health staff occupationally exposed to low radiation doses.
The formation of cataracts is a process involving many factors, and exposure to ionising radiation has been associated with posterior sub-capsular opacities, the most common form of the injury, followed by cortical cataracts.
There are several studies that have evaluated the effects of occupational exposure due to ionising radiation in the crystalline lens in interventionist cardiologists, and comparing them with non-exposed controls. They conclude that there is a higher prevalence of posterior sub-capsular opacities in personnel exposed to ionising radiation, especially in interventionist cardiologists (due to working very near the X-ray generator). These are associated with the duration of the practice of cardiac interventions, and decrease with the regular use of leaded glasses.
The low use of radiation protection wear by interventionist cardiologists is highlighted in many studies, especially glasses and a leaded screen, which have shown to be effective in the reduction in the ionising radiation by the staff in the cardiac catheterisation room.
En las últimas décadas el número y la complejidad de los procedimientos de diagnóstico e intervencionismo cardiovascular han incrementado de manera significativa, lo cual genera mayor exposición a dosis bajas de radiación ionizante tanto para el cardiólogo intervencionista como para el personal de la sala de cateterismo, siendo el origen de esta la radiación dispersa por el paciente durante los diferentes procedimientos.
La exposición a radiación ionizante ha sido asociada a un incremento en el riesgo de varias enfermedades oftalmológicas, como tumores malignos de párpados y anexos (carcinoma de células basales, escamosas y sebáceas), neoplasia conjuntival de células escamosas, neoplasia corneal intraepitelial y daño en la retina. Sin embargo, debido a que el cristalino es una de las estructuras más sensibles a la radiación y a que las cataratas son la enfermedad más estudiada y frecuente en el personal de la salud ocupacionalmente expuesto a dosis bajas de radiación, este será el foco de esta revisión1.
Las cataratas se definen como una opacidad en el lente del ojo, el cristalino. Los cambios en la transparencia y el índice refractivo llevan a diferentes niveles de deterioro visual, el cual está asociado con disminución en la calidad de vida debido a que restringe la capacidad de realizar las actividades cotidianas y ser independiente, incrementando el riesgo de accidentes y caídas. Las cataratas seniles o relacionadas con la edad son la forma más común. En los Estados Unidos la incidencia de cataratas a los 65 y 89 años es del 25 y del 70%, respectivamente, con niveles más altos en mujeres en comparación con los hombres2.
De acuerdo con el área de la lente afectada pueden clasificarse en tres grupos diferentes:
- •
Nuclear
- •
Cortical
- •
Subcapsular posterior
La formación de cataratas es un proceso multifactorial y pueden ser causadas por factores genéticos, trauma, inflamación, desórdenes metabólicos (síndrome metabólico, diabetes mellitus tipo 2) o nutricionales (obesidad o malnutrición) y exposición a la radiación (ionizante y ultravioleta B). Adicionalmente, factores de riesgo como el tabaquismo, la alta ingesta de alcohol y el uso crónico de esteroides sistémicos incrementan la probabilidad de su aparición. Las opacidades subcapsulares posteriores son la forma más común de lesión en el cristalino por radiación ionizante, seguida por las cataratas corticales1.
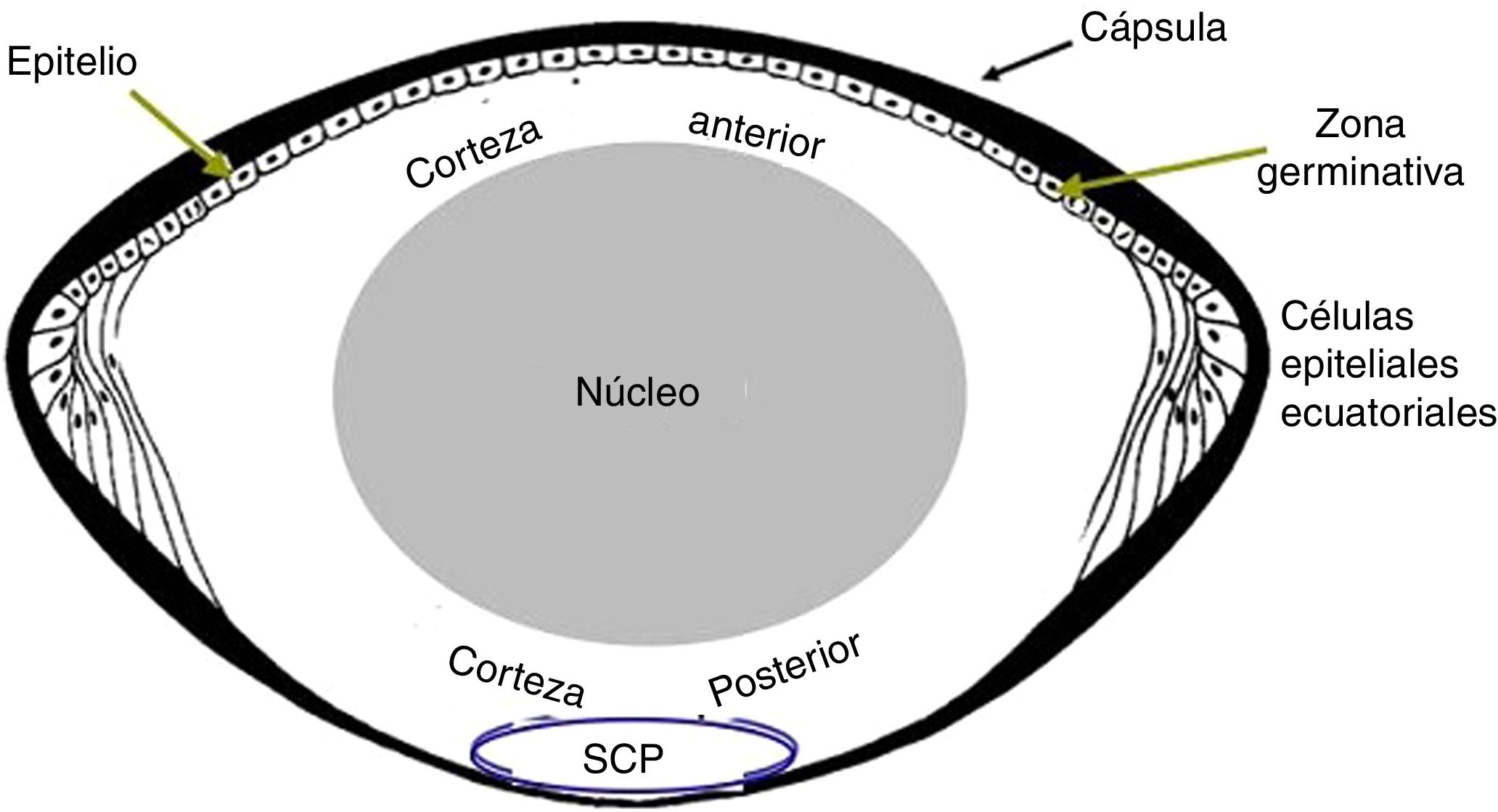
Patogénesis de las cataratas inducidas por radiación2El cristalino es un lente transparente, incoloro, flexible y sin vasos sanguíneos, formado por células alargadas (fibras) y rodeado por una cápsula de colágeno, debajo de la cual y en su porción anterior descansan las células epiteliales (zona germinativa), que migran lateralmente hacia la zona del Ecuador donde se elongan y pierden sus organelas (por ejemplo las mitocondrias) para diferenciarse en células de fibra del lente. A medida que se forman las fibras del cristalino, las fibras circundantes dan lugar a la corteza y las más centrales se compactan para originar el núcleo. Estas fibras del lente continúan produciéndose durante toda la vida (fig. 1).
Las cataratas nucleares y corticales se desarrollan por cambios patológicos en las células de fibra del cristalino, mientras que las subcapsulares posteriores se asocian con anormalidades en la zona germinativa2. La patogénesis de las cataratas inducidas por radiación no se entiende por completo. Sin embargo, es claro que es un proceso multifactorial con factores genéticos y ambientales asociados, y han sido clasificadas como una reacción tisular (antes llamado efecto determinístico).
El principal mecanismo propuesto para las cataratas subcapsulares posteriores es el daño por radiación del proceso de división de las células germinativas, el cual induce un corto período de inhibición mitótica en la membrana basal seguido por una sobrecompensación con mitosis anormal y desorganizada. Esto trae como resultado la acumulación de células de fibra del lente aberrantemente organizadas con núcleos picnóticos que, en teoría, producen cuerpos lentoides turbios o nubados en la región subcapsular posterior. Estas alteraciones se manifiestan histológicamente como puntos y vacuolas de opacificación las cuales se fusionan, formando grandes conglomerados que son los responsables de las opacidades y en muchos casos de las cataratas inducidas por radiación ionizante.
Las células epiteliales del cristalino expresan al menos 92 genes específicos para reparar el ADN y hay evidencia que aberraciones en los genes involucrados en las interacciones intercelulares, inflamación, supresión de tumores, reparación de la escisión de nucleótidos y del ADN de doble cadena pueden afectar el desarrollo de cataratas por radiación ionizante a baja dosis. Estos estudios sugieren un efecto estocástico en la generación de cataratas por radiación (lineal, sin umbral). Aunque este concepto no ha sido probado, en un estudio de cohorte, prospectivo con encuestas enviadas por correo electrónico a tecnólogos de radiología en los Estados Unidos. De los 67.246 tecnólogos elegibles que respondieron las encuestas,12.336 (18%) reportaron antecedentes de diagnóstico de cataratas, con un seguimiento promedio acumulado de la dosis de exposición ocupacional a radiación, de 5 años.
En este estudio se encontró evidencia de exceso de riesgo de cataratas a una dosis absorbida por el cristalino menor a 100 mGy. Este estudio de exposición a radiación a bajas dosis y baja tasa de dosis sugiere que hay un efecto lineal, pero sin umbral para las cataratas inducidas por radiación3.
De acuerdo con la dosis, el tiempo de exposición y un período de latencia variable, la exposición a radiación ionizante produce opacidades en el cristalino; el umbral para el desarrollo de cataratas tanto en la exposición aguda como crónica ha sido establecido en es de 0,5 Gy. Adicionalmente, la sensibilidad del cristalino a la radiación es mayor en las personas jóvenes y en las mujeres, y a mayor dosis de exposición a la radiación menos latencia en la aparición de las opacidades y finalmente de las cataratas4.
¿Cuál es la evidencia de la relación entre cataratas y radiación ionizante?La génesis de las cataratas por radiación ionizante ha sido descrita en animales experimentales desde 1897 y en humanos desde 1903. Las cataratas observadas en los sobrevivientes de la bomba atómica y en trabajadores de ciclotrón despertaron el interés en la evaluación y protección del cristalino, y en 1959 la comisión internacional de protección radiológica o ICRP (su sigla en inglés por International Commission on Radiological Protection) catalogó las cataratas como efecto de la radiación ionizante y dio recomendaciones para establecer un límite a la exposición a la misma. Posteriormente, dicha entidad clasificó el efecto de la radiación ionizante en el cristalino como determinístico, posteriormente, en 2007, como reacción tisular, y luego en el 2011 actualizó las recomendaciones de la dosis umbral para inducción de cataratas a 0,5Gy durante toda la vida, y la dosis equivalente límite por exposición ocupacional a 20 mSv/año (100 mSv en un período de 5 años, sin exceder más de 50 mSv en un solo año). Este nuevo umbral de 0,5Gy es independiente de la dosis de radiación recibida y la severidad de la opacificación; así, el concepto del umbral se explica como una exposición a 0,5Gy de baja transferencia lineal de energía (LET) que induce opacidades menores en 1% de los individuos expuestos a más de 20 años, las cuales progresan a cataratas5.
Existen varios estudios prospectivos, observacionales, de casos y controles (personal no expuesto) y metaanálisis que han evaluado los efectos de la exposición ocupacional por radiación ionizante en el cristalino en cardiólogos intervencionistas, comparándolos con controles no expuestos. Se han utilizado dos escalas diferentes para la clasificación de las opacidades del cristalino: la LOCS III y la modificada de Merriam-Focht Scale (MFS)5,6.
En 2017, Elmaraezy7 publicó una revisión sistemática y metaanálisis del riesgo de cataratas en cardiólogos intervencionistas. Evaluó 8 estudios realizados entre el 2010 y 2015 con 2.559 cardiólogos intervencionistas, enfermeros y técnicos, y sujetos no expuestos (1.224 cardiólogos intervencionistas expuestos) con 5 a más de 20 años de trabajo en salas de cateterismo cardíaco. Encontró que el riesgo relativo para opacidades subcapsulares posteriores en relación con el grupo control fue de 3,21; 95% cardiólogos intervencionistas [2,14 - 4,83], p <0,00001, sin diferencias entre ambos grupos para opacidades corticales o nucleares. Lo interesante de este metaanálisis es que, de manera global, no hubo relación entre el tiempo de exposición y el desarrollo de las opacidades del cristalino. Un segundo aspecto fue el bajo uso de gafas plomadas entre los cardiólogos intervencionistas, que en los estudios reportados fue del 13 y 18%, y en el análisis multivariado el uso frecuente de las gafas plomadas confirió protección para el desarrollo de opacidades subcapsulares posteriores. Solo un estudio del metaanálisis concluyó que las opacidades del cristalino estuvieron asociadas con la duración de la exposición y la falta de uso de medidas de protección. Así, los cardiólogos intervencionistas, con más de 25 años de trabajo y que usaron las gafas plomadas menos del 75% del tiempo, tenían cerca de seis veces más de riesgo de presentarlas.
El estudio francés, O’CLOC (Occupational Cataracts and Lens Opacities in Interventional Cardiology) el cual incluyó 106 cardiólogos intervencionistas y 99 controles no expuestos, encontró resultados similares al metaanálisis de Elmaraezy, sin diferencias en opacidades nucleares o corticales, y una mayor prevalencia de opacidades subcapsulares posteriores en cardiólogos intervencionistas comparados con los expuestos (17% vs. 5%, p=0,006), OR=3,9 [1,3 - 11,4]. Esta mayor prevalencia está relacionada con la duración de la práctica del intervencionismo cardíaco y disminuye con el uso regular de los lentes plomados8.
Existen tres estudios9–11 en los que la evaluación de los cardiólogos intervencionistas y los sujetos de control no expuesto se realizaron durante los congresos de la especialidad. Estos son: RELID (The International Retrospective Evaluation of Lens Injuries and Dose) que evaluó un grupo de cardiólogos intervencionistas durante el congreso de la Sociedad Latinoamericana de Cardiología Intervencionista (SOLACI) en 2008 en Bogotá y en el 2010 y 2014 en Argentina; el IC-CATARACT (CAtaracts ARtributed to RAdiation in the CaTh Lab) en el congreso de la Society for Cardiovascular Angiology and Interventions (SCAI) en Orlando, Florida, y un último estudio realizado en la ciudad de Bogotá durante el congreso del Colegio Colombiano de Hemodinamia e Intervencionismo Cardiovascular y las jornadas del SOLACI en el año 2017.
En los tres estudios las evaluaciones del personal expuesto y de control fueron hechas por 1 a 3 oftalmólogos ciegos al estado de exposición del sujeto, y la clasificación de las opacidades se realizó con la escala modificada de Merriam-Focht Scale (MFS) iniciando en 0, y con incrementos de 0,5 hasta 4. En el estudio RELID9 se incluyeron 116 sujetos, 58 cardiólogos intervencionistas, 58 técnicos de rayos X y enfermeras, en tanto que el grupo control estuvo conformado por 93 voluntarios no expuestos evaluados en las cohortes de Bogotá y Montevideo en 2008 y 2009. La prevalencia de opacidades subcapsulares posterior fue del 38% en los cardiólogos intervencionistas (p <0,005 RR: 3,2 95% IC 1,7-6,1) y del 21% en los técnicos y enfermeras (p 0,13 RR: 1,7 95% IC 0,8-3,7), comparados con 12% en los sujetos no expuestos. En conclusión, en ausencia de otro factor de riesgo conocido para catarata subcapsular posterior hay una prevalencia tres veces mayor en los cardiólogos intervencionistas comparado con los sujetos no expuestos, y combinado con un promedio acumulativo de exposición del cristalino a los rayos X (evaluado de forma retrospectiva) mayor a 6Sv sugiere fuertemente una relación causal con la exposición a radiación ionizante. En este estudio se documentó bajo uso de los elementos de protección en el grupo con opacidades tanto de los lentes plomados como de la pantalla o mampara plomada9.
En el estudio IC-CATARACT10 se evaluaron 99 sujetos expuestos a radiación ionizante y 18 controles no expuestos. Llama la atención la distribución de la localización de las opacidades en la población expuesta; la más frecuente fue la cortical en 37%, seguida por la nuclear en un 13% y por último la subcapsular posterior en el 12%. La prevalencia de opacidades corticales/subcapsulares posteriores fue más frecuente en los expuestos en 47% vs. los no expuestos en 17%, p 0,015. La exposición ocupacional y la edad mayor de 60 años fueron los predictores independientes de los cambios en el cristalino OR (95% IC): 6,07 (1,38 - 43,45) y 7,72 (1,60 - 43,34) respectivamente; la mayor parte de los cambios ocurrió en la periferia del cristalino y no tuvo impacto en la agudeza visual10.
Finalmente, en el estudio realizado por el colegio colombiano de Hemodinamia con la Fundación Oftalmológica Nacional en el xiii Congreso de Cardiología Intervencionista y Conferencia SOLACI 201711, se evaluaron 89 sujetos, 58 ocupacionalmente expuestos (51,7% cardiólogos intervencionistas, 31% técnicos y 8,6% enfermeras) y 31 controles no expuestos. La prevalencia de opacidades subcapsulares posteriores en los expuestos fue del 30,3% vs. 21% en los no expuestos p 0,008. Los expuestos tenían el doble de riesgo de presentar opacidades subcapsulares posteriores (OR 2,49, IC 1,14 - 5,23). Una mayor edad, una vida media laboral más larga y el ser médicos (cardiólogos intervencionistas) se asociaron con mayor frecuencia de opacidades en el cristalino con una p 0,001 en las tres variables. En este estudio el personal expuesto no médico (técnicos y enfermeras) no se asoció con mayor prevalencia de opacidades del cristalino, contrario a otros estudios ya presentados en esta revisión, lo que confirma la mayor exposición a radiación ionizante de los cardiólogos intervencionistas debido a su trabajo muy cerca del generador de rayos X. Finalmente, en las medidas de protección el uso de las gafas plomadas fue del 69%, pero de la mampara plomada solo del 2%, punto que será discutido en los siguientes párrafos, dada su importancia en la disminución de la exposición a radiación ionizante11.
Elementos de radioprotecciónEl principal origen de la radiación en la sala de cateterismo cardiaco es el paciente, en quien inciden los rayos X y son dispersados de una manera no uniforme hacia el personal presente en el lugar. Los elementos básicos para la protección de la radiación ionizante son: delantal plomado, idealmente de 2 piezas (70% del peso en la cadera y 30% en los hombros), cuello de protección tiroidea (0,5mm de plomo equivalente), gafas plomadas (0,75mm de plomo equivalente y 0,5mm lateral) y escudo plomado transparente de dos componentes (0,5mm de plomo equivalente); recientemente se ha sugerido la utilización adicional de gorro, pantorrilleras, hombrera izquierda plomada y campos estériles blindados12.
Para reducir las opacidades en el cristalino existen varios elementos de protección que se describen a continuación.
Lentes o gafas plomados. Los modelos actuales ofrecen una protección de 0,75mm plomo equivalente frontal y 0,5mm lateral (algunos modelos). El factor de reducción de la dosis de radiación de los lentes plomados en el cristalino,en los modelos experimentales es de 10, la cual es incompleta y depende de la posición del intervencionista en relación al paciente y al tubo de rayos x, y a lo ajustado de los lentes plomados al contorno de la cara. Así, si el intervencionista está al lado derecho del paciente ofrecen mayor protección al ojo izquierdo que es más expuesto, y poca o ninguna, de acuerdo con algunos estudios con modelos experimentales, al ojo derecho. Y en los lentes panorámicos no ajustados a la cara, protegen de la radiación dispersa que incide de frente y no de la que incide de manera oblicua o tangencial en la cara. En los estudios clínicos realizados en la sala de cateterismo cardíaco el factor de reducción de la dosis va de 1,1 a 3,4 en el ojo más cercano al tubo de rayos X (izquierdo) y en un factor de 2,3 hasta 4,8 en el ojo contralateral, que depende del modelo de lente plomado; es mayor la protección para los modelos que se ajustan más estrechamente a la cara del cardiólogo intervencionista (los modelos deportivos o sportwrap y los goggle que tienen protección lateral) y con protección lateral12,13.
Campos estériles blindados y desechables. Son campos de tungsteno y antimonio, o bismuto y antimonio, 0,25mm de plomo equivalente, estériles, que se colocan en posición craneal al sitio de acceso femoral y caudal a la mampara plomada suspendida del techo. El factor de reducción de la dosis de radiación al cristalino de los campos blindados en los modelos experimentales es de 5 a 25, y cuando se usa de manera simultánea con los lentes plomados es de 25 o más (hasta 132). En este mismo estudio experimental se evaluó la utilidad de la mampara o pantalla plomada suspendida del techo para reducir la dosis de radiación al cristalino encontrando dosis no detectables cuando la mampara se utilizó como única barrera de radioprotección durante la fluoroscopia; así mismo, obtuvo la mayor reducción de la dosis de radiación del cristalino en sustracción digital, lo que confirma los hallazgos en los estudios clínicos en los que el factor de reducción de dosis del cristalino de la mampara es de 2,5 a 2,8 y es uno de los elementos de protección radiológica indispensables en la sala de cateterismo cardiaco para la protección, no solo al cristalino sino de todo el staff involucrado, como se describe a continuación12–14.
El acceso radial ha incrementado su uso de manera significativa (en algunos países más del 90%) por menos complicaciones, en particular de sangrado en comparación con el acceso femoral. Inicialmente se documentó mayor exposición a radiación ionizante, pero en estudios posteriores se demostró que dicha exposición está relacionada con la curva de aprendizaje de la técnica radial, que disminuye con una adecuada curva de entrenamiento a valores semejantes en algunos estudios al obtenido en el acceso femoral16. El uso de campos estériles con protección plomo-equivalente en pacientes sometidos a acceso radial se ha evaluado mediante campos en el brazo y la muñeca del paciente apoyado en el tórax o un panel plomado, entre la axila y la cintura en acceso radial derecho, y con protectores plomados en la pelvis. En el estudio en el que se usaron campos plomo equivalentes en brazo derecho y tórax de paciente, con dosímetros colocados en tórax, ojo izquierdo, tiroides y muñeca izquierda del operador se demostró una reducción del 13,5% (ojo izquierdo) a 34,2% (muñeca izquierda) de la dosis de radiación recibida con relación a la no protección. Al usar protectores plomados en la pelvis del paciente y comparar ambas vías de acceso se encontró una reducción significativa en estas últimas (p <0,0001 en ambas), pero con mayores dosis totales de radiación en el acceso radial.
Uso de la mampara en Cardiología IntervencionistaEn cardiología intervencionista, específicamente en los procedimientos de intervención coronaria, existen dos factores adicionales que incrementan la exposición; el primero es el mayor uso de cine, que equivale a diez veces más exposición comparado con la fluoroscopia; el segundo es la utilización de diferentes proyecciones para evaluar la anatomía coronaria, especialmente en las proyecciones oblicuas (más la izquierda) que incrementan la cantidad de radiación dispersa hacia el operador.
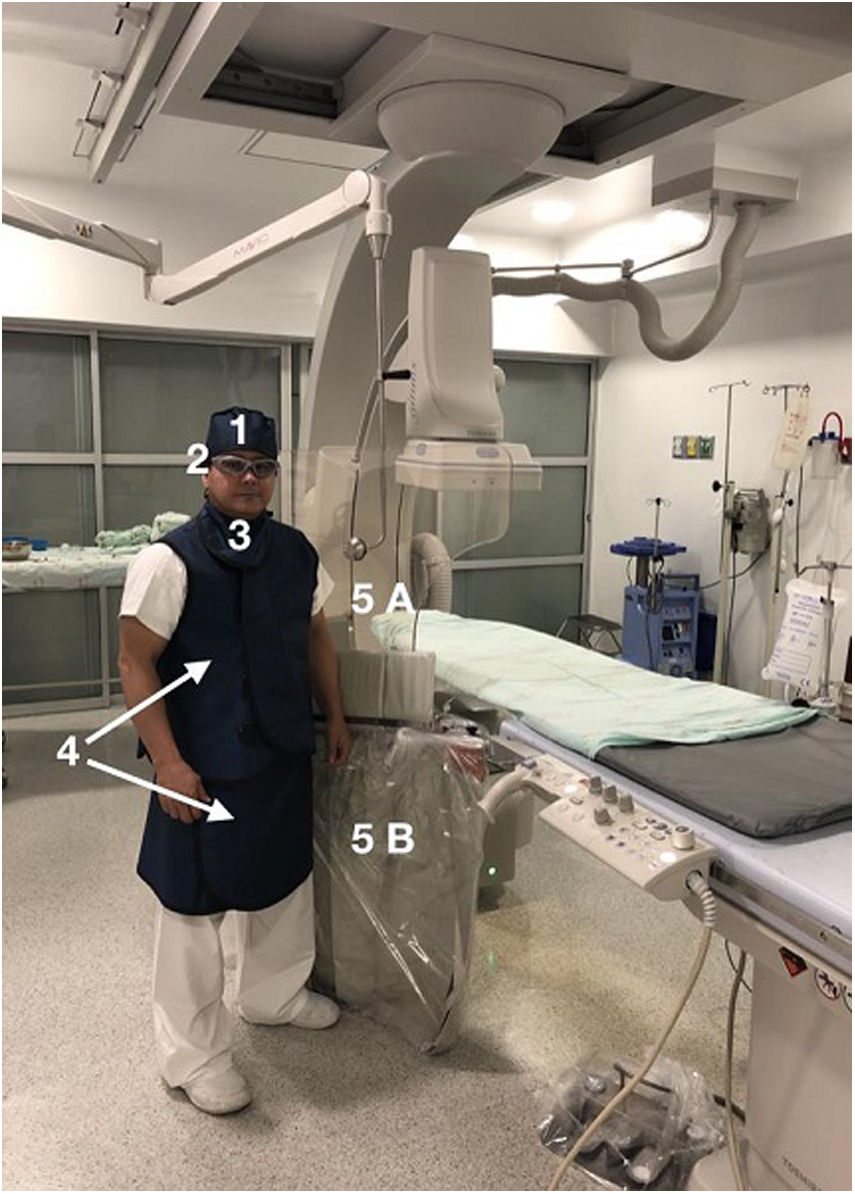
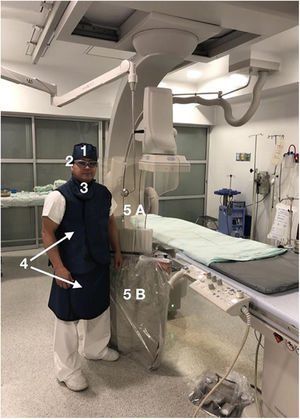
Adicional a los implementos de protección personal durante los procedimientos con rayos X, como delantal, cuello de protección tiroidea, casco y gafas plomadas, es fundamental el uso de escudos plomados (0,5mm plomo equivalente) durante todos los procedimientos de Cardiología intervencionista (fig. 2).
Elementos de radioprotección: 1. Gorro plomado 2. Lentes plomados con adecuado ajuste a la cara del intervencionista 3. Cuello de protección de tiroides 4. Delantal plomado de dos piezas, 5. Mampara plomada con dos componentes: A. Suspendida de techo y B. Escudo montado en la mesa con extensión vertical. Durante las intervenciones la mampara se debe mantener los más cerca posible al operador.
Para obtener una protección adecuada con la mampara o escudo plomado, este debe tener dos componentes, con 0,5mm plomo equivalente y una superposición de 10cm:
- 1.
Pantalla plomada suspendida del techo.
- 2.
Escudo plomado de la parte inferior del cuerpo (montado en la mesa de angiografía), el cual tiene una extensión vertical que sobrepasa 30cm la altura de la mesa de angiografía.
Ambos componentes deben usarse de manera simultánea para que haya protección contra la radiación dispersa.
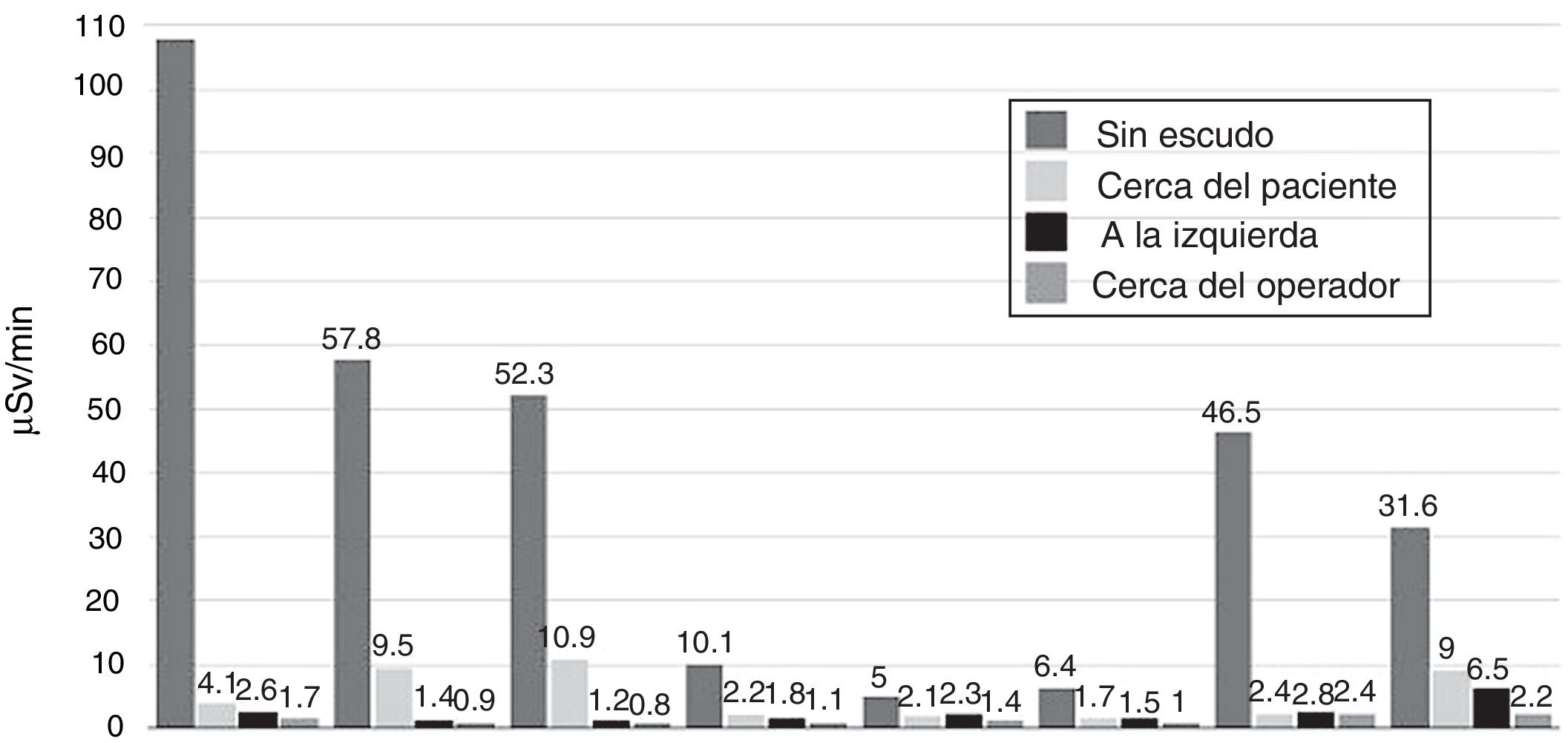
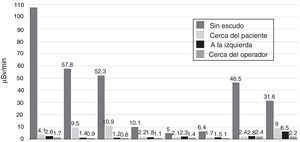
La utilidad de la mampara plomada (dos componentes) fue evaluada en un estudio14 en el que se emplearon modelos antropomórficos del paciente y dos operadores, durante procedimientos de Cardiología intervencionista en diferentes angulaciones del tubo de rayos X (oblicua anterior izquierda (LAO) 45°, oblicua anterior derecha (RAO) 30°, craneal (Cran) 25°, caudal (Caud) 25°, LAO 45°/Cran 25°, LAO 45°/Caud 25°, RAO 30°/Cran 25° and RAO 30°/Caud 25°). Para la evaluación se utilizó la dosis de radiación dosimetría electrónica de tiempo real en ocho sitios diferentes de cada operador (glabela, cuello, región superior izquierda del tórax, epigastrio, hipogastrio, muslo izquierdo, pantorrilla izquierda y tobillo izquierdo). La dosis de radiación recibida fue evaluada en el primer y segundo operador sin la mampara y con la mampara (dos componentes) en tres posiciones diferentes: cerca del paciente, lateral izquierda y cerca al operador. La dosis de radiación dispersa recibida por el primer operador sin la mampara plomada de dos componentes fue en promedio de 67,2 (± 49,0) μSv/min, con un mínimo de 2,3 (± 0,3) μSv/min en la proyección LAO 45°/Cran 25° y un máximo de 227,9 (± 12,5) μSv/min en la proyección Cran 25°. La dosis recibida por el segundo operador fue menor, con un promedio de 20,1 (± 19.6) μSv/min, un mínimo de 2,0 (± 0,3) μSv/min en la proyección RAO 30° y un máximo de 94,3 (± 3,8) μSv/min en la proyección Cran 25°. El uso de la mampara (dos componentes) en tres posiciones diferentes (cerca al paciente, lateral izquierda y cerca del operador) logró una disminución de la dosis de radiación dispersa recibida para el primer operador de 76,8%, 81,9% y 93,5% y para el segundo operador de 70,3%, 76,7% y 90,0%, respectivamente. La mampara de dos componentes cerca al operador (posición recomendada) obtuvo una reducción significativa de la radiación recibida cuando se comparó con las otras dos posiciones o con la no utilización de la misma (p <0,013).
En la figura 3 se muestran las dosis de radiación del primer operador en las diferentes proyecciones a nivel de la glabela (dosis del cristalino) y el porcentaje de reducción con la mampara en las tres diferentes posiciones vs. sin la mampara.
Medidas adicionalesUna de las estrategias fundamentales para reducir la dosis de radiación ionizante no solo al cristalino sino al staff de la sala de cateterismo cardiaco son todas las maniobras que buscan reducir la dosis de radiación en cada procedimiento al paciente y que se basan en el principio ALARA (su sigla en inglés As Low As Reasonably Achievable). A continuación se enumeran las recomendaciones del grupo de radioprotección del OIEA (Organismo Internacional de Energía Atómica) que se publicaron en la revista Catheterization and Cardiovascular Interventions en 201317, avaladas por Asian Pacific Society of Interventional Cardiology, European Association of Percutaneous Cardiovascular Interventions, Latin American Society of Interventional Cardiology, y Society for Cardiovascular Angiography and Interventions (SCAI):
- 1.
Minimice el tiempo de fluoroscopia.
- 2.
Minimice el número de imágenes adquiridas.
- 3.
Use las tecnologías disponibles para reducir la dosis al paciente.
- 4.
Use una buena geometría en la cadena de imagen: aumente la distancia entre el tubo de rayos X y el paciente, disminuya la distancia entre el detector plano y el paciente. Evite las proyecciones extremas, especialmente la craneal-izquierda que es la que más irradia junto a la lateral izquierda.
- 5.
Use colimación: colime en forma virtual, utilice los filtros en todo momento y evite la magnificación de la imagen durante la adquisición.
- 6.
Ubíquese en el área de menor radiación dispersa. “Un paso atrás”: si el operador duplica la distancia que lo separa del haz de rayos X la dosis de radiación recibida es solo un 25% (Ley del cuadrado de la distancia).
- 7.
Use los campos, las pantallas plomadas y todos los elementos de protección radiológica.
- 8.
Use los equipos de imagen adecuados para los procedimientos realizados.
- 9.
Utilice equipos de imagen cuyo rendimiento se controle a través de un programa de aseguramiento de la calidad.
- 10.
Obtenga entrenamiento adecuado.
- 11.
Porte los dosímetros y conozca su dosis de exposición.
Algunas recomendaciones adicionales:
- 1.
Disminuya al mínimo la adquisición en cineangiografía, utilizando la función de almacenamiento en fluoroscopia en lugar del cine.
- 2.
Use dos dosímetros, uno colocado fuera del delantal plomado en el hombro izquierdo o en el cuello y otro por debajo del delantal a la altura del tórax.
- 3.
Contacte de manera permanente al Físico Médico de su hospital y al servicio de mantenimiento del equipo de rayos X.
El número de procedimientos en intervencionismo coronario y periférico y en cardiopatías estructurales se ha incrementado de manera exponencial en las últimas décadas. Este fenómeno conlleva mayor exposición a dosis bajas de radiación ionizante debido principalmente a la radiación dispersa del paciente durante los procedimientos. Esta mayor exposición se ha asociado en varios estudios clínicos con mayor prevalencia de opacidades subcapsulares posteriores/corticales y cataratas en los cardiólogos intervencionistas. En este artículo de revisión se presentan las estrategias que han demostrado reducir de manera significativa la dosis de radiación en el cristalino; se describen las características que ofrecen mejor protección, como lentes plomados, así como el uso de otras estrategias que han demostrado utilidad, por ejemplo los campos blindados y ciertas medidas generales, y finalmente se resalta la utilidad fundamental de la mampara plomada (dos componentes), la cual debe ser usada de manera simultánea y sin excepción, adicional a las medidas descritas.
Creative commonsCreative Commons Reconocimiento-No Comercial-Sin Obra Derivada (CC BY-NC-ND).
Conflicto de interesesNinguno.