A resistência bacteriana aos antibióticos é atualmente um dos problemas de saúde pública mais relevantes a nível global, dado que apresenta consequências clínicas e económicas preocupantes, estando associada ao uso inadequado de antibióticos. Portugal é, no contexto europeu, um país com um elevado consumo de antibióticos, apesar de uma diminuição no consumo destes fármacos nos últimos anos. A resistência bacteriana tem crescido acentuadamente, sendo que as bactérias Gram‐positivas mais resistentes aos antibióticos são da espécie Staphylococcus aureus e do género Enterococcus, ao passo que as bactérias Gram‐negativas mais resistentes aos antibióticos são das espécies Acinetobacter baumannii, Pseudomonas aeruginosa e da família Enterobacteriaceae.
The bacterial resistance to antibiotics is actually one of the most relevant public health problems at global level, since it presents clinical and economic worrying consequences, and is associated with the inappropriate use of antibiotics. Portugal is, in the European context, a country with high antibiotic consumption, despite a decrease in the consumption of these drugs in the last years. The bacterial resistance to antibiotics has markedly increased being Staphylococcus aureus and Enterococcus the Gram‐positive bacteria more resistant to antibiotics, whereas the Gram‐negative bacteria more resistant to antibiotics belong to the Acinetobacter baumannii, Pseudomonas aeruginosa species and the Enterobacteriaceae family.
A resistência bacteriana aos antibióticos é atualmente um dos problemas de saúde pública mais relevantes, uma vez que muitas bactérias anteriormente suscetíveis aos antibióticos usualmente utilizados deixaram de responder a esses mesmos agentes1. O desenvolvimento de resistência bacteriana aos antibióticos é um fenómeno natural resultante da pressão seletiva exercida pelo uso de antibióticos, mas que tem sofrido uma expansão muito acelerada devido à utilização inadequada destes fármacos, existindo uma correlação muito clara entre um maior consumo de antibióticos e níveis mais elevados de resistência microbiana1.
A resistência aos antibióticos é responsável por consequências clínicas1–4 e económicas1,5,6 graves, relacionadas com o aumento da morbilidade e mortalidade1–4, devido aos atrasos na administração de tratamentos eficazes contra as infeções causadas por bactérias resistentes1. Por sua vez, a hospitalização prolongada e o uso de antibióticos diferentes dos de primeira linha aumentam também, de forma acentuada, os custos dos cuidados de saúde1, o que constitui um problema particularmente relevante, considerando os recursos finitos que sustentam os sistemas de saúde e tendo em conta a atual conjuntura de crise económica e financeira.
Tendo em conta a importância do problema da resistência microbiana e a sua crescente ameaça para a saúde pública a nível mundial, várias organizações nacionais, como a Direção‐Geral de Saúde, e internacionais, como a Comissão Europeia e a Organização Mundial de Saúde, reconheceram a relevância do estudo da emergência da resistência microbiana e do desenvolvimento de sistemas de vigilância e controlo da resistência microbiana, como o Programa de Prevenção e Controlo de Infeções e de Resistência aos Antimicrobianos7, a nível nacional, e o Sistema Europeu de Vigilância da Resistência Microbiana («European Antimicrobial Resistance Surveillance System [EARSS]»)8, a nível europeu.
Este trabalho pretende, assim, alertar para a importância do problema da resistência microbiana na saúde pública atualmente, analisando fatores que podem influenciar o consumo de antibióticos e, consequentemente, o nível de resistência aos mesmos. Apresenta‐se uma revisão da evolução da resistência microbiana no contexto mundial, europeu e nacional.
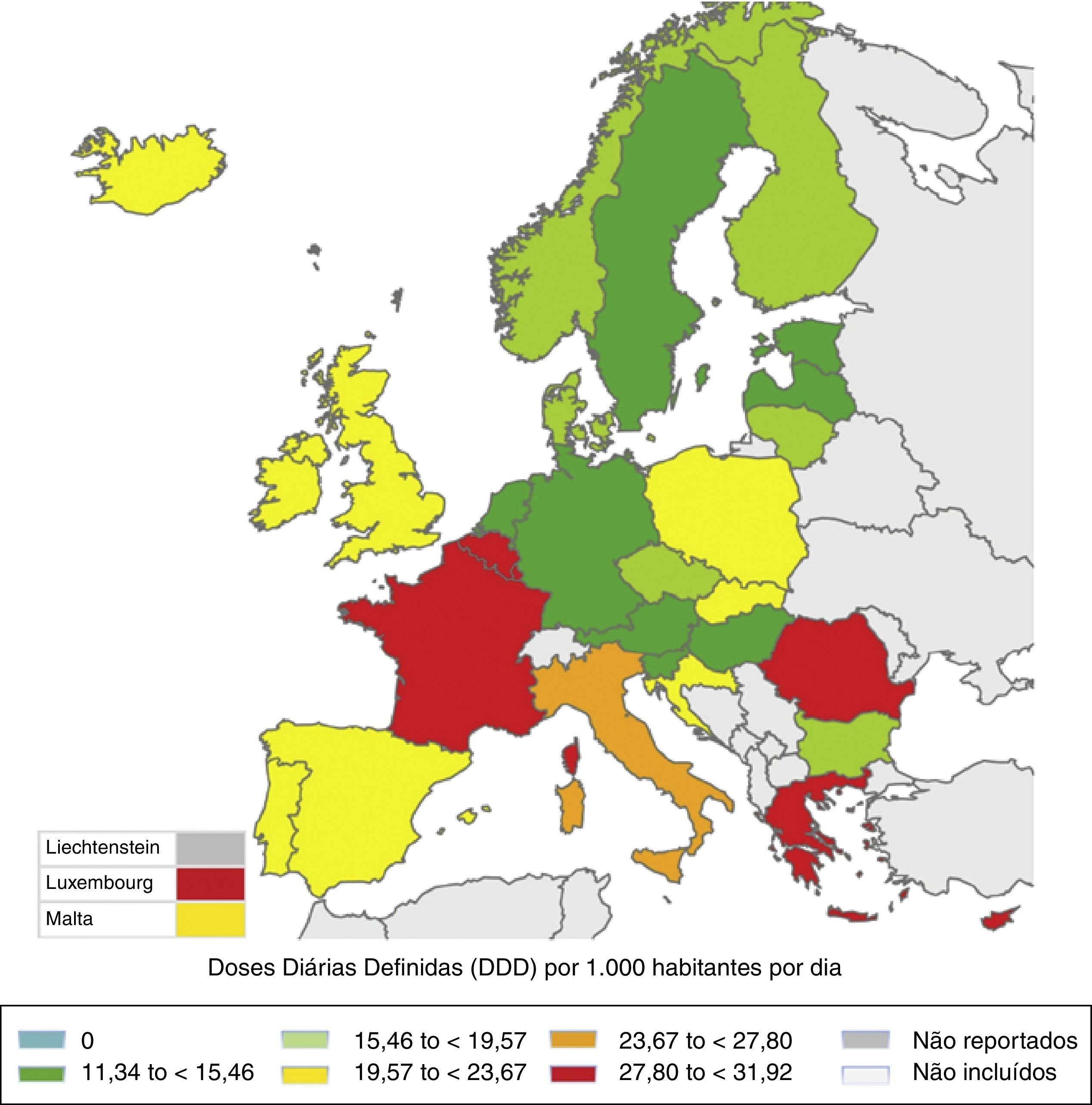
Consumo de antibióticos em Portugal e na EuropaSegundo os dados divulgados no relatório «European Centre for Disease Prevention and Control (ECDC) Surveillance Report: Surveillance of antimicrobial consumption in Europe, 2012», existe uma grande variabilidade no consumo de antibióticos na Europa, avaliado em doses diárias definidas (DDD) /1.000 habitantes /dia (DHD)9. O país com maior consumo de antibióticos, a Grécia (31,9 DHD), apresenta um valor em DHD cerca de 3 vezes superior ao país com menor consumo, a Holanda (11,3 DHD). Observa‐se também que o maior nível de consumo de antibióticos ocorre nos países do sul da Europa, comparativamente com os países do norte da Europa (fig. 1)9.
Consumo de antibióticos em ambulatório em 30 países europeus, em 2012, em doses diárias definidas/1.000 habitantes/dia.
Fonte: ECDC Surveillance Report: Surveillance of antimicrobial consumption in Europe, 20129.
Considerando a utilização relativa dos diferentes grupos de antibióticos, verifica‐se que as penicilinas constituem o grupo mais utilizado na comunidade em todos os países, variando o seu uso de 30% (Alemanha) a 67% (Eslovénia). Por sua vez, o uso de cefalosporinas varia de 0,2% (Dinamarca) a 23,5% (Malta), o uso de tetraciclinas de menos de 1,9% (Itália) a 24,4% (Suécia), o uso de macrólidos‐lincosamidas‐streptograminas (MLS) de 4,4% (Suécia) a 24,5% (Eslováquia) e o uso das quinolonas de 2,1% (Reino Unido) a 13,9% (Hungria) do uso total de antibióticos em ambulatório9.
Têm sido apontadas inúmeras razões para explicar as diferenças no consumo de antibióticos entre os países europeus, destacando‐se a incidência de infeções adquiridas na comunidade e os fatores que podem levar a diferenças nessa incidência, determinantes culturais e sociais, organização das estruturas prestadoras de cuidados de saúde, os recursos humanos e financeiros disponíveis e a sua utilização, o conhecimento acerca dos antibióticos, o mercado farmacêutico e as práticas de regulamentação existentes10.
Segundo dados do relatório «ECDC Surveillance Report: Surveillance of antimicrobial consumption in Europe, 2012», verifica‐se que no período entre 2002‐2012 a taxa do consumo de antibióticos em Portugal apresentou uma tendência de decréscimo de 26,5 DHD para 22,7 DHD, sendo que, apesar desta redução na utilização de antibióticos, Portugal continuou a apresentar um consumo elevado relativamente a outros países europeus, sendo superior à média dos valores de consumo (20,4 DHD) dos países que integram o projeto «Vigilância Europeia do Consumo de Antimicrobianos» («European Surveillance of Antimicrobial Consumption» [ESAC])9.
Tendo em conta a utilização dos diferentes grupos de antibióticos em Portugal, verifica‐se que, segundo dados do relatório «ECDC Surveillance Report: Surveillance of antimicrobial consumption in Europe, 2012», as penicilinas constituem o grupo de antibióticos mais utilizado (12,4 DHD), seguindo‐se o grupo dos MLS (3,2 DHD), sendo que os grupos menos utilizados são as tetraciclinas (1,1 DHD) e a associação de sulfonamidas e trimetoprim (0,5 DHD)9. Estes dados estão de acordo com dados de outros países europeus, particularmente de países do sul da Europa9. É de notar que, entre 2000‐2012, se verificou uma diminuição do consumo nos grupos das cefalosporinas, quinolonas e macrólidos, enquanto ocorreu um aumento do consumo no grupo das penicilinas, o grupo mais utilizado e que constitui, frequentemente, a primeira linha de tratamento para muitas infeções bacterianas9,11.
Uso inadequado de antibióticos e a sua relação com o aparecimento de resistênciasO uso inapropriado dos antibióticos, particularmente a sua utilização excessiva, tem sido considerado um dos fatores que mais contribui para o problema da resistência microbiana2,12–15, constituindo um sério problema de saúde pública global, dado que tem aumentado a frequência de doenças infeciosas estabelecidas e emergentes em consequência da ineficácia dos antibióticos16. Dessa forma, verifica‐se que os países do norte da Europa, que apresentam um menor consumo de antibióticos, são também os países onde o nível de resistência é menor, verificando‐se o oposto nos países do sul da Europa, incluindo Portugal12. Com efeito, o consumo inadequado de antibióticos tem custos elevados para a sociedade e consequências nefastas para a saúde, como a diminuição da eficácia dos tratamentos, o prolongamento das doenças, o crescimento do número de hospitalizações14,17 e o aumento da morbilidade e mortalidade2,14,16,17.
Têm sido apontados vários fatores que podem levar à prescrição inadequada de antibióticos, destacando‐se a incerteza no diagnóstico14,18–20, a pressão exercida sobre os médicos por parte dos doentes e/ou seus familiares, e a existência de muitas consultas por dia, o que dificulta a precisão do diagnóstico e da terapêutica e aumenta a prescrição de antibióticos pelos médicos14,18,21. Para além disso, existem níveis elevados de não adesão à terapêutica por parte dos doentes, em que os doentes tomam doses diferentes ou por períodos diferentes do que o prescrito16, a par de um nível elevado de automedicação, em que os doentes utilizam frequentemente antibióticos de tratamentos anteriores ou obtidos na farmácia sem prescrição médica14,16,22–26. A prática de automedicação entre a população resulta de características culturais, crenças e conhecimentos sobre os antibióticos, o que pode ser constatado quando se observa que grande parte da população desconhece que os antibióticos apenas atuam nas infeções bacterianas, consumindo antibióticos para tratar infeções virais comuns como a gripe14,23,27.
É ainda importante salientar que uma proporção considerável do uso inadequado de antibióticos, que tem também um importante papel na emergência e disseminação da resistência bacteriana aos antibióticos, é devida ao uso de antibióticos em atividades como a veterinária, a zootecnia e a pecuária, verificando‐se que aproximadamente 50% da totalidade dos agentes antimicrobianos consumidos na União Europeia não são utilizados em humanos28. Efetivamente, verifica‐se que, em países onde o antibiótico avoparcina, semelhante à vancomicina, foi usado na produção animal, ocorreu um aumento do nível de Enterococcus resistentes à vancomicina na flora intestinal dos animais de consumo tratados com avoparcina, assim como na flora fecal de humanos saudáveis e de animais domésticos28,29. Posteriormente, verificou‐se uma diminuição do nível de resistências após a abolição do uso da avoparcina na produção animal pela União Europeia28,30. Dessa forma, a transmissão horizontal de genes de resistência através de elementos genéticos móveis, como plasmídeos, transposões e integrões, entre diferentes espécies e géneros bacterianos, patogénicos e não patogénicos, assim como a transmissão subsequente dessas bactérias entre vários hospedeiros e reservatórios ambientais, parece desempenhar um papel importante na emergência e disseminação da resistência bacteriana aos antibióticos28,31.
Evolução da resistência microbiana a nível mundialDesde a introdução da utilização dos antibióticos que o nível de resistência microbiana tem crescido progressivamente, tendo aumentado acentuadamente nos últimos 15 anos13. Os 4 principais mecanismos de resistência bacteriana aos antibióticos são: a modificação ou destruição enzimática do antibiótico (ex: destruição dos agentes ß‐lactâmicos pelas enzimas ß‐lactamases); a prevenção da acumulação intracelular do antibiótico através da redução da permeabilidade celular ao antibiótico (ex: resistência da bactéria Pseudomonas aeruginosa [P. aeruginosa] ao imipenem) ou da existência de bombas de efluxo dos antibióticos das células bacterianas (ex: resistência da família das enterobacteriáceas às tetraciclinas); as alterações nas moléculas alvo dos antibióticos (ex: resistência intrínseca das bactérias do género Enterococcus às cefalosporinas), e a produção de moléculas alvo alternativas que não são inibidas pelo antibiótico, enquanto se continua a produzir as moléculas alvo originais, contornando desse modo a inibição induzida pelo antibiótico (ex: resistência da bactéria Staphylococcus aureus [S. aureus] à meticilina)32,33.
Considerando a evolução da resistência aos antibióticos nas bactérias Gram‐positivas, verifica‐se que a espécie S. aureus13,34 e o género Enterococcus são as bactérias Gram‐positivas que apresentam maiores problemas de resistência aos antibióticos13.
Relativamente à espécie S. aureus, é de salientar que as primeiras estirpes produtoras de penicilinases e que eram também resistentes aos outros antibióticos usualmente disponíveis causaram problemas clínicos consideráveis na década de 50, que levaram à introdução da meticilina e de outras penicilinas semissintéticas, resultando numa redução acentuada dessas estirpes13. No entanto, pouco tempo depois da introdução da meticilina em 1960, foram isoladas amostras de S. aureus resistentes à meticilina (MRSA] no Reino Unido, o que marcou o aparecimento das estirpes de S. aureus resistentes à meticilina («methicillin‐resistant S. aureus»)34–36, que posteriormente se disseminaram a nível mundial13,34,35,37.
A informação da prevalência de MRSA em inúmeros países revela uma grande variação, desde cerca de 1,0% em países como a Holanda até níveis de 25,0‐50,0% em muitos países do continente americano, na Austrália e em alguns países do sul da Europa13,35,37.
Relativamente às bactérias do género Enterococcus, verifica‐se que, apesar de apresentarem normalmente uma baixa virulência, estas bactérias podem causar infeções em doentes imunodeprimidos, particularmente naqueles que estiveram submetidos a tratamentos com antibióticos13. O aparecimento de Enterococcus faecium resistentes à vancomicina em 1986, no Reino Unido, precedeu o aparecimento nos Estados Unidos e, depois, noutras regiões do mundo, de bactérias do género Enterococcus altamente resistentes e causadoras de infeções difíceis de tratar13,37,38. Nos Estados Unidos verificou‐se o aparecimento de surtos causados por vários clones, em que existe um elevado número de portadores assintomáticos e de doentes infetados provenientes da comunidade admitidos nos hospitais, pelo que um controlo de infeções eficaz é bastante difícil13,39,40.
Considerando a evolução da resistência aos antibióticos nas bactérias Gram‐negativas, verifica‐se que o mais importante mecanismo de resistência aos antibióticos nestas bactérias é a produção de enzimas ß‐lactamases34. Relativamente à família das enterobacteriáceas, é de referir que, após a introdução da ampicilina na década de 1960, a resistência aos agentes ß‐lactâmicos tornou‐se um importante problema clínico, devido à transferência por plasmídeos de genes de resistência codificando ß‐lactamases de serina temoniera (TEM) e «sulfhydryl variable» (SHV)13.
Nos anos 80, após a introdução das cefalosporinas de terceira geração, foram reportados genes TEM e SHV mutados, que se disseminaram principalmente entre o género Klebsiella spp e a espécie Escherichia coli (E. coli), o que marcou a emergência das estirpes produtoras de ß‐lactamases de largo espectro (ESBL – «extended spectrum ß‐lactamases»), que se definem por serem capazes de hidrolisar cefalosporinas de terceira geração e monobactamos13,34,41.
Posteriormente, surgiu uma nova família de ß‐lactamases, designada como enzimas «cefotaximases Munich» (CTX‐M), que se disseminou por todos os continentes13,42. Na Europa, verificaram‐se na última década (2000‐2010) alterações consideráveis nos tipos de ESBL com maior prevalência, com as estirpes produtoras de CTX‐M a tornarem‐se dominantes, particularmente as de CTX‐M‐15, dominantes no Reino Unido e em França, e as de CTX‐M‐14, frequentes em Espanha13,34. É de salientar que o aumento do uso de carbapenemos no tratamento de infeções por enterobacteriáceas multirresistentes tem levado ao aumento da disseminação da resistência a estes agentes13,34, a qual é mediada pela transferência de enzimas carbapenemases (que destroem os carbapenemos), particularmente das famílias imipenemases (IMP) e «Verona integron‐encoded metallo‐ ß lactamases» (VIM), através de plasmídeos13,34,37,43.
Existem ainda outras bactérias Gram‐negativas associadas a problemas de resistência aos antibióticos, tais como as pertencentes aos géneros Pseudomonas (principalmente a bactéria Pseudomonas aeruginosa [P. aeruginosa]) e Acinetobacter (particularmente a espécie Acinetobacter baumannii [A. baumannii])13,34,37. As bactérias da espécie P. aeruginosa e da espécie A. baumannii são bactérias ambientais altamente disseminadas, que causam problemas significativos em doentes imunodeprimidos e em doentes internados em unidades de cuidados intensivos hospitalares, onde existem reservatórios destas bactérias13,44,45.
As bactérias P. aeruginosa apresentam resistência à maioria dos agentes ß‐lactâmicos e às fluoroquinolonas, o que fez com que os carbapenemos fossem usados crescentemente para o tratamento de infeções por Pseudomonas, levando à disseminação da resistência destas bactérias mediada pelas carbapenemases dos tipos VIM e IMP por todo o mundo13,34.
As bactérias do género Acinetobacter produzem uma grande variedade de ß‐lactamases e apresentam um largo espectro de mecanismos intrínsecos de resistência, pelo que algumas estirpes são resistentes a todos os antibióticos conhecidos, exceto à colistina13,37.
Evolução da resistência microbiana em Portugal e o seu enquadramento no contexto europeuConsiderando a evolução da resistência microbiana em Portugal, observa‐se que, à semelhança do que acontece a nível mundial, as bactérias patogénicas mais resistentes aos antibióticos em Portugal são: MRSA, Enterococcus resistentes à vancomicina, Streptococcus pneumoniae (S. pneumoniae) resistentes à penicilina, enterobacteriáceas produtoras de ESBL ou de carbapenemases, e P. aeruginosa e A. baumannii resistentes aos carbapenemos46.
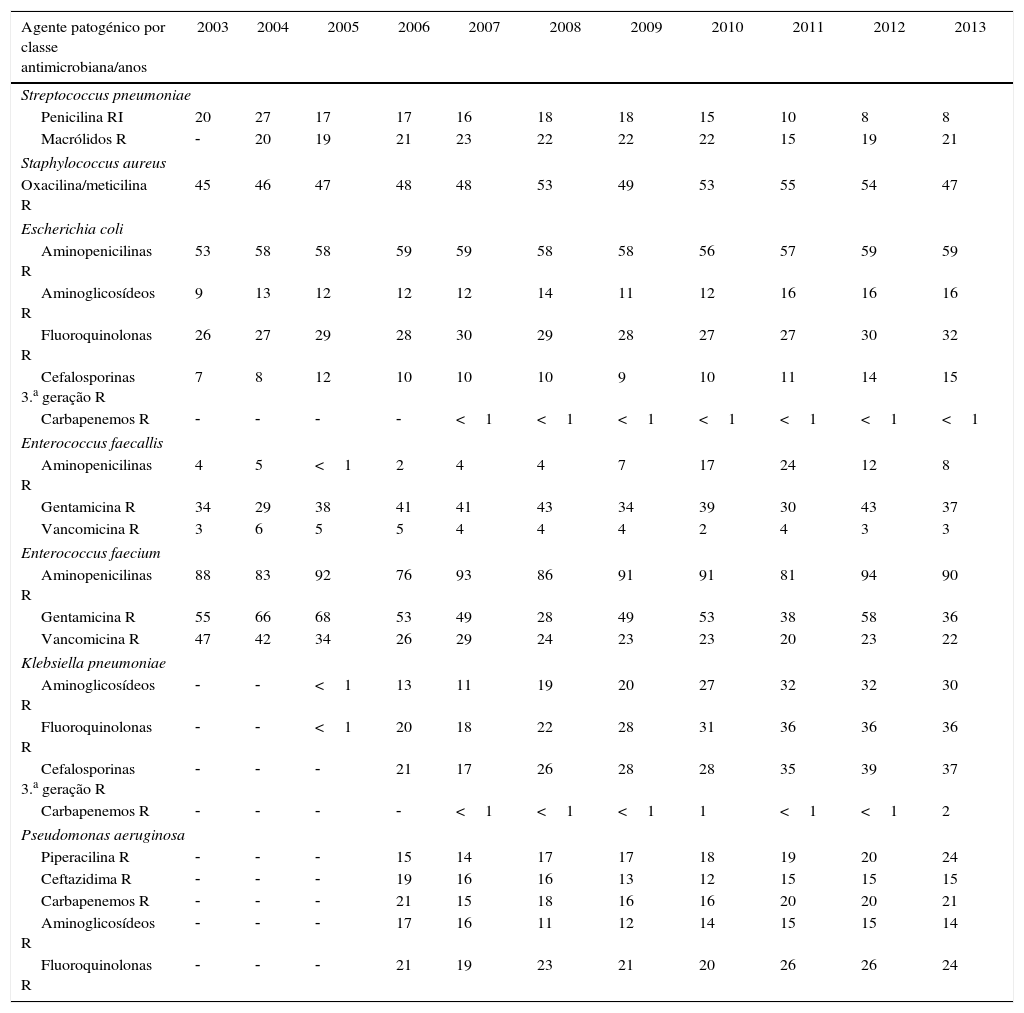
A tabela 1 apresenta dados do Centro Europeu de Prevenção e Controlo de Doenças relativos aos perfis de resistência microbiana em Portugal, nos anos de 2003‐201347.
Proporções (em %) de amostras isoladas das bactérias mais frequentes não‐suscetíveis às diferentes classes de antibióticos em Portugal
| Agente patogénico por classe antimicrobiana/anos | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Streptococcus pneumoniae | |||||||||||
| Penicilina RI | 20 | 27 | 17 | 17 | 16 | 18 | 18 | 15 | 10 | 8 | 8 |
| Macrólidos R | ‐ | 20 | 19 | 21 | 23 | 22 | 22 | 22 | 15 | 19 | 21 |
| Staphylococcus aureus | |||||||||||
| Oxacilina/meticilina R | 45 | 46 | 47 | 48 | 48 | 53 | 49 | 53 | 55 | 54 | 47 |
| Escherichia coli | |||||||||||
| Aminopenicilinas R | 53 | 58 | 58 | 59 | 59 | 58 | 58 | 56 | 57 | 59 | 59 |
| Aminoglicosídeos R | 9 | 13 | 12 | 12 | 12 | 14 | 11 | 12 | 16 | 16 | 16 |
| Fluoroquinolonas R | 26 | 27 | 29 | 28 | 30 | 29 | 28 | 27 | 27 | 30 | 32 |
| Cefalosporinas 3.a geração R | 7 | 8 | 12 | 10 | 10 | 10 | 9 | 10 | 11 | 14 | 15 |
| Carbapenemos R | ‐ | ‐ | ‐ | ‐ | <1 | <1 | <1 | <1 | <1 | <1 | <1 |
| Enterococcus faecallis | |||||||||||
| Aminopenicilinas R | 4 | 5 | <1 | 2 | 4 | 4 | 7 | 17 | 24 | 12 | 8 |
| Gentamicina R | 34 | 29 | 38 | 41 | 41 | 43 | 34 | 39 | 30 | 43 | 37 |
| Vancomicina R | 3 | 6 | 5 | 5 | 4 | 4 | 4 | 2 | 4 | 3 | 3 |
| Enterococcus faecium | |||||||||||
| Aminopenicilinas R | 88 | 83 | 92 | 76 | 93 | 86 | 91 | 91 | 81 | 94 | 90 |
| Gentamicina R | 55 | 66 | 68 | 53 | 49 | 28 | 49 | 53 | 38 | 58 | 36 |
| Vancomicina R | 47 | 42 | 34 | 26 | 29 | 24 | 23 | 23 | 20 | 23 | 22 |
| Klebsiella pneumoniae | |||||||||||
| Aminoglicosídeos R | ‐ | ‐ | <1 | 13 | 11 | 19 | 20 | 27 | 32 | 32 | 30 |
| Fluoroquinolonas R | ‐ | ‐ | <1 | 20 | 18 | 22 | 28 | 31 | 36 | 36 | 36 |
| Cefalosporinas 3.a geração R | ‐ | ‐ | ‐ | 21 | 17 | 26 | 28 | 28 | 35 | 39 | 37 |
| Carbapenemos R | ‐ | ‐ | ‐ | ‐ | <1 | <1 | <1 | 1 | <1 | <1 | 2 |
| Pseudomonas aeruginosa | |||||||||||
| Piperacilina R | ‐ | ‐ | ‐ | 15 | 14 | 17 | 17 | 18 | 19 | 20 | 24 |
| Ceftazidima R | ‐ | ‐ | ‐ | 19 | 16 | 16 | 13 | 12 | 15 | 15 | 15 |
| Carbapenemos R | ‐ | ‐ | ‐ | 21 | 15 | 18 | 16 | 16 | 20 | 20 | 21 |
| Aminoglicosídeos R | ‐ | ‐ | ‐ | 17 | 16 | 11 | 12 | 14 | 15 | 15 | 14 |
| Fluoroquinolonas R | ‐ | ‐ | ‐ | 21 | 19 | 23 | 21 | 20 | 26 | 26 | 24 |
Relativamente ao nível de resistência à meticilina da espécie S. aureus, observa‐se que este aumentou entre 2003‐2013 (de 45,0 para 47,0%), embora tendo descido em 2013 face ao nível superior a 50% verificado nos anos anteriores, o que constitui um nível de resistência que compromete seriamente o uso das penicilinas para o tratamento de infeções por S. aureus, particularmente tendo em conta que Portugal é o terceiro país da Europa com um nível de resistência mais elevado47. Este fenómeno foi observado em 2005 por Amorim et al.48, num estudo sobre o perfil de resistência desta bactéria à meticilina num hospital português, onde se verificou um nível de resistência de 55%.
Considerando o nível de resistência à vancomicina das bactérias do género Enterococcus (particularmente da espécie Enterococcus faecium), verifica‐se que este diminuiu para aproximadamente metade (de 47,0 para 22,0% das amostras isoladas) no período compreendido entre 2003‐2013, sendo que, ainda assim, Portugal apresenta um valor bastante superior ao valor do conjunto dos países europeus (8,9%), sendo um dos países europeus com maior nível de resistência destas bactérias à vancomicina47.
Relativamente à taxa de resistência à penicilina da espécie S. pneumoniae, observa‐se que esta diminuiu entre 2003‐2013, apresentando um valor relativamente baixo (7,6% em 2013) e inferior ao valor do conjunto dos países europeus (13,6%), existindo alguns países europeus com valores bastante superiores (ex: Espanha [27,6%] e França [22,4%])47. Em 2007, Correa et al.49 realizaram um estudo num hospital em Espanha, onde verificaram uma taxa de resistência de 17,9%, valor superior ao apresentado por Portugal e ao apresentado pelo conjunto dos países europeus.
Considerando o nível de resistência da espécie E. coli a antibióticos habitualmente usados, observa‐se que este aumentou no período entre 2003‐2013, sendo que o valor de resistência às cefalosporinas de terceira geração em 2013 (14,9%) é superior ao valor do conjunto dos países europeus (12,6%), existindo, porém, muitos países europeus com valores superiores de resistência a estes agentes (ex: Bulgária [39,6%] e Itália [26,2%]), causada em grande parte pela produção de ESBL47. Picozzi et al. realizaram um estudo entre janeiro de 2008 e dezembro de 2010 em hospitais de Milão, em Itália, onde observaram um nível de E. coli produtoras de ESBL superior aos valores verificados em Portugal e no conjunto dos países europeus50.
Em relação à espécie Klebsiella pneumoniae (K. pneumoniae), verifica‐se que, no período entre 2005‐2013, ocorreu um grande aumento da resistência desta bactéria a antibióticos habitualmente usados como os aminoglicosídeos (de<1,0 para 30,3% do total das amostras isoladas), apesar de existirem vários países europeus (ex: Polónia [58,4%] e Eslováquia [64,0%]) com valores mais elevados em 2013, e as fluoroquinolonas (de<1,0 para 35,7% do total das amostras isoladas), existindo, no entanto, muitos países europeus (ex: Grécia [67,6%] e Polónia [70,1%]) com valores mais elevados em 201347. Neonakis et al.51 realizaram um estudo num hospital universitário da Grécia, em 2008, em que observaram um nível de resistência da K. pneumoniae às fluoroquinolonas de 64%, o que corrobora o elevado nível de resistência desta espécie às fluoroquinolonas na Grécia.
Considerando o nível de resistência aos antibióticos da espécie P. aeruginosa, verifica‐se que ocorreu uma diminuição do nível de resistência na maioria das classes de antibióticos habitualmente usadas entre 2006‐2013, apesar dessa diminuição ter sido pouco acentuada (ex: resistência aos carbapenemos desceu de 21,0 para 20,6%), sendo que o valor da resistência aos carbapenemos era, em 2013, superior ao valor do conjunto dos países europeus (17,6%), apesar de existirem países europeus com valores mais elevados (ex: Grécia [49,3%] e Itália [25,9%])47.
É importante salientar que os dados divulgados no relatório «SURVEILLANCE REPORT: Antimicrobial resistance surveillance in Europe, 2013» referem‐se exclusivamente a isolados provenientes de bacteriemias e de infeções no líquido cefalorraquidiano, excluindo todos os outros isolados provenientes de outras infeções comuns, como as infeções respiratórias ou urinárias, pelo que estes resultados apresentam uma importante limitação.
Relativamente ao nível de resistência na espécie A. baumannii, dados da Direção‐Geral de Saúde relativos às unidades de cuidados intensivos hospitalares11 revelam que este apresentou uma tendência de crescimento entre 2006‐2009, atingindo valores muito elevados de resistência às fluoroquinolonas (89,2%) e aos carbapenemos (90,0%). Nos últimos anos, verificou‐se o aparecimento de um clone epidémico de A. baumannii em Portugal, o «sequence type 118» (ST 118), que produz carbapenemases do tipo oxacilinases – 23 (OXA‐23), tendo‐se disseminado por vários hospitais e estando a substituir os clones, até então, mais frequentes em Portugal; o «sequence type 92» (ST 92), produtor de carbapenemases do tipo OXA‐23 e o «sequence type 98» (ST 98), produtor de carbapenemases do tipo oxacilinases – 24 (OXA‐24)52,53.
ConclusõesA resistência bacteriana aos antibióticos é um dos problemas de saúde pública mais graves atualmente, estando associada ao uso inadequado de antibióticos. Portugal é, no contexto europeu, um país com um consumo de antibióticos elevado, apesar de se verificar uma diminuição em anos recentes, pelo que é importante tomar medidas no sentido de reduzir o consumo destes medicamentos. Em Portugal, verificou‐se um aumento da resistência aos antibióticos nas bactérias S. aureus, K. pneumoniae e A. baumannii, enquanto as bactérias do género Enterococcus apresentam uma diminuição da resistência. É, assim, necessário adotar estratégias que minimizem a resistência nas espécies em que esta apresenta um nível elevado, ou em que houve um aumento da resistência em anos recentes, tais como o uso adequado de antibióticos no tratamento de infeções causadas por essas espécies13 e um melhor controlo de infeções hospitalares13,54. Os dados publicados sobre resistências bacterianas são dados recolhidos exclusivamente em meio hospitalar, não tendo sido encontrados dados de resistências recolhidos em cuidados primários. Apesar de considerarmos que as infeções causadas por estirpes resistentes em meio ambulatório são, não raras vezes, tratadas em meio hospitalar, parece‐nos ser fundamental a recolha de dados de resistência bacteriana nos cuidados primários. Desse modo, poderia ser elaborado um mapa microbiológico das resistências em ambulatório a ser, subsequentemente, divulgado pelos profissionais de saúde e população. Além disso, a promoção da comunicação e do fluxo de informação entre os cuidados primários e os cuidados diferenciados poderá melhorar as medidas de combate ao problema de saúde pública que as resistências bacterianas representam.
Uma outra medida a tomar, com vista a prevenir a emergência e disseminação das resistências bacterianas, é restringir o consumo de antibióticos na prática veterinária e na produção animal, atividades responsáveis pelo consumo inadequado de muitos antibióticos e pela seleção de estirpes resistentes que depois se transmitem para outros animais e para os humanos.
FinanciamentoProjeto financiado pela Fundacão para a Ciência e Tecnologia (FCT) (PTDC/SAU‐ESA/105530/2008), Ministério da Educacão e Ciência e co‐financiado pelo FEDER através do POFC‐COMPETE. iB.
AgradecimentosOs autores agradecem ao iBiMED (UID/BIM/04501/2013).