Nuestro objetivo principal es realizar la validación externa de los sistemas de puntuación actuales para predecir el estado libre de cálculos (ELC) después de la cirugía intrarrenal retrógrada (CRIR) para cálculos renales de 2-4 cm y desarrollar un nuevo sistema de puntuación reexaminando los posibles factores predictivos relacionados con el ELC.
MétodosSe evaluaron retrospectivamente los pacientes que recibieron CRIR para el tratamiento de cálculos renales con diámetro acumulado de 2-4 cm, entre enero de 2017 y marzo de 2021. Los cálculos residuales ≤ 2 mm se definieron como clínicamente insignificantes, y estos casos se consideraron como ELC. Se examinaron los posibles factores predictivos relacionados con el ELC mediante el análisis de regresión logística multivariante. Se elaboró un nomograma y se creó un sistema de puntuación utilizando variables predictivas independientes. Mediante el análisis ROC se evaluó la capacidad de predicción de los sistemas de puntuación actuales y del recién desarrollado.
ResultadosLos sistemas de puntuación existentes resultaron insuficientes para predecir el ELC (AUC < 0,660 en todos los casos). Se identificaron como predictores independientes del ELC el área de superficie (OR: 0,991, p < 0,001), la densidad (OR: 0,998, p < 0,001), el número (OR: 0,365, p = 0,033) y la localización de los cálculos (p = 0,037). Utilizando estos marcadores predictivos, se desarrolló un nuevo sistema de puntuación cuyos resultados oscilan entre 4 y 15. El valor AUC de este sistema de puntuación fue de 0,802 (0,734-0,870).
ConclusiónLos sistemas de puntuación RUSS, S-ReSC y RIRS y el nomograma de Ito no lograron predecir el ELC en cálculos de > 2 cm. Nuestro nuevo sistema de puntuación tuvo una capacidad predictiva del ELC mayor en cálculos de > 2 cm, en comparación con los otros sistemas de puntuación.
Our primary aim is to perform the external validation of the current scoring systems in predicting stone-free status (SFS) after retrograde intrarenal surgery (RIRS) for renal stones 2-4 cm and develop a novel scoring system by re-examining possible predictive factors related to SFS.
MethodsPatients who underwent RIRS due to renal stones with a cumulative stone diameter of 2-4 cm between January 2017 and March 2021 were retrospectively screened. Residual stones ≤ 2 mm were defined as clinically insignificant, and these cases were considered to have SFS. Possible predictive factors related to SFS were examined using the multivariate logistic regression analysis. A nomogram and a scoring system were developed using independent predictive variables. The prediction ability of the previous and the new scoring system were evaluated with the ROC analysis.
ResultsThe existing scoring systems were found to be insufficient in predicting SFS (AUC < 0.660 for all). The independent predictors of SFS were identified as stone surface area (OR: 0.991, p < 0.001), stone density (OR: 0.998, p < 0.001), number of stones (OR: 0.365, p = 0.033), and stone localization (p = 0.037). Using these predictive markers, a new scoring system with a score ranging between 4 and 15 was developed. The AUC value for this scoring system was 0.802 (0.734-0.870).
ConclusionThe RUSS, S-ReSC and RIRS scoring systems and Ito's nomogram failed to predict SFS in stones > 2 cm. The SFS predictive ability of our new scoring system was higher in > 2 cm stones compared to the other scoring systems.
La nefrolitotomía percutánea (NLPC) se recomienda en las guías actuales para el tratamiento de los cálculos renales mayores de 2 cm1. A pesar de su elevada tasa libre de cálculos (TLC), la NLPC se asocia a complicaciones severas. La NLPC también está limitada o contraindicada por factores asociados al paciente, como obesidad mórbida, tratamiento anticoagulante, enfermedad pulmonar obstructiva grave y contracturas/cifoescoliosis severas2. Gracias a los avances recientes en la ureterorrenoscopia flexible (URS-f), así como a una mayor experiencia en su realización, la cirugía intrarrenal retrógrada (CRIR) tiene ahora una TLC similar a la NLPC, y menores tasas de complicaciones en el tratamiento de los cálculos renales de gran tamaño3–5. Como consecuencia del incremento del uso de la CRIR y de sus resultados prometedores, la elección del tratamiento óptimo para los cálculos de 2-4 cm no es una tarea fácil. En estos pacientes, la elección del método quirúrgico adecuado mediante la predicción preoperatoria del estado libre de cálculos (ELC) es fundamental para evitar las complicaciones de la NLPC, así como las complicaciones derivadas de la anestesia de varias sesiones de CRIR. Los sistemas de puntuación se utilizan para predecir el éxito de la cirugía de cálculos en el sistema urinario, informar a los pacientes y estandarizar las publicaciones de los estudios académicos. Hasta la fecha, se han desarrollado la puntuación de cálculos de Resorlu-Unsal6, la puntuación de complejidad de cálculos renales de la Universidad Nacional de Seúl (S-ReSC) modificada7 y la puntuación de RIRS8, así como el sistema de puntuación basado en el nomograma de Ito9 para predecir el ELC tras la CRIR. Los estudios originales basados en estos sistemas de puntuación informaron de su capacidad predictiva del ELC6-9. Sin embargo, se ha visto que no se lleva a cabo una clasificación específica para los cálculos de > 2 cm, y todos los cálculos mayores de 2 cm se clasifican como el peor grupo en todos los sistemas de puntuación, excepto en el RUSS. Hasta nuestro conocimiento, no hay ningún estudio en la literatura que evalúe la eficacia de los sistemas de puntuación existentes en litiasis mayores de 2-4 cm. Por lo tanto, el objetivo del presente estudio es realizar la validación externa de los sistemas de puntuación existentes para pacientes con cálculos renales de 2-4 cm y desarrollar un sistema de puntuación reevaluando los factores relacionados con el ELC.
Material y métodosSe examinaron retrospectivamente los pacientes a los que se les realizó una CRIR por cálculos renales con un diámetro acumulado (DAC) de 2-4 cm en los centros participantes en el estudio entre enero de 2017 y marzo de 2021. Se excluyeron del estudio los pacientes menores de 18 años, los que tenían cálculos ureterales o de estruvita y aquellos que carecían de datos para su análisis. El estudio se realizó de acuerdo con la Declaración de Helsinki revisada en 2013. Se obtuvo la aprobación del Comité de Ética Local (Decisión n°:2021-11-09).
En los centros participantes en el estudio, el manejo estándar para los cálculos del sistema urinario es la NLPC para los cálculos mayores de 2 cm, con excepción de los pacientes que utilizan fármacos anticoagulantes y antiagregantes, pacientes con cálculos residuales después de un procedimiento fallido de NLPC, o aquellos con temor a las complicaciones de la NLPC, en quienes se indica la URS-f como primera o segunda opción, dependiendo de la preferencia del paciente y/o del cirujano.
Todas las intervenciones fueron realizadas por dos cirujanos experimentados en los centros participantes en el estudio. Se colocó una vaina de acceso ureteral (10,7 o 12 F, Cook Medical, o 11/13 o 13/15 F, Boston Scientific) en todos los pacientes. Todos los procedimientos se realizaron con diferentes tipos de URS-f (7,5 F; Karl Storz Flex-X2, Tuttlingen, Alemania y Olympus P-5TM, Olympus, Tokio, Japón) y láser de Holmio de 270 μm. Se introdujo un catéter DJ en el preoperatorio de los pacientes con cólico renal resistente al tratamiento, pielonefritis y un uréter estrecho que pudiese impedir el acceso al cálculo. Se colocó un catéter DJ o un catéter ureteral posoperatorio, según la preferencia del cirujano y la necesidad clínica. El catéter uretral se retiró en el primer día de la intervención y el catéter DJ se retiró dos a cuatro semanas después de la intervención.
El ELC se evaluó con una tomografía computarizada sin contraste (TCSC) en el primer mes. Los cálculos residuales de 2 mm se definieron como clínicamente insignificantes, y se consideró alcanzado el ELC en estos pacientes.
Las características clínicas de los pacientes, las características de los cálculos y los hallazgos perioperatorios se obtuvieron de las historias clínicas y las imágenes radiológicas. Las complicaciones se calificaron según la clasificación de Clavien-Dindo. El grado de hidronefrosis se midió según el sistema de clasificación de hidronefrosis de la Society for Fetal Urology (SFU)10. El DAC se midió como el diámetro longitudinal mayor en el corte axial o coronal reconstruido de la TCSC. La superficie del cálculo (SC) se obtuvo mediante la fórmula longitud x ancho x π x 0,2511. El volumen del cálculo (VC) y el ángulo infundibulopélvico del polo inferior (AIP) se midieron y calcularon como se ha descrito en estudios anteriores8,9. La media de unidades Hounsfield (UH) se midió tomando el centro y los bordes del cálculo. En caso de cálculos múltiples, se calcularon independientemente cada uno de los valores DAC, área cálculo (AC) y VC y se sumaron para determinar el tamaño total. El valor de la UH de los cálculos múltiples se calculó con la media de las UH individual de cada cálculo.
Sistemas de puntuación actualesRUSSSe trata de un sistema de puntuación en el que cada uno de los parámetros (es decir, tamaño del cálculo > 20 mm, localización del cálculo en el polo inferior e AIP < 45°, número de cálculos en diferentes cálices > 1 y anatomía renal anormal en las imágenes radiológicas) se puntúa como un punto. Los autores también proporcionaron una puntuación adicional por cada 10 mm para los cálculos de más de 20 mm. La puntuación total oscila entre 0 y 5, con variaciones según el tamaño del cálculo6.
S-ReSC modificadaEn este sistema de puntuación, la localización de los cálculos en el sistema pielocalicial se marca y puntúa individualmente. Se da una puntuación adicional a los cálculos localizados en el polo inferior. Las localizaciones de los cálculos y su puntuación son las siguientes: pelvis renal1, grupo calicial mayor superior2 e inferior3, y grupo calicial menor anterior y posterior del cáliz superior (4-5), medio (6-7) e inferior (8-9)7.
Nomograma de ItoSe trata de un sistema de puntuación basado en un nomograma que proporciona una puntuación total entre 0 y 25 y que se basa en los parámetros del volumen del cálculo, localización del cálculo en el polo inferior, experiencia del cirujano, hidronefrosis y número de cálculos. Una puntuación alta indica una mayor probabilidad de ELC9.
RIRSEste sistema de puntuación contempla la densidad del cálculo (DC) (≤ 1.000 o > 1.000), la localización en el polo inferior (no inferior o inferior con AIP > 30° e AIP ≤ 30°), la longitud infundibular (≤ 25 o > 25 mm), la superficie del cálculo (≤ 10 o > 10 y ≤ 20 o > 20 mm). El rango de puntuación total es de cuatro a 10 puntos. Las puntuaciones altas se asocian a cálculos de mayor complejidad8.
Análisis estadísticoLos datos categóricos se presentaron como números y porcentajes por columnas. La conformidad de los datos continuos con la distribución normal se analizó con la prueba de Shapiro-Wilk. Los datos que se ajustaban a la distribución normal se presentaron como media ± desviación estándar, y los que no presentaban una distribución normal, como mediana y rango intercuartil (RIC). En la comparación de datos continuos, se utilizó la prueba t de muestras independientes o la prueba U de Mann-Whitney, según correspondiera. Para comparar los datos categóricos se realizó la prueba de χ2 de Pearson. Se evaluó la capacidad del DAC, el AC, el VC y los sistemas de puntuación para predecir el ELC mediante el análisis de las características operativas del receptor (ROC). Se comprobó que el AC y el VC tenían valores AUC similares para predecir el ELC. En los análisis posteriores se utilizó el AC, ya que puede obtenerse y calcularse fácilmente en la práctica clínica a partir de la TCSC o de la radiografía de riñón, uréter y vejiga.
Los parámetros que se encontraron significativamente correlacionados con el ELC y los que no fueron estadísticamente significativos, pero que se consideraron asociados al ELC, se incluyeron en el análisis de regresión logística multivariante. Se construyó un nuevo nomograma utilizando los coeficientes de regresión de las variables predictivas independientes. La capacidad predictiva del nomograma se evaluó con el análisis ROC, y se validó mediante el método bootstrap (n = 1.000). A continuación, se definió un nuevo sistema de puntuación basado en las ponderaciones de las variables del nomograma. El sistema de puntuación se evaluó con el análisis ROC. Un valor p < 0,05 se consideró estadísticamente significativo. Se utilizó el paquete de software SPSS (versión 23.0; IBM Corporation, Armonk, NY, EE. UU.) para los análisis estadísticos y el software R-project para la construcción del nomograma y la validación bootstrap.
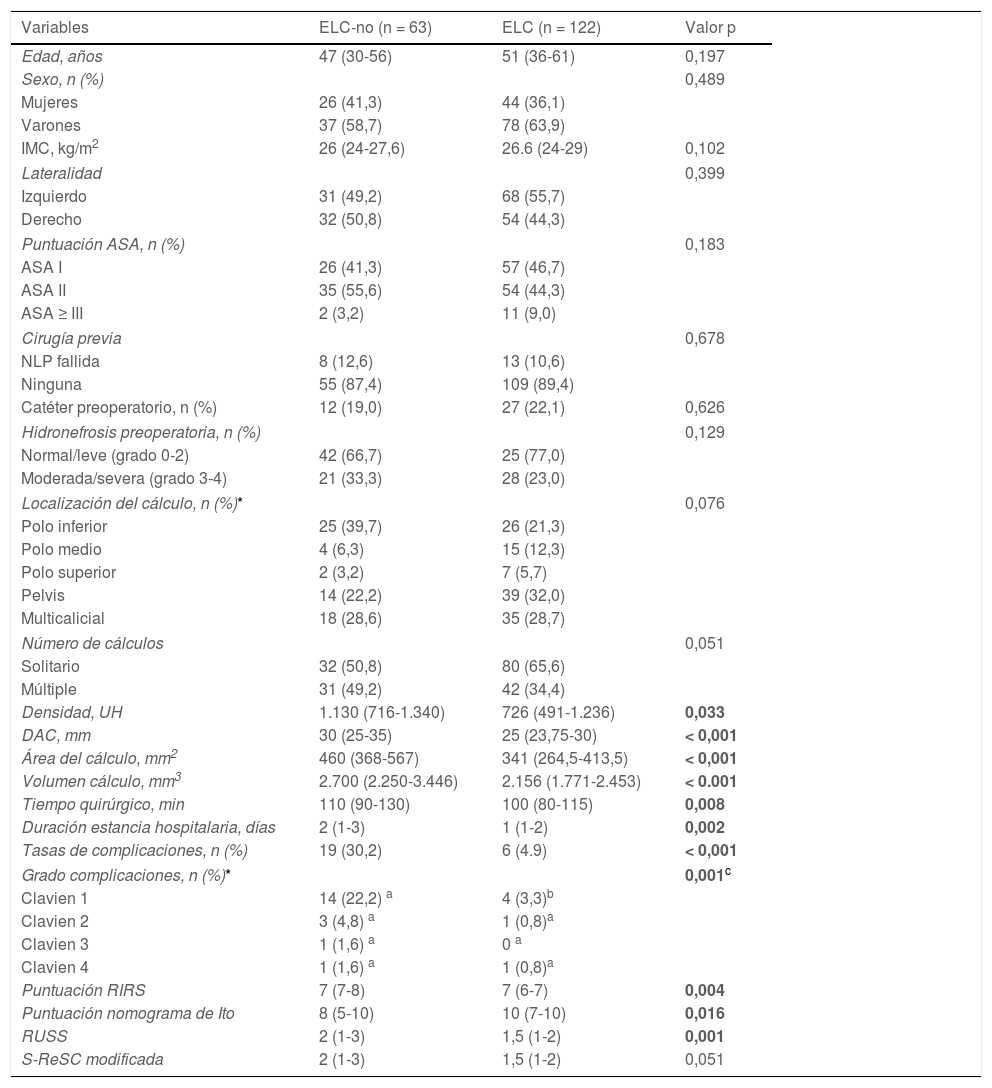
ResultadosSe incluyeron en el estudio un total de 185 pacientes. La mediana de edad de los pacientes era de 48 años (35-59). Las medianas del DAC, el AC y el VC fueron de 28 (25-32) mm, 368 (280-462) mm2 y 2.293 (1.933-2.732) mm3, respectivamente. La localización más frecuente de los cálculos fue la pelvis (28,6%), multicalicial (28,6%) y cáliz inferior (27,6%). La TLC total fue del 65,9% y las tasas de complicaciones fueron del 13,5%. Se produjeron complicaciones mayores en tres (1,6%) pacientes (urosepsis en dos y estenosis ureteral en uno). La comparación de las características y rasgos clínicos de los pacientes, según el ELC, se presenta en la tabla 1.
Comparación de las características de los pacientes según el ELC posoperatorio
| Variables | ELC-no (n = 63) | ELC (n = 122) | Valor p |
|---|---|---|---|
| Edad, años | 47 (30-56) | 51 (36-61) | 0,197 |
| Sexo, n (%) | 0,489 | ||
| Mujeres | 26 (41,3) | 44 (36,1) | |
| Varones | 37 (58,7) | 78 (63,9) | |
| IMC, kg/m2 | 26 (24-27,6) | 26.6 (24-29) | 0,102 |
| Lateralidad | 0,399 | ||
| Izquierdo | 31 (49,2) | 68 (55,7) | |
| Derecho | 32 (50,8) | 54 (44,3) | |
| Puntuación ASA, n (%) | 0,183 | ||
| ASA I | 26 (41,3) | 57 (46,7) | |
| ASA II | 35 (55,6) | 54 (44,3) | |
| ASA ≥ III | 2 (3,2) | 11 (9,0) | |
| Cirugía previa | 0,678 | ||
| NLP fallida | 8 (12,6) | 13 (10,6) | |
| Ninguna | 55 (87,4) | 109 (89,4) | |
| Catéter preoperatorio, n (%) | 12 (19,0) | 27 (22,1) | 0,626 |
| Hidronefrosis preoperatoria, n (%) | 0,129 | ||
| Normal/leve (grado 0-2) | 42 (66,7) | 25 (77,0) | |
| Moderada/severa (grado 3-4) | 21 (33,3) | 28 (23,0) | |
| Localización del cálculo, n (%)* | 0,076 | ||
| Polo inferior | 25 (39,7) | 26 (21,3) | |
| Polo medio | 4 (6,3) | 15 (12,3) | |
| Polo superior | 2 (3,2) | 7 (5,7) | |
| Pelvis | 14 (22,2) | 39 (32,0) | |
| Multicalicial | 18 (28,6) | 35 (28,7) | |
| Número de cálculos | 0,051 | ||
| Solitario | 32 (50,8) | 80 (65,6) | |
| Múltiple | 31 (49,2) | 42 (34,4) | |
| Densidad, UH | 1.130 (716-1.340) | 726 (491-1.236) | 0,033 |
| DAC, mm | 30 (25-35) | 25 (23,75-30) | < 0,001 |
| Área del cálculo, mm2 | 460 (368-567) | 341 (264,5-413,5) | < 0,001 |
| Volumen cálculo, mm3 | 2.700 (2.250-3.446) | 2.156 (1.771-2.453) | < 0.001 |
| Tiempo quirúrgico, min | 110 (90-130) | 100 (80-115) | 0,008 |
| Duración estancia hospitalaria, días | 2 (1-3) | 1 (1-2) | 0,002 |
| Tasas de complicaciones, n (%) | 19 (30,2) | 6 (4.9) | < 0,001 |
| Grado complicaciones, n (%)* | 0,001c | ||
| Clavien 1 | 14 (22,2) a | 4 (3,3)b | |
| Clavien 2 | 3 (4,8) a | 1 (0,8)a | |
| Clavien 3 | 1 (1,6) a | 0 a | |
| Clavien 4 | 1 (1,6) a | 1 (0,8)a | |
| Puntuación RIRS | 7 (7-8) | 7 (6-7) | 0,004 |
| Puntuación nomograma de Ito | 8 (5-10) | 10 (7-10) | 0,016 |
| RUSS | 2 (1-3) | 1,5 (1-2) | 0,001 |
| S-ReSC modificada | 2 (1-3) | 1,5 (1-2) | 0,051 |
ELC: estado libre de cálculos; IMC: índice de masa corporal; ASA: American Society of Anesthesiologists; UH: unidades Hounsfield; DAC, diámetro acumulado de los cálculos; S-ReSC: puntuación de la complejidad de cálculos renales de la Universidad Nacional de Seúl. Los valores en negritas muestra un valor de p < 0,05 que es considerado como estadísticamente significativo.
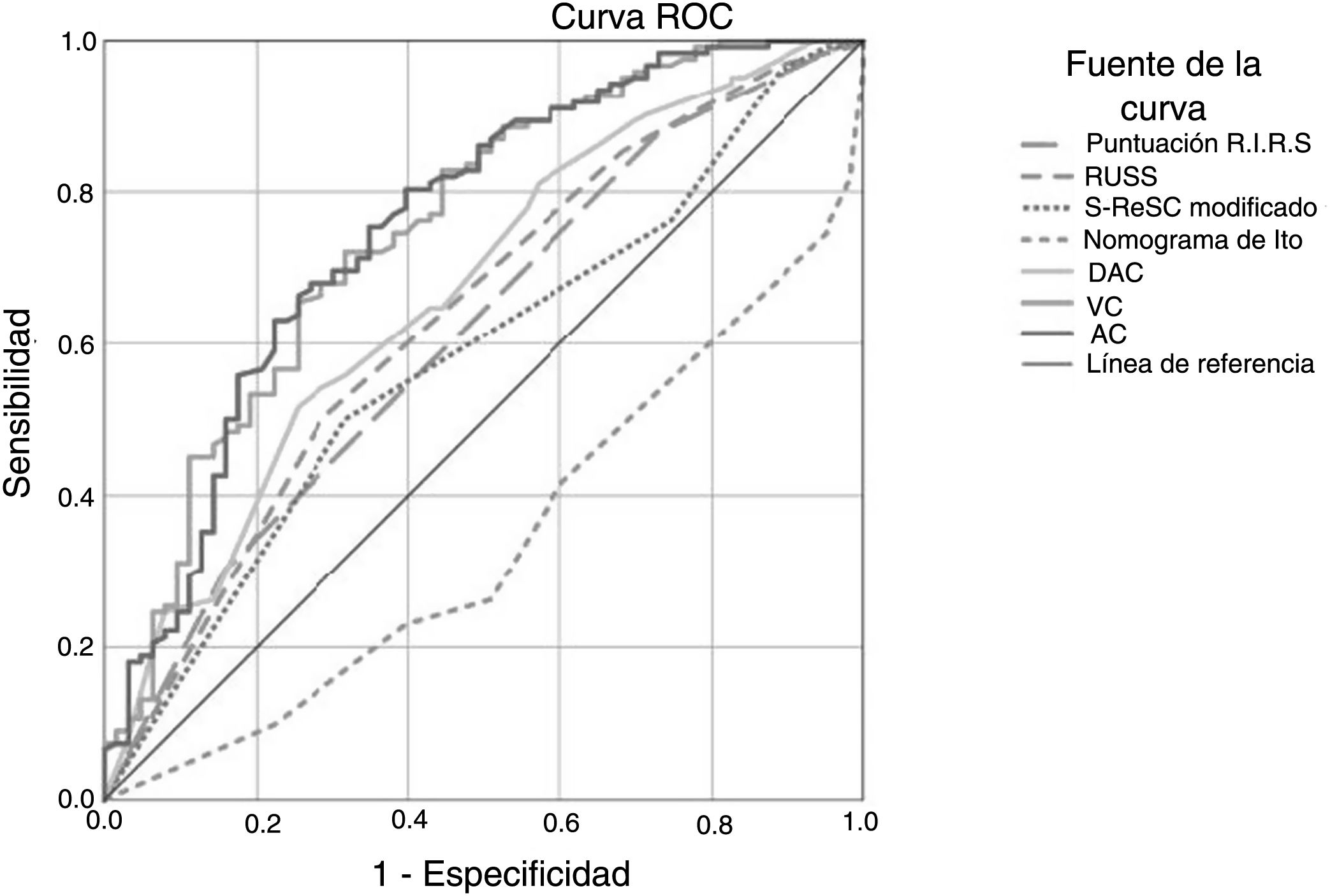
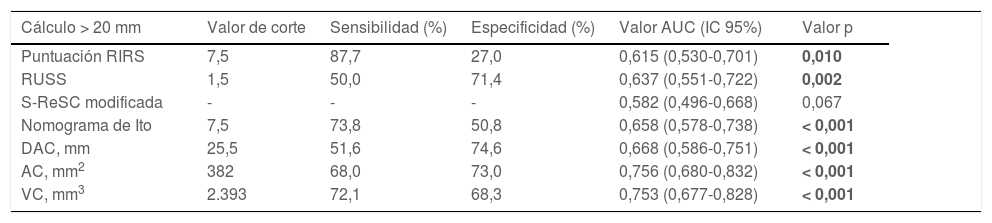
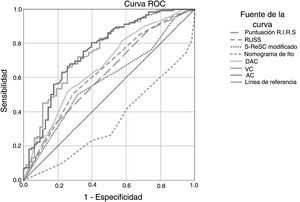
Se determinó que la densidad de los cálculos, el DAC, el AC, el VC, el tiempo quirúrgico, la duración de la estancia hospitalaria y la tasa de complicaciones fueron estadísticamente menores en los pacientes con ELC. Mientras que las puntuaciones RIRS y RUSS y el nomograma de Ito se asociaron con el ELC, no hubo asociación del ELC en la puntuación S-ReSC modificada. Las curvas ROC de los sistemas de puntuación, el DAC, el AC y el VC para la predicción del ELC se muestran en la figura 1, y sus valores de corte, sensibilidad, especificidad y AUC se tabulan en la tabla 2. Los resultados muestran que el sistema de puntuación S-ReSC modificado no tuvo capacidad predictiva del ELC. Aunque los demás sistemas de puntuación y el DAC pudieron predecir el ELC, se observó que sus valores AUC estaban alejados del valor óptimo. Se observó que el AC y el VC proporcionaban valores de predicción de AUC adecuados de 0,756 y 0,753, respectivamente. La tabla 3 muestra los resultados del análisis de regresión logística multivariante de los posibles factores predictivos. Solo la DC y el AC resultaron ser factores predictivos independientes del ELC. En el modelo creado mediante el método de eliminación hacia atrás, la DC, el AC, los cálculos múltiples y la localización de los cálculos resultaron ser marcadores independientes del ELC.
Valores de corte, sensibilidad, especificidad y AUC de los sistemas de puntuación, DAC, AC y VC para predecir el estado libre de cálculos
| Cálculo > 20 mm | Valor de corte | Sensibilidad (%) | Especificidad (%) | Valor AUC (IC 95%) | Valor p |
|---|---|---|---|---|---|
| Puntuación RIRS | 7,5 | 87,7 | 27,0 | 0,615 (0,530-0,701) | 0,010 |
| RUSS | 1,5 | 50,0 | 71,4 | 0,637 (0,551-0,722) | 0,002 |
| S-ReSC modificada | - | - | - | 0,582 (0,496-0,668) | 0,067 |
| Nomograma de Ito | 7,5 | 73,8 | 50,8 | 0,658 (0,578-0,738) | < 0,001 |
| DAC, mm | 25,5 | 51,6 | 74,6 | 0,668 (0,586-0,751) | < 0,001 |
| AC, mm2 | 382 | 68,0 | 73,0 | 0,756 (0,680-0,832) | < 0,001 |
| VC, mm3 | 2.393 | 72,1 | 68,3 | 0,753 (0,677-0,828) | < 0,001 |
AUC: área bajo la curva; DAC: diámetro acumulado del cálculo; AC: área cálculo; VC: volumen cálculo; S-ReSC: puntuación de la complejidad de cálculos renales de la Universidad Nacional de Seúl. Los valores en negritas muestra un valor de p < 0,05 que es considerado como estadísticamente significativo.
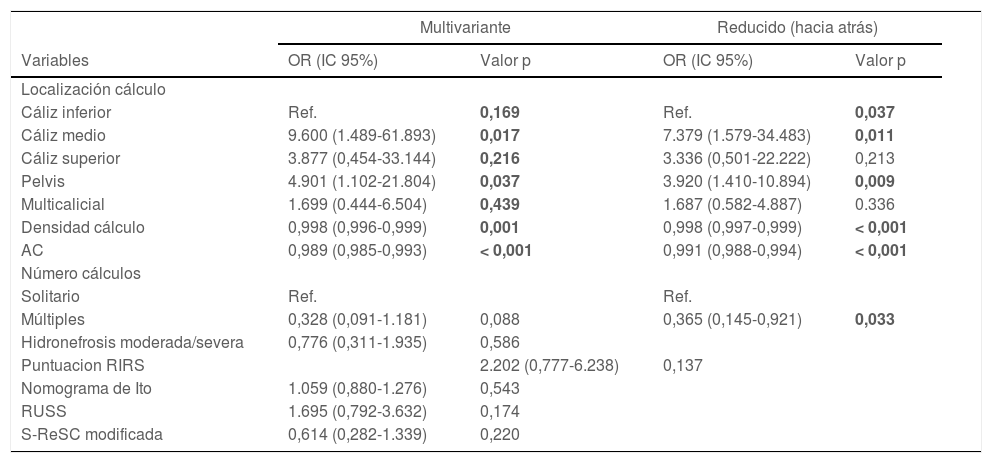
Análisis de regresión logística multivariante de los predictores independientes del estado libre de cálculos en el postoperatorio
| Multivariante | Reducido (hacia atrás) | |||
|---|---|---|---|---|
| Variables | OR (IC 95%) | Valor p | OR (IC 95%) | Valor p |
| Localización cálculo | ||||
| Cáliz inferior | Ref. | 0,169 | Ref. | 0,037 |
| Cáliz medio | 9.600 (1.489-61.893) | 0,017 | 7.379 (1.579-34.483) | 0,011 |
| Cáliz superior | 3.877 (0,454-33.144) | 0,216 | 3.336 (0,501-22.222) | 0,213 |
| Pelvis | 4.901 (1.102-21.804) | 0,037 | 3.920 (1.410-10.894) | 0,009 |
| Multicalicial | 1.699 (0.444-6.504) | 0,439 | 1.687 (0.582-4.887) | 0.336 |
| Densidad cálculo | 0,998 (0,996-0,999) | 0,001 | 0,998 (0,997-0,999) | < 0,001 |
| AC | 0,989 (0,985-0,993) | < 0,001 | 0,991 (0,988-0,994) | < 0,001 |
| Número cálculos | ||||
| Solitario | Ref. | Ref. | ||
| Múltiples | 0,328 (0,091-1.181) | 0,088 | 0,365 (0,145-0,921) | 0,033 |
| Hidronefrosis moderada/severa | 0,776 (0,311-1.935) | 0,586 | ||
| Puntuacion RIRS | 2.202 (0,777-6.238) | 0,137 | ||
| Nomograma de Ito | 1.059 (0,880-1.276) | 0,543 | ||
| RUSS | 1.695 (0,792-3.632) | 0,174 | ||
| S-ReSC modificada | 0,614 (0,282-1.339) | 0,220 | ||
OR: odds ratio; IC: intervalo de confianza; AC: área del cálculo; S-ReSC: puntuación de la complejidad de cálculos renales de la Universidad Nacional de Seúl. Los valores en negritas muestra un valor de p < 0,05 que es considerado como estadísticamente significativo.
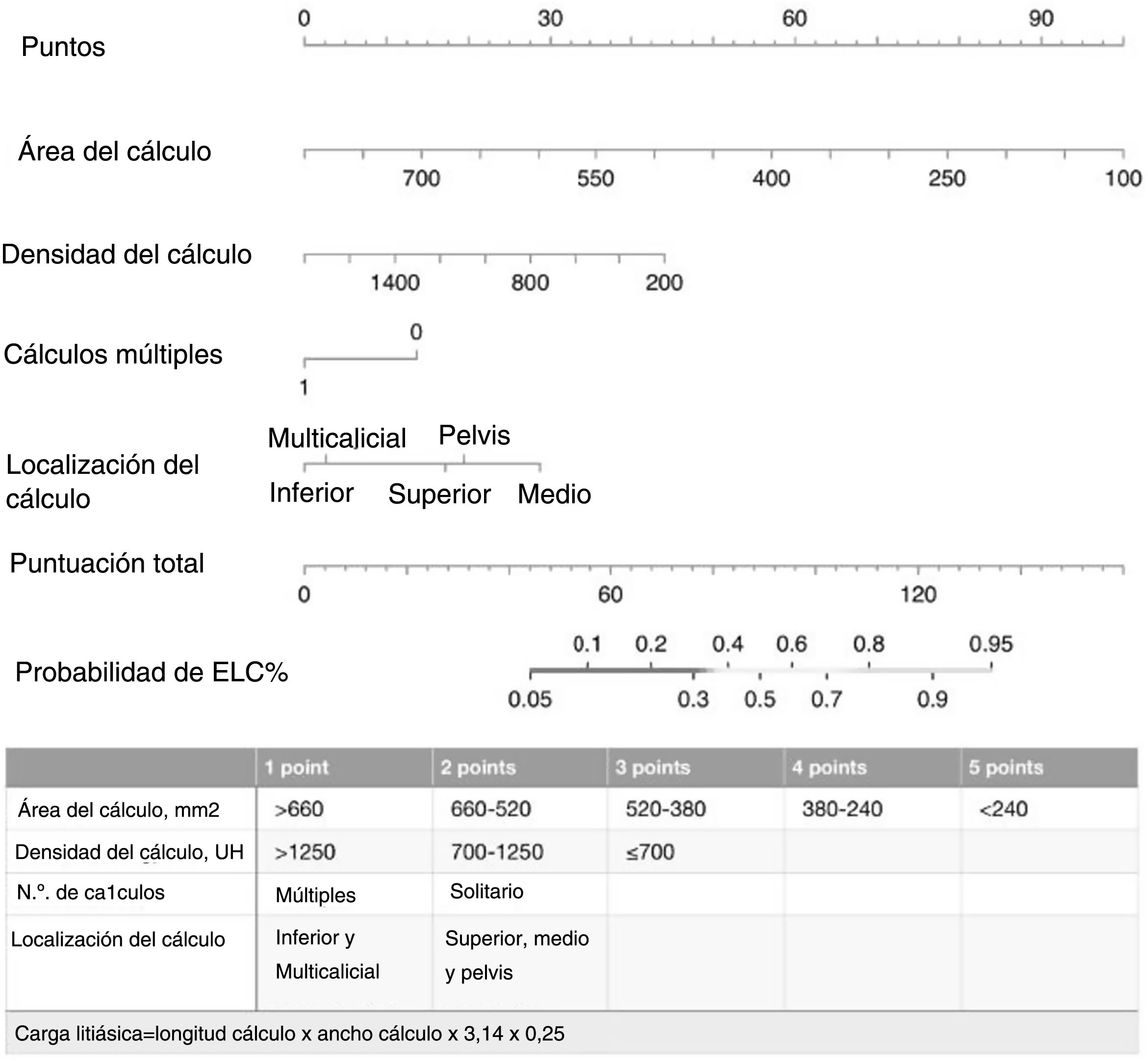
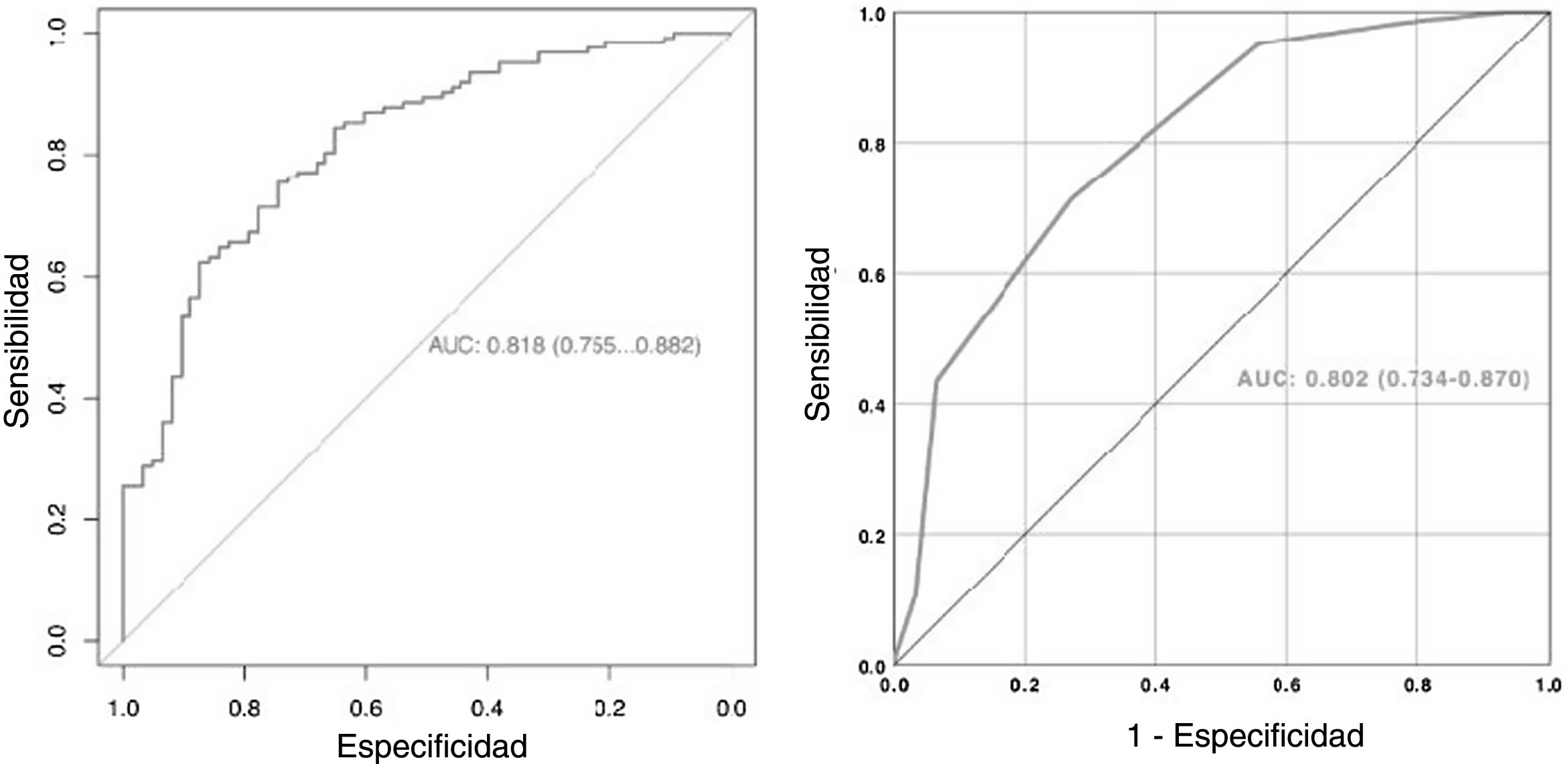
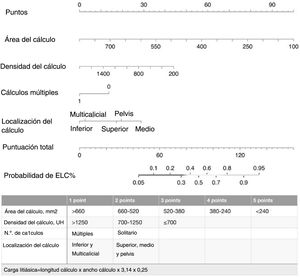
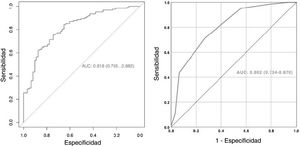
Se creó un nomograma utilizando los parámetros determinados como factores predictivos del ELC en el análisis multivariante. El valor AUC del nomograma se determinó como 0,818 (0,755-0,882). En la validación interna mediante el método bootstrap, el valor AUC medio optimizado del nomograma fue de 0,795 (figs. 2 y 3). Con el fin de hacerlo fácilmente aplicable en la práctica clínica, se desarrolló un sencillo sistema de puntuación (fig. 2). El AC se calificó con cinco puntos, la DC con tres puntos, y el número y la localización de los cálculos con dos puntos cada uno. La puntuación total osciló entre 4 y 12. Una puntuación alta indicaba una mayor probabilidad de ELC. El nuevo sistema de puntuación se aplicó a los pacientes de nuestra muestra uno a uno, y se procedió a su validación interna. La puntuación media fue de 9,2 ± 1,13 en el grupo con ELC y de 7,6 ± 1,46 en el grupo que no consiguió ELC (p < 0,001). El valor AUC del sistema de puntuación fue de 0,802 (0,734-0,870) (figs. 2 y 3). El valor de corte del sistema de puntuación para la predicción del ELC fue de 8,5, con el que obtuvo una sensibilidad del 71,3% y una especificidad del 73%.
La CRIR es una modalidad de tratamiento menos invasiva que la NLPC en el tratamiento de los cálculos renales. Las ventajas de la URS-f y los avances tecnológicos han hecho de la URS-f el método de elección en el tratamiento de cálculos renales de gran tamaño3,12. En estudios prospectivos en los que se comparó la URS-f con la NLPC estándar (cálculos de más de 20 mm) y la mini NLPC (cálculos de entre 20 y 30 mm), se informó de que la URS-f tenía una TLC final comparable a la de la NLPC, y se indicó como opción de tratamiento adecuada para los cálculos renales voluminosos13,14. En los estudios, la mini-NLP tiene un tiempo quirúrgico similar y una TLC inicial más alta en comparación con la URS-f en cálculos de 2-3 cm. Sin embargo, la URS-f tiene una duración más corta de estancia hospitalaria, menores tasas de complicaciones y una TLC final similar a la mini-NLP con una media de 1,5 procedimientos14. Según un metaanálisis reciente, la TLC inicial de la URS-f fue del 71,2%, y la TLC final del 89,4%, con un número medio de 1,4 procedimientos15. En otro estudio, la TLC inicial fue del 73,3% y la TLC final del 93% con un número medio de 1,2 procedimientos para cálculos de 2-2,9 cm y la TLC final fue del 84,5% con un número medio de 1,8 procedimientos para cálculos de 3-3,9 cm. En el mismo estudio, la TLC global fue del 61,9% en una sola sesión3. En nuestro estudio, la TLC global tras una única sesión fue del 65,9%, y nuestra tasa de complicaciones del 13,5% resultó ser similar a la publicada16,17.
La precisión en la predicción de la TLC es importante a la hora de considerar las modalidades quirúrgicas y la necesidad de cualquier procedimiento complementario. En este contexto, se han desarrollado numerosos sistemas de puntuación para la CRIR. La escala RUSS, S-ReSC, el nomograma de Ito y RIRS son los sistemas de puntuación más conocidos6–9. Se han realizado estudios de validación individuales y múltiples de estos sistemas de puntuación y se han discutido ampliamente16,18–21. Sin embargo, todos los estudios sobre sistemas de puntuación y su validación, excepto el nomograma de Ito, consistieron en pacientes con cálculos < 2 cm. Ito et al. desarrollaron un nomograma en una serie con cálculos de tamaño medio de 22 mm e informaron de que el valor del AUC era de 0,870. En los estudios de validación, el valor del AUC osciló entre 0,697 y 0,735 en cálculos de un tamaño medio de 10,9-15,6 mm9,16,18. Aunque el nomograma de Ito incluyó a pacientes con cálculos > 2 cm, su utilidad en cálculos renales grandes sigue sin estar clara, ya que tanto el tamaño medio de los cálculos como la presencia simultánea de cálculos < 2 cm provocarían un sesgo positivo.
En nuestro estudio se realizó la validación externa de los sistemas de puntuación existentes en cálculos renales de 2-4 cm, y se observó que no tenían suficiente capacidad predictiva del ELC. Se comprobó que el DAC, el AC y el VC eran superiores a los sistemas de puntuación cuando se evaluaban individualmente. Se determinó que el sistema de puntuación con peor desempeño era el S-ReSC modificado (AUC: 0,582). Este resultado puede atribuirse al hecho de que este sistema de puntuación no contempla las características de los cálculos. Según este sistema de puntuación, se puede asignar la misma puntuación a un cálculo de 1 cm y a un cálculo de 3 cm si tienen la misma localización. Además, los autores recomiendan la NLPC para los cálculos más grandes, por lo que excluyen estos cálculos de su análisis7. También se observó que el nomograma de Ito (AUC: 0,658) y el RUSS (AUC: 0,637) tuvieron mejores resultados que otros sistemas de puntuación. La característica más importante que distingue a estos sistemas de puntuación de los demás es la clasificación de los cálculos de gran tamaño6,9. Aunque el nomograma de Ito calificó el VC y el RUSS los cálculos de más de 20 mm no predijeron completamente el ELC. Esto puede deberse al uso del diámetro del cálculo para indicar la carga litiásica en el sistema de puntuación RUSS. El DAC no refleja plenamente la carga litiásica en los cálculos renales grandes22. El nomograma de Ito y el RUSS no incluyen la densidad de los cálculos, cuya correlación con el ELC se ha demostrado en muchos estudios23. Aunque se sabe que la litotricia láser puede fragmentar cualquier cálculo, hay una fragmentación más indirecta y un menor tiempo operatorio en los cálculos con baja densidad23,24. Además, el nomograma de Ito detectó la presencia de hidronefrosis como marcador independiente, mientras que la presencia de hidronefrosis moderada/severa no se detectó como marcador en nuestro conjunto de datos9. Todas las cuestiones indicadas anteriormente pueden explicar la insuficiencia del RUSS y del nomograma de Ito en la predicción del ELC.
Los estudios que evaluaron los factores predictivos del ELC tras la CRIR en cálculos renales grandes informaron de la carga litiásica, la localización en el cáliz inferior, la localización multicalicial y la hidronefrosis moderada/severa como factores predictivos25,26. En nuestro estudio, el AC, la densidad, el número y la localización de los cálculos se determinaron como marcadores predictivos independientes del ELC. La relación entre el AIP y el ELC se ha demostrado en la literatura27. Sin embargo, en nuestro estudio, aunque la TLC fue baja en los pacientes con un AIP bajo, no fue estadísticamente significativa. Esto puede deberse al número reducido de pacientes con un AIP bajo y a la inclusión de pacientes con cálculos ubicados en otras zonas además del cáliz inferior. Los cálculos del cáliz inferior y los cálculos multicaliciales tuvieron las TLC más bajas, con un 51 y un 66%, respectivamente. Huang et al. informaron de resultados similares para los cálculos del cáliz inferior y los cálculos multicaliciales3. En nuestro estudio, aunque el antecedente de NLPC fallida y la presencia de hidronefrosis fueron elevados entre los pacientes con cálculos residuales, esto no fue estadísticamente significativo. Pensamos que la TLC baja en los pacientes con NLPC fallida puede estar relacionada con la dificultad de acceso al cálculo debido a los cambios anatómicos y a una probabilidad menor de eliminación espontánea del cálculo. Resultados similares se obtuvieron en los estudios de Güzel et al.28 En nuestro estudio, la colocación preoperatoria de un stent no se asoció al ELC. En la literatura se afirma que la colocación de un stent en el preoperatorio aumenta el éxito de la inserción de una vaina de acceso ureteral y que no se asocia al ELC29.
Nuestro estudio es el primero en la literatura que evalúa la eficacia de los sistemas de puntuación existentes para predecir el éxito de la CRIR en cálculos de 2-4 cm y presenta un nuevo sistema de puntuación desarrollado a partir de marcadores predictivos. Se confirmó la utilidad de este sistema en cálculos de gran tamaño (valor AUC de 0,802). Las principales limitaciones de nuestro estudio son su naturaleza retrospectiva y el número limitado de pacientes. Otras limitaciones son la exclusión de casos complejos, como las anomalías musculoesqueléticas y los cálculos de estruvita, así como la imposibilidad de evaluar la composición de los cálculos. Por otro lado, nuestro estudio tiene ciertas fortalezas, como la estandarización del ELC mediante la realización de una TCSC de control al primer mes en todos los pacientes, el diseño multicéntrico y la reproducibilidad de los resultados. Sin embargo, sigue siendo necesario realizar estudios prospectivos con una serie más amplia centrada sobre todo en las complicaciones y la validación del sistema en cálculos más pequeños.
ConclusiónEl sistema de puntuación desarrollado, basado en el AC, la densidad, el número y la localización de los cálculos tuvo una capacidad predictiva mayor que las escalas de puntuación existentes. Nuestro nuevo sistema de puntuación puede predecir de forma fiable el ELC en pacientes con cálculos de 2 a 4 cm, lo que puede orientar al cirujano en la elección del tratamiento óptimo.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.