Programa de Actividades Preventivas y de Promoción de la Salud-PAPPS 2024
Más datosEl envejecimiento de la población es un fenómeno global que está aumentando la proporción de las personas mayores, especialmente aquellas de más de 80 años. Este incremento en la longevidad no siempre se traduce en años de buena calidad de vida. Este documento evalúa la evidencia más reciente sobre las principales actividades preventivas en las personas mayores, comenzando por los grandes síndromes geriátricos como la fragilidad, el deterioro cognitivo y el aislamiento social. Se analizan intervenciones directas en nutrición, deprescripción y ejercicio físico. Además, por primera vez, se incluye un análisis de actividades preventivas en relación con el suicidio en las personas mayores, coordinado con programas de salud mental. La fragilidad, definida como el deterioro progresivo de los sistemas fisiológicos, es un predictor significativo de eventos adversos de salud y se considera potencialmente reversible, especialmente en sus fases tempranas. El diagnóstico y manejo de la fragilidad mediante una valoración geriátrica integral (VGI) y la implementación de intervenciones específicas como el ejercicio multicomponente, la nutrición adecuada y la revisión de medicamentos, son clave para mejorar la funcionalidad y calidad de vida de las personas mayores.
Population aging is a global phenomenon that is increasing the proportion of older people, particularly those over 80 years old. This increase in longevity does not always translate into years of good quality of life. This document reviews the latest evidence on the main preventive activities for older adults, starting with major geriatric syndromes such as frailty, cognitive impairment, and social isolation. It evaluates direct interventions in nutrition, deprescription, and physical exercise. Additionally, for the first time, it includes an analysis of preventive activities related to suicide in older adults, coordinated with mental health promotion programs. Frailty, defined as the progressive deterioration of physiological systems, is a significant predictor of adverse health events and is considered potentially reversible, especially in its early stages. The diagnosis and management of frailty through comprehensive geriatric assessment (CGA) and the implementation of specific interventions such as multicomponent exercise, adequate nutrition, and medication review are key to improving the functionality and quality of life of older adults.
El envejecimiento de la población es un fenómeno global que está incrementando la proporción de las personas mayores, especialmente la de mayores de 80 años. Sin embargo, este aumento en la longevidad no siempre se traduce en años con buena calidad de vida.
Esta actualización busca evaluar la evidencia más reciente en torno a las principales actividades preventivas en las personas mayores. Empezando por el análisis de grandes síndromes geriátricos y situaciones como fragilidad, deterioro cognitivo (DC) y aislamiento social, posteriormente se evalúan las intervenciones más directas en nutrición, deprescripción y ejercicio físico. Por primera vez se incluye un análisis de las actividades preventivas en relación con el suicidio en las personas mayores, realizada de forma coordinada con el programa de actividades preventivas y promoción de la salud mental, a cuya actualización remitimos para ampliar información.
Prevención y manejo de la fragilidad en la persona mayorLa fragilidad se define como el deterioro progresivo relacionado con la edad de los sistemas fisiológicos que provoca una disminución de las reservas de la capacidad intrínseca, lo que confiere una mayor vulnerabilidad a los factores de estrés y aumenta el riesgo de una serie de resultados sanitarios adversos1,2.
Está íntimamente relacionada con la pérdida de funcionalidad de las personas mayores, y es uno de los mejores predictores de eventos como hospitalización, caídas, discapacidad y muerte. En España, la prevalencia de fragilidad en las personas de 65 o más años es del 18% (15-21%) siendo algo menor a nivel comunitario 12% (10-15%) y mucho mayor en ámbitos no comunitarios 45% (27-63%). Aunque aumenta con la edad, no es una consecuencia inevitable del proceso de envejecimiento. Se trata de una entidad potencialmente reversible especialmente en fases tempranas, de ahí la relevancia de su detección y manejo precoz con el propósito de retrasar o evitar el deterioro funcional. La detección precoz e intervención sobre fragilidad constituye una de las principales estrategias en el objetivo global de promover el envejecimiento activo sin discapacidad o dependencia, siendo la atención primaria (AP) el medio asistencial primordial en esta estrategia2.
La referencia clave en nuestro medio para su desarrollo e implantación es el documento de consenso sobre prevención de la fragilidad en la persona mayor del Ministerio de Sanidad, actualizado en 20222.
Principales herramientas para la detección y el diagnóstico de fragilidad2-9Existen 2 modelos conceptuales de fragilidad en los cuales se basa, principalmente, el diagnóstico de este síndrome geriátrico:
- •
El modelo físico o fenotipo de Fried concibe la fragilidad como un síndrome biológico, cuyo exponente es la escala de Fried que basa el diagnóstico en 5 criterios: pérdida de peso, debilidad muscular, baja energía, lentitud en la marcha y bajo nivel de actividad física. Su aplicación lleva unos 10min, y tiene la limitación de requerir un dinamómetro.
- •
El modelo acumulativo de déficits o multidimensional entiende la fragilidad como el efecto final de acumulación de déficits en diferentes dominios o áreas (enfermedades, signos o síntomas, hallazgos de laboratorio, funcional, mental y social), cuyo prototipo es el índice de fragilidad (FI) o su versión electrónica (eFI), basado en los ítems de una valoración geriátrica integral (VGI); es más complejo de obtener por lo que apenas se emplea en nuestro medio, bien por el tiempo que requiere, la calidad de registros en la historia electrónica o la falta de desarrollo de su versión electrónica.
Se ha propuesto también como herramienta para el diagnóstico de fragilidad la escala de rasgos de fragilidad - forma corta - 5 items2 (Frailty Trait Scale-Short Form [FTS-5]) desarrollada y validada en población española, pero que no se utiliza en nuestro entorno de AP. Identifica 7 dimensiones de la fragilidad: equilibrio energético/nutricional, actividad física, sistema nervioso, sistema vascular, resistencia y velocidad de marcha.
En base a estos 2 modelos conceptuales se han desarrollado múltiples herramientas para su uso en el cribado/case-finding de fragilidad que identifican a aquellos en riesgo de fragilidad o que ya la han desarrollado. Algunas de ellas son:
- •
La escala FRAIL7: comparte características de ambos modelos, el físico (pérdida de peso, cansancio, deambulación, marcha) y el multidimensional (tener más de 5 enfermedades). Numerosos estudios han validado su capacidad predictiva. Destaca por la sencillez de su aplicación al no requerir material complementario ni apenas instrucción. Demuestra una buena validez de criterio y confiabilidad test-retest, sin embargo, se necesita más investigación sobre la validez de constructo y capacidad para detectar cambios a lo largo del tiempo8. Una revisión sistemática (RS) reciente encuentra el punto de corte óptimo para la detección de fragilidad en 2 puntos9.
- •
Las pruebas de ejecución: son las más recomendadas y usadas para el cribado de fragilidad en nuestro ámbito. Valoran la capacidad y el tiempo de realización por la persona de determinadas acciones de marcha, movilidad o equilibrio. Por lo tanto, se relacionan fundamentalmente con el dominio físico de la fragilidad. Son rápidas y factibles de realizarse en la mayoría de las consultas de AP.
- •
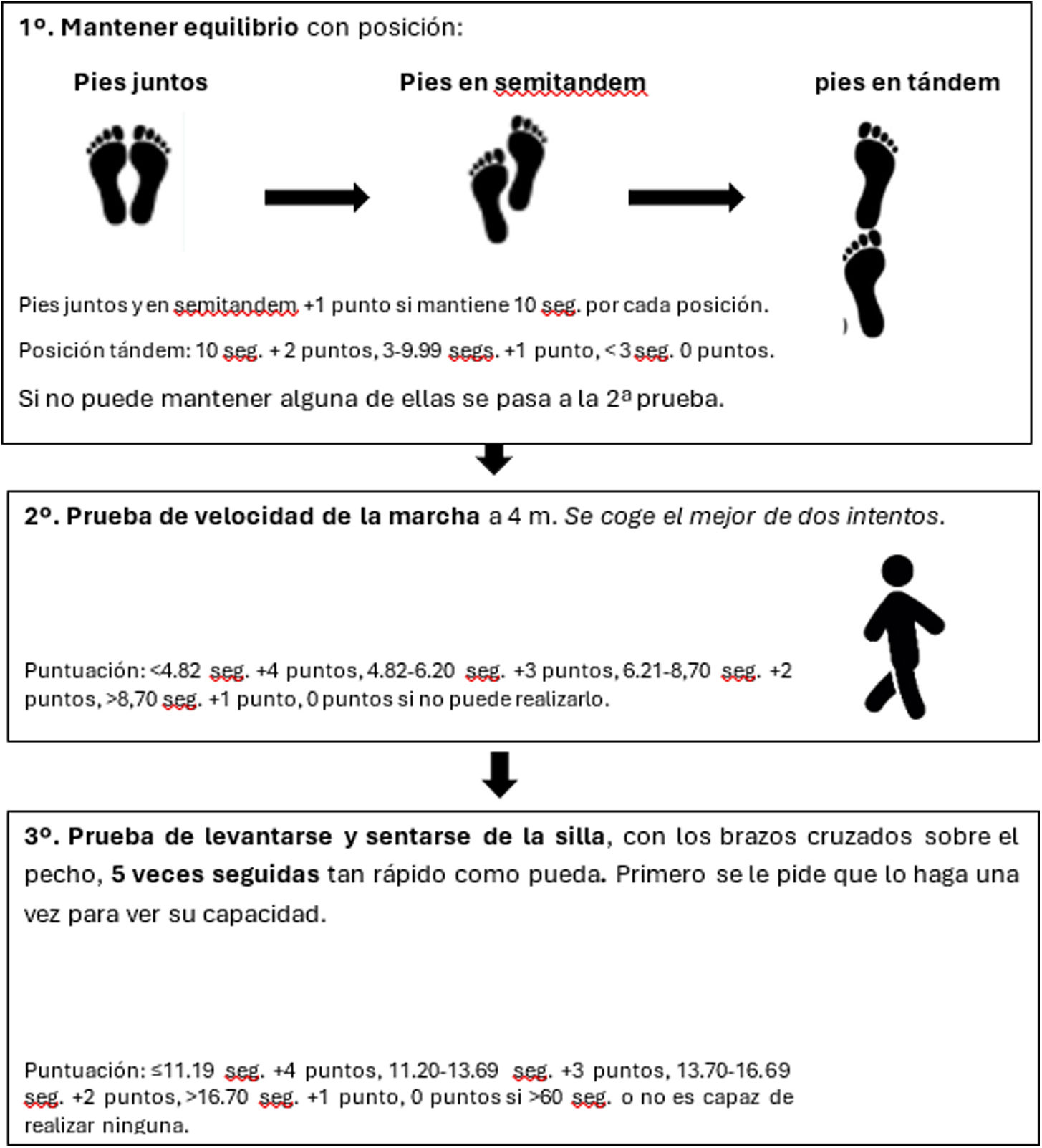
Prueba corta de desempeño físico o Short Physical Performance Battery (SPPB). Validada y normalizada en nuestro medio, es la más completa. Combina pruebas de equilibrio (en posición de pies juntos, en semitándem y en tándem) velocidad de la marcha (VM) en 4m, y levantarse y sentarse de una silla con los brazos cruzados) (fig. 1). Con una puntuación <10s se considera que existe una alta probabilidad de fragilidad.
Figura 1.Short Physical Performance Battery (SPPB) o test de Guralnik. Fuente: Traducida y modificada por el autor de Hagedorn et al.68.
(0.17MB). - •
La VM: tiempo que se tarda en caminar 3, 4 o 6m. El punto de corte con mejor valor predictivo de fragilidad se sitúa en los 0,8m/s.
- •
Prueba levántate y anda cronometrado o Test Up and Go (TUG): Tiempo que se tarda en levantarse de la silla, caminar 3m, y volver a sentarse de nuevo en la silla. Punto de corte para fragilidad situado en >12s.
Otras escalas utilizadas en la detección de fragilidad son: la escala de fragilidad clínica Clinical Frailty Scale (CFS)4. Utiliza descriptores clínicos y representaciones gráficas para estratificar los adultos mayores según el nivel de vulnerabilidad. Va desde el estadio 1 (robusto) al 9 (enfermo terminal), se basa en el juicio clínico y considera fragilidad una puntuación ⪈5. Su administración requiere muy poco tiempo (<30s). La escala PRISMA-7 y el instrumento Integrated Care for Older People (ICOPE) de la Organización Mundial de la Salud (OMS), que se desarrolló para cribar la pérdida de capacidad intrínseca a través de 6 áreas: estado cognitivo, movilidad, malnutrición, alteración visual o auditiva, o depresión; se dispone de una versión electrónica de este último que facilita su aplicación7. El índice frágil-VIG10, basado en la VGI, se utiliza en AP en Cataluña, como instrumento que permite una evaluación rápida del grado de fragilidad, en los pacientes crónicos complejos (calculadora disponible en: https://es.c3rg.com/index-fragil-vig).
No siempre existe un límite claro entre las pruebas de detección y las de diagnóstico. La mayoría de los estudios sobre las herramientas de valoración de la fragilidad se han llevada a cabo en cohortes poblacionales y menos en el ámbito clínico, donde se ha observado una escasa concordancia entre los diferentes instrumentos, una gran variabilidad en cuanto a su factibilidad, tiempo de aplicación y diferencias según el entorno clínico de aplicación (atención primaria, geriatría…); como demuestra el estudio Frailtools4 que compara 8 herramientas de evaluación de fragilidad comúnmente empleadas (el fenotipo de fragilidad, SHARE-FI, la escala de rasgos de fragilidad FTS-3 y FTS-5, la escala FRAIL, el FI-35, la herramienta de evaluación de fragilidad del Gérontopole (GFST) y la CFS; los hallazgos sugieren que la mayoría de las herramientas evaluadas están abordando diferentes constructos de fragilidad o la existencia de distintos subtipos clínicos de fragilidad, posibilidad planteada recientemente por algunos autores y que requiere una mayor investigación.
En su mayoría son herramientas sensibles, pero a menudo muestran una baja especificidad y muy bajo valor predictivo positivo4, lo que cuestiona su utilidad en la práctica clínica.
El consenso del Ministerio de Sanidad2 propone para la AP la selección, mediante captación activa oportunista, de las personas de 70 o más años sin alteración importante en actividades básicas de la vida diaria (ABVD, índice de Barthel ≥90 puntos). Recomienda como herramientas de cribado preferentemente las pruebas de ejecución SPPB o el test de VM en 4m como otras posibles opciones, el TUG o la escala FRAIL. La escala FRAIL puede ser de utilidad cuando los pacientes no pueden ser valorados presencialmente, ante imposibilidad de realizar las pruebas de ejecución o bien, en estrategias de detección en otros espacios del ámbito comunitario.
Considera una alta probabilidad de fragilidad cuando las pruebas de detección precoz están alteradas (SPPB<10 puntos, VM<0,8m/s, TUG>12s, FRAIL≥1) y dada la dificultad para establecer el diagnóstico en AP utilizando el fenotipo de Fried o el multidimensional FI, propone el inicio de la intervención para abordar la fragilidad, a ser posible en el marco de una VGI, en las personas con dichas pruebas alteradas.
Intervenciones en fragilidadEl manejo tras el diagnóstico de fragilidad debiera hacerse, idealmente, en forma de una VGI, que se caracteriza por un enfoque multidimensional y centrado en la función. Permite establecer e individualizar intervenciones específicas en el marco de una valoración global.
La VGI no está extendida en la AP, además de su complejidad, la evidencia de su efectividad en este medio es menos clara. Una RS11 de ensayos clínicos aleatorios (ECA) que evalúa la efectividad de diferentes intervenciones en fragilidad en el ámbito comunitario encuentra que la VGI redujo la fragilidad en comparación al grupo control, en base principalmente a los resultados de un ensayo clínico en ≥75 años con multimorbilidad y 3 o más ingresos en el último año, en una unidad geriátrica ambulatoria. La RS Cochrane de Briggs et al.12 concluyen que la VGI en el anciano frágil o de riesgo en la comunidad, no tiene impacto en la mortalidad o institucionalización y, con una evidencia de calidad baja, que puede disminuir el riesgo de hospitalización no planificada.
Por otro lado, se ha desarrollado alguna experiencia de la VGI adaptada o rápida como, p, ej., la dirigida al manejo (identificación de posibles causas subyacentes y su tratamiento) de los 5 componentes de la escala FRAIL7.
En esta línea, la herramienta VALINTAN (http://www.valintan.com) es una informatización de la VGI dirigida a la AP, orientada a la funcionalidad y fragilidad, que facilita su realización y se focaliza en intervenciones facilitadas en base a diagnósticos geriátricos que a su vez se relacionan con la pérdida de función o fragilidad13. Su efectividad ha de ser explorada más ampliamente.
Tras la valoración, los aspectos clave de la intervención en fragilidad son: el ejercicio físico (programas de ejercicio multicomponente), evaluación y recomendaciones nutricionales y revisión/adecuación de la medicación.
Varias RS de ensayos clínicos aleatorizados exploran el efecto del ejercicio y/o la nutrición en ancianos frágiles en la comunidad, una de ellas citada anteriormente11, concluye que el ejercicio físico (predominantemente ejercicios de resistencia) solo o con educación nutricional puede reducir la fragilidad física. En la misma línea, una RS con metaanálisis en red de 56 ECA (33, ámbito comunitario)14, recientemente publicada, compara la eficacia de varias intervenciones no farmacológicas en la reducción de la fragilidad en el mayor (ejercicio físico, suplementación nutricional, entrenamiento cognitivo, intervención multicomponente, VGI, telemonitorización en domicilio). El ejercicio físico, intervención multicomponente e intervención nutricional se asociaron con una reducción de la fragilidad en comparación con la atención habitual, de ellas el ejercicio fue el tipo de intervención más eficaz y de las modalidades de ejercicio, el entrenamiento de resistencia (certeza de la evidencia de moderada a muy baja).
En otra RS15, con una calidad de evidencia moderada, las intervenciones en nutrición (incluida la suplementación proteica) o combinadas con actividad física producen un pequeño pero significativo efecto en medidas de función física y movilidad. En la RS de Khoret al.16, las intervenciones multifactoriales fueron más eficaces que la nutricional aislada en mejorar el estatus de fragilidad y rendimiento físico.
El programa de ejercicios de Otago17 dirigido a adultos mayores con fragilidad o prefragilidad puede también reducir la fragilidad, mejorar la capacidad de equilibrio físico y movilidad (certeza baja a moderada).
El programa VIVIFRAIL (http://www.vivifrail.com) es un ejemplo de programa de promoción de ejercicio físico multicomponente que se ha implantado en algunas comunidades autónomas.
Otras intervenciones, aunque no específicas de fragilidad, incluyen las dirigidas a la valoración y prevención del riesgo de caídas, manejo de la multimorbilidad y otros síndromes geriátricos.
Además, el abordaje de la fragilidad debe ser interdisciplinar, requiere la coordinación de los diferentes agentes implicados, sociales, comunitarios y niveles asistenciales sanitarios.
Recomendaciones
- •
Se recomienda una detección activa oportunista de fragilidad en atención primaria (AP) en las personas ≥70 años.
- •
En AP se recomiendan, para la detección de fragilidad, herramientas sencillas, validadas y aplicables en este medio asistencial.
- •
La detección se inicia con una preselección en base a la edad (≥70 años), sin alteración en las actividades básicas de la vida diaria (ABVD, índice de Barthel ≥90 puntos), seguido de pruebas de ejecución (Short Physical Performance Battery [SPPB] o la velocidad de la marcha [VM]) y valoración del riesgo de caídas.
- •
También pueden emplearse en la detección de fragilidad el test levántate y anda o Test Up and Go (TUG) o la escala FRAIL.
- •
El manejo posterior de las personas frágiles se aconseja realizar a través de una valoración geriátrica integral (VGI), de la que se derivan las intervenciones específicas individualizadas a llevar a cabo. Herramientas como VALINTAN facilitan la aplicación de la VGI en AP.
- •
Se recomienda el ejercicio multicomponente, adaptado en intensidad y estructurado, como intervención principal para prevenir y/o retrasar la pérdida funcional en la fragilidad. Ejemplo: programa VIVIFRAIL (http://www.vivifrail.com).
- •
Otras intervenciones recomendadas son: la intervención nutricional, revisión y adecuación de la medicación y el correcto manejo de situaciones clínicas coincidentes (multimorbilidad y otros síndromes geriátricos).
La demencia es una de las principales causas de discapacidad y dependencia de las personas mayores y la séptima causa de muerte a nivel mundial, por lo que la OMS la ha reconocido como una prioridad de salud pública. Se estima que hay 10 millones de casos nuevos en el mundo todos los años. Puede estar provocada por diferentes causas, pero la más frecuente es la enfermedad de Alzheimer, que supone el 60-70% de los casos18. La prevalencia de demencia aumenta con la edad, oscilando entre el 3% entre las personas de 65 a 70 años y el 35% entre las personas de 90 o más años19.
La demencia tiene impactos físicos, psicológicos, sociales y económicos, no solo para las personas que viven con demencia, sino también para sus cuidadores, sus familias y la sociedad en general18. Las mujeres se ven mucho más afectadas, tanto por la enfermedad como por el cuidado, ya que proporcionan el 70% de horas de cuidado18.
En la demencia hay una disminución significativa en uno o más dominios cognitivos (atención compleja, función ejecutiva, aprendizaje y memoria, lenguaje, función motora perceptiva y cognición social) respecto al nivel previo, que interfiere con la independencia de la persona en las actividades de la vida diaria20,21.
En el deterioro cognitivo leve (DCL), los déficits adquiridos (uno o varios) no interfieren, o lo hacen muy levemente, en las actividades de la vida diaria. Esta situación puede revertir, estacionarse en el tiempo, o progresar a demencia, por lo que es importante su evaluación y seguimiento20.
El término DC (resultado de pruebas cognitivas objetivas por debajo de lo esperable por edad y educación)21se aplica a ambas situaciones.
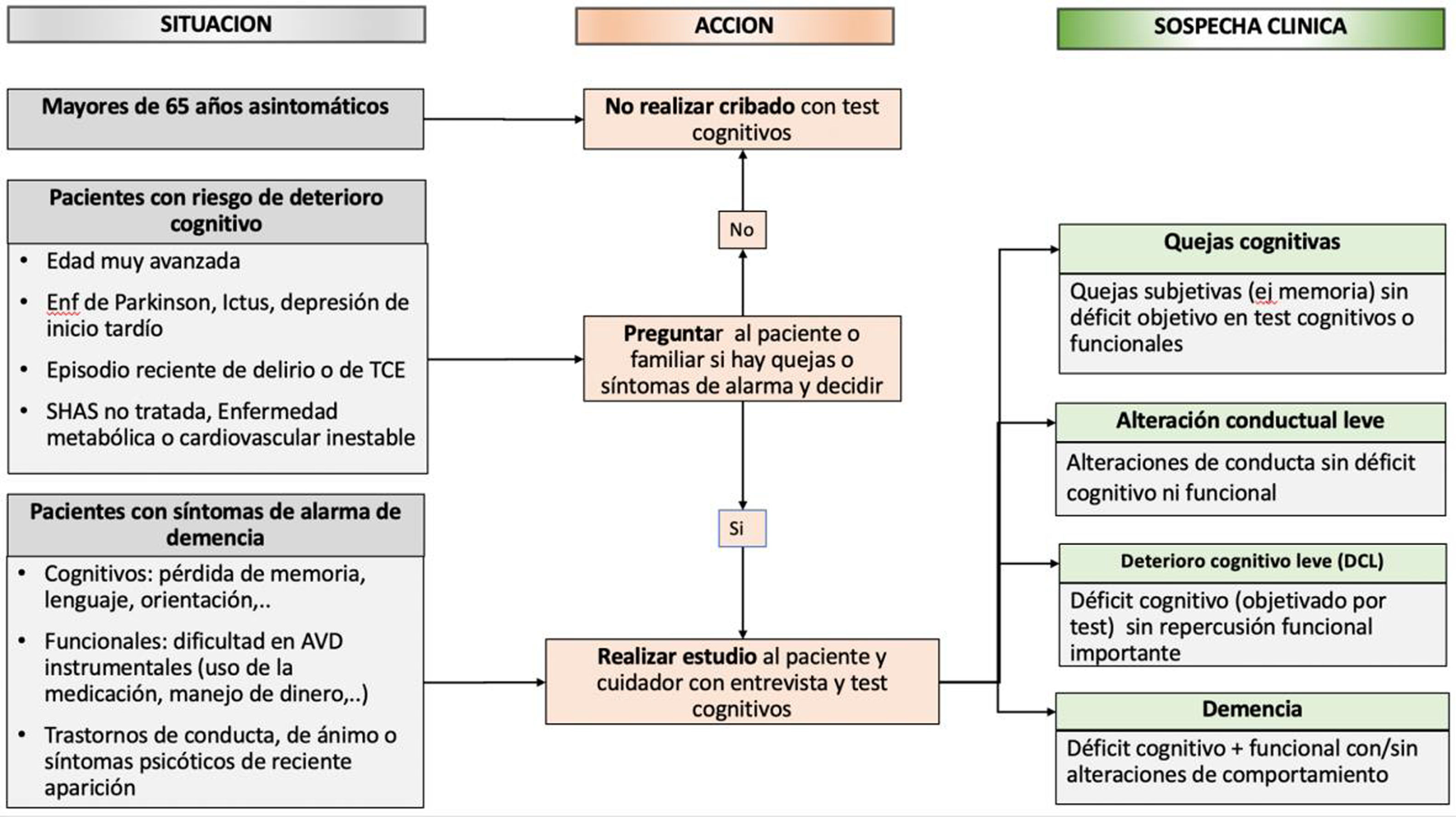
Cribado de deterioro cognitivo y demenciaEn la figura 2 se explica el esquema de las situaciones en las que se puede plantear realizar test cognitivos, de cribado y/o para constatar una sospecha de DC:
- •
En población general mayor de 65 años sin síntomas o signos de DC no está indicado el cribado con test cognitivos, que tendrán en esta población un valor predictivo positivo (VPP) bajo, alrededor del 20%20,22. Un cribado a toda la población podría detectar DC en las personas que no consulten por ello, pero implica emplear recursos que podrían utilizarse en otra actividad más rentable y posibles consecuencias en los pacientes ante el resultado, sobre todo en los falsos positivos (estigma social, tratamientos innecesarios). La evidencia actual es insuficiente para evaluar el balance daño/beneficio20.
- •
En las personas con mayor riesgo de DCL o demencia, como los mayores de 85 años, los pacientes con ictus previo, enfermedad de Parkinson o con episodio reciente de delirio, la realización de test resultará más eficiente con VPP mayores del 50%20. También, en mayores con mucha comorbilidad y/o polimedicados, sobre todo si viven solos, por el riesgo de descompensación de sus enfermedades basales si no son capaces de realizar un buen autocontrol.
- •
En pacientes con síntomas de alarma de DC como fallos de memoria o lenguaje, problemas de funcionalidad derivados de problemas cognitivos (p. ej., no ser capaces de controlar su medicación) o cambios en comportamiento o personalidad previa, los test cognitivos son obligados, dentro de una evaluación amplia del paciente20,22 que incluya entrevista al paciente y a un familiar o cuidador. En la entrevista debe explorarse cómo y cuándo empezó el deterioro y en qué medida le afecta en las actividades de la vida diaria, preguntar si hay trastornos emocionales y/o de conducta nuevos y revisar los antecedentes familiares y personales de riesgo para demencia vascular o degenerativa.
Aunque no existe cura para la demencia, un diagnóstico temprano de DCL o demencia permite entender quejas o comportamientos del paciente, ayuda a pacientes y cuidadores a prepararse en el manejo de los síntomas que puedan ir apareciendo y permite planificar el futuro tanto médico como legal o financiero, mientras el paciente aún conserva la capacidad de tomar decisiones20. También permitirá tratar los DCL o demencias potencialmente reversibles como los causados por depresión, polifarmacia, apnea del sueño o tumores cerebrales20,21.
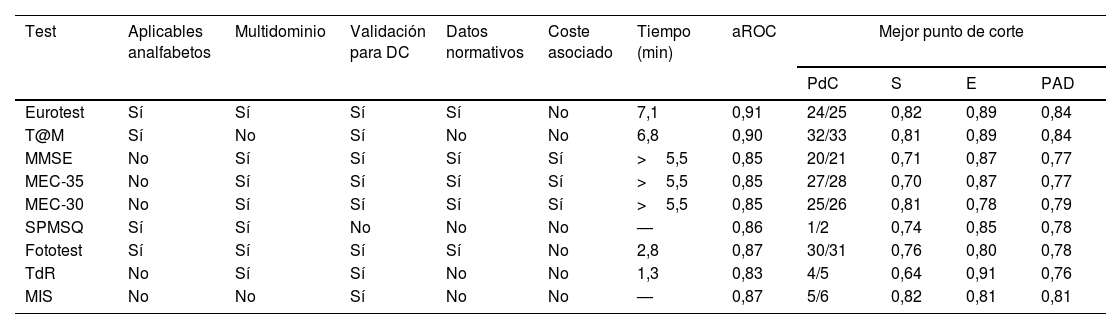
Hay múltiples test cognitivos que ayudan a diferenciar bien la demencia del estado cognitivo normal como el minimental (MMSE) o Mini Examen Cognoscitivo (MEC), el Montreal Cognitive Assessment (MoCA), las pruebas de fluidez verbal, el test del reloj, el Memory Impairment Screen (MIS) o el Mini-Cog®. Sin embargo, la precisión (sensibilidad y especificidad) de los test son más bajas para la detección del DCL que para demencia20,23 y es más difícil diferenciar con test cognitivos la normalidad del DCL o el DCL de la demencia23. El Eurotest, el T@M y el Fototest, diseñados y validados en España y de uso libre, no están influenciado por la educación y han demostrado tener gran capacidad discriminativa en la detección del DCL en las personas con sospecha de deterioro en AP24,25 (tabla 1). Dentro de los test con mayor duración, el MoCa (10-15min) explora más áreas cognitivas y tiene mayor sensibilidad que el MMSE para detectar fallos de memoria y disfunción ejecutiva, lo que lo hace mejor para detectar el DCL22,25. El uso conjunto de Fototest y Mini-Cog® permite explorar todas las áreas cognitivas con menos tiempo (4-5min), por lo que es más eficiente para el entorno de AP25.
Características de test cognitivos breves con estudios en atención primaria. Utilidad diagnóstica y efectividad comparada en condiciones de práctica habitual (sospecha de deterioro cognitivo en atención primaria)
| Test | Aplicables analfabetos | Multidominio | Validación para DC | Datos normativos | Coste asociado | Tiempo (min) | aROC | Mejor punto de corte | |||
|---|---|---|---|---|---|---|---|---|---|---|---|
| PdC | S | E | PAD | ||||||||
| Eurotest | Sí | Sí | Sí | Sí | No | 7,1 | 0,91 | 24/25 | 0,82 | 0,89 | 0,84 |
| T@M | Sí | No | Sí | No | No | 6,8 | 0,90 | 32/33 | 0,81 | 0,89 | 0,84 |
| MMSE | No | Sí | Sí | Sí | Sí | >5,5 | 0,85 | 20/21 | 0,71 | 0,87 | 0,77 |
| MEC-35 | No | Sí | Sí | Sí | Sí | >5,5 | 0,85 | 27/28 | 0,70 | 0,87 | 0,77 |
| MEC-30 | No | Sí | Sí | Sí | Sí | >5,5 | 0,85 | 25/26 | 0,81 | 0,78 | 0,79 |
| SPMSQ | Sí | Sí | No | No | No | — | 0,86 | 1/2 | 0,74 | 0,85 | 0,78 |
| Fototest | Sí | Sí | Sí | Sí | No | 2,8 | 0,87 | 30/31 | 0,76 | 0,80 | 0,78 |
| TdR | No | Sí | Sí | No | No | 1,3 | 0,83 | 4/5 | 0,64 | 0,91 | 0,76 |
| MIS | No | No | Sí | No | No | — | 0,87 | 5/6 | 0,82 | 0,81 | 0,81 |
aROC: área bajo la curva ROC; E: especificidad; MEC: Mini-Examen Cognoscitivo; MIS: Memory Impairment Screen; MMSE: Mini-Mental State Examination; PAD: proporción de aciertos diagnósticos; PdC: punto de corte; S: sensibilidad; SPMSQ: Short Portable Mental State Questionnaire; TdR: test del reloj; T@M: test de alteración de memoria.
Fuente: modificada de Carnero et al.24.
La precisión diagnóstica mejora si junto con los test cognitivos al paciente se realizan cuestionarios a los cuidadores como el Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE o test del informador) o el cuestionario Ascertain Dementia 8 (AD8), que ayudan a detectar alteraciones cognitivas y/o cambios funcionales del paciente22, o escalas que analicen alteraciones de comportamiento del paciente como el inventario neuropsiquiátrico (NPI-Q)22.
Es importante remarcar que el diagnóstico de demencia no puede hacerse exclusivamente con el resultado de los test cognitivos o funcionales22, pero el resultado de los test a lo largo del tiempo permitirá ayudar a confirmar un DC previamente dudoso y/o a comprobar la evolución a diferentes fases de demencia22, lo que permitirá dar el consejo adecuado en cada situación.
PrevenciónMientras no haya alternativas terapéuticas para curar la demencia, conseguir retrasar unos años el inicio de DC y demencia puede reducir la prevalencia y la carga humana y socioeconómica asociada a la enfermedad26, siendo esta una de las áreas de acción estratégicas del plan de acción mundial de la OMS para la demencia18.
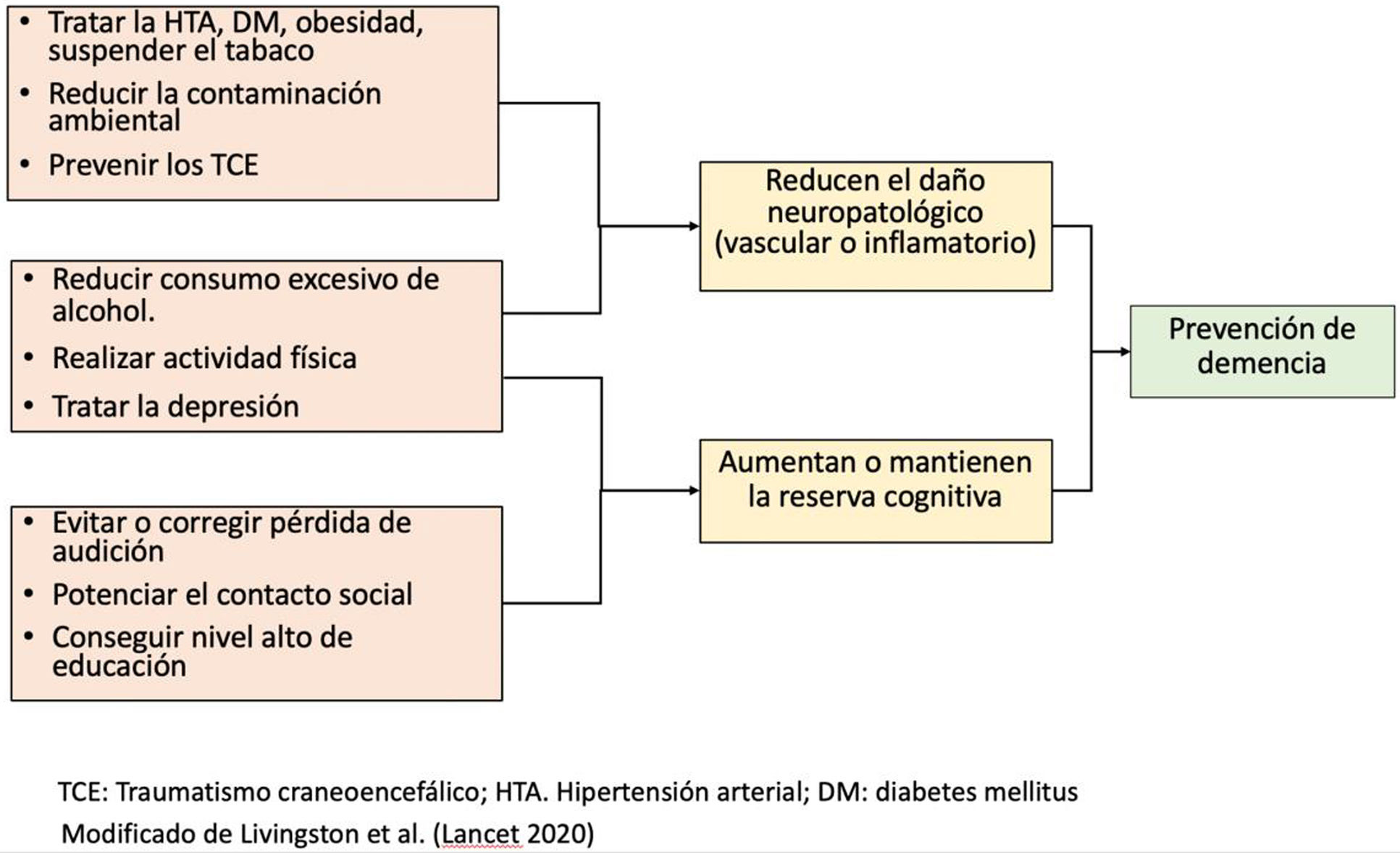
Factores de riesgo y protección del deterioro cognitivo y la demenciaLa edad, el sexo y algunas alteraciones genéticas son factores de riesgo (FR) para la demencia no modificables20. Sin embargo, hay evidencia de que alrededor del 40% de las demencias puede atribuirse a una combinación de doce FR potencialmente modificables que pueden darse en diferentes etapas de la vida: menor educación, contaminación del aire, tabaquismo, consumo excesivo de alcohol, obesidad, sedentarismo, hipertensión arterial (HTA), diabetes mellitus (DM), lesión cerebral traumática, discapacidad auditiva, depresión y aislamiento social27. El control de los FR modificables con un enfoque de salud pública podría tener un efecto protector20, reduciendo o retrasando el desarrollo de demencia26,27, en unos casos protegiendo contra el riesgo vascular, en otros aumentando la reserva cognitiva, entendiendo por tal la capacidad de preservar la cognición y funcionalidad durante más tiempo, a pesar de patología cerebral (fig. 3). Hay que advertir que el riesgo relativo (RR) de todos estos factores modificables es bajo (entre 1,1 y 1,9) frente al de la edad, las alteraciones genéticas o los marcadores de neurodegeneración (con RR entre 2 y 25 según edad)21.
La pérdida de visión28 o la fragilidad física20,22, también se han asociado en estudios recientes con disminución de DC. Dentro de los FR que pueden empeorar el DC no hay que olvidar el uso de fármacos con propiedades anticolinérgicas22 o con efecto sedante, como los neurolépticos y los opioides29.
Por el contrario, algunos factores dietéticos y de estilo de vida se han descrito como protectores de DC: consumo adecuado de ácido fólico, consumo bajo de grasas saturadas, consumo elevado de ácidos grasos omega-3 de cadena larga, consumo elevado de frutas y verduras, dieta mediterránea, consumo moderado de alcohol, mayores niveles de actividad física, así como un mayor nivel educativo, compromiso cognitivo y compromiso social20.
Intervenciones en prevenciónEs un tema controvertido ya que la aparición de DC o demencia es un proceso de años de evolución y los ensayos realizados tienen un seguimiento a muy corto plazo, insuficiente para poder demostrar resultados. Sin embargo, estudios poblacionales en países de ingresos altos indican que la incidencia de demencia no está creciendo a la velocidad prevista, lo que se ha atribuido a mejoras en las condiciones sociosanitarias de la población26,27, y avalaría que las intervenciones sobre los FR modificables podrían reducir o retrasar el desarrollo de demencia19,27. Para ello son necesarias estrategias de salud pública que promuevan conductas saludables y orienten en el control de FR cardiovascular y enfermedades crónicas. Estas intervenciones son especialmente importantes en las poblaciones más vulnerables, donde son más frecuentes la agrupación de varios de estos FR.
Hasta la fecha, no hay datos de ECA que confirmen de manera concluyente qué intervenciones dirigidas a FR modificables puedan prevenir la demencia. Sin embargo, abordar los FR puede tener otros beneficios para la salud y debe considerarse19. El resultado de las intervenciones difiere de la etapa de la vida en que se realizan. Así, es más eficaz la educación realizada en la infancia que el entrenamiento cognitivo de los mayores27, el control de la HTA, la DM o la obesidad es fundamental en edad adulta27, mientras que en mayores un control demasiado estricto puede ser contraproducente. La vigilancia de la medicación con actividad colinérgica o evitar el aislamiento social es más importante en los mayores.
Las normas de hábitos de vida saludable sobre alimentación, mantenerse activo física y mentalmente, evitar tabaco, exposición a ruido excesivo y traumatismos craneales, deberían darse en todas las etapas de la vida, comenzando desde la infancia. En la figura 4 se hace una propuesta sobre las intervenciones que se podrían implementar en cada etapa de la vida.
Una de las actividades que tiene mayor base es la potenciación del ejercicio físico que protege del DC por varios mecanismos, disminuyendo los FRCV (ayudando a controlar la HTA, la DM y la obesidad) y mejorando la neurogénesis del hipocampo20,26.
En cuanto a los fármacos estudiados para la prevención del DC (estatinas, AAS, AINE, dehidroepiandrosterona [DHEA] y otras hormonas gonadales, complementos nutricionales con o sin vitaminas, L-carnitina), según varios ensayos clínicos y revisiones Cochrane, hasta ahora ninguno ha demostrado que prevenga la aparición de demencia20,21,26,27, encontrando solo leve mejoría de algunos aspectos de la función cognitiva, el comportamiento y la calidad de vida con ginseng21.
La evidencia es actualmente insuficiente para recomendar el uso de medicamentos antidepresivos a fin de reducir el riesgo de DC o de demencia26. El tratamiento específico para la demencia (anticolinesterásicos y memantina) no mejora el nivel cognitivo en pacientes con DCL20 ni detiene el paso de DCL a demencia22.
En resumen, en el momento actual no se recomienda ningún fármaco y/o complemento vitamínico para prevenir el DC o el paso de DCL a demencia, y solo estarán indicados aquellos necesarios para tratar las comorbilidades de base (p. ej., hipercolesterolemia, ictus, fibrilación auricular, depresión).
Intervenciones en pacientes con deterioro cognitivo leve y demenciaEl objetivo de las intervenciones sobre DCL y demencia debe ser el bienestar de los pacientes y sus familias27. Actualmente, el tratamiento farmacológico y no farmacológico está destinado a retrasar temporalmente la discapacidad y aliviar el malestar psicológico20,21.
Los anticolinesterásicos y la memantina pueden producir una leve mejoría a corto plazo de la cognición y/o la función en los pacientes con enfermedad de Alzheimer leve/moderada por lo que están indicados, tanto en enfermedad de Alzheimer como en otras demencias, siempre que sean bien tolerados19,20. Los anticolinesterásicos pueden tener efectos secundarios, entre ellos síncopes, aunque no aparecen más caídas ni fracturas30. Se recomienda suspenderlos cuando hay efectos secundarios, falta de adherencia, si no se observó mejoría o estabilización de los síntomas cognitivos y/o neuropsiquiátricos con el tratamiento y/o cuando ya no se espera ningún beneficio de ellos (p. ej., demencia terminal). En caso de deprescripción, la dosis debe reducirse lentamente22.
En las personas con DCL o demencia leve a moderada se recomienda terapia de estimulación cognitiva grupal (estimulación de memoria, concentración y pensamiento en grupos pequeños)22. La estimulación cognitiva produce pequeños beneficios cognitivos a corto plazo, con mejorías clínicamente relevantes en la comunicación y la interacción social y efectos beneficiosos en calidad de vida, el estado de ánimo y el comportamiento31.
El ejercicio multicomponente (programa de ejercicios que combina ejercicios aeróbicos, de resistencia, de equilibrio y de flexibilidad) mejora la cognición global y la función ejecutiva en pacientes con DCL o con demencia. Además, en pacientes con demencia, también mejoró la fuerza muscular, la agilidad, movilidad, flexibilidad y las actividades de la vida diaria32. En la intervención debe incluirse ejercicio aeróbico para que tenga efecto sobre la cognición33.
En los pacientes con demencia leve/moderada el control de la fibrilación auricular y de los FR cardiovasculares (HTA, hipercolesterolemia, DM), puede evitar patología cerebrovascular que empeore el curso de la demencia29. Esta prevención ya no tiene mucho sentido en loa pacientes con demencia avanzada y expectativa de vida corta; en caso de caídas frecuentes o mala adherencia al tratamiento, será preciso individualizar, ya que en estas situaciones no está claro si los beneficios superan los riesgos (hemorragia cerebral con anticoagulantes, mareos o caídas con antihipertensivos)29.
Las personas con DCL o demencia pueden tener menos acceso a la atención médica por dificultad para expresar sus dolencias, por ello es importante realizar seguimiento médico planificado de las comorbilidades asociadas ya que permite disminuir la carga de enfermedad y deterioro funcional y reducir los ingresos hospitalarios que favorecen el delirio, empeoran el DC y aumentan el gasto sanitario27,29.
En el control de las enfermedades crónicas es preciso racionalizar el uso de fármacos22 y valorar periódicamente riesgo/beneficio de cada intervención29, con especial cuidado a los fármacos que más afectan a la cognición (opioides, fármacos con actividad anticolinérgica) y a las interacciones en pacientes polimedicados, ya que pueden contribuir a empeorar el DC, producir sedación o riesgo de caídas29.
Los síntomas neuropsiquiátricos (apatía, delirios, agitación, etc.) se presentan de forma frecuente en el curso del DCL o demencia, pudiendo desencadenarse o empeorar por factores relacionados con el paciente, el cuidador o el entorno. Se aconseja el enfoque DICE (Describir, Investigar, Crear y Evaluar) para ayudar a identificar una posible causa subyacente, e intentar aliviarlos con intervenciones no farmacológicas dirigidas tanto a los pacientes como al cuidador (entrenamiento de habilidades, adaptación de actividades). Estas últimas consiguen disminuir la gravedad de los síntomas neuropsiquiátricos y la angustia del cuidador19. Los medicamentos psicotrópicos tienen evidencia mínima de eficacia para tratar estos síntomas y se asocian con riesgos clínicamente significativos de caídas y DC y, en el caso de neurolépticos, con mayor mortalidad e ictus19,29. Cuando se utilizan medicamentos psicotrópicos para tratar un síntoma, si no hay respuesta eficaz, deben retirarse antes de administrar un nuevo fármaco comprobando además las posibles interacciones (p. ej., benzodiacepinas o gabapentinas con opioides) o efectos secundarios (p. ej., malestar gastrointestinal con antidepresivos)19. Solo hay que usar neurolépticos en situaciones agitación o psicosis grave con riesgo para el paciente o la familia, revisando la indicación periódicamente y retirándolos cuando cese el trastorno de comportamiento y/o haya efectos secundarios (sedación, DC rápido, efectos extrapiramidales)29. Los antidepresivos no deben usarse para tratar la apatía y hay que retirarlos si no hay respuesta en caso de depresión.
Las intervenciones específicas para cuidadores (asesoramiento, información sobre servicios, mejora de las habilidades para atender al paciente y manejar el estrés) han logrado pequeñas mejoras en ansiedad y depresión y calidad de vida en cuidadores20,22,27.
Los trabajos publicados sobre intervenciones para reducir el riesgo de DC y demencia no tienen resultados alentadores. No suele haber ensayos a largo plazo, las intervenciones son muy heterogéneas y el desarrollo de la enfermedad es lento, lo que dificulta obtener resultados y/o interpretarlos. Sin embargo, los numerosos estudios observacionales a largo plazo sobre factores de riesgo y demencia apoyan la intervención sobre los mismos, empezando de forma temprana y continuando toda la vida.
Recomendaciones
- •
No se recomienda la realización de pruebas cognitivas en mayores de 65 años asintomáticos que viven en la comunidad.
- •
Si aparecen síntomas de alarma de DC, se recomienda realizar test cognitivos, dentro de una evaluación completa del paciente, para intentar diagnosticar el DCL o la demencia tempranamente.
- •
Se recomienda vigilar periódicamente a los pacientes con mayor riesgo de DC (por edad y/o patologías previas) y a los pacientes en los que el DC pueda dificultar el control de sus enfermedades (polimedicados, fragilidad).
- •
Durante toda la vida, se recomiendan hábitos saludables en nutrición y ejercicio físico, higiene del sueño, protección contra accidentes y ruido y evitar en lo posible ambientes con mucha contaminación.
- •
Se recomienda control de los FRCV (HTA, DM, obesidad, tabaco, alcohol) y corregir la apnea del sueño, sobre todo en edad media de la vida.
- •
En los mayores, se recomienda corregir los defectos visuales y/o auditivos, evitar medicación con efecto anticolinérgico o sedante, mantener actividad mental estimulante y evitar sedentarismo y aislamiento social.
- •
No se recomienda ningún fármaco o complemento nutricional para prevenir el DCL y/o demencia.
- •
No se recomienda el uso habitual de neurolépticos en el tratamiento de síntomas neuropsiquiátricos asociados a DCL y demencia, salvo síntomas graves con riesgo para el paciente o la familia.
El aislamiento social es uno de los problemas sociales más graves y comunes en las sociedades que envejecen. Según la definición de la OMS el aislamiento social se relaciona con «la falta de contacto con familiares, amigos u otras personas»34.
Según datos del Instituto Nacional de Estadística (INE) publicados en junio del 2024, los hogares en los que vive una sola persona aumentarán en los próximos 15 años, llegando a ser el 33,5% del total en 2039. El número de personas que viven solas pasaría a representar el 11,2% de la población en 203935.
Se estima que en España un 13,4% de las personas sufren soledad no deseada (SND), que quienes la padecen llevan aproximadamente 6 años en dicha situación y el 22,9% experimenta este sentimiento de soledad durante todo el día. Asimismo, en Europa alrededor de treinta millones de personas se sienten solas con frecuencia36.
La soledad se define como «un sentimiento emocional, que puede ir acompañado o no de aislamiento social y solo puede evaluarse preguntando a las personas si se sienten solas». Si bien estos conceptos históricamente no se han distinguido bien, más recientemente se han identificado como distintos34.
Causas del aislamiento social y la soledadEl aislamiento social en mayores puede ser resultado de múltiples factores, incluyendo cambios en la estructura familiar, pérdida de seres queridos, movilidad reducida, problemas de salud crónicos, y falta de acceso a servicios y actividades sociales. Estos factores pueden interactuar de manera compleja, exacerbando el riesgo de aislamiento.
Las personas con recursos económicos limitados también están en mayor riesgo debido a la falta de acceso a tecnologías de comunicación y transporte37.
Consecuencias del aislamiento socialEl aislamiento social y la soledad tienen una alta prevalencia en la población mayor, y está demostrado que afectan negativamente al bienestar físico y emocional. Es un factor de riesgo de enfermedad cardiovascular, accidente cerebrovascular, demencia, depresión, trastornos del sueño, necesidad de atención a largo plazo y mortalidad34,37.
La soledad está asociada con deterioro de múltiples dominios cognitivos en mayores. Hay suficiente evidencia que demuestra que la soledad constituye un factor de riesgo independiente para el DC y la demencia, incluso después de controlar el efecto de la depresión. El mantenimiento de la participación comunitaria y las redes sociales puede representar una estrategia para reducir el riesgo de DCL y demencia38,39.
Identificación de las personas en riesgo de aislamiento socialHasta ahora el aislamiento social y la soledad no son condiciones que los profesionales de atención primaria detectemos y registremos de manera habitual. Es de vital importancia aumentar la conciencia de los profesionales para fomentar la detección, evaluación y posterior implementación de intervenciones34,37.
La soledad es un sentimiento subjetivo que puede ser difícil de valorar. Las herramientas de medición pueden ayudar a interpretar y comprender mejor el impacto que la soledad supone en las personas mayores.
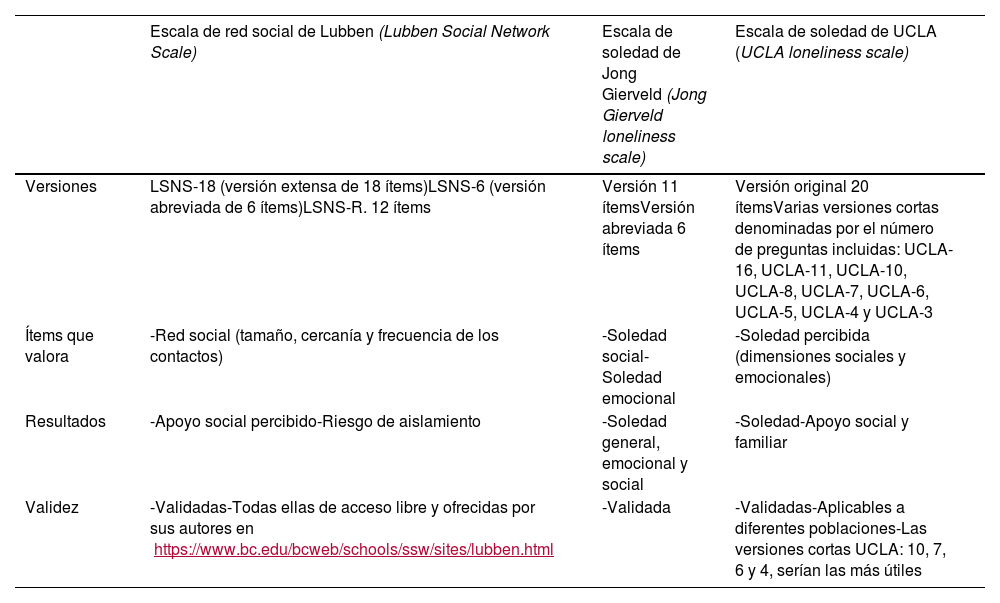
Existen diferentes instrumentos para medir el aislamiento social. En la tabla 2 describimos las más utilizadas.
Escalas para detectar el aislamiento social34,40
| Escala de red social de Lubben (Lubben Social Network Scale) | Escala de soledad de Jong Gierveld (Jong Gierveld loneliness scale) | Escala de soledad de UCLA (UCLA loneliness scale) | |
|---|---|---|---|
| Versiones | LSNS-18 (versión extensa de 18 ítems)LSNS-6 (versión abreviada de 6 ítems)LSNS-R. 12 ítems | Versión 11 ítemsVersión abreviada 6 ítems | Versión original 20 ítemsVarias versiones cortas denominadas por el número de preguntas incluidas: UCLA-16, UCLA-11, UCLA-10, UCLA-8, UCLA-7, UCLA-6, UCLA-5, UCLA-4 y UCLA-3 |
| Ítems que valora | -Red social (tamaño, cercanía y frecuencia de los contactos) | -Soledad social-Soledad emocional | -Soledad percibida (dimensiones sociales y emocionales) |
| Resultados | -Apoyo social percibido-Riesgo de aislamiento | -Soledad general, emocional y social | -Soledad-Apoyo social y familiar |
| Validez | -Validadas-Todas ellas de acceso libre y ofrecidas por sus autores en https://www.bc.edu/bcweb/schools/ssw/sites/lubben.html | -Validada | -Validadas-Aplicables a diferentes poblaciones-Las versiones cortas UCLA: 10, 7, 6 y 4, serían las más útiles |
La prevención del aislamiento social en ancianos requiere un enfoque holístico y proactivo, abordando tanto los factores individuales como los contextuales que contribuyen a este fenómeno. Es fundamental implementar intervenciones personalizadas y sostenibles que promuevan la participación social y la conexión emocional entre los adultos mayores.
Los profesionales de atención primaria debemos detectar y captar al mayor que está en situación de aislamiento social y registrarlo como diagnóstico en su historia clínica. Esto nos permitirá proponer intervenciones que disminuyan el riesgo de que el hecho de «vivir solo» y «sentirse solo» representan para la calidad de vida. Los objetivos serían: conservar autonomía, adecuación de la vivienda, fomentar las redes de apoyo sanitario y social, realizar programas de enriquecimiento y participación social y actividades que aumenten la amistad, la autoestima y el bienestar34.
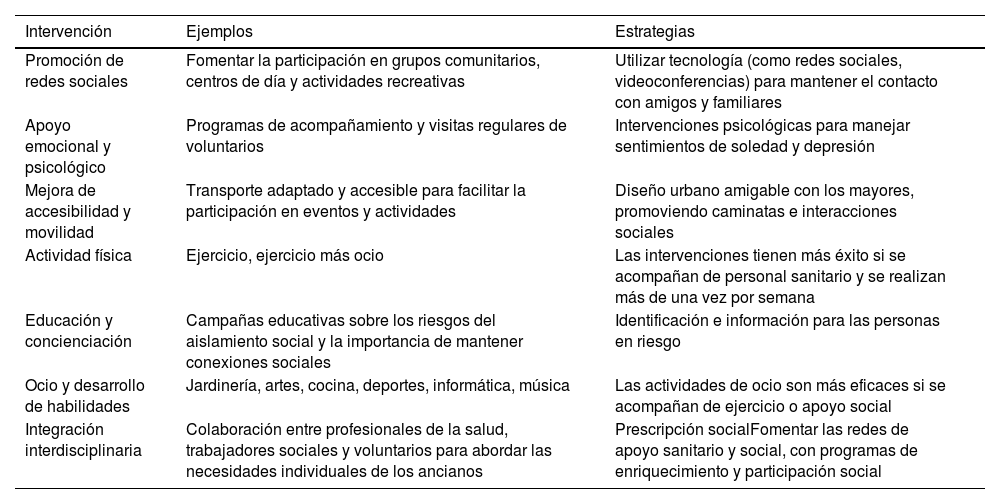
Se han estudiado diversas intervenciones dirigidas a reducir la soledad y el aislamiento social, resumidas en la tabla 3. Múltiples revisiones sistemáticas que evalúan estas intervenciones han llegado a conclusiones diferentes y a menudo contradictorias34,41.
Intervenciones para abordar el aislamiento social y la soledad1,8,9
| Intervención | Ejemplos | Estrategias |
|---|---|---|
| Promoción de redes sociales | Fomentar la participación en grupos comunitarios, centros de día y actividades recreativas | Utilizar tecnología (como redes sociales, videoconferencias) para mantener el contacto con amigos y familiares |
| Apoyo emocional y psicológico | Programas de acompañamiento y visitas regulares de voluntarios | Intervenciones psicológicas para manejar sentimientos de soledad y depresión |
| Mejora de accesibilidad y movilidad | Transporte adaptado y accesible para facilitar la participación en eventos y actividades | Diseño urbano amigable con los mayores, promoviendo caminatas e interacciones sociales |
| Actividad física | Ejercicio, ejercicio más ocio | Las intervenciones tienen más éxito si se acompañan de personal sanitario y se realizan más de una vez por semana |
| Educación y concienciación | Campañas educativas sobre los riesgos del aislamiento social y la importancia de mantener conexiones sociales | Identificación e información para las personas en riesgo |
| Ocio y desarrollo de habilidades | Jardinería, artes, cocina, deportes, informática, música | Las actividades de ocio son más eficaces si se acompañan de ejercicio o apoyo social |
| Integración interdisciplinaria | Colaboración entre profesionales de la salud, trabajadores sociales y voluntarios para abordar las necesidades individuales de los ancianos | Prescripción socialFomentar las redes de apoyo sanitario y social, con programas de enriquecimiento y participación social |
Fuente: elaboración propia.
Las evidencias de las que disponemos hasta ahora confirman que las relaciones sociales, tanto en cantidad como en calidad contribuyen a reducir la discapacidad, la morbilidad y la mortalidad. La soledad es menos común entre las personas que viven en vecindarios con mayor número de recursos, más seguros y físicamente accesibles. Las conexiones sociales mejoran la adherencia a los regímenes médicos y reducen el tiempo de hospitalización34.
La prescripción social es una estrategia que ofrece resultados positivos, a través de actividades comunitarias que aumentan la participación social, la amistad, la autoestima y el bienestar, pero se necesitan estudios más rigurosos para poder evaluar su efectividad42.
Las tecnologías de la información y la comunicación (TIC), han demostrado una reducción significativa de los niveles de soledad en adultos mayores que viven en la comunidad, pero se necesitan más datos para conocer su efecto en el tiempo y durabilidad41.
El aislamiento social y la soledad podrían ser los nuevos «gigantes geriátricos»35. De ahí que los gobiernos y las instituciones cada vez estén más preocupados por su efecto sobre la salud.
En los últimos años han surgido iniciativas para combatir la Soledad no deseada (SND):
- 1.
Observatorio Estatal de la Soledad no Deseada (SoledadES) de la Fundación ONCE: https://www.soledades.es/
- 2.
Estrategia Municipal contra la soledad 2020-2030 del Ayuntamiento de Barcelona: https://ajuntament.barcelona.cat/dretssocials/es/barcelona-contra-la-soledad/formacion
- 3.
Página sobre la soledad no deseada del Ayuntamiento de Madrid: https://soledadnodeseada.es/
- 4.
Proyecto «Te acompaña» de Cruz Roja: https://www2.cruzroja.es/web/cruzroja/-/cruz-roja-presenta-te-acompana-un-servicio-para-combatir-la-soledad-que-duele-smta-act-
- 5.
Plan de acción contra la soledad no deseada y el aislamiento social 2022-2025 de la Junta de Castilla y León: https://serviciossociales.jcyl.es/web/es/plan-accion-castilla-leon.html
Recomendaciones
- •
Se recomienda realizar detección del aislamiento social, mediante entrevista, a los mayores que están en riesgo, en las consultas de atención primaria.
- •
Aunque no hay suficiente evidencia sobre la efectividad de las intervenciones para mejorar el aislamiento social, las recomendadas, ya que parecen ser más efectivas, son aquellas que ofrecen una actividad social y/o apoyo dentro de un formato grupal y en las que los individuos participan de manera activa.
- •
A nivel individual se recomienda el mantenimiento de relaciones sociales de calidad durante toda la vida ya que es fundamental para prevenir el aislamiento social.
- •
Se recomienda que las autoridades a nivel nacional, regional y local trabajen junto con las comunidades para evaluar el contexto social e implementar las intervenciones de acuerdo con las necesidades de los ciudadanos.
La prevención del suicidio en las personas mayores dentro de la atención primaria es crucial, dado que este grupo etario a menudo tiene mayor riesgo debido a varios factores exclusivos. Las actividades preventivas en atención primaria han de centrarse en la identificación y cuidado de sus factores de riesgo, el uso de herramientas específicas y la implementación de estrategias de intervención efectivas43.
El suicidio en las personas mayores es una preocupación de salud pública significativa, dado que las tasas de suicidio en este grupo etario suelen ser más altas que en otras poblaciones. Diversos estudios han mostrado que los hombres mayores de 65 años tienen las tasas de suicidio más altas, especialmente entre europeos y, en general, caucásicos y habitantes del norte global. En contraste, las mujeres mayores tienen tasas de suicidio más bajas, aunque los intentos de suicidio no fatales son más comunes en comparación con los hombres. En muchos países, las tasas de suicidio aumentan con la edad. Por ejemplo, en EE. UU., los varones mayores de 85 años tienen una tasa de suicidio aproximadamente 4 veces mayor que la población general. En otros países desarrollados, como Japón y algunos países europeos, se observan patrones similares, donde los adultos mayores presentan tasas de suicidio significativamente más altas en comparación con grupos etarios más jóvenes43,44.
Entre los factores de riesgo más destacados para el suicidio en las personas mayores se encuentran los factores psicosociales asociados a la pobreza, la soledad, el aislamiento y la marginación, así como la depresión y otros trastornos mentales. La depresión en esta población a menudo no se diagnostica ni se trata adecuadamente, y puede estar asociada con enfermedades somáticas, DC y eventos vitales estresantes. La soledad, el aislamiento social, la pobreza o la marginación son factores de riesgo destacados que, además, pueden facilitar la depresión y otros trastornos mentales o el agravamiento de estos, incluso en mayor proporción que en otras edades45. Los adultos mayores que carecen de una red de apoyo social sólida son más vulnerables a las ideaciones suicidas. La pérdida de seres queridos también es un factor de riesgo importante. La muerte de un cónyuge o un familiar cercano aumenta el riesgo, particularmente durante los primeros 6 meses tras la pérdida. Además, los problemas de salud física juegan un papel significativo. Las enfermedades crónicas y el dolor físico pueden contribuir al riesgo de suicidio, ya que los adultos mayores que enfrentan problemas de salud debilitantes a menudo experimentan una disminución en la calidad de vida, lo que puede llevar a la desesperación43.
La detección de esos factores de riesgo puede realizarse mediante la entrevista clínica, o mediante la relación continuada entre el profesional de atención primaria de salud y el/los consultantes. En caso de duda, pueden utilizarse evaluaciones estandarizadas como la escala de depresión geriátrica (GDS), la escala de estrés percibido, o escalas más generalistas, como la Escala de Actitudes Disfuncionales de Weissman y Beck (EADG). Como se recomienda también en el Programa de Salud Mental del PAPPS45 es esencial que los profesionales de atención primaria realicen evaluaciones regulares y sistemáticas del estado mental de los pacientes mayores.
En cuanto a las medidas de prevención terciaria y tratamiento, es necesario insistir en la mejora de la red social del mayor, tanto personal como informatizada. Los planes de conexión, similares a los planes de seguridad utilizados en emergencias, están diseñados para ayudar a los ancianos deprimidos a mantenerse conectados con su comunidad y sus seres queridos. Estos planes pueden incluir actividades comunitarias, grupos de apoyo, telefonemas periódicos y el uso de las TIC para mantenerse en contacto con proveedores de salud y redes sociales. Enviar mensajes de cuidado continuado, como postales, correos electrónicos o llamadas telefónicas, ha demostrado reducir significativamente los intentos de suicidio posteriores. Este enfoque proporciona un sentido de conexión y apoyo continuo a los pacientes después de un alta hospitalaria o durante el tratamiento ambulatorio. Además, hay que pensar en restringir el acceso a medios letales, especialmente armas de fuego y fármacos.
La integración de gestores de cuidados, acompañantes terapéuticos y personal no profesional coetáneo o de otras edades (infancia y adolescencia) como acompañantes han mostrado ser efectivas para reducir las tasas de suicidio. El uso de intervenciones farmacológicas a corto plazo es mucho más discutido45,46. Las medidas terapéuticas más eficaces son las que se basan en la red social y en medidas psicoterapéuticas. En ese sentido han demostrado utilidad algunas terapias cognitivo-conductuales (TCC), las terapias interpersonales y psicoanalíticas y la terapia dialéctica conductual (TDC)45,46. Fomentar la actividad física y una buena nutrición puede mejorar significativamente el estado de ánimo y la salud mental de los adultos mayores, y los programas de ejercicio pueden ser una intervención coadyuvante valiosa. El uso de tecnologías para el seguimiento y la intervención, como la telemedicina y los chequeos virtuales, puede ser especialmente beneficioso para los adultos mayores con problemas de movilidad, permitiendo un seguimiento continuo y el acceso a servicios de salud mental desde el hogar. En resumen, la capacitación del personal de atención primaria y el fortalecimiento de las redes de apoyo social, tanto personales como informatizadas, son los componentes clave para reducir la incidencia de suicidios en esta población vulnerable.
Recomendaciones
- •
Realizar evaluaciones sistemáticas del estado mental de los pacientes mayores, utilizando la entrevista clínica y, si es necesario, escalas para identificar la depresión y otros trastornos mentales.
- •
Fomentar la red social y planes de conexión que incluyan actividades comunitarias, grupos de apoyo y el uso de tecnologías para mantener a los pacientes en contacto con sus seres queridos, con su entorno social y con los proveedores de salud.
- •
Asegurar que los pacientes mayores en riesgo no tengan fácil acceso a medios letales, especialmente armas de fuego y/o fármacos con potencial letal.
- •
Sensibilizar a los profesionales del centro de salud a través de actividades como sesiones clínicas u otras actividades formativas sobre el tema, a partir de los casos de suicidio o intento de suicidio realizados en la población del centro.
La nutrición a lo largo de la vida es un factor determinante en el envejecimiento saludable, ya que preserva las capacidades físicas y psíquicas del individuo. Una nutrición inadecuada está estrechamente relacionada con la pérdida de capacidad funcional y la dependencia, disminuye la calidad de vida, favorece la aparición de enfermedades y aumenta la mortalidad.
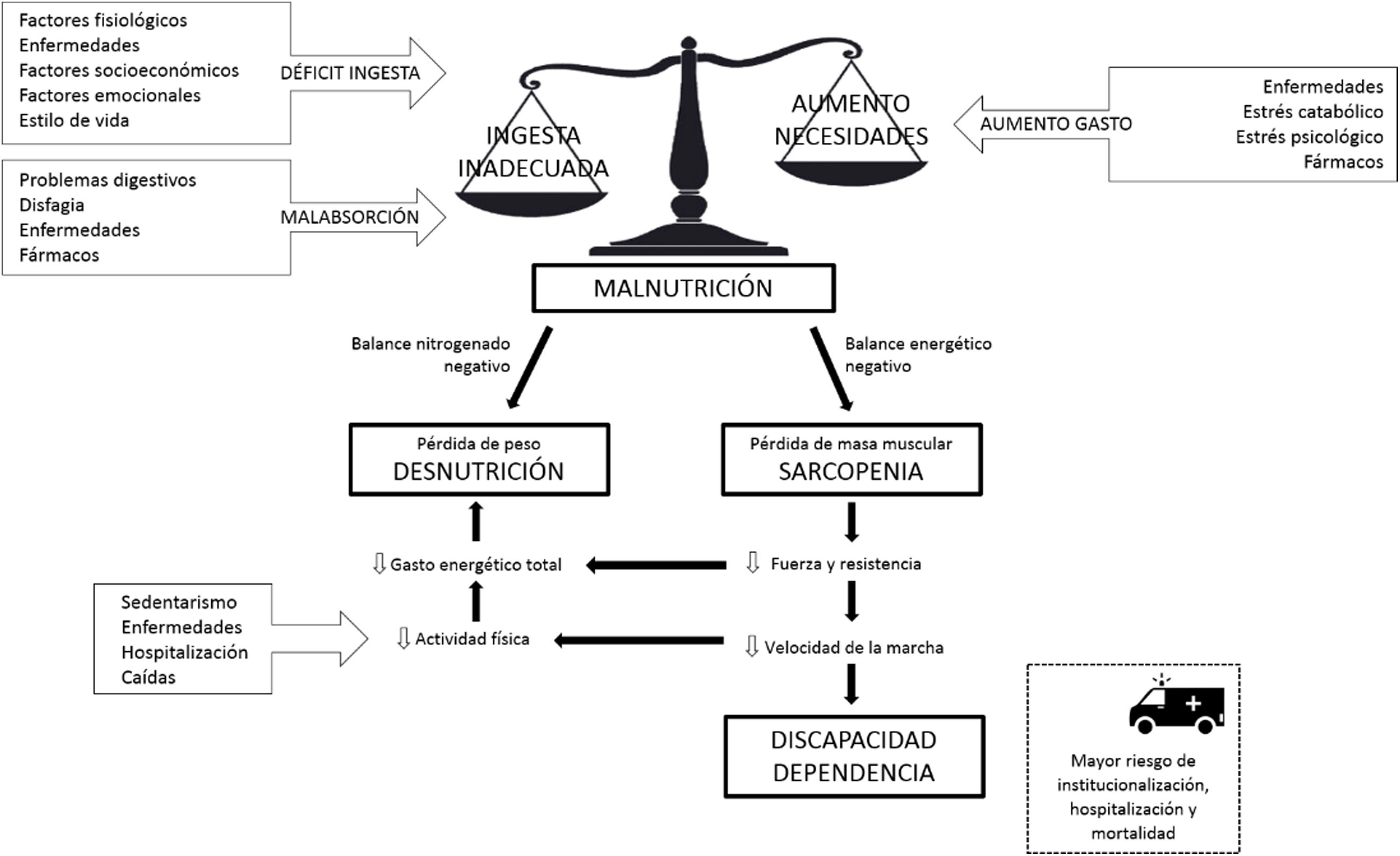
Las personas mayores tienen un riesgo aumentado de malnutrición por defecto (o desnutrición) debido a múltiples factores (fisiológicos, enfermedades asociadas, fármacos, problemas psicosociales, etc.) que conducen a una ingesta inadecuada, balance negativo de proteínas, y un mayor gasto energético basal, contribuyendo a la etiología compleja de la sarcopenia y la fragilidad47 (fig. 5). La prevalencia de desnutrición aumenta con la edad, variando considerablemente según la población estudiada (3,1% en ámbito ambulatorio; 22,0% en hospitalizados)48. La malnutrición se asocia a mayores tasas de infección, aumento de caídas, aparición de úlceras por presión, estancias hospitalarias más largas y aumento de la mortalidad34,48.
Por otro lado, la malnutrición por exceso (obesidad) es un problema creciente en la población mayor, afectando al 18-30% de la población mundial mayor de 65 años47. Diversos estudios han demostrado que un índice de masa corporal (IMC) entre 25-28kg/m2 se asocia a un mejor estado de salud34,47,49. Sin embargo, la obesidad (IMC>30kg/m2) y especialmente la obesidad grave (IMC>35kg/m2), se asocian a aumento de riesgo cardiovascular, problemas de movilidad, pérdida de masa muscular y fragilidad34,47.
Ingestas recomendadas de energía y nutrientesExisten algunas diferencias entre los requerimientos nutricionales de los adultos jóvenes y las personas mayores.
Con la edad, el consumo energético disminuye, debido fundamentalmente a la pérdida de masa muscular y disminución del metabolismo basal. Se recomienda la ingesta de al menos 30kcal/kg/día, aunque esta cantidad será mayor en caso de malnutrición, actividad física intensa o presencia de enfermedad34,47–49.
Las necesidades proteicas aumentan con la edad, aconsejándose una ingesta de 0,8-1,2g/kg/día de proteínas. En caso de enfermedad, estas necesidades son mayores, recomendándose 1,2-1,5g/kg/día, o incluso 2g/kg/día en caso de enfermedad severa, úlceras o malnutrición34,47–49. Sin embargo, en los pacientes prediálisis con filtrado glomerular <30ml/min/1,73m2, se aconseja restricción proteica (<0,8mg/kg/día)49. Es importante recordar que una ingesta calórica insuficiente aumenta los requerimientos proteicos, así que debemos garantizar ambos.
Las recomendaciones de micronutrientes no difieren entre jóvenes y ancianos. Sin embargo, debido a la ingesta disminuida y la prevalencia aumentada de afecciones digestivas, los mayores tienen mayor riesgo de déficit de vitaminas del grupo B, vitamina D, hierro, calcio, zinc, entre otros47.
Se aconseja una dieta rica en fibra (25g/día) y una adecuada hidratación para regular el tránsito intestinal47.
Con la edad se produce una importante disminución de la sed, de la capacidad renal para concentrar la orina, y es frecuente el uso de fármacos que aumentan el riesgo de deshidratación (p.ej., diuréticos). Se aconsejan al menos 1,6 l/día en mujeres y 2 l/día en varones, siendo mayores los requerimientos en caso de altas temperaturas, ejercicio físico, diarrea o vómitos. Por otro lado, en caso de insuficiencia renal o cardiaca, puede ser necesario restringir la ingesta de líquidos47.
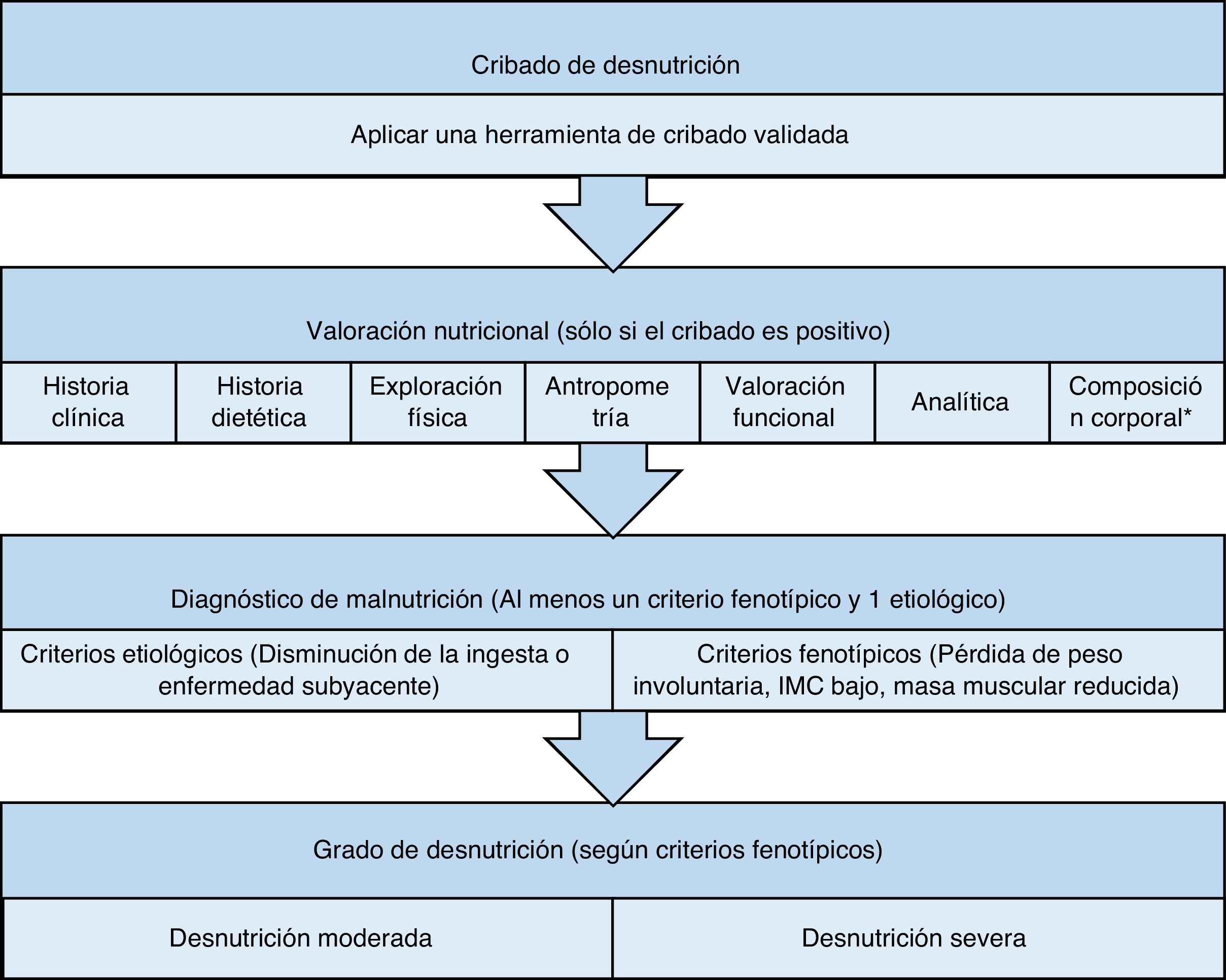
Diagnóstico de malnutriciónAunque el concepto de malnutrición se refiere a la idea de una dieta desequilibrada, ya sea por exceso o por defecto, en la mayoría de la bibliografía revisada se considera la palabra malnutrición como sinónimo de desnutrición, y en esta revisión hablaremos de ambos conceptos de forma equivalente (tabla 4).
Diagnóstico de malnutrición según los criterios GLIM
| Criterios etiológicos | |
| Ingesta alimentaria reducida y/o malabsorción intestinal | Ingesta <50% del requerimiento energéticoReducción de la ingesta durante más de 2 semanasCualquier condición digestiva que afecte a la asimilación de alimentos |
| Inflamación subyacente | Enfermedad agudaEnfermedad inflamatoria crónica |
| Criterios fenotípicos | ||
|---|---|---|
| Desnutrición moderada | Desnutrición severa | |
| Pérdida de peso involuntaria | 5-10% en 6 meses10-20% en más de 6 meses | >10% en 6 meses>20% en más de 6 meses |
| IMC bajo | <20kg/m2 en <70 años<22kg/m2 en >70 años | <18,5kg/m2 en <70 años<20kg/m2 en >70 años |
| Masa muscular reducidaa | Déficit leve/moderado | Déficit severo |
IMC: índice de masa corporal.
Las personas mayores con factores de riesgo de desnutrición (bajo peso, pérdida de peso involuntaria, afección concomitante,…) deben someterse a un test de cribado nutricional con una herramienta validada, independientemente del IMC que presenten al inicio del estudio. El objetivo será identificar la presencia de desnutrición o el riesgo de desarrollarla, y beneficiarse de una intervención dietética precoz47-49. Solo en el caso de resultado positivo en el test de cribado se realizará una valoración nutricional para confirmar el diagnóstico, valorar la severidad del mismo, identificar posibles factores etiológicos, y desarrollar un plan terapéutico34,47–50. Existen múltiples herramientas de cribado con resultados variables entre ellas48,50. Ante la ausencia de un gold standard, los criterios Global Leadership Initiative on Malnutrition (GLIM) son el resultado de un consenso entre las principales sociedades científicas de nutrición clínica para identificar y diagnosticar la malnutrición de forma objetiva y mundialmente aceptada34,48–50.
Intervención nutricionalUna vez establecido el diagnóstico, es preciso establecer un plan terapéutico individualizado con objeto de mantener y/o mejorar el estado nutricional, la capacidad funcional y la calidad de vida. Las causas potenciales de malnutrición y deshidratación deben ser corregidas lo antes posible34,47–49.
Los factores ambientales influyen en la ingesta. Comer en compañía, en un entorno agradable, con platos atractivos visualmente que respeten las preferencias personales, pueden aumentar considerablemente la ingesta34,47,51. Los servicios de comida a domicilio, ofrecer aperitivos entre horas, o la asistencia a la hora de comer en pacientes que no sean autónomos también pueden ser de utilidad34,47,48.
La dieta será variada y equilibrada (dieta mediterránea), ofreciendo alimentos saludables y medioambientalmente sostenibles, con abundancia de productos frescos (hortalizas, verduras, frutas) y cereales integrales, además de tubérculos, frutos secos, lácteos, carne de ave, pescado, huevos y aceite de oliva; reduciendo el consumo de carne roja y/o procesada, grasas saturadas, sal y azúcares simples51. Ofrecer líquidos con frecuencia (agua, infusiones, zumos, consomés, gazpachos) para asegurar una buena hidratación34,47,49,51. Las dietas restrictivas (diabética, hiposódica, hipocalórica) tienen menos beneficios en los mayores de 75 años o frágiles y favorecen la malnutrición, por lo que deben evitarse34,47–49,51.
La mayoría de los nutrientes, si no todos, deben obtenerse de la alimentación oral. En las personas con problemas de masticación y deglución será preciso adaptar la textura y densidad de los alimentos con dietas de fácil masticación o trituradas. Las comidas enriquecidas (con huevo, leche en polvo, aceite de oliva, etc.) aportan mayor cantidad calórica y proteica en pequeñas cantidades de comida34,47,49,51.
Los suplementos nutricionales se utilizan para aportar energía y nutrientes cuando las medidas anteriores no son suficientes y son un complemento de la dieta enriquecida (no sustitutos de esta). Los suplementos deben aportar al menos 400kcal/día y 30g/día de proteínas. El tratamiento debe mantenerse al menos un mes, y reevaluar su indicación periódicamente34,47-49.
Las intervenciones nutricionales son más eficaces combinadas con ejercicio físico, mejorando la masa muscular y la capacidad funcional, especialmente en pacientes obesos34,47,48.
Recomendaciones
- •
Se recomienda una dieta variada y equilibrada, con alimentos frescos y medioambientalmente sostenibles (dieta mediterránea), si es posible desde la infancia.
- •
Se aconseja una dieta rica en proteínas, ya que las necesidades de este nutriente aumentan con la edad, especialmente en presencia de enfermedad.
- •
Se recomienda beber líquidos con frecuencia para evitar la deshidratación.
- •
Las personas mayores, especialmente aquellas con pérdida de peso involuntaria, deben someterse a un test de cribado nutricional con una herramienta validada, para identificar el riesgo o la presencia de malnutrición e iniciar un tratamiento dietético adecuado.
- •
Se recomienda combinar las intervenciones nutricionales con ejercicio físico, ya que se obtienen mejores resultados que solo con tratamiento dietético.
La polifarmacia suele definirse como el consumo de 5 o más medicamentos34, afectando a uno de cada 3 mayores en España, aunque también se define como el uso de más fármacos que los correctamente indicados, puesto que habrá una polifarmacia difícil de evitar con las comorbilidades en este grupo etario34.
Las personas mayores son más sensibles a los efectos secundarios de los fármacos, siendo escasos los ensayos clínicos en este grupo de población. Por ello, la prescripción debe ser más prudente y se debe basar en aportar beneficios en términos de morbimortalidad, calidad de vida y, sobre todo, funcionalidad, que es lo que más pierden los mayores34. La polifarmacia incrementa las interacciones farmacológicas, empeora la adherencia terapéutica, aumenta las reacciones adversas a medicamentos (RAM), el uso de fármacos inapropiados, el riesgo de ingreso hospitalario, caídas y mortalidad prematura34.
La deprescripción se define como el cese de un tratamiento de larga duración bajo supervisión médica52. Este concepto se asocia a otros como la revisión sistemática de la medicación, que puede concluir con la disminución, cambio o retirada de dosis de un medicamento con el objetivo de conseguir la mejor relación riesgo y beneficio en base a la mejor evidencia disponible, que en muchas ocasiones no será la aportada por ensayos clínicos aleatorizados. Sin embargo, la deprescripción es obligatoria, al margen de la edad, la polifarmacia o las comorbilidades34,53, si hay RAM moderadas/severas, interacciones relevantes, duplicidades de fármacos, indicación dudosa, falta de eficacia, enfermedades terminales, final de la vida, y si existe sobretratamiento farmacológico, frecuente en la HTA y la DM34. Sin embargo, existen importantes barreras para la deprescripción34, que dependen del sistema sanitario, del propio médico y del paciente y su entorno, sintetizadas en la tabla 5.
Barreras que dificultan la deprescripción
| Dependientes del médico | Acto médico que no se enseña en las facultadesReticencias de los profesionalesInercia terapéuticaIntervencionismo de las guías de práctica clínica |
| Dependientes del sistema | Automatización de la receta electrónicaImpersonalidad del sistemaPrescripción inducidaMedicalización y mercantilización de la medicinaImplicación de múltiples profesionales |
| Dependientes del paciente | Actitud contraria a la deprescripciónReticencias de los cuidadoresFalta de diálogo médico/paciente |
Fuente: elaboración propia.
Una reciente revisión sistemática de estudios randomizados54 ha mostrado que la deprescripción es segura y reduce el número y dosis de fármacos en los mayores, sin afectar a la mortalidad, hospitalización, visitas a urgencias y caídas, con resultados superiores respecto a la calidad de vida y costes sanitarios. Otra revisión sistemática con metaanálisis55 mostró que la deprescripción no modificaba significativamente la mortalidad en estudios randomizados (OR: 0,82; IC 95%: 0,61-1,11), aunque sí en estudios no randomizados (OR: 0,32; IC 95%: 0,17-0,60). La deprescripción no disminuyó el riesgo de una primera caída, pero sí de las siguientes55. Otra RS mostró que la revisión de la medicación redujo un 24% las caídas en mayores institucionalizados56. Una revisión sistemática57 identificó 2 ensayos clínicos en los que la deprescripción de antihipertensivos no era inferior a la continuación del tratamiento en las cifras de presión arterial. Otra revisión sistemática mostró que la disminución del tratamiento hipoglucemiante no modificó los niveles de hemoglobina glicosilada significativamente, sin cambios en caídas, hipoglucemias y hospitalizaciones58. La deprescripción de estatinas en pacientes frágiles de edad avanzada (>74 años) tampoco modificó la mortalidad y aumentó la calidad de vida59. Otros estudios34 avalan la deprescripción de benzodiacepinas e hipnóticos-Z, antidepresivos tras 6 meses sin sintomatología depresiva, inhibidores de la bomba de protones si no están bien indicados, inhibidores de la acetilcolinesterasa y la memantina si no son eficaces o en caso de demencia avanzada, neurolépticos si no hay respuesta clínicamente significativa y/o efectos secundarios y bifosfonatos tras 5 años de tratamiento, RAM graves y situaciones de corta esperanza de vida.
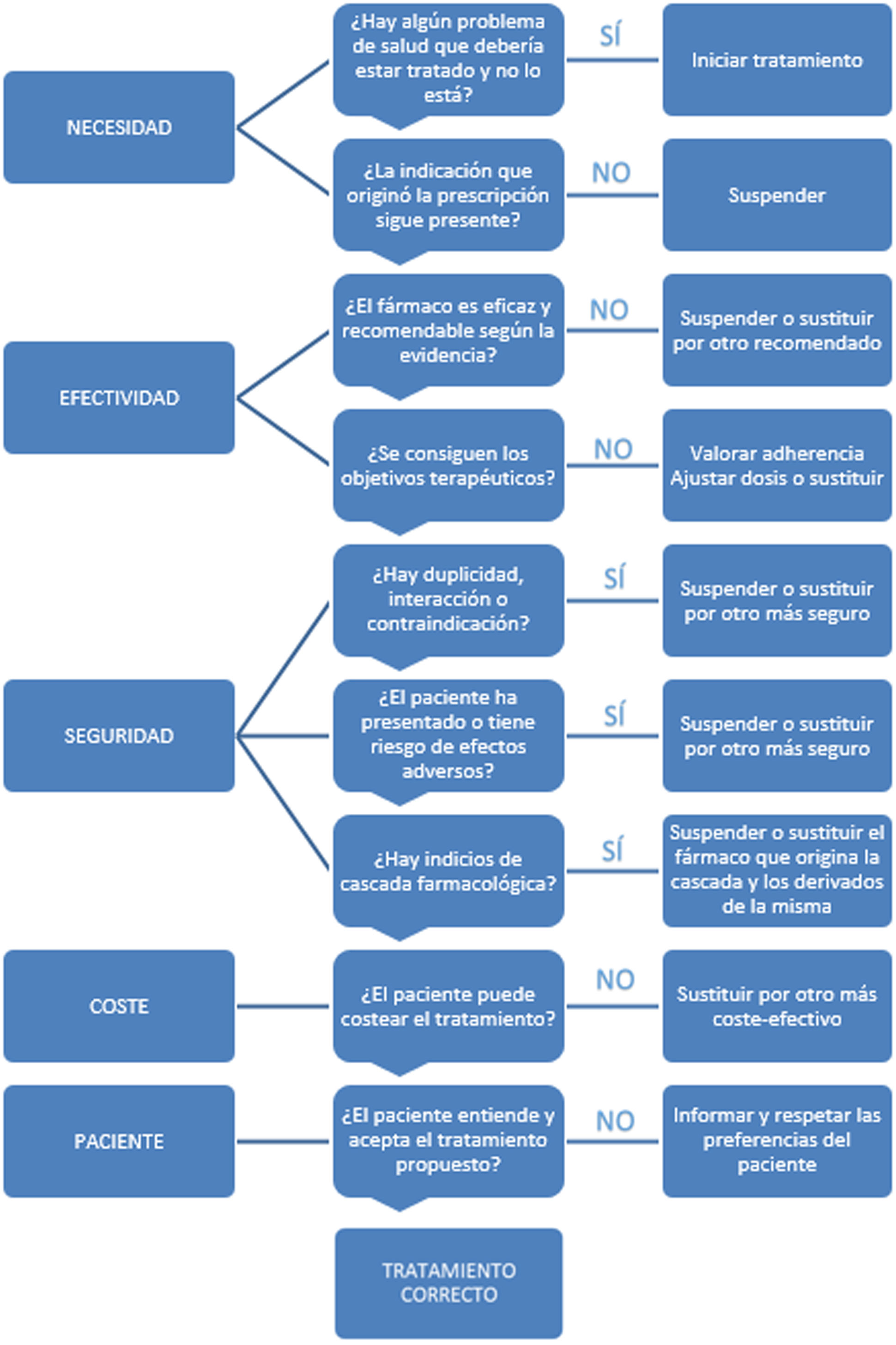
La deprescripción paso a pasoEl ámbito idóneo de la deprescripción es la atención primaria, al ser el medio sanitario que mejor conoce a los pacientes34,53. Se inicia revisando la lista de medicación con el paciente y/o cuidador, valorando las indicaciones, objetivos del tratamiento, riesgo de efectos secundarios, interacciones y los beneficios/perjuicios percibidos por el paciente34,53,60. El algoritmo de la figura 6 puede orientarnos en el proceso.
Algoritmo de revisión de la medicación. Fuente: Acosta Benito et al.34.
Diversas herramientas pueden facilitar la deprescripción (tabla 6), con métodos implícitos (centrados en el paciente) o explícitos (centrados en la medicación), aunque no sustituyen el criterio médico, las preferencias y las necesidades de cada paciente individual34,61. Los más utilizados son los criterios de Beers y los criterios de STOPP/START. Listados más específicos son los STOPP-Frail, orientados a pacientes con poca esperanza de vida, y LESS-CHRON, orientados a pacientes pluripatológicos34.
Herramientas de detección de la prescripción inadecuada1
| Herramienta | Características |
|---|---|
| Criterios Beers | Creados en 1991 y actualizados en el 2023. Tiene 3 listados de fármacos: a evitar siempre, a evitar en determinadas situaciones, y a usar con precaución en >75 años. Es el más usado en España |
| Criterios Screening Tool of Older Persons Prescriptions/Screening Tool to Alert doctors to Right Treatment (STOPP/START) | Publicados en 2008 y actualizados en 2023. Serían la alternativa europea a los criterios de BeersLos criterios STOPP son prescripciones inapropiadas en pacientes mayoresLos criterios START son prescripciones que podrían beneficiarlos en determinadas situaciones clínicas |
| Criterios STOPP-Frail o STOPP-Pal | Publicados en 2017 y desarrollados específicamente para pacientes frágiles con limitada esperanza de vida. Tiene 27 criterios ordenados por sistemas fisiológicos |
| Criterios List of Evidence baSed depreScribing from CHRONic patients (LESS-CHRON) | Elaborados en España en 2017 para pacientes con multimorbilidadConsta de 27 criterios o situaciones clínicas susceptibles de deprescripción, indicando cuáles precisan monitorización y seguimiento una vez retirada la medicación |
| Criterios Improved Prescribing in the Elderly Tool (IPET) | Elaborados en el año 2000, es un listado de los 14 errores de prescripción más frecuentes en mayores de 70 añosFácil de aplicar, su aceptación es limitada fuera de Canadá |
| Proyecto MARC | Promovido por el Ministerio de Sanidad, Servicios Sociales e Igualdad en 2014, es un listado de 14 grupos de medicamentos y 4 medicamentos específicos considerados como de alto riesgo |
| Listado Anticholinergic Risk Scale (ARS) | Elaborado en 2008, incluye 33 fármacos con efecto anticolinérgico, que se puntúan entre 1 (riesgo bajo) y 3 (riesgo alto) |
| Proyecto Assessing care of Vulnerable Elders (ACOVE) | Elaborado en 2001 en EE. UU. Consta de 217 indicadores de calidad basados en la mejor evidencia científica, destinados a pacientes geriátricos vulnerables. Solo el 29% se refieren a fármacos |
| Australian Prescribing Indicators Tool | Publicada en 2008, recoge 48 indicadores de determinadas condiciones médicas y escenarios clínicos. No está validada |
| Listado PRISCUS | Publicados en Alemania en 2010, consta de 83 medicamentos inapropiados en >65 años |
| Recomendaciones Polypharmacy | Publicados en Escocia en 2012, actualizados en 2018 y 2023. Tiene 49 recomendaciones y clasifica los fármacos en apropiados o no según la indicación para la que fueron prescritos por su eficacia o su seguridad |
| Anticholinergic Burden Calculator (ABC Calculator) | Desarrollada en 2017 en España, es una web gratuita que calcula la carga anticolinérgica en 9 escalas diferentes. Los resultados se muestran de forma cuantitativa, cualitativa, y mediante un código de colores en función del riesgo anticolinérgico |
| MedStopper | Página web para tomar decisiones en deprescripción. Se introducen los medicamentos que recibe el paciente y la herramienta secuencia las posibilidades de interrupción representado con caras. Incluye enlaces con calculadoras online de riesgo/beneficio y NNT |
| Deprescribing | Página que aborda la deprescripción según los riesgos asociados a diversos medicamentos en pacientes geriátricos (anticolinesterásicos y memantina, benzodiacepinas e hipnóticos-Z, antipsicóticos, hipoglucemiantes e inhibidores de la bomba de protones) |
| NICE Multimorbidity Guidance | Guía que aborda la optimización de la atención para adultos pluripatológicos al reducir la carga de tratamiento. Prioriza la toma de decisiones compartidas, valorando las prioridades de salud del paciente, estilo de vida y objetivos personales |
| NHS Polypharmacy Guidance | Publicada en Escocia en 2018, esta guía ofrece una estructura centrada en el paciente tanto para iniciar un tratamiento, como para revisar el existente. Incluye indicadores de polifarmacia, toxicidad acumulativa por anticolinérgicos y NNT |
| Método Medication Appropriateness Index (MAI) | Desarrollado en 1992 y validado para atención primaria y hospitalaria. Consta de 10 ítems, que puntúan de 1 a 3 según la adecuación terapéutica. Precisa bastante tiempo |
NNT: número de personas que es necesario tratar.
Fuente: elaboración propia.
El primer paso es comprobar qué fármacos toma el paciente, si tiene problemas con alguna medicación, si es efectiva, si le cuesta tomarla, si la puede costear, o si le produce efectos secundarios34.
El siguiente paso es identificar fármacos que se pueden deprescribir, revisando y retirando exclusivamente los fármacos inadecuados o innecesarios34,52,53, ya que deprescribir medicamentos esenciales podría ser nocivo. Es importante establecer con el paciente una relación de confianza y utilizar un lenguaje apropiado, para que comprenda la información34. En pacientes con déficit cognitivo será necesaria una mayor participación de los cuidadores.
El tercer paso, es el orden en que se van a retirar los fármacos. Se recomienda hacerlo de uno en uno, aunque podrían ser 2 o más simultáneamente en caso de reacciones adversas o prescripción en cascada. La deprescripción no es un proceso irreversible, hecho que tranquiliza a los pacientes y cuidadores34. Es aconsejable bajar la dosis progresivamente para evitar síntomas de retirada e identificar la dosis más baja eficaz, que minimizaría el riesgo de efectos adversos si no se puede retirar totalmente. Los pacientes y cuidadores serán advertidos de las posibles consecuencias de la retirada del fármaco, siendo preciso por ello un seguimiento estrecho, con un plan de visitas para monitorizar los cambios realizados, modificar el tratamiento y/o valorar nuevas prescripciones si fuese preciso34.
En todo caso, la toma de decisiones ha de ser compartida, valorando los objetivos del tratamiento según la situación clínica, funcional y social del paciente, su expectativa de vida, y sus preferencias personales34.
Recomendaciones
- •
Se recomienda la revisión sistemática de la medicación en los mayores.
- •
Se recomienda el uso de herramientas de ayuda a la deprescripción, como los criterios Beers 2023 o los STOPP-START 2023, así como otras herramientas adaptadas al entorno español (LESS-CHRON) y a situaciones de terminalidad (STOPP-Pal).
- •
La deprescripción debe priorizarse en mayores polimedicados, sobre tratados, frágiles, con enfermedades terminales y en el final de la vida.
- •
Se debe contar con la opinión del paciente y los cuidadores, discutiendo riesgos y beneficios, y tomando las decisiones de forma conjunta.
- •
El seguimiento es fundamental para establecer si se puede interrumpir un fármaco totalmente, reducir la dosis, o si hay que restaurarlo.
Una de las principales preocupaciones del aumento de envejecimiento en la población es la fragilidad, que se manifiesta en la pérdida de tonificación muscular, menor movilidad, rigidez articular y pérdida del control postural, factores que incrementan el riesgo de caídas y dependencia62. En este contexto, la actividad física emerge como una intervención crucial para mejorar la calidad de vida de las personas mayores62.
Ejercicio físico como medida preventivaEl ejercicio es una herramienta comprobada para prevenir múltiples patologías y la dependencia funcional. En personas mayores, el ejercicio reduce la incidencia de enfermedades como la DM y la obesidad, disminuye la mortalidad y retrasa la aparición de la fragilidad y la dependencia. Los beneficios del ejercicio se observan independientemente del estado funcional y nivel de fragilidad del paciente. Las recomendaciones de la OMS sugieren al menos 150 min de actividad aeróbica moderada o 75 minutos de actividad vigorosa a la semana, complementados con ejercicios de fortalecimiento muscular y de equilibrio 63. En la prevención de caídas, el ejercicio debe ser multifactorial, abordando el control postural, equilibrio, movilidad articular, fuerza, coordinación, agilidad, velocidad de reacción y capacidad aeróbica64,65. Los programas de acondicionamiento físico individualizados son esenciales para mantener la autonomía y prevenir la dependencia66.
Recomendaciones de ejercicio físico para las personas mayoresLas recomendaciones generales para la actividad física en las personas mayores se basan en la combinación de ejercicios aeróbicos, de equilibrio y de resistencia.
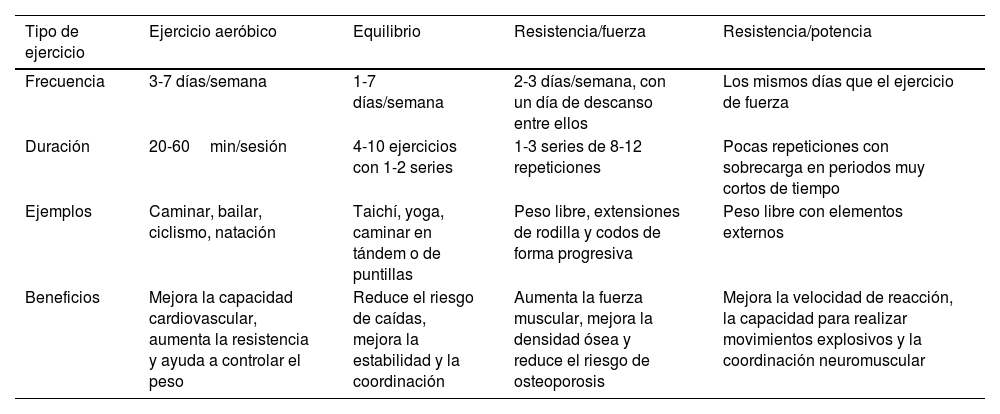
En la tabla 7, se detallan las indicaciones específicas para cada tipo de ejercicio.
Recomendaciones sobre ejercicio físico en el mayor
| Tipo de ejercicio | Ejercicio aeróbico | Equilibrio | Resistencia/fuerza | Resistencia/potencia |
|---|---|---|---|---|
| Frecuencia | 3-7 días/semana | 1-7 días/semana | 2-3 días/semana, con un día de descanso entre ellos | Los mismos días que el ejercicio de fuerza |
| Duración | 20-60min/sesión | 4-10 ejercicios con 1-2 series | 1-3 series de 8-12 repeticiones | Pocas repeticiones con sobrecarga en periodos muy cortos de tiempo |
| Ejemplos | Caminar, bailar, ciclismo, natación | Taichí, yoga, caminar en tándem o de puntillas | Peso libre, extensiones de rodilla y codos de forma progresiva | Peso libre con elementos externos |
| Beneficios | Mejora la capacidad cardiovascular, aumenta la resistencia y ayuda a controlar el peso | Reduce el riesgo de caídas, mejora la estabilidad y la coordinación | Aumenta la fuerza muscular, mejora la densidad ósea y reduce el riesgo de osteoporosis | Mejora la velocidad de reacción, la capacidad para realizar movimientos explosivos y la coordinación neuromuscular |
Fuente: elaboración propia.
La prescripción de ejercicio debe ser personalizada, considerando el estado funcional, nivel de dependencia y preferencias del individuo. El ejercicio multicomponente, que incluye actividades aeróbicas, de resistencia y de equilibrio, es especialmente efectivo34,64. Programas como Vivifrail67 ofrecen una guía estructurada para la prescripción de ejercicio en las personas mayores, adaptándose a su nivel de fragilidad y proporcionando ejercicios específicos para mejorar su capacidad función.
Recomendaciones
- •
Promover la actividad física en todas las personas mayores, adaptándose a sus capacidades y estado funcional, a través de una combinación de ejercicios aeróbicos, de equilibrio y de resistencia para prevenir la fragilidad y mejorar la calidad de vida.
- •
Implementar programas individualizados de ejercicio que se adapten a las necesidades específicas de cada persona mayor. Para maximizar los beneficios y minimizar los riesgos, estos programas deberían ser supervisados por profesionales cualificados
- •
Realizar evaluaciones regulares del riesgo de caídas en mayores de 70 años ayudan a identificar las personas en riesgo y a ajustar las intervenciones de ejercicio en consecuencia.
- •
Fomentar el envejecimiento activo y la participación social a través del ejercicio físico, entre otros.
Esta publicación no ha empleado casos de pacientes, investigación directamente con los mismos, no incluye datos personales, no es un ensayo clínico. No existe ninguna consideración ética en relación con la publicación.
FinanciaciónLos autores declaran no haber recibido ningún tipo de financiación para la realización de esta publicación.
Conflicto de interesesLos autores declaran no presentar conflictos de intereses relevantes para esta publicación.