Introducción
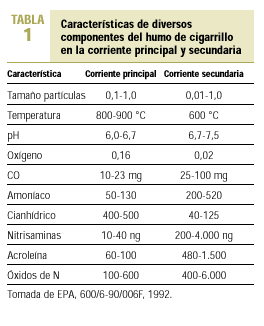
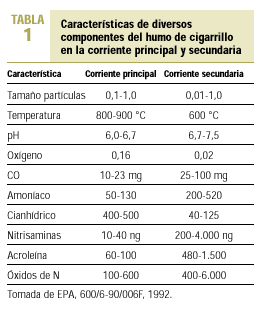
Se considera fumador pasivo a la persona que en un ambiente cerrado inhala humo de tabaco procedente de otros fumadores. Esta situación puede reproducir en el no fumador la situación del fumador activo que consume 4-10 cigarrillos. Esto es debido a que el humo que aspira el fumador pasivo o involuntario contiene una concentración de determinados componentes tóxicos muy superior a la del humo que aspira el fumador directamente del cigarrillo1 (tabla 1).
Hasta hace 20 años, el consumo de tabaco se consideraba un problema de elección y se pensaba que el fumador asumía sus riesgos personalmente; sin embargo, desde el informe del Surgeon General de 1986 quedó perfectamente documentado que el humo ambiental de tabaco era una causa de cáncer de pulmón en no fumadores2. Esto generó una respuesta social entre las administraciones responsables de la salud pública y se comenzó a generar toda una serie de medidas legislativas tendentes a proteger a los ciudadanos del humo ambiental de tabaco y a considerar que en caso de conflicto debía prevalecer el derecho a la salud de los no fumadores. La industria tabaquera intenta constantemente sembrar la confusión sobre esta cuestión mediante la contratación directa o indirecta de científicos con pocos escrúpulos. Una revisión de 106 estudios sobre fumadores pasivos desveló que un 37% (39/106) de los trabajos concluían que el fumar de forma pasiva no resultaba peligroso para la población. Un análisis de estos trabajos demostró que las tres cuartas partes de los estudios (29/39, 74%) que decían que el consumo pasivo de tabaco no era perjudicial estaban escritos por personas relacionadas de algún modo con la industria tabaquera3. En 1988 tuvo lugar una reunión de British American Tobacco (BAT) cuyo objetivo era planificar la supresión de la evidencia de los efectos para la salud del humo ambiental de tabaco. Una nota informativa de uno de los ejecutivos que participó tenía el siguiente contenido: «Los grupos de científicos deberían ser capaces de generar investigación o estimular la polémica de tal manera que las personas que lleven los asuntos públicos en los países pertinentes pudiesen usar, o difundir, esta información». Una reunión informativa de varias tabaqueras celebrada en 1988 confirmaba lo siguiente: «La estrategia mundial de Philip Morris consiste en coordinar y pagar a todos los científicos internacionales que haga falta para mantener viva la controversia relativa al humo ambiental del tabaco».4 Hace unos pocos años una potente campaña financiada por las compañías tabaqueras a través de los «independientes» «clubes de fumadores por la tolerancia», comparaba los riesgos del humo de segunda mano con beber algo de leche o tomar unas galletas, que es la técnica que usaron en el pasado para minimizar los riesgos del tabaquismo activo5,6. Aunque la evidencia científica tenga un margen de error, sólo existe una posibilidad entre 10.000 de que 24 de los 30 estudios que han encontrado asociación entre exposición al humo de tabaco y cáncer de pulmón se deban al azar7.
Morbilidad y mortalidad por tabaquismo pasivo
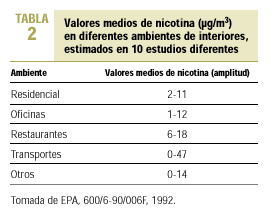
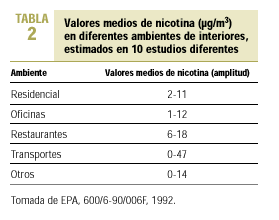
Como se ha dicho antes, se ha comprobado que los niveles de nicotina y de alquitrán en la corriente secundaria del cigarrillo son tres veces superiores a los de la corriente principal, y la concentración de monóxido de carbono (CO) alrededor de cinco veces superior. Existen otros productos químicos en forma de partículas o de gases. El humo del tabaco incluye irritantes y tóxicos sistémicos, como cianhídrico, dióxido de azufre, CO, amoníaco y formaldehído. El amoníaco se encuentra en dosis superiores a la esperada en el humo del tabaco. Hay pruebas de que los fabricantes de cigarrillos añaden amoníaco a las labores de tabaco con el fin de aumentar el poder adictivo de la nicotina y su acción cerebral. Existen iniciativas legislativas en la Unión Europea para evitar estas prácticas ilegales. El tabaco contiene asimismo, al menos, 42 sustancias cancerígenas y mutágenas como arsénico, cromo, nitrosaminas y benzopireno. La Agencia Estadounidense de Protección Medioambiental lo ha clasificado como carcinógeno de «clase A», o humano, para el cual no hay un nivel seguro de exposición1. El cadmio es un agente productor de cáncer en personas y en animales y se encuentra también en una concentración seis veces superior en la corriente secundaria8. Esto hace que el humo de la corriente secundaria pueda provocar trastornos a los no fumadores que conviven con fumadores9,10. La exposición al humo de tabaco ambiental puede producir irritación de la conjuntiva y de la mucosa de nariz, garganta y tracto respiratorio, y ocasiona en los sujetos expuestos picor de ojos con lagrimeo, congestión nasal con rinorrea y estornudos y picor de garganta con tos irritativa. Los modernos sistemas de limpieza de aire utilizados en lugares cerrados no son eficaces frente a muchos componentes del aire contaminado por el humo del tabaco (ACHT), dado que son efectivos para retirar las partículas del aire, pero no tanto para eliminar los gases11 (tabla 2).
Se estima que el ACHT es 57 veces más carcinógeno que cualquier otro elemento contaminante o radiaciones en función de la proporción de individuos expuestos y de la intensidad de esta exposición. En países con hábitos tabáquicos similares a los españoles, se estima que está expuesto un 30% de las personas en su lugar de trabajo y un 12-16% en el domicilio. Un 12% de los no fumadores son fumadores pasivos durante al menos 8 horas diarias y el 30-40% al menos una hora diaria12,13. Hachshaw et al realizaron un metaanálisis de los 37 estudios epidemiológicos en los que se analizaba la relación entre tabaquismo pasivo y cáncer. Concluyeron que estar casado con un fumador/a aumentaba el riesgo de cáncer de pulmón en un 26% (IC del 95%, 8-49%) y que hay una buena correlación según el número de años y el de horas diarias de convivencia14.
Desde 1984 se han publicado al menos 19 estudios que han demostrado que el humo de tabaco ambiental afecta a los lípidos de la sangre y contribuye a la presentación de angina de pecho y/o infarto de miocardio. Un metaanálisis de estudios epidemiológicos indica un 23% de exceso de riesgo (IC del 95%, 14-33%) de mortalidad por enfermedad coronaria después de ajustar los factores dietéticos de confusión en los que nunca han fumado que respiran el tabaco de sus cónyuges15. El riesgo relativo de enfermedad respiratoria crónica en el adulto fumador pasivo es del 25% (IC del 95%, 10-43%)16.
Hasta el momento la mortalidad relacionada con el ACHT se ha estudiado poco. En Estados Unidos se ha estimado que el tabaquismo pasivo es responsable de 3.000 fallecimientos anuales por cáncer de pulmón y de 35.000-62.000 a causa de cardiopatía isquémica. En la Unión Europea las estimaciones más conservadoras del programa «Europa contra el Cáncer» son de 22.000 fallecimientos al año debido al tabaquismo pasivo. Realizar un cálculo preciso del número de muertes atribuibles al ACHT en España es difícil. Esta estimación se limita a los 2 grupos de enfermedades para los que existe una fuerte y consistente evidencia sobre el efecto de la exposición al ACHT en el incremento de riesgo de fallecimiento (cáncer de pulmón y muertes perinatales e infantiles en menores de un año). En el primer caso, muertes por cáncer de pulmón, se utilizan estimaciones realizadas para la población de Canadá, asumiendo cierta relación entre el número de muertes atribuibles al consumo de tabaco y las debidas a la exposición al ACHT7. Las muertes por cáncer de pulmón en fumadores pasivos equivalen al 2,92% de los fallecimientos por cáncer de pulmón atribuibles al consumo activo de tabaco. Según esto, la estimación para España es que cada año se originan 376 muertes por cáncer de pulmón en fumadores pasivos. Por procedimientos parecidos, también se ha estimado que el número de muertes en niños españoles menores de un año por exposición al ACHT es de 240. El número de fallecimientos por cardiopatía isquémica en España es difícil de evaluar, pero nosotros los estimamos, al menos, en 2.000 casos anuales sobre la base de los datos de la Agencia de Protección Ambiental de California17. La estimación se hace en función de la cifra estimada en Estados Unidos para los no fumadores fallecidos por cardiopatía isquémica, teniendo en cuenta la proporcionalidad de poblaciones y las tasas relativamente bajas de cardiopatía isquémica en nuestro país. Extrapolando estos datos, la estimación más conservadora para España es de 2.500-3.000 fallecimientos cada año a causa del tabaquismo pasivo (considerando solamente las muertes por cardiopatía isquémica, cáncer de pulmón y mortalidad infantil).
El impacto que el humo del tabaco ambiental tiene sobre la mortalidad humana es dos veces mayor que el producido por el conjunto de todos los contaminantes ambientales reconocidos como tóxicos y que son objeto de control, lo cual contrasta con las tímidas iniciativas de control del tabaquismo pasivo en nuestro país y con el pobre cumplimiento de la legislación española sobre restricción de fumar en los lugares de trabajo (particularmente centros sanitarios y docentes) y espacios públicos cerrados18.
Tabaquismo pasivo en la infancia y la gestación
Son fundamentalmente los niños, y en especial los de edades más tempranas (los menores de 18 meses), los más afectados por el tabaquismo pasivo, dado que, por un lado, no pueden evitar la exposición al tabaco, ya que pasan la mayor parte del día en casa, en donde los padres fuman, y a que por otro lado tienen un aparato respiratorio todavía inmaduro y no se encuentran suficientemente desarrollados los mecanismos de defensa de éste19. Distintas investigaciones han mostrado cómo el potencial de contaminación del humo del tabaco en el domicilio es más importante que el grado de contaminación atmosférica urbana; a pesar de esto, según algunos trabajos, hasta un 75% de las madres fumadoras lo hace cerca del recién nacido y un 47-60% de estos neonatos presenta niveles significativos de cotinina (metabolito de la nicotina) en orina20-23. No obstante, como un 90% de las mujeres que fuma durante el embarazo continúa haciéndolo en los 5 años posteriores, es muy difícil separar los efectos de la exposición intrauterina de la ambiental a la que se ve sometido el neonato, aunque es probable que ambas tengan un efecto perjudicial independiente y aditivo24. Un 70% de los niños occidentales vive en casas en las que uno de los padres es fumador, el 30% de estos niños está expuesto diariamente al humo del tabaco y en un 10% pueden detectarse cotinurias importantes cuando son escogidos al azar en un colegio25. Del mismo modo, se ha comprobado que los niños de padres y madres que fuman inhalan nicotina en cantidad equivalente a un tabaquismo activo de 60-150 cigarrillos/año26.
Así, se ha asociado la exposición pasiva al humo del tabaco durante la infancia con un incremento del riesgo relativo de presentar enfermedades agudas del tracto respiratorio (laringotraqueítis, bronquitis, neumonía, asma...), síntomas respiratorios inespecíficos (tos, esputos, sibilancias, etc.), enfermedades agudas otorrinolaringológicas (sinusitis, rinitis, otitis...), con una mayor frecuencia de procesos tumorales en niños, muerte súbita del lactante, bajo peso al nacer y menor incremento de peso en neonatos hijos de fumadoras que de no fumadoras27. En relación con la asociación tabaquismo pasivo en la infancia-enfermedades respiratorias, se ha calculado que un 42% de los niños con enfermedad respiratoria crónica es fumador pasivo; se ha hallado una relación causal entre el consumo de tabaco de los convivientes con el desarrollo de enfermedades agudas del tracto respiratorio inferior en niños de 0-3 años, con una odds ratio (OR) de 1,57 cuando fumaba alguno de los padres, 1,72 si lo hace la madre y 1,29 cuando no fuma la madre pero lo hace cualquier otro conviviente28,29. También se ha encontrado asociación entre el número de cigarrillos consumidos por los progenitores y la presencia de sibilancias en sus hijos, de tal forma que el riesgo relativo de presentarlas era de 1,3 cuando los padres consumían 10 cigarrillos/día y de 1,6 si fumaban 2030.
La frecuencia de asma e hiperreactividad bronquial es mayor entre los hijos de fumadores que de no fumadores, aunque hay controversia sobre si puede actuar como factor etiológico del asma o sólo aumentar el número de reagudizaciones o interferir en su buen control31-33. La relación entre el número de exacerbaciones del asma y el tabaquismo pasivo no está todavía suficientemente probada, dado que mientras unos estudios28,34 encuentran que los hijos asmáticos de padres fumadores presentan un 70-80% más de reagudizaciones, otros estudios sólo han detectado asociación con el asma, pero no con el número de exacerbaciones35,36. También se ha demostrado que los hijos de madres fumadoras tienen un 28% más de ingresos hospitalarios por bronquiolitis y neumonía37. Se ha hallado una asociación positiva entre el consumo de tabaco por parte de los padres y la presentación de enfermedad meningocócica invasiva en niños, relacionándose el tabaquismo materno con un incremento del riesgo de la enfermedad de casi cinco veces. El consumo de tabaco por parte del padre aumentaba el riesgo casi cuatro veces, y cuando fumaban los 2 progenitores el riesgo presentado por sus hijos fumadores pasivos era nueve veces más elevado que el de los hijos de no fumadores38.
Los niños fumadores pasivos tienen un 70% más de infecciones de las vías respiratorias altas que los no expuestos al humo del tabaco y presentan además un mayor riesgo de otitis purulentas crónicas (causa más común de sordera y cirugía en los niños), faringitis y amigdalitis39.
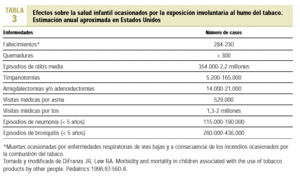
El hecho de que las madres fumadoras produzcan menor cantidad de leche y con menor contenido de grasa condiciona que los hijos de fumadoras ganen menos peso que los de las no fumadoras, lo que provoca un retraso en el desarrollo estatoponderal del lactante40,41. El tabaquismo pasivo durante la infancia también se ha relacionado con un mayor riesgo de desarrollar cáncer, tanto en los cinco primeros años de vida como en la edad adulta; así Janerich encontró que un 17% de los casos de carcinoma primario de pulmón en no fumadores adultos se podía atribuir a la exposición al humo del tabaco en la infancia y adolescencia42,43. También se ha observado que el absentismo escolar de los niños fumadores pasivos es significativamente superior al de aquellos que se mueven en ambientes no contaminados por el humo de los cigarrillos (21% frente al 17%)44. En la tabla 3 se exponen los principales efectos que el humo del tabaco ocasiona en los fumadores pasivos en Estados Unidos45.
Gestación y tabaco
La repercusión del humo del tabaco en el feto es un hecho constatado, tanto si se trata de una madre fumadora activa como pasiva, dado que en fetos de madres no fumadoras pero expuestas involuntariamente al humo del cigarrillo se producen respuestas orgánicas mensurables debidas al paso a través de la placenta de distintos compuestos de dicho humo, por lo que los fetos de mujeres fumadoras pasivas se pueden equiparar a los de fumadoras activas de un consumo medio de 4-6 cigarrillos/día46. Esta circunstancia es la que nos hace hablar del «fumador terciario intrauterino»27.
De este modo el consumo de tabaco por parte del padre adquiere gran importancia, dado que se ha objetivado que los fetos hijos de padres fumadores de 20 cigarrillos/día, con madre fumadora pasiva, pesan unos 88 g menos al nacer, y cuando la madre es fumadora los recién nacidos pesan 150-250 g menos que los nacidos de matrimonios donde ninguno de los progenitores fuma47,48. A pesar de ello, un 58% de las mujeres españolas embarazadas fuma al principio de la gestación, abandona el tabaco durante el embarazo tan sólo un tercio e incluso un 24% no reconocía la recomendación de su médico para abandonar el tabaco19. El consumo de tabaco en la mujer se ha relacionado con una disminución de su fertilidad, tanto por el número de años con capacidad para la concepción (la menopausia se adelanta 1-2 años y la menarquia se retrasa), como por trastornos hormonales (alteración del perfil estrogénico durante el ciclo menstrual, dismenorrea, amenorrea, mayor degeneración de los ovarios y de los folículos maduros y mayor frecuencia de infecciones en los órganos reproductivos)27,49.
Una vez fecundado el óvulo, el humo del tabaco sigue actuando en el feto, dado que parte de sus componentes son capaces de atravesar la barrera hematoplacentaria, comprobándose que los niveles de cotinina (metabolito de la nicotina) del feto pueden alcanzar hasta un 90% de los maternos durante el embarazo50. La placenta presenta alteraciones anatomopatológicas (necrosis isquémica, infartos retroplacentarios, aumento del espacio intravelloso...) que, junto con un incremento de los niveles de carboxihemoglobina en la sangre de la gestante, condicionan un mayor número de complicaciones del embarazo (hemorragias, depósitos fibrosos subcoriónicos, placenta previa, desprendimiento prematuro de placenta...) y una mayor hipoxia fetal que en las embarazadas no expuestas al humo del tabaco51,52. El conjunto de alteraciones presentes en los fetos de madres fumadoras se ha denominado «síndrome del tabaco fetal», que incluye: bajo peso al nacer, aumento del riesgo de complicaciones obstétricas, embarazo ectópico, alteración de las pruebas funcionales respiratorias, endocrinas, mutaciones en distintos tipos celulares, mayor riesgo de cáncer en los niños e incremento de la mortalidad perinatal27,53.
Se ha estimado que el riesgo de síndrome de muerte súbita del lactante (SMSL) (muerte repentina de un lactante sin que se encuentre la causa clínica ni necrópsica) en madres fumadoras durante la gestación es tres veces superior al de las no fumadoras54, y Anderson y Cook encuentran una odds ratio de 2,08 para el tabaquismo materno prenatal y un 1,94 para el posnatal, aumentando el riesgo con el número de cigarrillos fumados al día55,56. Se considera que dicho incremento de riesgo puede ser debido, por un lado, a que el humo del tabaco puede provocar anormalidades en el desarrollo pulmonar y cerebral del lactante, detectando en los niños «fumadores» cambios en el control y maduración del sistema autonómico durante el sueño REM, desequilibrio que puede provocar una tendencia a presentar apneas centrales; por otro lado, como dicho humo puede irritar directamente las vías respiratorias y/o facilitar infecciones en éstas, también se ha especulado sobre si la nicotina tiene capacidad de alterar la respuesta ventilatoria a la hipoxia57-60.
Se ha observado que la exposición intraútero al tabaquismo de la gestante puede afectar a la función pulmonar del niño tras su nacimiento, alteración que puede persistir en la edad adulta61. Así, Gilliland encontró que, cuando la exposición se produce durante el embarazo, son las medidas de la pequeña vía aérea, MMEF y FEF75, las que principalmente se ven afectadas, mientras que cuando la exposición se produce tras el nacimiento el parámetro más alterado respecto a los niños no expuestos es el FEV25-75/FVC, aunque debemos reseñar que en este último estudio no consideraron la posible exposición intraútero a la que pudieron estar sometidos los fetos62,63.
Filippini, en un estudio realizado en 244 niños de 0-15 años con cáncer en el sistema nervioso central (SNC), halló que fumar antes del embarazo no se asociaba con un aumento del riesgo de presentar tumores en el SNC durante la infancia; sin embargo, el consumo activo de cigarrillos por la madre en las primeras 5 semanas de embarazo estaba asociado con un riesgo aumentado de presentar un tumor del SNC, (OR, 1,5; IC del 95%, 1,0-2,3). También detectaron un incremento del riesgo en los hijos de madres no fumadoras, pero muy expuestas al humo del tabaco durante los 2 primeros meses de embarazo (OR, 1,8; IC del 95%, 1,2-2,6) y al final de éste (OR, 1,7; IC del 95%, 1,2-2,5)64,65. Todo ello nos hace reflexionar sobre la necesidad de incluir dentro de nuestros programas de deshabituación tabáquica a este grupo de especial riesgo que forman las mujeres embarazadas.
Tabaquismo pasivo en el medio laboral
Wells analizó 14 estudios que abordaban el problema del tabaquismo pasivo en el medio laboral. Se utilizaron 6 criterios de calidad para realizar un metaánalisis de estos trabajos de cara a obtener el riesgo combinado. Cinco estudios alcanzaron los estándares de calidad requeridos para el análisis. El riesgo relativo combinado fue de 1,39 (IC del 95%, 1,15-1,68%) y se basó en 835 cánceres de pulmón66. Un estudio reciente se realizó en una cohorte de camareros de 53 locales de la ciudad de San Francisco, a los que se entrevistó antes y después de la aplicación de la legislación. Se entrevistó un total de 53 camareros, todos ellos expuestos al humo de tabaco en su jornada laboral. Después de entrar en vigor la ley, su exposición al humo de tabaco pasó de 28 a 2 h semanales. Treinta y nueve camareros refirieron inicialmente síntomas de infección respiratoria. De éstos, un 59% no presentaba síntomas en la encuesta final. El 77% de los camareros refería inicialmente síntomas irritativos de mucosas. Al final del estudio, un 78% de estos sujetos no presentó estos síntomas. La desaparición al final del estudio de la mayoría del ACHT se asoció con una mejoría de la FVC y de la FEV1 después de controlar el hábito tabáquico personal y las infecciones respiratorias de vías altas. El estudio concluyó que los empleados de bares y tabernas experimentan menos síntomas respiratorios y de irritación de mucosas de forma clara cuando se elimina la exposición al humo de tabaco en los locales donde ejercen su actividad laboral67.
Aunque ya desde 1978 la Constitución Española, en su art. 43, reconoce el derecho a la protección de la salud, es durante los años ochenta del pasado siglo cuando se han empezado a desarrollar normativas en este sentido. La Ley General de Sanidad, en su art. 25.2, declara al tabaco «sustancia nociva para la salud de la persona», seguida de reales decretos que por una parte, de forma general, señalan que el derecho de los no fumadores a respirar aire sin humo prevalecerá sobre el derecho de los fumadores a consumir tabaco en lugares de uso común, como el Real Decreto 192/1988, de 4 de marzo, sobre limitaciones en la venta y uso del tabaco para la protección de la salud de la población, art. 1. Por otra hay regulaciones de la prohibición de consumo de tabaco en numerosos lugares públicos, como los Reales Decretos 192/1988 de 4 de marzo y 1293/1999 de 23 de julio, donde se prohíbe el consumo de tabaco en lugares donde exista mayor riesgo de la salud del trabajador por combinar el tabaco con otros contaminantes, en cualquier área laboral donde trabajen mujeres embarazadas, centros sanitarios y docentes y aquellos destinados a menores de 16 años (en estos dos últimos casos se diferenciarán y señalizarán áreas específicas donde se permita fumar), y zonas de oficinas de las Administraciones Públicas destinadas a la atención directa al público68. Esta legislación de ámbito nacional se ha visto ratificada en numerosas comunidades autónomas. En Aragón, la ley 3/2001 de prevención, asistencia y reinserción social en materia de drogodependencias contempla aspectos de limitación de consumo en su art. 14, señalización en su art. 15 y la preferencia del derecho de los no fumadores en su art. 1669. Centrándonos en el entorno laboral, la Ley de Prevención de Riesgos Laborales viene a garantizar la seguridad y la salud de los trabajadores, así como la vigilancia y control de su salud70. Por tanto, nos encontramos en un escenario en el que, por una parte, existe evidencia científica suficiente que demuestra que la exposición al humo del tabaco en el medio ambiente, y concretamente en el medio laboral, supone un riesgo para la salud, y por otra la reglamentación laboral exige a los empresarios, de un modo general, el velar por la protección de la salud de sus trabajadores; como consecuencia, el medio laboral debería constituir un entorno adecuado para actividades relacionadas con la promoción de la salud, entre las que se enmarca la prevención y control del tabaquismo71. Por otra parte, no debemos olvidar el gran impacto de salud pública que tiene el hecho de incluir estas actividades en el medio laboral, ya que hasta ahora en España las intervenciones sobre la cesación del hábito tabáquico se han desarrollado mayoritariamente en el ámbito individual desde las consultas médicas y/o de enfermería en el nivel asistencial de atención primaria. Pero este procedimiento alcanza fundamentalmente a aquella población con alto grado de demanda de servicios de salud, entre los que no se encuentran los varones en edad laboral. Por esta razón, los programas de cesación o de reducción del hábito tabáquico en el medio laboral constituyen una necesidad, dado que una elevada proporción de fumadores infrautiliza los servicios sanitarios, concentrándose en el medio laboral los recursos precisos para desarrollar dichos programas. Esta necesidad de proteger a las personas de la exposición al ACHT contrasta con que tradicionalmente en nuestro país la «salud laboral» o «medicina ocupacional» ha constituido un nivel sanitario caracterizado por sus actividades asistenciales y preventivas sobre los riesgos relacionados con las exposiciones específicas de cada medio laboral y que, referida al tabaco, se centraba casi exclusivamente en la prohibición de fumar por motivos de seguridad como, por ejemplo, evitar riesgos de incendio72. Actualmente, iniciativas de promoción de salud en el ámbito del tabaquismo todavía son escasas en nuestro país. Según una encuesta realizada por el Instituto Nacional de Seguridad e Higiene en el Trabajo, en el marco de la Red Europea de Promoción de la Salud en el puesto de trabajo, solamente habían realizado educación sanitaria sobre el tabaco un 48,9% de las empresas encuestadas en el sector servicios, el 57,7% en la industria y un 34,8% en la construcción73. No obstante, las posibilidades de intervención dependerán de las características de la empresa o lugar de trabajo. Como mínimo, la intervención debe garantizar el derecho de los trabajadores que no fuman a respirar un aire sin humo de tabaco70. Las actuaciones sobre el tabaquismo en el entorno laboral se pueden clasificar en varios niveles. Un primer nivel correspondería a las limitaciones para fumar en el lugar de trabajo. La principal motivación para implantar esta medida es la de proteger a los trabajadores no fumadores del humo del tabaco ambiental. La mayoría de los estudios establece que las restricciones incrementan el número de ex fumadores, e incluso aceleran el proceso de cambio de un mismo fumador, aumentando la motivación para dejar de hacerlo, con un mayor número de individuos en fase de contemplación; también a la disminución del número de cigarrillos/día en los trabajadores que aún siguen fumando71. Un segundo nivel de intervención sería los programas de ayuda al fumador en el entorno laboral, que se han demostrado útiles y efectivos72,74.
Correspondencia: Rodrigo Córdoba García. Centro de Salud Delicias Sur. C/ Dronda, 1. 50009 Zaragoza. España. Correo electrónico: rcordobag@papps.org
Manuscrito recibido el 14 de enero de 2002.
Manuscrito aceptado para su publicación el 13 de mayo de 2002.