La pancreatectomía izquierda laparoscópica (PIL) es una técnica quirúrgica cada vez más utilizada para el tratamiento de lesiones benignas y malignas del páncreas izquierdo. Analizamos los resultados de nuestra serie de PIL para el tratamiento de las lesiones primarias de cuerpo y cola pancreáticos.
MétodosDesde noviembre de 2011 a noviembre de 2017 se han intervenido 18pacientes por lesiones primarias del páncreas realizándose una pancreatectomía distal laparoscópica. En todos los casos se dejó un drenaje intraabdominal y se siguieron las recomendaciones del International Study Group for Pancreatic Fistula (ISGPF).
ResultadosLa mediana de edad fue de 66,5años (RIQ46-74). De las 18 pancreatectomías izquierdas, cuatro se realizaron con preservación esplénica, una de ellas una pancreatectomía central. Hubo dos conversiones. La mediana del tiempo operatorio fue de 247,5min (RIQ242-275). La mediana de estancia hospitalaria fue de 7días (RIQ6-8). A los 90días se detectaron complicaciones en cinco pacientes: tres gradoII, una gradoIII y una gradoV según la clasificación modificada de Clavien-Dindo. Hubo una fístula pancreática gradoB y cuatro pacientes reingresaron por colecciones peripancreáticas. La anatomía patológica evidenció malignidad en el 38,9% de los casos, presentando todos ellos márgenes negativos.
ConclusionesLa PIL puede ser considerada técnica de elección para el tratamiento de las lesiones pancreáticas benignas y una alternativa al abordaje abierto para pacientes seleccionados diagnosticados de neoplasias malignas, siempre que la realicen cirujanos con experiencia en cirugía pancreática y laparoscópica avanzada.
Laparoscopic left-sided pancreatectomy (LLP) is an increasingly used surgical technique for the treatment of benign and malignant lesions of the left side of the pancreas. The results of LLP as a treatment for primary pancreatic lesions of the head and tail of the pancreas were evaluated.
MethodsFrom November 2011 to November 2017, 18 patients underwent surgery for primary lesions of the pancreas by means of a laparoscopic distal pancreatectomy. An intra-abdominal drain tube was used in all cases, and the recommendations of the International Study Group for Pancreatic Fistula (ISGPF) were followed.
ResultsThe mean age was 66.5years (IQR 46-74). Among the 18 left pancreatectomies performed, four were with splenic preservation, and one was a central pancreatectomy. There were two conversions. The median surgical time was 247.5minutes (IQR 242-275). The median postoperative hospital stay was 7days (IQR 6-8). After 90days, complications were detected in five patients: three gradeII, one gradeIII and one gradeV according to the modified Clavien-Dindo classification. There was one gradeB pancreatic fistula, and four patients had to be readmitted to hospital because of peripancreatic collections. The anatomic pathology diagnosis was malignant neoplasm in 38.9% of cases, all of them with negative resection margins.
ConclusionsLLP can be considered the technique of choice in the treatment of primary benign pancreatic lesions and an alternative to the open approach in selected patients diagnosed with malignant pancreatic lesions.
La introducción del abordaje laparoscópico en la patología quirúrgica pancreática ha sido de las más tardías dentro de la cirugía mínimamente invasiva. El incremento en el diagnóstico de lesiones pancreáticas incidentales debido al mayor número de exploraciones radiológicas que se realizan actualmente ha generado un interés creciente por el aprendizaje de estas técnicas mínimamente invasivas1. Tanto la resección pancreática izquierda como la duodenopancreatectomía cefálica1-4 son posibles y seguras por laparoscopia, siendo la segunda técnicamente más exigente, ya que consta de una fase reconstructiva.
La pancreatectomía izquierda laparoscópica (PIL) está ampliamente aceptada para el tratamiento de las lesiones quísticas, benignas o premalignas, como la neoplasia quística mucinosa y la neoplasia mucinosa papilar intraductal, así como de los tumores neuroendocrinos localizados en el páncreas izquierdo5,6. También se considera indicada en el tratamiento de las lesiones malignas que precisan una resección pancreática con márgenes adecuados y linfadenectomía extendida2,6,7. Diversos grupos ya han demostrado su seguridad cuando se realiza por cirujanos laparoscopistas con experiencia8-11. No obstante, en muchos centros de nuestro país todavía no se contempla la PIL como el abordaje de elección sino exclusivamente para casos seleccionados12.
El objetivo de este trabajo es analizar los resultados de nuestra serie de pacientes intervenidos mediante PIL como tratamiento de las lesiones primarias de cuerpo y cola pancreáticos a fin de comprobar su efectividad y seguridad y sumar nuestra experiencia a las series publicadas.
MétodosPara la realización del estudio se ha empleado la base prospectiva de pacientes intervenidos mediante resección pancreática del servicio de cirugía del Hospital Doctor Peset. Desde noviembre de 2011 a noviembre de 2017 se realizaron 25 pancreatectomías izquierdas por lesiones pancreáticas primarias del cuerpo y cola: 18 (72%) laparoscópicas y 7 (28%) abiertas. Se seleccionaron para el abordaje laparoscópico los pacientes sin cirugías supramesocólicas previas, con tumores no excesivamente voluminosos y sin infiltración de otros órganos. La población final del estudio la componen los 18 pacientes intervenidos mediante abordaje laparoscópico.
Se considera pancreatectomía izquierda cualquier tipo de resección pancreática que precise la sección glandular completa a la izquierda de la arteria gastroduodenal. Este término incluye las pancreatectomías corporocaudales, las pancreatectomías centrales y las pancreatectomías distales12. La sección del parénquima pancreático se realizó con endograpadora lineal, con una profundidad de grapa de 3,8mm. En la pancreatectomía central además se realizó una anastomosis pancreatoyeyunal término-terminal del páncreas izquierdo remanente por intususcepción sobre asa en Yde Roux. En todos los casos se dejó un drenaje cerrado cercano a la línea de sección del parénquima pancreático. Durante la intervención se inició la administración de octreótido subcutáneo 100μg/8h13. Se determinó la cifra de amilasas en el líquido de drenaje al tercer día postoperatorio. Si el nivel de amilasas fue menor de tres veces el valor de la amilasemia, se retiró el drenaje y la administración de octreótido.
Se siguieron las recomendaciones del International Study Group for Pancreatic Fistula (ISGPF) para el diagnóstico y la clasificación de la fístula pancreática postoperatoria14. Se empleó la clasificación modificada de Clavien-Dindo para la gradación de las complicaciones postoperatorias que se contabilizaron a 90días15. La estancia hospitalaria se calculó desde el día de la intervención hasta el alta a domicilio y se consideraron como reingresos los casos en que la readmisión se produjo en los primeros 30días postoperatorios.
Ante la sospecha preoperatoria de neoplasia maligna del páncreas se planificó una esplenopancreatectomía en bloque con linfadenectomía estándar según la técnica RAMPS (esplenopancreatectomía corporocaudal modular radical anterógrada) descrita previamente por Strasberg et al.16.
Para el análisis estadístico descriptivo se ha utilizado el programa informático Excel. Las variables discretas se expresan como frecuencias y porcentajes. Las variables continuas se expresan como medianas y rangos intercuartílicos (RIQ).
ResultadosDurante el periodo de estudio fueron intervenidos 18 pacientes mediante PIL por lesión pancreática primaria localizada en el páncreas izquierdo. La serie consta de 12 mujeres y 6 hombres con una mediana de edad de 66,5años (RIQ46-74), un índice de masa corporal (IMC) de 30,1 (RIQ27-32) y, según la Asociación Americana de Anestesiología (ASA), el 88,9% de los pacientes se clasifican como ASA≥2. En la tabla 1 se muestran las características epidemiológicas y clínicas de estos pacientes.
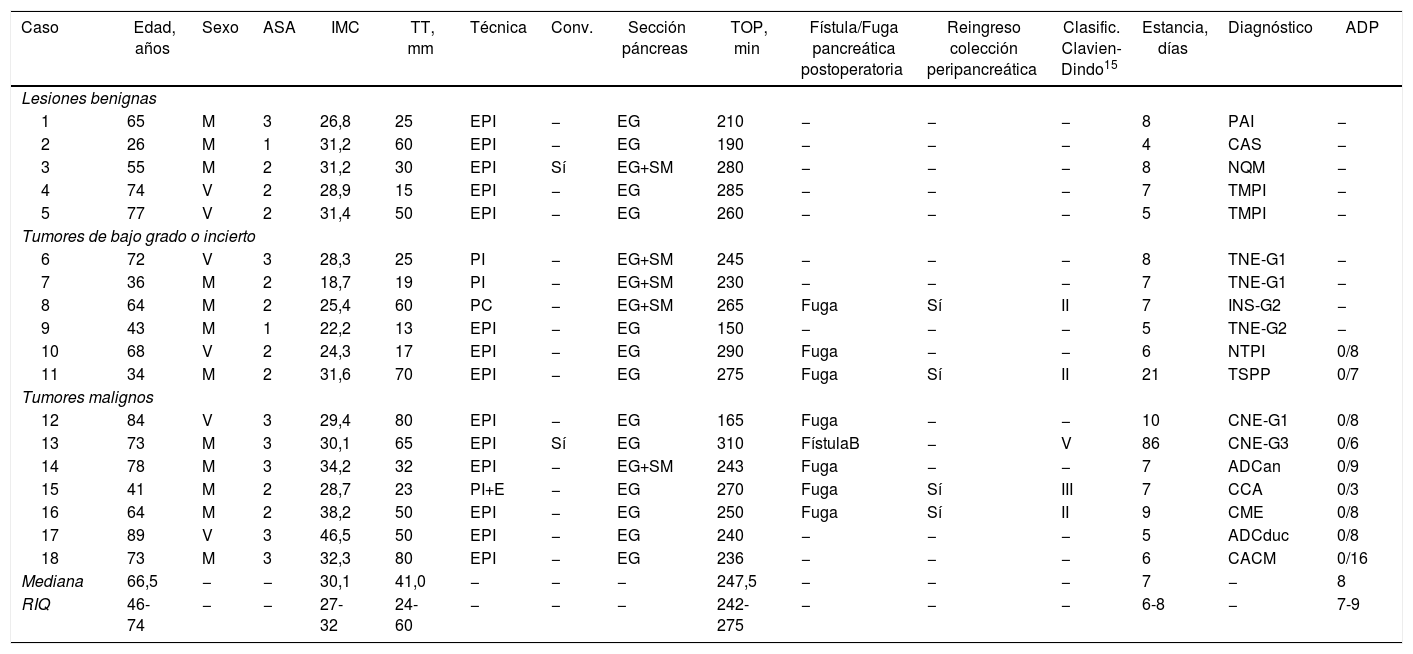
Datos demográficos, operatorios y postoperatorios de los pacientes intervenidos mediante pancreatectomía izquierda laparoscópica
| Caso | Edad, años | Sexo | ASA | IMC | TT, mm | Técnica | Conv. | Sección páncreas | TOP, min | Fístula/Fuga pancreática postoperatoria | Reingreso colección peripancreática | Clasific. Clavien-Dindo15 | Estancia, días | Diagnóstico | ADP |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Lesiones benignas | |||||||||||||||
| 1 | 65 | M | 3 | 26,8 | 25 | EPI | − | EG | 210 | − | − | − | 8 | PAI | − |
| 2 | 26 | M | 1 | 31,2 | 60 | EPI | − | EG | 190 | − | − | − | 4 | CAS | − |
| 3 | 55 | M | 2 | 31,2 | 30 | EPI | Sí | EG+SM | 280 | − | − | − | 8 | NQM | − |
| 4 | 74 | V | 2 | 28,9 | 15 | EPI | − | EG | 285 | − | − | − | 7 | TMPI | − |
| 5 | 77 | V | 2 | 31,4 | 50 | EPI | − | EG | 260 | − | − | − | 5 | TMPI | − |
| Tumores de bajo grado o incierto | |||||||||||||||
| 6 | 72 | V | 3 | 28,3 | 25 | PI | − | EG+SM | 245 | − | − | − | 8 | TNE-G1 | − |
| 7 | 36 | M | 2 | 18,7 | 19 | PI | − | EG+SM | 230 | − | − | − | 7 | TNE-G1 | − |
| 8 | 64 | M | 2 | 25,4 | 60 | PC | − | EG+SM | 265 | Fuga | Sí | II | 7 | INS-G2 | − |
| 9 | 43 | M | 1 | 22,2 | 13 | EPI | − | EG | 150 | − | − | − | 5 | TNE-G2 | − |
| 10 | 68 | V | 2 | 24,3 | 17 | EPI | − | EG | 290 | Fuga | − | − | 6 | NTPI | 0/8 |
| 11 | 34 | M | 2 | 31,6 | 70 | EPI | − | EG | 275 | Fuga | Sí | II | 21 | TSPP | 0/7 |
| Tumores malignos | |||||||||||||||
| 12 | 84 | V | 3 | 29,4 | 80 | EPI | − | EG | 165 | Fuga | − | − | 10 | CNE-G1 | 0/8 |
| 13 | 73 | M | 3 | 30,1 | 65 | EPI | Sí | EG | 310 | FístulaB | − | V | 86 | CNE-G3 | 0/6 |
| 14 | 78 | M | 3 | 34,2 | 32 | EPI | − | EG+SM | 243 | Fuga | − | − | 7 | ADCan | 0/9 |
| 15 | 41 | M | 2 | 28,7 | 23 | PI+E | − | EG | 270 | Fuga | Sí | III | 7 | CCA | 0/3 |
| 16 | 64 | M | 2 | 38,2 | 50 | EPI | − | EG | 250 | Fuga | Sí | II | 9 | CME | 0/8 |
| 17 | 89 | V | 3 | 46,5 | 50 | EPI | − | EG | 240 | − | − | − | 5 | ADCduc | 0/8 |
| 18 | 73 | M | 3 | 32,3 | 80 | EPI | − | EG | 236 | − | − | − | 6 | CACM | 0/16 |
| Mediana | 66,5 | − | − | 30,1 | 41,0 | − | − | − | 247,5 | − | − | − | 7 | − | 8 |
| RIQ | 46-74 | − | − | 27-32 | 24-60 | − | − | − | 242-275 | − | − | − | 6-8 | − | 7-9 |
ADCan: adenocarcinoma anaplásico; ADCduc: adenocarcinoma ductal; ADP: relación adenopatías positivas/totales resecadas (solo para neoplasias malignas); ASA: Asociación Americana de Anestesiología; CACM: cistoadenocarcinoma mucinoso; CAS: cistoadenoma seroso; CCA: carcinoma de células acinares; CME: carcinoma mucoepidermoide; CNE: carcinoma neuroendocrino; Conv.: conversión a cirugía abierta; EG: endograpadora; EG+SM: endograpadora y sutura continua manual de refuerzo del borde pancreático; EPI: esplenopancreatectomía izquierda; FístulaB: fístula pancreática grado B; Fuga: fuga bioquímica; G1, G2, G3: grado histológico bajo, intermedio, alto, según la Clasificación de la Organización Mundial de la Salud (OMS) para los tumores neuroendocrinos 2010-2017; IMC: índice de masa corporal; INS: insulinoma; M: mujer; NQM: neoplasia quística mucinosa; NTPI: neoplasia tubulopapilar intraductal; PAI: pancreatitis autoinmune; PC: pancreatectomía central; PI: pancreatectomía izquierda con preservación esplénica y de los vasos esplénicos; PI+E: pancreatectomía izquierda con preservación esplénica y esplenectomía en un segundo tiempo; RIQ: rango intercuartílico; TMPI: tumor mucinoso papilar intraductal; TNE: tumor neuroendocrino no funcionante; TOP: tiempo operatorio; TSPP: tumor sólido pseudopapilar; TT: tamaño tumoral; V: varón.
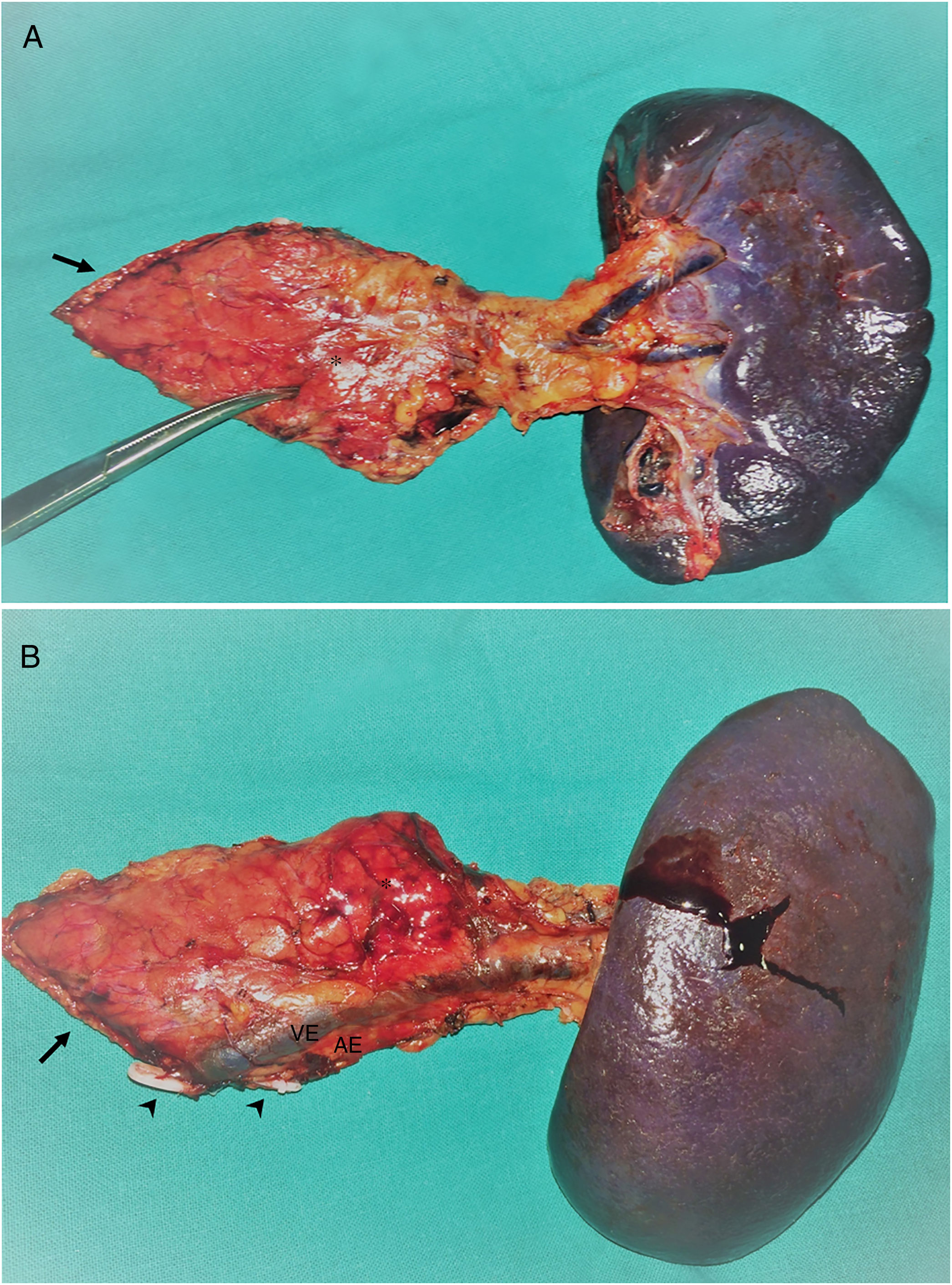
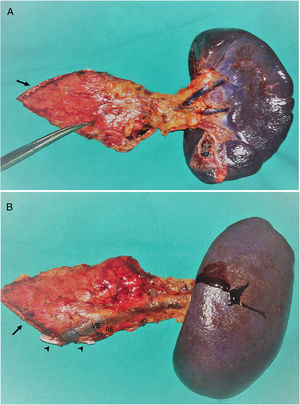
Se realizaron 17 (94,4%) pancreatectomías corporocaudales y una (5,6%) pancreatectomía central, cuatro de ellas (22,2%) con preservación esplénica y de los vasos esplénicos. En la figura 1 se muestra una pieza de pancreatectomía izquierda. La mediana de tiempo operatorio fue de 247,5min (RIQ242-275). En tres (16,7%) pacientes se asoció además otra cirugía: una colecistectomía, una miomectomía y una colecistectomía más gastrectomía atípica, esta última por infiltración tumoral. En dos (11,1%) pacientes fue necesaria la conversión a cirugía abierta: en uno por dificultades técnicas en la disección caudal del páncreas y en otro por una hemorragia intraoperatoria incontrolable por laparoscopia. Dos (11,1%) pacientes precisaron transfusión sanguínea en el perioperatorio.
Pieza de esplenopancreatectomía izquierda. A)Cara anterior. B)Cara posterior.
Asterisco: tumor neuroendocrino, también señalado con la pinza de Pean. Flecha: borde de sección pancreático; VE: vena esplénica; AE: arteria esplénica: ambas selladas con clips hem-o-lok (puntas de flecha).
En el postoperatorio se detectó una (5,6%) fístula pancreática que requirió drenaje percutáneo (gradoB). Este paciente falleció a los 86días por un episodio de insuficiencia respiratoria. También se detectaron siete (38,9%) fugas bioquímicas, que siguiendo la última revisión de la ISGPF14 no se consideran inicialmente como fístulas pancreáticas. Cuatro (22,2%) de estos pacientes reingresaron durante el primer mes tras el alta por colecciones peripancreáticas, de los que solo uno requirió drenaje percutáneo. Así pues, el porcentaje de fístulas fue del 27,8%. Ningún paciente precisó una reintervención quirúrgica durante el postoperatorio. Se detectaron complicaciones a los 90días en cinco (31,3%) pacientes del estudio: tres Clavien-Dindo gradoII, una gradoIII y una gradoV, que se muestran desglosadas en la tabla 2. La mediana de estancia hospitalaria fue de 7días (RIQ6-8).
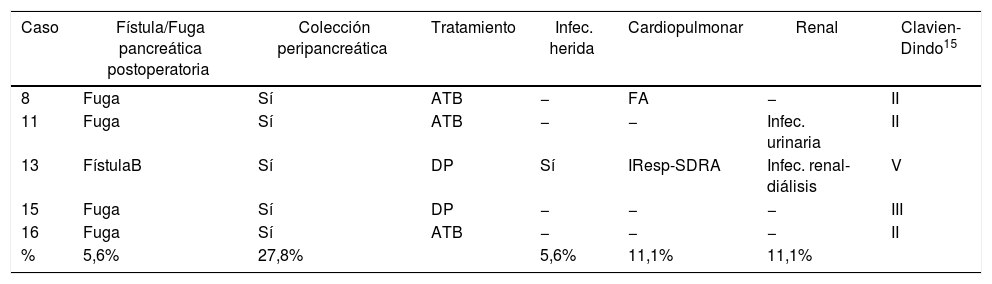
Complicaciones postoperatorias de los pacientes intervenidos mediante pancreatectomía izquierda laparoscópica
| Caso | Fístula/Fuga pancreática postoperatoria | Colección peripancreática | Tratamiento | Infec. herida | Cardiopulmonar | Renal | Clavien-Dindo15 |
|---|---|---|---|---|---|---|---|
| 8 | Fuga | Sí | ATB | − | FA | − | II |
| 11 | Fuga | Sí | ATB | − | − | Infec. urinaria | II |
| 13 | FístulaB | Sí | DP | Sí | IResp-SDRA | Infec. renal-diálisis | V |
| 15 | Fuga | Sí | DP | − | − | − | III |
| 16 | Fuga | Sí | ATB | − | − | − | II |
| % | 5,6% | 27,8% | 5,6% | 11,1% | 11,1% |
ATB: antibioterapia intravenosa; DP: drenaje percutáneo; FA: fibrilación auricular paroxística; FístulaB: fístula pancreática grado B; Fuga: fuga bioquímica; IResp: insuficiencia respiratoria; SDRA: síndrome de distrés respiratorio del adulto; %: porcentaje de pacientes respecto al total de pacientes intervenidos.
El tamaño de las lesiones fue variable, con una mediana de 41mm (RIQ24-60). Los diagnósticos definitivos se muestran en la tabla 1. En siete (38,9%) pacientes el diagnóstico definitivo fue de neoplasia maligna. A un paciente con sospecha diagnóstica preoperatoria de tumor sólido pseudopapilar se le realizó una PIL con preservación esplénica, y ante el diagnóstico definitivo de carcinoma de células acinares pancreáticas hubo que realizarle una esplenectomía radical laparoscópica en un segundo tiempo. En todos los casos los márgenes de sección pancreática estuvieron libres de enfermedad. La mediana de ganglios obtenidos en los pacientes con diagnóstico de malignidad fue de 8 (RIQ7-9). Tras una mediana de seguimiento de 22meses (RIQ17-41), el 71,4% de los pacientes con neoplasia maligna de páncreas izquierdo permanecen libres de enfermedad.
DiscusiónA pesar de que la PIL está aceptada actualmente para el tratamiento de las lesiones benignas localizadas en el páncreas izquierdo y de que se ha comprobado su seguridad para las lesiones malignas2,10, su uso todavía no se ha estandarizado en muchos centros debido a que se trata de una técnica muy demandante que requiere experiencia en cirugía pancreática y cirugía laparoscópica avanzada y también por el escaso número de pacientes, que hace difícil la adquisición de experiencia.
Las cifras publicadas de complicaciones, fístula pancreática clínicamente relevante y mortalidad para las resecciones del páncreas izquierdo alcanzan tasas muy dispares, del 25-70%, 6-40% y 0-7%, respectivamente5,12,17-22. El estudio europeo DISPACT22, que incluye 450 pacientes intervenidos de pancreatectomía izquierda mediante abordaje convencional, publica una tasa total de complicaciones postoperatorias del 70%, con un 45% de pacientes con al menos una complicación grave, un 6% de infección de herida y una mortalidad a 90días del 3%. Un estudio multicéntrico20 retrospectivo en 127 pacientes intervenidos en centros europeos con experiencia laparoscópica señala una tasa de complicaciones relacionadas con el páncreas del 31%, incluyendo un 17% de fístulas pancreáticas clínicamente relevantes, una tasa de conversión del 14%, un 6,3% de reintervenciones y una mortalidad del 0%. En nuestro país, Fernández-Cruz et al.5 publican ya en 2007 una amplia serie de PIL con una tasa de conversión del 7%, morbilidad postoperatoria del 25,2, del 16,7 y del 40%, y de fístula pancreática del 7,7, del 10 y del 35%, en el grupo de pancreatectomía izquierda con preservación esplénica, de pancreatoesplenectomía izquierda y de enucleación, respectivamente, con una mortalidad del 0%. La mayoría de estas series mezclan diferentes tipos de lesiones pancreáticas así como diferentes técnicas quirúrgicas. Además, los resultados obtenidos están estrechamente relacionados con la definición y clasificación de las complicaciones utilizada, con la minuciosidad en la recogida de datos, así como con la experiencia de los equipos quirúrgicos. Independientemente de ello, hasta el momento los resultados de los estudios retrospectivos comparativos entre el abordaje laparoscópico y abierto17-19,23 y metaanálisis publicados2,3,24,25 no han encontrado diferencias significativas en cuanto al tiempo operatorio, tasa de fístula pancreática en pancreatectomía izquierda, mortalidad e incluso radicalidad oncológica, y sí que encuentran ventajas a favor del abordaje laparoscópico en cuanto a reducción de las pérdidas sanguíneas, estancia postoperatoria, complicaciones totales y una recuperación postoperatoria más rápida. Recientemente, Konstantinidis et al.26, en un estudio en pacientes mayores de 70años y pacientes frágiles intervenidos de PIL encuentran menos complicaciones Clavien-Dindo gradoIV y menos mortalidad que en los intervenidos mediante cirugía abierta, con resultados estadísticamente significativos. Esto remarca la importancia del abordaje laparoscópico sobre todo en los pacientes con una reserva fisiológica disminuida.
En nuestra serie, cinco (27,8%) pacientes tuvieron una fístula o colección peripancreática. Tras la sección del páncreas con endograpadora, dependiendo de la calidad del grapado, del grosor y de la consistencia del páncreas, se reforzó con una sutura manual continua el margen de sección pancreático en cinco de los 18 pacientes, de los cuales únicamente uno presentó una fístula pancreática postoperatoria (FPPO). Con el propósito de prevenir la FPPO se han utilizado los análogos de la somatostatina13,27, así como diferentes métodos de cierre del muñón pancreático residual. Dos estudios DISPACT28,22, así como un metaanálisis Cochrane29, revelan que ni la sección del páncreas con endograpadora ni la sección con bisturí seguida de cierre manual del remanente pancreático muestran diferencias en términos de fístula pancreática o mortalidad postoperatoria. Actualmente, la elección de la técnica de cierre del muñón pancreático depende de la preferencia del cirujano y de las características anatómicas del páncreas. Independientemente de esto, estamos de acuerdo con Poves et al.12 en que la sección del páncreas se debe realizar a nivel del cuello, donde el parénquima es más delgado y el grapado suele ser más efectivo y seguro.
Recientemente la ISGPS ha revisado los criterios de FPPO aceptados en 200514. La nueva definición incluye cualquier volumen de líquido de drenaje con amilasas superior a tres veces el límite alto normal de la amilasa plasmática a partir del tercer día postoperatorio, y añade que esta condición ha de ser clínicamente relevante. Consecuentemente, la antigua fístula gradoA pasa a denominarse fuga bioquímica, puesto que no tiene relevancia clínica y ya no se considera una verdadera fístula pancreática ni una complicación. De hecho, muchas series ya habían excluido la fístula gradoA del análisis de sus resultados14. Sin embargo, aunque no puede llamarse fístula, tampoco puede ser ignorada, ya que implica una mínima fuga que puede ser motivo de colecciones tardías y reingresos, como ocurre en cuatro de nuestros pacientes. En un artículo publicado recientemente10 se disminuye significativamente la incidencia de FPPO dejando un pequeño drenaje aspirativo suave en el lecho de sección pancreática en lugar de un drenaje multitubular. Se señala que a pesar del riesgo de colecciones abdominales, estas permanecen asintomáticas en la mayoría de los casos. Las fístulas pancreáticas gradosB yC también adquieren una definición más exacta.
La PIL es una técnica compleja, con tiempos operatorios superiores a 3h en la mayoría de las series10,12,21. Nuestro tiempo operatorio fue de 247,5min, mayor que el publicado en algunos estudios17,18 y similar al de otros12,21,28. Los tumores de gran tamaño, la preservación esplénica o las resecciones oncológicas aumentan el tiempo operatorio, y en nuestra serie muchas lesiones pancreáticas son voluminosas (41mm de mediana), tenemos un 38,9% de patología maligna y pacientes con un IMC elevado (30,1 de mediana). Sin embargo, únicamente hubo que convertir a cirugía abierta en dos (12,5%) pacientes: en uno por dificultades técnicas y en otro por una hemorragia. Jusoh y Ammori1 señalan como causas más comunes de conversión la hemorragia, la dificultad en la exposición, las adherencias intraabdominales, las adherencias retroperitoneales secundarias a malignidad o pancreatitis crónica y el fallo en el progreso de la cirugía. La obesidad visceral dificulta la exposición, la identificación del páncreas y las maniobras de disección10, y también ha sido considerada como factor predictivo significativo de conversión en la pancreatectomía izquierda30.
En nuestra serie planteamos la cirugía de conservación esplénica cuando la sospecha diagnóstica preoperatoria es de benignidad, siempre que las condiciones anatómicas lo permitan. Esto subraya la importancia de determinar el tipo de lesión pancreática antes de la intervención para proponer la exéresis más adecuada. Sin embargo, las ventajas de la conservación esplénica deben sopesarse frente a los inconvenientes de una resección incompleta en caso de tumor maligno, como ocurrió en uno de nuestros pacientes que requirió una esplenectomía radical en un segundo tiempo.
Actualmente no hay estudios aleatorizados que comparen la pancreatectomía distal laparoscópica con la cirugía abierta en pacientes con neoplasias malignas de páncreas, y recientemente el grupo europeo DIPLOMA ha iniciado el primer ensayo clínico de estas características. Sin embargo, diversos grupos han señalado que es posible una óptima radicalidad oncológica y que el abordaje laparoscópico puede ser una alternativa segura al abierto en pacientes con adenocarcinoma2,5,8,9,11. Los datos de estudios retrospectivos sugieren que la tasa de márgenes negativos y el número de ganglios linfáticos resecados en el abordaje laparoscópico y el abierto son similares2,7,9, y aunque los datos de recidiva y de supervivencia son limitados, también se muestran similares7,9. En un estudio multicéntrico retrospectivo de cohortes pareadas obtienen un mayor porcentaje de resecciones R0 y un menor número de ganglios linfáticos extraídos en el abordaje laparoscópico, con una supervivencia media comparable31. Sin embargo, no deja de ser un estudio retrospectivo y los mismos autores señalan posibles sesgos y la necesidad de realizar estudios aleatorizados. En los siete pacientes con patología maligna intervenidos en nuestra serie obtenemos el 100% de márgenes de resección negativos y una mediana de ocho ganglios aislados. Tras una mediana de seguimiento de 22meses (RIQ17-41) el 71,4% de los pacientes con neoplasia maligna de páncreas izquierdo siguen vivos y sin recurrencia.
En conclusión, la PIL puede considerarse la técnica de elección para el tratamiento de las lesiones pancreáticas benignas y una alternativa al abordaje abierto para pacientes seleccionados diagnosticados de neoplasias malignas, siempre que la realicen cirujanos con experiencia en cirugía pancreática y laparoscópica avanzada. No cabe duda de que todavía quedan aspectos controvertidos pendientes de resolver en la PIL, pero está claro que el cirujano pancreático debe formarse en esta técnica que podemos considerar estándar para la resecciones pancreáticas izquierdas.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial, o entidades sin ánimo de lucro.
Conflicto de interesesNinguno.