El trasplante simultáneo páncreas-riñón es el tratamiento de elección en pacientes con diabetes mellitus tipo 1 que han desarrollado enfermedad renal crónica terminal, mejorando su supervivencia y calidad de vida1,2. La morbimortalidad del trasplante de páncreas es frecuentemente el resultado de las complicaciones secundarias de la inmunosupresión, infecciones oportunistas y complicaciones quirúrgicas de las anastomosis3–6.
Reportamos el caso de un paciente retrasplantado de páncreas aislado (TAP) con reciente disfunción pancreática por rechazo agudo, que ingresa por disnea y dolor abdominal, diagnosticándose durante su estancia de infección pulmonar por citomegalovirus (CMV), presentando finalmente abdomen agudo (fig. 1).
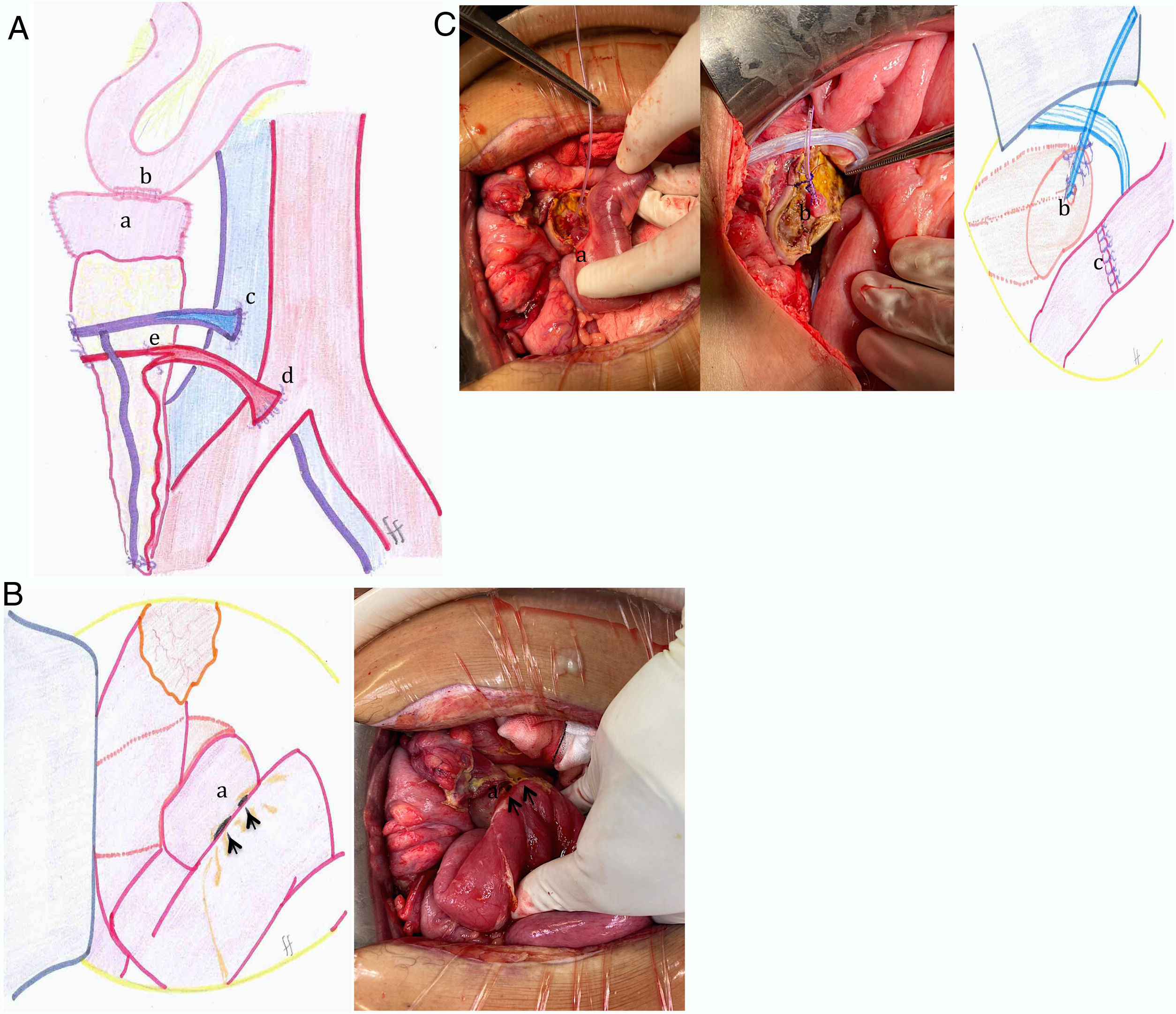
A. Figura esquemática del trasplante pancreático. a: segmento duodenal del injerto pancreático; b: anastomosis bicapa L-L manual entre el duodeno (injerto) y el yeyuno (receptor) a 60cm del ligamento de Treitz; c: anastomosis porto-cava T-L; d: reconstrucción arterial en «Y» mediante cirugía de banco, utilizando injerto de arteria iliaca del donante anastomosando la arteria mesentérica superior y esplénica; se realiza anastomosis T-L con la arteria iliaca primitiva derecha. B. Dehiscencia de anastomosis duodeno-yeyunal. a: segmento duodenal del injerto pancreático. Flechas negras: perforaciones de la anastomosis duodeno-yeyunal. C. Técnica quirúrgica realizada. a: duodenectomía (del injerto) y resección de la anastomosis duodeno-yeyunal; b: tutorización externa del conducto de Wirsung; c: restitución del tránsito intestinal mediante anastomosis T-T manual yeyuno-yeyunal.
Se trata de un varón de 54 años de edad, con antecedentes de trasplante simultáneo páncreas-riñón en el año 2000 por diabetes mellitus tipo 1, con enfermedad renal crónica terminal. Posteriormente tuvo fallo del injerto pancreático, realizándose TAP en 2009. Como tratamiento inmunosupresor recibía: prednisona 5mg/día, micofenolato de mofetilo 500mg/8h y tacrolimus 5mg/día. En 2020 manifestó deterioro de la función renal (Cr 2,7mg/dl) en contexto de infección por neurotoxoplasmosis, desescalándose la inmunosupresión a monoterapia con rapamicina 0,5mg/día. Dos meses antes del ingreso en Urgencias presentó: hiperglucemia, necesidad de insulina exógena e incremento de las enzimas pancreáticas. La biopsia del injerto corroboró rechazo agudo mediado por células. Los niveles séricos de rapamicina fueron subóptimos (1ng/ml), requiriendo bolos de corticoides.
Los síntomas de consulta a Urgencias fueron disnea y dolor abdominal. En el examen físico se hallaba hemodinámicamente estable (TA 91/59mmHg y FC 87lpm), afebril, con una frecuencia respiratoria de 21rpm y una saturación de O2 del 97%. En la analítica se objetivó: leucocitosis (12.460×106/l), amilasa 169U/l, dímero-D>2.000ng/ml y creatinina 3,8mg/dl. La radiografía de tórax presentó infiltrados bilaterales. Ante la sospecha inicial de infección pulmonar, ingresa en Nefrología.
Durante su estancia, se descartó infección por patógenos virales oportunistas en sangre mediante test de reacción en cadena de la polimerasa. La TAC toracoabdominal objetivó focos de consolidación pulmonares. Asimismo, se descartó infección por COVID-19. El análisis de lavado broncoalveolar mediante reacción en cadena de la polimerasa resultó positivo para CMV (900 copias), por lo que se administró ganciclovir intravenoso 2,5mg/kg/día. Inesperadamente, presentó exacerbación del dolor abdominal y fiebre, efectuándose TAC abdominal con hallazgos de perforación de víscera hueca y colecciones abdominales. Ante estos hallazgos se optó por realizar una laparoscopia exploratoria.
Los hallazgos intraoperatorios confirmaron la presencia de una peritonitis purulenta difusa y plastrón en fosa iliaca derecha; por lo que se decide conversión por sospecha de perforación del injerto duodeno-pancreático. Se corroboró dehiscencia de la anastomosis duodeno-yeyunal del injerto, realizándose resección de la anastomosis y restitución del tránsito mediante anastomosis yeyuno-yeyunal manual. Se practicó duodenectomía (injerto) y tutorización externa del Wirsung por el proceso inflamatorio local y la inestabilidad del paciente.
El postoperatorio fue óptimo, aislándose Enterococcus faecalis en cultivo del líquido peritoneal. El drenaje intraabdominal fue retirado el quinto día postoperatorio, tras análisis de amilasa negativos; se obliteró el tutor pancreático por débito nulo, siendo dado de alta en su octavo día postoperatorio.
En la revisión a 30 días, el paciente presentaba buen estado general y el tutor pancreático fue retirado sin incidencias. A los 60 días presentaba mejor control del perfil glucémico, con mínimos requerimientos de insulina exógena (12U/día), HbA1c 6,3%, péptido C 0,23nmol/l y con función renal estabilizada (Cr 2,3mg/dl).
La tasa de dehiscencia de la anastomosis duodeno-yeyunal del injerto es una complicación reportada en el 5-20%. Mayoritariamente se presenta en el postoperatorio temprano, siendo su manifestación tardía infrecuente3,4. La aparición de esta complicación tras 11 años del trasplante TAP es una de las más tardías publicadas en la literatura mundial7.
La etiología de la perforación duodenal del injerto se atribuyó a rechazo agudo debido a los hallazgos del estudio anatomopatológico, que incluyen infiltrado inflamatorio mixto predominantemente crónico. Asimismo, el análisis de inmunofluorescencia para CMV fue negativo. La serie de eventos acontecidos tras la neurotoxoplasmosis, en consecuencia, desescalada de inmunosupresión, desencadenaron el rechazo agudo del injerto pancreático, siendo la biopsia por rechazo del injerto y la infección entérica por CMV (la cual no pudo ser corroborada en nuestro caso) factores que han sido asociados a fístula del segmento duodenal4,7,8. Cabe señalar que pese a su alta sensibilidad, las pruebas histológicas e inmunohistoquímicas no pueden descartar infección intestinal por CMV9; por este motivo, su papel etiopatogénico en el presente caso clínico es incierto, dado que sí se confirmó en el lavado broncoalveolar.
Las técnicas habitualmente recomendadas para el manejo quirúrgico de dehiscencia de la anastomosis del injerto son: rafia primaria de la perforación (en caso de que las condiciones locales sean favorables) y trasplantectomía (en caso de sepsis y condiciones locales adversas)4,8. En el caso presentado, la duodenectomía y tutorización del Wirsung es una alternativa descrita excepcionalmente por el grupo de Minnesota10 frente a la opción de trasplantectomía que ha permitido salvaguardar la función endocrina a 2 meses de seguimiento en beneficio de la calidad de vida del paciente.
En conclusión, la dehiscencia de la anastomosis duodeno-yeyunal como complicación tardía del trasplante pancreático es inusual. En este contexto, el rechazo agudo así como la infección por CMV son factores de riesgo, por lo que resulta imprescindible un correcto equilibrio y la monitorización estrecha del tratamiento inmunosupresor. En este escenario, la duodenectomía con preservación del injerto pancreático es una opción quirúrgica válida que debe tenerse en cuenta.