Los pacientes con enfermedad valvular presentan mayor riesgo de complicaciones perioperatorias en el contexto de cirugía no cardiaca. La importancia del anestesiólogo desde la consulta de preanestesia para valorar la severidad de la enfermedad y su intervención activa es determinante.
El manejo de este caso clínico se reporta para poner en valor la necesidad que tiene el paciente cardiópata de ser atendido de manera multidisciplinar.
Presentamos el caso de un paciente de 80 años con estenosis aórtica severa, aneurisma de aorta abdominal infrarrenal de 46mm; enfermedad pulmonar obstructiva crónica, hipertensión arterial controlada; proceso linfoproliferativo. Tras valoración preanestésica se indicó cirugía valvular reparadora previa a la cirugía por cáncer de colon. La optimización preoperatoria mediante la cirugía cardiaca y el ajuste del tratamiento farmacológico, así como el apoyo en la monitorización hemodinámica para la toma de decisiones durante el periodo perioperatorio, mediante un dispositivo mínimamente invasivo (Vigileo®), fueron las claves en el correcto manejo de este paciente; combinamos raquianalgesia con morfina intratecal y anestesia general. El paciente se mantuvo estable con IC 2,3 - 3 l/min/m2, VVS 2 - 7% y ScvO2 74- 67%.
Tras el éxito del proceso anestésico-quirúrgico concluimos que hoy en día tenemos la obligación de conocer y aplicar las recomendaciones disponibles en las guías elaboradas por las sociedades de anestesiología y cardiología, de forma conjunta, que se actualizan continuamente y permiten al clínico protocolizar la toma de decisiones basándose en la evidencia científica.
Patients with valve disease are at a higher risk of perioperative complications in the context of non-cardiac surgery. The active involvement of the anaesthetist from the moment of the pre-anaesthesia assessment to determine the severity of the disease is crucial.
The purpose of this report on the management of a clinical case is to highlight the need for a multidisciplinary approach to the patient with heart disease.
We present the case of a patient in the eighth decade of life with severe aortic stenosis, and a 46mm infra-renal abdominal aortic aneurysm; chronic obstructive pulmonary disease, controlled arterial hypertension; and a lymphoproliferative process. Following the pre-anaesthesia assessment, valve repair surgery was indicated prior to a surgical procedure for colon cancer resection. Key to the successful management of this patient was pre-operative optimization with cardiac surgery and adjustment of the pharmacological treatment, plus haemodynamic monitoring as a basis for decision-making during the perioperative period using a minimally invasive device (Vigileo®). Spinal analgesia with intrathecal morphine was combined with general anaesthesia. The patient remained stable with CI 2.3 - 3 l/min/m2, SVV 2 - 7% and ScvO2 74- 67%.
As a result of the successful anaesthetic and surgical process, we concluded that it is our duty at the present time to know and apply the recommendations contained in the guidelines developed by the anaesthesia and cardiology societies and their regular updates, as they allow clinicians to make decisions in accordance with evidence-based protocols.
Desde la puesta en marcha de forma protocolizada de la consulta de preanestesia, el anestesiólogo juega un papel fundamental en la optimización de los resultados del acto anestésico-quirúrgico. Este objetivo es todavía más crucial en el paciente con una cardiopatía. Para ello se han creado las guías de recomendaciones de cuidados del paciente cardiópata1,2 que deben aplicarse en el periodo preoperatorio, intraoperatorio y postoperatorio y que abarcan desde la modificación de la pauta de un tratamiento farmacológico crónico no idóneo, a la cirugía cardiaca previa o la monitorización hemodinámica intra- y postoperatoria minuciosas. Dichas guías se basan en la evidencia científica y se crean entre expertos cardiólogos y anestesiólogos. En la bibliografía se demuestra que en octogenarios con estenosis aórtica severa, como nuestro caso, la supervivencia mejora significativamente si el paciente es intervenido respecto a los que no se intervienen3–5.
En la actualidad el anestesiólogo juega un papel fundamental para conseguir «la pieza clave»: el logro del estado óptimo del paciente sin que ello suponga una demora significativa.
Caso clínicoPaciente varón de 80 años con neoplasia de recto en cuya valoración destacaba una estenosis aórtica severa (área valvular 0,8cm2) asintomática; aneurisma de aorta abdominal infrarrenal de 46mm; enfermedad pulmonar obstructiva crónica, hipertensión arterial; proceso linfoproliferativo. Tras consulta con cardiología, se decidió realizar cirugía de reparación valvular a través de miniesternotomía con prótesis biológica n.° 23.
El paciente fue remitido 4 meses más tarde para nueva evaluación tras el recambio valvular y quimioterapia neoadyuvante para reducir la masa tumoral y ser reevaluado tras la indicación de cirugía oncológica.
La nueva ecocardiografía mostró: ventrículo izquierdo ligeramente dilatado y normofuncionante (FEVI 65%), sin alteraciones de la contractilidad. Prótesis biológica disfuncionante con gradientes máximo y medio de 45 y 23mmHg con leaks periprotésico que impresionaba de severo. Insuficiencia tricúspide moderada-severa con PSAP estimado de 50mmHg. Dilatación biauricular (AI 47mm-31cm2).
Durante este periodo posrecambio valvular y tratamiento quimioterápico, sufrió dos episodios de insuficiencia cardiaca izquierda que respondieron al tratamiento farmacológico. Cateterismo cardiaco: coronarias normales.
El paciente estaba en tratamiento con bisoprolol, terazosina, budesonida, bromuro de ipratropio, atorvastatina, irbesartan, sulfato ferroso, suplementos de potasio y ranitidina.
El diagnóstico tras reevaluarlo fue: insuficiencia aórtica severa posquirúrgica por disfunción de prótesis biológica con buena función sistólica. Clase funcional II. EPOC e hipertensión pulmonar moderada. Se optimizó el tratamiento farmacológico retirando bisoprolol y atorvastatina y añadiendo enalapril y furosemida. Se informó al paciente del riesgo anestésico-quirúrgico y se obtuvo el consentimiento informado.
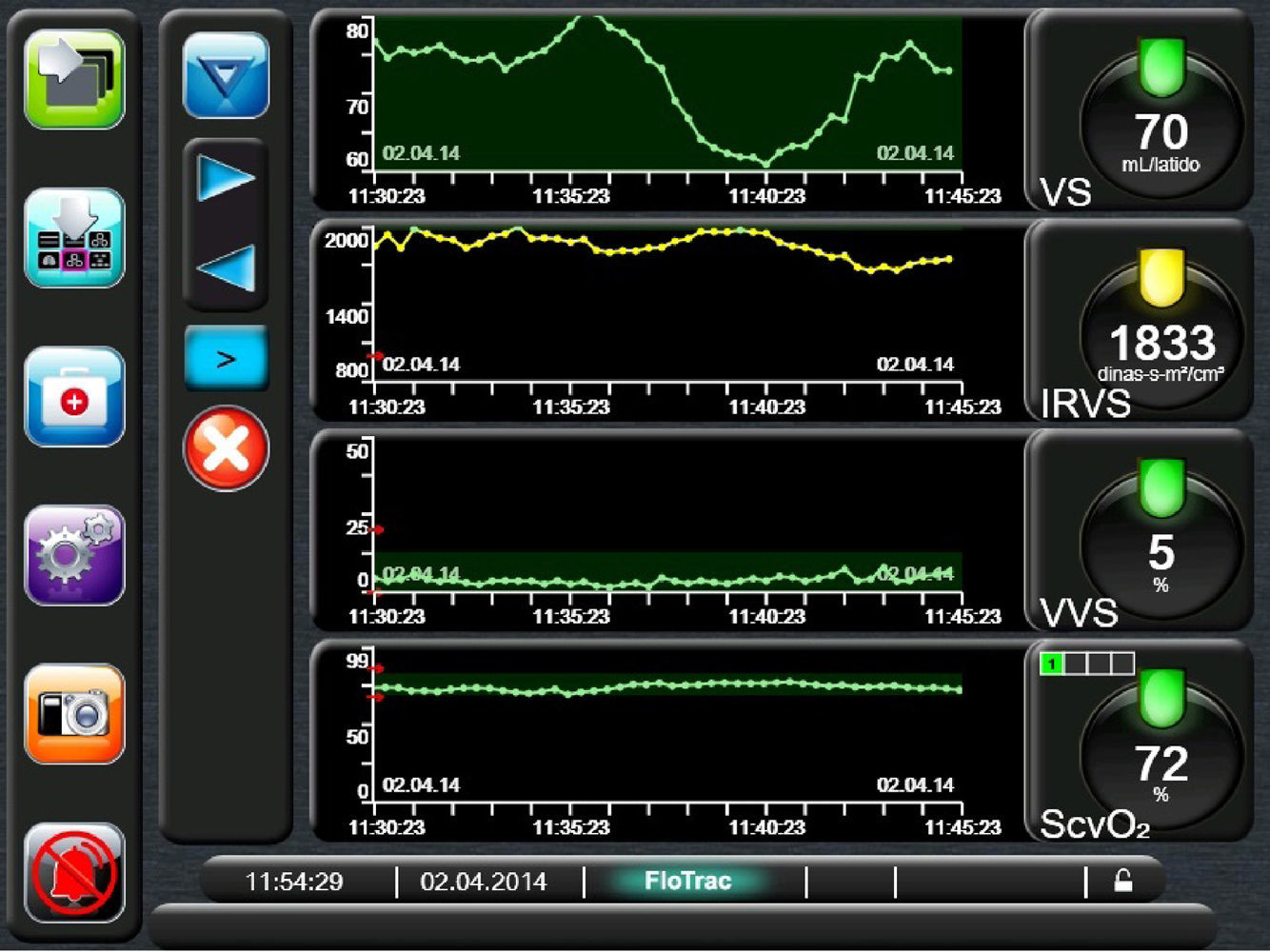
Premedicamos al paciente con lorazepam oral, salbutamol y budesonida inhalados y actocortina iv. En el quirófano se monitorizó con electrocardiografía de 5 derivaciones (II y V5) y registro continuo de profundidad anestésica. Se administró midazolam y se canalizó vía arterial radial izquierda para monitorización de presión arterial invasiva y gasto cardiaco. Realizamos raquianalgesia con aguja 25G Whitacre a nivel L2-L3 administrando morfina 200μg y lidocaína 18mg intratecales, posteriormente se indujo la anestesia con etomidato 12mg, midazolam 2mg, ketamina 40mg, fentanilo 100μg y rocuronio 50mg. Se mantuvo con sevofluorano, fentanilo y rocuronio; procedimos al registró de la diuresis horaria y a la inserción de catéter PreSep® para la monitorización de las variables hemodinámicas: gasto cardiaco, volumen sistólico (VS), variación del volumen sistólico (VVS), saturación venosa central de O2 (ScvO2), resistencias vasculares sistémicas a través de sistema Flo Trac/Vigileo (Edwards Lifesciences®) (fig. 1).
Monitorización hemodinámica mediante sistema Flo-Trac/Vigileo (Edwards Lifesciences®).Visualización de pantalla de quirófano de los parámetros hemodinámicos registrados; volumen sistólico (VS mL/latido), índice de resistencias vasculares sistémicas (dinas-s-m2/cm2), variación del volumen sistólico (VSS %) y saturación venosa central de oxígeno (ScvO2%).
Fuente: autores.
El paciente se mantuvo estable con IC 2,3 - 3 l/min/m2, VVS 2 - 7% y ScvO2 74-67%. Se practicó una laparotomía media cuya duración fue de 160min. Durante la extracción de la pieza quirúrgica estimamos 600ml de sangrado que repercutió en el VS (62ml/latido, previo 70) y aumento del 10% IRVS –sin descenso significativo de la presión arterial media– que se resolvió incrementando la fluiodoterapia y la transfusión de un concentrado de hematíes (fig. 1). La ScvO2 se mantuvo entre 76-72%. Tras la intervención el paciente se trasladó bajo ventilación mecánica a reanimación requisito para continuar la vigilancia hemodinámica con Vigileo®. En las primeras 24 h registramos 1.000 cc por el drenaje quirúrgico y trombocitopenia de 60.000 plaquetas, por lo que requirió una nueva transfusión de dos concentrados de hematíes y plaquetas. Durante las primeras h fue necesario mantener al paciente en ventilación controlada para poder utilizar la información del sistema Flo Trac® e iniciar perfusión de dobutamina (dosis decrecientes desde 12μg/kg/min) durante cuatro días para mantener la presión arterial media sin un incremento significativo de las RVS, que perjudicaría la insuficiencia aórtica. Al 9.° día postoperatorio fue dado de alta de cuidados críticos. Evolucionó favorablemente en hospitalización.
DiscusiónLa bibliografía demuestra que en octogenarios con estenosis aórtica severa la supervivencia de los pacientes sometidos a remplazo valvular mejora significativamente respecto a los que no se intervienen3–5. Sin embargo, según las recomendaciones preoperatorias de la Sociedad Europea de Cardiología2, en el paciente con estenosis aórtica severa asintomático no estaría justificado realizar la cirugía reparadora valvular previa a la cirugía oncológica si dicha cirugía está catalogada como de riesgo bajo-medio. En nuestro paciente la cirugía se catalogó de «moderado-alto» riesgo dada la posibilidad de sangrado; la edad y la comorbilidad del paciente apoyaron la decisión. Pero la válvula repuesta presentaba un alto grado de insuficiencia postoperatoria que sí repercutió clínicamente, presentando el paciente dos episodios de insuficiencia cardiaca. Se objetivó, previamente a la cirugía oncológica, una buena fracción de eyección (FEVI: 67%) a pesar de una IT moderada-severa por lo que se indicó no demorar más la resección tumoral. Por parte del servicio de cardiología, tal como aconsejan las guías en la insuficiencia aórtica, se reevaluó el tratamiento (en concreto se introdujo enalapril y se retiraron los betabloqueantes). El manejo anestésico tuvo en cuenta la labilidad hemodinámica que conlleva una valvulopatía6 y las potenciales alteraciones de la coagulación por lo que combinamos raquianalgesia con morfina intratecal y anestesia general, como proponen algunos autores7,8, ya que nos pareció una alternativa adecuada a la analgesia epidural (sin necesidad de utilizar un catéter postoperatorio) y proporcionó una gran estabilidad hemodinámica.
Utilizamos un dispositivo de monitorización hemodinámica continua mínimamente invasivo (Vigileo®), manteniendo cifras de SvO2 superiores a 70. Esto resultó de gran ayuda ante la toma de decisiones. Un corazón fisiológicamente normal puede ser insuficiente en el caso de que exista una gran demanda de O2 (estado hiperdinámico: sepsis, tirotoxicosis, cirugía, etc.), en el supuesto concreto de una válvula no funcionante, el exquisito control hemodinámico se hace indispensable2,6. El «gold standard» de la monitorización ha sido desde su instauración el catéter de Swan-Ganz en arteria pulmonar, sin embargo la relación coste/beneficio, el hecho de que no esté exento de riesgos y la difícil interpretación de los datos por personal no habituado a su uso hacen que su disponibilidad en un quirófano de cirugía no cardiaca sea baja. Los nuevos dispositivos de monitorización hemodinámica mínimamente invasivos de fácil manejo y gran utilidad clínica, resultan una pieza fundamental y es deseable que puedan estar a disposición de todos los hospitales. El impacto del uso de estos sistemas sobre la morbimortalidad es un campo actualmente en estudio9,10.
Concluimos que: la correcta evaluación, tratamiento y control hemodinámico del paciente cardiópata, en el perioperatorio, gracias a un abordaje multidisciplinar, juega un papel fundamental sobre el pronóstico. La toma de decisiones debe basarse en las directrices recogidas en las guías de las sociedades implicadas y el manejo hemodinámico sustentarse en un algoritmo cuyo objetivo sea garantizar el aporte de oxígeno tisular óptimo. La demora de 4 meses en realizar la hemicolectomía fue realmente tiempo de optimización activa y así se le explicó al paciente: a) cirugía cardiaca, b) ajuste farmacológico y c) quimioterapia.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.