El objetivo de este consenso es esclarecer el papel de los iDPP-4 en el manejo de los pacientes con diabetes durante la pandemia por COVID-19.
Material y métodosSe llevó a cabo una búsqueda bibliográfica en PubMed (diciembre 2019-febrero de 2021). Se empleó la metodología Oxford y se establecieron de forma consensuada posibles recomendaciones.
ResultadosLa diabetes parece ser un factor independiente en la enfermedad de COVID-19 (evidencia 2b). No se demuestra mayor riesgo de contagio con iDPP-4 (evidencia 2b), y su uso ha demostrado ser seguro (evidencia 2b). Los iDPP-4 pueden presentar un cierto beneficio en la reducción de la mortalidad, particularmente su uso intrahospitalario (evidencia 2a), reduciendo la admisión a unidades de cuidados intensivos (evidencia 2b) y la necesidad de ventilación mecánica (evidencia 2b).
ConclusionesLos iDPP-4 parecen ser fármacos seguros en pacientes con COVID-19, y se necesitan estudios de calidad que aclaren sus posibles ventajas.
This consensus aims to clarify the role of Dipeptidyl Peptidase-4 inhibitors (iDPP-4) in managing patients with diabetes during the COVID-19 pandemic.
Materials and methodsA PubMed bibliographic search was carried out (December 2019-February 2021). Oxford methodology was used for the evaluation of evidence and possible recommendations were established by consensus.
ResultsDiabetes appears to be an independent factor in COVID-19 disease (evidence 2b). No increased risk of contagion with iDPP-4 is demonstrated (evidence 2b), and its use has been shown to be safe (evidence 2b). The use of this drug may present a specific benefit in reducing mortality, particularly in in-hospital use (evidence 2a), reducing admission to intensive care units (evidence 2b) and the need for mechanical ventilation (evidence 2b).
ConclusionsThe use of iDPP-4 appears to be safe in patients with COVID-19, and quality studies are needed to clarify their possible advantages further.
El manejo del paciente con diabetes en la pandemia de COVID-19 es un aspecto que ha cobrado especial relevancia, ya que las personas con diabetes infectadas por SARS-CoV-2 han demostrado presentar un mayor riesgo de peor pronóstico y mortalidad1. La razón de la peor evolución de los pacientes con diabetes no está todavía del todo clara, pudiendo deberse a la respuesta inmune deteriorada frente al SARS-CoV-2 como resultado de la hiperglucemia crónica2 y/o a la inflamación crónica de bajo grado asociada a la diabetes3.
Algunos fármacos antidiabéticos (ADA), como los inhibidores de la dipeptidil-peptidasa-4 (iDPP-4), han suscitado un interés considerable ya que se ha sugerido que pueden desempeñar un papel en reducir el posible contagio del virus y mitigar la gravedad de las complicaciones asociadas con COVID-194.
El objetivo de este documento de revisión y consenso es resumir todos los datos disponibles sobre el impacto potencial de los iDPP-4 en los resultados clínicos de pacientes con diabetes durante la COVID-19, tanto en pacientes con diabetes atendidos en medio extrahospitalario como en aquellos que requirieron manejo intrahospitalario, y establecer recomendaciones basadas en la evidencia disponible hasta la fecha. Puede acceder al documento completo en el siguiente enlace véase el material adicional:
MetodologíaPara llevar a cabo este documento de revisión y consenso se convocó a varias sociedades científicas y a una fundación, relacionadas todas ellas con el manejo clínico de la diabetes (Sociedad Española de Medicina Interna, Sociedad Española de Diabetes, Sociedad Española de Endocrinología y Nutrición, y Fundación redGDPS).
Después de revisar y seleccionar la bibliografía, llevar a cabo el análisis pertinente de la evidencia disponible, y acordar las preguntas clínicas a plantearse, se establecieron de forma consensuada posibles recomendaciones.
Búsqueda bibliográficaSe llevó a cabo una búsqueda bibliográfica en la base de datos PubMed desde diciembre 2019 hasta febrero de 2021 según la estrategia de búsqueda especificada en la tabla 1.
Planteamiento de la estrategia de búsqueda (Mesh descriptors)
| •Búsqueda dirigida: Cruce del término Mesh (Dipeptidyl-Peptidase IV Inhibitors) y los términos Mesh (COVID-19) y (Sars-Cov2) |
| Ampliación de búsqueda con el término Mesh (Dipeptidyl-Peptidase IV Inhibitors) y (DPP4) en texto libre con los términos MesH (COVID) y (Sars Cov 2) |
| •Búsqueda ampliada: esta segunda búsqueda obtiene más número de artículos, pero menos específicos |
| Number Search terms |
| 1Mesh descriptor:(diabetes mellitus) explode all trees |
| 2((diabetes mellitus) or (diabetes) or (diabetic)):ti,ab,kw |
| 3Or 1–2 |
| 4Mesh descriptor:(coronavirus) explode all trees |
| 5((2019 novel coronavirus disease) or (COVID19) or (COVID-19 pandemic) or (COVID-19 virus disease) or (2019 novel coronavirus infection) or (coronavirus disease 2019) or (coronavirus disease-19) or (COVID-19 virus infection) or (coronavirus) or (coronavirus covid-19) or (corona virus)):ti,ab,kw |
| 6Or 4–5 |
| 7Mesh descriptor:(Dipeptidyl peptidase-4) explode all tres |
| 8((Dipeptidyl Peptidase IV Inhibitors) or (Inhibitors, Dipeptidyl-Peptidase IV) or (Gliptins) or (Dipeptidyl-Peptidase 4 Inhibitors) or (Dipeptidyl Peptidase 4 Inhibitors) or (CD26 Antigen) or (Antigen, CD26) or (Antigens, CD26) or (Adenosine Deaminase Complexing Protein 2) or (Dipeptidyl-Peptidase IV) or (Dipeptidyl Peptidase IV) or (CD26 Antigens)):ti,ab,kw |
| 9Or 7–8 |
| 103 and 6 and 9 |
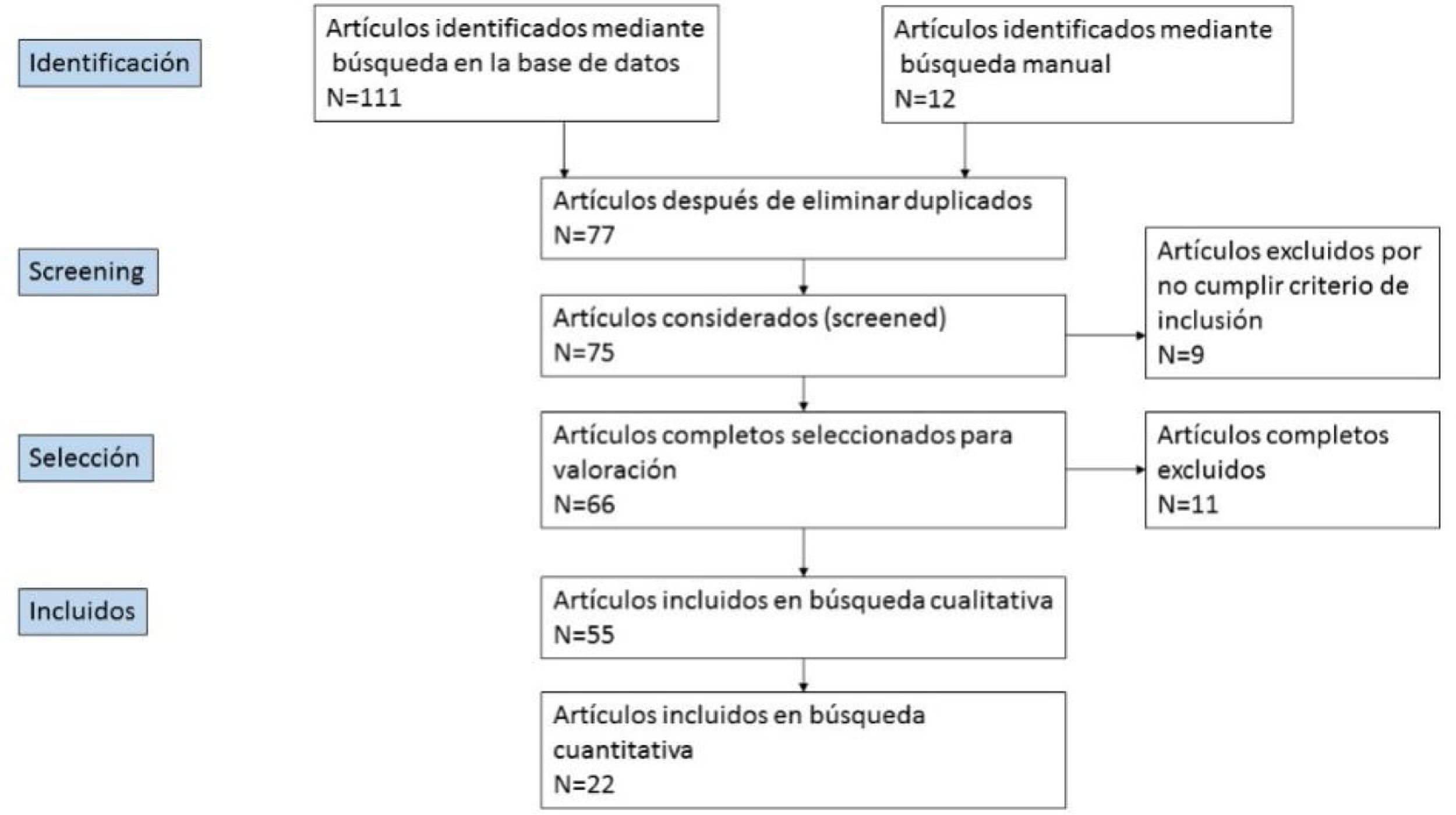
Los resultados se completaron con una segunda búsqueda manual. Los revisores llevaron a cabo de forma independiente la selección de la literatura, el análisis de datos, la evaluación de los temas más relevantes y el análisis de calidad. La figura 1 presenta el diagrama PRISMA de cómo se llevó a cabo el proceso de selección de los artículos. En función de esta revisión se establecieron las preguntas clínicas de interés.
Metodología OxfordLa calidad de los artículos seleccionados se valoró mediante el empleo de Oxford Centre for Evidence-Based Medicine (CEBM) Levels of Evidence (Oxford CEBM, 2009).
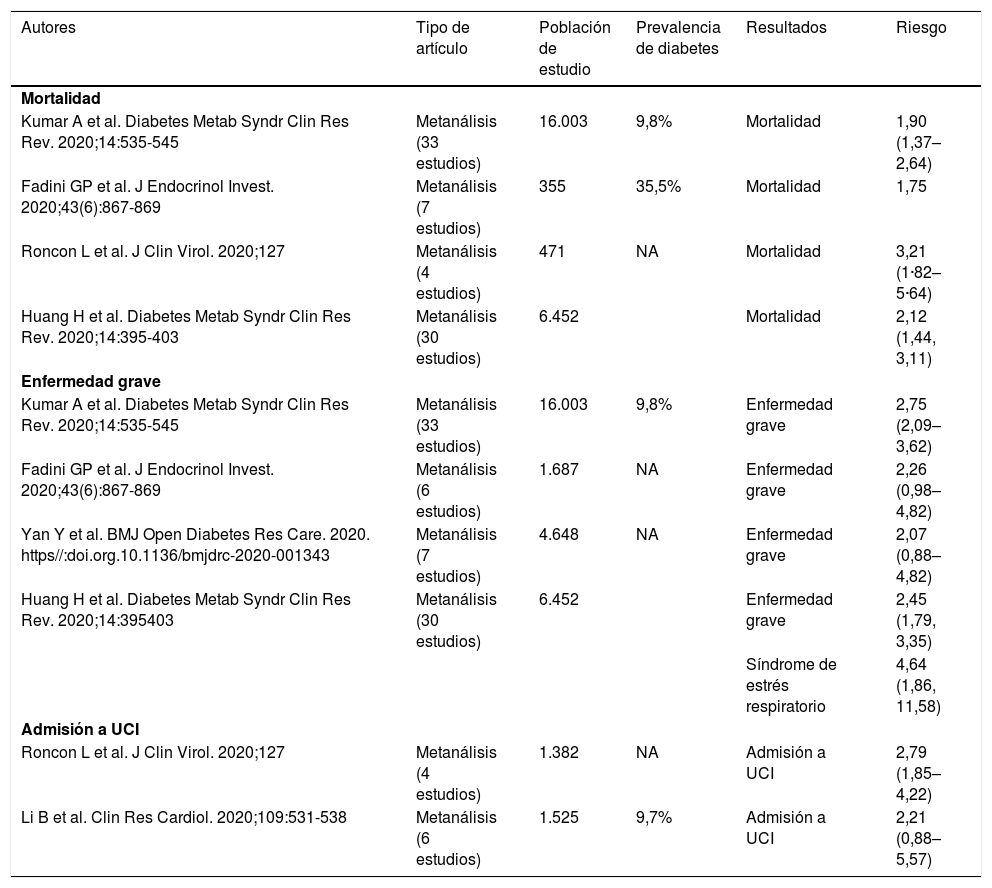
Resultados¿Puede considerarse la diabetes un factor de riesgo independiente en la evolución del paciente con SARS-CoV-2?Los datos publicados hasta la fecha señalan que la diabetes no parece aumentar el riesgo de infección por COVID-19, pero la presencia de diabetes en pacientes con COVID-19 es un factor de riesgo en lo que respecta a mortalidad, gravedad de la enfermedad y necesidad de ingreso en la unidad de cuidados intensivos (UCI)1(evidencia 2a) (tabla 2).
Resultados de la enfermedad de COVID-19 en función de la presencia de diabetes
| Autores | Tipo de artículo | Población de estudio | Prevalencia de diabetes | Resultados | Riesgo |
|---|---|---|---|---|---|
| Mortalidad | |||||
| Kumar A et al. Diabetes Metab Syndr Clin Res Rev. 2020;14:535-545 | Metanálisis (33 estudios) | 16.003 | 9,8% | Mortalidad | 1,90 (1,37–2,64) |
| Fadini GP et al. J Endocrinol Invest. 2020;43(6):867-869 | Metanálisis (7 estudios) | 355 | 35,5% | Mortalidad | 1,75 |
| Roncon L et al. J Clin Virol. 2020;127 | Metanálisis (4 estudios) | 471 | NA | Mortalidad | 3,21 (1·82–5·64) |
| Huang H et al. Diabetes Metab Syndr Clin Res Rev. 2020;14:395-403 | Metanálisis (30 estudios) | 6.452 | Mortalidad | 2,12 (1,44, 3,11) | |
| Enfermedad grave | |||||
| Kumar A et al. Diabetes Metab Syndr Clin Res Rev. 2020;14:535-545 | Metanálisis (33 estudios) | 16.003 | 9,8% | Enfermedad grave | 2,75 (2,09–3,62) |
| Fadini GP et al. J Endocrinol Invest. 2020;43(6):867-869 | Metanálisis (6 estudios) | 1.687 | NA | Enfermedad grave | 2,26 (0,98–4,82) |
| Yan Y et al. BMJ Open Diabetes Res Care. 2020. https//:doi.org.10.1136/bmjdrc-2020-001343 | Metanálisis (7 estudios) | 4.648 | NA | Enfermedad grave | 2,07 (0,88–4,82) |
| Huang H et al. Diabetes Metab Syndr Clin Res Rev. 2020;14:395403 | Metanálisis (30 estudios) | 6.452 | Enfermedad grave | 2,45 (1,79, 3,35) | |
| Síndrome de estrés respiratorio | 4,64 (1,86, 11,58) | ||||
| Admisión a UCI | |||||
| Roncon L et al. J Clin Virol. 2020;127 | Metanálisis (4 estudios) | 1.382 | NA | Admisión a UCI | 2,79 (1,85–4,22) |
| Li B et al. Clin Res Cardiol. 2020;109:531-538 | Metanálisis (6 estudios) | 1.525 | 9,7% | Admisión a UCI | 2,21 (0,88–5,57) |
UCI: Unidad de cuidados intensivos. NA = no aportado.
Adaptada de Apicella M et al1.
No está del todo claro si este aumento del riesgo se debe a la diabetes per se o a que los pacientes con diabetes suelen presentar mayor prevalencia de otros factores de riesgo implicados en un peor pronóstico por COVID-19. Se ha comprobado que los niveles circulantes de algunas citoquinas como la interleucina-6 (IL-6) son mayores en pacientes con COVID-19 y diabetes, presentando peor pronóstico que en pacientes sin diabetes, lo que sugiere que en presencia de un entorno proinflamatorio subyacente la diabetes sería un factor de riesgo independiente de peores resultados (evidencia 5)5. Consenso de expertos: Basándose en esto, en la diabetes, independientemente de un adecuado control de comorbilidades como la obesidad o la enfermedad cardiovascular, se recomendaría sensibilizar respecto a la importancia de un control óptimo de la glucemia, precaución en la discontinuación prematura de la terapia establecida y optimización de la terapia antidiabética valorando posibles implicaciones de los fármacos en la inflamación. En el paciente con diabetes y COVID-19, podrían ser factores a considerar la selección de fármacos que garanticen poca fluctuación en el control de la glucemia y hayan demostrado ser seguros en las distintas situaciones (prehospitalización, hospitalización, UCI).
Utilizando un enfoque de modelización, una publicación reciente demostró que el dominio S1 de la glucoproteína de espiga SARS-CoV-2 podría interactuar con la membrana humana DPP-4 permitiendo la entrada del virus6. Sin embargo, un registro llevado a cabo en Italia exploró la posible asociación entre los iDPP-4 para la diabetes y el riesgo de infección por COVID-19, y se concluyó que los iDPP-4 no parecen tener ningún efecto protector o perjudicial en la incidencia de COVID-197(evidencia 2b) constatando datos recientes sobre su papel neutro en la incidencia de infecciones respiratorias8. Consenso de expertos: Aunque existe una posible interacción entre el SARS-CoV-2 y la DPP-4, el uso de iDPP-4 no parece incrementar, pero tampoco reducir el riesgo de infección por SARS-CoV-2.
Un estudio de casos y controles constató que la tasa de exposición a iDPP-4 entre los pacientes con diabetes mellitus tipo 2 (DM2) infectados con SARS-CoV-2 hospitalizados por COVID-19 era superponible a la de los pacientes emparejados en la misma región o a los de la clínica ambulatoria local9. Estos datos sugieren que los iDPP-4 no aumentan el riesgo de hospitalización en pacientes con COVID-19, y se consideran una opción terapéutica válida para el manejo de pacientes con diabetes y COVID-19 sintomático (evidencia 4). Consenso de expertos: Con los datos existentes en la actualidad los iDPP-4 no aumentan el riesgo de hospitalización en pacientes con COVID-19. Por ello, se sugiere mantener el tratamiento con iDPP-4 en caso de situaciones epidemiológicas de alto o muy alto riesgo y en caso de enfermedad COVID-19 leve o moderada sin necesidad de hospitalización.
Los iDPP-4 presentan efectos antiadipogénicos, antiagregantes y antinflamatorios. Los estudios han demostrado que la iniciación de los iDPP-4 da lugar a la reducción de la producción de citoquinas y un metaanálisis reciente señala, así mismo, una reducción significativa en los niveles de la reacción en cadena de la polimerasa (PCR) después de la terapia con iDPP-4 en comparación con placebo10. Consenso de expertos: Los efectos antinflamatorios, antiagregantes y antiadipogénicos de los iDPP-4, así como la posible modulación de los receptores DPP4 en la entrada del virus, son mecanismos fisiológicos potenciales que podrían interactuar en un desarrollo más favorable de la enfermedad por COVID-19.
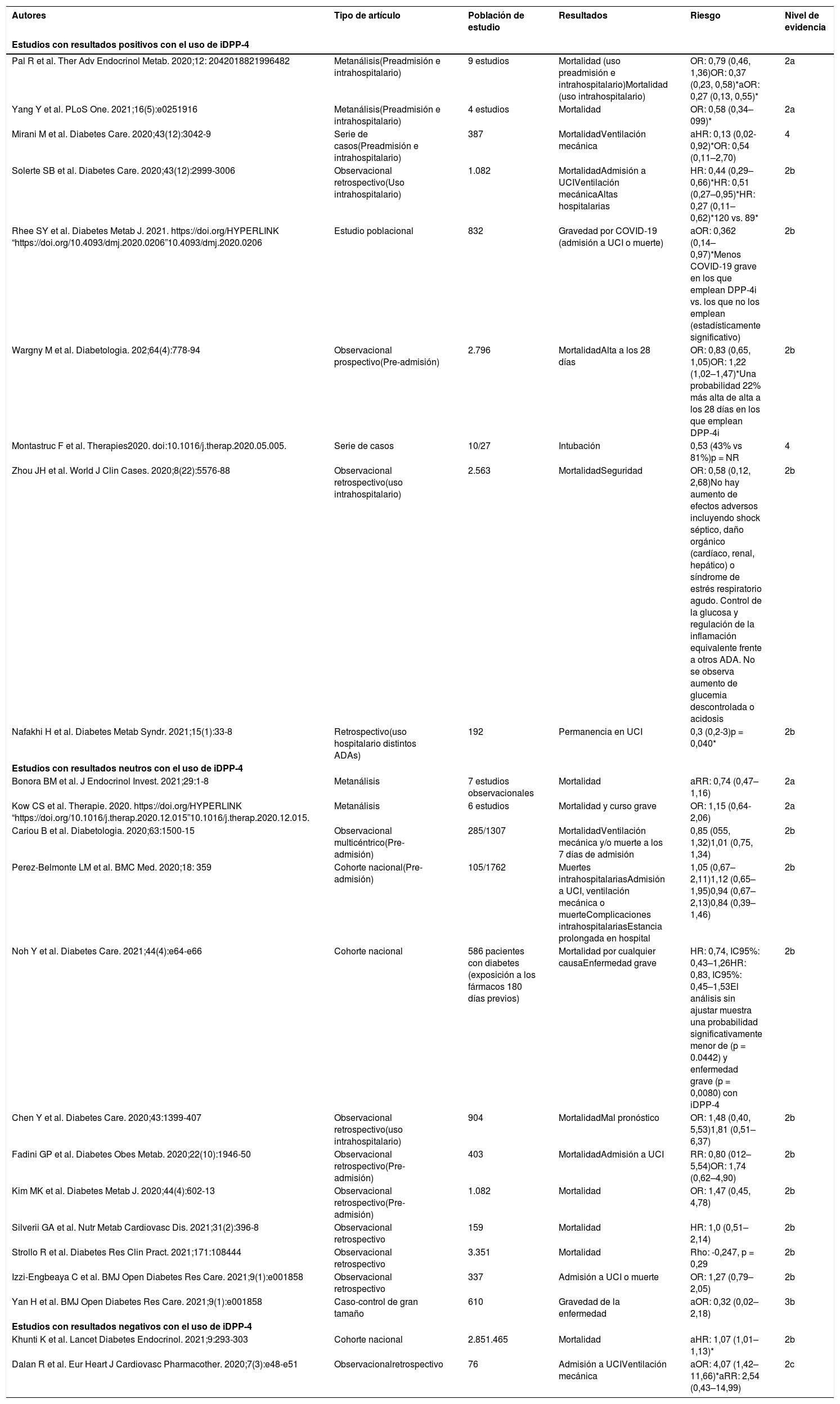
Los resultados de la valoración de los estudios indican un efecto beneficioso o neutro de este grupo de ADA (evidencia 2a). Cuatro metaanálisis señalan un efecto beneficioso o neutro de los iDPP-4 sobre la mortalidad. Un estudio de cohortes señala un pequeño (1,07 [1,01-1,13]), pero significativo aumento de la mortalidad, que puede explicarse por el gran tamaño muestral y un probable sesgo de selección al prescribirse preferentemente a pacientes mayores y frágiles (tabla 3).
Resultados de los estudios con iDPP-4 en pacientes con COVID-19
| Autores | Tipo de artículo | Población de estudio | Resultados | Riesgo | Nivel de evidencia |
|---|---|---|---|---|---|
| Estudios con resultados positivos con el uso de iDPP-4 | |||||
| Pal R et al. Ther Adv Endocrinol Metab. 2020;12: 2042018821996482 | Metanálisis(Preadmisión e intrahospitalario) | 9 estudios | Mortalidad (uso preadmisión e intrahospitalario)Mortalidad (uso intrahospitalario) | OR: 0,79 (0,46, 1,36)OR: 0,37 (0,23, 0,58)*aOR: 0,27 (0,13, 0,55)* | 2a |
| Yang Y et al. PLoS One. 2021;16(5):e0251916 | Metanálisis(Preadmisión e intrahospitalario) | 4 estudios | Mortalidad | OR: 0,58 (0,34–099)* | 2a |
| Mirani M et al. Diabetes Care. 2020;43(12):3042-9 | Serie de casos(Preadmisión e intrahospitalario) | 387 | MortalidadVentilación mecánica | aHR: 0,13 (0,02-0,92)*OR: 0,54 (0,11–2,70) | 4 |
| Solerte SB et al. Diabetes Care. 2020;43(12):2999-3006 | Observacional retrospectivo(Uso intrahospitalario) | 1.082 | MortalidadAdmisión a UCIVentilación mecánicaAltas hospitalarias | HR: 0,44 (0,29–0,66)*HR: 0,51 (0,27–0,95)*HR: 0,27 (0,11–0,62)*120 vs. 89* | 2b |
| Rhee SY et al. Diabetes Metab J. 2021. https://doi.org/HYPERLINK “https://doi.org/10.4093/dmj.2020.0206”10.4093/dmj.2020.0206 | Estudio poblacional | 832 | Gravedad por COVID-19 (admisión a UCI o muerte) | aOR: 0,362 (0,14–0,97)*Menos COVID-19 grave en los que emplean DPP-4i vs. los que no los emplean (estadísticamente significativo) | 2b |
| Wargny M et al. Diabetologia. 202;64(4):778-94 | Observacional prospectivo(Pre-admisión) | 2.796 | MortalidadAlta a los 28 días | OR: 0,83 (0,65, 1,05)OR: 1,22 (1,02–1,47)*Una probabilidad 22% más alta de alta a los 28 días en los que emplean DPP-4i | 2b |
| Montastruc F et al. Therapies2020. doi:10.1016/j.therap.2020.05.005. | Serie de casos | 10/27 | Intubación | 0,53 (43% vs 81%)p = NR | 4 |
| Zhou JH et al. World J Clin Cases. 2020;8(22):5576-88 | Observacional retrospectivo(uso intrahospitalario) | 2.563 | MortalidadSeguridad | OR: 0,58 (0,12, 2,68)No hay aumento de efectos adversos incluyendo shock séptico, daño orgánico (cardíaco, renal, hepático) o síndrome de estrés respiratorio agudo. Control de la glucosa y regulación de la inflamación equivalente frente a otros ADA. No se observa aumento de glucemia descontrolada o acidosis | 2b |
| Nafakhi H et al. Diabetes Metab Syndr. 2021;15(1):33-8 | Retrospectivo(uso hospitalario distintos ADAs) | 192 | Permanencia en UCI | 0,3 (0,2-3)p = 0,040* | 2b |
| Estudios con resultados neutros con el uso de iDPP-4 | |||||
| Bonora BM et al. J Endocrinol Invest. 2021;29:1-8 | Metanálisis | 7 estudios observacionales | Mortalidad | aRR: 0,74 (0,47–1,16) | 2a |
| Kow CS et al. Therapie. 2020. https://doi.org/HYPERLINK “https://doi.org/10.1016/j.therap.2020.12.015”10.1016/j.therap.2020.12.015. | Metanálisis | 6 estudios | Mortalidad y curso grave | OR: 1,15 (0,64-2,06) | 2a |
| Cariou B et al. Diabetologia. 2020;63:1500-15 | Observacional multicéntrico(Pre-admisión) | 285/1307 | MortalidadVentilación mecánica y/o muerte a los 7 días de admisión | 0,85 (055, 1,32)1,01 (0,75, 1,34) | 2b |
| Perez-Belmonte LM et al. BMC Med. 2020;18: 359 | Cohorte nacional(Pre-admisión) | 105/1762 | Muertes intrahospitalariasAdmisión a UCI, ventilación mecánica o muerteComplicaciones intrahospitalariasEstancia prolongada en hospital | 1,05 (0,67–2,11)1,12 (0,65–1,95)0,94 (0,67–2,13)0,84 (0,39–1,46) | 2b |
| Noh Y et al. Diabetes Care. 2021;44(4):e64-e66 | Cohorte nacional | 586 pacientes con diabetes (exposición a los fármacos 180 días previos) | Mortalidad por cualquier causaEnfermedad grave | HR: 0,74, IC95%: 0,43–1,26HR: 0,83, IC95%: 0,45–1,53El análisis sin ajustar muestra una probabilidad significativamente menor de (p = 0.0442) y enfermedad grave (p = 0,0080) con iDPP-4 | 2b |
| Chen Y et al. Diabetes Care. 2020;43:1399-407 | Observacional retrospectivo(uso intrahospitalario) | 904 | MortalidadMal pronóstico | OR: 1,48 (0,40, 5,53)1,81 (0,51–6,37) | 2b |
| Fadini GP et al. Diabetes Obes Metab. 2020;22(10):1946-50 | Observacional retrospectivo(Pre-admisión) | 403 | MortalidadAdmisión a UCI | RR: 0,80 (012–5,54)OR: 1,74 (0,62–4,90) | 2b |
| Kim MK et al. Diabetes Metab J. 2020;44(4):602-13 | Observacional retrospectivo(Pre-admisión) | 1.082 | Mortalidad | OR: 1,47 (0,45, 4,78) | 2b |
| Silverii GA et al. Nutr Metab Cardiovasc Dis. 2021;31(2):396-8 | Observacional retrospectivo | 159 | Mortalidad | HR: 1,0 (0,51–2,14) | 2b |
| Strollo R et al. Diabetes Res Clin Pract. 2021;171:108444 | Observacional retrospectivo | 3.351 | Mortalidad | Rho: -0,247, p = 0,29 | 2b |
| Izzi-Engbeaya C et al. BMJ Open Diabetes Res Care. 2021;9(1):e001858 | Observacional retrospectivo | 337 | Admisión a UCI o muerte | OR: 1,27 (0,79–2,05) | 2b |
| Yan H et al. BMJ Open Diabetes Res Care. 2021;9(1):e001858 | Caso-control de gran tamaño | 610 | Gravedad de la enfermedad | aOR: 0,32 (0,02–2,18) | 3b |
| Estudios con resultados negativos con el uso de iDPP-4 | |||||
| Khunti K et al. Lancet Diabetes Endocrinol. 2021;9:293-303 | Cohorte nacional | 2.851.465 | Mortalidad | aHR: 1,07 (1,01–1,13)* | 2b |
| Dalan R et al. Eur Heart J Cardiovasc Pharmacother. 2020;7(3):e48-e51 | Observacionalretrospectivo | 76 | Admisión a UCIVentilación mecánica | aOR: 4,07 (1,42–11,66)*aRR: 2,54 (0,43–14,99) | 2c |
*p < 0,05; ADA: fármacos antidiabéticos; HR: hazard ratio; aHR; hazard ratio ajustada; NR: no reportado; OR: odds ratio; aOR: odds ratio ajustada; RR: riesgo relativo; UCI: unidad de cuidados intensivos.
El posible efecto de estos fármacos podría ser más evidente en pacientes hospitalizados, tal y como refleja el metaanálisis de Pal et al.11, que identificaron 9 estudios observacionales de alta calidad con información de 7.008 pacientes con diabetes afectados de COVID-19. En el análisis de subgrupos, los autores observaron que el uso intrahospitalario de iDPP-4 se asociaba con una reducción de la mortalidad (OR ajustada: 0,27; IC 95%: 0,13-0,55; p=0,0003).
Dado el posible impacto positivo del uso de los iDPP-4, particularmente en pacientes hospitalizados, se han puesto en marcha varios estudios aleatorizados para aclarar este aspecto (NCT04365517, NCT04341935 y NCT04371978). Consenso de expertos: El uso extrahospitalario de iDPP-4 ha demostrado no aumentar el riesgo de mortalidad en pacientes con diabetes y COVID-19. El uso intrahospitalario de iDPP-4 podría estar asociado con una reducción significativa de la mortalidad en pacientes con diabetes y COVID-19. Por lo tanto, sería prudente iniciar o continuar con los iDPP-4 en pacientes con COVID-19 si no estuviese contraindicado.
El metaanálisis de Kow et al. demuestra que no hay un aumento del riesgo de mayor gravedad (evidencia 2a)12. Otra evidencia de que los iDPP-4 no aumentan la gravedad de los pacientes se mostró en el estudio Coronavirus Disease and Diabetes Outcome (CORONADO). En este estudio no se observó ninguna asociación entre un curso grave de COVID-19 y el tratamiento con iDPP-4 antes del ingreso (OR: 1,01; IC 95%: 0,75-1,34).
El uso de estos fármacos en el momento de la hospitalización, sin embargo, parece reducir significativamente la necesidad de ventilación mecánica (HR: 0,27 [0,11-0,62]), la admisión a la UCI (HR: 0,51 [0,27-0,95]) y aumenta el número de pacientes que reciben el alta a los 30 días según un estudio retrospectivo multicéntrico llevado a cabo en 338 pacientes con DM2 y COVID-19 (evidencia 2b)13. Consenso de expertos: El tratamiento con iDPP-4 en pacientes hospitalizados estables parece ser una opción de tratamiento segura que no incide sobre la evolución en la gravedad de la enfermedad.
Algunas revisiones y guías recientes13 señalan que los iDPP-4 son muy seguros, y que incluso pueden ser potencialmente beneficiosos para la mayoría de los pacientes hospitalizados con diabetes y COVID-19.
Los iDPP-4 han demostrado ser fármacos seguros, y además no necesitan ajustes en los días de enfermedad en el paciente con diabetes y COVID-19 en comparación con otros fármacos ADA (tabla 4)14. Aunque solo un ensayo aleatorizado puede responder definitivamente a esta pregunta, basándonos en estudios moleculares, fisiopatológicos y retrospectivos, el uso de los iDPP-4 es seguro y ciertamente beneficioso en el control metabólico. Consenso de expertos: Estos datos respaldan la seguridad de los iDPP-4 para el control de la diabetes durante la pandemia de COVID-19. Los iDPP-4 son un grupo de fármacos asociados a muchas ventajas, incluso en casos graves de COVID-19, porque son bien tolerados, tienen un bajo riesgo de hipoglucemia y pueden usarse, con ajuste de dosis si es pertinente, en situaciones de función renal deteriorada. En este sentido, se podría considerar el uso de los iDPP-4 incluso en pacientes hospitalizados con diabetes y COVID-19.
Recomendaciones con los distintos fármacos antidiabéticos en pacientes con sospecha de COVID-19
| Panel: Consideración de los posibles efectos de interferencia metabólica de los fármacos antidiabéticos en pacientes con diabetes tipo 2 y con sospecha de COVID-19 o confirmado |
|---|
| Metformina |
| • Ante un proceso agudo, como otros aumenta el riesgo de deshidratación y acidosis láctica, por lo que se recomienda la suspensión del medicamento y seguir las recomendaciones para los días de enfermedad |
| Inhibidores del cotransportador sodio-glucosa tipo 2 |
| • Incluyen canagliflozina, dapagliflozina, empagliflozina y ertugliflozina |
| • En la fase aguda existe riesgo de deshidratación y cetoacidosis diabética durante la enfermedad, por lo que los pacientes deben suspender los medicamentos y seguir las recomendaciones para los días de enfermedad, a excepción de dapagliflozina que parece ser, según datos del DARE-19, un fármaco seguro en paciente monitorizado hospitalizado |
| • Los pacientes deben evitar iniciar el tratamiento durante la enfermedad respiratoria |
| Agonistas del receptor del péptido-1 similar al glucagón |
| • Incluyen dulaglutida, exenatida, liraglutida, lixisenatida y semaglutida |
| • Las molestias digestivas pueden ocasionar deshidratación y conducir a enfermedad grave, por lo que los pacientes deben ser monitorizados de cerca |
| • Se debe fomentar la ingesta adecuada de líquidos y las comidas regulares |
| Inhibidores de la dipeptidil peptidasa-4 |
| • Incluyen alogliptina, linagliptina, saxagliptina, sitagliptina y vildagliptina |
| • Estos fármacos son generalmente bien tolerados y pueden continuarse |
| Insulina |
| • El tratamiento con insulina no debe interrumpirse |
| • Se debe fomentar el autocontrol regular de la glucosa en sangre cada 2-4h, o la monitorización continua de la glucosa |
| • Ajustar cuidadosamente la terapia regular si es apropiado para alcanzar los objetivos terapéuticos de acuerdo con el tipo de diabetes, las comorbilidades y el estado de salud |
| • Los modelos de salud en red y la telemedicina deben utilizarse para continuar las revisiones periódicas y los programas de educación sobre la autogestión de manera virtual y garantizar que los pacientes se adhieran a la terapia |
Fuente: adaptada de Bornstein SR et al.14
En pacientes con COVID-19, se ha sugerido la hipótesis de que debido a su efecto antiinflamatorio podría ayudar a prevenir las complicaciones asociadas al COVID-1915. Actualmente se están desarrollando estudios como el estudio SIDIACO Sitagliptin (NCT04365517) que permitirá esclarecer las posibles ventajas de estos fármacos en pacientes con estas patologías de base. Consenso de expertos: Los pacientes con diabetes y COVID-19 podrían beneficiarse hipotéticamente del empleo de iDPP-4 en presencia de enfermedad cardiovascular adicional o enfermedad renal crónica.
Los iDPP-4 han demostrado ser fármacos seguros y no necesitan ajustes en los días de enfermedad en el paciente con diabetes y COVID-19 en comparación con otros ADA orales16; su uso en comparación con otros ADA orales se ha relacionado con un menor tiempo de estancia en la UCI (evidencia 2b) y posibles beneficios en el paciente intrahospitalario. Consenso de expertos: Sobre la base de los estudios publicados hasta la fecha, podría considerarse que los iDPP-4 presentan un perfil adecuado para el tratamiento de la diabetes en pacientes hospitalizados.
Los iDPP-4 son un grupo de fármacos asociados a muchas ventajas en el contexto de la pandemia de COVID-19, incluso en casos graves, porque son bien tolerados, tienen un bajo riesgo de hipoglucemia, no necesitan de ajuste de dosis en días de enfermedad y pueden usarse en pacientes con la función renal deteriorada.
Después de valorar toda la bibliografía aportada no hay evidencia de calidad suficiente como para recomendar de forma concluyente el tratamiento con iDPP-4 en pacientes con diabetes y COVID-19. Sin embargo, tampoco las hay para desaconsejar su uso.
Por otro lado, la bibliografía revisada plantea hipótesis que apuntan a beneficios potencialmente sustanciales del tratamiento con iDPP-4 que esperamos sean resueltos con la mayor brevedad en los ensayos clínicos aleatorizados, prospectivos y de alta calidad puestos en marcha.
AutoríasTodos los autores han contribuido por igual a la elaboración del artículo.
FinanciaciónLa asistencia en la redacción médica ha sido financiada por el Grupo Menarini. No obstante, ninguno de sus miembros ha asistido a las reuniones realizadas para revisar bibliografía y consensuar decisiones, y tampoco ha influido en las decisiones que los expertos han tomado.
Conflicto de interesesFrancisco Javier Carrasco-Sánchez: consultor y/o asesor para Boehringer-Lilly, Novo Nordisk, Sanofi, AstraZeneca, MSD y Mundipharma. Trabajos remunerados para AstraZeneca, Boehringer-Lilly, Novartis, Novo-Nordisk y Sanofi.
Enrique Carretero-Anibarro: investigador, ponente y/o consultor para Almirall, AstraZeneca, Boehringer-Ingelheim, Eli Lilly, Esteve, Janssen, Menarini, MSD, Mundipharma, Novartis, Novo Nordisk y Sanofi Diabetes.
Manuel Ángel Gargallo: ponente y/o consultor para Sanofi Diabetes, Mundipharma, Novo Nordisk, Lilly y AstraZeneca.
Ricardo Gómez-Huelgas: consultor y/o asesor para Boehringer-Lilly, Novo Nordisk, Sanofi, AstraZeneca, MSD y Janssen. Trabajos remunerados para AstraZeneca, Boehringer-Lilly, Novartis, Novo-Nordisk y Sanofi. Estudios de investigación para Boehringer-Lilly, Novo-Nordisk, Sanofi y Janssen.
Juan Francisco Merino-Torres: investigador, ponente y/o consultor para Abbott, Amgen, AstraZeneca, Ascensia Diabetes Care, Bristol-Myers Squibb, Esteve, Glaxo-Smith-Kline, Janssen, Kabi-Fresenius, Lilly, Menarini, Merck-Sharp-Dohme, Novartis, Novo-Nordisk, Nutricia, Pfizer, Rovi y Sanofi-Aventis.
Domingo Orozco-Beltrán: participación en actividades formativas patrocinadas de forma no condicionada por MSD, Lilly, Novo Nordisk, Boehringer y Fundación Bamberg, así como en otras patrocinadas por sociedades científicas.
Pedro José Pines Corrales: ponente y/o consultor para AstraZeneca, Boehringer-Ingelheim, Eli Lilly, Menarini, MSD, Novo Nordisk y Sanofi Diabetes.
Manuel Antonio Ruiz Quintero: ponente para Sanofi/Aventis, GSK, Novartis, Novo Nordisk, Lilly, Boehringer Ingelheim, Almirall, Janssen, Mundifarma, AstraZeneca y Servier, y consultor/ponente para MSD y Esteve.
Los autores agradecen a Ana Isabel Ortega en nombre de Springer Healthcare la búsqueda bibliográfica y su clasificación, así como la asistencia en la elaboración del manuscrito. También agradecen a M. Ángeles Caldeiro, de Springer Healthcare, la coordinación en todas las fases del proyecto. Esta asistencia ha sido financiada por el Grupo Menarini.