El linfoma del manto (LM) es un linfoma no Hodgkin, muy agresivo, que comúnmente involucra el tracto gastrointestinal (TGI), pero rara vez se presenta como un linfoma gastrointestinal primario colónico1,2. Cuando lo hace, ha sido descrito como una poliposis múltiple linfomatosa (PML) y conlleva mal pronóstico. Reportamos el caso de una paciente adulta, joven, portadora de un LM primario colónico, con una presentación clínica larvada y un patrón endoscópico inusual.
Mantle cell lymphoma is a very aggressive non-Hodgkin lymphoma that commonly involves the gastrointestinal tract, but rarely presents as primary gastrointestinal colonic lymphoma. When it does, it has been described as multiple lymphomatous polyposis and has a very poor prognosis. We report the case of a young woman with primary colonic MCL with a latent clinical course and a rare endoscopic presentation.
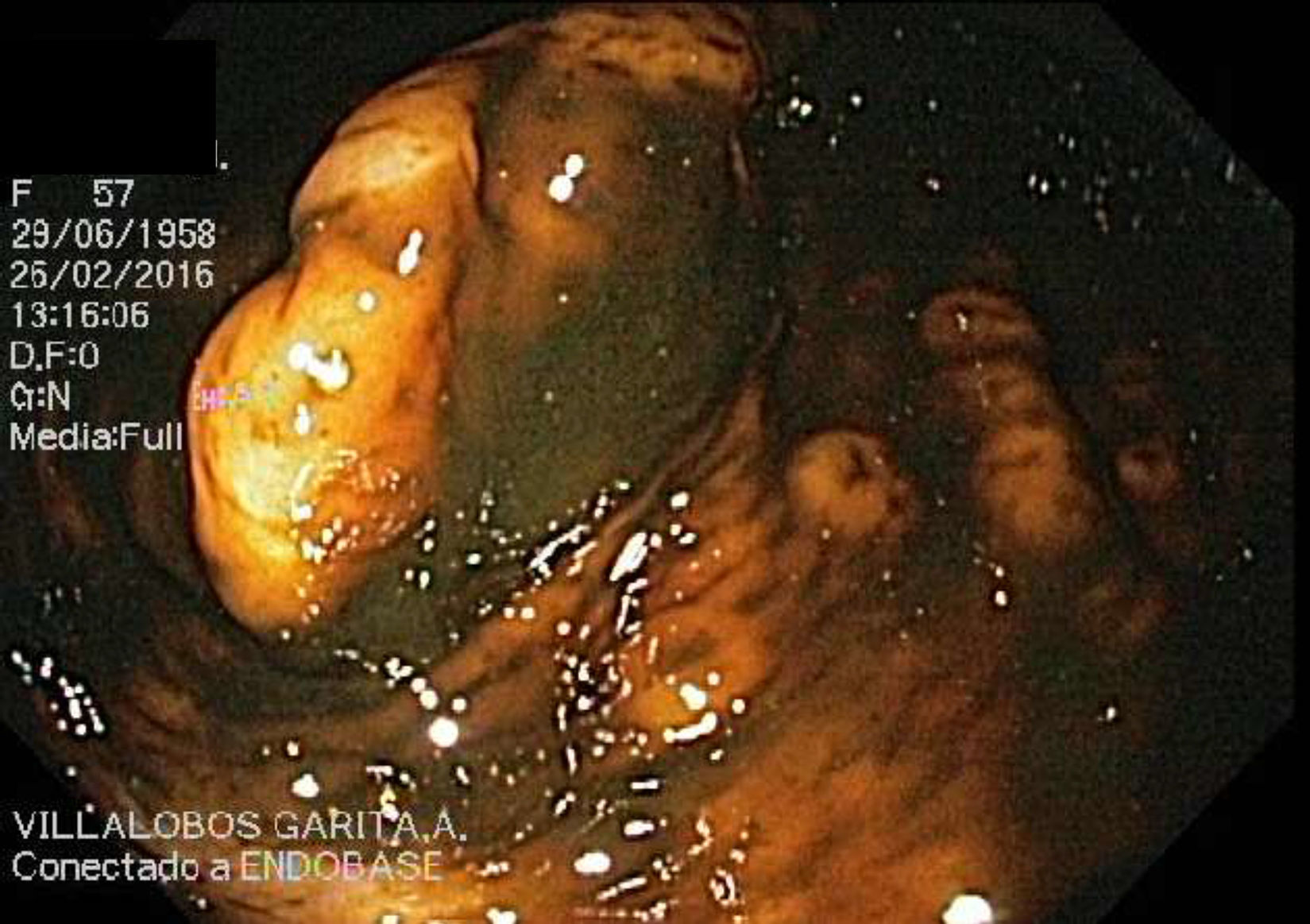
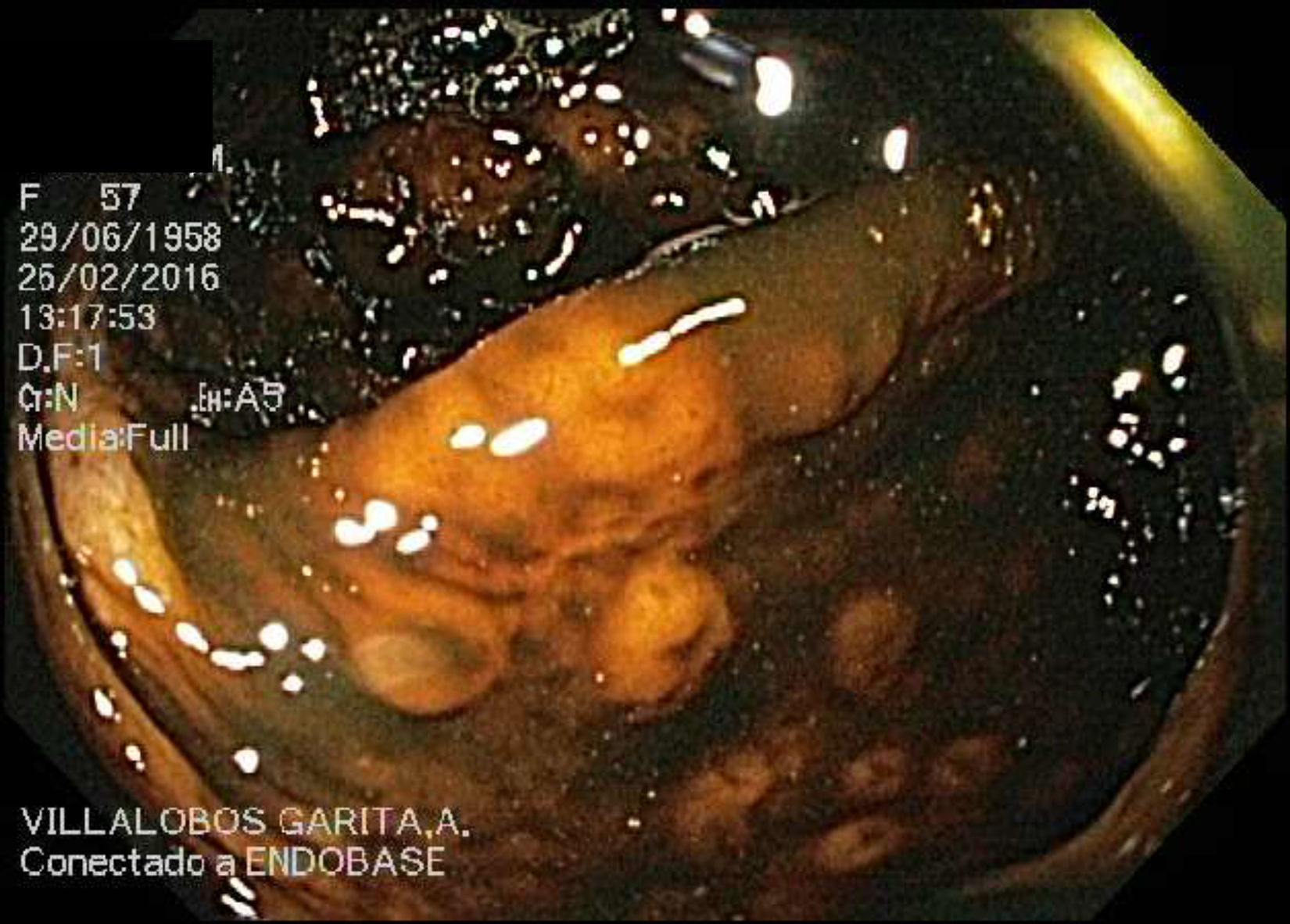
El linfoma del manto (LM) gastrointestinal primario es conocido por ser infrecuente e incurable, con cortos períodos de remisión y frecuentes recaídas1. Tiende a presentarse agresivamente en varones, con edad promedio de 60 años, y afecta el tracto gastrointestinal inferior hasta en un 88% de los casos2. La presentación endoscópica colónica más frecuente es la poliposis múltiple linfomatosa (PML)3. Presentamos el caso de una paciente adulta, joven, portadora de un LM primario colónico, con una presentación clínica y un patrón endoscópico inusual (figs. 1-5).
Mujer de 54 años con antecedentes personales patológicos (APP) de fibromialgia, quien consulta en el 2010 por dolor crónico en fosa ilíaca derecha. Los laboratorios generales, el ultrasonido y la tomografía axial computarizada (TAC) abdominal no reportaron anomalías. La gastroscopia evidenció una gastritis erosiva leve, y la colonoscopía un patrón micronodular inespecífico de la mucosa colónica derecha, semejante a la hiperplasia linfoide gástrica. El reporte histológico reportó una lámina propia edematosa y congestiva, con agregados linfoides y una población inflamatoria adecuada, con relación a la hiperplasia linfoide colónica. Se diagnosticó de síndrome de intestino irritable.
En el 2012, ante la persistencia sintomática se repite el ultrasonido abdominal, el cual estaba normal. Una nueva colonoscopía presentó el mismo patrón nodular sugestivo de hiperplasia linfoide con el reporte histológico de hiperplasia linfoide en ciego, íleon y recto. Se continuó manejo sintomático. Un ultrasonido de control en el 2014 no mostró alteraciones, por lo que fue referida a la clínica del dolor.
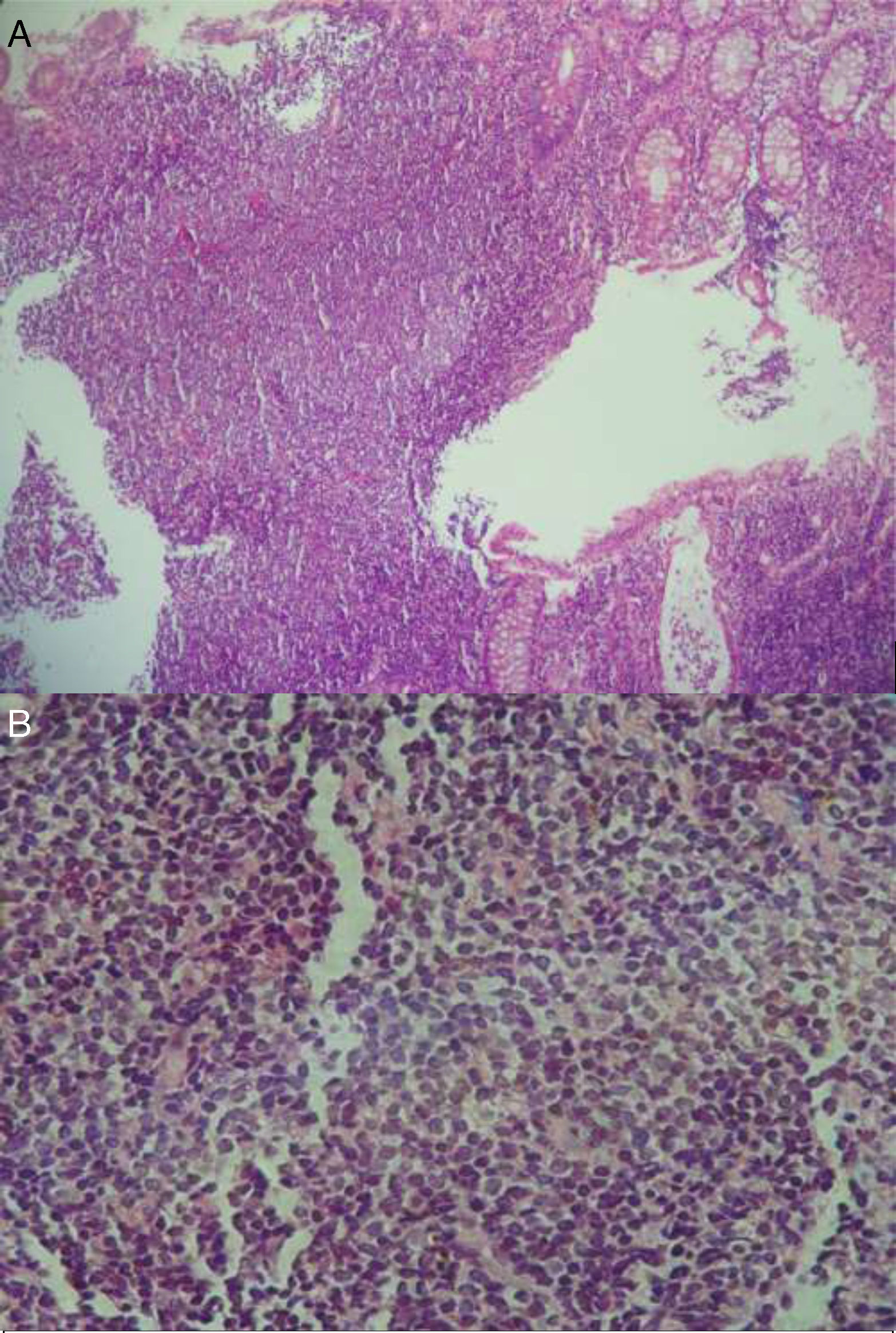
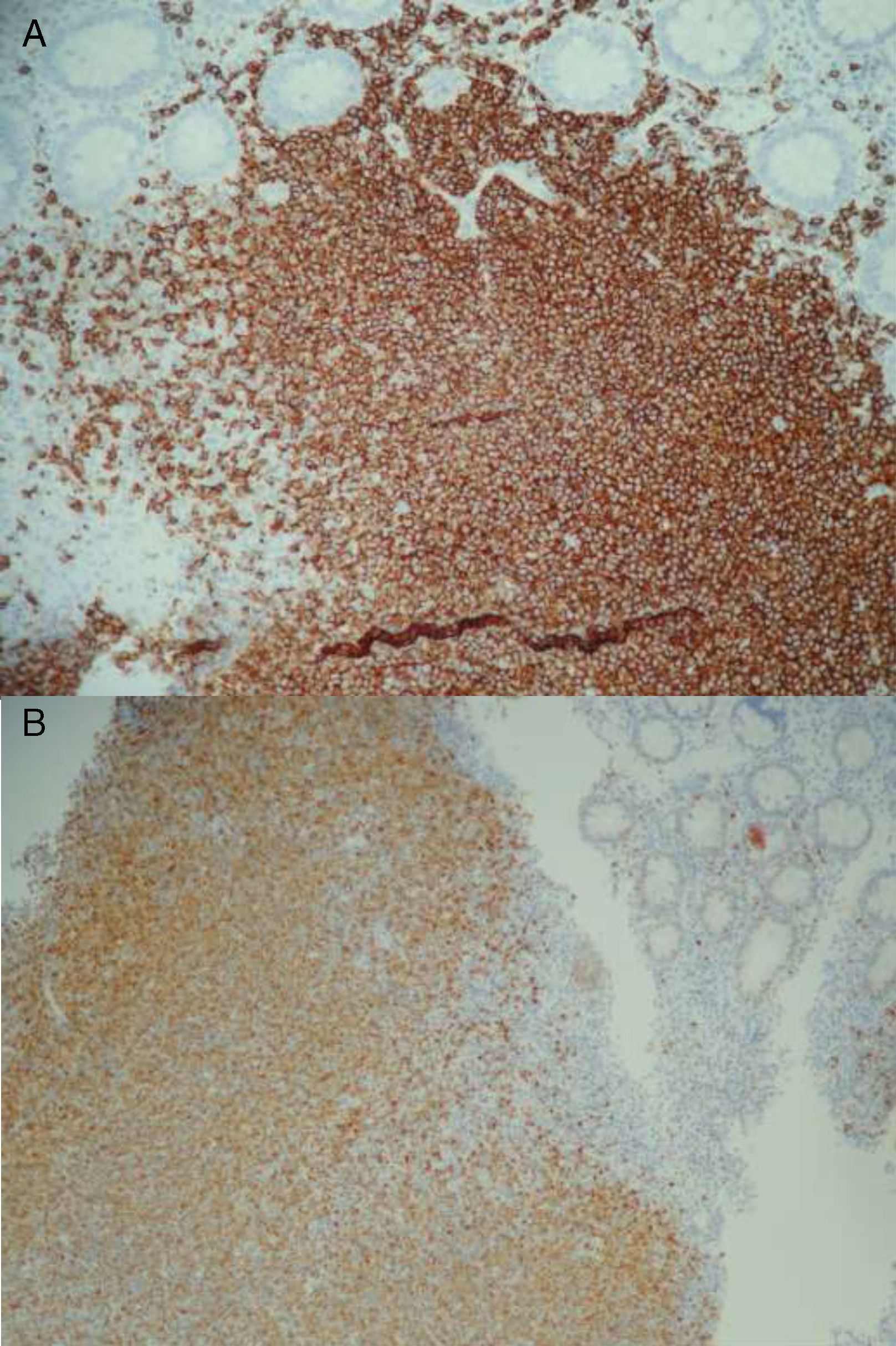
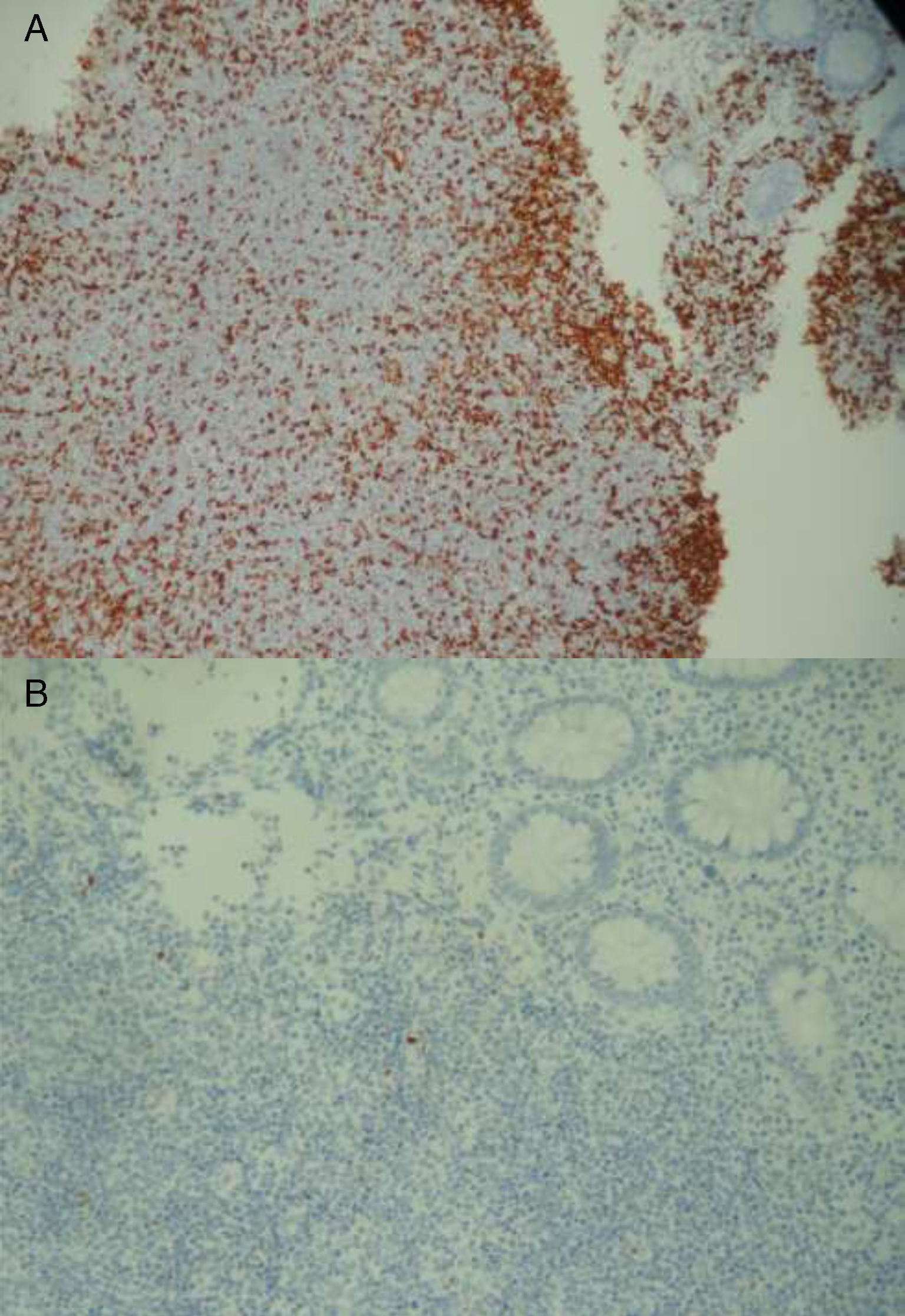
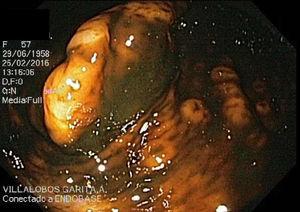
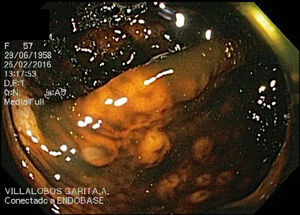
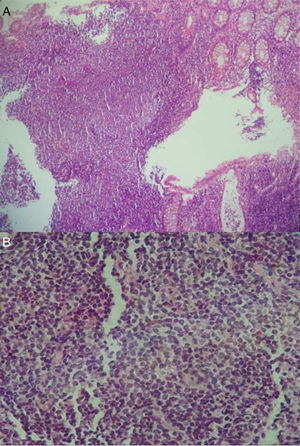
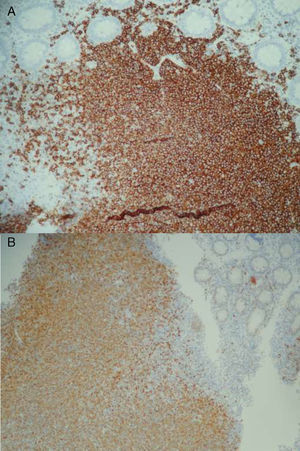
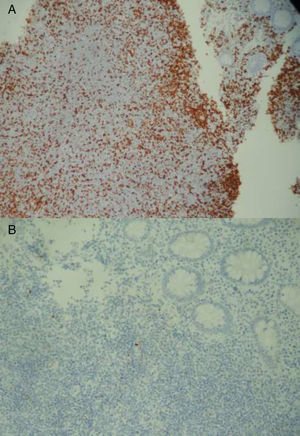
En el 2015 es revalorada por exacerbación del dolor. Se repite la colonoscopía evidenciando un patrón empedrado de la mucosa de colon transverso, ascendente y ciego con relación a la hiperplasia linfoide. La biopsia de ciego presentó la mucosa infiltrada por una neoplasia linfoide de células pequeñas y núcleos irregulares que se disponen en un patrón de aspecto difuso con escasos folículos residuales y expansión de la zona del manto. La inmunohistoquímica evidenció positividad para CD20, BCL2 y ciclina D1, y fue negativa para CD3, CD5, CD23, CD10 y BCL6. La FISH evidenció un patrón anormal de señalización detectando la translocación: t(11;14)(q13;q32) en el 80% de las células, que involucra el gen ciclina D1. Ambos hallazgos fueron compatibles con un LM primario CD5 negativo.
Se complementó el estudio con una TAC toraco-abdomino-pélvica, la cual no evidenció masas ni adenopatías sugestivas de otra afección extranodal o metástasis. El QuantiFERON® para tuberculosis fue negativo, al igual que las serologías para virus de la inmunodeficiencia humana (VIH) y la calprotectina fecal. Se determinó una deshidrogenasa láctica (DHL) y una beta-2 microglobulina dentro de los límites normales. Se estableció un MIPI de 8,8 correspondiente a un alto riesgo. Se refirió a hematología para iniciar tratamiento.
DiscusiónPese a que el tracto gastrointestinal (TGI) es el sitio extranodal más comúnmente afectado por los linfomas (5-20% de los casos), constituyen solo el 1-4% de las neoplasias gastrointestinales3. Dentro de ellos, el LM abarca aproximadamente el 6% de los linfomas no Hodgkin (LNH), y presenta infiltración del TGI en un 10-28% de los pacientes1,3. Sin embargo, solo el 2% de los linfomas gastrointestinales primarios son LM y, usualmente, se presentan en varones mayores de 60 años, y en estadios avanzados1,3.
Genéticamente se caracteriza por la translocación t(11;14)(q13;q32), la cual provoca la sobreexpresión de la ciclina D1, una de las proteínas responsables de regular la progresión durante el ciclo de división celular4.
Cuando la afección es colónica los síntomas más comunes son dolor abdominal, diarrea, pérdida de peso y, en raros casos, enteropatía perdedora de proteínas, ascitis quilosa, malabsorción, perforación e intususcepción5. Estudios recientes han demostrado que un 10- 15% de los LM tienen un curso indolente6.
Los reportes de lesiones en colon han mostrado que la PML es el patrón endoscópico más común (80%), seguidas por lesiones protruidas (18%) y reportes de casos de masas rectales solitarias, úlceras sangrantes y lesiones superficiales2.
En cuanto a su pronóstico, el Mantle Cell Lymphoma International Prognostic Index funcionan como un sistema de estratificación de riesgo de los pacientes al clasificarlos en 3 grupos pronósticos, con base en sus características clínicas4.
Actualmente, la inmunoquimioterapia estándar ha demostrado no ser curativa en la mayoría de los casos, y el pronóstico es pobre3. Los nuevos regímenes (R-CHOP, trasplante de células madre autógeno, R-Hiper-CVAD, bortezomib) han mejorado significativamente la sobrevida, con remisiones prolongadas. Aun así, la sobrevida total tiende a ser solamente de 4 a 7 años3,5.
ConclusiónEste reporte de caso ejemplifica una forma de presentación atípica y larvada de una enfermedad sumamente infrecuente. El estudio endoscópico evidenció un patrón mucoso muy inespecífico, sin poder encontrar reportes de caso en la literatura, con imágenes similares. Se enfatiza en mantener al LM primario colónico dentro del diagnóstico diferencial de cuadros similares.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciamientoEl presente artículo no ameritó ninguna fuente de financiamiento.
Conflicto de interesesEl presente artículo no representa ningún conflicto de interés por parte de los autores.
A los técnicos de endoscopía del Hospital Calderón Guardia por su excelente labor.