El ultrasonido endoscópico has sido un método útil para la evaluación de la enfermedad pancreatobiliar por más de una década, sin embargo no es un escenario raro el encontrar resultados patológicos no concluyentes en el tejido obtenido para el diagnóstico. Entre los factores que alteran el rendimiento diagnóstico se encuentran la experiencia del endosonografista, el volumen de procedimientos realizados, el tipo, el tamaño y la localización, entre otros. El objetivo del presente estudio fue evaluar el rendimiento diagnóstico de la segunda USE-BAAF en las lesiones no pancreáticas.
Material y métodosSe realizó un estudio retrospectivo y transversal. Se incluyeron pacientes >18 años a los que se les realizó USE-BAAF durante el periodo de 8 años.
ResultadosSe realizaron 150 procedimientos en 132 pacientes con lesiones no pancreáticas. Finalmente, el diagnóstico se logró por USE-BAAF en 114/132 pacientes, para un rendimiento diagnóstico global de 86.63%. En total, la mediana (intervalo mínimo-máximo) de biopsias fue de 1 (1-5). El rendimiento diagnóstico de la primera USE-BAAF fue de 77.3% (102/132). Se realizó una segunda biopsia en 16/132 (12.1%) pacientes. Con la segunda USE-BAAF se observó un aumento del rendimiento global a 113/132 pacientes (11/16=68.7%; global 85.6%). No se observaron complicaciones.
ConclusiónEl repetir la USE-BAAF en lesiones no pancreáticas es necesario en pacientes con una primera negativa USE-BAAF, ya que mejora el rendimiento diagnóstico.
Endoscopic ultrasound has been a useful method for the evaluation of pancreatobiliary pathology for more than a decade, however it is not unusual to find inconclusive pathological results in tissue obtained for diagnosis. The factors affecting diagnostic performance include; endosonographist experience, the volume of procedures performed, type, size and location, amongst others. The aim of this study was to evaluate the diagnostic performance of the second EUS-FNA in non-pancreatic lesions.
Material and methodsA retrospective cross-sectional study that includedpatients>18 years who underwent EUS-FNA over a period of 8 years.
Results150 procedures were performed in 132 patients with non-pancreatic lesions. Finally, the diagnosis was obtained by EUS-FNA in 114/132 patients for a diagnostic yield of 86.6%. In total, the biopsy median (minimum/maximum interval) was 1 (1-5). The diagnostic yield of the first EUS-FNA was 77.3% (102/132). With the second EUS-FNA 11/16 patients had a histological diagnosis (11/16=68.7%; global 85.6%). No complications were reported.
ConclusionRepeat EUS-FNA in patients with non-pancreatic lesions is necessary in patients with a first negative EUS-FNA because it improves the diagnostic yield.
El ultrasonido endoscópico ha sido un método útil para la evaluación de la enfermedad pancreatobiliar por más de una década1. La capacidad de obtener muestras histológicas de biopsias por aspiración con aguja fina guiada por ultrasonido endoscópico (USE-BAAF) ha permitido la mejor atención de los pacientes con lesiones quísticas o sólidas de páncreas2. Los rangos de precisión diagnóstica de la USE-BAAF varían entre el 78% y el 94% para el diagnóstico y la estratificación, para la estratificación de lesiones nodales entre el 64% y el 82%, obteniendo así diagnósticos citológicos entre el 80% y el 95% de los casos con una sensibilidad del 90% y especificidad del 100%. Los tumores pancreáticos son los retos más importantes en el diagnóstico, con los valores más bajos de rendimiento diagnóstico, entre el 76-90% y una tasa de falsos negativos del 15%3,4.
Sin embargo, no es un escenario raro el encontrar resultados patológicos no concluyentes con tejido obtenido para el diagnóstico; algunos de los factores que intervienen en la inexactitud de diagnóstico se han descrito previamente, tales como la experiencia del endosonografista, el volumen de procedimientos realizados, el tipo, el tamaño y la localización de la lesión, así como la presencia de un patólogo en la sala de endoscopia, el número de pases de la aguja, el uso de estilete y la aspiración durante el procedimiento, al igual que determinar la mejor opción de aguja para obtener tejido (núcleo) o aspirado celular5,6.
En realidad no existe un consenso sobre el método ideal para el abordaje diagnóstico en pacientes que ya habían sido sometidos a USE-BAAF, ya que a menudo se obtiene material no concluyente como resultado histológico. Hay pocos estudios en la literatura que proporcionan datos sobre la segunda utilidad de la USE-BAAF en lesiones pancreáticas, siendo la mayoría reporte de casos y de series de casos con rangos de rendimiento diagnóstico entre el 63% y 91% en la segunda USE-BAAF5,7–9; sin embargo, no existe información previa respecto a la segunda USE-BAAF en lesiones no pancreáticas.
El objetivo del presente estudio fue evaluar el rendimiento diagnóstico de la segunda USE-BAAF en las lesiones no pancreáticas.
Material y métodosSe realizó un estudio retrospectivo y transversal. Se incluyeron pacientes>18 años a los que se les realizó USE-BAAF durante el periodo comprendido entre enero de 2005 a diciembre de 2012 en el Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. Los datos fueron obtenidos de la base de datos del departamento de endoscopia gastrointestinal, los reportes oficiales de los estudios realizados y del expediente electrónico. Se colectaron datos demográficos (género, edad), datos en relación con los estudios realizados (fecha de estudio, indicación y resultado del estudio endoscópico, número de estudios realizados, resultados de histopatología de biopsias realizadas o de piezas quirúrgicas) y la presencia de complicaciones. Fueron excluidos aquellos pacientes en los que no se logró obtener los datos completos. Los pacientes incluidos antes del estudio proporcionaron su consentimiento informado previa explicación del procedimiento.
Técnica de ultrasonido endoscópicoLos ultrasonidos endoscópicos fueron realizados bajo sedación asistida por un anestesiólogo y bajo monitorización continua, con un ecoendoscopio lineal marca FUJI con ecoendoscopio EG-530UT con procesador SU-8000. Una vez localizada la lesión se introdujo una aguja calibre 19 o 22G (Wilson-Cook Echotip Ultra o ProCore). Durante los procedimientos no se contó con citopatólogo en la sala. Los estudios fueron realizados por 2 endosonografistas con experiencia en el campo (>500 procedimientos). Posterior al estudio los pacientes permanecían en vigilancia al menos durante 2h para valorar probables complicaciones.
Biopsia por aspiración con aguja fina guiada por ultrasonido endoscópico (ultrasonido endoscópico-biopsia por aguja fina, aguja estándar)Como paso inicial el transductor se coloca en una posición estable frente a la lesión diana. Posteriormente se introduce la espiral de metal en el canal de biopsia, observando cuidadosamente que el pistón de la aguja esté cerrado con seguridad y la aguja se encuentre retraída por completo. Con el estilete retraído, pero aún dentro de la aguja, esta se avanza en la lesión bajo control total del ultrasonido en tiempo real. Después de penetrar en el medio de la lesión el estilete se remueve completamente. Al llegar a la posición óptima dentro de la lesión, una aguja de 10ml con dispositivo de vacío se atornilla firmemente en el extremo proximal de la misma, el cual se activa tirando del émbolo de la jeringa para crear presión baja. La aguja se mueve en diversas direcciones, de 5-10 veces dentro de la lesión bajo control ultrasonográfico. Con la punta de la aguja todavía en la lesión, la succión se libera y se retrae la aguja de forma segura dentro de la funda de la misma y se bloquea en una posición segura.
Biopsia por aspiración con aguja fina guiada por ultrasonido endoscópico (aguja Procore)La biopsia con aguja fina usando las agujas ProCore (25G y 22G) se realiza de una manera similar a la USE-BAAF, pero sin el mecanismo de aspiración, ya que esta se obtiene mediante aspiración capilar, por lo que a diferencia de la técnica previa el estilete se retira lentamente durante 40seg.
Todas las muestras recuperadas se fijaron en formalina y se procesaron para el análisis histológico y citológico, las cuales fueron evaluadas por un patólogo pancreático experto. El diagnóstico final (estándar oro) se basó en los resultados de la pieza quirúrgica, la evaluación clínica, radiológica y el seguimiento de los casos no operados.
DefinicionesSe consideró una biopsia no diagnóstica en los siguientes casos: 1) material insuficiente; 2) material inadecuado para diagnóstico (necrosis, tejido inflamatorio, órgano biopsiado diferente al sitio propuesto); y 3) material suficiente pero diagnóstico quirúrgico diferente al resultado del material obtenido por biopsia.
Análisis estadísticoSe utilizó estadística descriptiva con medidas de tendencia central (media y mediana) y dispersión para una población de distribución paramétrica (desviación estándar) o no-paramétrica (intervalo mínimo-máximo) según correspondiera de acuerdo con la variable evaluada. Se utilizaron frecuencias absolutas y relativas. Todas las pruebas estadísticas se realizaron con el programa estadístico SPSS v20 para Mac.
ResultadosDurante el periodo se realizaron un total de 2,068 ultrasonidos endoscópicos con un total de 705 biopsias. Un total de 88 biopsias no se pudieron localizar de manera inicial, dejando un total de 617 estudios iniciales; 58 biopsias fueron excluidas por ser realizadas con pinza convencional y USE para estatificación, 104 procedimientos fueron excluidos por no contar con información completa. De los 455 estudios finales, un total de 150 procedimientos se efectuaron en 132 pacientes con lesiones no pancreáticas. Se incluyeron 66 (50%) mujeres. La media±DE de la edad fue 59.5±14.6 años. Los órganos de los cuales se tomaron las biopsias se muestran en la tabla 1.
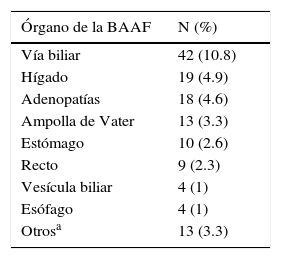
Sitio biopsiado en los 132 pacientes con USE-BAAF incluidos en el estudio
| Órgano de la BAAF | N (%) |
|---|---|
| Vía biliar | 42 (10.8) |
| Hígado | 19 (4.9) |
| Adenopatías | 18 (4.6) |
| Ampolla de Vater | 13 (3.3) |
| Estómago | 10 (2.6) |
| Recto | 9 (2.3) |
| Vesícula biliar | 4 (1) |
| Esófago | 4 (1) |
| Otrosa | 13 (3.3) |
El diagnóstico se logró por USE-BAAF en 114/132 pacientes para un rendimiento diagnóstico de 86.63%. La mediana (intervalo mínimo-máximo) de biopsias fue de 1 (1-5). El rendimiento diagnóstico de la primera USE-BAAF fue de 77.3% (102/132).
Pacientes con segunda biopsia por aspiración con aguja fina guiada por ultrasonido endoscópicoDieciocho biopsias se repitieron en 16/132 (12.1%) pacientes. Cinco (31.2%) de estos pacientes fueron mujeres. Los órganos de los cuales se tomó una segunda USE-BAAF fueron la vía biliar (n=11; 68.7%), la ampolla de Vater (n=3; 18.7%), ovario (n=1; 6.2%) y recto (n=1; 6.2%).
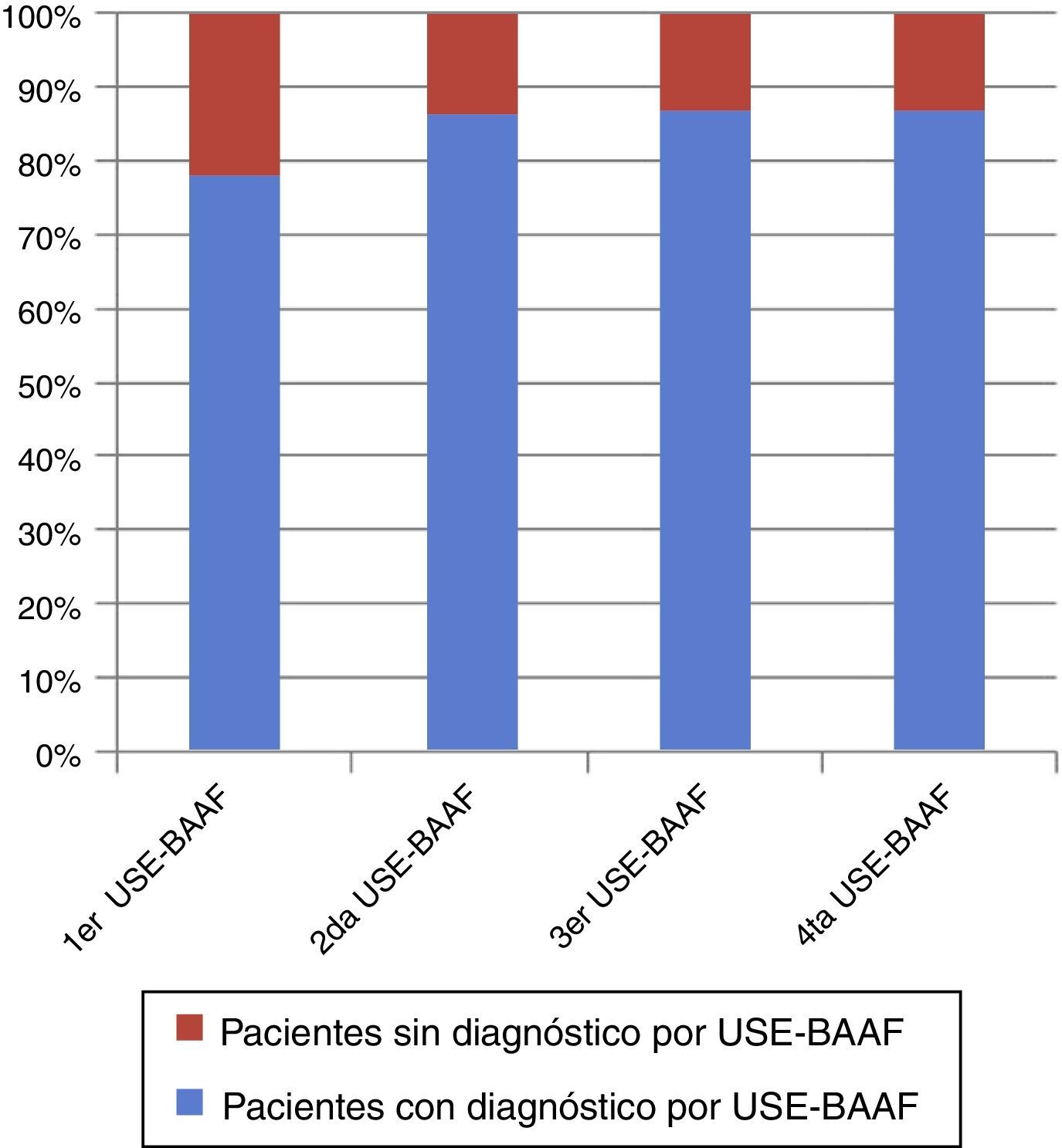
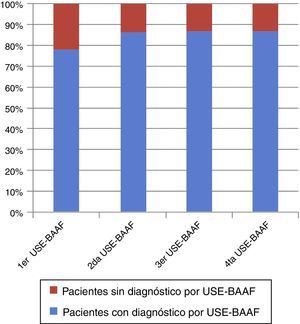
Con la segunda USE-BAAF se observó un aumento del rendimiento global a (113/132; 11/16=68.7%; global 85.6%). La mediana (intervalo mínimo-máximo) de biopsias en los pacientes en los que sí se obtuvo el diagnóstico fue 1 (1-3). En la figura 1 se observa el incremento global en el número de diagnósticos con la repetición de USE-BAAF.
El rendimiento diagnóstico de acuerdo con el órgano biopsiado fue de 92.8% para lesiones de la vía biliar, 84.2% para lesiones hepáticas, 83.3% para adenopatías, 76.9% para lesiones de la ampolla de Vater, 90% para lesiones gástricas, 100% para lesiones rectales, 75% para lesiones en vesícula biliar, 100% en lesiones esofágicas y 69.2% en otras localizaciones.
No se presentaron complicaciones mayores en ninguno de los pacientes estudiados.
DiscusiónDe acuerdo con nuestros resultados, repetir una USE-BAAF en pacientes con lesiones no-pancreáticas y con primera biopsia negativa es necesario, ya que mejora el rendimiento diagnóstico. De acuerdo con lo que investigamos, el presente estudio representa la muestra más grande para biopsias repetidas por USE-BAAF en lesiones no pancreáticas.
Afortunadamente no con demasiada frecuencia un ecoendoscopista puede enfrentarse a la situación donde una biopsia tomada con guía ultrasonográfica no fue diagnóstica. El dilema principal es decidir qué hacer a continuación, para lo cual existen varias opciones: 1) observación; 2) exploración por cirugía; y 3) repetir la USE-BAAF. De acuerdo con los resultados de nuestro trabajo esta última opción en lesiones no-pancreáticas parece ser adecuada, ya que tiene alto rendimiento diagnóstico con menor riesgo y costos que una cirugía, así como menos riesgos de perder diagnósticos malignos como cuando únicamente se realiza seguimiento clínico.
Existen trabajos publicados que tienen datos principalmente de pacientes con lesiones pancreáticas10,11; los datos del presente trabajo muestran que la misma idea se hace extensiva a pacientes con lesiones no pancreáticas. Aunque la mayoría de los pacientes de nuestro centro con USE-BAAF son por lesiones pancreáticas, 132 (33.9%) pacientes con lesiones no pancreáticas fueron incluidos en el presente estudio. Consideramos que otros centros enfrentan también este tipo de situaciones (una primera USE-BAAF no diagnóstica) en pacientes con este tipo de lesiones y, por lo tanto, consideramos que nuestros datos pueden ser de importancia para ellos. Por supuesto que debemos considerar que de acuerdo con el tipo de lesión que se esté estudiando existen alternativas para tratar de conseguir el diagnóstico histológico. Por ejemplo, en la vía biliar se podría optar por el cepillado de la vía biliar por colangiopancreatografía retrógrada endoscópica o la biopsia guiada por tomografía computarizada (TC). Sin embargo, el cepillado por colangiopancreatografía retrógrada endoscópica está asociado con complicaciones posprocedimiento como la pancreatitis, y la biopsia guiada por TC lleva el riesgo de siembra tumoral. Es evidente que después de un segundo USE-BAAF tenemos que considerar muy cuidadosamente si una nueva biopsia es realmente necesaria y cómo es posible que esta tercera (o cuarta) pueda darnos el diagnóstico histológico.
Somos conscientes del hecho de que la USE-BAAF tiene algunas limitaciones, o que hay algunos pacientes en los que no es apropiada. En nuestro centro, cuando la sospecha clínica y de imagen es alta, nuestra práctica es recomendar la exploración quirúrgica a pesar de una USE-BAAF negativa. La cohorte de este estudio consistió en pacientes que se consideraron inicialmente con lesiones no resecables por cualquiera de los métodos de estadificación USE o TC, debido a que en los pacientes con una lesión resecable se recomienda la cirugía directa, sin USE-BAAF.
Existen datos previos acerca de la utilidad de la USE repetida en un centro de referencia terciario, con un impacto clínico en el 63% de los pacientes cuando es realizada por expertos12. Un aspecto importante de este estudio es que todos los procedimientos USE-BAAF de repetición se llevaron a cabo en la misma institución, por el mismo grupo de médicos y hemos sido capaces de seguir de cerca la evolución clínica de los pacientes. Este estudio no incluyó a los pacientes que con USE-BAAF previa fallida o con diagnóstico «perdido» referido por otros médicos de la comunidad.
La limitación mayor de este estudio es su naturaleza retrospectiva; sin embargo, estos datos representan la mayor muestra para el uso USE-BAAF de repetición en lesiones no pancreáticas.
En conclusión, repetir la USE-BAAF en lesiones no pancreáticas es necesario en pacientes con una primera USE-BAAF negativa, ya que mejora el rendimiento diagnóstico.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinaciamientoNingún autor recibió financiamiento para la realización del estudio.
Conflicto de interesesNingún autor manifiesta conflicto de intereses.