La erradicación de la infección por Helicobacter pylori representa un desafío clínico.
ObjetivoEvaluar la eficacia y seguridad de la terapia cuádruple con esomeprazol más una cápsula 3 en 1 que contiene subcitrato de bismuto, metronidazol y tetraciclina, más probióticos en pacientes diagnosticados de infección por H. pylori en la práctica clínica habitual.
MétodosEstudio prospectivo, intervencional, unicéntrico y abierto realizado en pacientes consecutivos con indicación confirmada de erradicación de infección por H. pylori. Los pacientes fueron tratados con 3 cápsulas de Pylera® 4veces al día (desayuno, comida, merienda y cena), más 40mg de esomeprazol, 2veces al día durante 10días (30min antes de desayuno y cena) y probióticos durante 30días. La erradicación de la infección por H. pylori se confirmó mediante la prueba del aliento con urea marcada realizada al menos 28días después del final del tratamiento.
ResultadosUn total de 100 pacientes fueron incluidos consecutivamente. Veinticinco (25,0%) pacientes tenían historia previa de tratamiento de su infección por H. pylori. En la población por intención de tratar, las tasas de erradicación fueron del 90,7% (68/75) y del 80,0% (20/25) en los pacientes tratados con Pylera® como primera línea o como terapia de rescate, respectivamente. Dieciocho pacientes (18%) presentaron, al menos, un acontecimiento adverso, la mayoría (89%) leves.
ConclusiónDiez días de tratamiento con un régimen cuádruple de bismuto, metronidazol y tetraciclina más esomeprazol y probióticos es una estrategia eficaz y segura en pacientes con infección por H. pylori.
The eradication of Helicobacter pylori infection represents a clinical challenge.
ObjectiveTo evaluate the efficacy and safety of quadruple therapy with esomeprazole plus a 3-in-1 capsule containing bismuth subcitrate, metronidazole and tetracycline, plus probiotics in patients diagnosed with H. pylori infection in routine clinical practice.
MethodsA prospective, interventional, single-centre and open-label study in consecutive patients with a confirmed indication for eradication of H. pylori infection. Patients were treated with three capsules of Pylera® four times a day (breakfast, lunch, afternoon snack and dinner), plus 40mg of esomeprazole twice daily for 10 days (30min before breakfast and dinner) and probiotics for 30 days. Eradication of H. pylori infection was confirmed by labelled urea breath test performed at least 28 days after the end of treatment.
ResultsA total of 100 patients were consecutively enrolled. Twenty-five patients (25.0%) had a prior history of treatment for their H. pylori infection. In the intention-to-treat population, eradication rates were 90.7% (68/75) and 80.0% (20/25) in patients treated with Pylera® as the first line or as rescue therapy, respectively. Eighteen patients (18%) had at least one adverse event, most of which (89%) were mild.
ConclusionTen days of treatment with a quadruple regimen of bismuth, metronidazole and tetracycline plus esomeprazole and probiotics is an effective and safe strategy in patients with H. pylori infection.
El Helicobacter pylori es uno de los patógenos más prevalentes en humanos, llegando a afectar a más del 50% de la población1,2.
La infección por H. pylori causa inflamación crónica en la mucosa gástrica y es responsable de un número significativo de enfermedades digestivas, tales como úlceras duodenales o gástricas (se desarrollan en el 1-10% de los pacientes infectados), cáncer gástrico (en el 0,1-3%) y linfoma linfoide asociado a la mucosa gástrica (MALT) (en el 0,01%)3-6.
Inicialmente, el tratamiento de elección para erradicar la infección por H. pylori consistía en una terapia triple con un inhibidor de la bomba de protones (IBP), más 2 de los 3 antibióticos siguientes: claritromicina, amoxicilina o metronidazol. Sin embargo, en los últimos años su eficacia ha disminuido a niveles inaceptables en muchos países, especialmente debido al aumento de los niveles de resistencia bacteriana7-10.
De acuerdo con las recomendaciones de la IVConferencia Española de Consenso sobre el tratamiento de la infección por H. pylori, un tratamiento efectivo sería aquel capaz de erradicar la infección por H. pylori en aproximadamente el 90% de los pacientes11.
La triple terapia con omeprazol, amoxicilina y claritromicina (OAC) es inapropiada, cuando las tasas locales de resistencia a la claritromicina superan el 15%11,12. En España, se han publicado unas cifras medias de resistencia a claritromicina del 18,3%, a metronidazol del 40,8% y frente a ambos del 10,1%13. Es más, en un estudio publicado recientemente se han identificado tasas de resistencia a la claritromicina del 33% en niños14.
El descenso en la tasa de erradicación de la infección por H. pylori ha llevado al desarrollo de nuevas estrategias terapéuticas15-17.
En España, la terapia de primera línea, recomendada actualmente, es una pauta cuádruple concomitante sin bismuto (IBP, claritromicina, amoxicilina y metronidazol)11.
Las recomendaciones de la IVConferencia Española de Consenso sobre el tratamiento de la infección por H. pylori indican que, tras el fracaso de un tratamiento —bien triple, o cuádruple— que incluya claritromicina, se recomienda una pauta con levofloxacino preferiblemente cuádruple (IBP, amoxicilina, levofloxacino y bismuto) o, como alternativa, una terapia cuádruple con bismuto (IBP, bismuto, tetraciclina y metronidazol)11.
Es posible utilizar doxiciclina en lugar de tetraciclina, aunque la experiencia es mucho más limitada y existen dudas sobre su equivalencia terapéutica11.
Las recomendaciones del VDocumento de consenso de MaastrichtV/Florencia12 indican que un régimen cuádruple de bismuto, metronidazol y tetraciclina (BMT) más omeprazol (IBP) obtiene una tasa de erradicaciones alta en pacientes en los que anteriormente habían fracasado otras alternativas terapéuticas.
De acuerdo con la evidencia científica disponible hasta el momento, las terapias BMT-IBP consiguen unas tasas de erradicación altas tanto administradas como primera línea18-23 como administradas como tratamiento de rescate24-29. Una de las ventajas de la terapia BMT-IBP es que, hasta el momento, no se ha demostrado la existencia de resistencias del H. pylori al bismuto30 y que, esta terapia, no se ve afectada por las resistencias a la claritromicina o a las fluoroquinolonas31.
El objetivo de este estudio es evaluar la eficacia y seguridad de la terapia cuádruple con esomeprazol más una cápsula 3 en 1 que contiene subcitrato de bismuto, metronidazol y tetraciclina en pacientes diagnosticados de infección por H. pylori en la práctica clínica habitual.
Material y métodosEstudio prospectivo, intervencional, unicéntrico y abierto realizado, entre febrero de 2016 y marzo de 2017, en pacientes consecutivos con indicación confirmada de erradicación de la infección por H. pylori, que recibieron tratamiento con una terapia cuádruple basada en bismuto, en condiciones de la práctica clínica habitual.
El protocolo del estudio fue aprobado por el comité ético del Hospital Universitario de la Zarzuela. Todos los pacientes fueron informados de los detalles del protocolo del estudio y los pacientes proporcionaron un consentimiento informado por escrito antes de comenzar el estudio. Se siguieron los principios éticos establecidos en la Declaración de Helsinki y la buena práctica clínica.
Población de estudioPacientes con una infección confirmada de H. pylori e indicación para ser tratados con un tratamiento erradicador, de edad igual o superior a 18 años. La infección por H. pylori se confirmó mediante, al menos, uno de los siguientes métodos: prueba de urea en aliento, histología o test rápido de ureasa.
Se excluyeron aquellos pacientes que presentaron contraindicaciones/alergias a cualquiera de los fármacos utilizados en el estudio, deterioro orgánico importante, cirugía del tracto gastrointestinal superior, presencia de comorbilidades significativas (neoplasias, trastornos de la coagulación y enfermedades hepáticas, cardiorrespiratorias o renales), embarazo o lactancia.
Tratamiento de erradicación de Helicobacter pyloriEl tratamiento erradicador administrado en el estudio consistió en una preparación galénica que contenía subcitrato de bismuto de potasio 140mg, metronidazol 125mg y tetraciclina clorhidrato 125mg en cada cápsula (Pylera® Allergan, Inc., Irvine, CA).
Los pacientes recibieron 3 cápsulas de Pylera® 4veces al día (desayuno, comida, merienda y cena), durante 10 días, más 40mg de esomeprazol, 2veces al día (30min antes del desayuno y de la merienda) 10días y probióticos 1c/24h durante 30días. Se indicó a los pacientes que se abstuvieran de beber alcohol y fumar durante el tratamiento, y también que evitaran tanto la ingesta de lácteos coincidiendo con la toma de Pylera® como tomar el sol.
La erradicación de la infección por H. pylori se confirmó mediante prueba de urea en aliento realizada al menos 28días después del final del tratamiento (no se permitió la toma de antibióticos o IBP durante 4 semanas).
El cumplimiento terapéutico se clasificó como bueno o insuficiente según el recuento del fármaco en las visitas médicas. Los pacientes que tomaron un 80% o más de la medicación prescrita se consideraron como buenos cumplidores, mientras que los que tomaron menos de un 80% de la medicación de estudio fueron considerados como cumplidores insuficientes.
Variables del estudioEl criterio principal de valoración fue la tasa de erradicación de H. pylori, definida como una prueba de urea en aliento o una prueba rápida de ureasa negativa realizada, al menos, 28días después del final del tratamiento.
El objetivo secundario fue la seguridad, monitorizado a través de la incidencia de acontecimientos adversos identificados verbalmente, mediante preguntas genéricas del tipo: ¿Cómo se encuentra? ¿Ha experimentado alguna molestia o síntoma nuevo desde la última visita? Según su gravedad, los acontecimientos adversos se clasificaron en (1) leves: el paciente es consciente del signo o síntoma, pero fácilmente tolerable. No requiere terapia o intervención médica; (2) moderados: molestia que produce interferencia con las actividades habituales. Requiere intervención médica o terapia mínima; y (3) graves: incapacita e inhabilita para trabajar o efectuar actividades habituales (puede significar un riesgo para la vida del paciente). Requiere intervención o terapia médica.
Análisis estadísticoTodos los análisis estadísticos se realizaron con el programa informático MedCalc versión 17.4 (MedCalc Software bvba, Ostend, Bélgica).
Antes de comenzar el estudio se calculó que sería necesario incluir 94 pacientes para estimar una proporción de éxitos del 87,5%, con un nivel de confianza del 95% y una precisión del 7,5%. Se asumió una pérdida de seguimiento del 20% de los pacientes.
Los datos fueron expresados como número (porcentaje), media (desviación estándar [DE]), media (intervalo de confianza del 95% [IC 95%]) o mediana (IC 95%) según corresponda.
Las variables categóricas fueron comparadas mediante el estadístico de la Chi cuadrado o el test exacto de Fisher, según correspondiera.
El análisis de eficacia por intención de tratar (ITT) incluyó a todos los pacientes que recibieron la medicación del estudio y tomaron al menos una dosis de la medicación del estudio. Los pacientes sin un resultado observado se consideraron como fracasos de tratamiento. Los análisis por protocolo (PP) excluyeron a aquellos pacientes que no completaron el estudio o presentaron violaciones mayores del protocolo.
Se realizó un análisis univariante comparando las características basales de los pacientes con éxito y fracaso de erradicación de H. pylori utilizando la prueba de la Chi cuadrado de Pearson. Los factores asociados con fracaso en el análisis univariante con un valor de p≤0,15 fueron incluidos en el modelo multivariante. Se utilizó un modelo de regresión logística para el análisis multivariante.
Se consideró como estadísticamente significativo un valor de p<0,05.
ResultadosDe los 150 pacientes que fueron evaluados, 100 cumplieron los criterios de inclusión/exclusión y fueron incluidos en el análisis ITT. De los 100 pacientes incluidos en el análisis ITT, 10 fueron excluidos del análisis PP: 5 fueron pérdidas de seguimiento y no aportaron información sobre las causas de su abandono; 3 pacientes fueron retirados de forma prematura del estudio por mala tolerancia al tratamiento (2 por vómitos y uno por ansiedad) que, en ningún caso, requirieron ingreso hospitalario y 2 pacientes por ausencia de los resultados de la prueba de confirmación. Las principales características demográficas y clínicas de las poblaciones ITT y PP se muestran en la tabla 1.
Características demográficas y clínicas de la población de estudio
| Población de estudio | ||
|---|---|---|
| ITT | PP | |
| n=100 | n=90 | |
| Edad, años | ||
| Media (DE) | 47,1 (15,4) | 47,9 (15,8) |
| IC 95% | 44,0 a 50,2 | 44,5 a 51,2 |
| Sexo, n (%) | ||
| Hombre | 40 (40,0) | 39 (43,3) |
| Mujer | 60 (60,0) | 51 (56,7) |
| Hábito tabáquico, n (%) | ||
| No | 88 (88,0) | 79 (87,8) |
| Sí | 12 (12,0) | 11 (12,2) |
| Consumo de alcohol, n (%) | ||
| No | 93 (93,0) | 84 (93,3) |
| Leve | 1 (1,0) | 1 (1,1) |
| Moderado | 6 (6,0) | 5 (5,6) |
| Indicación para erradicación, n (%) | ||
| Dispepsia funcional | 69 (69,0) | 59 (65,6) |
| Úlcera péptica | 10 (10,0) | 10 (11,1) |
| ERGE | 21 (21,0) | 21 (23,3) |
| Indicación IBP-BMT, n (%) | ||
| Primera línea | 75 (75,0) | 69 (76,7) |
| Segunda línea | 18 (18,0) | 15 (16,7) |
| Tercera línea | 4 (4,0) | 4 (4,4) |
| Cuarta línea | 2 (2,0) | 1 (1,1) |
| Quinta línea | 1 (1,0) | 1 (1,1) |
| Alergias medicamentosas, n (%)a | ||
| No | 94 (94,0) | 85 (94,4) |
| Penicilina | 6 (6,0) | 5 (5,6) |
| Rifampicina | 1 (1,0) | 1 (1,1) |
DE: desviación estándar; ERGE: enfermedad por reflujo gastroesofágico; IBP: inhibidor de la bomba de protones; IBP-BMT: inhibidor de la bomba de protones-bismuto subcitrato, metronidazol y tetraciclina; IC 95%: intervalo de confianza del 95%; ITT: intención de tratar; PP: por protocolo.
Veinticinco (25%) pacientes tenían historia previa de tratamiento de su infección por H. pylori, mayoritariamente con claritromicina, amoxicilina y un IBP (tabla 2).
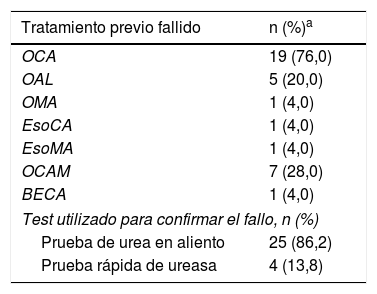
Historial de los regímenes de erradicación de Helicobacter pylori en los pacientes tratados con terapia cuádruple basada en inhibidores de la bomba de protones y bismuto (IBP-BMT) como terapia de rescate (población por intención de tratar)
| Tratamiento previo fallido | n (%)a |
|---|---|
| OCA | 19 (76,0) |
| OAL | 5 (20,0) |
| OMA | 1 (4,0) |
| EsoCA | 1 (4,0) |
| EsoMA | 1 (4,0) |
| OCAM | 7 (28,0) |
| BECA | 1 (4,0) |
| Test utilizado para confirmar el fallo, n (%) | |
| Prueba de urea en aliento | 25 (86,2) |
| Prueba rápida de ureasa | 4 (13,8) |
El porcentaje total puede ser mayor de 100 porque 7 pacientes recibieron más de un régimen de tratamiento.
BECA: bismuto/esomeprazol/claritromicina/amoxicilina; DE: desviación estándar; EsoCA: esomeprazol/claritromicina/amoxicilina; EsoMA: esomeprazol/metronidazol/amoxicilina; IC 95%: intervalo de confianza del 95%; OAL: omeprazol/amoxicilina/levofloxacino; OCA: omeprazol/claritromicina/amoxicilina; OCAM: omeprazol/claritromicina/amoxicilina/metronidazol; OMA: omeprazol/metronidazol/amoxicilina.
En la población ITT la tasa de erradicación fue del 88,0% (IC 95%: 81,6-94,4%), mientras que en la población PP la infección se erradicó en el 97,8% (IC 95%: 94,5-99,6%).
De acuerdo con el hecho de si los pacientes habían recibido el tratamiento como primera línea o como tratamiento de rescate, las tasas de erradicación fueron, en la población ITT, del 90,7% (IC 95%: 84,1-97,3%) (68/75) y del 80,0% (IC 95%: 64,3-95,7%) (20/25), respectivamente.
En la población PP, las tasas de erradicación fueron del 98,6% (IC 95%: 93,8-99,9) (68/69) y del 95,2% (IC 95%: 90,1-100,0%) (20/21) en los pacientes que recibieron el tratamiento como terapia de primera línea o como tratamiento de rescate, respectivamente. No se encontró ninguna diferencia en la tasa de erradicación entre los pacientes que recibieron el tratamiento como primera línea y los que lo recibieron como tratamiento de rescate, ni en la ITT (p=0,1553), ni en la población PP (p=0,3543).
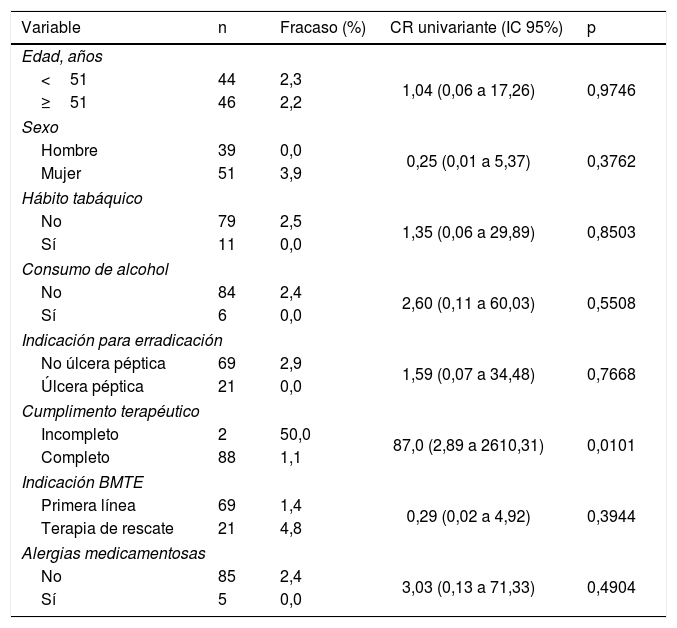
Factores relacionados con el fracaso de la erradicaciónEn el análisis univariante (tabla 3) el fracaso en la erradicación se asoció con un tratamiento incompleto.
Potenciales factores de riesgo para el fracaso de erradicación de Helicobacter pylori en un análisis univariante entre los 90 pacientes incluidos en el análisis por protocolo
| Variable | n | Fracaso (%) | CR univariante (IC 95%) | p |
|---|---|---|---|---|
| Edad, años | ||||
| <51 | 44 | 2,3 | 1,04 (0,06 a 17,26) | 0,9746 |
| ≥51 | 46 | 2,2 | ||
| Sexo | ||||
| Hombre | 39 | 0,0 | 0,25 (0,01 a 5,37) | 0,3762 |
| Mujer | 51 | 3,9 | ||
| Hábito tabáquico | ||||
| No | 79 | 2,5 | 1,35 (0,06 a 29,89) | 0,8503 |
| Sí | 11 | 0,0 | ||
| Consumo de alcohol | ||||
| No | 84 | 2,4 | 2,60 (0,11 a 60,03) | 0,5508 |
| Sí | 6 | 0,0 | ||
| Indicación para erradicación | ||||
| No úlcera péptica | 69 | 2,9 | 1,59 (0,07 a 34,48) | 0,7668 |
| Úlcera péptica | 21 | 0,0 | ||
| Cumplimento terapéutico | ||||
| Incompleto | 2 | 50,0 | 87,0 (2,89 a 2610,31) | 0,0101 |
| Completo | 88 | 1,1 | ||
| Indicación BMTE | ||||
| Primera línea | 69 | 1,4 | 0,29 (0,02 a 4,92) | 0,3944 |
| Terapia de rescate | 21 | 4,8 | ||
| Alergias medicamentosas | ||||
| No | 85 | 2,4 | 3,03 (0,13 a 71,33) | 0,4904 |
| Sí | 5 | 0,0 | ||
Se considera estadísticamente significativo un valor de p<0,05.
BMTE: bismuto, metronidazol, tetraciclina y esomeprazol; CR: cociente de riesgo; IBP: inhibidor de la bomba de protones; IC 95%: intervalo de confianza 95%.
Dado que solo una de las variables obtuvo un nivel de significación igual o inferior a 0,15 en el análisis univariante, no se realizó el análisis multivariante.
Perfil de seguridadDe los 100 pacientes incluidos en el análisis ITT, 81 (81%) pacientes refirieron buena tolerancia al tratamiento. Tres pacientes fueron retirados prematuramente del estudio por mala tolerancia al tratamiento (2 por vómitos y uno por ansiedad) que, en ningún caso, requirieron ni ingreso hospitalario ni tratamiento adicional.
Durante el seguimiento, 18 (18%, IC 95%: 10,5-25,5%) pacientes reportaron al menos un acontecimiento adverso relacionado con el tratamiento, la mayoría (9%) clasificados como leves y ninguno de ellos clasificado como grave. La media (DE) de duración de los acontecimientos adversos fue de 7,4 (2,3) días.
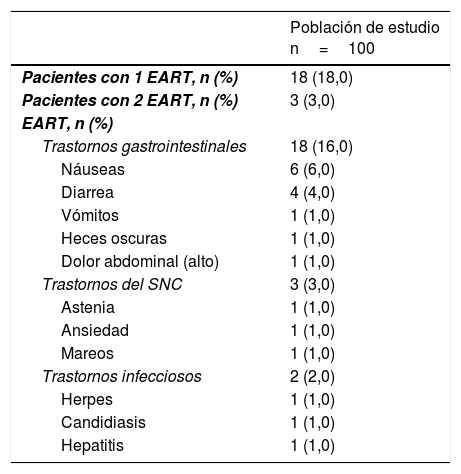
Dieciséis (16,0%) pacientes reportaron acontecimientos adversos relacionados con el tracto digestivo alto, 3 (3,0%) refirieron acontecimientos adversos relacionados con el sistema nervioso central y 3 (3,0%) pacientes presentaron problemas infecciosos. Los diferentes acontecimientos adversos se resumen en la tabla 4.
Efectos adversos relacionados con el tratamiento en la población por intención de tratar
| Población de estudio n=100 | |
|---|---|
| Pacientes con 1 EART, n (%) | 18 (18,0) |
| Pacientes con 2 EART, n (%) | 3 (3,0) |
| EART, n (%) | |
| Trastornos gastrointestinales | 18 (16,0) |
| Náuseas | 6 (6,0) |
| Diarrea | 4 (4,0) |
| Vómitos | 1 (1,0) |
| Heces oscuras | 1 (1,0) |
| Dolor abdominal (alto) | 1 (1,0) |
| Trastornos del SNC | 3 (3,0) |
| Astenia | 1 (1,0) |
| Ansiedad | 1 (1,0) |
| Mareos | 1 (1,0) |
| Trastornos infecciosos | 2 (2,0) |
| Herpes | 1 (1,0) |
| Candidiasis | 1 (1,0) |
| Hepatitis | 1 (1,0) |
EART: efectos adversos relacionados con el tratamiento; SNC: sistema nervioso central.
Los resultados de este estudio, realizado según condiciones de la práctica clínica habitual, mostraron que 10 días de tratamiento con un régimen cuádruple de bismuto, metronidazol y tetraciclina más esomeprazol proporciona altas tasas de erradicación no solo como tratamiento de primera línea, sino también como terapia de rescate, con un perfil de seguridad aceptable.
Además, los resultados de este estudio mostraron que una mala adherencia al tratamiento se asoció, de manera significativa, con el fracaso en la erradicación de la infección.
Las tasas de erradicación observadas en este estudio fueron similares a las publicadas anteriormente por otros estudios que utilizaron la misma preparación (cápsulas 3 en 1) 4veces al día con un IBP 2veces al día, cuyas tasas de erradicación oscilaron entre el 80-93,2%18,19,22,26.
En un estudio prospectivo, realizado en Italia, en el que se evaluó la eficacia y seguridad de 3 cápsulas de Pylera® administradas 4veces al día más omeprazol (20mg) o esomeprazol (40mg) 2veces al día, durante 10 días, se observaron tasas de erradicación, en la población ITT, del 94,7% (IC 95%: 89,3-97,8%) y en la población PP del 97,6% (IC 95%: 93,3-99,2%)32. Además, de manera similar a nuestro estudio, no encontraron diferencias significativas en función del hecho de si el tratamiento había sido administrado como primera línea o como tratamiento de rescate, tanto en el análisis ITT como en el análisis PP32.
Un estudio realizado en China, en pacientes con dispepsia funcional e infección con H. pylori, comparó la eficacia de 2 regímenes terapéuticos: claritromicina 500mg+amoxicilina 1g+pantoprazol 40mg administrados 2veces al día, 7días, frente a metronidazol (400mg 3veces al día)+tetraciclina (750mg 4veces al día)+subcitrato de bismuto (220mg 4veces al día), 10 días33. Las tasas de erradicación fueron significativamente mayores en el grupo tratado con la terapia cuádruple basada en bismuto que en el grupo que recibió la triple terapia, tanto en la población por ITT (89,4% frente a 63,5%, respectivamente, p<0,05) como en la población PP (91,6% frente a 65,1%, respectivamente, p<0,05)33.
En un estudio aleatorizado y controlado realizado en China que comparó la eficacia de la terapia triple (CAO) (claritromicina 500mg+amoxicilina 1g+omeprazol 20mg administrados 2veces al día, 10 días) frente a una terapia cuádruple basada en bismuto (CAO+subcitrato de bismuto 120mg 4veces al día, 10 días), en pacientes con infección por H. pylori y sintomatología gastrointestinal, se encontraron tasas de erradicación, en la población por ITT, del 58,4 y del 86%, respectivamente, p<0,0123.
Como tratamiento de rescate, los resultados obtenidos en este estudio (población PP) son similares a los publicados previamente.
Un estudio multinacional europeo, que incluyó pacientes de Francia, Alemania, Italia y España, encontró unas tasas de erradicación que oscilaron entre el 93,2 y el 93,8%26.
En un estudio prospectivo y multicéntrico se observó que, en pacientes con infección por H. pylori y alergia a la penicilina, la terapia cuádruple con bismuto (IBP, bismuto, tetraciclina y metronidazol) se mostró como una mejor opción, en terapia de primera línea, que el régimen triple de IBP, claritromicina y metronidazol34.
Se ha publicado recientemente un estudio prospectivo que evaluó la eficacia y seguridad de la terapia cuádruple con omeprazol más una cápsula 3 en 1 que contiene subcitrato de bismuto, metronidazol y tetraciclina en pacientes diagnosticados de infección con H. pylori, en el área de Sevilla, en condiciones de práctica clínica habitual35. Los resultados de este estudio mostraron, en la población por ITT, unas tasas de erradicación del 97,6 y del 82,4% en los pacientes tratados con Pylera® como primera línea o como terapia de rescate, respectivamente35.
En un estudio realizado en Francia, Müller et al.36 encontraron tasas de erradicación con Pylera®, como tratamiento de rescate, que van del 83 al 87%.
Se han postulado diversos factores asociados al fracaso de erradicación, incluyendo la edad, el sexo, el tabaquismo, el alcohol y antecedentes de fármacos específicos (por ejemplo, ácido acetilsalicílico)36,37.
El cumplimiento terapéutico se asoció, de forma significativa, con el fracaso en la erradicación del H. pylori.
La adherencia al tratamiento es un parámetro muy importante a la hora de valorar el resultado de un régimen erradicador de H. pylori y debe ser tenida en cuenta al evaluar las razones de fallo terapéutico. En este estudio una mala adherencia al tratamiento se identificó como un factor de riesgo independiente de fracaso terapéutico.
Los resultados de este estudio están de acuerdo con los publicados por Müller et al., quienes observaron que una mala adherencia terapéutica se asociaba con el fracaso en la erradicación del H. pylori36.
Recientemente se ha publicado un estudio realizado en población pediátrica tratada por infección por H. pylori y en la que se observó que, en la población que recibió al menos un 90% de la medicación prescrita, la tasa de erradicación fue del 89,9%, mientras que en los pacientes con una mala adherencia la tasa de erradicación fue, tan solo, del 36,6%38.
En cuanto al perfil de seguridad, 18 pacientes reportaron acontecimientos adversos, siendo las alteraciones gastrointestinales las más comunes. Tres pacientes refirieron acontecimientos adversos relacionados con el sistema nervioso central y 2 con problemas infecciosos. Uno de los pacientes presentó una hepatitis, que fue diagnosticada por la presencia de ictericia e hipertransaminasemia en la analítica sanguínea. Este paciente no requirió discontinuación del tratamiento.
Los síntomas fueron, en general, bien tolerados y no se observaron acontecimientos adversos graves. Estos datos concuerdan con la evidencia científica disponible, en la que una terapia cuádruple con bismuto para la erradicación de H. pylori se considera segura y bien tolerada18-38.
En este estudio se utilizó esomeprazol en lugar de omeprazol. Aunque la utilización del esomeprazol puede aumentar el coste del tratamiento, se ha publicado que esomeprazol mostraba unas tasas de erradicación del H. pylori mejores que omeprazol39-41.
En relación con el uso de probióticos, de acuerdo con las recomendaciones de la IVConferencia Española de Consenso sobre el tratamiento de la infección por H. pylori, no se recomendaba, de manera generalizada, asociar probióticos al tratamiento erradicador11. Sin embargo, la evidencia científica actual muestra que, en comparación con placebo, la mayoría de las estrategias terapéuticas con probióticos han sido consideradas útiles debido a que mejoraron las tasas de erradicación de H. pylori y redujeron los efectos secundarios relacionados con la terapia42-44. Sin embargo, estos resultados han de ser interpretados con cautela. El análisis de subgrupos de régimen terapéutico y de la duración de la terapia de erradicación mostró que la suplementación con probióticos aumentó las tasas de erradicación en el subgrupo de terapia triple42-44, el subgrupo de terapia de erradicación de 7días42-44 y el subgrupo de terapia de erradicación de 14días42,44. Estos efectos positivos no fueron confirmados para los pacientes que recibieron una terapia cuádruple o una terapia secuencial42.
Este estudio presenta limitaciones que han de ser tenidas en consideración. Dentro de las limitaciones cabe destacar que se trata de un estudio abierto, no aleatorizado y no controlado.
Otra limitación es el hecho de que es un estudio realizado en un solo centro, lo que supone la posibilidad de incluir un número limitado de pacientes. Sin embargo, antes de comenzar el estudio, se realizó el cálculo del tamaño muestral.
Al haber realizado el estudio en un área geográfica determinada, hay que ser cautos a la hora de generalizar los resultados de este estudio.
En resumen, 10días de tratamiento con un régimen cuádruple de bismuto, metronidazol y tetraciclina más esomeprazol y probióticos es una estrategia eficaz y segura en pacientes con infección confirmada por H. pylori.
Serán necesarios estudios comparativos en nuestro medio, principalmente prospectivos y aleatorizados, entre la terapia cuádruple concomitante sin bismuto y la cuádruple con bismuto.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores desean agradecer a los Laboratorios Allergan su colaboración con la asistencia en la redacción médica.
Cabe señalar que Allergan S.A. no participó en la preparación del documento ni la empresa influyó de ninguna manera en las conclusiones alcanzadas.
La asistencia editorial en la preparación de este manuscrito fue proporcionada por el Dr. Antonio Martínez de Ciencia y Deporte S.L. El apoyo para esta asistencia fue financiado por Allergan S.A.