El tofacitinib es un inhibidor de las cinasas Janus o Jak, sobre todo las JAK 1 y JAK 3, actuando a nivel intracelular y permitiendo bloquear la acción de múltiples citoquinas. A diferencia de otros fármacos biológicos, que actúan bloqueando una citoquina concreta, tofacitinib se administra de forma oral, lo que supone una vía de administración más sencilla y posiblemente preferida por los pacientes. Además, presenta otras ventajas, como su corta vida media, su rapidez de acción y su bajo peso molecular que hace que no induzca inmunogenicidad.
Hemos realizado un estudio retrospectivo descriptivo analizando los siete pacientes con colitis ulcerosa tratados con tofacitinib en el Hospital Torrecárdenas hasta el momento. En la tabla 1 se resumen las principales características de los mismos.
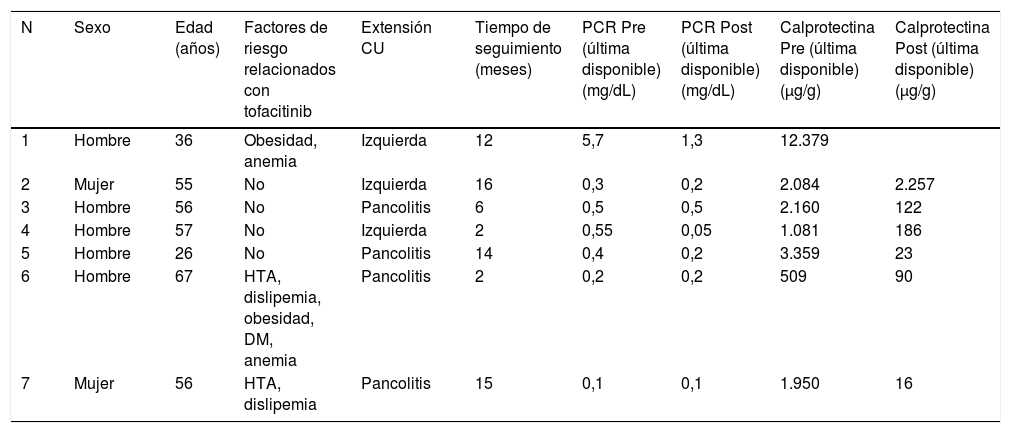
Características de los pacientes con colitis ulcerosa tratados con tofacitinib en el Hospital Torrecárdenas
| N | Sexo | Edad (años) | Factores de riesgo relacionados con tofacitinib | Extensión CU | Tiempo de seguimiento (meses) | PCR Pre (última disponible) (mg/dL) | PCR Post (última disponible) (mg/dL) | Calprotectina Pre (última disponible) (μg/g) | Calprotectina Post (última disponible) (μg/g) |
|---|---|---|---|---|---|---|---|---|---|
| 1 | Hombre | 36 | Obesidad, anemia | Izquierda | 12 | 5,7 | 1,3 | 12.379 | |
| 2 | Mujer | 55 | No | Izquierda | 16 | 0,3 | 0,2 | 2.084 | 2.257 |
| 3 | Hombre | 56 | No | Pancolitis | 6 | 0,5 | 0,5 | 2.160 | 122 |
| 4 | Hombre | 57 | No | Izquierda | 2 | 0,55 | 0,05 | 1.081 | 186 |
| 5 | Hombre | 26 | No | Pancolitis | 14 | 0,4 | 0,2 | 3.359 | 23 |
| 6 | Hombre | 67 | HTA, dislipemia, obesidad, DM, anemia | Pancolitis | 2 | 0,2 | 0,2 | 509 | 90 |
| 7 | Mujer | 56 | HTA, dislipemia | Pancolitis | 15 | 0,1 | 0,1 | 1.950 | 16 |
De los siete pacientes tratados, cinco son varones (75% de los mismos) y dos mujeres (25%). La edad se encuentra comprendida entre los 26 años y los 67 años (edad media 50,4 años, mediana 56 años). Cuatro pacientes presentaban pancolitis, y tres presentaban colitis izquierda. Ninguno de ellos presentaba manifestaciones extraintestinales.
Todos los pacientes habían estado previamente tratados con, al menos, tres fármacos biológicos (2 antiTNF y vedolizumab). Asimismo, todos los pacientes tenían actividad endoscópica grave (subíndice endoscópico de Mayo 3), así como histológica (grado 4 de Rutter).
Todos fueron tratados inicialmente con dosis de 10 mg/12 horas, observando respuesta clínica en todos ellos en las primeras ocho semanas, con disminución significativa del número de deposiciones diarias, del número de deposiciones con sangre y las molestias abdominales, estando cinco de ellos en situación de remisión clínica, que definimos como la normalización del hábito intestinal y la ausencia de sangre en las deposiciones. Cinco de ellos ya refirieron respuesta en las primeras dos semanas de tratamiento, uno en la semana 4 y el último en la semana 8. En cinco pacientes se redujo la dosis a 5 mg/12 horas en un período comprendido entre ocho y 16 semanas, desde el inicio del tratamiento y dos pacientes están próximos a cumplir la octava semana de tratamiento y, por tanto, aún con la dosis de inducción. Un paciente ha precisado volver a dosis de 10 mg/12 horas por empeoramiento clínico, con buena respuesta al aumento de dosis. El seguimiento de estos pacientes varía desde los dos a los 16 meses, con una mediana de 12 meses y una media de 9,57 meses. Se han reportado efectos adversos en tres pacientes: en dos de ellos aumento de colesterol con necesidad de inicio de terapia con estatinas y una enterocolitis por C. jejuni con buena respuesta a antibioterapia, sin otros efectos adversos significativos en el resto de pacientes.
Analíticamente, la calprotectina se encontraba elevada previamente en todos los casos. Tras el uso del fármaco, se determinó en seis de ellos, habiéndose normalizado en cinco (consideramos normalización cuando no se encuentra elevada de forma significativa, con valor < 200 μg/g) y permanecido elevada en uno de ellos, en el que, no obstante, y a pesar de no haber alcanzado una remisión clínica, la mejoría clínica era notoria. La proteína C reactiva sólo estaba elevada en dos pacientes, normalizándose en ambos. Sólo se realizó colonoscopia posterior en dos pacientes, estando ambos en remisión endoscópica.
Nuestros resultados nos permiten concluir que tofacitinib es un fármaco eficaz para el tratamiento de la colitis ulcerosa, habiendo conseguido respuesta clínica en todos los pacientes tratados, así como mejoría de los biomarcadores, en la mayoría de ellos, todo ello en un período de tiempo muy rápido, y sin efectos adversos graves. Cabe resaltar, además, el difícil escenario en el que hemos manejado el fármaco al tratarse de pacientes con actividad grave que habían sido tratados con fracaso o pérdida de respuesta al resto de los diferentes fármacos biológicos disponibles. Entre ellos, destaca un paciente de 67 años con factores de riesgo cardiovasculares, con fallo previo a dos antiTNF, vedolizumab y ustekinumab, al que, tras rechazar la alternativa quirúrgica, se le propuso tratamiento con tofacitinib, previa información de las restricciones recogidas en ficha técnica de este fármaco y de los riesgos existentes. Nuestra serie es corta y aún queda por valorar el mantenimiento de la eficacia a más largo plazo, si bien cuatro de los pacientes han superado ya el año de tratamiento.