La leucemia linfocítica crónica (LLC) es la forma más frecuente de leucemia en los adultos de los países occidentales, con una edad mediana al diagnóstico de 72 años. Esta guía, elaborada por el Grupo Español de Leucemia Linfocítica Crónica (GELLC), tiene el objetivo de facilitar y ayudar en el proceso diagnóstico, establecer recomendaciones terapéuticas para la elección del mejor tratamiento en cada tipo de paciente, homogeneizar el manejo de la LLC y facilitar la equidad en los distintos centros hospitalarios, para la utilización de los diversos regímenes de tratamiento disponibles.
MetodologíaLas referencias obtenidas se clasificaron de acuerdo con el nivel de evidencia, y siguiendo los criterios establecidos por la Agency for Health Research and Quality, y las recomendaciones que se obtuvieron se clasificaron según los criterios del National Comprehensive Cancer Network (NCCN).
DiagnósticoEl diagnóstico de LLC requiere la presencia de 5×109/l linfocitos B clonales con el fenotipo característico (CD19, CD5, CD20, CD23 y restricción de cadenas kappa o lambda) demostrados por citometría de flujo en sangre periférica y mantenidos al menos 3 meses. La presencia de una citopenia causada por un infiltrado típico en médula ósea establece el diagnóstico de LLC, independientemente del número de linfocitos circulantes o de la afectación ganglionar existente. La LLC y el linfoma linfocítico de célula pequeña (LLCP) son la misma enfermedad con formas de presentación diferente, por lo que deben tratarse de la misma forma.
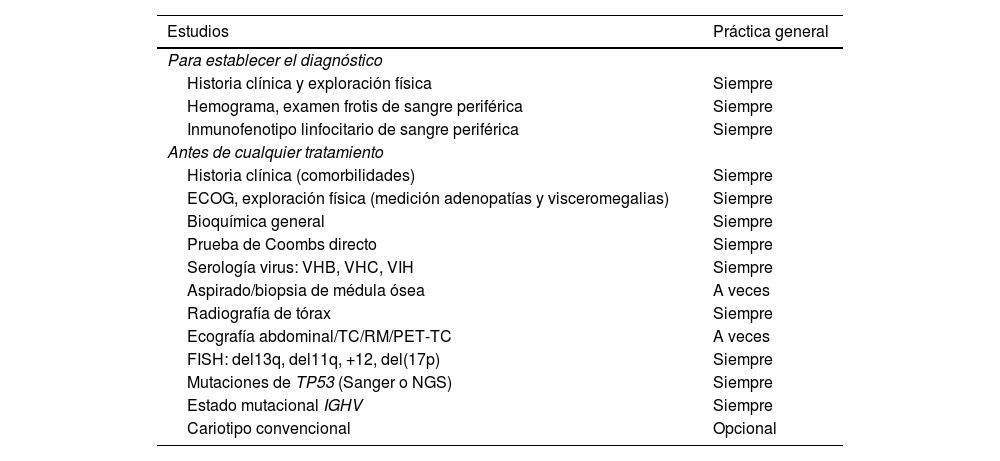
Las guías internacionales actuales establecen la determinación de alteraciones citogenéticas mediante hibridación in situ fluorescente (FISH) como prueba obligatoria en la práctica clínica para orientar el pronóstico de los pacientes. Asimismo, debe realizarse la determinación del estado mutacional de la región variable de la cadena pesada de las inmunoglobulinas (IGHV) antes del primer tratamiento y la detección de las mutaciones de TP53 antes del primero y en las sucesivas recaídas.
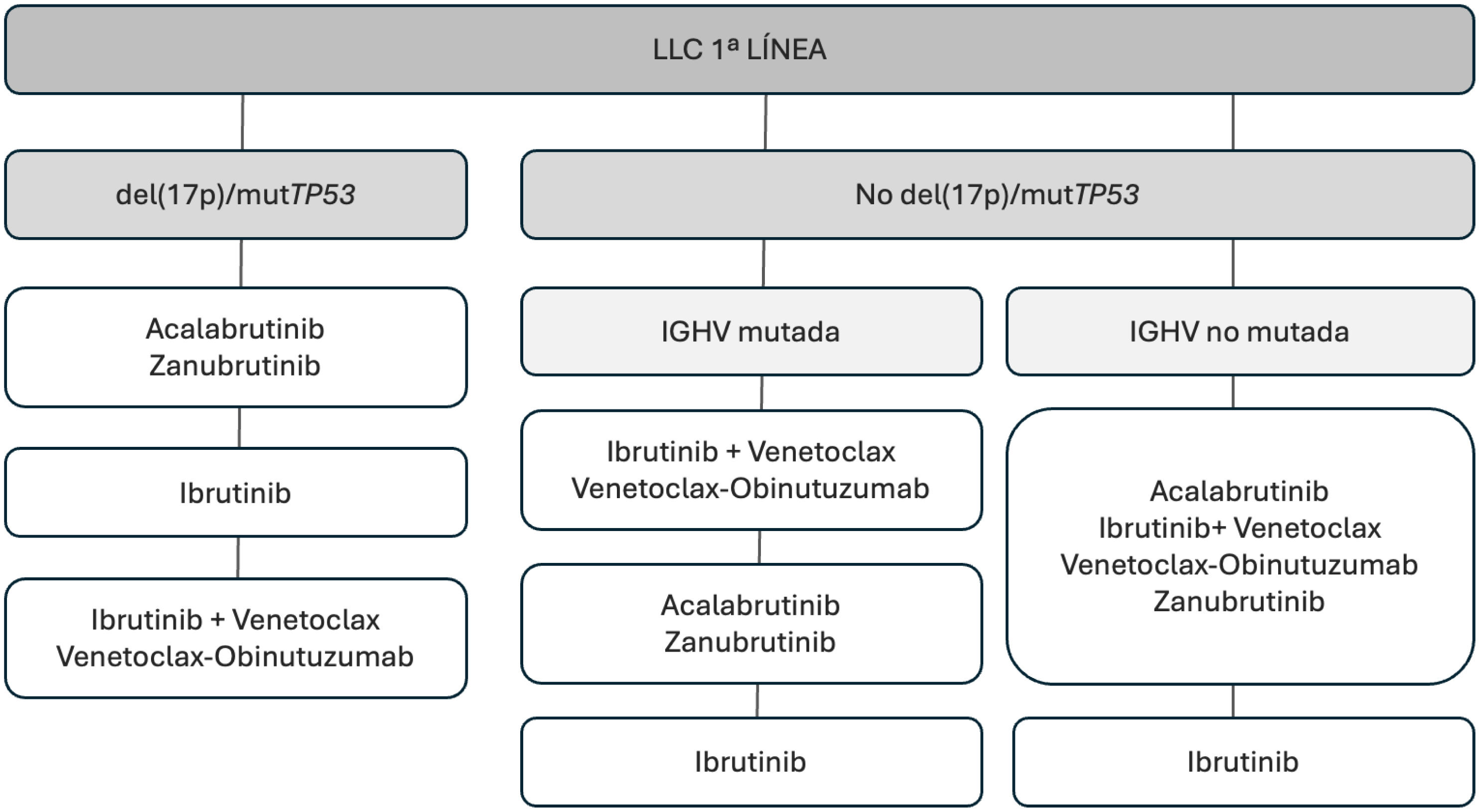
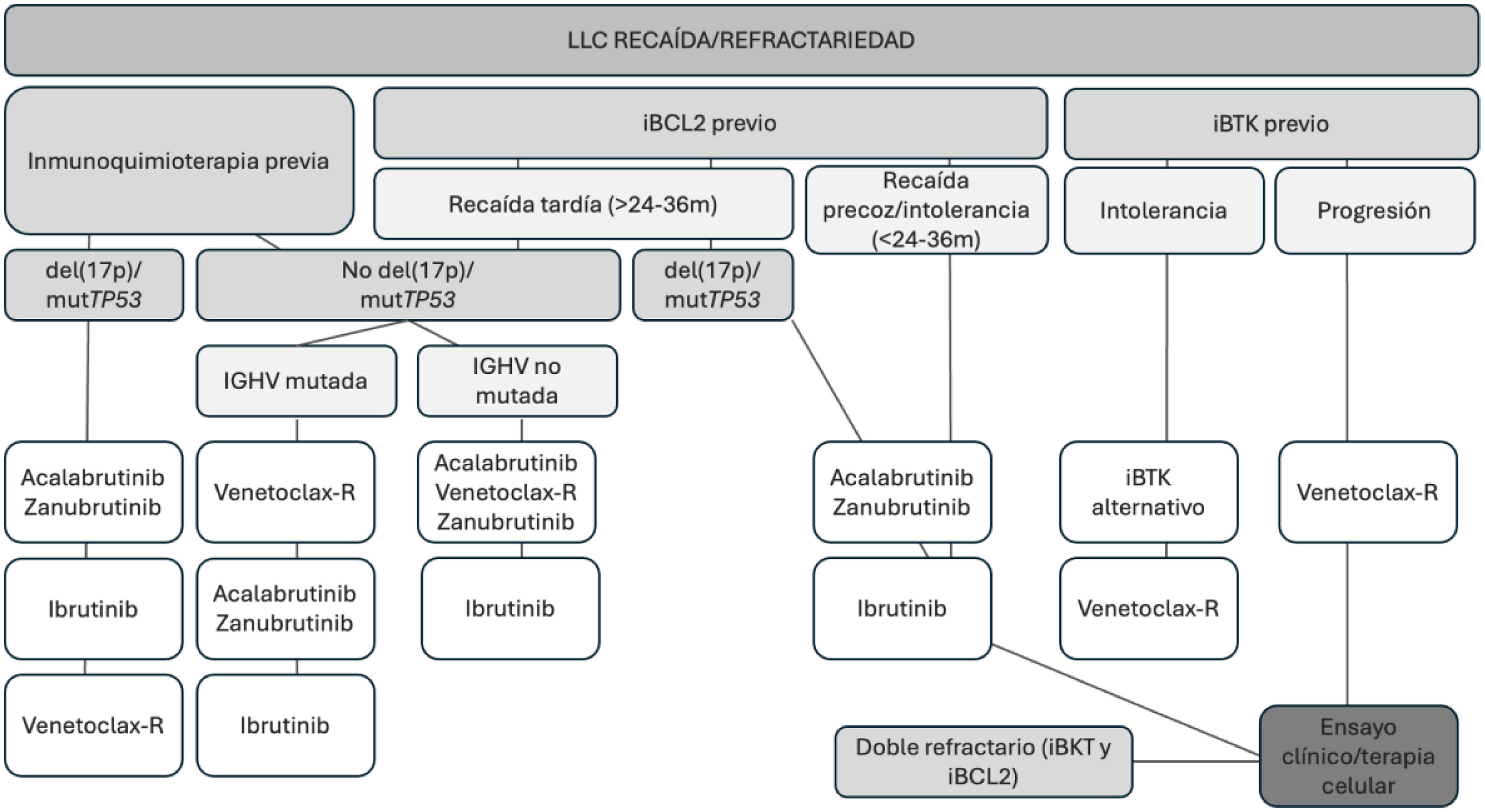
TratamientoSe debe iniciar tratamiento en pacientes sintomáticos con criterios de enfermedad activa. El primer aspecto para destacar es el posicionamiento de las terapias dirigidas por delante de la inmunoquimioterapia. En el tratamiento de primera línea, en los pacientes con del(17p) y/o mutación de TP53, la mejor opción terapéutica es un inhibidor de la tirosina cinasa de Bruton (iBTK) covalente de segunda generación administrado de forma indefinida, mientras que en los casos sin del(17p) ni mutación de TP53 con IGHV mutada (IGHV-M), debe considerarse como primera opción terapéutica la terapia finita con alguna combinación que incluya un inhibidor de BCL2 (iBCL2). Respecto a los pacientes con IGHV no mutada, tanto los iBTK administrados de forma indefinida como el tratamiento finito con iBCL2 son opciones válidas, que deberán valorarse de forma individualizada tras tener en cuenta posibles toxicidades, interacciones farmacológicas, preferencia del paciente y aspectos logísticos. En pacientes muy frágiles, deben valorarse tratamientos de soporte o paliativos. En las recaídas debe considerarse cuál ha sido el tratamiento previo, el riesgo biológico de la LLC, la duración de la respuesta (si tratamiento previo finito) o el motivo de la suspensión del iBTK (si tratamiento previo continuado).
Chronic lymphocytic leukemia (CLL) is the most common form of leukemia in adults in Western countries, with a median age at diagnosis of 72 years. This guide, developed by the Spanish Group for Chronic Lymphocytic Leukemia (GELLC), addresses the most relevant aspects of CLL, with the objectives of facilitating and aiding the diagnostic process, establishing therapeutic recommendations for choosing the best treatment for each type of patient, as well as standardizing the management of CLL and ensuring equity across different hospitals in terms of the use of the various available treatment regimens.
MethodologyThe references obtained were classified according to the level of evidence and following the criteria established by the Agency for Health Research and Quality, and the recommendations were classified according to the criteria of the National Comprehensive Cancer Network (NCCN).
DiagnosisThe diagnosis of CLL requires the presence of 5 × 109/l clonal B lymphocytes with the characteristic phenotype (CD19, CD5, CD20, CD23, and kappa or lambda chain restriction) demonstrated by flow cytometry in peripheral blood and maintained for at least 3 months. The presence of cytopenia caused by a typical bone marrow infiltrate establishes the diagnosis of CLL, regardless of the number of circulating lymphocytes or existing lymph node involvement. CLL and small lymphocytic lymphoma (SLL) are the same disease with different presentations, so they should be treated the same way.
Current international guidelines recommend FISH with the 4 probes as a mandatory test in clinical practice to guide the prognosis of patients. They also recommend determining the mutational status of the immunoglobulin heavy chain variable region (IGHV) before the first treatment and detecting TP53 mutations before the first and subsequent relapses.
TreatmentTreatment should be initiated in symptomatic patients with criteria for active disease according to iwCLL. The first aspect to highlight is the prioritization of targeted therapies over immunochemotherapy. In first-line treatment, for patients with del(17p) and/or TP53 mutation, the best therapeutic option is a second-generation covalent Bruton's tyrosine kinase inhibitor (BTKi) administered indefinitely, while in cases without del(17p) or TP53 mutation with mutated IGHV, time-limited therapy with a combination including a BCL2 inhibitor (BCL2i) should be considered as the first therapeutic option. For patients with unmutated IGHV, both continuous BTKi and finite therapy with BCL2i are valid options that should be individually evaluated considering potential toxicities, drug interactions, patient preference, and logistical aspects. In very frail patients, supportive treatment should be considered. In relapse/refractory patients, prior treatment, the biological risk of CLL, the duration of response (if prior finite treatment), or the reason for stopping BTKi (if prior continuous treatment) should be considered.