La enfermedad pulmonar obstructiva crónica (EPOC) es una patología de elevado infradiagnóstico. La utilización de cuestionarios breves diseñados para detectar casos de posible obstrucción crónica al flujo aéreo puede ayudar en el diagnóstico temprano de la EPOC.
Paciente y métodoEstudio epidemiológico observacional y transversal de validación de la versión traducida y adaptada del cuestionario Chronic Obstructive Pulmonary Disease-Population Screener (COPD-PS). Se recogieron datos sociodemográficos y clínicos, así como las respuestas a los cuestionarios COPD-PS y EQ-5D y el parámetro volumen espiratorio forzado en el primer segundo/volumen espiratorio forzado en 6 segundos (FEV1/FEV6) medido mediante el dispositivo COPD-6. Se estudiaron las propiedades psicométricas del cuestionario y la capacidad diagnóstica del cociente FEV1/FEV6 tomando como referencia el cociente FEV1/capacidad vital forzada (FEV1/FVC) posbroncodilatador < 0,7.
ResultadosParticiparon 10 centros de atención primaria que incluyeron 94 controles y 79 casos con obstrucción crónica al flujo aéreo. Las características del cuestionario fueron: factibilidad, 2,3% de los participantes no contestó algún ítem; el tiempo medio de cumplimentación fue de 47,7 segundos; el 4,1% de la muestra obtuvo puntuación cero. Validez, correlación moderada con puntuaciones del cuestionario EQ-5D y moderada-alta con el FEV1; la puntuación en el cuestionario se asoció con todos los parámetros indicativos de EPOC estudiados. El punto de corte 4 presentó el mejor balance sensibilidad/especificidad y un 78% de individuos correctamente clasificados. Para el cociente FEV1/FEV6 un punto de corte de 0,75 clasifica correctamente al 85% de los individuos.
ConclusionesEl cuestionario COPD-PS demostró buenas propiedades psicométricas. Un punto de corte 4 presenta propiedades predictivas óptimas. El cociente FEV1/FEV6<0,75 ofrece una excelente correlación con el cociente FEV1/FVC y es útil para el cribado de obstrucción crónica al flujo aéreo.
The chronic obstructive pulmonary disease (COPD) is a highly undiagnosed disease. The use of short screening questionnaires designed to detect chronic airflow obstruction may help to the early diagnosis of COPD.
Patients and methodThis was an observational, cross-sectional epidemiological study aimed to validate the translated into Spanish version of the COPD-PS questionnaire. Socio-demographic and clinical data of participants were collected, as well as their answers to the COPD-PS and EQ-5D questionnaires. The ratio FEV1/FEV6 was measured with the COPD-6 device. The psychometric properties of the questionnaire and the diagnostic yield of the FEV1/FEV6 ratio were analysed, both referred to the gold standard of post-bronchodilator FEV1/FVC < 0.7.
ResultsTen primary care centers participated in the study and included 94 controls and 79 cases with chronic airflow obstruction. Questionnaire characteristics were: feasibility, 2.3% of participants did not answer at least one item; mean time to fill the questionnaire was 47.7seconds; 4.7% of individuals had a 0 score. Validity, moderate correlation with EQ-5D scores and moderate-high with FEV1; the scores of COPD-PS were related to all parameters associated with COPD. A cut off of 4 units had the best sensitivity/specificity ratio and correctly classified 78% of participants. For the FEV1/FEV6 ratio, a cut off of 0.75 correctly classified 85% of individuals.
ConclusionsThe COPD-PS questionnaire demonstrated good psychometric properties. A cut off score of 4 has excellent predictive value. A ratio of 0.75 in the FEV1/FEV6 provides an excellent correlation with the ratio FEV1/FVC and is useful for the identification of individuals with chronic airflow obstruction.
El reconocimiento de la enfermedad pulmonar obstructiva crónica (EPOC) como una enfermedad de elevada prevalencia y alto índice de infradiagnóstico obliga a diseñar estrategias para mejorar la detección temprana de casos1,2. En este contexto, la utilización de cuestionarios breves, sencillos y específicos para la detección de obstrucción crónica al flujo aéreo puede ser de gran ayuda para identificar a la población que debe derivarse para la realización de una espirometría diagnóstica3. El cuestionario Chronic Obstructive Pulmonary Disease-Population Screener (COPD-PS) ha sido desarrollado en EE.UU. y validado recientemente como un instrumento de adecuadas propiedades psicométricas para su uso como herramienta de cribado de EPOC en población general mayor de 35 años4. Es un instrumento sencillo, autoadministrado y de corrección inmediata. Está formado por 2 ítems relacionados con la clínica de la EPOC (falta de aliento, tos productiva), un ítem de impacto de la enfermedad (limitación de la actividad debida a problemas respiratorios), un ítem sobre la historia como fumador y un ítem sobre la edad del participante.
Otra estrategia para mejorar la detección de casos en atención primaria (AP) es dotar a los médicos de espirómetros sencillos que permitan medir el flujo aéreo en las condiciones que se dan en las consultas5. Uno de estos sistemas es el aparato COPD-6, un espirómetro de bolsillo que mide el volumen espiratorio forzado en el primer segundo (FEV1) y en 6 segundos (FEV6) y que ofrece el cálculo del cociente FEV1/FEV6 como medida de obstrucción alternativa al cociente FEV1/capacidad vital forzada (FVC)6. La ventaja de la utilización del FEV6 radica en que no es necesario alargar más allá de 6 segundos la duración de la espiración forzada, con lo que se reduce el riesgo de error diagnóstico derivado de un FVC falsamente reducido7.
En el presente trabajo presentamos la validación de una versión previamente traducida y adaptada al castellano del cuestionario COPD-PS. De este modo se pretende conseguir un instrumento útil, sencillo y autoadministrado para la detección de EPOC en población general mayor de 35 años. Como objetivo secundario analizamos el rendimiento diagnóstico de la medición del cociente FEV1/FEV6 medido mediante el dispositivo COPD-6, con el fin de estudiar su aplicabilidad en AP como instrumento de cribado.
MétodoSe trata de un estudio epidemiológico observacional y transversal con el objetivo de validar la nueva versión del cuestionario COPD-PS traducido al español. Como objetivo secundario se investigó la validez diagnóstica de la medición del cociente FEV1/FEV6 mediante un dispositivo portátil de medida del FEV6 (COPD-6).
El tamaño muestral necesario para la validación se calculó de modo que permitiera la optimización del punto de corte del cuestionario para cualquier nivel de sensibilidad y especificidad. Se partió de la premisa de equilibrio entre sensibilidad y especificidad; al considerar el peor escenario de sensibilidad del 50%, un recorrido de 10 puntos para los intervalos de confianza de sensibilidad y especificidad, y un error alfa del 5%, se requeriría un tamaño muestral de 96 individuos con EPOC y 96 sin EPOC. De acuerdo con esto, se planificó el reclutamiento de 100 individuos sin EPOC (grupo control) y 100 casos de EPOC (grupo casos) provenientes de 10 consultas de AP de diversos centros en España.
En primer lugar se invitó a participar a los integrantes del grupo control. Con el fin de obtener una muestra aleatoria, se invitó a participar al último sujeto del día citado en la consulta de AP participante en el estudio por cualquier motivo, que tuviera una edad igual o superior a 35 años y que no tuviera un diagnóstico previo de EPOC. En el caso de que alguno de estos participantes resultara positivo para el diagnóstico de EPOC una vez realizada la espirometría, se clasificaba como caso, y se sustituía en el grupo control por el último sujeto del siguiente día. Una vez incluidos los 10 sujetos del grupo control, se inició la selección de los sujetos con EPOC, hasta completar el número de 10 casos por cada investigador. Los individuos reclutados como caso debían tener diagnóstico previo de EPOC estadio I o II de GOLD (espirometría forzada previa con FEV1/FVC posbroncodilatador<0,7 y FEV1 posbroncodilatador > 50%). Con el fin de evaluar la discriminación del cuestionario no se incluyeron como casos a los pacientes con EPOC estadios III y IV de GOLD.
Los criterios de exclusión generales fueron: acudir a la consulta por un episodio respiratorio agudo, tener otras enfermedades pulmonares que pueden causar obstrucción, alergia a los broncodilatadores, tener alguna contraindicación para la espirometría, tener una comorbilidad significativa, estar participando en algún ensayo clínico y presentar incapacidad física o mental para comprender la información del estudio.
Las espirometrías se realizaron según la normativa SEPAR8. Se debían obtener al menos 3 curvas espirométricas válidas y se consideró el resultado del mejor FEV1 y la mejor FVC. Todos los participantes debían realizar una prueba espirométrica prebroncodilatadora. Los participantes que presentaron un FEV1/FVC prebroncodilatador > 0,7 se confirmaron como controles. Los participantes que presentaron un FEV1/FVC prebroncodilatador < 0,7 realizaron una espirometría posbroncodilatador 15 minutos después de la inhalación de 200 μg de salbutamol. Tras la prueba broncodilatadora se podían presentar tres situaciones: a) el cociente FEV1/FVC fue > 0,7, se clasificaron como controles; b) cociente FEV1/FVC < 0,7 y FEV1<50%, en este caso se excluyeron del estudio para seguir estudiándolos según práctica clínica habitual, y c) en cambio, los que tras la prueba broncodilatadora persistían con un cociente FEV1/FVC < 70% y un FEV1>50% debían ser considerados casos de EPOC para el estudio.
Además de las respuestas a los cuestionarios y las variables clínicas referidas al propio estudio, se recogió para cada participante una serie de datos sociodemográficos, datos sobre hábito tabáquico y enfermedades crónicas. Los participantes cumplimentaron la versión española del cuestionario COPD-PS. Esta versión se obtuvo mediante un proceso de traducción y tras la realización de un panel con 5 especialistas expertos en EPOC y 25 pacientes con EPOC procedentes de diferentes consultas de neumología. El cuestionario está constituido por 5 preguntas que toman valores de 0 a 2, con lo que la puntuación final oscila entre 0 (mínimo riesgo de EPOC) y 10 (máxima probabilidad de EPOC) (fig. 1). Se recogió el tiempo de cumplimentación mediante una entrada en el mismo cuestionario. Así mismo, los participantes completaron el Cuestionario de Salud EQ-5D9 en su versión traducida y validada en español10. Este cuestionario ha demostrado tener unas propiedades que lo hacen apto para la medición de la calidad de vida en la EPOC11.
Se midió el cociente FEV1/FEV6 mediante el dispositivo portátil COPD-6 (Vitalograph copd-6, Ennis, Irlanda). Para la determinación del cociente FEV1/FEV6 se requirieron al menos 3 maniobras válidas y se consideró la mejor de ellas. Esta prueba se debía realizar necesariamente el mismo día que la espirometría, antes de la administración del broncodilatador.
Los 2 primeros participantes de cada grupo debían realizar un retest mediante la cumplimentación del COPD-PS 15 días después de la primera visita.
El estudio fue aprobado por el Comité de Ética e Investigación Clínica del Hospital Clínic de Barcelona el 28 de enero de 2010 (N°. 2010/5565) y todos los participantes dieron su consentimiento por escrito para participar.
Análisis estadísticoSe realizó una descripción de las variables sociodemográficas y clínicas recogidas durante el estudio, así como de las puntuaciones en los cuestionarios. Se realizaron contrastes (ji al cuadrado para variables categóricas, U de Mann-Whitney para variables continuas) entre los grupos control y casos para cada variable considerada.
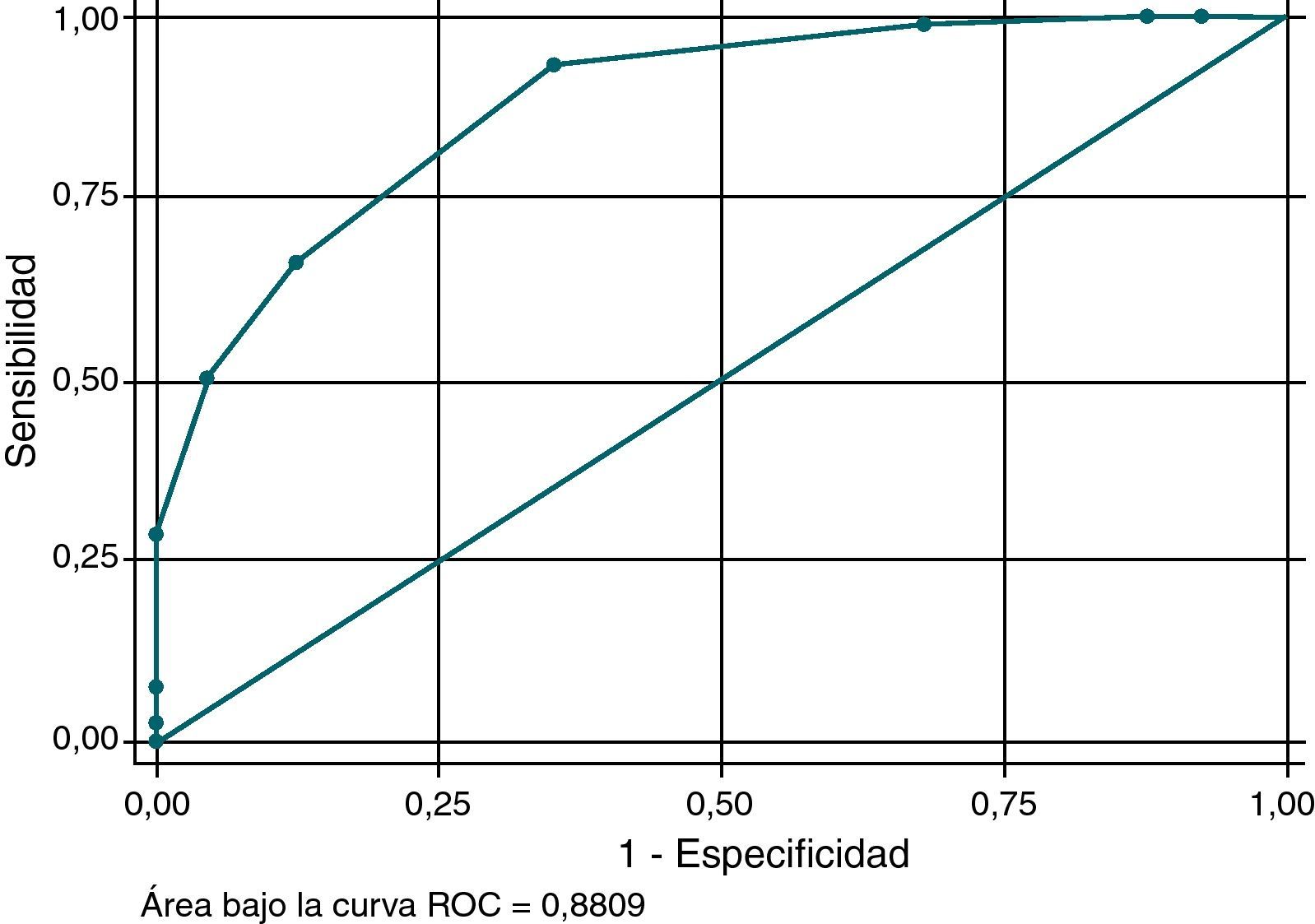
Se estudiaron las características psicométricas del cuestionario COPD-PS. Para la factibilidad se evaluó el porcentaje de no respuesta de cada ítem y el porcentaje de sujetos que no respondió a algún ítem, el tiempo de cumplimentación y el efecto techo y suelo para cada ítem y para el cuestionario en conjunto. Respecto a la validez, se evaluó la convergente mediante un análisis de la correlación (rho de Spearman) entre las puntuaciones del COPD-PS y las del cuestionario EQ-5D. La validez discriminante se analizó mediante la relación entre las puntuaciones del cuestionario COPD-PS y las variables clínicas referidas al estado de salud del participante. Las características predictivas para los diferentes puntos de corte posibles se estudiaron mediante los análisis de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo realizados en la validación de la versión original del cuestionario. Se tomó como patrón de referencia la clasificación final de los pacientes determinada por el resultado de la espirometría. Se analizó así mismo la curva ROC (receiver operating characteristic) para la que se representa, para cada punto de corte posible, la razón de verdaderos positivos del cuestionario (sensibilidad) con respecto a la razón de falsos positivos (1-especificidad). El área bajo la curva ROC representa la probabilidad de que un sujeto con diagnóstico positivo de EPOC obtenga una puntuación más alta en el cuestionario que un control. La curva permite, además, analizar de forma gráfica la capacidad predictiva del cuestionario con los diferentes puntos de corte, de modo que el mejor método predictivo se representaría mediante un punto en la coordenada (0, 1) del gráfico, es decir, 100% especificidad y 100% sensibilidad. La fiabilidad se evaluó a través del coeficiente de correlación intraclase (CCI) entre las respuestas iniciales y las de 2 semanas después, para aquellos sujetos que realizaron el retest en el plazo previsto de 15 días.
Se evaluó la capacidad diagnóstica del cociente FEV1/FEV6<0,7, medido por el dispositivo portátil COPD-6, respecto al diagnóstico espirométrico. Para ello, se analizó la sensibilidad, la especificidad y los valores predictivos del resultado obtenido mediante el COPD-6.
Los análisis se realizaron con el paquete estadístico STATA v10. No se asignaron valores a los ítems con valores perdidos. Las puntuaciones de los cuestionarios y, en consecuencia, los análisis que implicaban el manejo de dichas puntuaciones, se calcularon únicamente para aquellos sujetos que habían dado respuesta a todos los ítems. Se empleó un nivel de significación estadística (α) de 0,05.
ResultadosSe incluyeron 199 participantes, de los que se excluyeron uno por no cumplir criterios de inclusión, 4 por presentar un FEV1<50% y 21 por no proporcionar valores completos de las pruebas espirométricas. De esta forma, la población del estudio fue de 173 participantes, 94 controles y 79 casos. Cabe destacar que, de los 79 casos, 6 no tenían diagnóstico previo de EPOC.
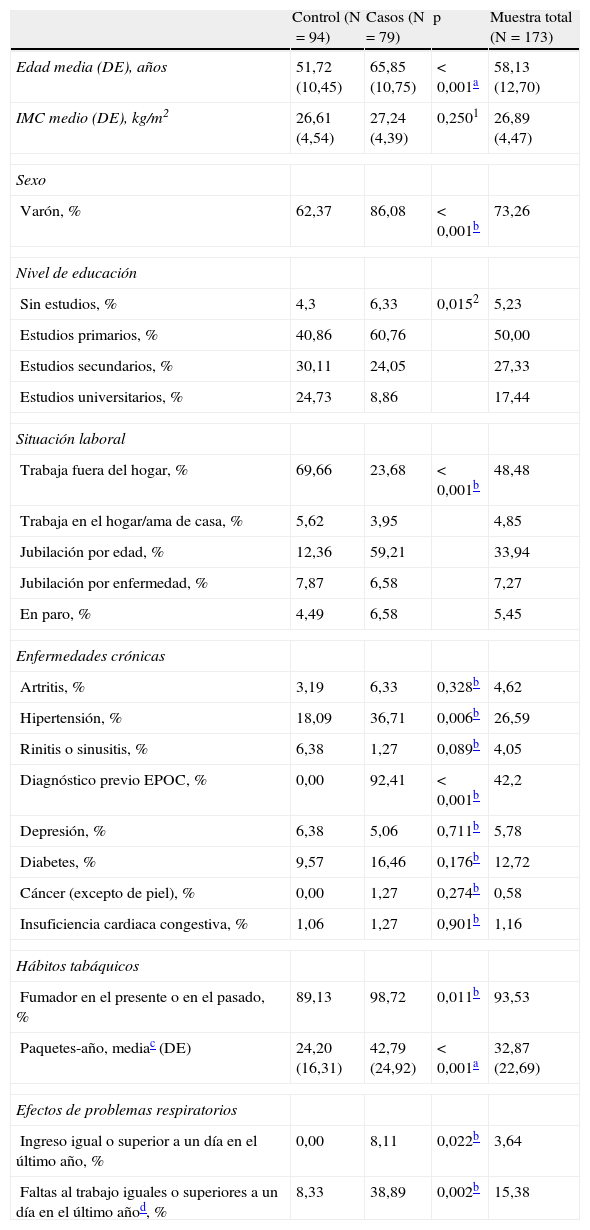
La mayoría de los participantes fueron varones (73%) y la edad media (DE) fue de 58 (12,7) años. El 94% de la muestra eran fumadores y el número medio de paquetes-año fue de 32,8 (22,7). Existieron diferencias estadísticamente significativas entre los grupos control y casos para la edad, sexo, nivel de educación, situación laboral, hipertensión, hábito tabáquico e impacto de la enfermedad respiratoria (tabla 1).
Datos sociodemográficos y clínicos básicos
| Control (N=94) | Casos (N=79) | p | Muestra total (N=173) | |
| Edad media (DE), años | 51,72 (10,45) | 65,85 (10,75) | < 0,001a | 58,13 (12,70) |
| IMC medio (DE), kg/m2 | 26,61 (4,54) | 27,24 (4,39) | 0,2501 | 26,89 (4,47) |
| Sexo | ||||
| Varón, % | 62,37 | 86,08 | < 0,001b | 73,26 |
| Nivel de educación | ||||
| Sin estudios, % | 4,3 | 6,33 | 0,0152 | 5,23 |
| Estudios primarios, % | 40,86 | 60,76 | 50,00 | |
| Estudios secundarios, % | 30,11 | 24,05 | 27,33 | |
| Estudios universitarios, % | 24,73 | 8,86 | 17,44 | |
| Situación laboral | ||||
| Trabaja fuera del hogar, % | 69,66 | 23,68 | < 0,001b | 48,48 |
| Trabaja en el hogar/ama de casa, % | 5,62 | 3,95 | 4,85 | |
| Jubilación por edad, % | 12,36 | 59,21 | 33,94 | |
| Jubilación por enfermedad, % | 7,87 | 6,58 | 7,27 | |
| En paro, % | 4,49 | 6,58 | 5,45 | |
| Enfermedades crónicas | ||||
| Artritis, % | 3,19 | 6,33 | 0,328b | 4,62 |
| Hipertensión, % | 18,09 | 36,71 | 0,006b | 26,59 |
| Rinitis o sinusitis, % | 6,38 | 1,27 | 0,089b | 4,05 |
| Diagnóstico previo EPOC, % | 0,00 | 92,41 | < 0,001b | 42,2 |
| Depresión, % | 6,38 | 5,06 | 0,711b | 5,78 |
| Diabetes, % | 9,57 | 16,46 | 0,176b | 12,72 |
| Cáncer (excepto de piel), % | 0,00 | 1,27 | 0,274b | 0,58 |
| Insuficiencia cardiaca congestiva, % | 1,06 | 1,27 | 0,901b | 1,16 |
| Hábitos tabáquicos | ||||
| Fumador en el presente o en el pasado, % | 89,13 | 98,72 | 0,011b | 93,53 |
| Paquetes-año, mediac (DE) | 24,20 (16,31) | 42,79 (24,92) | < 0,001a | 32,87 (22,69) |
| Efectos de problemas respiratorios | ||||
| Ingreso igual o superior a un día en el último año, % | 0,00 | 8,11 | 0,022b | 3,64 |
| Faltas al trabajo iguales o superiores a un día en el último añod, % | 8,33 | 38,89 | 0,002b | 15,38 |
EPOC: enfermedad pulmonar obstructiva crónica; IMC: índice de masa corporal.
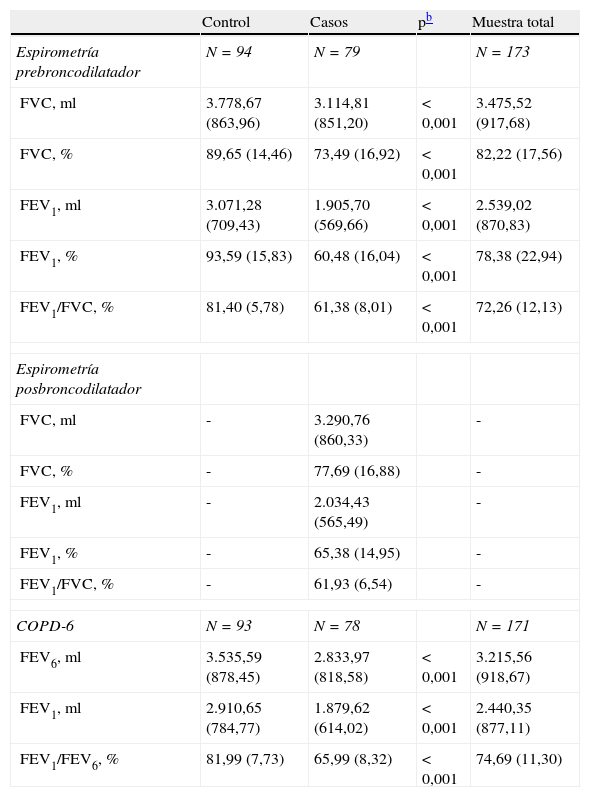
La espirometría mostró un FEV1 medio del 78,4 (22,9) %, con diferencias significativas entre casos y controles (60,5 frente a 93,6%; p<0,001) (tabla 2). También los valores obtenidos con el COPD-6 fueron significativamente distintos para casos y controles (FEV1/FEV6 en casos del 65,9% frente al 81,9% en controles; p<0,001) (tabla 2).
Descriptivos de las pruebas espirométricasa
| Control | Casos | pb | Muestra total | |
| Espirometría prebroncodilatador | N=94 | N=79 | N=173 | |
| FVC, ml | 3.778,67 (863,96) | 3.114,81 (851,20) | < 0,001 | 3.475,52 (917,68) |
| FVC, % | 89,65 (14,46) | 73,49 (16,92) | < 0,001 | 82,22 (17,56) |
| FEV1, ml | 3.071,28 (709,43) | 1.905,70 (569,66) | < 0,001 | 2.539,02 (870,83) |
| FEV1, % | 93,59 (15,83) | 60,48 (16,04) | < 0,001 | 78,38 (22,94) |
| FEV1/FVC, % | 81,40 (5,78) | 61,38 (8,01) | < 0,001 | 72,26 (12,13) |
| Espirometría posbroncodilatador | ||||
| FVC, ml | - | 3.290,76 (860,33) | - | |
| FVC, % | - | 77,69 (16,88) | - | |
| FEV1, ml | - | 2.034,43 (565,49) | - | |
| FEV1, % | - | 65,38 (14,95) | - | |
| FEV1/FVC, % | - | 61,93 (6,54) | - | |
| COPD-6 | N=93 | N=78 | N=171 | |
| FEV6, ml | 3.535,59 (878,45) | 2.833,97 (818,58) | < 0,001 | 3.215,56 (918,67) |
| FEV1, ml | 2.910,65 (784,77) | 1.879,62 (614,02) | < 0,001 | 2.440,35 (877,11) |
| FEV1/FEV6, % | 81,99 (7,73) | 65,99 (8,32) | < 0,001 | 74,69 (11,30) |
FEV1: volumen espiratorio forzado en el primer segundo; FEV6: volumen espiratorio forzado en 6 segundos; FVC: capacidad vital forzada.
En el análisis de factibilidad del cuestionario se encontró que los ítems 1-3 fueron contestados por los 173 participantes, mientras que el ítem 4 no fue contestado por 2 participantes del grupo control, y el ítem 5 por uno del grupo control y otro del grupo de casos. Esto supone para los ítems 4 y 5 un porcentaje de no respuesta del 1,16% de la muestra total. El porcentaje de sujetos que no respondieron a algún ítem fue del 2,31%. En cuanto a los efectos suelo y techo, 7 participantes del grupo control obtuvieron la mínima puntuación en el cuestionario, lo que supone un 4,14% de la muestra total. Ningún participante obtuvo la puntuación máxima. El tiempo medio de cumplimentación fue de 47,7 (37,6) segundos, con un tiempo de cumplimentación máximo de 180 segundos.
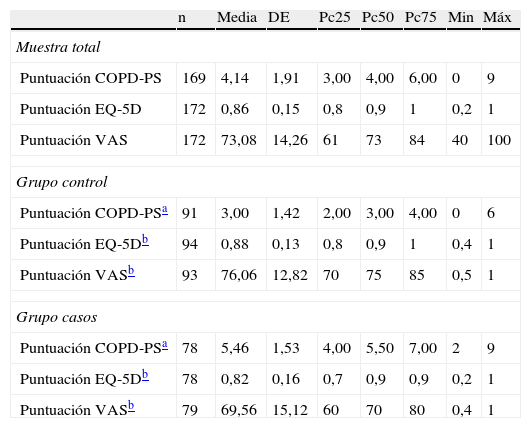
Las puntuaciones obtenidas en cuestionario COPD-PS se muestran en la tabla 3. Existieron diferencias estadísticamente significativas entre los grupos control y casos (3,0 frente a 5,46; p<0,01); destaca que la puntuación máxima en el grupo control fue de 6. También la calidad de vida medida por el EQ-5D fue significativamente peor para los casos que los controles (tabla 3).
Descriptivos de las puntuaciones en los cuestionarios
| n | Media | DE | Pc25 | Pc50 | Pc75 | Min | Máx | |
| Muestra total | ||||||||
| Puntuación COPD-PS | 169 | 4,14 | 1,91 | 3,00 | 4,00 | 6,00 | 0 | 9 |
| Puntuación EQ-5D | 172 | 0,86 | 0,15 | 0,8 | 0,9 | 1 | 0,2 | 1 |
| Puntuación VAS | 172 | 73,08 | 14,26 | 61 | 73 | 84 | 40 | 100 |
| Grupo control | ||||||||
| Puntuación COPD-PSa | 91 | 3,00 | 1,42 | 2,00 | 3,00 | 4,00 | 0 | 6 |
| Puntuación EQ-5Db | 94 | 0,88 | 0,13 | 0,8 | 0,9 | 1 | 0,4 | 1 |
| Puntuación VASb | 93 | 76,06 | 12,82 | 70 | 75 | 85 | 0,5 | 1 |
| Grupo casos | ||||||||
| Puntuación COPD-PSa | 78 | 5,46 | 1,53 | 4,00 | 5,50 | 7,00 | 2 | 9 |
| Puntuación EQ-5Db | 78 | 0,82 | 0,16 | 0,7 | 0,9 | 0,9 | 0,2 | 1 |
| Puntuación VASb | 79 | 69,56 | 15,12 | 60 | 70 | 80 | 0,4 | 1 |
COPD-PS: Chronic Obstructive Pulmonary Disease-Population Screener; DE: desviación estándar; Máx: máximo; Min: mínimo; Pc: percentil.
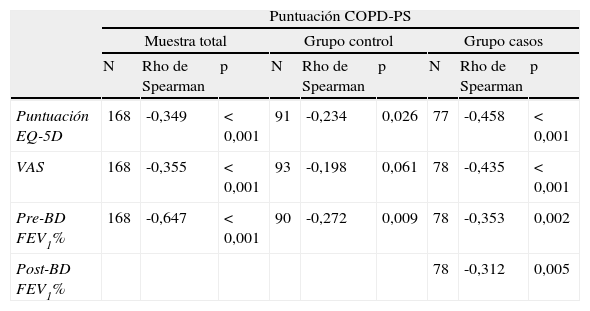
Para el análisis de la validez convergente se estudió la correlación entre la puntuación del COPD-PS, el cuestionario genérico EQ-5D y su escala analógica visual (tabla 4). La correlación observada en ambos análisis fue significativa pero moderada (rho=−0,349, p<0,001; y rho=−0,355, p<0,001).
Validez convergente y validez discriminante
| Puntuación COPD-PS | |||||||||
| Muestra total | Grupo control | Grupo casos | |||||||
| N | Rho de Spearman | p | N | Rho de Spearman | p | N | Rho de Spearman | p | |
| Puntuación EQ-5D | 168 | -0,349 | < 0,001 | 91 | -0,234 | 0,026 | 77 | -0,458 | < 0,001 |
| VAS | 168 | -0,355 | < 0,001 | 93 | -0,198 | 0,061 | 78 | -0,435 | < 0,001 |
| Pre-BD FEV1% | 168 | -0,647 | < 0,001 | 90 | -0,272 | 0,009 | 78 | -0,353 | 0,002 |
| Post-BD FEV1% | 78 | -0,312 | 0,005 | ||||||
| N | Media (DE) | pa | |
| Clasificación final | |||
| Control | 91 | 3,00 (1,42) | <0,001 |
| Caso | 78 | 5,46 (1,53) | |
| Ingresos hospitalarios | |||
| No | 155 | 3,97 (1,80) | <0,001 |
| Sí | 6 | 7,17 (1,17) | |
| Faltas trabajo | |||
| No | 64 | 3,00 (1,52) | 0,001 |
| Sí | 12 | 4,58 (1,93) | |
COPD-PS: Chronic Obstructive Pulmonary Disease-Population Screener; DE: desviación estándar; FEV1: volumen espiratorio forzado en el primer segundo.
La validez discriminante se estudió mediante la correlación de la puntuación del cuestionario COPD-PS con el FEV1(%). Esta correlación fue significativa y moderada-alta (rho=−0,647, p<0,001); además, existió una correlación significativa y moderada entre la puntuación del cuestionario y el FEV1(%) para los grupos control y casos por separado. A continuación se estudió la relación entre la puntuación del cuestionario y otros parámetros clínicos relacionados con la enfermedad (tabla 4). Se detectó una diferencia significativa en la puntuación media en el cuestionario entre controles y casos, entre participantes con o sin ingresos hospitalarios en el último año debido a problemas respiratorios, y entre participantes con o sin faltas al trabajo en el último año debido a problemas respiratorios. La media en el cuestionario fue siempre significativamente mayor para aquellos grupos con condiciones relacionadas con EPOC.
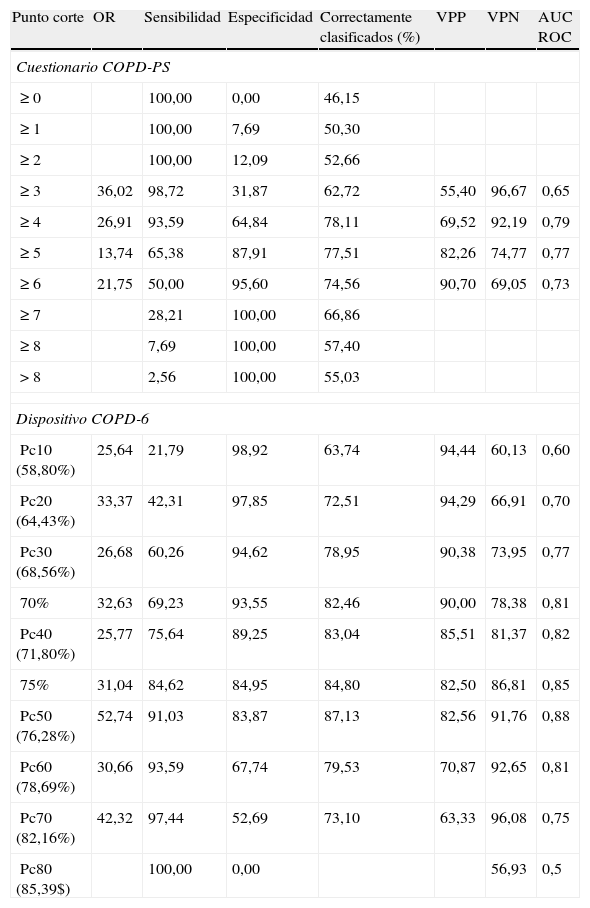
Para la utilización práctica del cuestionario es preciso determinar un punto de corte que nos permita clasificar con la máxima fiabilidad a cada individuo como posible caso de EPOC o normal. En la tabla 5 se muestra el análisis realizado para evaluar el rendimiento del cuestionario en la predicción de EPOC para los diferentes puntos de corte posibles. Los puntos de corte 4 y 5 presentaron un buen balance entre sensibilidad y especificidad, y permitieron la correcta clasificación del 78% de los participantes. Para una prueba de cribado preferimos el 4, ya que ofrece una mayor sensibilidad que el 5 (93,59 frente a 65,38%), aun a costa de una menor especificidad (64,84 frente a 87,91%). Con este punto de corte, existe una asociación moderada entre la clasificación obtenida por el cuestionario y aquella según espirometría y con haber faltado al trabajo debido a problemas respiratorios (tabla 6). En la figura 2 se presenta la curva ROC para las distintas puntuaciones del cuestionario tomando como patrón de referencia la clasificación según espirometría.
Características de los diferentes puntos de corte del cuestionario COPD-PS y para el dispositivo COPD-6 en la predicción de la clasificación según pruebas espirométricas
| Punto corte | OR | Sensibilidad | Especificidad | Correctamente clasificados (%) | VPP | VPN | AUC ROC |
| Cuestionario COPD-PS | |||||||
| ≥ 0 | 100,00 | 0,00 | 46,15 | ||||
| ≥ 1 | 100,00 | 7,69 | 50,30 | ||||
| ≥ 2 | 100,00 | 12,09 | 52,66 | ||||
| ≥ 3 | 36,02 | 98,72 | 31,87 | 62,72 | 55,40 | 96,67 | 0,65 |
| ≥ 4 | 26,91 | 93,59 | 64,84 | 78,11 | 69,52 | 92,19 | 0,79 |
| ≥ 5 | 13,74 | 65,38 | 87,91 | 77,51 | 82,26 | 74,77 | 0,77 |
| ≥ 6 | 21,75 | 50,00 | 95,60 | 74,56 | 90,70 | 69,05 | 0,73 |
| ≥ 7 | 28,21 | 100,00 | 66,86 | ||||
| ≥ 8 | 7,69 | 100,00 | 57,40 | ||||
| > 8 | 2,56 | 100,00 | 55,03 | ||||
| Dispositivo COPD-6 | |||||||
| Pc10 (58,80%) | 25,64 | 21,79 | 98,92 | 63,74 | 94,44 | 60,13 | 0,60 |
| Pc20 (64,43%) | 33,37 | 42,31 | 97,85 | 72,51 | 94,29 | 66,91 | 0,70 |
| Pc30 (68,56%) | 26,68 | 60,26 | 94,62 | 78,95 | 90,38 | 73,95 | 0,77 |
| 70% | 32,63 | 69,23 | 93,55 | 82,46 | 90,00 | 78,38 | 0,81 |
| Pc40 (71,80%) | 25,77 | 75,64 | 89,25 | 83,04 | 85,51 | 81,37 | 0,82 |
| 75% | 31,04 | 84,62 | 84,95 | 84,80 | 82,50 | 86,81 | 0,85 |
| Pc50 (76,28%) | 52,74 | 91,03 | 83,87 | 87,13 | 82,56 | 91,76 | 0,88 |
| Pc60 (78,69%) | 30,66 | 93,59 | 67,74 | 79,53 | 70,87 | 92,65 | 0,81 |
| Pc70 (82,16%) | 42,32 | 97,44 | 52,69 | 73,10 | 63,33 | 96,08 | 0,75 |
| Pc80 (85,39$) | 100,00 | 0,00 | 56,93 | 0,5 | |||
AUC: área bajo la curva ROC; OR: odds ratio; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
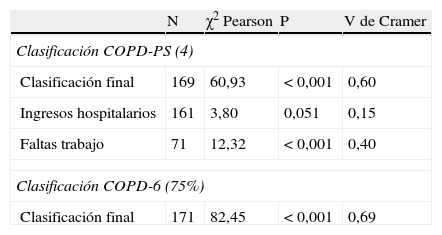
Análisis de la asociación de la clasificación según cuestionario COPD-PS con punto de corte 4 y según punto de corte 75% para el dispositivo COPD-6 con diferentes variables relacionadas con enfermedad pulmonar obstructiva crónica
| N | χ2 Pearson | P | V de Cramer | |
| Clasificación COPD-PS (4) | ||||
| Clasificación final | 169 | 60,93 | < 0,001 | 0,60 |
| Ingresos hospitalarios | 161 | 3,80 | 0,051 | 0,15 |
| Faltas trabajo | 71 | 12,32 | < 0,001 | 0,40 |
| Clasificación COPD-6 (75%) | ||||
| Clasificación final | 171 | 82,45 | < 0,001 | 0,69 |
COPD-PS: Chronic Obstructive Pulmonary Disease-Population Screener.
También se intentó establecer un punto de corte para el cociente FEV1/FEV6 medido por el dispositivo COPD-6 en la predicción de EPOC, utilizando los correspondientes percentiles. Como se puede observar en la tabla 5, para un valor del 76,28% (Pc50) se obtiene un buen balance entre sensibilidad y especificidad y se clasifica correctamente el 87% de los casos. En la misma tabla se presentan también las propiedades de los puntos de corte 70% (el propuesto por el fabricante) y 75% (cercano al Pc50 y que se consideró más intuitivo cara a su uso en la práctica clínica habitual). En la tabla 6 se muestra la existencia de una asociación moderada-fuerte entre la clasificación según el dispositivo COPD-6 con punto de corte 75% y la clasificación según prueba espirométrica.
En un grupo de 30 participantes se estudió la correlación intraclase entre la puntuación en el COPD-PS en la visita inicial y a las 2 semanas. Para la muestra total, el CCI fue 0,94 con una media en el test de 4,07 (1,60) y en el retest de 4,17 (1,46). Para el subgrupo de 16 controles, el CCI fue 0,89, con una media en el test de 3,31 (1,35) y en el retest de 3,44 (1,26). Para el subgrupo de 14 casos el CCI fue 0,94, con una media en test de 4,93 (1,44) y en el retest de 5,00 (1,24).
DiscusiónLa versión traducida y culturalmente adaptada del COPD-PS ha demostrado presentar óptimas características psicométricas para su utilización como prueba de cribado de EPOC en AP. Con un punto de corte de 4 podemos clasificar de forma adecuada a un 78% de los individuos, con una sensibilidad del 93,6%; es decir, tan solo un 6,4% de posibles casos de EPOC pasarían inadvertidos al usar este valor discriminante.
La utilización de cuestionarios de cribado para la EPOC está justificada por la elevada prevalencia de la enfermedad y su alto índice de infradiagnóstico2. Estos cuestionarios nunca sustituirán a la espirometría, pero permiten seleccionar a aquellos sujetos que tienen un mayor riesgo de sufrir la enfermedad y, sobre todo, descartar con la máxima fiabilidad a aquellos que no precisan espirometría por su escasísimo riesgo de tener una EPOC1.
El COPD-PS es un cuestionario desarrollado en EE.UU. de tan solo 5 preguntas y que se completa en un tiempo medio de unos 45 segundos. Fue diseñado en EE.UU. para facilitar el autodiagnóstico, al utilizarlo en campañas publicitarias en las que se estimulaba su uso por la población y se aconsejaba acudir al médico de cabecera en caso de un resultado positivo. El cuestionario incluye preguntas relativas a la edad, el hábito tabáquico, la disnea, la actividad y la tos con expectoración, que son la mayoría de las preguntas identificadas como predictores importantes de EPOC12. En su versión inicial en inglés se escogió un punto de corte de 5, que ofrecía una sensibilidad del 84,4% y una especificidad del 60,7% y clasificaba de forma correcta al 69,7% de los individuos4. En nuestra población, hemos observado que el mejor punto de corte es el 4, ya que permite una mayor sensibilidad, que es la característica principal de un instrumento de cribado (evitar que personas con la enfermedad no sean detectadas), aun a costa de perder algo de especificidad (sospechar la enfermedad en individuos sanos). Con el punto de corte de 4 clasificamos de forma correcta al 78% de los participantes en nuestro estudio.
El cuestionario presenta una adecuada factibilidad, el porcentaje de no respuesta a cada ítem y el de sujetos que no respondieron algún ítem del cuestionario fue muy inferior al 5%. No existe efecto techo y el efecto suelo es mínimo y observado solo en sujetos del grupo control, como era esperable. En la gran mayoría de casos, el tiempo medio de cumplimentación fue inferior a un minuto, tiempo que lo hace compatible con la dinámica de la práctica clínica habitual en AP. Presenta también una adecuada validez convergente, ya que las correlaciones con ambas puntuaciones del cuestionario EQ-5D son significativas y en la dirección esperada. Ofrece una buena validez discriminante, observándose diferencias de medias en las puntuaciones de acuerdo a los parámetros clínicos indicativos de EPOC. La buena correlación con el FEV1(%) indica que la puntuación del cuestionario no solo permite distinguir entre individuos con EPOC o sanos, sino que correlaciona con la gravedad de la afección pulmonar. El cuestionario se ha demostrado fiable, siendo alta la reproducibilidad en las respuestas, con unos coeficientes de correlación muy elevados tanto para la muestra total, como para los subgrupos de controles y casos. En la adaptación y validación se han seguido todos los pasos exigibles en este tipo de estudios13.
Los cuestionarios de cribado se han mostrado útiles en detectar obstrucción al flujo aéreo en individuos adultos con factores de riesgo. La mayoría incluyen preguntas sobre el hábito tabáquico y síntomas respiratorios, pero existen grandes diferencias en el uso de información demográfica, historia personal u otros tipos de información3. Price et al.14,15 desarrollaron un cuestionario con 8 ítems para la detección de EPOC en AP. Utilizando 2 puntos de corte distintos, su sensibilidad oscilaba entre el 58,7 y el 80,4%, aunque en un estudio posterior de validación obtuvo una pobre discriminación entre sujetos con EPOC y sanos (área bajo la curva ROC de 0,65), lo que ponía en duda su utilidad práctica16. Kida et al.17 diseñaron un cuestionario de 11 ítems para la detección de EPOC. Con este instrumento consiguieron una especificidad del 76,8% y una sensibilidad del 66,7%, con un área bajo la curva ROC de 0,69, inferiores a las conseguidas en nuestro estudio. Mejores resultados ofrece el Personal level screener for COPD, que consta de 8 ítems, en su mayoría de respuesta dicotómica «sí/no», y que en una muestra reducida de individuos consiguió clasificar correctamente al 86,5% de los casos, con una sensibilidad del 92% y una especificidad del 72,4%18. Más recientemente, Yawn et al.19 han propuesto un cuestionario de 5 ítems que incluyen la edad, historia de tabaquismo, presencia de sibilantes, disnea y expectoración; ofrece una sensibilidad del 58,2% y una especificidad del 73,2%, con un área bajo la curva ROC de 0,72. De la revisión de los resultados obtenidos con una muestra de los cuestionarios existentes, se deduce que las propiedades de la versión española del COPD-PS son óptimas, superiores a las de la mayoría de cuestionarios existentes previamente y solo comparables a las observadas con el «Personal level screener for COPD»18, que tiene 3 ítems más que el COPD-PS.
Una estrategia diferente para la detección de EPOC en población general es la utilización de la espirometría en las consultas de AP. Está fuera de toda duda la eficacia de esta medida en la detección de personas afectadas por una obstrucción al flujo aéreo que estaban indiagnosticadas20,21, y además la utilización de la espirometría en AP puede resultar en una mejoría en las pautas de tratamiento y seguimiento de la EPOC en este ámbito22. Sin embargo, esta estrategia no está exenta de polémica por la dificultad que entraña la correcta realización de la prueba y el tiempo que precisa, que en muchas ocasiones supera el disponible para la atención a los pacientes en las consultas23. A pesar de que se ha demostrado que con los medios adecuados es factible la realización de espirometrías de calidad en AP24, las dificultades del día a día hacen que, con el tiempo, el número de exploraciones realizadas vaya disminuyendo de forma progresiva y deje de utilizarse de forma habitual25. En cualquier caso, el problema técnico más frecuente en la realización de la espirometría tiene relación con la terminación de la espiración forzada, que puede dar lugar a falsos negativos al ofrecer un valor de FVC falsamente bajo, con un cociente resultante FEV1/FVC que puede ser normal en presencia de obstrucción5. En un estudio previo de cribado se observó que entre la espirometría en AP y la realizada por el laboratorio de función pulmonar existía una buena concordancia para el FEV1 (r=0,78), pero mala para la FVC (r=0,47)20. Para intentar solventar este problema se ha propuesto la utilización del cociente FEV1/FEV66,26,27. En un trabajo previo se observó una excelente concordancia entre el FVC y el FEV66, y en un metaanálisis reciente, el cociente FEV1/FEV6 ofrecía una sensibilidad del 89% y una especificidad del 98% para el diagnóstico de obstrucción con respecto al cociente FEV1/FVC7. En nuestro estudio hemos utilizado un dispositivo portátil COPD-6 de sencillo manejo para evaluar la utilidad del FEV1/FEV6 en la muestra estudiada. Nuestros resultados indican que un cociente FEV1/FEV6 < 0,75 permite clasificar correctamente al 82,4% de los individuos como portadores de obstrucción crónica al flujo aéreo. Este punto de corte es el mismo que recomiendan Rosa et al.26 y está en el intervalo de los distintos estudios (0,70 a 0,76)7; se ha demostrado que valores superiores, como 0,80, no ofrecen una adecuada discriminación28.
En resumen, hemos investigado la validez de 2 métodos distintos para el cribado de EPOC en AP. El cuestionario COPD-PS, utilizando un punto de corte de 4, ha demostrado ser un instrumento fiable, válido y fácil de administrar. El cociente FEV1/FEV6 medido mediante el espirómetro portátil COPD-6, con un punto de corte de 0,75, es también un instrumento útil para la detección de obstrucción al flujo aéreo. No hay que olvidar que estos métodos se han validado frente al patrón de referencia, que es la obstrucción al flujo aéreo demostrada por un FEV1/FVC posbroncodilatador < 0,7, pero el diagnóstico de EPOC es algo más que la espirometría y requiere una evaluación clínica adicional29. En cualquier caso, la utilización de uno u otro método dependerá de las posibilidades de cada centro, pero sin duda pueden ayudar a paliar el elevado infradiagnóstico de la EPOC y conseguir que se pueda detectar a los pacientes en estadios más tempranos, cuando las medidas preventivas, como la cesación del hábito tabáquico y la correcta utilización de los inhaladores, tendrán un mayor impacto sobre el pronóstico a largo plazo29–32.
Conflicto de interesesEl presente estudio ha sido financiado por Boehringer Ingelheim España S. A.y Pfizer S.A.
Los autores quieren agradecer la colaboración de los investigadores del estudio: Agustín Martínez González, Centro de Salud La Paz, Cruces-Barakaldo; Álvaro Pérez Martín, Centro de Salud Los Valles, Mataporquera; Ana Moragas Moreno, Carles Llor Vilà, Silvia Hernández Anadón, Centro de Salud Jaume I, Tarragona; Araceli Fernández Revuelta, Centro de Salud Delicias Sur, Zaragoza; Eduardo Calvo, Centro de Salud Universitario Pozuelo 1, Pozuelo de Alarcón, Enric Hernández Huet, Centro de Salud Corró D’Avall, Les Franqueses del Vallés; José Ignacio Sánchez González, Centro de Salud Fuente de San Luis, Valencia; José Miguel Solís de Dios, Centro de Salud Mairena del Aljarafe; Manuel Espigares Arroyo, Centro de Salud La Paz, Badajoz.