La presencia de múltiples imágenes puntiformes hiperintensas en la sustancia blanca (IPHSB) en las secuencias de resonancia magnética (RM) ponderadas en T2 es un hallazgo muy frecuente y, en ocasiones, un reto diagnóstico para el radiólogo.
Este artículo pretende, a través de una aproximación a la anatomía de la microcirculación cerebral, así como a estudios de correlación anatomopatológica, simplificar la tarea de interpretación de estas imágenes a partir de la descripción de tres principales patrones de presentación de IPHSB: patrón vascular (PV), que corresponde a lesiones microvasculares, patrón perivascular (PpV), que representa a la enfermedad inflamatoria cuyo paradigma es la esclerosis múltiple (EM), y patrón inespecífico (PI), que suele deberse a enfermedad microvascular.
A partir de varios elementos semiológicos en las imágenes de RM se puede determinar un patrón predominante en cada caso y, de este modo, acotar el diagnóstico diferencial.
The presence of hyperintense punctiform images in the white matter in T2 weighted magnetic resonance (MR) sequences is a very common finding and is occasionally a diagnostic challenge for the radiologist.
The present article attempts, using an anatomical approach to the brain circulation, as well as from histopathology correlation studies, to simplify the task of interpreting these images from the description of the three main patterns of hyperintense punctiform images in the white matter: vascular pattern, which corresponds to microvascular lesions; perivascular pattern, which represents inflammatory disease of which the paradigm is multiple sclerosis; and a non-specific pattern, which has to be a microvascular disease.
From the various semiological elements in the MR images, a predominant pattern can be determined in each case and, in this way, helps in the differential diagnosis.
La interpretación de las imágenes puntiformes hiperintensas múltiples en las secuencias ponderadas en T2 en la sustancia blanca cerebral, que se detectan a diario en los estudios de la resonancia magnética (RM) cerebral del adulto, ocupa una parcela muy importante en la práctica habitual del neurorradiólogo.
Haciendo un paralelismo con el término unidentified bright objects (UBO), común en la bibliografía inglesa1, presentamos el término «imágenes puntiformes hiperintensas en la sustancia blanca» (IPHSB), como una entidad semiológica que incluye cualquier caso en que contabilicen al menos 5 focos hiperintensos únicos de hasta un centímetro de diámetro máximo en las imágenes de RM obtenidas con secuencias ponderadas en T2, con o sin lesiones confluentes con un diámetro superior a un centímetro conjuntamente.
El principal objetivo de este artículo es tratar de facilitarel trabajo del radiólogo ante los casos de IPHSB para que pueda encuadrarlos hallazgos dentro de un patrón predominante, de manera que la orientación diagnóstica sea más aproximada. Hemos definido tres principales patrones de IPHSB en función de sus características semiológicas: un patrón vascular (PV), que representa a la afección microvascular (que suele ser arteriolar); un patrón perivascular (PpV), que representa a la enfermedad inflamatoria (sobre todo desmielinizante); y un patrón inespecífico (PI), que suele representar a la enfermedad microvascular. El patrón semiológico predominante debe considerarse junto con el contexto clínico del paciente y los datos epidemiológicos para emitir un juicio diagnóstico.
Anatomía básica de la microcirculación cerebralLa microcirculación cerebral conforma una red vascular de anatomía muy compleja y variable según los individuos. Para tratar de entender los patrones de IPHSB propuestos es útil una aproximación básica a la anatomía microvascular cerebral.
Sistema microvascular arterialLas arterias corticales atraviesan la corteza cerebral y profundizan en la sustancia blanca perpendicularmente a la superficie cortical, formando arteriolas terminales piales o medulares de hasta 4-5cm. En su camino dan ramas cortas corticales que irrigan todo el espesor de la corteza cerebral y las fibras de sustancia blanca yuxtacortical (3-4mm), también denominadas fibras en «U», y establecen múltiples anastomosis que proporcionan a la corteza cerebral una rica red arteriolar. Las arterias piales, en su trayecto profundo en la sustancia blanca, establecen muy pocas anastomosis capilares con las arteriolas piales vecinas, constituyendo unidades metabólicas arteriolares relativamente independientes.
Por otro lado, las arterias profundas subependimarias, que tienen su origen en las arterias coroideas, dan ramas penetrantes hacia la sustancia blanca, aunque su trayecto es más corto que el de las arterias piales.
Existe un segundo sistema terminal de arterias corticales y subependimarias (arterias lentículo-estriadas y tálamo-perforantes) que irrigan a los ganglios basales (GB).
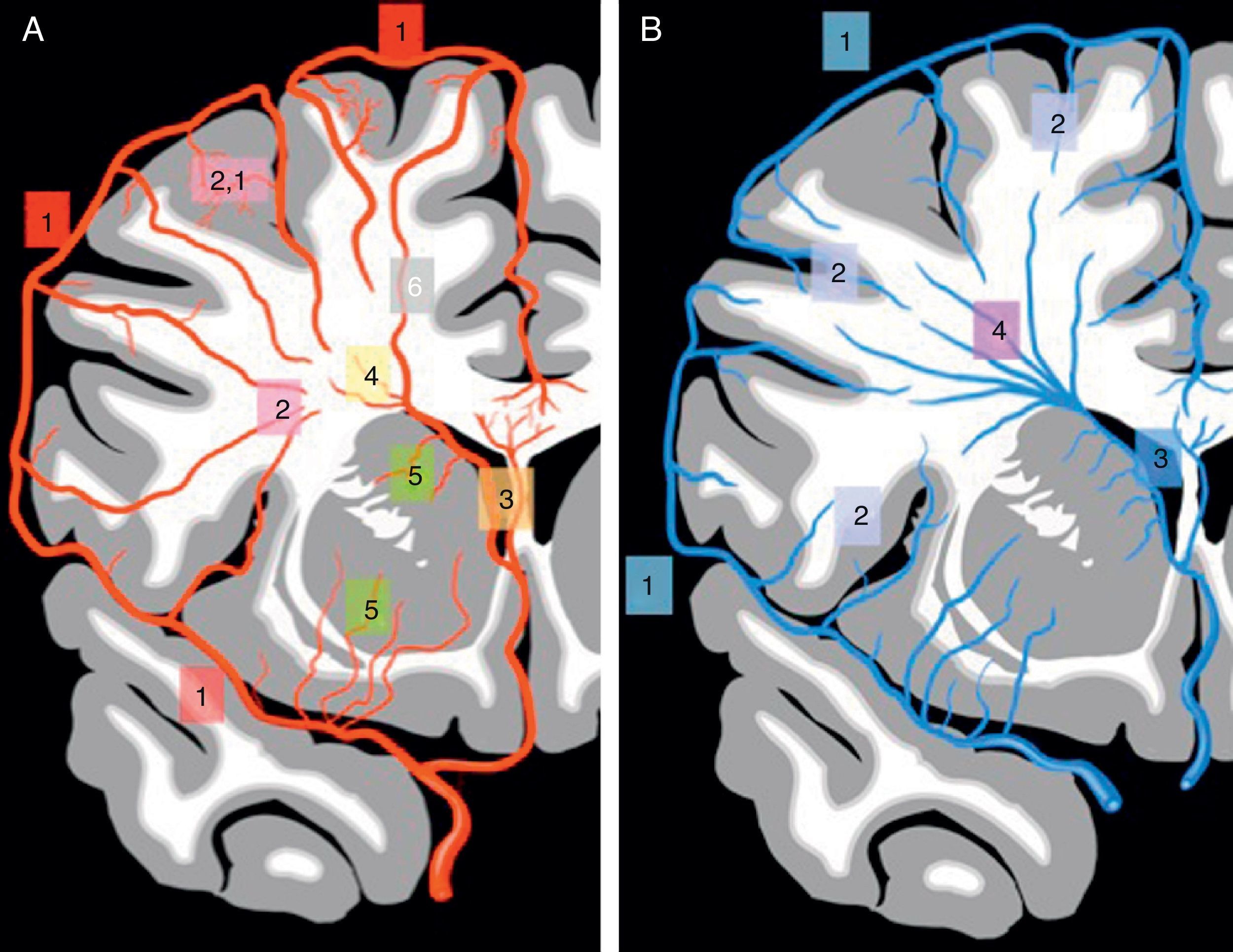
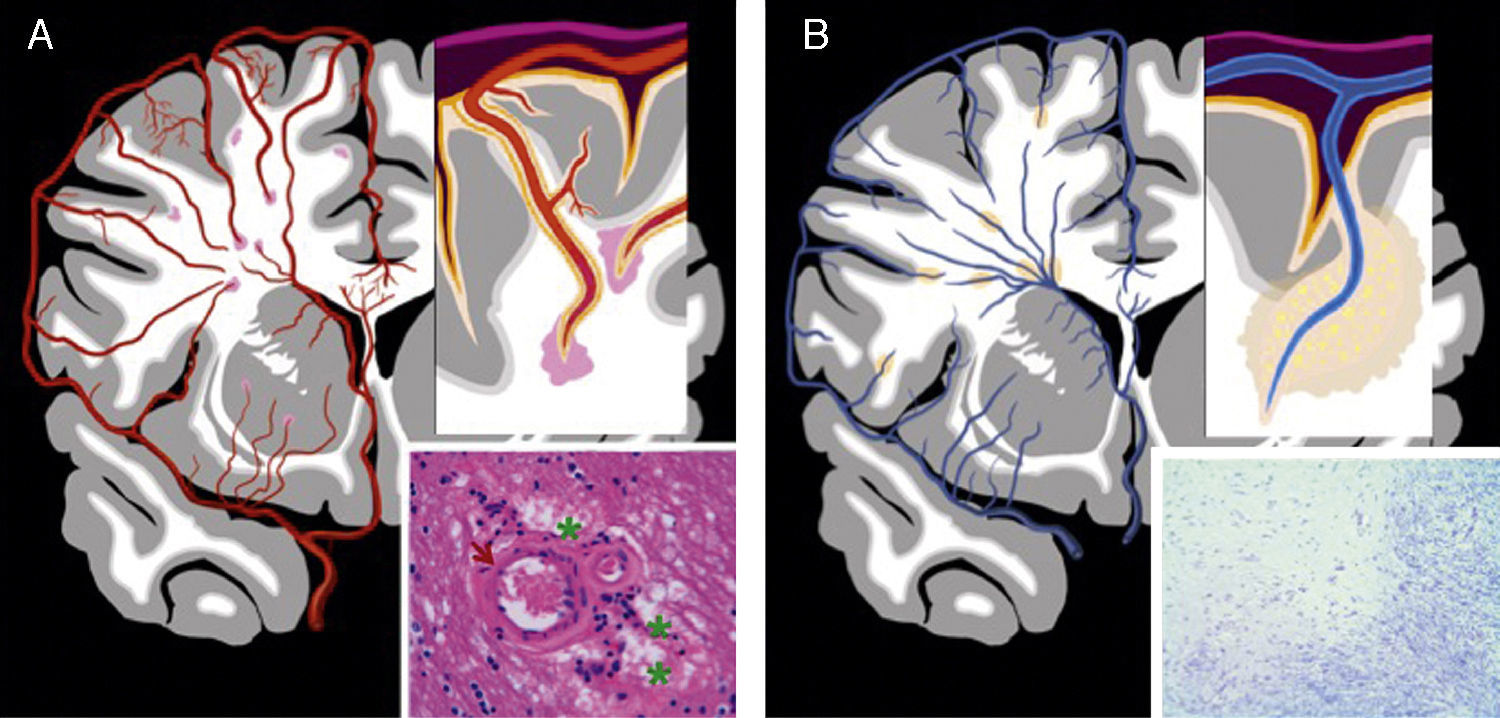
Entre los sistemas arteriolares superficiales y profundos (arterias penetrantes piales y subependimarias) existen muy pocas anastomosis. Así pues, el parénquima situado en las áreas limítrofes entre la circulación superficial y profunda está menos vascularizado, mientras que las fibras en «U» presentan una mayor y mejor vascularización que el resto de la sustancia blanca y que los GB2,3 (fig. 1A).
Microcirculación cerebral. A) microcirculación arterial. 1: arterias corticales; 2: arteriolas piales; 2.1: ramas cortas; 3: arterias subependimarias; 4: arteriolas perforantes subependimarias; 5: arteriolas lentículo-estriadas y tálamo-perforantes; 6: arteriola transcerebral. B) microcirculación venosa. 1: venas corticales; 2: vénulas medulares superficiales; 3: vénulas subependimarias; 4: vénulas medulares profundas.
Las vénulas cerebrales, también llamadas vénulas medulares, se dividen en dos grandes grupos: vénulas medulares superficiales, que son canales venosos cortos que desde aproximadamente 1 o 2 cm por debajo de la corteza cerebral drenan hacia la superficie cortical; y las vénulas medulares profundas, que son canales más largos que drenan perpendicularmente a la superficie ventricular, hacia las venas subependimarias. Existe un tercer grupo de vénulas transcerebrales, más escasas, que comunican ambos sistemas2,4 (fig. 1B).
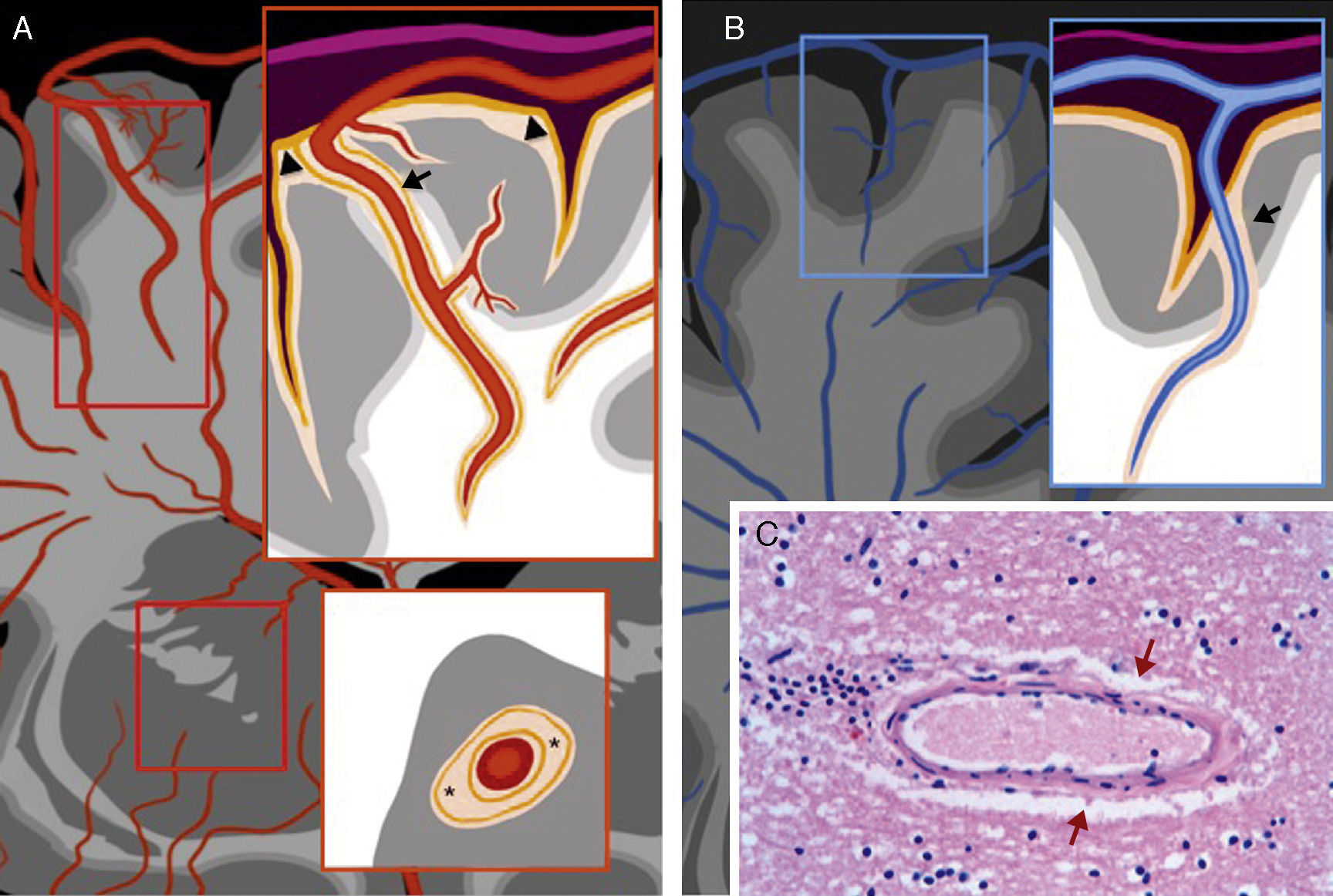
Espacio perivascularLos sistemas arterial y venoso son anatómicamente bastante paralelos. El espacio perivascular rodea la pared de arterias y arteriolas (espacio de Virchow-Robin), y la de venas y vénulas (espacio perivenular), desde el espacio subaracnoideo hasta su trayecto intraparenquimatoso. Las arteriolas superficiales o corticales están rodeadas por una hoja leptomeníngea que delimita la superficie vascular del espacio periarteriolar; la superficie parenquimatosa de este espacio está delimitado por la piamadre. El endotelio de las arteriolas penetrantes de los GB está rodeado por dos capas leptomeníngeas que delimitan su espacio perivascular. El espacio perivenular, tanto superficial como profundo, aparentemente comunica directamente con el espacio subpial, sin hojas leptomeníngeas interpuestas (fig. 2)5,6.
Espacio perivascular. A) Espacio periarteriolar de las arteriolas piales, envuelto por una hoja leptomeníngea que lo separa del espacio subpial (flecha). Espacio periarteriolar de arteriolas lentículo-estriadas, envuelto por dos hojas leptomeníngeas que lo separan del espacio subpial (cabezas de flecha en recuadro superior y asteriscos en recuadro inferior); B) espacio perivenular, en comunicación con el espacio subpial (flecha); y C) detalle fotomicrográfico del espacio perivascular de Virchow-Robin (flechas) (cortesía de la Dra. Susana Boluda)5.
La presencia en la RM de una pequeña cantidad de focos puntiformes hiperintensos en la sustancia blanca cerebral es un hallazgo muy habitual y, en una gran parte de casos, se puede considerar intrascendente. Estos puntos brillantes considerados «normales» pueden corresponder tanto a una dilatación de los espacios perivasculares como a pequeños focos glióticos o isquémicos lacunares.
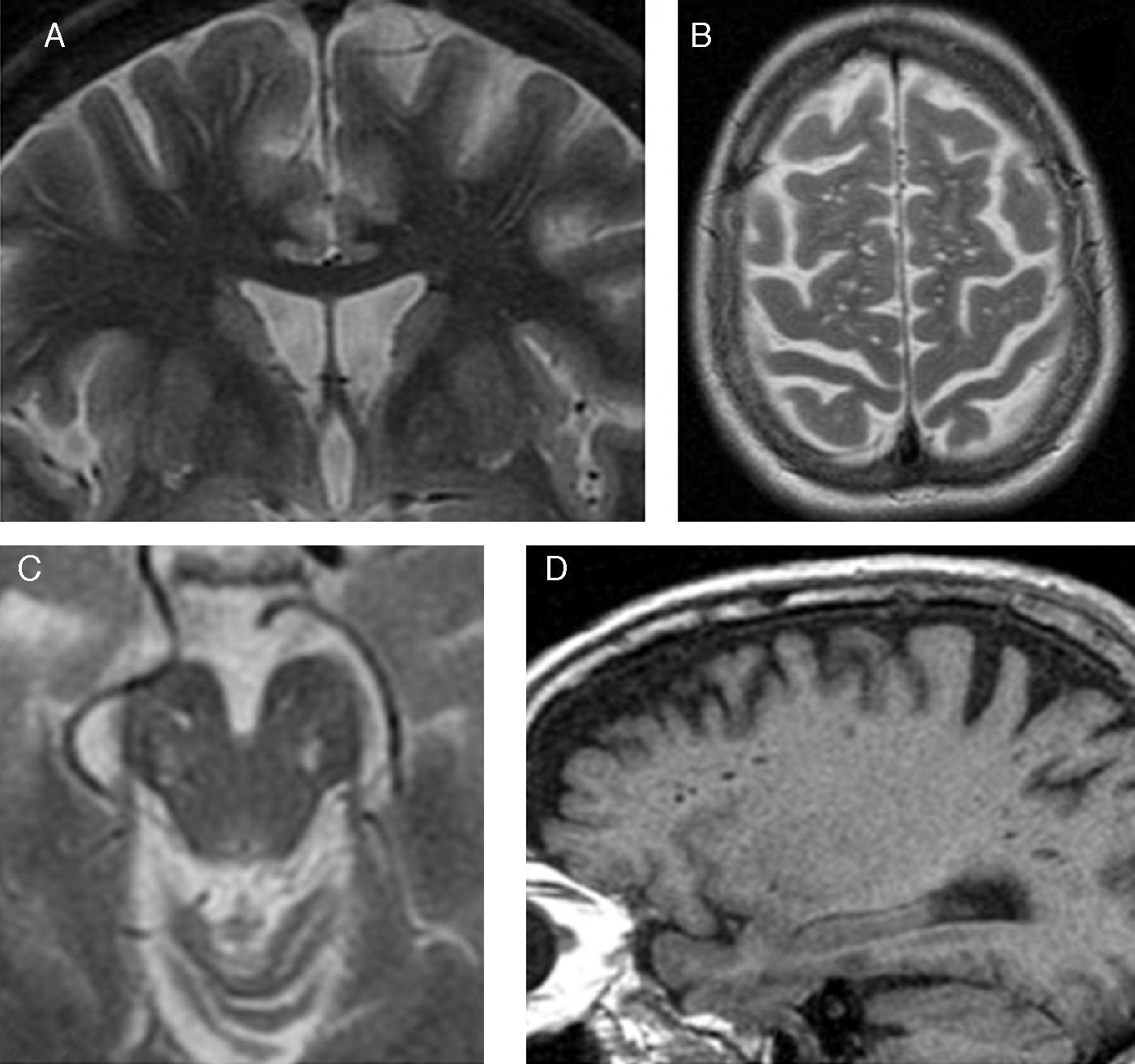
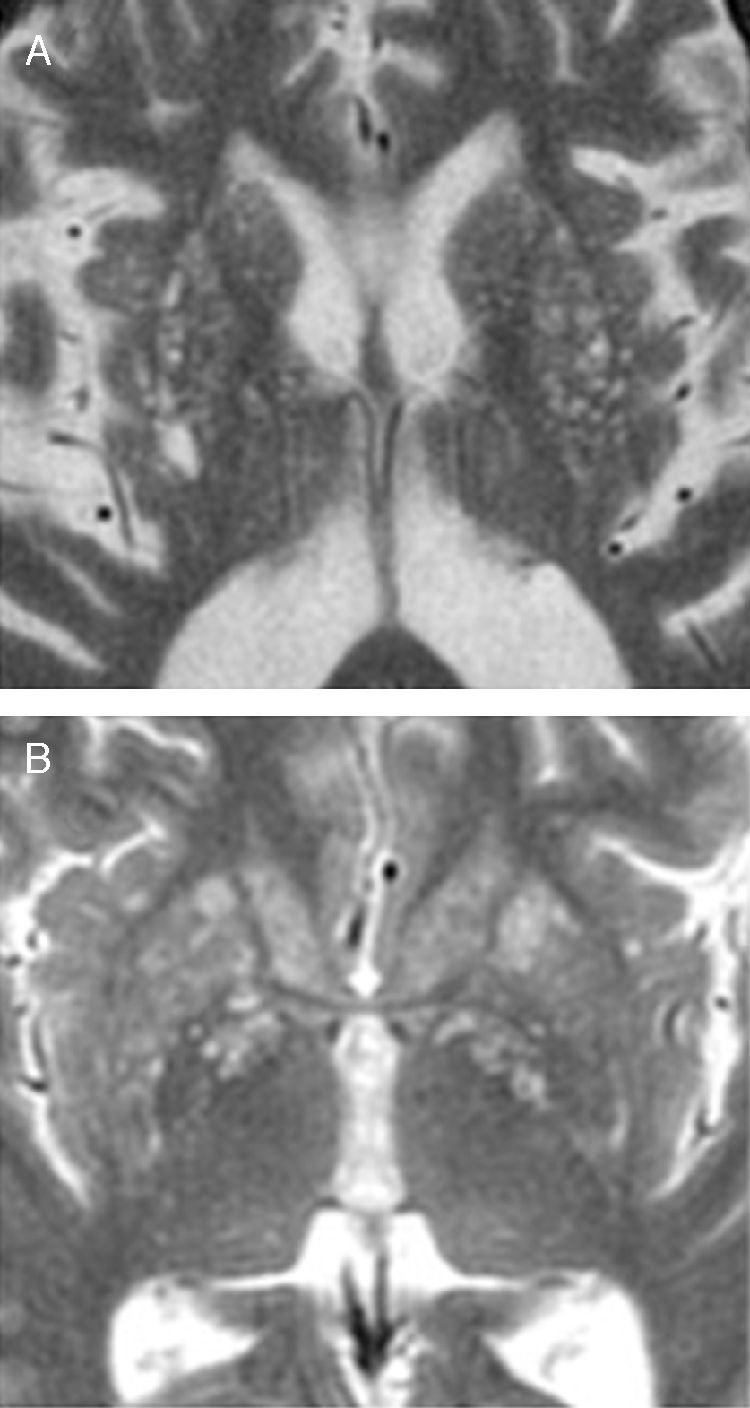
En la RM convencional, los espacios perivasculares se observan dilatados (EPVd) en un 13% de los adultos sanos, y solo en el 3% de niños entre 20 meses y 16 años de edad7,8. En un estudio observacional multicéntrico reciente en que se revisaron los estudios de RM cerebral que incluían secuencias 3D de alta resolución de 1.818 individuos mayores de 65 años sanos (sin demencia ni antecedente de infarto cerebral), se detectaron EPVd en todos ellos y EPVd de más de 3mm en aproximadamente un tercio de ellos9. Los EPVd aparecen como focos lineales o fusiformes con la misma señal que la del líquido cefalorraquídeo en todas las secuencias (fig. 3). Mientras que los espacios perivasculares pequeños (<2mm) se han considerado una variante anatómica7,8, los espacios perivasculares de mayor tamaño (>2mm) se ha relacionado con el envejecimiento6, la demencia, los estadios inflamatorios precoces en la esclerosis múltiple10 y la reacción inflamatoria en el traumatismo craneoencefálico8. Varios trabajos recientes han llegado a la conclusión de que los EPVd se asocian con lesiones isquémicas lacunares y, por tanto, este hallazgo puede considerarse un marcador de la enfermedad cerebrovascular de pequeño vaso11–13. Excepcionalmente, los espacios perivasculares pueden estar marcadamente dilatados, típicamente en la región mesencéfalo-talámica. Pueden ocasionar un efecto de masa significativo e hidrocefalia, y plantear el diagnóstico diferencial con otras lesiones quísticas tumefactivas. En muchas ocasiones estos espacios perivasculares gigantes son hallazgos incidentales y no siempre su presencia se relaciona con las manifestaciones clínicas9,14. Algunos estudios han descrito una asociación débil con diferentes grados de retraso del desarrollo, cefaleas, alteraciones del comportamiento y epilepsias no específicas, y la macrocefalia benigna en la población pediátrica15 (fig. 4).
La aparición de focos lacunares de aspecto isquémico en la sustancia blanca periventricular y subcortical es, asimismo, un proceso «fisiológico», puesto que se considera que la edad constituye, en sí misma, un factor de riesgo cerebrovascular16,17. La presencia de lesiones en la sustancia blanca es prácticamente ubicua (95%) en mayores de 65 años18.
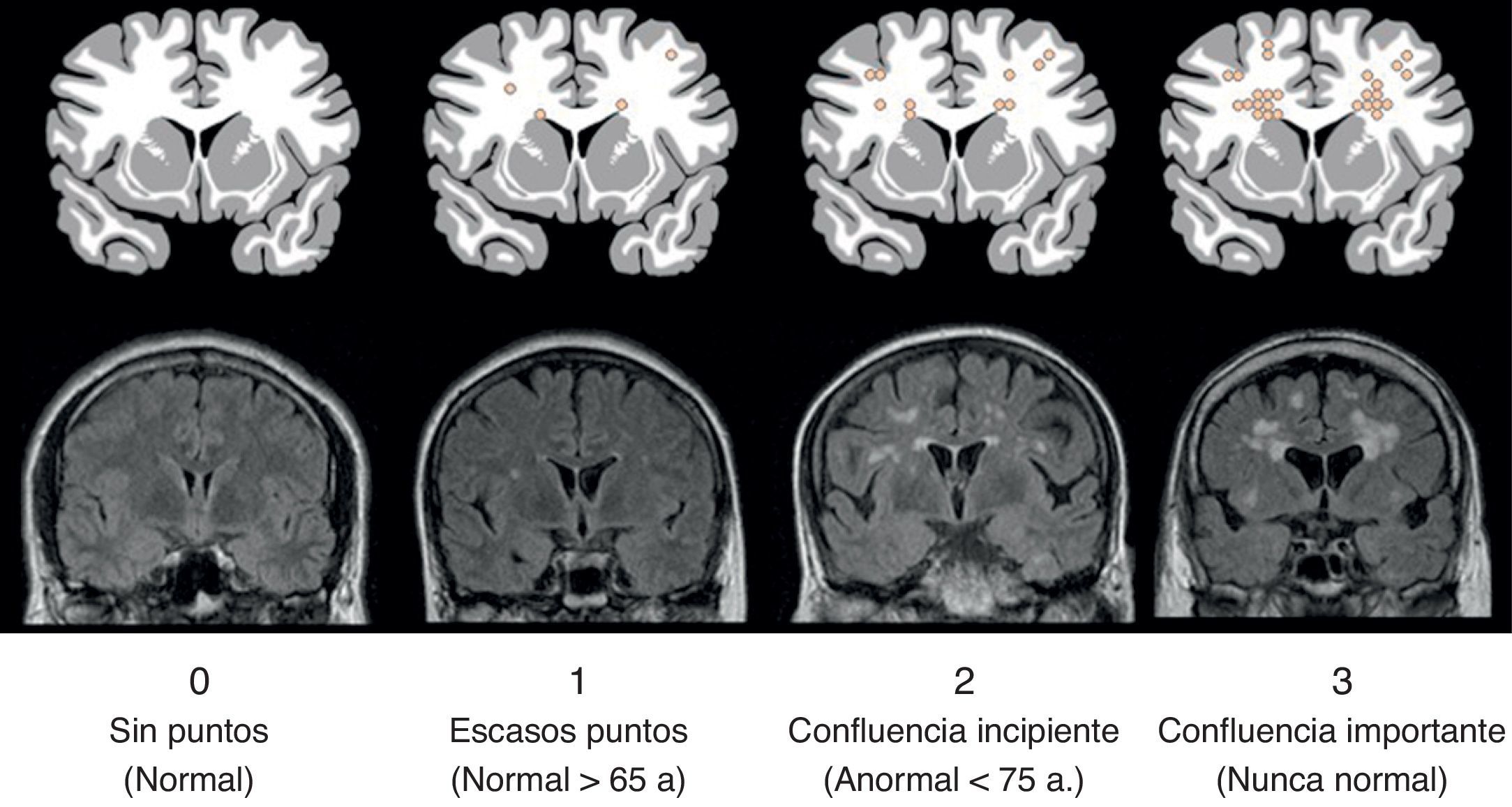
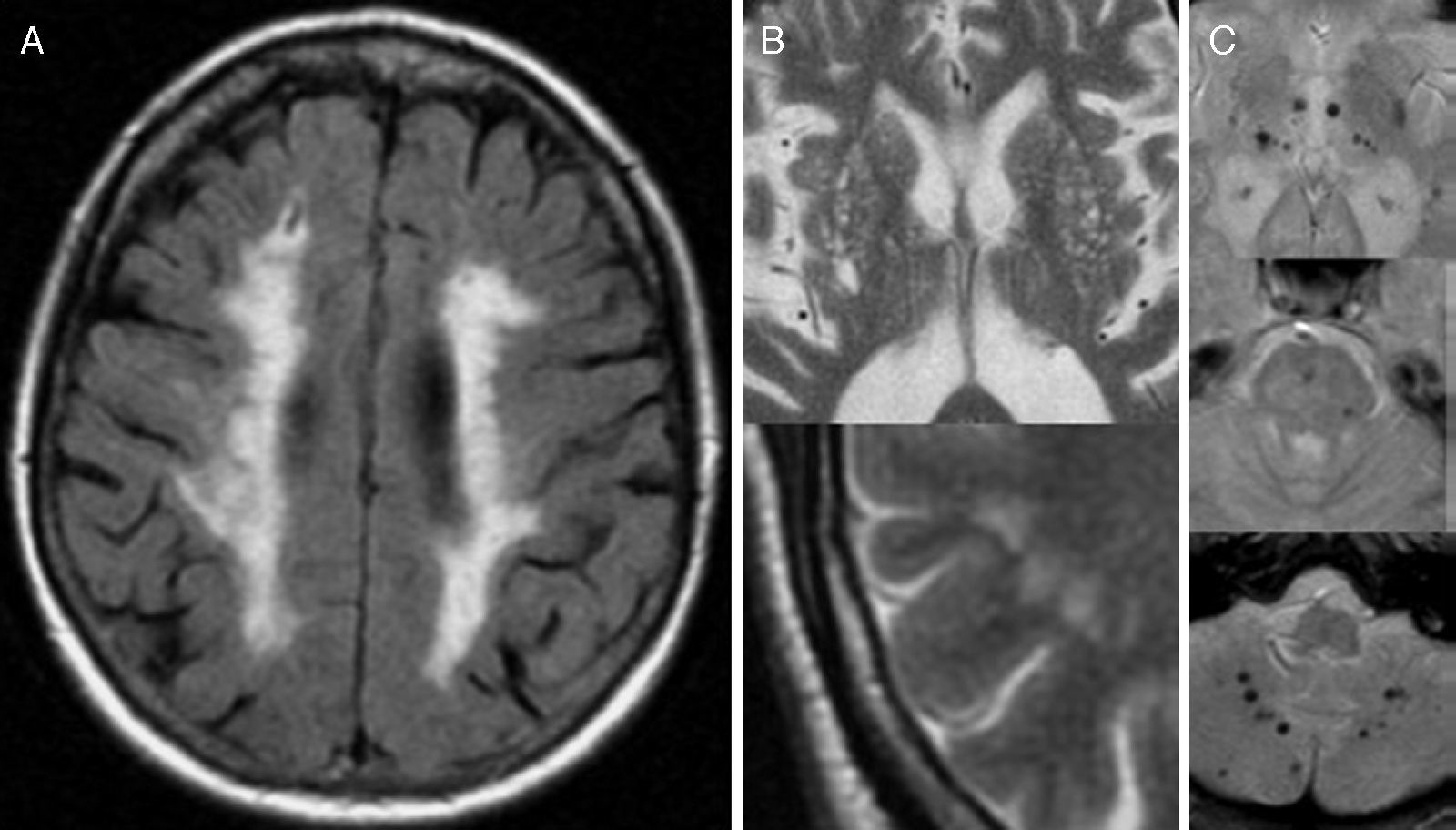
Existen varias escalas visuales que permiten valorar las lesiones de la sustancia blanca relacionadas con el envejecimiento, o leucoaraiosis, con una buena correlación entre ellas19. Una de las más conocidas es la de Fazekas20, la cual ha sido incorporada a la escala ARWMC (age-related white matter changes)21, recomendada en caso de que no se pretenda cuantificar las lesiones de la sustancia blanca mediante TC o RM22. Esta escala contempla 4 grados de lesión microvascular puntiforme en la sustancia blanca: su ausencia corresponde a un grado 0; la presencia de lesiones focales no confluentes, a un grado 1; las lesiones inicialmente confluentes, a un grado 2; y la afectación difusa confluente, a un grado 3 (fig. 5). A partir de esta escala, se ha tratado de delimitar la «normalidad» (atribuible al envejecimiento) de la afección, de manera que se considera el grado 1 normal con el envejecimiento, el grado 2 patológico en menores de 75 años y el grado 3 patológico en todos los casos23.
Se han publicado varios estudios de correlación anatomopatológica24–27 y radiológicos con técnicas de RM de transferencia de magnetización (TM), comparando ratios de transferencia de magnetización (RTM)28–30, que han tratado de dilucidar la naturaleza de estas imágenes y han descrito diferencias entre las lesiones de la sustancia blanca periventricular y las lesiones subcorticales. Sus resultados indican que con el envejecimiento se establecen defectos en la membrana ependimaria que permiten una filtración del líquido cefalorraquídeo que condiciona una gliosis y una desmielinización focal del parénquima. Además, la microcirculación penetrante subependimaria degenera, por lo que también existe un cierto componente isquémico, sobre todo en los casos en los que la leucopatía periventricular presenta bordes irregulares. Por otro lado, las lesiones de la sustancia blanca subcortical tienen un carácter eminentemente isquémico debido a la degeneración senil de la microcirculación24–30.
Imágenes puntiformes hiperintensas «anormales» en la sustancia blancaCuando la presencia de IPHSB es patológica, puede traducir una afección adquirida o hereditaria. Dentro de las afecciones adquiridas de la sustancia blanca, la causa hipóxico-isquémica microvascular es, con mucho, la más frecuente, ya sea aterotrombótica, por factores de riesgo cerebrovascular (FRCV), o embolígena. Debe considerarse siempre en primer lugar, aún en ausencia de FRCV típicos, a no ser que existan indicios clínicos y analíticos que hagan pensar en otra etiología. La esclerosis múltiple (EM) es la segunda causa en frecuencia, seguida de lejos por la vasculitis, las infecciones, las intoxicaciones o los traumatismos, entre otras causas31. Existe un gran grupo de pacientes con escaso riesgo vascular que presentan lesiones de aspecto microvascular para los que, con relativa frecuencia, no hay un diagnóstico alternativo o definitivo.
En cuanto a la afección hereditaria, las leucodistrofias constituyen un grupo de enfermedades consideradas raras que, aunque suelen aparecer en la edad pediátrica, pueden debutar en el adulto. Estas enfermedades metabólicas suelen afectar a la sustancia blanca de forma bastante simétrica y extensa (no puntiforme), y suelen dañar el tronco encefálico y el cerebelo, con la excepción de las enfermedades mitocondriales, que muestran lesiones más asimétricas y suelen afectar a la sustancia gris. Las más frecuentes en el adulto son la leucodistrofia metacromática, la leucodistrofia de células globoides, la adrenomieloneuropatía, las enfermedades mitocondriales, la sustancia blanca evanescente y la xantomatosis cerebrotendinosa31.
Fisiopatología básicaUn posible mecanismo de lesión de la sustancia blanca es la afectación primaria de una arteriola o vénula cerebral. Ésta compromete la irrigación del parénquima que depende de ellas y produce una lesión. La afectación de la sustancia blanca por enfermedad microvascular comprende un gran espectro de patología: hipoxia-isquemia, inflamación granulomatosa o no granulomatosa, infección, enfermedad por depósito de sustancias, tóxicos, enfermedades metabólicas, traumatismos, etc. Otro posible mecanismo fisiopatológico de la leucoencefalopatía es una infiltración celular o un acúmulo de sustancias patológicas en el espacio perivascular que también se puede manifestar radiológicamente como lesiones focales en la sustancia blanca. Su causa suele ser inflamatoria no infecciosa (como en el caso de la EM u otras enfermedades desmielinizantes, de algunas vasculitis o de algunas enfermedades granulomatosas), infecciosa atípica (enfermedad de Lyme, criptococosis, cisticercosis parenquimatosa), metabólica (mucopolisacaridosis) o traumática (lesión axonal difusa). Ambos procesos fisiopatológicos pueden coexistir en una misma enfermedad.
Teniendo en cuenta la anatomía de la microcirculación cerebral y la de su intersticio, se puede abordar la afección de la sustancia blanca considerando qué elementos se hallan más afectados en los diferentes grupos de leucoencefalopatías. En este sentido, trataremos de aproximarnos a la fisiopatología de la enfermedad que condiciona las IPHSB a partir de la identificación de un patrón semiológico predominante. Considerando varios elementos semiológicos definiremos tres grandes patrones:
- •
Patrón vascular (PV) o microvascular, que suele ser debido a una lesión arteriolar. Es el más prevalente (fig. 6A).
Figura 6.A) fisiopatología del patrón vascular. El esquema representa la lesión microvascular mural y/o endoluminal que conduce a la lesión isquémica del parénquima. Obsérvese la hialinización mural por arteriopatía hipertensiva (flecha) y la vacuolización isquémica adyacente (*); B) fisiopatología del patrón perivascular. El esquema representa un proceso patológico perivascular y la lesión parenquimatosa adyacente. Placa desmielinizante por inflamación perivenular en un paciente con esclerosis múltiple.
(0.21MB). - •
Patrón perivascular (PpV), que suele ser debido a una inflamación perivascular, entre otras causas menos frecuentes. El paradigma de este patrón es la EM, en la que se ha descrito una inflamación perivenular de origen autoinmune que ocasiona la desmielinización32 (fig. 6B).
- •
Patrón inespecífico (PI), en los casos en que no identificamos ninguno de los dos anteriores, y que suele ser debido a enfermedad microvascular.
Para el abordaje radiológico de un caso de IPHSB los elementos semiológicos básicos a analizar son su distribución y localización, la forma, el tamaño, el realce tras la administración de contraste, la presencia de hemorragia o microhemorragia y la afectación de la sustancia gris. La descripción de cada uno de estos elementos nos puede ayudar a identificar uno de los tres patrones semiológicos propuestos, de manera que nos facilitará un diagnóstico diferencial adecuado en cada caso.
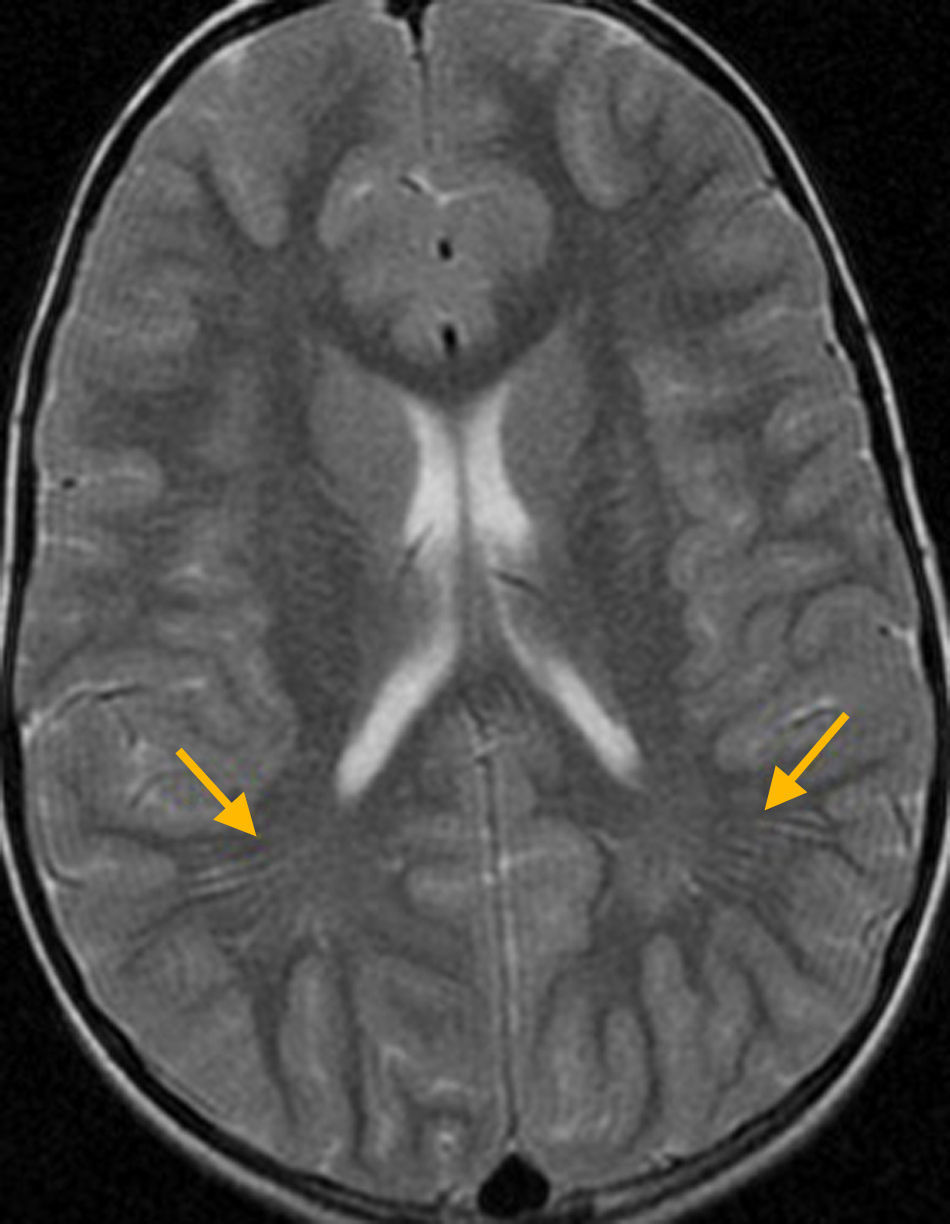
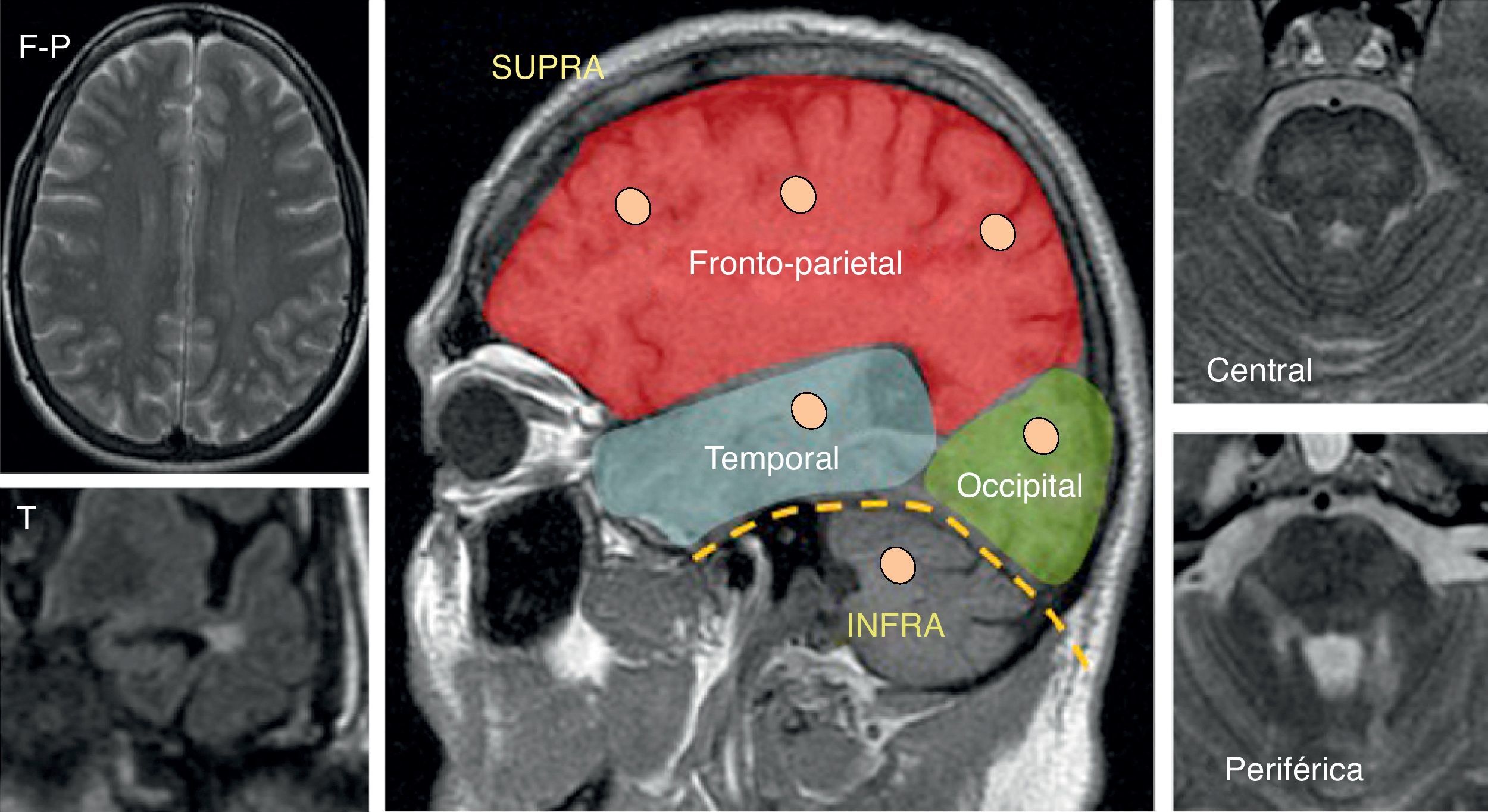
Distribución y localizaciónLas IPHSB pueden aparecer con una distribución preferentemente supratentorial, infratentorial o tanto supra como infratentorial. Como veremos más adelante, en general la presencia de lesiones de distribución fundamentalmente supratentorial nos sugerirá en primer lugar que nos encontramos ante una enfermedad de pequeño vaso y, por tanto, favorecerá un PV. El hecho de que además la distribución preferentemente frontoparietal reforzará esta sospecha (fig. 7).
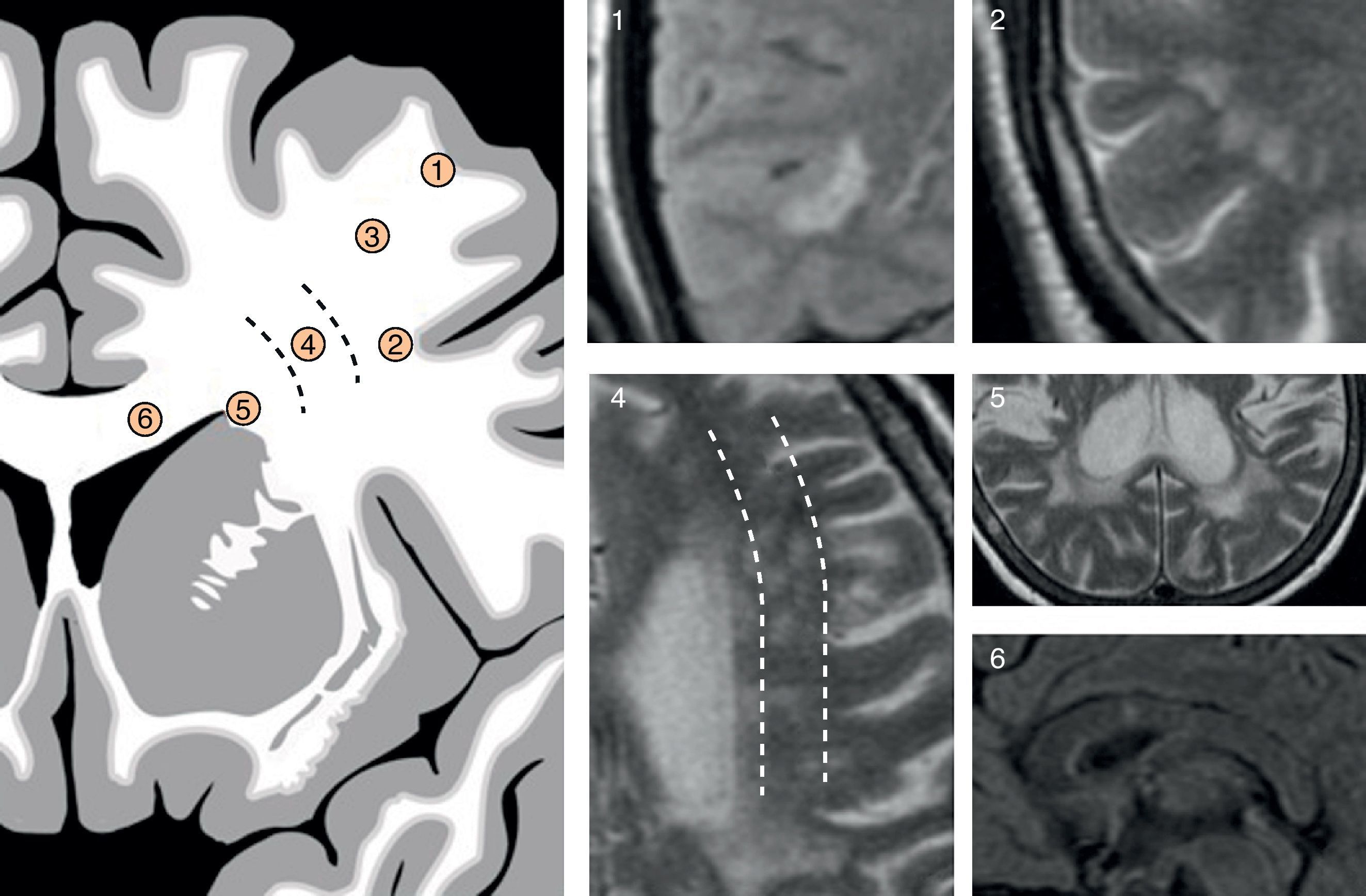
Dentro de la distribución supratentorial se pueden definir 4 grandes áreas: subcortical, periventricular, profunda o en el cuerpo calloso (fig. 8).
Localización: 1) yuxtacortical; 2) subcortical sub-«U»; 3) subcortical profunda no limítrofe; 4) subcortical limítrofe; 5) periventricular, y 6) cuerpo calloso. La afectación básicamente yuxtacortical o básicamente del cuerpo calloso va en contra del patrón vascular (PV); el resto de localizaciones favorecen un PV o patrón inespecífico y, por tanto, sugieren una causa microvascular. La lesiones periventriculares pueden traducir PV o patrón perivascular en función de su forma.
Si una lesión es subcortical puede situarse en contacto íntimo con la corteza cerebral o yuxtacortical, afectando a las fibras de la sustancia blanca subcorticales en «U», o, por el contrario, situarse inmediatamente por dentro de las fibras en «U», sin afectarlas, en cuyo caso se clasificará como subcortical sub-«U». Una lesión subcortical sub-«U» sugerirá un PV33, mientras que una lesión yuxtacortical será más sugestiva de un PpV, típica de la EM (aparece en un tercio de los casos de EM)34.
Una lesión se considerará periventricular cuando se sitúe en contacto, o prácticamente en contacto (a menos de 1cm)35, con la superficie ependimaria. Tanto una lesión microvascular como perivascular puede presentar una localización periventricular; su forma será el elemento semiológico clave.
Entre la región subcortical y la periventricular encontramos la profunda, que se clasificará como limítrofe, si se sitúa en una zona fronteriza entre dos territorios vasculares, propia de un PV, o como no limítrofe, si no se sitúa claramente en una región fronteriza, PI. Finalmente, el cuerpo calloso constituirá otra localización especial, que observaremos en algunas enfermedades como la EM, típicamente en la unión calloso-septal34, en el síndrome de Susac34,36,37 o en la arteriopatía cerebral autosómica dominante con infartos subcorticales y leucoencefalopatía (CADASIL)38, entre otras.
Las lesiones infratentoriales pueden mostrar una localización periférica, en contacto con la superficie del parénquima, o central, sin afectación de la superficie. Una lesión central será más propia de un PV, mientras que una lesión periférica lo será de un PpV34 (fig. 7).
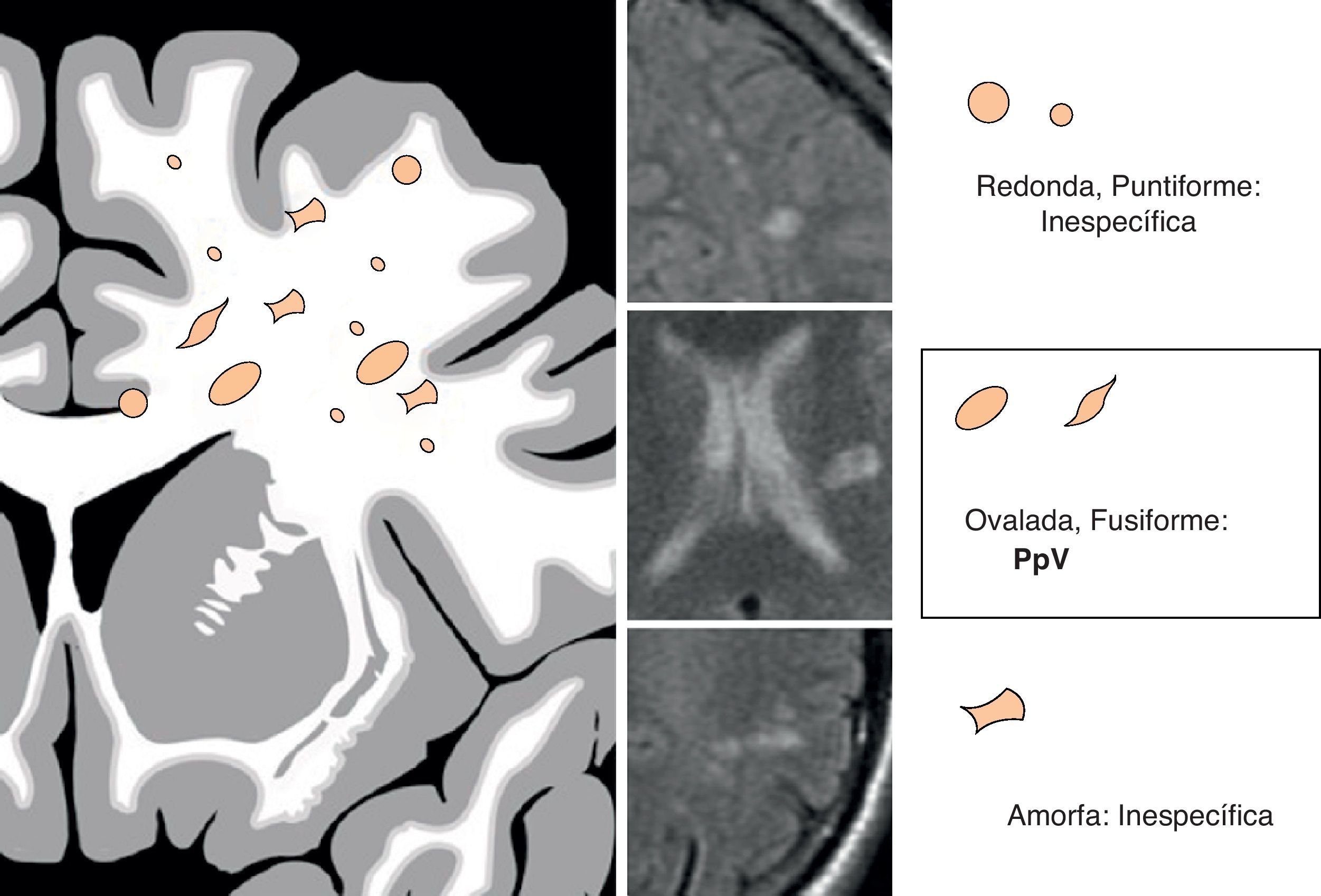
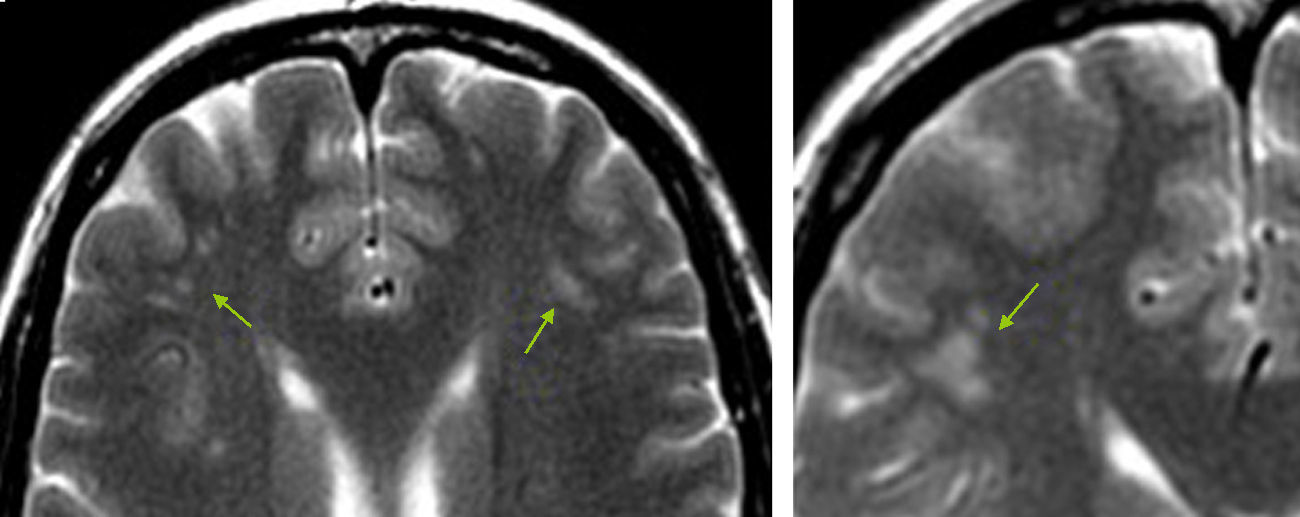
MorfologíaCon respecto a la forma, podemos distinguir varios tipos de lesiones: ovaladas o fusiformes, puntiformes o redondeadas, y amorfas (fig. 9). Mientras que las lesiones puntiformes, redondeadas y amorfas son inespecíficas, las ovaladas o fusiformes suelen tener una distribución paralela a la microcirculación cerebral, por lo que suelen corresponder a un PpV. Las lesiones periventriculares ovaladas o fusiformes en disposición radial, perpendicular al eje longitudinal de los ventrículos laterales, son bastante características de la EM. Se las conoce como «dedos de Dawson»34, en honor al neuropatólogo James Dawson, quien describió células inflamatorias venulares y perivenulares en forma de dedos en pacientes con EM39. La confluencia de estas lesiones conforma una imagen «en sierra», también típica de la EM34. La leucoencefalopatía periventricular de causa microvascular por FRCV tiene bordes típicamente más irregulares3,40.
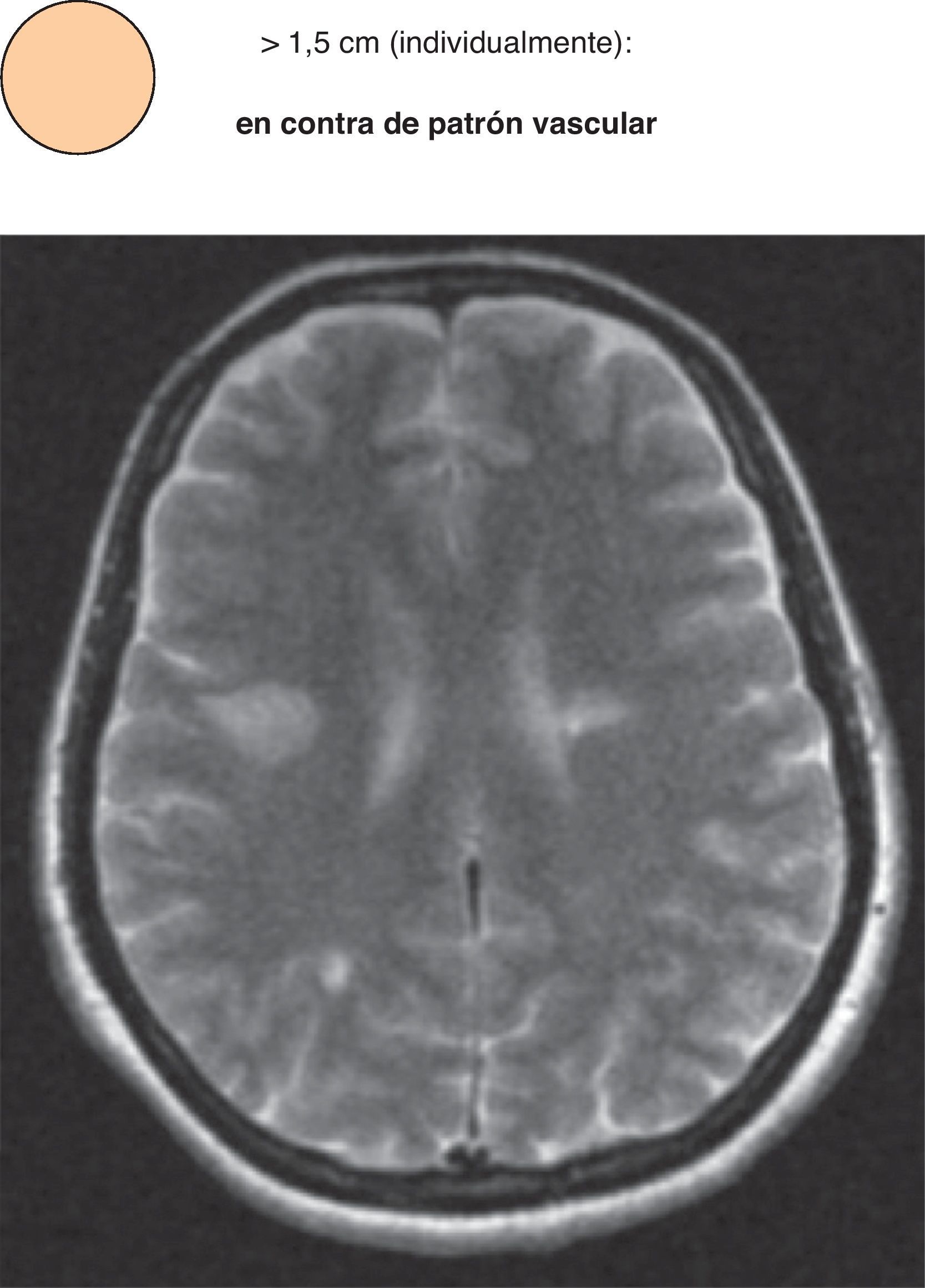
TamañoCuando identifiquemos una lesión aislada (no varias lesiones confluentes), de tamaño superior a 10-15mm, nuestra sospecha será la de un PpV (se admite que un infarto lacunar puede alcanzar los 15mm)41. Lesiones de menor tamaño son inespecíficas, y pueden traducir tanto una lesión microvascular como una perivascular (fig. 10).
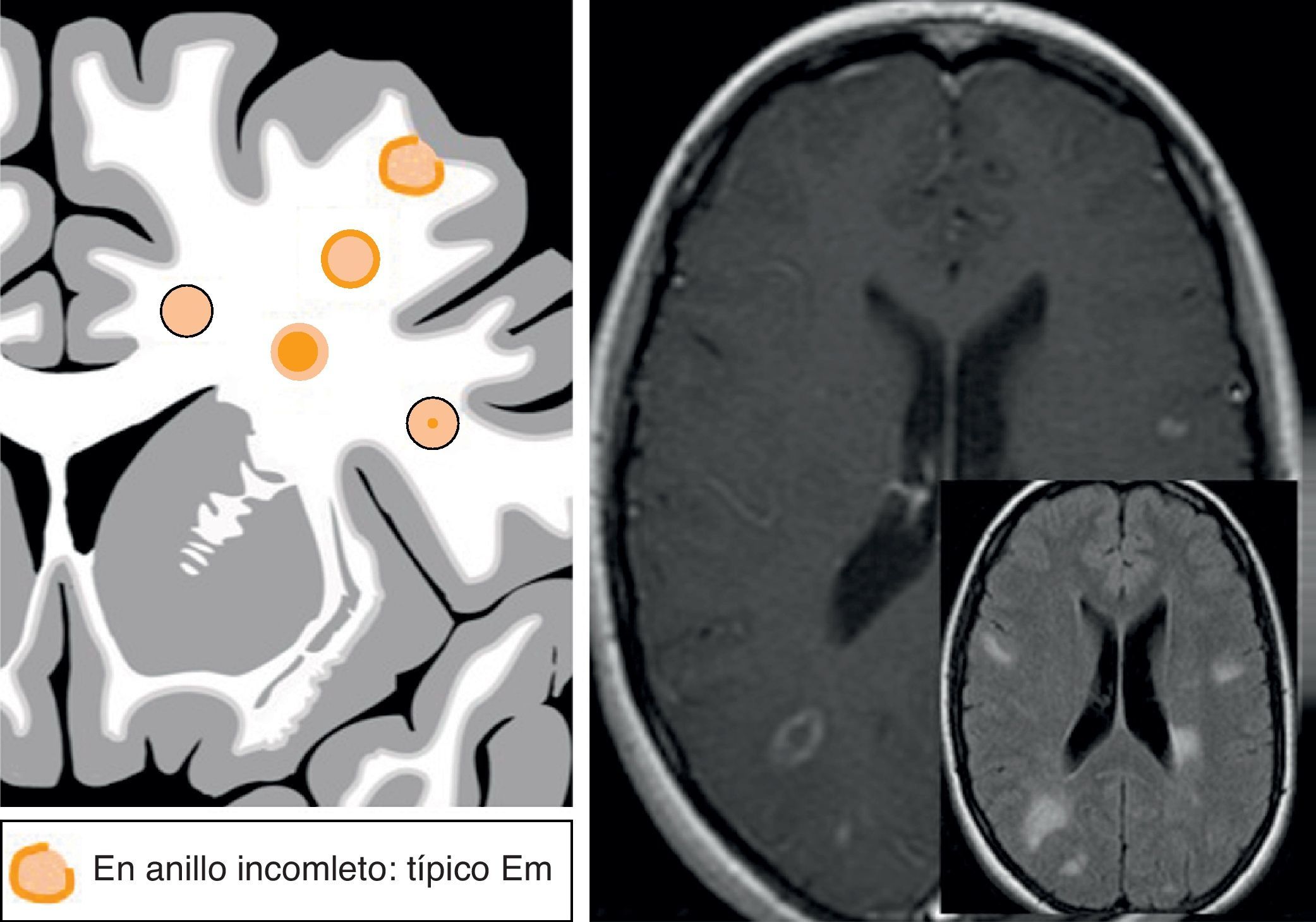
Realce tras la administración de contrasteLa ausencia de realce en los focos de leucopatía, aunque es un hallazgo inespecífico, sugiere que nos encontramos en una fase inactiva de la enfermedad. Por el contrario, en la fase inflamatoria activa de la enfermedad suele existir un aumento de permeabilidad o ausencia de la barrera hematoencefálica y se puede apreciar un realce de la lesión con gadolinio. Podemos observar captaciones puntiformes, periféricas (en anillo completo o incompleto) o centrales (homogéneas o heterogéneas). En general, el patrón de realce es un hallazgo inespecífico, con la excepción de realce periférico en anillo incompleto, que se ha descrito como un hallazgo típico en la EM34,36, y, por tanto, sugerirá un PpV (fig. 11).
Realce tras la administración de contraste. La ausencia de realce es un hallazgo semiológico inespecífico. La captación en anillo periférico incompleto va a favor de un patrón perivascular por esclerosis múltiple. Paciente con múltiples lesiones yuxtacorticales con captación en anillo incompleto típica en alguna de ellas.
En el caso de sospechar por imagen una EM, los criterios diagnósticos actuales del grupo MAGNIMS (Magnetic Imaging in MS)42 no requieren demostrar realce con gadolinio para el diagnóstico de diseminación en el espacio; sin embargo, una lesión captante entre otras no captantes en un mismo estudio de resonancia magnética es suficiente para determinar una diseminación en el tiempo.
En el seguimiento de la enfermedad, muchos autores abogan por el uso de contraste para valorar la inflamación activa y la eficacia del tratamiento. El número de lesiones captantes también puede dar información acerca del pronóstico de la enfermedad34.
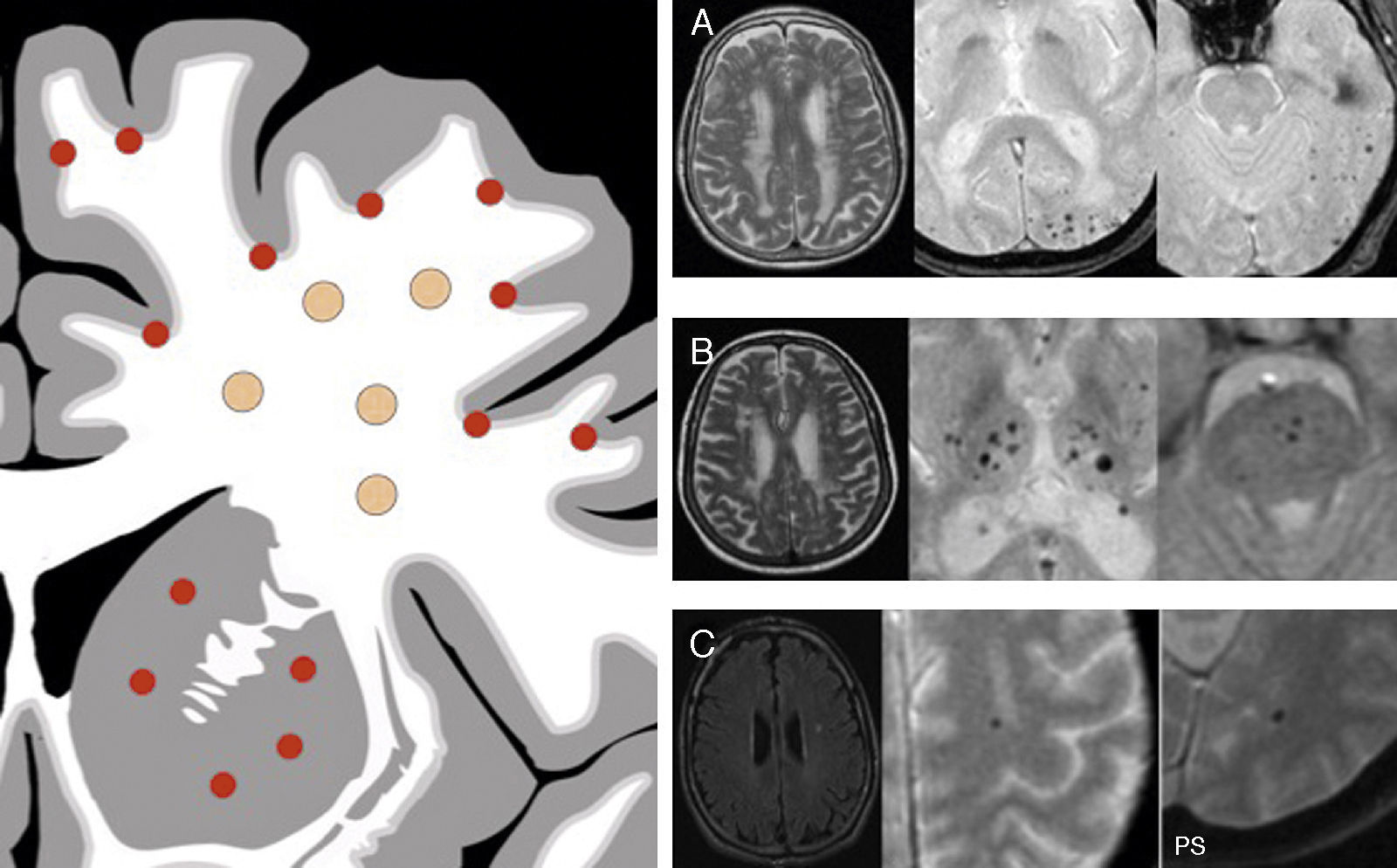
Hemorragia o microhemorragiaEn RM, las imágenes de microsangrado se encuentra asociadas a las IPHSB en al menos el 18% de la población a partir de los 60 años. Las IPHSB están presentes en más del 95% de la población mayor de 65 años. Estos datos refuerzan el concepto de enfermedad microvascular mixta, con un origen fisiopatológico común entre la enfermedad de sustancia blanca y los microsangrados18. Ante un PV con a focos de microsangrado en las secuencias potenciadas en T2* nos plantearemos dos entidades patológicas principales: la hipertensión arterial (HTA) y la angiopatía amiloide (AA). La afectación de la región profunda en los GB, así como infratentorial, sugiere una microangiopatía hipertensiva o arteriosclerótica, mientras que la localización periférica cortical o lobar de los sangrados es típica de la AA43 (fig. 12).
En los pacientes con vasculitis se encuentran focos de sangrado cerebral asociados a lesiones de sustancia blanca de aspecto microvascular y a lesiones isquémicas corticales, como manifestación inicial o secundaria a la transformación de un infarto44.
Otra causa de IPHSB con restos de sangrado es la lesión axonal difusa en el contexto de un traumatismo de alta energía. Frecuentemente se identifican focos de leucopatía residuales con restos de hemosiderina en la interfase entre la sustancia gris y la sustancia blanca, de predominio frontal, y típicamente en la región de los núcleos basales y en el esplenio del cuerpo calloso45 (fig. 12).
Afectación de sustancia grisGran parte de los casos de IPHSB se asocian a lesiones corticales o de la región de los GB.
La coexistencia de lesiones de la corteza cerebral y múltiples focos brillantes en la sustancia blanca es un hallazgo inespecífico. En pacientes con enfermedad microvascular por vasculitis, no es raro hallar lesiones periféricas con afectación cortical, que normalmente representan áreas de infarto isquémico44. En la EM suelen existir lesiones corticales, aunque son difíciles de visualizar con las secuencias convencionales de RM34.
En los pacientes con microangiopatía hipertensiva o arteriosclerótica es típica la afectación de los GB40 (fig. 13), mientras que en la EM es excepcional34. Los pacientes con encefalomielitis aguda diseminada (ADEM), que pueden presentar lesiones indistinguibles a las de EM, suelen tener afectada la región de los GB, además de la médula espinal36,46. Diversas vasculitis (lupus eritematoso sistémico [LES], Behçet, etc.) y la neurosarcoidosis pueden afectar a los GB44,47,48. En los pacientes inmunodeprimidos con criptococosis es típica la formación de quistes gelatinosos en el espacio perivascular de las arteriolas tálamo-perforantes y lentículo-estriadas de los GB49.
Afectación asociada de la sustancia gris (ganglios basales). A) focos porencefálicos lacunares, que probablemente se asocian a espacios de Virchow-Robin dilatados, en un paciente con hipertensión arterial no controlada. B) Quistes gelatinosos en los espacios de Virchow-Robin de la circulación lentículo-estriada en un paciente VIH de 30 años, que debutó con una criptococosis.
Teniendo en cuenta cada uno de los elementos semiológicos descritos, se pueden definir las características generales de cada patrón (tabla 1). Identificando el patrón predominante, así como las particularidades concretas de cada caso, se puede plantear un diagnóstico diferencial adecuado.
Características semiológicas
| Patrón vascular |
| – No yuxtacortical |
| – Subcortical sub-U |
| – Profundo limítrofe |
| – Periventricular irregular |
| – Supra>infratentorial |
| – Supratentorial frontoparietal |
| – Ganglios basales |
| – No realce (si no agudo) o realce tenue |
| Patrón perivascular |
| – Periventricular ovoide |
| – Yuxtacortical |
| – Fusiforme u ovoide |
| – Dedos de Dawson |
| – Supra e infratentorial |
| – Lesiones grandes |
| Patrón inespecífico |
| – Profundo no limítrofe |
| – Amorfo, puntiforme, redondo |
El patrón vascular por enfermedad microvascular hipóxico-isquémica secundaria a FRCV (sobre todo HTA, dislipemia y diabetes) presenta un gran número de lesiones que suelen mostrar casi todos los hallazgos semiológicos descritos de este patrón. En la HTA se observan restos de hemosiderina en las secuencias ponderadas en T2*, fundamentalmente en el cuerpo estriado, los tálamos, el cerebelo y el tronco encefálico (fig. 14).
Patrón vascular: factores de riesgo cerebrovascular. Pacientes con hipertensión arterial que muestran: A) focos de leucopatía confluentes en la sustancia blanca periventricular; B) afectación de los ganglios basales y de la sustancia blanca subocortical que respeta a las fibras subcorticales en «U»; y C) restos de sangrado en los ganglios basales, el tronco encefálico y el cerebelo.
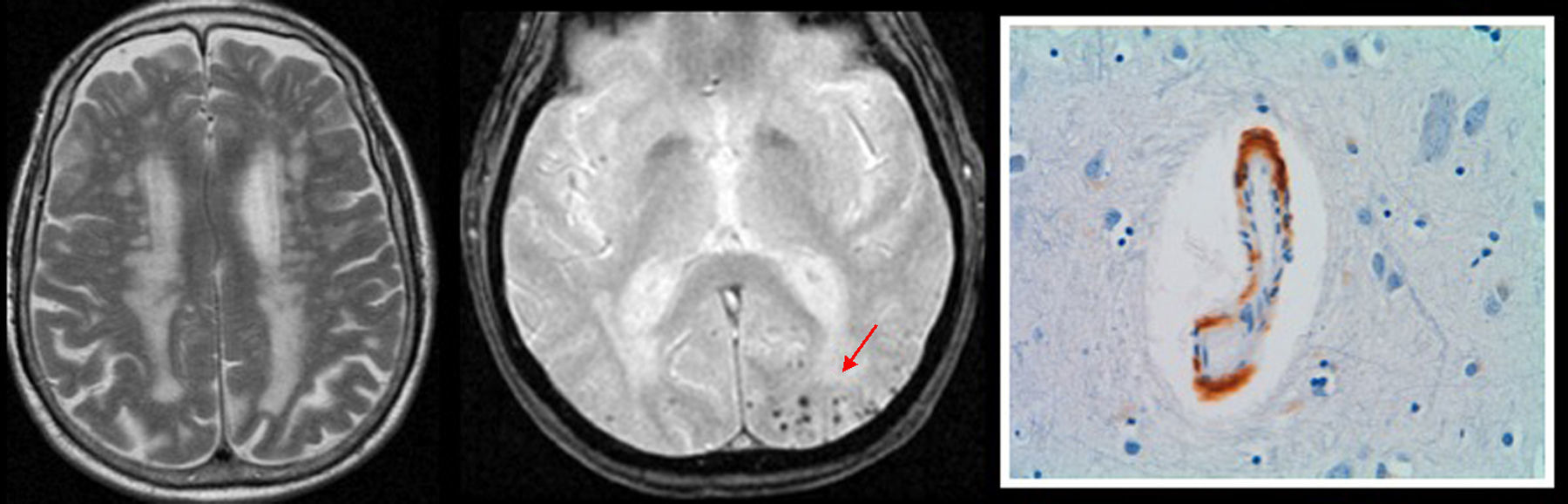
Como se ha descrito, la semiología afectación microvascular en la AA es característica del PV, típicamente con focos de microsangrado periférico cortical o áreas de hemorragia lobar18,50,51 (fig. 15).
Patrón vascular: angiopatía amiloide. Marcados cambios de enfermedad microvascular en la sustancia blanca supratentorial fronto-parieto-occipital con patrón vascular (imagen de la izquierda). En las secuencias potenciadas en eco de gradiente (imagen central) se ponen de manifiesto focos puntiformes de hemosiderina en la unión córtico-subcortical, de predominio posterior (flecha), que sugieren una angiopatía amiloide subyacente. A la derecha, detalle del depósito mural arteriolar de sustancia β-amiloide, congófila.
Los estudios en pacientes con migraña han mostrado IPHSB de aspecto microvascular52,53, fundamentalmente frontales y en los centros semiovales54 (fig. 16). Un reciente estudio con 780 participantes confirma esta asociación tanto en los pacientes con cefalea migrañosa como en los que presentan otros tipos de cefalea, especialmente tensional, con una prevalencia del 34 y 32% respectivamente, ambas muy superiores a la prevalencia de IPHSB en el grupo de pacientes control (7,4%)35. En pacientes con migraña precedida de aura se ha demostrado una mayor asociación con infartos isquémicos clínicos o subclínicos, especialmente en el territorio posterior (cerebelo, protuberancia)54. Por otro lado, con independencia del tipo de cefalea, la existencia de lesiones cerebrales no parece relacionarse con un deterioro cognitivo35.
En gran parte de las vasculitis del sistema nervioso central encontramos IPHSB propias de un PV, con un cierto predominio subcortical, asociadas a lesiones isquémicas corticales y focos de sangrado intraparenquimatoso, como manifestación inicial, o secundaria a la transformación de un infarto44. En las vasculitis de causa séptica se suelen encontrar restos de sangrado periférico50, y en las vasculitis por sustancias vasoactivas, como la cocaína y los derivados alcaloides, las anfetaminas, las efedrinas o la fenilpropanolamina, en los GB44,50 (fig. 17).
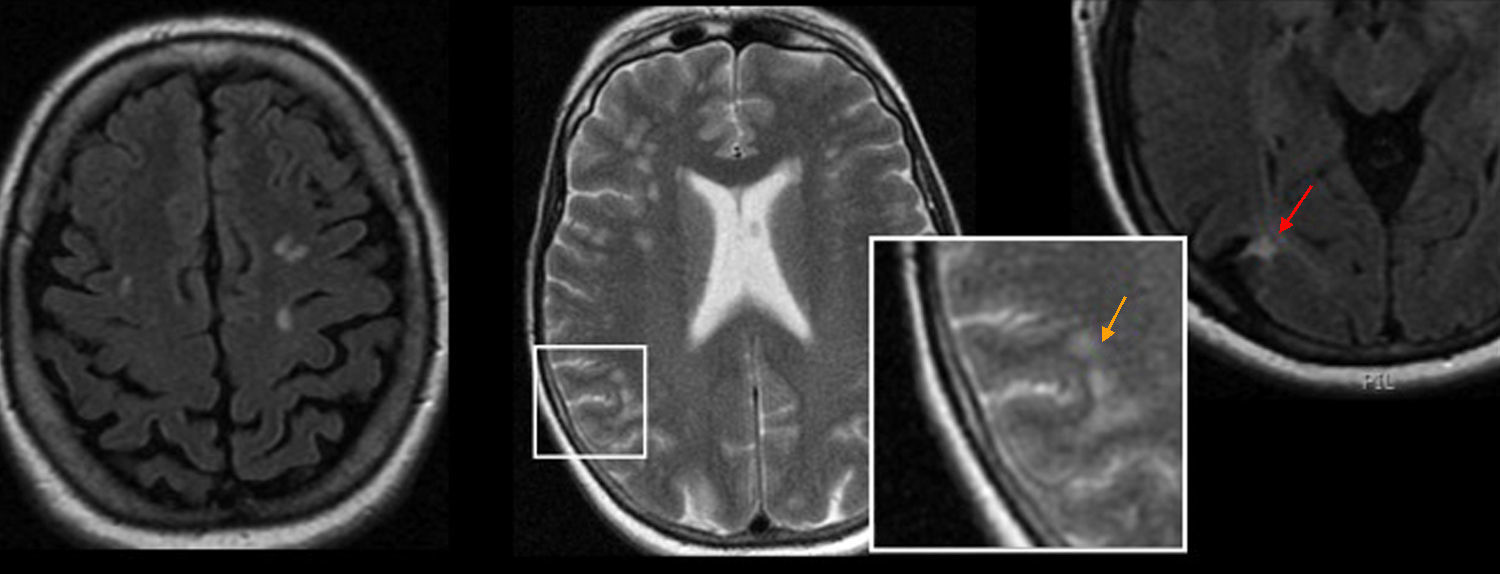
Patrón vascular: vasculitis. Mujer de 63 años, sin factores de riesgo cerebrovascular típicos, con discreta hiperhomocisteinemia y anticuerpos anti-fosfolípido. Mostraba lesiones puntiformes en la sustancia blanca supratentorial que respetaban las fibras sub-«U» (flecha naranja) y algún área de infarto córtico-subcortical témporo-parietal antiguo (flecha roja). La sospecha fue de vasculitis lúpica.
En la CADASIL podemos identificar todos los signos típicos del PV asociados a una afectación temporal bilateral en los polos anteriores, las cápsulas externas y el cuerpo calloso en la unión calloso-septal55–57 (fig. 18).
Patrón vascular: arteriopatía cerebral autosómica dominante con infartos subcorticales y leucoencefalopatía (CADASIL). Paciente de 50 años diagnosticado de CADASIL, con signos de enfermedad microvascular en la sustancia blanca supratentorial y afectación de los polos temporales anteriores (flechas).
En resumen, ante IPHSB con PV, si el paciente tiene FRCV, la leucoencefalopatía podrá ser atribuida a éstos. En caso contrario, el diagnóstico diferencial se centraría en otras causas de afección microvascular como la AA, las cefaleas, las enfermedades tóxico-metabólicas, algunas vasculitis o la CADASIL, entre otras entidades.
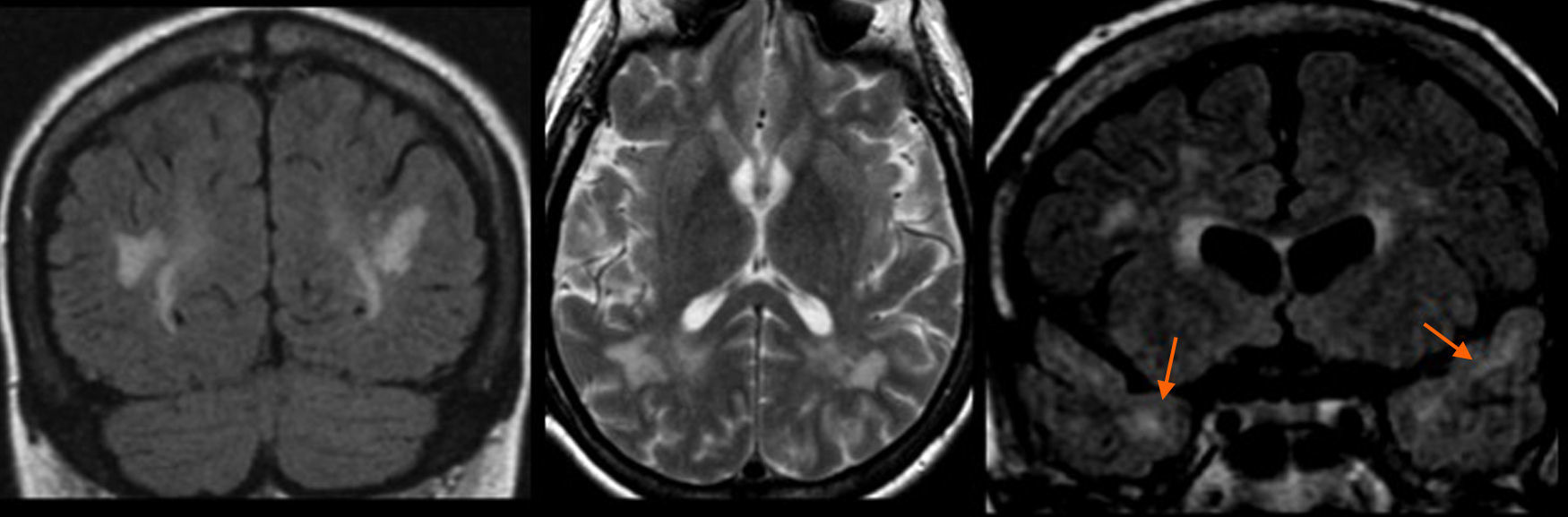
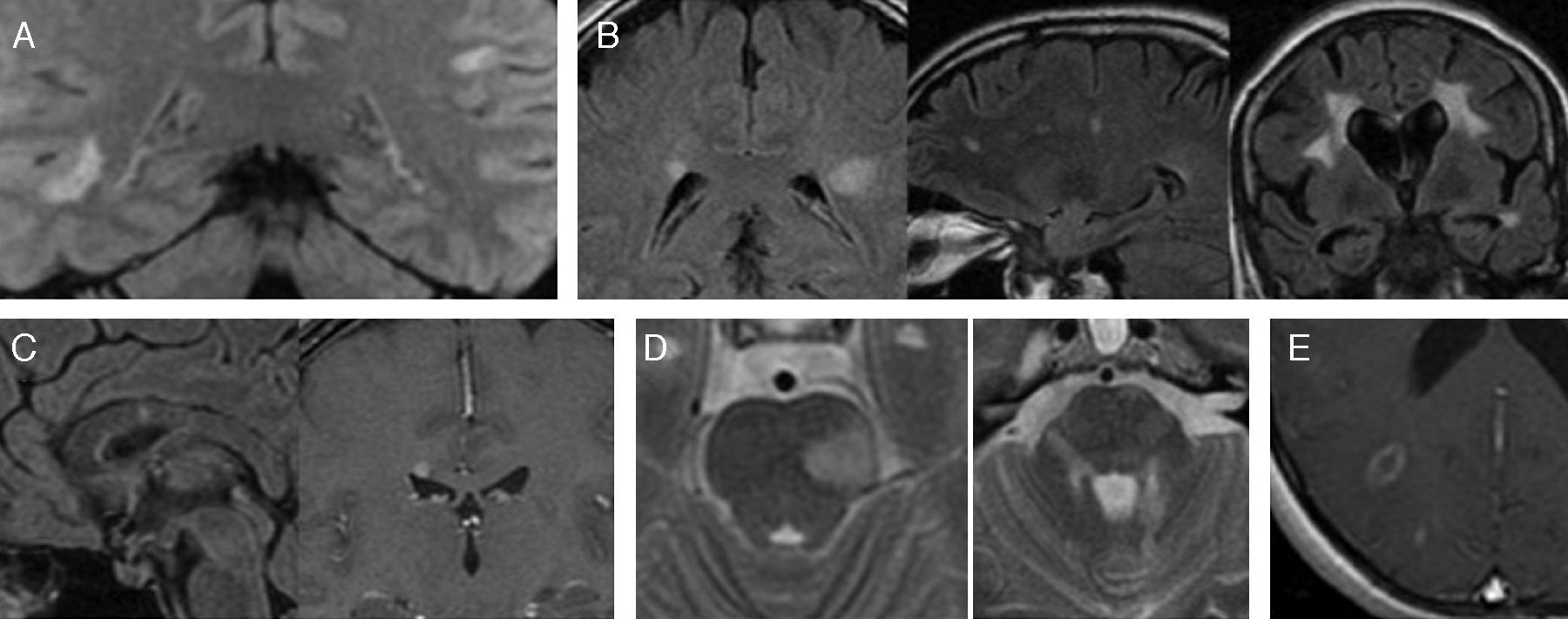
Patrón perivascularLas IPHSB con un patrón perivascular debe hacer pensar en la EM como primera opción diagnóstica. Los hallazgos semiológicos más característicos son las lesiones ovoideas yuxtacorticales y periventriculares en «dedos de Dawson», típicamente en contacto con la vertiente inferior del cuerpo calloso (calloso-septales), o adyacentes a la vertiente anterior del asta temporal, así como lesiones infratentoriales periféricas adyacentes al suelo del cuarto ventrículo, en los pedúnculos cerebelosos medios y en el tronco encefálico 34 (fig. 19).
Patrón perivascular: esclerosis múltiple (EM). A) lesiones yuxta-corticales; B) lesiones periventriculares en «dedos de Dawson» (izquierda y centro). Lesiones confluentes «en sierra» en la EM crónica y lesión temporal anterior (derecha); C) lesiones calloso-septales; D) lesiones infratentoriales periféricas; y E) captación periférica en «anillo incompleto».
Si hay otros indicios clínicos y analíticos a favor de una EM, orientaremos al paciente como tal hasta el diagnóstico definitivo de diseminación en espacio y tiempo, según los criterios de MAGNIMS42. Si el contexto clínico no apunta a la EM, el diagnóstico diferencial incluirá otras enfermedades de probable etiología autoinmune como la EM atípica, la ADEM, el LES, la enfermedad de Sjögren o la sarcoidosis47,48, las infecciones como la enfermedad de Lyme58 o la criptococosis49, algunas vasculitis como la enfermedad de Behçet59, o las enfermedades metabólicas como la mucopolisacaridosis6.
Patrón inespecíficoAnte un caso de IPHSB con PI, si el paciente presenta FRCV, la leucoencefalopatía podrá ser atribuida a éstos. En caso contrario, el diagnóstico diferencial se centrará en primer lugar en las causas de afección microvascular atípica, y, en segundo lugar, en causas infrecuentes de enfermedad perivascular.
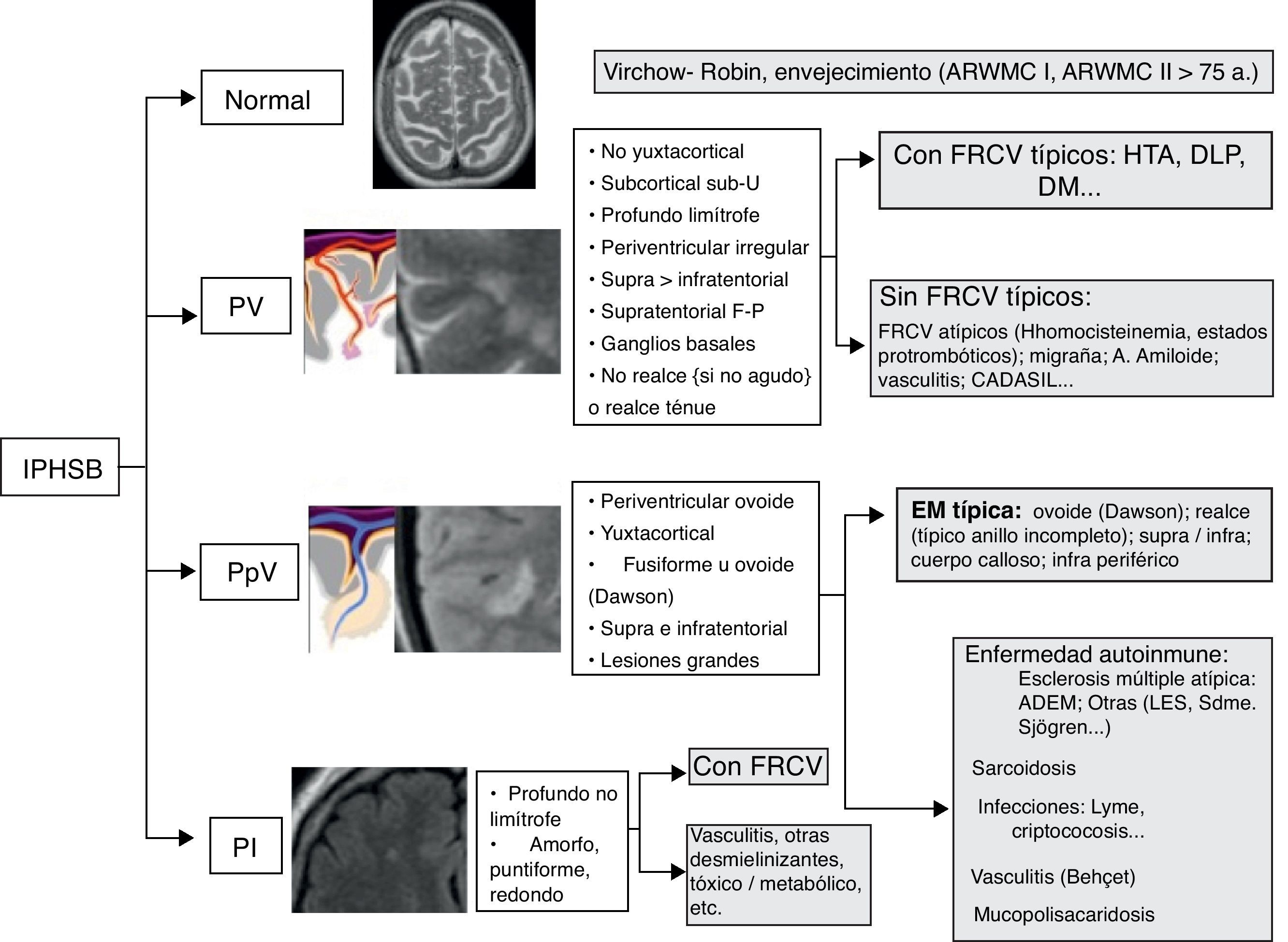
En el cuadro-resumen de la figura 20 se sugiere un algoritmo diagnóstico ante un caso de IPHSB, que nos puede ayudar a establecer un diagnóstico diferencial adecuado una vez identificado el patrón predominante.
Algoritmo diagnóstico de las imágenes puntiformes hiperintensas en la sustancia blanca (IPHSB), patrón vascular (PV), patrón perivascular (PpV) y patrón inespecífico (PI). ARWMC: Escala ARWMC (Age-Related White Matter Changes); FRCV: Factores de riesgo cardiovascular; HTA: Hipertensión arterial; DLP: Dislipemia; DM: Diabetes mellitus; CADASIL: Arteriopaía cerebral autosómica dominante con infartos subcorticales y leucoencefalopatía; EM: Esclerosis múltiple.
Este trabajo propone una herramienta diagnóstica práctica y simple definiendo tres grandes patrones semiológicos de imágenes puntiformes hiperintensas de sustancia la blanca: patrón vascular, perivascular e inespecífico, basándose ena la anatomía de la microcirculación cerebral. El reconocimiento del patrón semiológico predominante permite acotar el diagnóstico etiológico. La mayoría de casos de puntos brillantes encontrados en la RM craneal son de etiología vascular. La EM es la causa más frecuente de PpV. El PI es más probable que sea una presentación atípica de etiología vascular.
Autoría- 1.
Responsable de la integridad del estudio: SM.
- 2.
Concepción del estudio: SM, MC y DG.
- 3.
Diseño del estudio: SM.
- 4.
Obtención de los datos: SM.
- 5.
Análisis e interpretación de los datos: SM, MC, DG, JC y SG.
- 6.
Tratamiento estadístico: No aplicable.
- 7.
Búsqueda bibliográfica: SM, MC y DG.
- 8.
Redacción del trabajo: SM, MC y DG.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: SM, MC, DG, JC y SG.
- 10.
Aprobación de la versión final: SM, MC, DG, JC y SG.
Los autores declaran no tener ningún conflicto de intereses.
AgradecimientosA Susana Boluda, neuropatóloga en la Unidad de Neuropatología del Hospital de Bellvitge, por aportar microfotografías de correlación anatomopatológica; a Dolores Cocho, neuróloga de la Unidad de Neurología del Hospital de Granollers, por facilitar bases de datos de casos representativos para la iconografía, y a Txomin Medrano, ilustrador, por los esquemas anatómicos.