Nuestro objetivo es describir aquellas técnicas de intervencionismo musculoesquéletico guiadas por imagen (ecografía y/o tac) que pueden ser realizadas por un radiólogo general, ya sea en hospitales, centros de salud, consultas privadas, etc. El primer requisito para la realización de estos procedimientos es el disponer de un adecuado conocimiento de la anatomía del sistema musculoesquelético. El segundo, que el paciente debe ser informado adecuadamente sobre la técnica, riesgos y alternativas al mismo, relativo por tanto, a la obtención del consentimiento firmado. El tercero es que estos procedimientos se realizan siguiendo los principios de asepsia de la zona de punción, así como del material empleado y lo que acontece durante la realización del procedimiento. Los principales procedimientos que pueden realizarse guiados por ecografía son los siguientes: punción aspiración con aguja fina (PAAF), biopsia con aguja gruesa (BAG), artrocentesis diagnósticas y/o terapéuticas, drenajes de colecciones yuxtaarticulares, drenajes de abscesos, drenaje de hematomas, tratamiento de quiste de Baker, tratamiento de gangliones, tratamiento de las bursitis, infiltraciones y tratamiento de la fascitis plantar, la fibrosis plantar, las epicondilitis, las tendinopatía del tendón de Aquiles o del neuroma de Morton, punción- lavado de calcificaciones en la tendinopatía calcificante. En cuanto a los procedimientos guiados por tac, revisaremos los siguientes: diagnóstico de las espondilodiscitis, PAAF de las metástasis, artrografía, drenajes. También haremos un recordatorio de procedimientos más complejos que deben realizarse en el entorno adecuado: biopsias óseas, tratamiento del dolor facetario, radiofrecuencia terapéutica.
We aim to describe imaging-guided (ultrasound and CT) interventional techniques in the musculoskeletal system that can be performed by general radiologists, whether in hospitals, primary care clinics, private offices, or other settings.
The first requirement for doing these procedures is adequate knowledge of the anatomy of the musculoskeletal system. The second requirement is to inform the patient thoroughly about the technique, the risks involved, and the alternatives available in order to obtain written informed consent. The third requirement is to ensure that the procedure is performed in accordance with the principles of asepsis in relation to the puncture zone and to all the material employed throughout the procedure.
The main procedures that can be done under ultrasound guidance are the following: fine needle aspiration cytology (FNAC), core needle biopsy (CNB), diagnostic and/or therapeutic arthrocentesis, drainage of juxta-articular fluid collections, drainage of abscesses, drainage of hematomas, treatment of Baker's cyst, treatment of ganglia, treatment of bursitis, infiltrations and treatment of plantar fasciitis, plantar fibrosis, epicondylitis, Achilles tendinopathy, and Morton's neuroma, puncture and lavage of calcifications in calcifying tendinopathy. We also review the following CT-guided procedures: diagnosis of spondylodiscitis, FNAC of metastases, arthrography, drainages. Finally, we also mention more complex procedures that can only be done in appropriate settings: bone biopsies, treatment of facet joint pain, radiofrequency treatment.
El presente artículo es un trabajo de revisión destinado a mostrar al radiólogo general los principales procedimientos de intervencionismo en el área de musculoesquelético tanto diagnósticos como terapéuticos con guía de imagen (ecografía y tomografía computarizada [TC], principalmente).
En primer lugar, debemos recordar que el paciente debe ser informado del procedimiento que se le va a realizar, las alternativas diagnósticas o terapéuticas y los riesgos e inconvenientes de su práctica. El paciente tendrá que consentir por escrito su realización. La ley de autonomía del paciente regula que el consentimiento informado debe obtenerse con antelación, de modo que el paciente tenga tiempo para reflexionar o consultar cualquier duda.
En segundo lugar, es necesario disponer antes de la realización del procedimiento de un recuento plaquetario, un estudio de coagulación, así como conocer si está bajo tratamiento anticoagulante y antiagregante. De forma general, consideramos que es suficiente un recuento plaquetario superior a 50 000 plaquetas/μl y un valor normal del índice internacional normalizado (INR) entre 1-1,2 (no existe consenso en el caso del tiempo de protrombina). Por lo general, si el paciente está en tratamiento con fármacos anticoagulantes orales, se pasará previamente a heparinas de bajo peso molecular, que se suspenderán 8-12 h antes del procedimiento. En el caso de los pacientes que están en tratamiento con antiagregantes (aspirina, clopidogrel, etc.), en los procedimientos con alto riesgo de sangrado (radiofrecuencia de tumores óseos) es necesario suspender el tratamiento 7-10 días antes de su realización, mientras que en aquellos procedimientos con bajo riesgo de sangrado (drenaje de colección superficial, punción-aspiración con aguja fina, etc.) no sería necesaria su retirada.
Será conveniente disponer de una vía intravenosa, por si es necesario administrar medicación intravenosa durante el procedimiento (analgesia o ansiolíticos).
El paciente se colocará en una posición cómoda.
A continuación se procederá con la asepsia de la piel, bien con povidona yodada o con clorhexidina, que se prefiere en pacientes alérgicos al yodo, embarazadas o lactantes.
El tipo de aguja (intradérmica, intramuscular, Chiba, espinal o de biopsia conectada a un sistema automático) dependerá del procedimiento que se vaya a realizar, la profundidad de la lesión o la región anatómica a la que se pretende acceder.
Los anestésicos locales de tipo amida (bupivacaína, lidocaína, mepivacaína, prilocaína, ropivacaína) son los más utilizados. Nosotros empleamos normalmente mepivacaína al 1% o al 2%.
El bicarbonato potencia el efecto anestésico del fármaco, con una inyección previa a la del anestésico o bien mezclado con este.
Podemos resumir los procedimientos de los que vamos a hablar en la tabla 1.
Listado de procedimientos intervencionistas en patología musculoesquelética
| Procedimientos guiados por ecografía |
| 1. Diagnósticos |
| PAAF |
| Biopsias |
| Artrocentesis |
| 2. Terapéuticos |
| Drenajes: |
| Colecciones |
| Abscesos |
| Hematomas |
| Quiste de Baker |
| Gangliones, |
| Bursitis |
| Infiltraciones: |
| Fascitis plantar / fibromatosis plantar |
| Epicondilitis |
| Tendón de Aquiles |
| Neuroma de Morton |
| Punción / lavado de Calcificaciones |
| Procedimientos guiados por TC |
| 1. Diagnósticos |
| PAAF |
| Biopsias |
| Infecciones |
| Tumores/metástasis |
| Tumores óseos. |
| Artrocentesis |
| 2. Terapéuticos |
| Drenajes: |
| Dolor facetario |
| Infiltracion terapéutica |
| RF facetaria |
| Infiltración epidural |
| Radiofrecuencia de otras lesiones |
Es importante que la sonda y parámetros de imagen sean los más adecuados para una óptima visualización ecográfica de la zona. A menudo se podrán utilizar sondas lineales de alta frecuencia, con mayor resolución, en estructuras superficiales. Si se trata de estructuras a mayor profundidad, será necesario el uso de sondas de menor frecuencia.
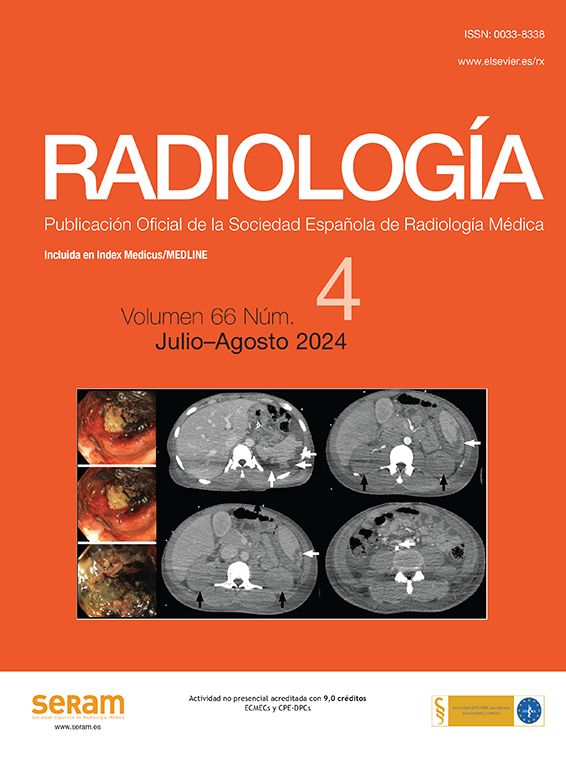
Existen dos modalidades de visualización ecográfica de la aguja: en plano o longitudinal y fuera de plano o transversal (fig. 1). Generalmente se utiliza el primero, que permite la visualización en tiempo real de todo el eje longitudinal de la aguja y el avance del disparo. La desventaja es que el recorrido de la aguja es mayor y requiere también más espacio cutáneo de trabajo, lo que puede ser dificultoso en estructuras pequeñas, como la mano o el pie. Además, cuando la lesión es profunda y requiere una angulación de la aguja de más de 45°, la visualización ecográfica de esta es dificultosa con el abordaje en plano.
Procedimientos diagnósticosPunciones y biopsiasLa biopsia percutánea es un procedimiento mínimamente invasivo, indicado siempre que sea necesario disponer de histología, para confirmar un diagnóstico (tumor primario, recidiva o metástasis) o disponer de información con interés terapéutico o pronóstico (genética, marcadores, etc.)1–7.
En relación con las técnicas de biopsia percutánea diferenciamos:
- •
Punción con aguja fina (PAAF): se obtiene un aspirado celular para su análisis citológico. Se utilizan agujas finas (20-25 G). Su principal ventaja es ser poco traumática, frente a su principal limitación: no aporta información estructural.
- •
Biopsia con aguja gruesa (BAG): se usan agujas más gruesas (14-18 G), las cuales pueden ser de disparo manual o automático.
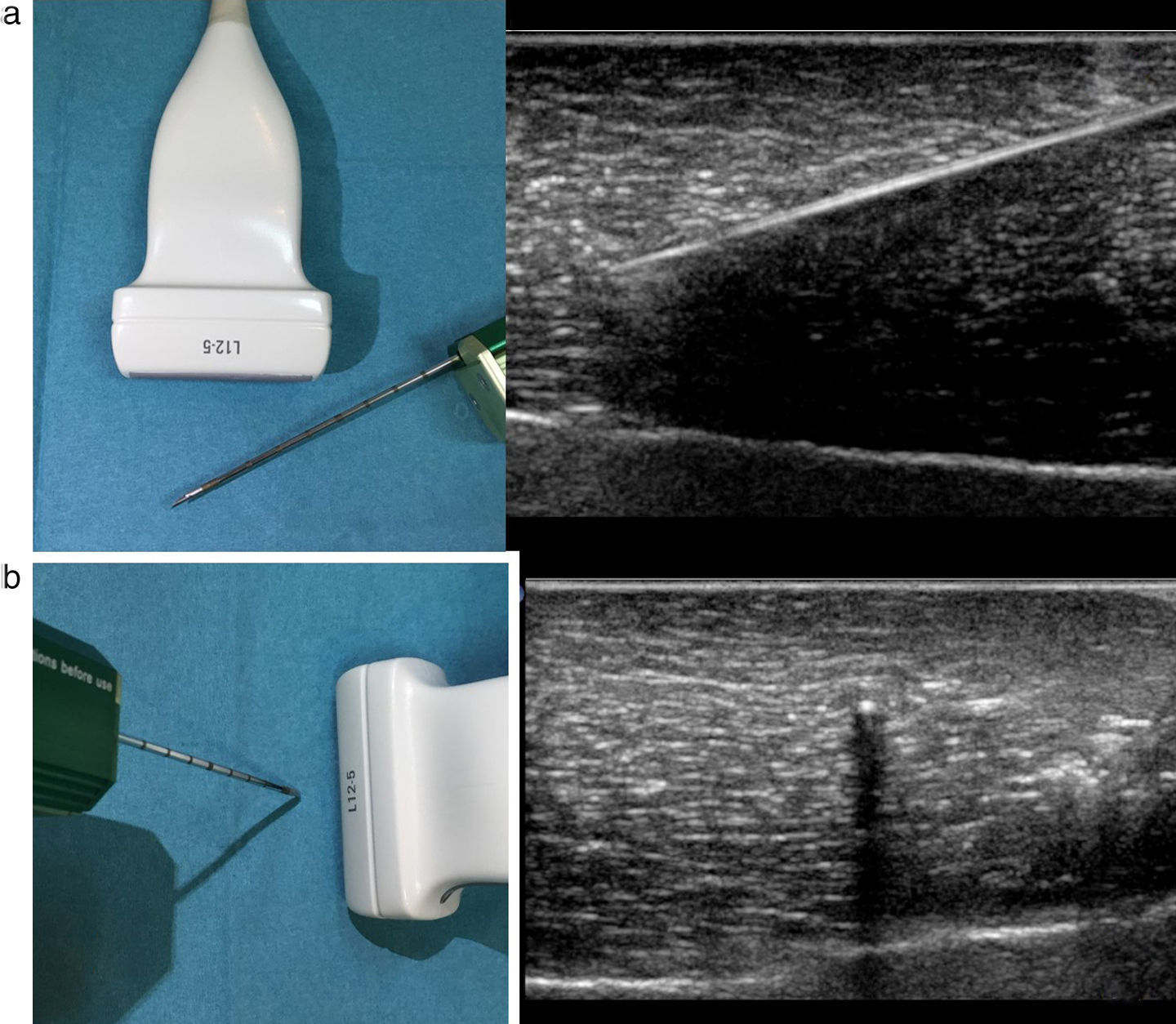
Se pueden utilizar dos tipos de agujas: de corte frontal, en el que el cilindro externo en el disparo secciona circunferencialmente el cilindro de tejido, o de corte lateral (conocidas como “trucut”), en el que el corte es lateral o semicircunferencial (fig. 2). En las lesiones óseas que rompen la cortical se podrán realizar biopsias del componente tumoral de partes blandas, preferible por ser el componente más activo o agresivo.
Si se trata de un tumor primario sospechoso de malignidad, tras la elección de la aguja, se planificará la toma de biopsia bajo dos requisitos: a) Utilizar el recorrido más corto sin contaminar un compartimento anatómico no afectado directamente por la lesión. Para ello es fundamental conocer la anatomía compartimental3 y disponer previamente de un buen estudio de resonancia magnética (RM) de estadificación locorregional. b) Hacer coincidir la toma de biopsia con el posterior abordaje quirúrgico del tumor. Para ello es fundamental el estudio multidisciplinario (con el cirujano).
En casos con trayectos más difíciles o con mayor riesgo de diseminación, es útil el uso de una aguja introductora, y realizar los distintos pases mediante una técnica coaxial (por el interior de dicha aguja).
En tumores de partes blandas se recomienda la toma de hasta cinco muestras para mejorar el rendimiento diagnóstico, con cilindros de 10mm de longitud4.
La biopsia debe dirigirse a la zona más activa de la tumoración (sólida, vascularizada, con mayor actividad PET o componente de partes blandas de un tumor óseo).
Las muestras de citología (PAAF) se envían en cristales portaobjeto al laboratorio de anatomía patológica en seco y en alcohol. Los cilindros de biopsia se envían en solución de formol al 10%, con las consiguientes precauciones durante la manipulación, en relación con las medidas de prevención de cada centro, para evitar la contaminación del personal que trabaje con dicho compuesto químico.
ArtrocentesisSe define como la punción de la articulación y aspiración del líquido articular de la misma con dos fines: diagnóstico y terapéutico.
Las indicaciones más comunes son: a) El diagnóstico de diferentes artropatías mediante el análisis del líquido sinovial: por ejemplo, en la artritis séptica o artritis inducida por cristales (urato monosódico o pirofosfato de calcio). b) Con fines diagnósticos para completar el estudio articular mediante la inyección de medios de contraste intraarticular para una artro-RM o artro-TC. c) Confirmación de un hemartros como expresión de una lesión ósea o ligamentosa, así como el alivio terapéutico mediante la descompresión de la articulación con su evacuación.
Las artrocentesis habitualmente las practican otros especialistas, pero en ocasiones precisan de control ecográfico, bien por fracaso de la realizada “a ciegas” (en derrames pequeños o pacientes obesos, derrames muy loculados o muy densos) o bien en articulaciones poco accesibles como la cadera.
Es contraindicación absoluta no poder evitar atravesar tejidos infectados al acceder a la articulación, ya que la aguja podría infectar una articulación previamente estéril. Con respecto al tratamiento anticoagulante, diferentes estudios establecen que es segura la realización de una artrocentesis en pacientes con tratamiento crónico con anticoagulantes5.
Técnica: No es necesaria la administración previa de anestésico local en la mayoría de los casos, aunque en articulaciones profundas se puede optar por anestesiar el trayecto. La punción de la cadera en niños suele requerir sedación.
La elección de la aguja depende, como en todos los procedimientos intervencionistas, de la región anatómica, el objetivo y la consistencia del fluido que va a ser aspirado. Por lo general, es conveniente utilizar agujas con calibre 14-18 G. En cambio, para la administración de sustancias, son preferibles agujas más finas. Cuando el contenido intraarticular es muy espeso, es necesario el uso de catéteres con calibre 7-8 F, que permitan el drenaje de este.
Articulaciones específicas:
- 1.
Articulación glenohumeral: con visualización ecográfica en tiempo real es preferible el acceso posterior: con el brazo en aducción y rotación externa, introduciendo la aguja de fuera hacia dentro hacia el espacio articular, a través del tendón infraespinoso, en dirección a la cabeza humeral.
- 2.
Articulación del codo: se coloca al paciente con el brazo apoyado y el codo colocado en flexión de 90°. Se obtiene una visión longitudinal y transversal del receso posterior (en la fosa olecraneana), con un abordaje en el plano longitudinal de la aguja. El abordaje transversal al receso articular permite evitar más fácilmente el tendón del tríceps (con un trayecto profundo al mismo).
- 3.
Articulación de la cadera: la punción se realiza en la concavidad existente entre la cabeza del fémur y la superficie anterior del cuello quirúrgico, con el paciente en decúbito supino y la cadera en rotación externa, estando la aguja alineada con el eje del cuello quirúrgico del fémur.
- 4.
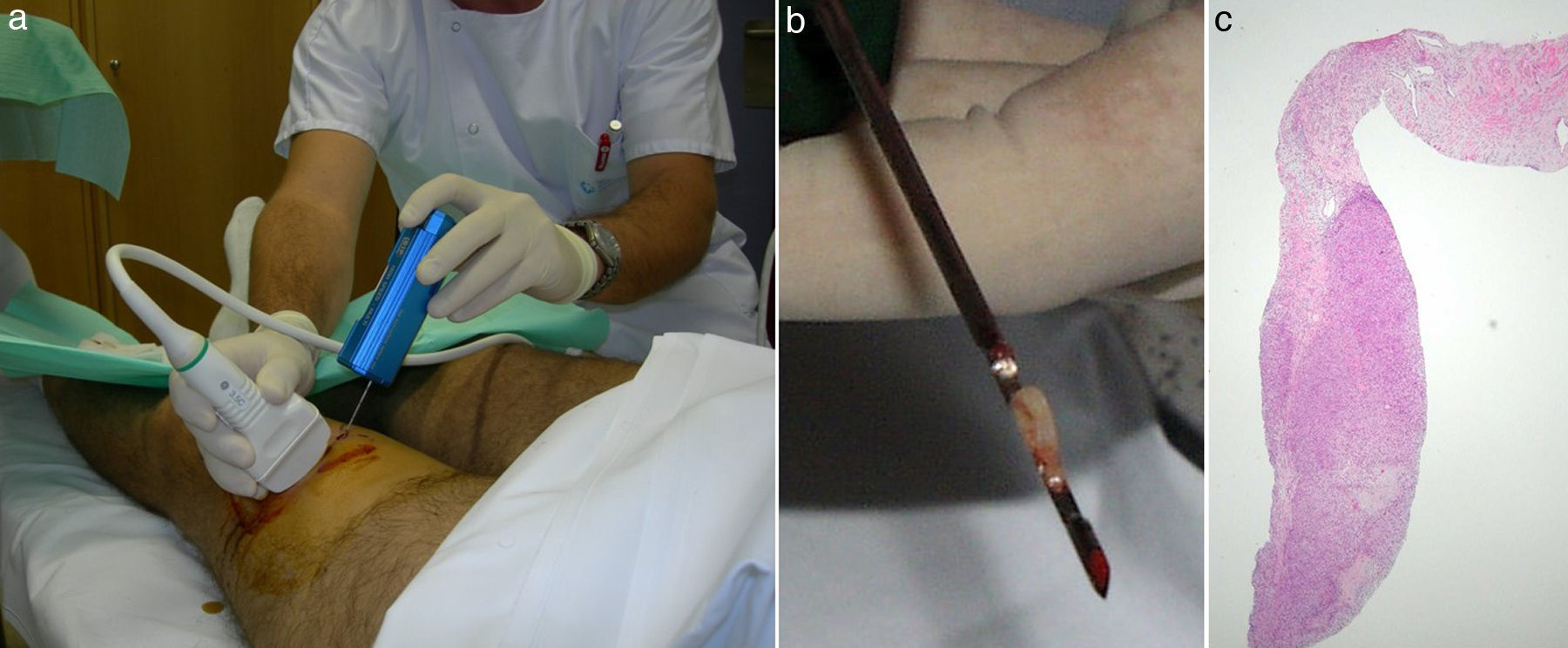
Articulación de la rodilla: con el paciente en decúbito supino y la rodilla en ligera flexión, el abordaje es lateral entre la rótula y el fémur, evitando el tendón rotuliano (fig. 3).
- 5.
Articulación del tobillo: con la rodilla en flexión y el pie apoyado sobre la camilla, la aguja se introduce en la cara anterior del tobillo, en el receso tibiotalar anterior.
Entre las sustancias que podemos introducir con fines terapéuticos en la artrocentesis disponemos de:
- •
Corticoides: Se utiliza 1 ampolla de 40mg de triamcinolona (trigon depot®) mezclado con 1ml aproximadamente de anestésico(1-2ml de lidocaína o mepivacaína), con el siguiente principio: no inyectar más de dos articulaciones a la vez, más de 3 veces al año una misma articulación ni con una frecuencia de más de 1 vez en 2-3 meses, aunque no está del todo establecido el número máximo de veces, si bien no se recomienda abusar de esta técnica, dado que el exceso de corticoides se ha asociado a una pérdida de elasticidad del cartílago en las articulaciones de carga.
- •
Ácido hialurónico para lubricar la articulación.
- •
Urocinasa intraarticular, con el fin de lisar hemartros con coágulos y tabiques de fibrina, para favorecer su drenaje. Se usa habitualmente una dosis de 100 000-250 000 UI de urocinasa disuelta en 30ml de suero salino. Tras una espera de 1-2h, se aspira el contenido intraarticular. La colocación de un drenaje favorece el vaciado de contenido espeso y se retira cuando se produzca la resolución del hemartros.
- •
La sinoviortesis química o la radioisotópica escapa al objetivo de nuestro trabajo.
El tratamiento de algunas colecciones yuxtaarticulares se puede realizar guiado por TC, ecografía o fluoroscopio6,7. Dichas entidades incluyen quistes dependientes de una articulación, incluyendo a los gangliones intraneurales, que deben ser debidamente identificados. El tratamiento de elección de estas colecciones yuxtaarticulares es mediante guía ecográfica.
Los quistes yuxtaarticulares son de ecoestructura más o menos homogénea hipo o anecogénica. La punción aspiración de estos, por un lado, alivia por descompresión y, por otro, cuando existe sospecha clínica, permite el estudio bacteriológico de una posible infección y el tratamiento por drenaje (véase más adelante). Descartada la infección, la aspiración y posterior infiltración de corticoides puede ser una alternativa, mínimamente invasiva, a la cirugía. Por ejemplo, en el tratamiento de los quistes parameniscales o en la grasa de Hoffa, y en quistes paralabrales del hombro y la cadera, asociados a desgarro del labrum, que pueden ser dolorosos o dar síntomas por compresión neural.
AbscesosEn ocasiones, pese a instaurar un tratamiento antibiótico adecuado, es preciso evacuar colecciones de pus que se forman en el seno de un quiste, bursa, articulación o cualquier otra zona infectada. El drenaje guiado por imagen es de elección en todas aquellas colecciones sintomáticas, no solo como herramienta diagnóstica (muestras microbiológicas), sino por su eficacia terapéutica. Hasta en un 80% de los casos consigue resolver el absceso y evitar la cirugía, controlando la infección y facilitando una posterior cirugía electiva1.
Técnica:
- •
Aspiración directa con aguja: mediante una aguja de calibre grueso (14–21 G), en colecciones pequeñas (<3cm) y no demasiado espesas.
- •
Colocación de catéteres de drenaje. Los catéteres diseñados para tal fin son tubos de plástico de diferente material y grosor (5-12 Fr que equivale a 2-4 mm), con un extremo distal curvo o en “cola de cerdo” (pigtail), que evita que se salga fácilmente, y en el cual existen varias perforaciones para favorecer el drenaje (fig. 4):
- –
Técnica de Seldinger. La técnica consiste en la punción directa mediante una aguja gruesa (14 G-18 G). A continuación se retira el estilete y se introduce coaxial una guía al interior del absceso. Se retira la aguja y se deja la guía, a través de la cual se introduce el catéter, directamente o tras el uso de tubos progresivamente más gruesos llamados dilatadores. Aunque es más laborioso, es aconsejable si el trayecto es rígido o duro, como por ejemplo por fibrosis.
- –
Técnica trócar. En estos casos, el catéter viene montado sobre una guía rígida metálica hueca, a través del cual se introduce un estilete metálico. El trócar se introduce en la colección por punción directa a través de la piel. Una vez el extremo en la colección, se retira el estilete y se desliza el catéter propiamente sobre la guía metálica, hasta progresar en el interior de la colección todo el extremo curvo, con los agujeros de drenaje. Es una técnica más rápida y sencilla, siempre que el trayecto no sea demasiado rígido.
- –
El drenaje deberá controlarse periódicamente, con lavados con 10-20ml de suero salino cada 6-8h, y se registra la cantidad de volumen drenado diariamente. El catéter se retirará cuando el paciente permanezca afebril, mejoren los reactantes de fase aguda en la analítica y el débito del drenaje sea inferior a 10ml durante 3 días consecutivos. En ocasiones, para favorecer el drenaje, es preciso el uso de agentes fibrinolíticos para disminuir la densidad y romper los septos que pudieran formarse en el interior de la colección.
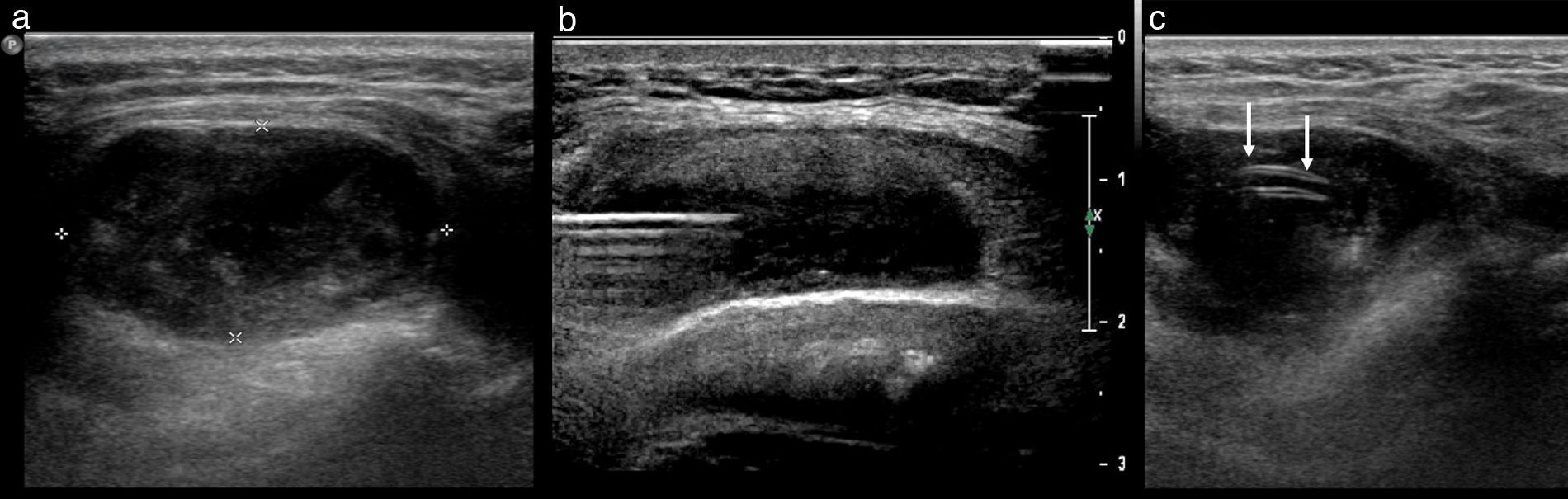
HematomasEl origen de los hematomas musculoesqueléticos suele ser por traumatismo deportivo. Circunstancias como la anticoagulación o trastornos de la coagulación pueden predisponer a su formación. La evacuación ecoguiada permite, por un lado, un alivio de los síntomas compresivos que produce, y por el otro favorece la curación de la lesión subyacente, acortando el tiempo de inactividad. Una contraindicación del drenaje de los hematomas es el sangrado activo. Ante la evacuación persistente de sangre roja (frente a la oscura del hematoma normal) se deberá sospechar esta posibilidad y realizar angio-TC. La técnica es superponible al drenaje de abscesos, aunque es más frecuente en el hematoma agudo-subagudo la necesidad de fibrinolíticos como la urocinasa (a dosis de 100 000-200 000 UI), para disolver los coágulos y favorecer el drenaje7.
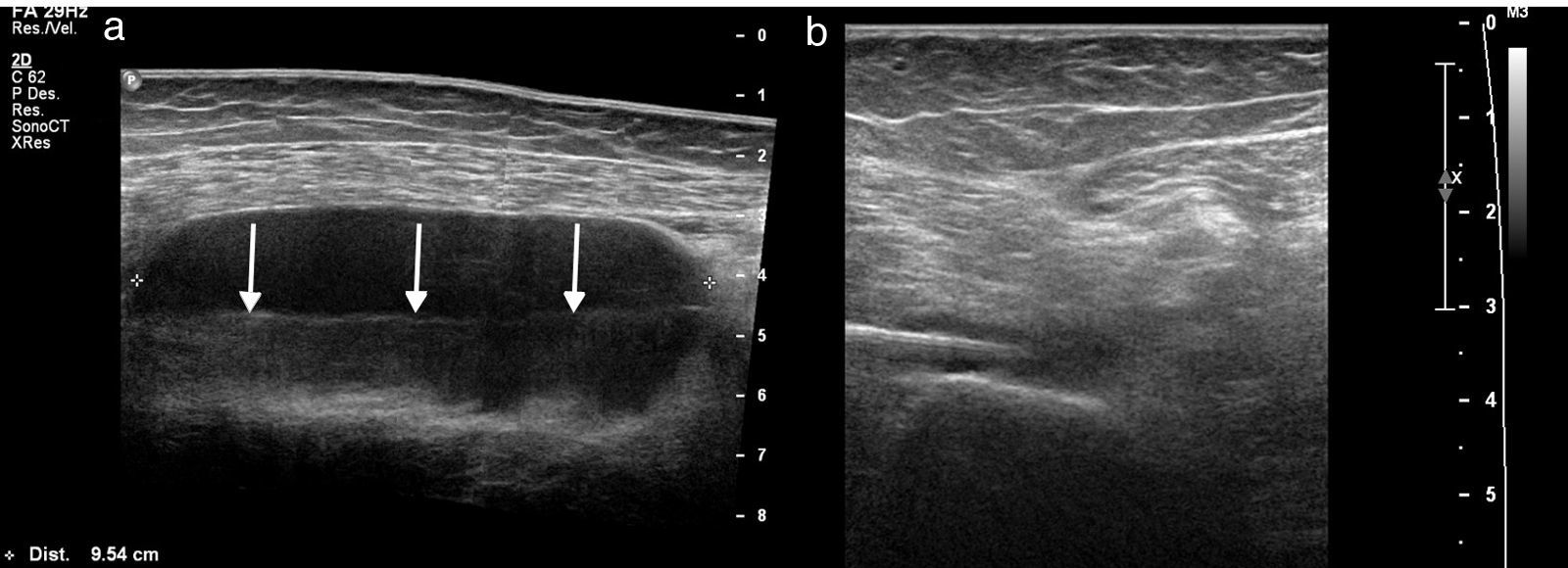
Los hematomas susceptibles de drenaje característicos de rotura miofascial son los localizados entre gastrocnemio medial y sóleo (“pierna de tenista”) (fig. 5), y en el recto anterior y vasto intermedio o crural del cuádriceps femoral. Debe pautarse profilaxis de trombosis venosa profunda con heparinas de bajo peso molecular y profilaxis antibiótica.
a) Drenaje de hematoma de gran tamaño entre gastrocnemio medial y sóleo, como complicación de una rotura mioaponeurótica distal del gastrocnemio medial. Puede observarse el contenido ecogénico que requiere la introducción de urocinasa, previamente al drenaje. b) Catéter de drenaje (flechas).
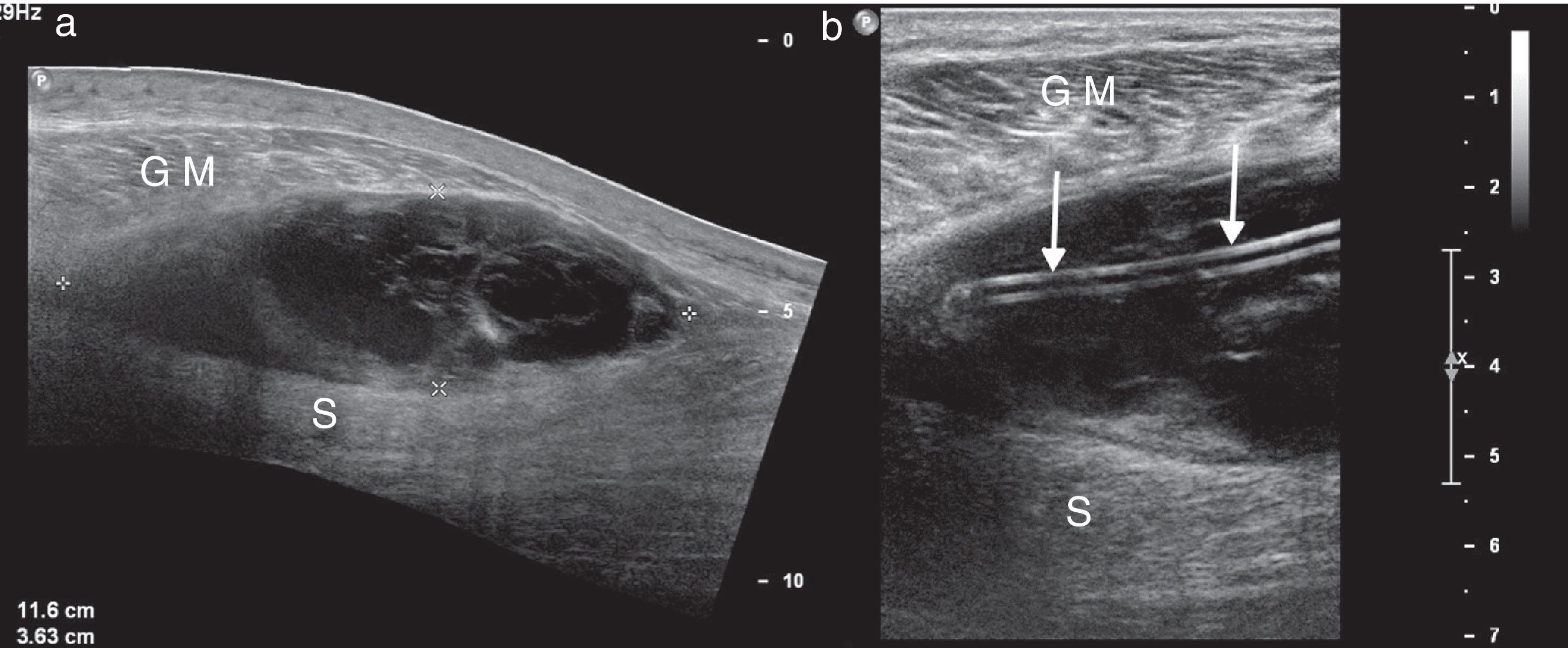
El tratamiento de este quiste mediante procedimientos ecoguiados se ofrece a aquellos pacientes muy sintomáticos, bien por efecto compresivo sobre estructuras adyacentes debido a su gran tamaño, que puede derivar en otras complicaciones, o bien por dolor crónico e impotencia funcional. Las inyecciones ciegas en estos quistes pueden potencialmente dañar el paquete vasculonervioso poplíteo. El uso de guía ecográfica también ayuda a identificar septos dentro del quiste, que permiten modificar la estrategia de la punción, atravesando los septos o efectuando más de un acceso.
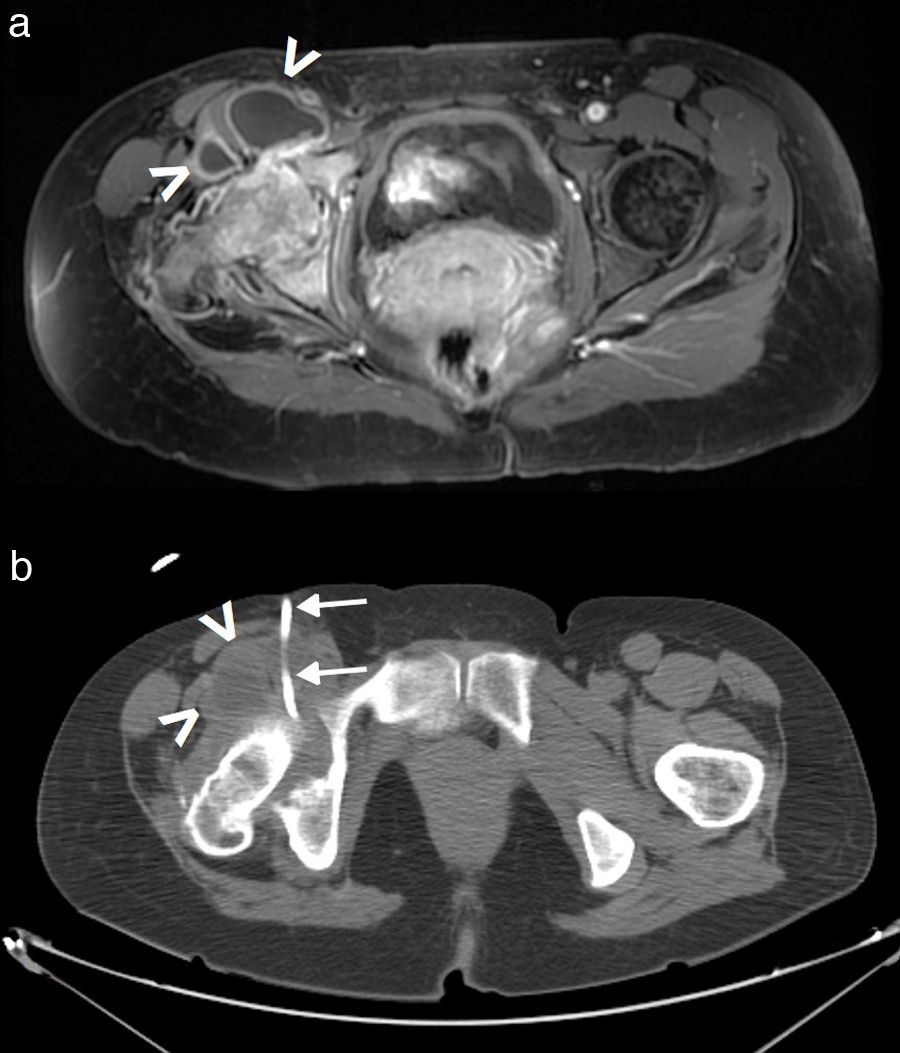
Técnica: El paciente se coloca en decúbito prono con la rodilla en ligera flexión. Una exploración preliminar confirma su dependencia de la bursa entre los tendones gastrocnemio medial y semimembranoso, y se identifican las estructuras neurovasculares poplíteas. El transductor se coloca en el plano más adecuado que permita un abordaje cómodo y más directo con visualización de la aguja en plano (longitudinalmente). Con una aguja de 18-20 G o bien con catéteres de acceso vascular de esos mismos calibres, se aspira el líquido y a continuación se inyecta corticoide solo (40mg de acetónido de triamcinolona), o en combinación con anestésicos locales (1-2ml de lidocaína o mepivacaína), para evitar la recidiva y tratar la inflamación (fig. 6).
a) Quiste de Baker sintomático. Imagen de RM, secuencia DP con saturación grasa, plano axial. b) Drenaje ecodirigido (aguja señalizada con las flechas). Se finalizó con infiltración de corticoides. Flechas huecas: tendones gastrocnemio medial y semimembranoso. c) Quiste completamente drenado.
Se utilizan generalmente agujas de calibre grueso (hasta 14 G), por el contenido denso del quiste. Puede ayudar la introducción de suero salino para su dilución y así facilitar la aspiración. Cuando son muy superficiales, puede ser eficaz la evacuación del contenido a través del tracto de la aguja (comprimiendo el ganglión una vez retirada esta).
Se ha establecido que la inyección de esteroides tras la aspiración presenta una tasa de resolución del 87%8, aunque es variable según autores. Como en otras localizaciones superficiales, debe tenerse presente que el paso de corticoides al tejido graso subcutáneo puede producir atrofia de la grasa y despigmentación de la piel. La metilprednisolona es más segura en este sentido que la triamcinolona. El uso de alcohol puro, dejándolo actuar durante una hora, estimula la fibrosis de la pared del ganglión y cicatrización del mismo.
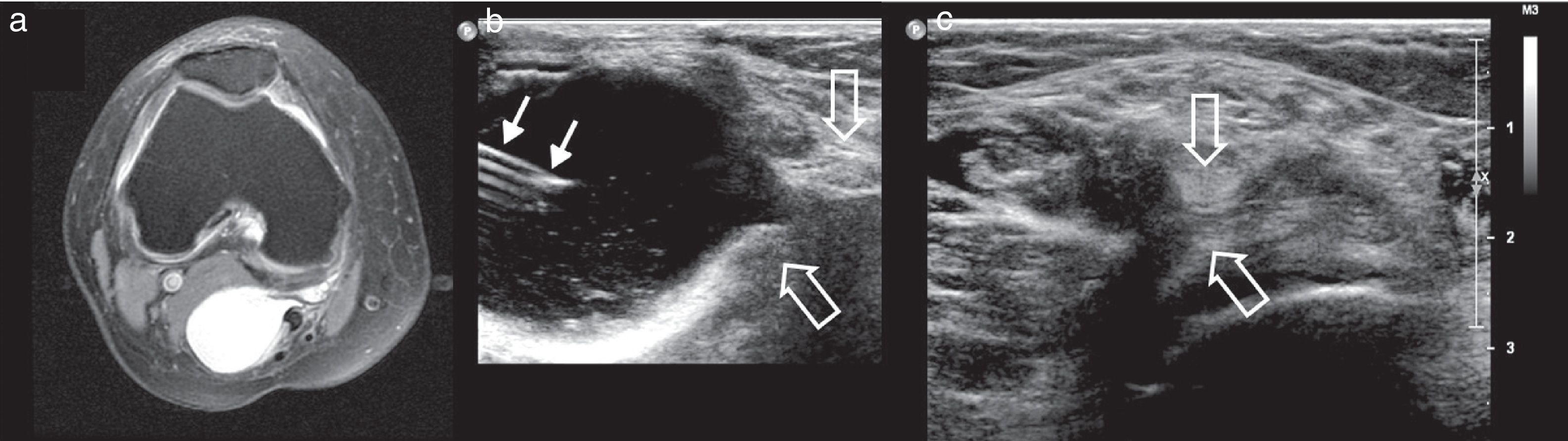
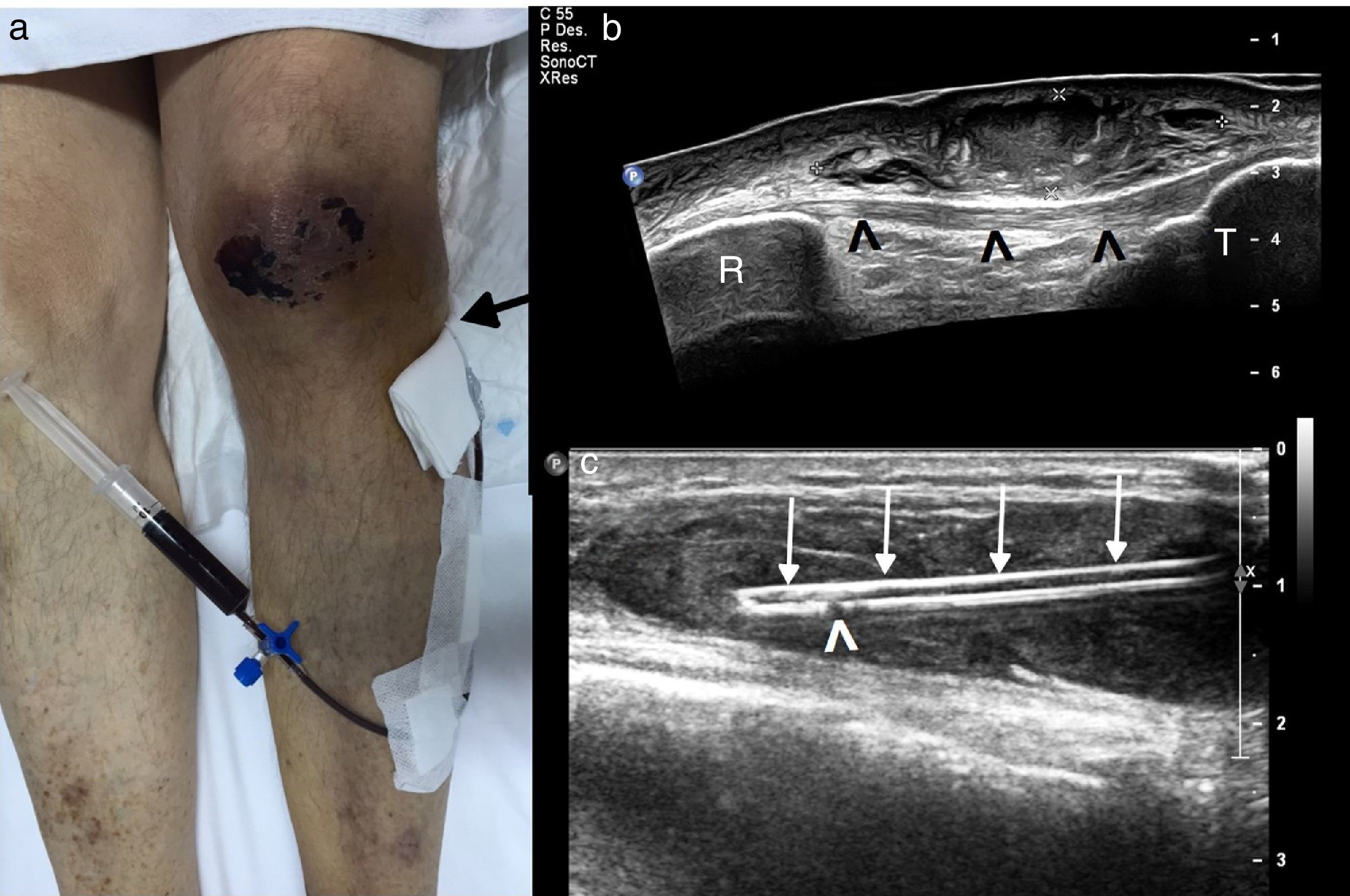
BursitisCuando no existe infección, se inyectan corticoides en el interior de la bursa. En los que hay colección líquida suficiente, se aspira previamente con agujas 16-21 G. En los casos infectados, se drena de manera similar al drenaje de abscesos, y está contraindicado el uso de corticoides. Las bursas que más frecuentemente se tratan9 son la subacromial, la peritrocantérea, el iliopsoas y la preaquílea (sobre todo en el síndrome de Haglund). También se tratan la prepatelar (fig. 7), la olecraneana y la retroaquílea. Al ser superficiales, se dispone de buena visualización de toda la aguja con técnica longitudinal o en plano10.
a) Drenaje de hematoma en la bursa prepatelar que se extiende a hematoma subcutáneo en margen lateral de la rodilla, mediante catéter 5 Fr (flecha negra marca la entrada en la piel), tras introducción de 200 000 U de urocinasa durante 2 horas. Se extrajeron 40ml y se envió muestra para estudio microbiológico, con resultado negativo. b) Colección delimitada por las marcas de medición. Puntas de flecha negra: tendón patelar. c) Flechas blancas: catéter. Puntas de flecha blanca: orificio lateral del catéter.
Cuando el tratamiento conservador falla, antes de recurrir al tratamiento quirúrgico debemos considerar los procedimientos terapéuticos mínimamente invasivos guiados por ecografía. En este sentido, la inyección de corticoides (1 ampolla de 40mg de triamcinolona) es una manera eficaz de tratarla de forma conservadora. Una complicación añadida al uso de corticoides es la atrofia de la almohadilla grasa subcutánea.
Con el paciente en decúbito prono, preferimos un abordaje transversal a la fascia, con infiltración perifascial inmediatamente proximal a su inserción calcánea, con técnica longitudinal de la sonda respecto de la aguja, que se introduce desde medial (fig. 8).
Infiltración de la fascia plantar con abordaje transversal a la fascia y visualización en plano (a). b) Infiltración para-fascial profunda y proximal. TC: tuberosidad calcánea de inserción fascial. c) Infiltración parafascial superficial y más distal que en b. C: calcáneo. d) Plano longitudinal de la fascia plantar engrosada (fascitis), tras la infiltración, con líquido perifascial (*). Puntas de flecha: fascia plantar. Flechas: aguja.
Otra alternativa efectiva (hasta en el 70% de los pacientes) es la punción seca, que consiste en la punción repetida de la fascia plantar engrosada hasta el periostio, con un abordaje paralelo a la orientación de las fibras de colágeno o longitudinal.
Fibrosis plantarUna alternativa al tratamiento quirúrgico de esta patología consiste en la infiltración perifascial con corticoides, ecoguiada y con aguja fina. Se puede realizar un abordaje lateral o longitudinal a la fascia en función de la morfología de la fibrosis, en plano con el eje largo de la aguja.
Epicondilitis y otras tendinopatíasLa infiltración de corticoides se dirige a la unión miotendinosa11 de la zona más afectada, normalmente la anterior (extensor radial corto del carpo), donde habitualmente se demuestra aumento de señal de flujo Doppler. Se puede realizar también una perforación seca del conjunto tendinoso extensor, en el eje longitudinal hasta el plano óseo, y terapia esclerosante (véase más adelante en tendón de Aquiles). La técnica ecodirigida evita además la infiltración de corticoides directamente en el tendón o bien en el tejido celular subcutáneo.
Infiltraciones en tendón de AquilesEl tratamiento conservador para la tendinopatía del tendón de Aquiles fracasa en casi el 50% de los casos. De nuevo una alternativa interesante a la cirugía es el tratamiento mínimamente invasivo ecodirigido12. Se coloca al paciente en decúbito prono con una almohada debajo del tobillo, dejando al pie colgando libremente. Colocamos el transductor perpendicular a las fibras del tendón y el acceso de la aguja se suele hacer desde la parte medial del tobillo, para evitar la lesión del nervio sural. El procedimiento comienza con la administración de anestesia local a nivel de la piel y el tejido celular subcutáneo (otra opción que considerar sería la anestesia troncular del nervio tibial):
- •
La inyección local de corticoides en el tratamiento de la tendinopatía crónica del tendón de Aquiles es controvertida, fundamentalmente por el riesgo potencial de rotura del tendón relacionada con la inyección intratendón. No obstante, no hay estudios concluyentes que hayan demostrado un efecto adverso de la inyección de esteroides en el paratenón. La inyección de otras sustancias peritendón como el factor de necrosis tumoral α (adalimumab) o el antagonista del receptor de la interleucina 1, han ofrecido buenos resultados en cuanto a la mejoría de los síntomas, así como la disminución del componente inflamatorio del propio tendón. Sin embargo, su combinación con rehabilitación se ha relacionado con recaídas precoces.
- •
La adhesiotomía de volumen mediante inyección de grandes volúmenes de solución salina normal en el tendón de Aquiles (previa inyección en la almohadilla grasa de anestésico local con un poco de esteroides) produce efectos mecánicos locales con rotura u oclusión de los neovasos, lo que conlleva a una reducción significativa del dolor y la mejoría de la función del tendón.
- •
Terapia esclerosante: basada en la proliferación de pequeños vasos de alto flujo en el espesor del tendón afectado por tendinopatía, encontrándose en muchas ocasiones próximos a las fibras nerviosas y por tanto posible causa de dolor. La esclerosis de estos neovasos se lleva a cabo mediante sustancias como el polidocanol.
- •
Proloterapia mediante inyección de dextrosa hiperosmolar en el área de degeneración del colágeno.
- •
Punción seca y la inyección de sangre autóloga, ya mencionado en otras localizaciones.
- •
Tenotomía percutánea: algunos estudios han comparado sus resultados a los procedimientos quirúrgicos abiertos, aunque también es cierto que en algunos pacientes el estudio ecográfico posterior al procedimiento reveló que seguían existiendo alteraciones en el tendón.
El tratamiento y control de la tendinosis de Aquiles sigue siendo controvertido, agravado por la ausencia de criterios diagnósticos uniformes.
Neuroma de MortonLa inyección de corticoides o de alcohol13 en el neuroma puede proporcionar un alivio temporal y la mejoría funcional, con un intervalo libre de síntomas prolongado, lo que puede retrasar u obviar la cirugía.
Cuando existen dudas diagnósticas sobre si se trata de un neuroma de Morton o una bursitis, se prefiere la inyección de corticoides con guía ecográfica, dado que el tratamiento de la bursitis también es con corticoides.
Técnica: Para realizar esta inyección, se obtiene primero una vista longitudinal del neuroma hipoecoico y localizado en el espacio intermetatarsiano segundo o tercero, con la sonda en el margen plantar. Con abordaje dorsal y en el eje longitudinal de la sonda se introduce una aguja 22-25 G visualizando su entrada hasta entrar en el neuroma. Se inocula acetato de triamcinolona de 40mg o alcohol diluido al 30%. Estas inyecciones pueden repetirse hasta cuatro veces, con un intervalo de 4-6 semanas.
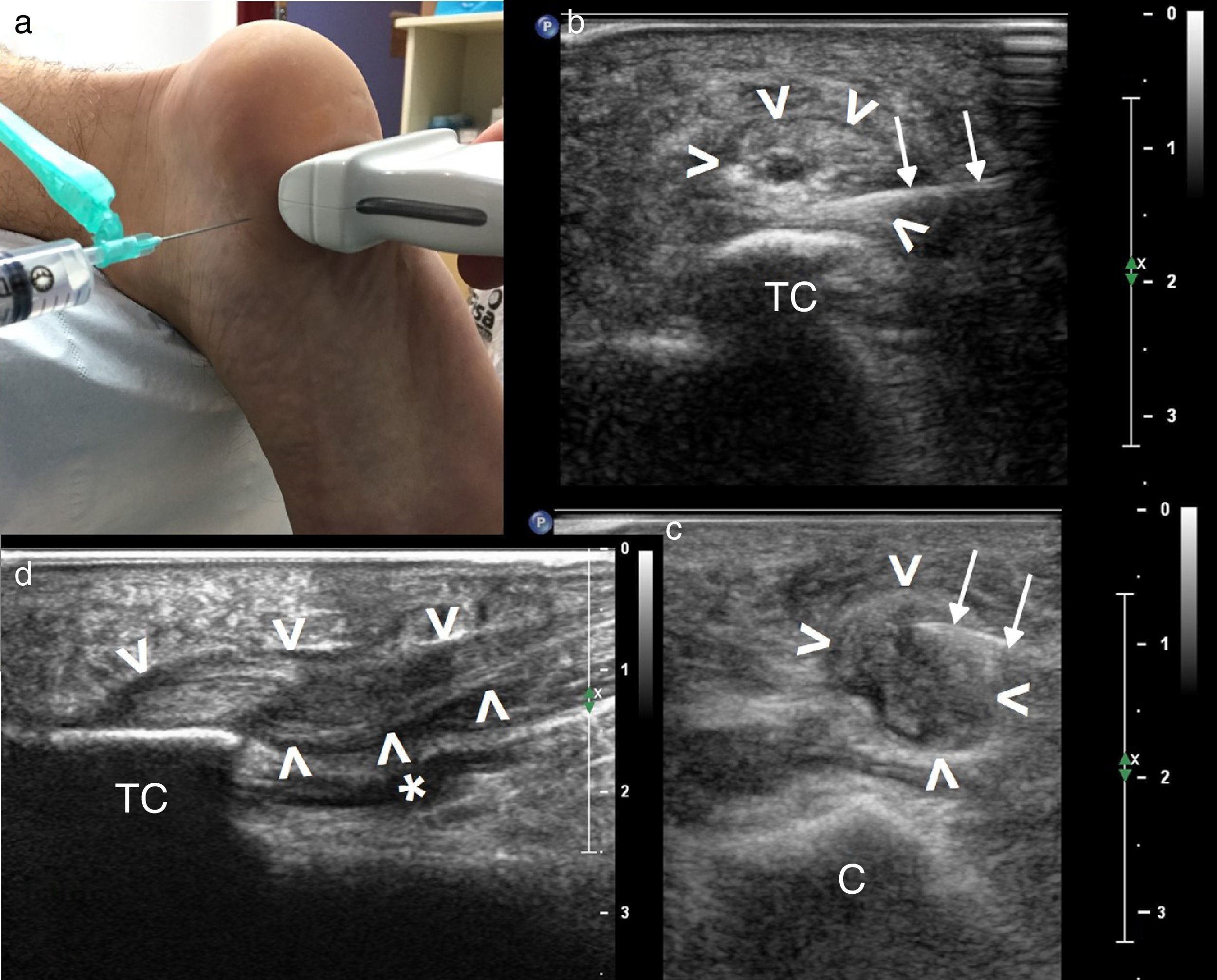
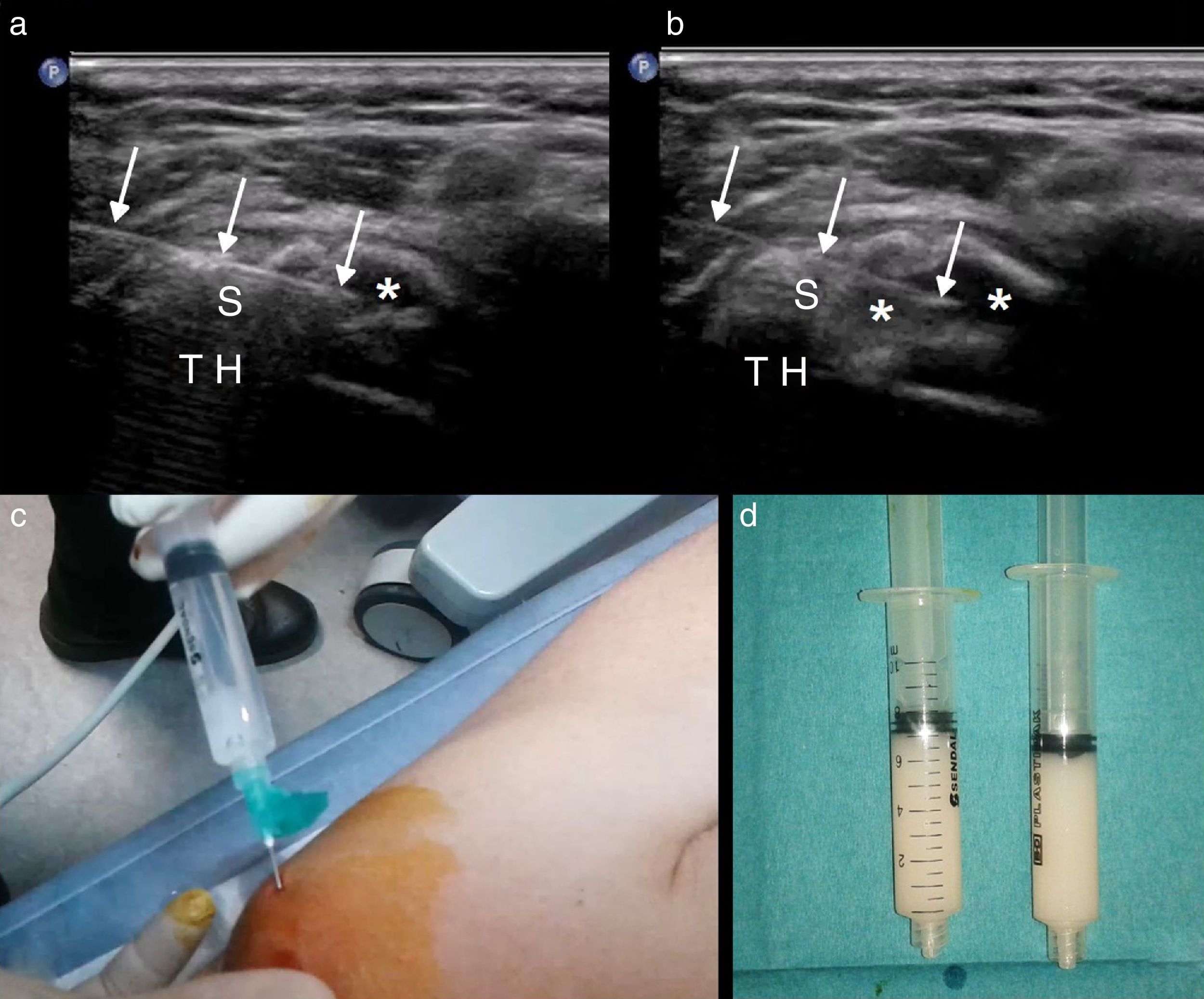
Punción-lavado de calcificacionesLa tendinosis calcificada del hombro causa dolor debilitante crónico y en consecuencia incapacidad funcional. No está indicado tratar aquellas calcificaciones asintomáticas. En los casos sintomáticos, la infiltración de la bursa con corticoides es mucho más efectiva que el tratamiento conservador con antiinflamatorios no esteroideos. Por otro lado, se ha demostrado que el lavado percutáneo ecodirigido del tendón, previo a la infiltración de la bursa, presenta mejores resultados a largo plazo1.
Técnica1: Se coloca al paciente en posición sentada o en decúbito supino, con la mano detrás de la espalda. El brazo se colocará en el grado de rotación más cómodo en función de la localización de la calcificación (externa para subescapular, interna para infraespinoso o supraespinoso), con un abordaje anterolateral. La aguja no debería tener un calibre inferior a 21 G para evitar que se obstruya con el calcio. La unión de la jeringa a la aguja ha de ser de rosca, que evita que por la presión se desconecten durante el procedimiento. Con visualización ecográfica en tiempo real se anestesia el trayecto de la aguja y la bursa, avanzando hasta llegar a la calcificación. Una vez alcanzada, se presiona y se suelta repetidamente el émbolo de la jeringa, una primera vez cargada con anestésico y en un segundo tiempo o posteriores, según el tamaño de la calcificación, con jeringas cargadas con solución salina, que permite el lavado del calcio con una técnica de barbotaje (una solución de calcio pasa a la jeringa por presión) (fig. 9). Cuando el contenido de la jeringa se vuelve turbio, se desconecta y se cambia por otra con suero salino. Se repite hasta que el calcio se sustituye por una pequeña cavidad de aspecto quístico. Finalmente, se canaliza la bursa subdeltoidea y se infiltra con corticoides (1ml de 40mg de triamcinolona con 1ml de mepivacaína).
Lavado percutáneo de tendinosis calcificada del supraespinoso (S), a través de una aguja 20 G (flechas). Técnica de barbotaje soltando (a) y presionando el émbolo (b), que sustituye la calcificación por una cavidad quística (*). TH: tuberosidad mayor humeral. c) Se observa como el calcio “lavado” va enturbiando el interior de la jeringa. d) Jeringas tras el procedimiento: lechada cálcica.
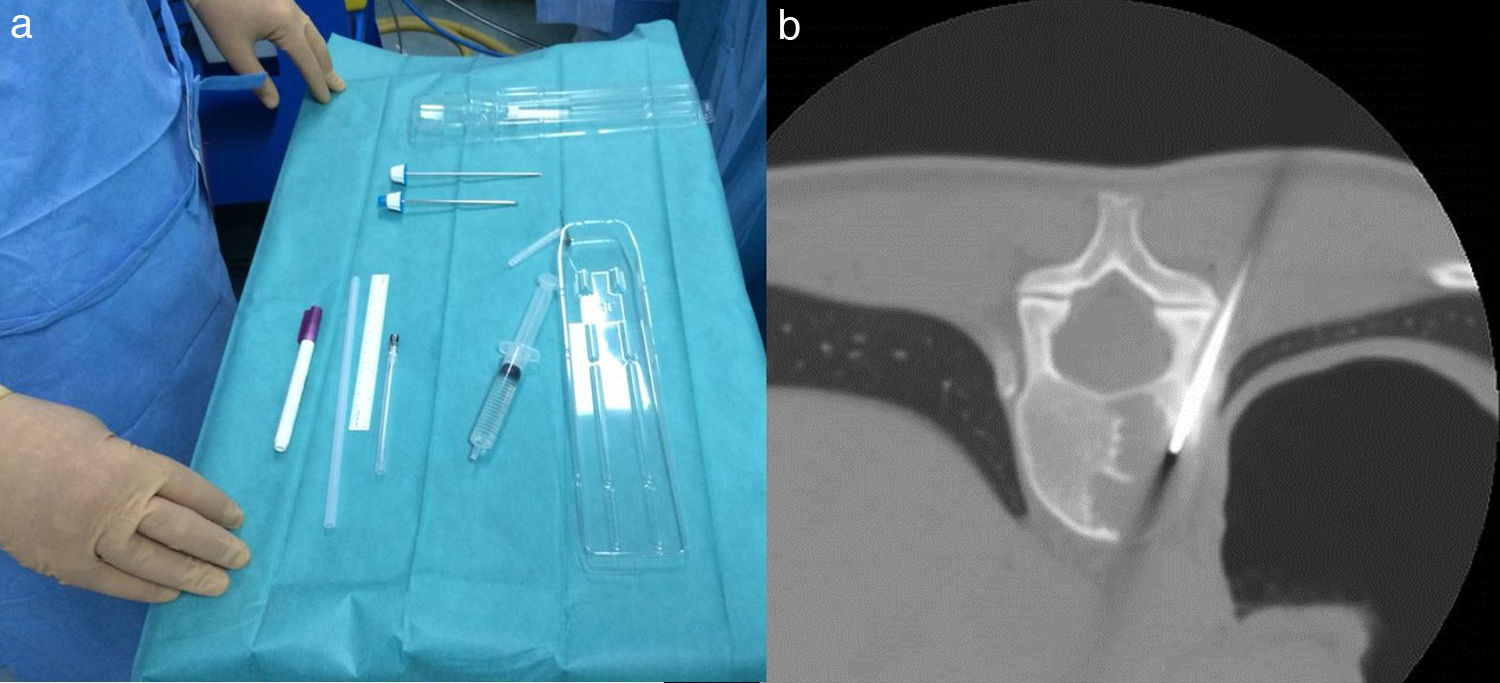
La mayoría de lesiones son espondilodiscitis (fig. 10). La punción comienza con una adecuada asepsia de la piel; algunos autores recomiendan realizarla dos y tres veces antes del procedimiento (para evitar la contaminación), la anestesia del trayecto de la aguja y teniendo en cuenta que se deberán tomar muestras separadas de varias áreas de la lesión: disco periférico, disco central, partes blandas y hueso vertebral, para un mejor rendimiento diagnóstico. Planificaremos de acuerdo con ello el tipo de aguja más adecuada (calibres 11 G hasta 18 G) y el trayecto con guía de TC óptimo.
Toma de muestras para el diagnóstico de metástasisLa biopsia de una metástasis ósea14 es indispensable en:
- •
Ausencia de tumor primario conocido, dado que el examen histológico con marcadores tumorales permite una orientación diagnóstica adecuada para plantear un tratamiento específico.
- •
Intervalo largo entre el diagnóstico de un tumor localizado y la aparición de las metástasis óseas, lo que plantea la posibilidad de otro cáncer metacrónico, distinto al anterior.
- •
Cuando las metástasis óseas aparecen en la evolución de un cáncer con baja probabilidad de metástasis óseas, lo que plantea que se trate de otro tumor primario distinto.
- •
Necesidad de estudio molecular con interés pronóstico y terapéutico.
La rentabilidad diagnóstica de las biopsias percutáneas de metástasis óseas es mayor que las biopsias percutáneas del tumor primitivo. También aumentan la exactitud y rentabilidad de la muestra cuando las lesiones son osteolíticas frente a las osteoblásticas, y cuando la localización es en columna vertebral, la exactitud es cercana al 100%.
La columna vertebral es un asiento frecuente de metástasis. El acceso a las lesiones que se localizan en el cuerpo vertebral puede ser paravertebral, costovertebral o transpedicular. En las biopsias de columna cervical alta se puede utilizar el abordaje oral.
La técnica para la toma de muestras más extendida es la coaxial, que consiste en un método que permite la realización de múltiples biopsias con una sola punción, con lo que disminuye el potencial de complicaciones, las molestias para el paciente, así como el tiempo empleado en su realización. Mediante esta técnica se coloca una aguja del tamaño adecuado para que a través de ella pase otra más fina por su interior y poder realizar múltiples pases.
Toma de muestras para el diagnóstico de tumores óseosComo se mencionó en la biopsia ecodirigida, el principio básico para el abordaje de la lesión3 es que el trayecto de la aguja sea el más corto posible, que no atraviese otro compartimento anatómico y que coincida con la vía de abordaje quirúrgica definitiva, evitando además contaminar el eje vasculonervioso y las articulaciones.
Uno de los aspectos técnicos importantes de la cirugía conservadora ortopédica es la eliminación de la cicatriz de biopsia durante la cirugía de resección tumoral debido a la “posible siembra local” durante el procedimiento.
La PAAF puede ser suficiente en algunos casos (como en el mieloma, granuloma eosinófilo, etc.). No obstante, la biopsia con aguja gruesa ofrece una mayor fiabilidad y aporta información estructural.
Aquí la técnica también empleada para la toma de muestras, al igual que en el apartado anterior, es la coaxial.
La TC permite visualizar el interior del hueso, identificando con facilidad el patrón permeativo óseo, el grado de destrucción, las erosiones secundarias a la lesión tumoral (fig. 11) y determinar el espesor de la matriz calcificada tumoral. Los estudios con contraste permiten, además, definir áreas de necrosis y hemorragia intratumoral que deben evitarse cuando se tomen muestras para biopsia. Las zonas de elección para obtener muestras son: la periferia del tumor y/o el componente de partes blandas, si lo hubiese. Es también preferible biopsiar la zona con mayor actividad metabólica de una lesión (gammagrafía ósea con SPECT o PET-TC). Se debe de pactar con el patólogo la cantidad de muestra necesaria para el diagnóstico.
ArtrografíaLa artrografía previa a la realización de una TC o una RM suele realizarse mediante control ecográfico o mediante fluoroscopia. El tipo de aguja que se emplea para la anestesia y posterior introducción del medio de contraste es una aguja espinal del calibre 21-22 G. Nos referiremos brevemente a las tres localizaciones más frecuentemente demandadas:
- 1.
Hombro: La técnica más usada es el abordaje anterior con el paciente en decúbito supino y el hombro en rotación externa parcial. En esta posición, el borde anterior de la cavidad glenoidea se encuentra medial a la cabeza humeral y el lugar de entrada es superficial al margen medial de la mitad inferior de la cabeza humeral. La aguja penetra a través de la piel, el tendón del subescapular y la cápsula articular, de tal manera que la punta de la aguja queda lateral al margen medial de la cabeza humeral, con lo que se evitan daños en el rodete glenoideo.
- 2.
Cadera: Colocaremos al paciente en decúbito supino y con la cadera en rotación interna, lo que proporciona una mejor visualización del cuello femoral. Se localiza el pulso femoral, de forma que el punto de entrada de la aguja será lateral a 2cm del lugar de la palpación del pulso, por debajo del pliegue inguinal. La dirección de entrada será de anterior a posterior, de lateral a medial y en dirección a la unión de la cabeza con el cuello femoral. La cara medial del cuello femoral es un punto en el que la cápsula articular suele ser más redundante y permite con mayor facilidad la adquisición de fluido de la articulación.
Uno de los problemas que podemos encontrar es que hagamos la inyección en la bursa del iliopsoas. Esto se produce con inyecciones sobre el centro de la cabeza femoral o cuando el abordaje ha sido oblicuo.
- 3.
Rodilla: El paciente se coloca en decúbito supino y con la rodilla ligeramente flexionada. El abordaje de la articulación puede ser lateral o medial, aunque se prefiere este último debido a que el ángulo más pronunciado de la faceta rotuliana medial facilita el acceso a la articulación. Así mismo, el punto de entrada de la piel debe estar a lo largo de la mitad inferior de la articulación femororrotuliana para evitar que la aguja penetre en la almohadilla grasa que se encuentra por detrás de la mitad superior de la rótula.
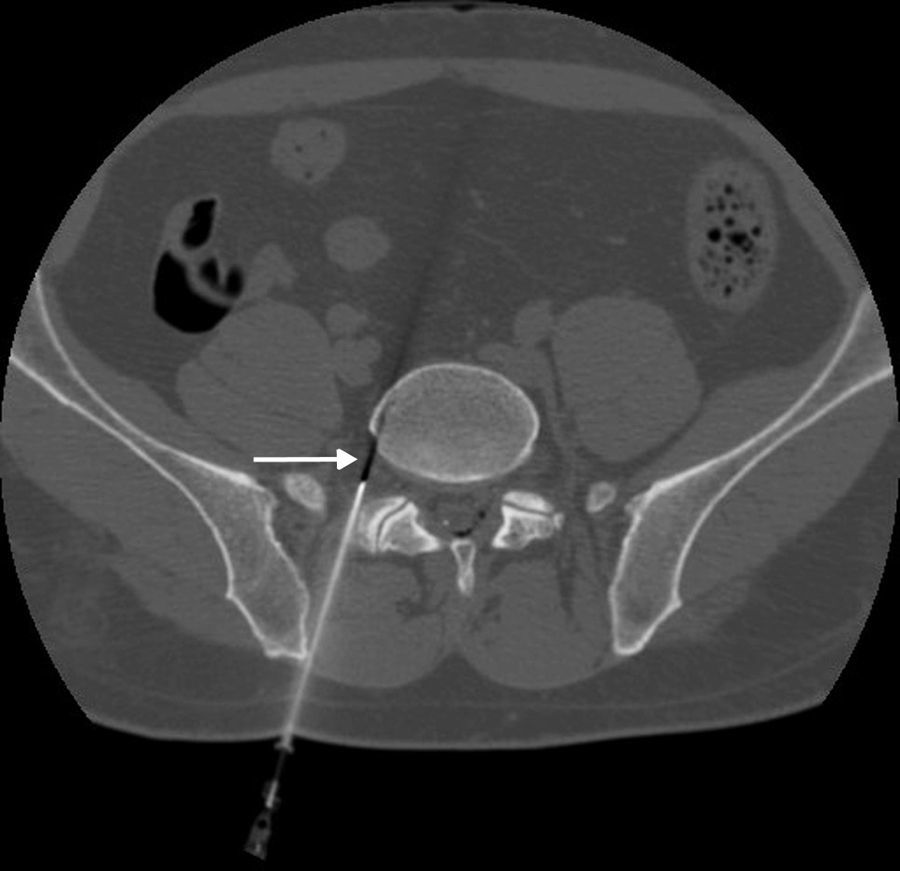
De forma general, hay dos casos en los que la TC es la técnica guía de elección: la articulación esternoclavicular y la articulación sacroilíaca, aunque en articulaciones profundas como la cadera tiene también su indicación (fig. 12). En el resto de las articulaciones, el procedimiento de artrocentesis está desarrollado en el apartado de ecografía.
La TC permite la visualización de las estructuras del mediastino vitales (vasculares) próximas a la articulación, que deberán evitarse durante el procedimiento. La aguja se hace avanzar en el interior de la articulación, y una vez dentro se puede confirmar que la entrada ha sido satisfactoria mediante la inyección de una pequeña cantidad de contraste yodado.
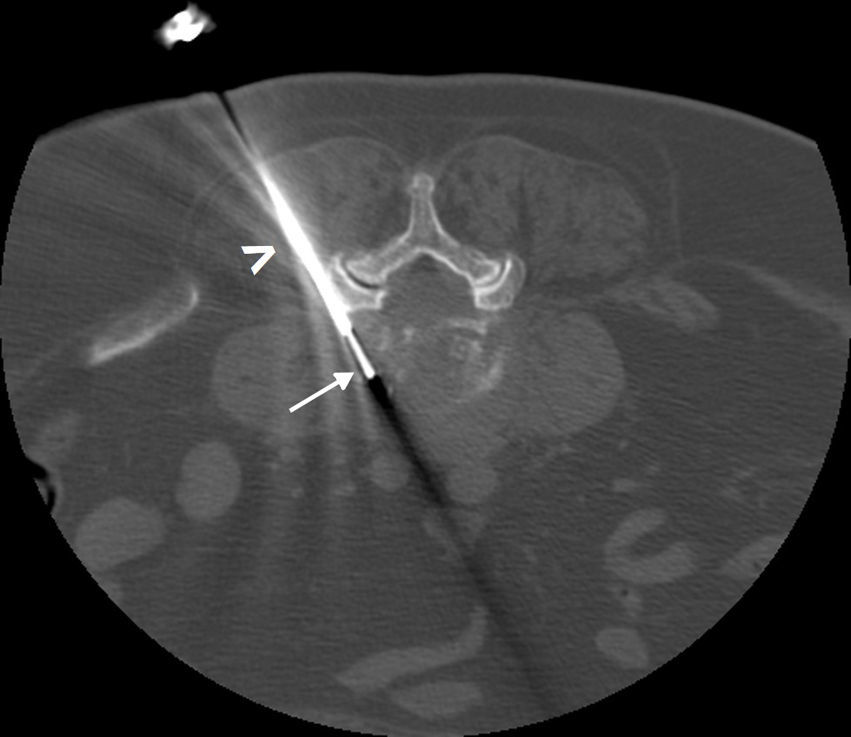
Articulación sacroilíacaDebido a la complejidad que estriba en la orientación de la articulación, la TC permite acceder a ella con más facilidad. Se tienen que considerar dos puntos fundamentales, el primero: la articulación sacroilíaca es curva, lo que significa que la parte posterior se encuentra en situación más medial que la parte anterior. Lo segundo: los dos tercios inferiores de la articulación tienen sinovial, mientras que el tercio superior es de tipo fibroso. Una estructura clave que hay que evitar cuando se interviene sobre la articulación sacroilíaca es el nervio ciático, que se encuentra por delante del músculo piriforme. El paciente se coloca en decúbito prono y la aguja se hace avanzar con un enfoque dirigido hacia el tercio inferior del espacio articular y con una angulación de medial a lateral con el fin de entrar en el mencionado espacio.
Dolor facetarioEl síndrome facetario se define como un dolor o disfunción secundarios a la afectación del ramo sensitivo posterior (responsable de la inervación de la articulación interapofisaria). Una opción de tratamiento consiste en el bloqueo nervioso facetario mediante radiofrecuencia percutánea, o bien, mediante infiltraciones con anestésico local y/o corticoides. La resolución de la clínica una vez aplicado el tratamiento confirma el diagnóstico14,15.
Se pueden realizar infiltraciones terapéuticas de las articulaciones facetarias (fig. 13), infiltraciones facetarias y radiofrecuencia facetaria. Todas ellas son técnicas algo más complejas y que no desarrollaremos en esta monografía.
RadiofrecuenciaEste procedimiento es más específico de los radiólogos especialistas en el área de músculo-esquelético, por lo que solo mencionaremos los aspectos más importantes sobre ella.
Las indicaciones de lesiones susceptibles de ablación por radiofrecuencia son16:
- •
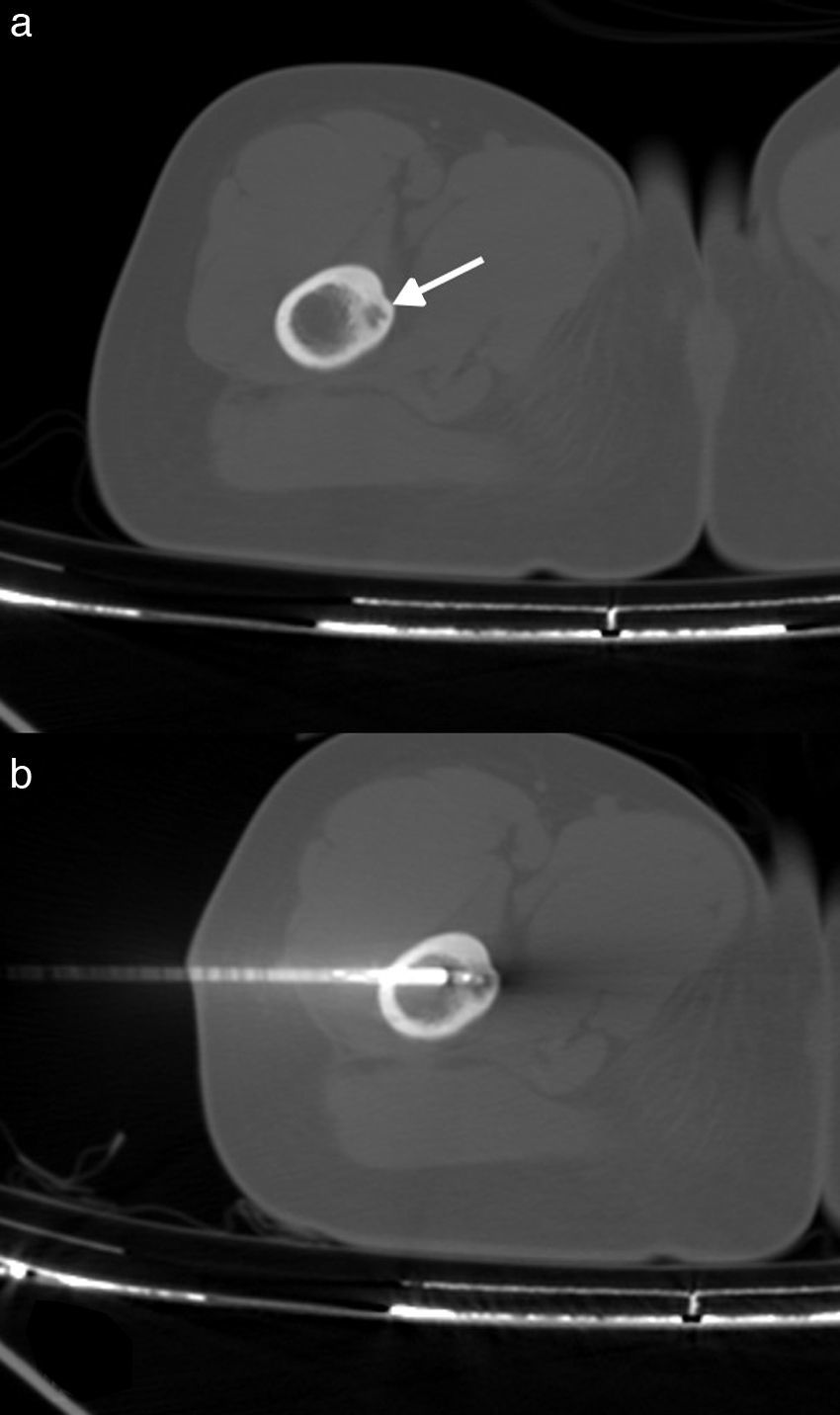
Tumores benignos como el osteoma osteoide (fig. 14), el osteoblastoma, el condroblatoma, el granuloma eosinófilo y otros. En ellas el tratamiento con radiofrecuencia es curativo.
Figura 14.a) Osteoma osteoide en localización característica en unión metafisiodiafisaria proximal del fémur. Flecha: nidus. b) Introducción de la punta activa del electrodo (17 G) en el interior del nidus. Se realiza un abordaje transóseo (por el margen opuesto del hueso para evitar el paquete vasculonervioso), coaxial por la aguja de biopsia ósea (11 G).
(0.07MB). - •
Recidiva local de ciertos tumores, como el tumor de células gigantes.
- •
Alivio sintomático del dolor ocasionado por las metástasis óseas, con una tasa de éxito cercana al 90% y que en casos de que haya recidiva de los síntomas, puede realizarse de nuevo.
- •
La combinación con vertebroplastia en el tratamiento de metástasis permite una distribución más homogénea del cemento dando estabilidad y colaborando a la potenciación de la analgesia por el efecto exotérmico del cemento.
- •
La osteonecrosis resultante de la termoablación es dolorosa y justifica la realización de este tipo de procedimientos bajo anestesia general.
Los autores declaran no tener ningún conflicto de intereses.