La región inguinal es un área anatómica compleja que ha sido tradicionalmente olvidada por los radiólogos dado que la mayoría de las lesiones pueden diagnosticarse mediante datos clínicos y con la exploración física. No obstante, cada vez es más frecuente la solicitud de ecografías, bien para confirmar la existencia de patología o para resolver casos dudosos. Por otra parte, la patología inguinal incluye entidades únicas de la edad infantil. El objetivo de este trabajo es describir los hallazgos radiológicos clave de las lesiones inguinales pediátricas, poniendo especial énfasis en los datos ecográficos
ConclusionesEl conocimiento de la patología inguinal pediátrica y sus claves en imagen ayudan a mejorar el rendimiento diagnóstico de la ecografía.
The groin is a complex anatomic region that has traditionally been ignored by radiologists because most lesions can be diagnosed from clinical data and physical examination. Nevertheless, ultrasound examinations of the groin are increasingly being requested to confirm injury or to resolve diagnostic uncertainty. On the other hand, some conditions involving the groin are found only in pediatric patients. This article describes the key imaging findings in pediatric groin injuries, placing special emphasis on the ultrasound appearance.
ConclusionsKnowledge about conditions that can affect the groin in pediatric patients and the key imaging findings associated with them helps improve the diagnostic performance of ultrasound.
El canal inguinal es un área anatómica muy importante para los cirujanos pediátricos, ya que en ella realizan la mayoría de sus intervenciones1.
A pesar de que la exploración física es la principal herramienta diagnóstica2, las técnicas de imagen tienen un papel cada vez más importante, sobre todo la ecografía y la resonancia magnética (RM).
Los objetivos de este trabajo son mostrar las patologías inguinales pediátricas más comunes y describir sus hallazgos característicos (tabla 1).
Patología inguinal pediátrica. Principales hallazgos ecográficos
| Hernias | En general indirectas: el contenido abdominal penetra en el canal inguinal por el anillo inguinal profundo. En niños puede condicionar isquemia testicular. En niñas pueden contener el ovario y complicarse con torsión del mismo |
| Hidroceles | Colección líquida inguinal comunicante o no con el peritoneo. En niñas reciben el nombre de anomalías del canal de Nuck. El hidrocele abdominoescrotal y la anomalía del canal de Nuck tipo III presentan morfología “en reloj de arena” |
| Criptorquidia | El canal inguinal es la localización más frecuente de los testes criptorquídicos. Su apariencia ecográfica es variable. Si muestran estructura heterogénea deben analizarse con Doppler-color por posible malignización |
| Adenopatías | La linfadenitis inguinal se manifiesta como adenopatías agrandadas y con inflamación en la grasa adyacente. Las adenopatías pueden presentar áreas anecogénicas en relación con necrosis o abscesificación |
| Tumores | Benignos como lipoma. En menores de 3 años destacan el hamartoma fibroso y el lipoblastoma, ambos con algún componente grasoMalignos, en general sarcomas. No muestran hallazgos específicos |
| Lesiones vasculares | Seudoaneurismas: lesiones anecogénicas con flujo turbulento (imagen de yin-yang en el Doppler-color).Malformaciones vasculares: lesiones hipo/anecogénicas con flebolitos en las venosas y posible flujo en su interior |
El canal inguinal es un conducto diagonal paralelo al ligamento inguinal (parte de la aponeurosis del músculo oblicuo externo) que atraviesa la pared abdominal y termina en el escroto en niños y en los labios mayores en niñas. Su longitud aumenta con la edad3.
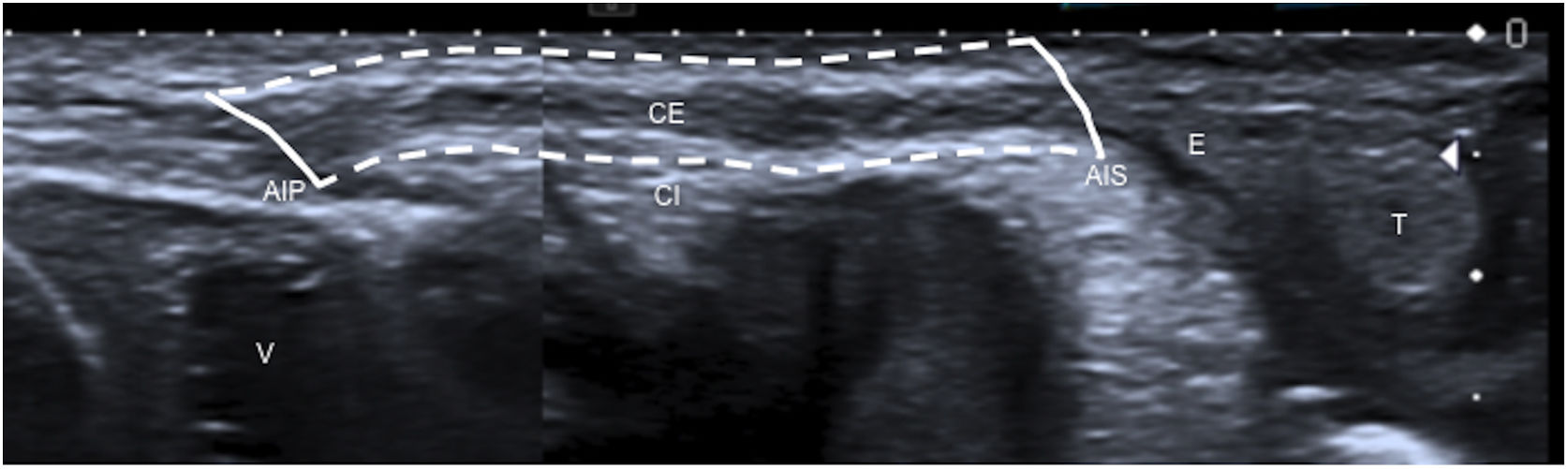
Presenta cuatro paredes formadas por la musculatura abdominal (anterior, posterior, superior e inferior) y dos anillos, uno profundo y otro superficial (fig. 1). El profundo se localiza lateral respecto al origen de los vasos epigástricos inferiores y el superficial se encuentra a la altura del tubérculo púbico4, una prominencia ósea adyacente a la sínfisis del pubis.
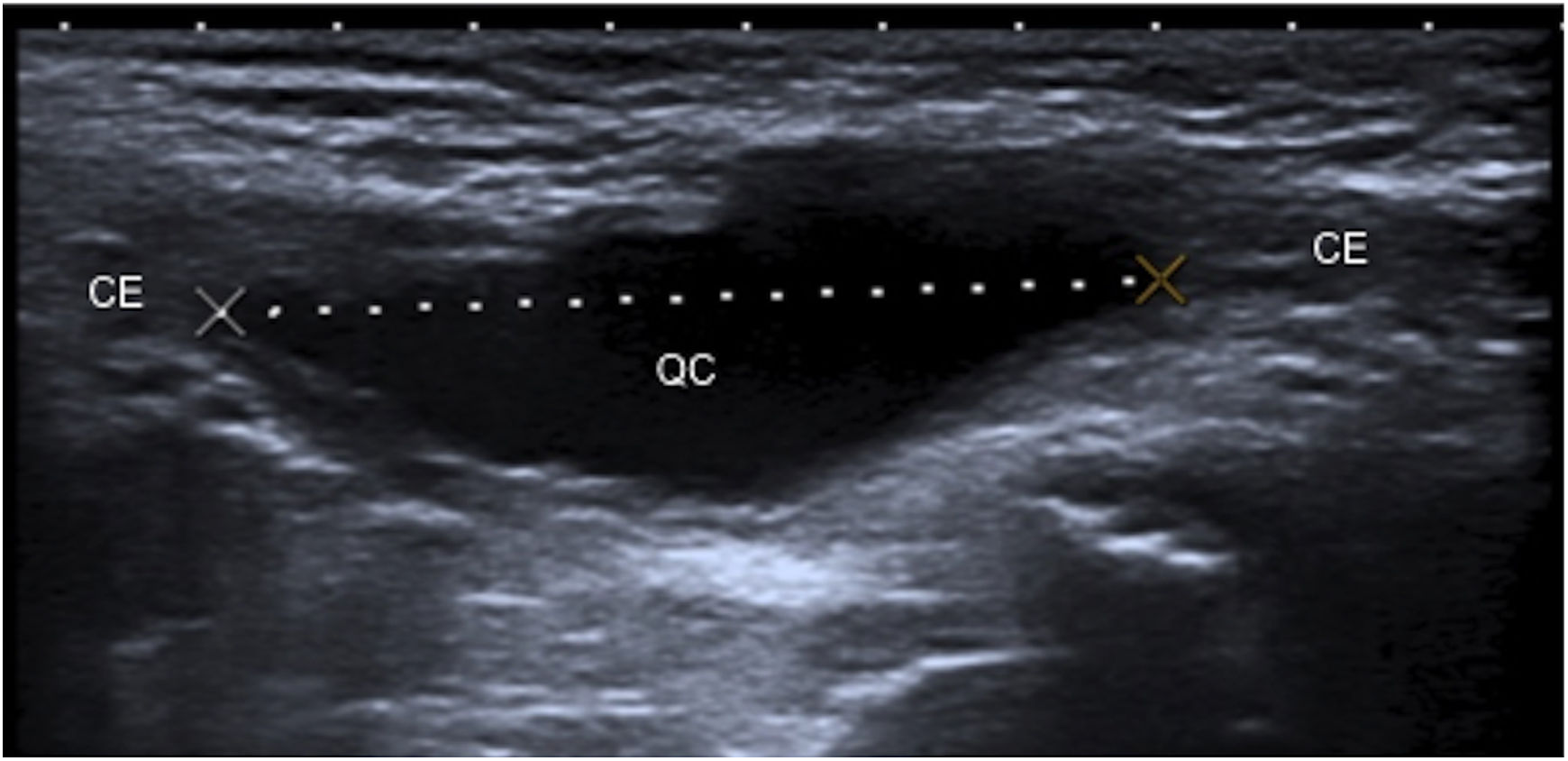
Niño de 1 mes con un canal inguinal normal. Se muestra una imagen de ecografía paralela al cordón espermático (CE) donse se representa el canal inguinal (CI) con líneas discontinuas y los anillos inguinales profundo (AIP) y superficial (AIS) con líneas continuas. También se marcan el testículo (T), el epidídimo (E) y la vejiga (V).
En niños contiene el cordón espermático (formado por el conducto deferente, la arterias deferente, testicular y cremastérica, el plexo venoso pampiniforme, la rama genital del nervio genitofemoral, vasos linfáticos y fibras simpáticas) y en niñas el ligamento redondo uterino. En ambos sexos también existe grasa, tejido conjuntivo, vasos linfáticos, el nervio ilioinguinal y el proceso vaginal3,4.
EmbriologíaEl desarrollo del canal inguinal no ha sido bien descrito1, pero se sabe que las estructuras más importantes son el gubernaculum y el proceso vaginal.
El gubernaculum es un ligamento fibromuscular, formado en la 7.ª semana de gestación, que guía el descenso de los testículos desde el abdomen al escroto1,3–5. En niñas se inserta en su tercio medio al útero e impide que los ovarios penetren en los canales inguinales3.
El proceso vaginal es un receso peritoneal formado en el 2.° y 3.er mes de gestación, que se hernia a través del defecto de la pared abdominal anterior creado por el gubernaculum3,4. Dicho receso se oblitera en sentido craneocaudal durante unas semanas antes y después del nacimiento. En niños, la parte inferior constituye la túnica vaginalis testicular y permanece permeable con una pequeña cantidad de líquido, pero en niñas se oblitera por completo3,5. El proceso vaginal permeable en niñas se denomina canal de Nuck3,4.
Evaluación por imagenLas principales técnicas de imagen en la evaluación del canal inguinal son la ecografía y la RM3.
La ecografía debe realizarse con sondas lineales de alta frecuencia (al menos de 10MHz), ya que las lesiones suelen ser superficiales. En niños obesos o si es necesaria una evaluación más profunda se utilizan sondas con menor frecuencia (3-5MHz). Es aconsejable iniciar el estudio con imágenes longitudinales, paralelas respecto al cordón espermático (fig. 1), y posteriormente transversales. También es útil realizar la exploración con el niño de pie o mientras lleva a cabo maniobras de Valsalva para identificar hernias o hidroceles comunicantes.
El Doppler aporta información relevante sobre la viabilidad de asas intestinales herniadas, así como de los testes criptorquídicos, pero debe optimizarse ya que son patologías propias de niños pequeños con bajo flujo en las gónadas. Para ello es importante incrementar la ganancia del Doppler, reducir la escala de velocidades (a 1-2 KHz) y utilizar valores bajos del filtro de pared (<100MHz).
La RM es la segunda técnica más relevante, útil sobre todo en la evaluación de masas tumorales por su resolución anatómica y capacidad de caracterización tisular. Aparte de las secuencias morfológicas, deben incluirse secuencias potenciadas en difusión, teniendo en cuenta que los testes y ovarios normales demuestran restricción de la difusión.
PatologíaHernias inguinales congénitasAfectan a entre el 1% y el 5% de los recién nacidos y a entre el 9% y el 11% de los prematuros6. Casi siempre son indirectas7,8, laterales respecto a los vasos epigástricos inferiores, y pueden clasificarse en reductibles, incarceradas y estranguladas. En las reductibles, el intestino herniado regresa fácilmente al abdomen, mientras que en las incarceradas se encuentra engrosado, edematoso y queda atrapado en el canal inguinal. Si además existe isquemia de las asas herniadas, se denominará hernia estrangulada, y constituye una emergencia quirúrgica por riesgo de necrosis intestinal.
Son más frecuentes en niños (relación niños:niñas: 3-5:1), unilaterales y derechas, ya que el proceso vaginal de ese lado se cierra después que el izquierdo1,4,6.
En general se presentan como bultomas que aparecen con las maniobras de Valsalva.
La ecografía tiene un papel importante para confirmar casos dudosos, valorar el contenido de la hernia (figs. 2 y 3) y demostrar datos de estrangulación de las asas herniadas como la ausencia de su peristaltismo. Además, con el Doppler color y pulsado se puede evaluar la vascularización del contenido de la hernia y del teste homolateral4 (fig. 2).
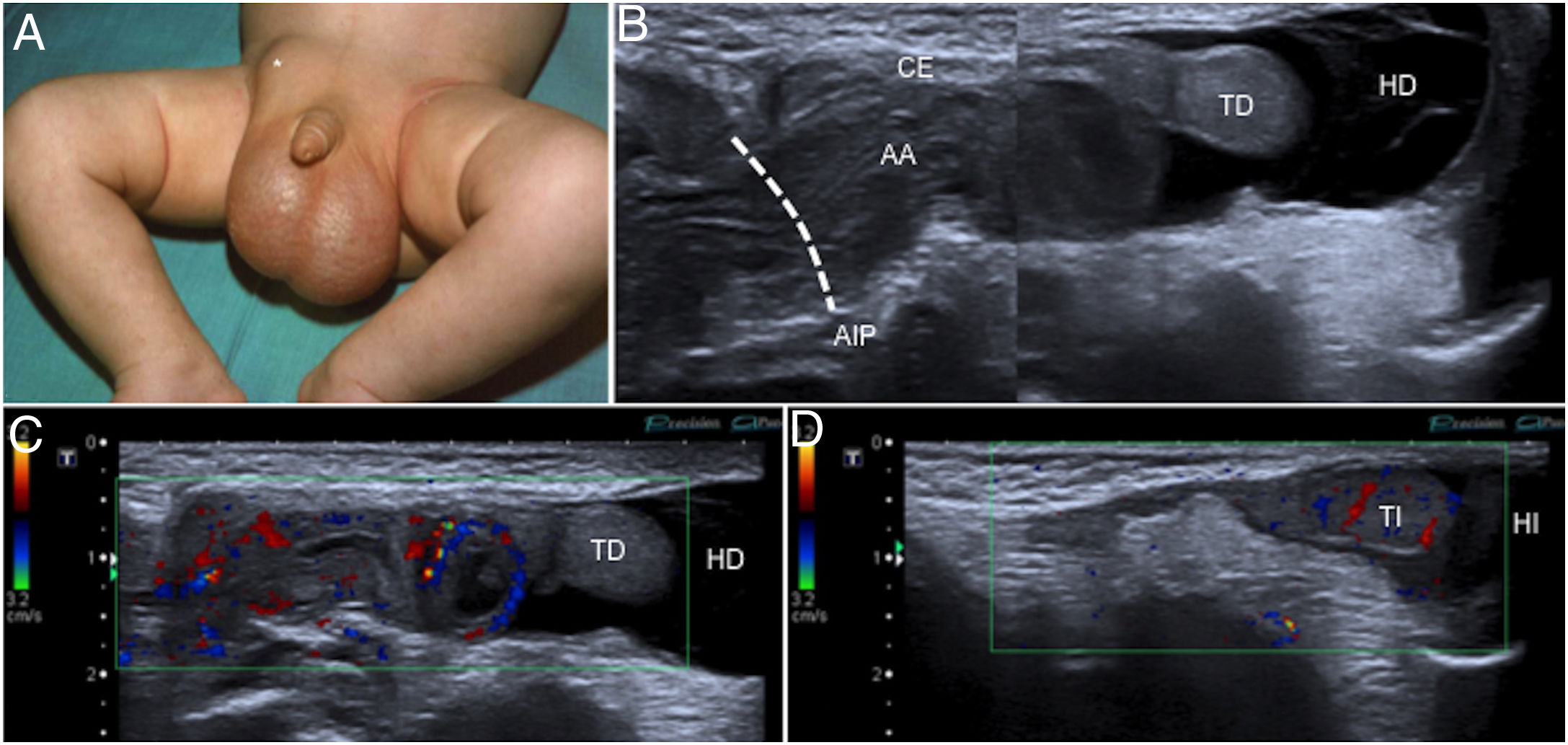
Niño de 3 meses con una hernia inguinal derecha. A) La fotografía demuestra dicha hernia (*) y un aumento del volumen escrotal. B) Ecografía inguinal derecha en modo B, corte paralelo al cordón espermático (CE), que confirma la existencia de una hernia inguinal con paso de asas intestinales (AA) a través del anillo inguinal profundo (AIP) y un hidrocele septado (HD). C y D) En el estudio con Doppler-color realizado en el mismo plano que la imagen previa se identifica flujo en las asas (AA) que sugiere viabilidad de estas, pero ausencia de flujo en el teste derecho (TD) en comparación con el izquierdo (TI), en probable relación con isquemia. Nótese el hidrocele escrotal izquierdo (HI).
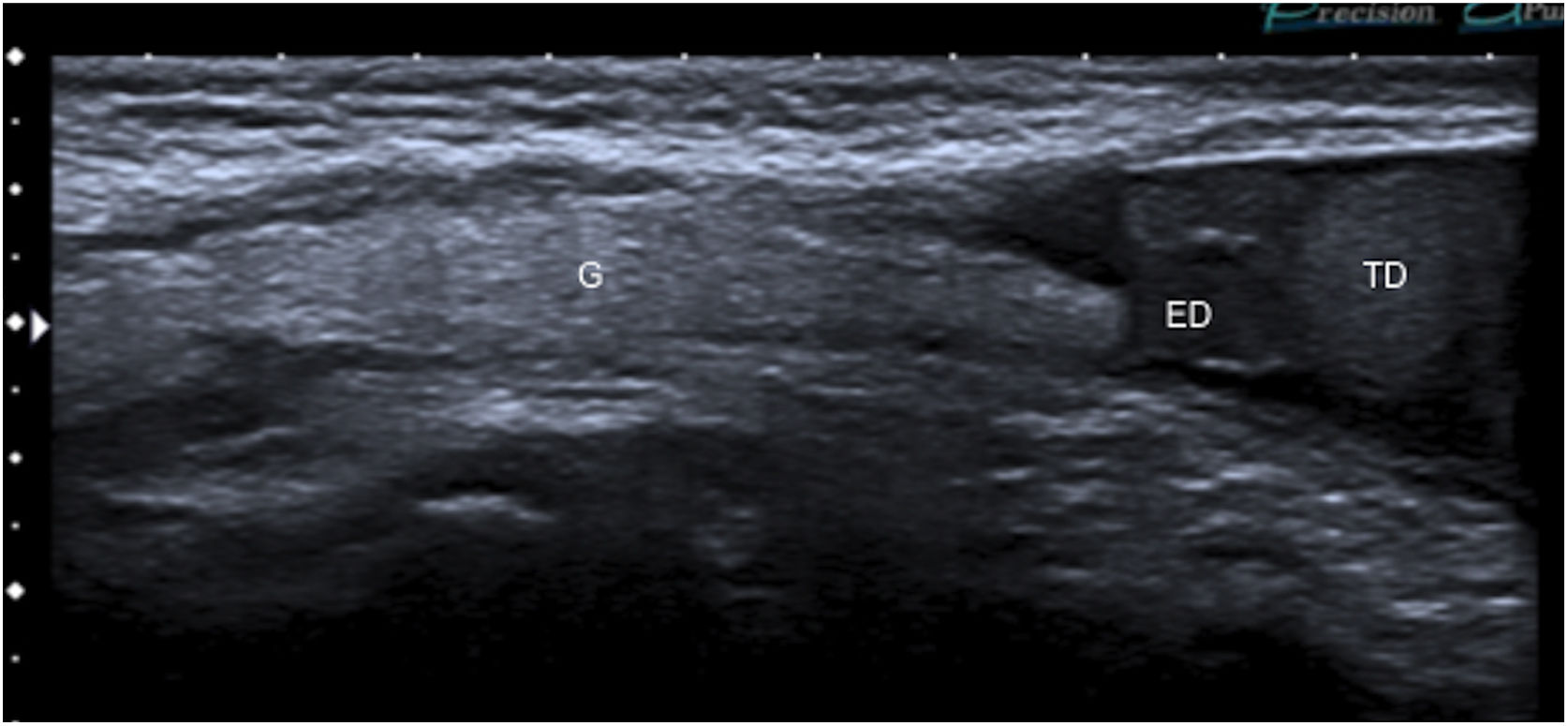
Niño de 3 años con una hernia inguinal derecha con contenido graso. Ecografía en modo B, corte longitudinal paralelo al canal inguinal, que demuestra una imagen que ocupa el canal inguinal y se aproxima al epidídimo y teste derechos (ED y TD, respectivamente) en relación con grasa abdominal.
La ecografía también es útil en las hernias del canal de Nuck en niñas, dado que pueden contener el ovario (fig. 4) e incarcerarse y producirse una torsión del mismo9.
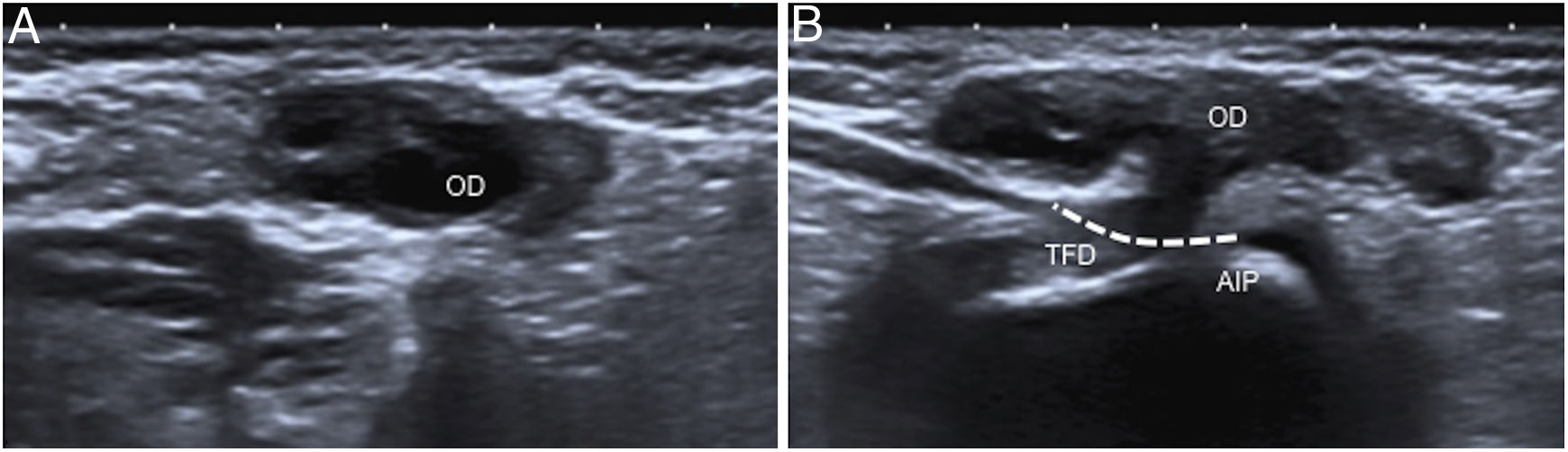
Niña de 3 meses con una hernia de Nuck derecha con el ovario en su interior. A) La ecografía en modo B en el plano axial demostró el ovario derecho (OD) en el canal inguinal. B) En el plano sagital se identifica el paso de la trompa de Falopio derecha (TFD) a través del anillo inguinal profundo (AIP).
Son colecciones anómalas en el proceso vaginal. Su comunicación con la cavidad peritoneal los clasifica en comunicantes o no comunicantes. Los comunicantes son los más frecuentes y suelen asociar hernias inguinales indirectas3.
En neonatos, la mayoría son congénitos10, afectan al 4,7% de recién nacidos11,12 y en general se resuelven espontáneamente antes de los 2 años10–12. En niños mayores y adolescentes pueden ser idiopáticos o secundarios a orquiepididimitis, traumatismos, tumores, torsiones testiculares, etc.10.
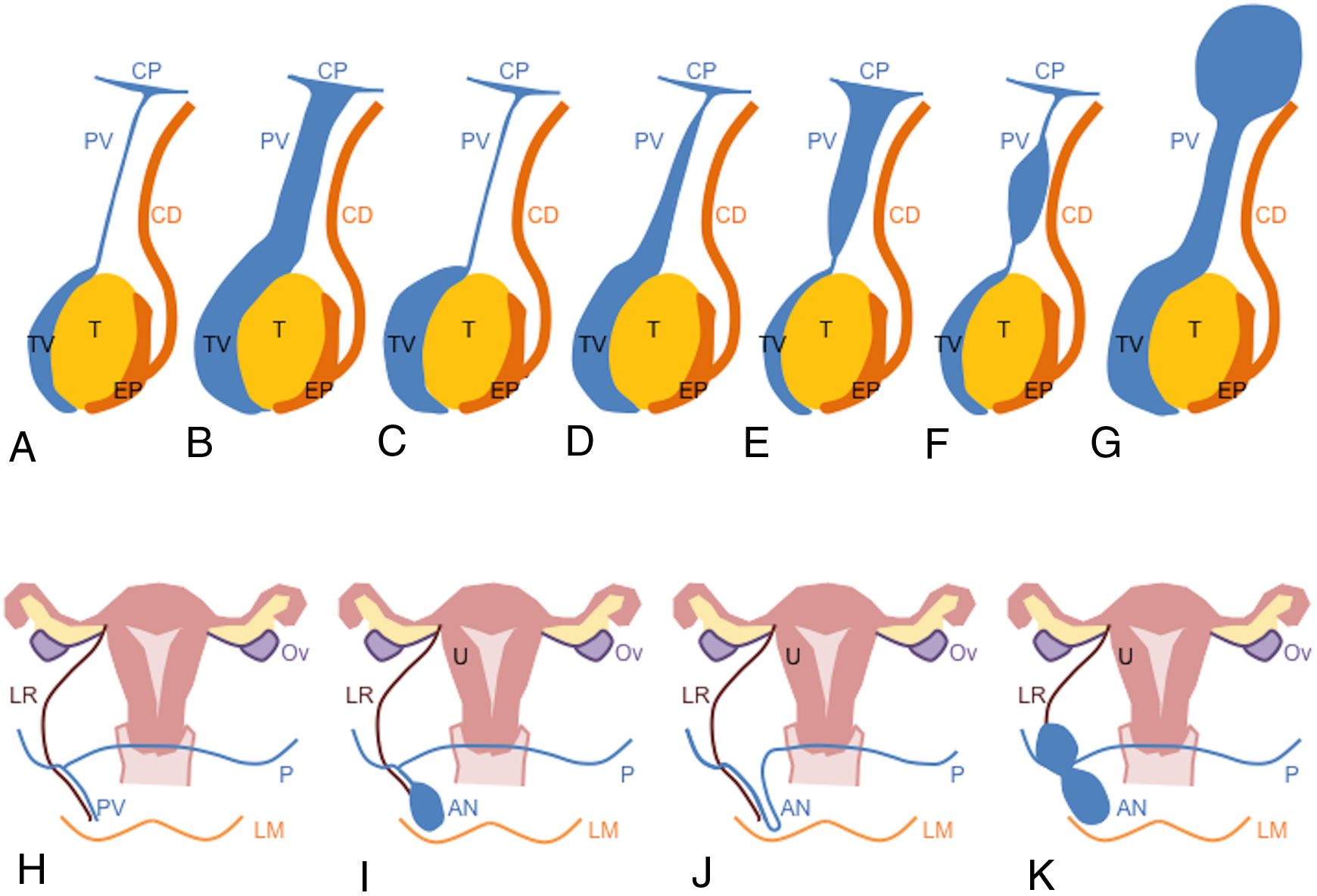
Se distinguen varios tipos de hidroceles congénitos en niños4,13, cuyo diagnóstico puede realizarse con ecografía (fig. 5A-G). En el comunicante, el proceso vaginal es permeable en todo su trayecto. Cuando se encuentra obliterado en su totalidad se denomina hidrocele escrotal o tipo adulto13.
Esquema de los tipos de hidrocele. A) Representación de un niño normal con el proceso vaginal obliterado (T: teste, EP: epidídimo, CD: conducto deferente, PV: proceso vaginal, TV: túnica vaginalis, CP: cavidad peritoneal). B) Hidrocele comunicante. C) Hidrocele escrotal o tipo adulto. D) Hidrocele inguinoescrotal o tipo infantil. E) Hidrocele tipo funicular. F) Quiste de cordón. G) Hidrocele abdominoescrotal. H) Representación de una niña normal con el proceso vaginal obliterado (U: útero, Ov: ovario, LR: ligamento redondo, LM: labios mayores, P: peritoneo, PV: proceso vaginal). I-K) Anomalías del canal de Nuck (AN) tipos I, II y III, respectivamente.
El hidrocele inguinoescrotal o tipo infantil afecta a la túnica vaginalis testicular y parte del proceso vaginal (figs. 5 D y 6 B). Cuando la colección se localiza en el proceso vaginal sin extenderse hacia el escroto hablamos de hidrocele del cordón espermático, que en caso de comunicar con el peritoneo recibe el nombre de hidrocele funicular y en caso contrario, quiste del cordón (fig. 7).
Si el hidrocele muestra un componente inguinoescrotal y otro abdominal adquiriendo una morfología en reloj de arena se denomina hidrocele abdominoescrotal, el menos frecuente (fig. 6). Cuando el componente abdominal es de gran tamaño puede causar complicaciones por efecto de masa, como uropatía obstructiva o edema del miembro inferior homolateral14.
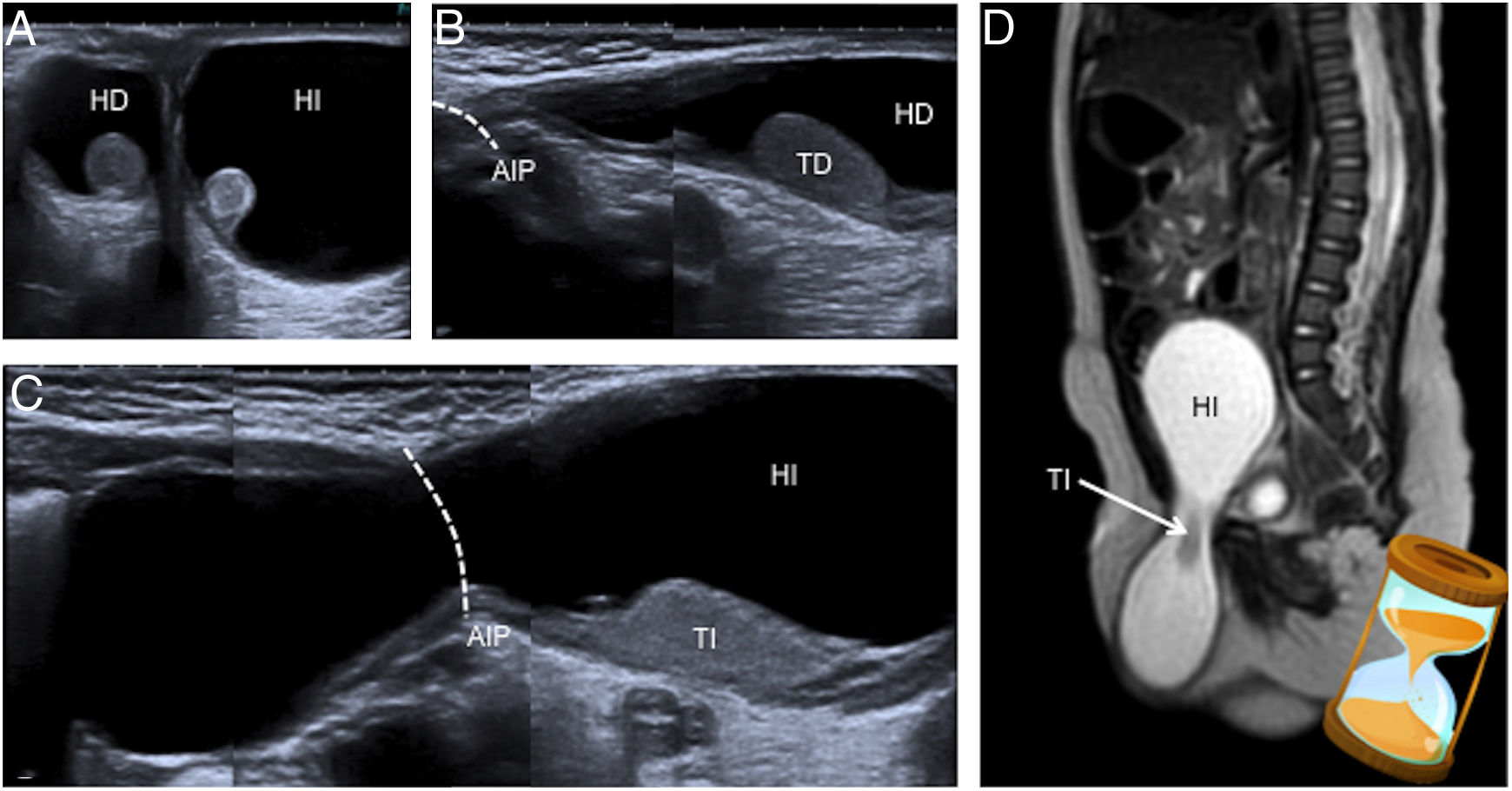
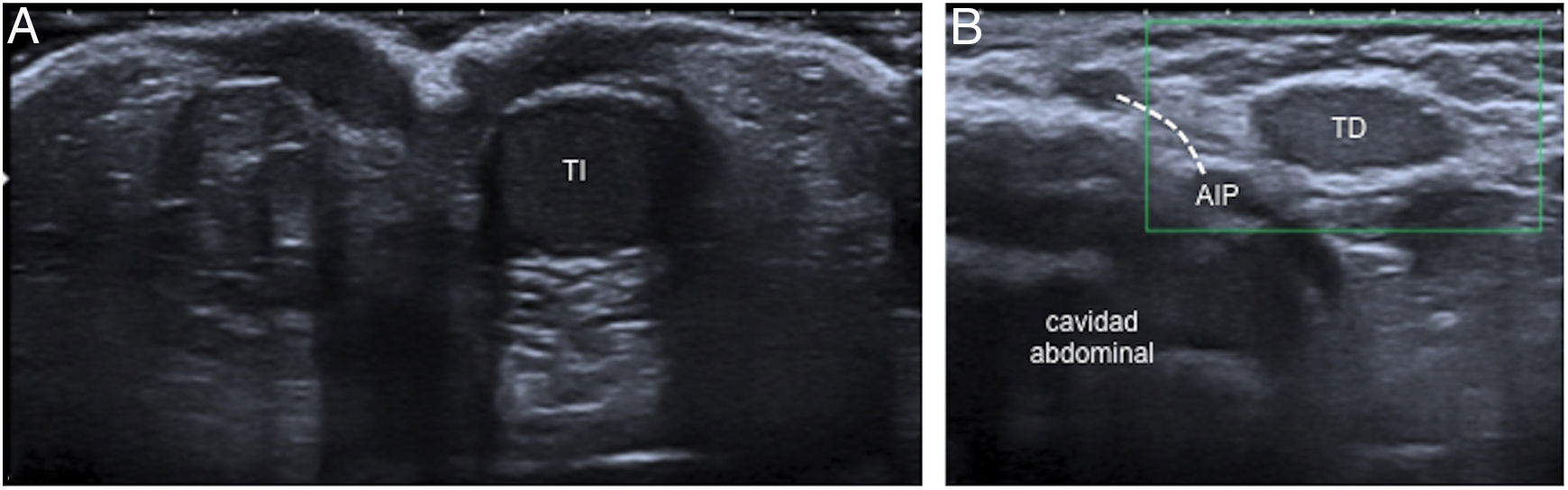
Niño de 5 meses con hidrocele inguinoescrotal derecho y abdominoescrotal izquierdo. A) La ecografía en el plano transversal muestra el hidrocele adyacente a los testes (derecho HD e izquierdo HI). B y C) En las imágenes realizadas en el plano de los canales inguinales se evidencia que el hidrocele derecho (HD) se extiende hasta el anillo inguinal profundo (AIP) y el izquierdo (HI) se continua con una cavidad quística abdominal proximal respecto a dicho anillo (AIP). D) En la resonancia magnética se identifican hallazgos similares: en el corte sagital potenciado en T2 presentado se delimita el gran hidrocele abdominoescrotal izquierdo (HI) con su morfología típica en reloj de arena.
Los hidroceles congénitos son raros en niñas y se conocen como anomalías del canal de Nuck; se distinguen tres tipos4,15,16 (fig. 5 H-K). El tipo I es el más habitual y consiste en una colección en el canal de Nuck sin comunicación con el peritoneo. En el tipo II, el canal de Nuck es totalmente permeable. El tipo III, al igual que el hidrocele abdominoescrotal, es el menos frecuente y adquiere morfología de reloj de arena.
CriptorquidiaSe considera criptorquídico u oculto aquel teste que no se encuentra en el escroto a los 4 meses de vida, ya que después de esa edad el descenso espontáneo es raro. De hecho, se aconseja realizar el descenso quirúrgico de los testes criptorquídicos lo antes posible antes de los 2 años, ya que mejora su crecimiento y función17.
Es la anomalía genital más frecuente17–19 y puede producirse por un fallo en el descenso del teste desde el abdomen o en casos raros por localización del mismo fuera de este trayecto, lo que se denomina teste ectópico3.
Afecta a entre el 1% y el 3% de los recién nacidos a término, al 30% de los prematuros19 y suele ser unilateral3. En el 70% de los pacientes, el teste se identifica en el canal inguinal, en un 20% adyacente al anillo inguinal superficial e intraabdominal en un 10%20.
La importancia del diagnóstico precoz radica en su asociación con el desarrollo de tumores testiculares y por el riesgo de infertilidad, torsión y traumatismos17.
La utilización de técnicas de imagen es controvertida. Algunos trabajos no demuestran beneficio en el uso de la ecografía para localizar testes ocultos, dado que la sensibilidad y especificidad son bajas, del 45% y 78%, respectivamente19,21. Sin embargo, otros autores como Vijayaraghavan abogan por el uso de esta técnica para seleccionar el abordaje quirúrgico22.
La apariencia ecográfica de los testes ocultos es variable, ya que pueden ser homogéneos, hipoecogénicos (fig. 8) o hiperecogénicos; con calcificaciones o heterogéneos. En este último caso es importante el Doppler para excluir una neoplasia subyacente3.
Niño de 8 meses con criptorquidia derecha. A) Ecografía en el plano axial a la altura del escroto en que tan solo se evidencia el teste izquierdo (TI). B) Imagen sagital a la altura del anillo inguinal profundo derecho (AIP) que demuestra el teste de ese lado (TD) en el canal inguinal. No se logró identificar flujo en ese teste en la exploración Doppler-color, probablemente por bajo flujo fisiológico dada la ausencia de síntomas sugestivos de complicación.
La RM, incluyendo secuencias morfológicas y potenciadas en difusión, presenta sensibilidad y especificidad elevadas (del 89,5% y 87,5%, respectivamente)19, pero aún no se han realizado estudios que apoyen su utilización generalizada.
Niños prepuberales con testes correctamente descendidos presentan con frecuencia testes retráctiles o en ascensor: adquieren una posición supraescrotal con el reflejo cremastérico, pero a diferencia de los criptorquídicos pueden ser descendidos manualmente23.
AdenopatíasEn la ingle existen ganglios fisiológicos que drenan la linfa de las extremidades inferiores, pelvis y genitales.
Al igual que en otras localizaciones, en la ecografía se muestran como estructuras ovaladas hipoecogénicas con hilio central hiperecogénico y flujo en el Doppler.
Pueden aumentar de tamaño en patologías tumorales como leucemias y linfomas o ser reactivos a infecciones perineales, genitales o del miembro inferior homolateral24,25. Si además existe inflamación en la piel adyacente, el diagnóstico será de linfadenitis inguinal, cuya etiología suele ser infecciosa24.
La ecografía en la linfadenitis demuestra ganglios aumentados de tamaño, en ocasiones con zonas anecogénicas en relación con necrosis25. También pueden existir hiperecogenicidad y aumento del flujo del tejido celular subcutáneo adyacente (fig. 9).
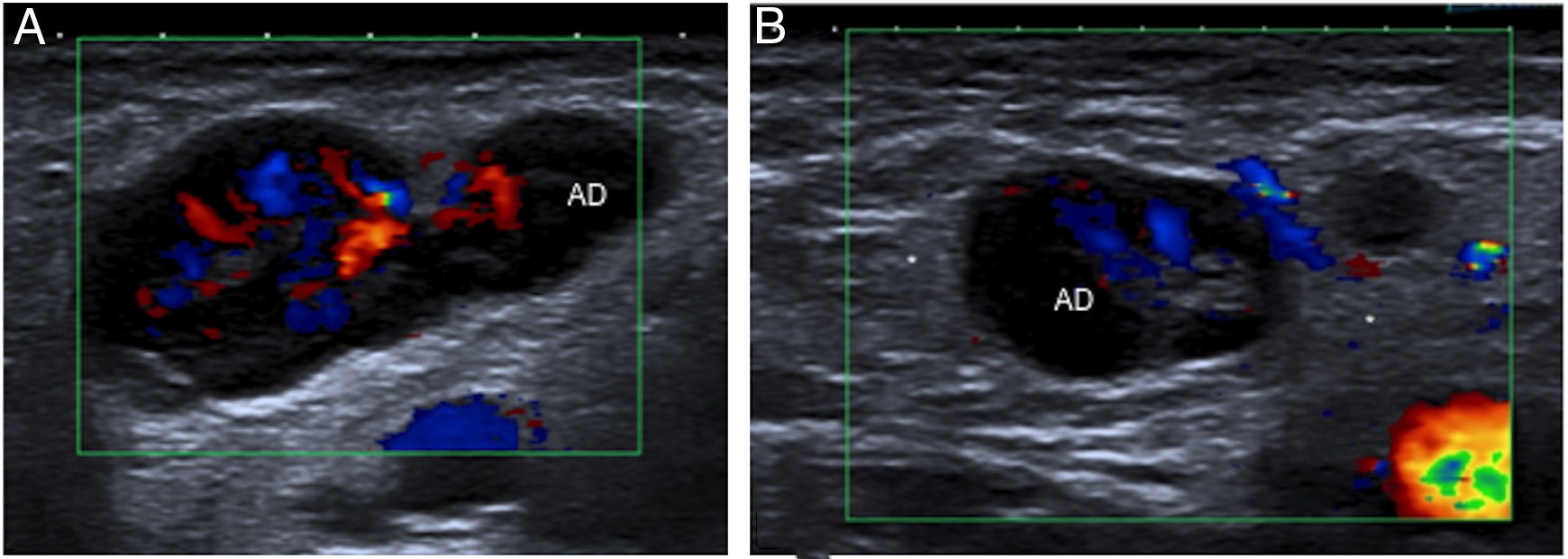
Niño de 12 años con linfadenitis inguinal derecha confirmada con ecografía. Las imágenes muestran una de las adenopatías (AD) en los planos longitudinal y transversal (A y B, respectivamente) con preservación de su estructura, pero tamaño prominente y marcado flujo en la exploración Doppler-color. También se evidencian zonas de ligero aumento de la ecogenicidad de la grasa adyacente (*) en relación con cambios inflamatorios.
Los tumores inguinales son raros y de múltiples estirpes por la gran cantidad de estructuras que confluyen en la zona3,24.
El tumor benigno más frecuente en la población general es el lipoma, pero en niños deben considerarse otras entidades como el hamartoma fibroso de la infancia en menores de 1 año (fig. 10), el lipoblastoma en menores de 3 años y el neurofibroma plexiforme en pacientes con neurofibromatosis tipo 1.
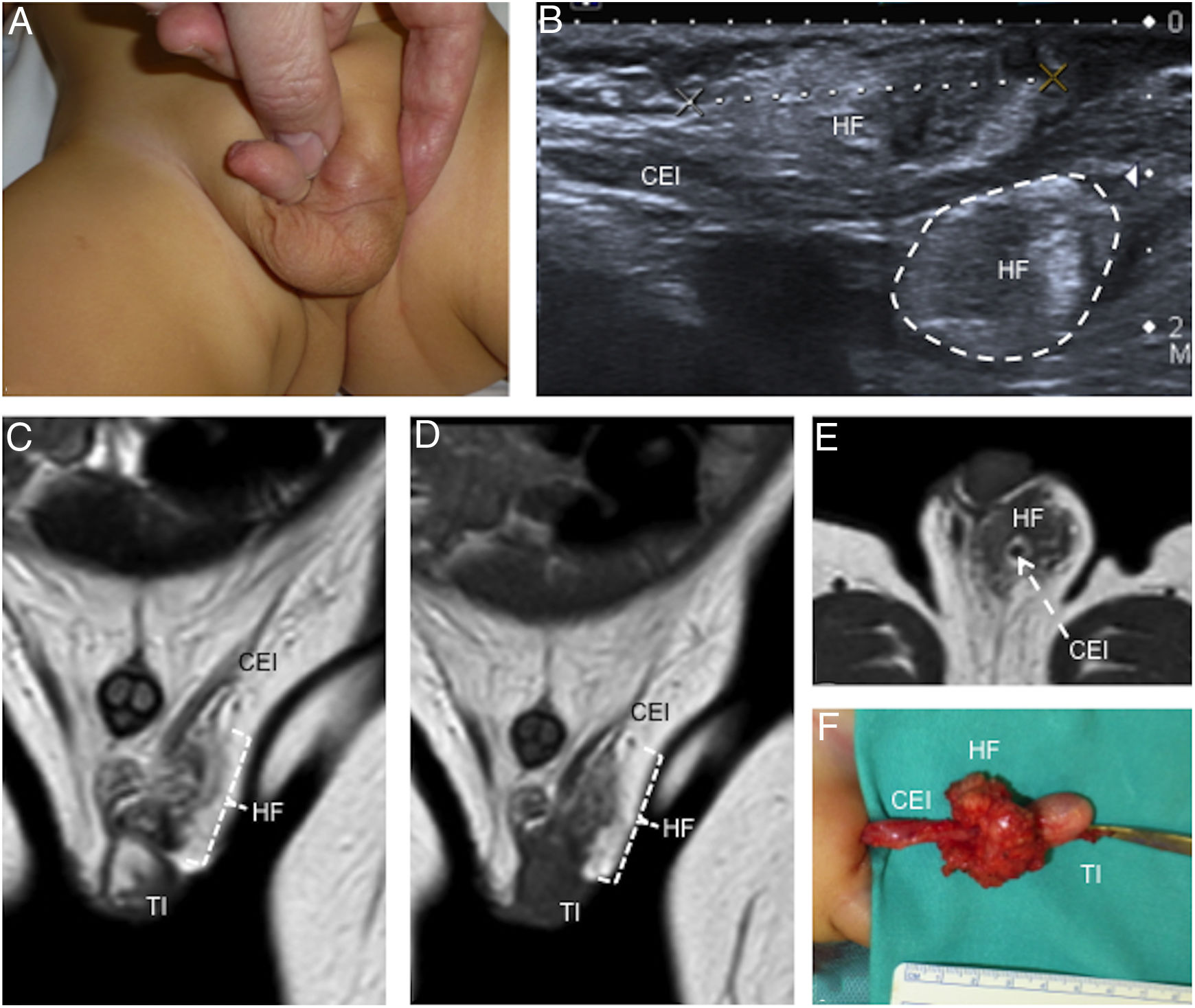
Niño de 1 año con un hamartoma fibroso inguinal. A) En la fotografía se señala una tumoración inguinal izquierda. B) Imagen de ecografía en el plano del canal inguinal donde se evidencia una masa (HF) poco definida alrededor del cordón espermático izquierdo (CEI) con un componente superficial marcado con “calipers” y otro profundo marcado con línea discontinua. Nótese la ecoestructura de la lesión ligeramente heterogénea. C y D) Imágenes de resonancia magnética (RM) coronales potenciadas en T2 y T1, respectivamente, que confirman la existencia de una masa (HF) adyacente al teste izquierdo (TI) y al cordón espermático (CEI), hipointensa en ambas secuencias y con algunas zonas elongadas isointensas con la grasa. E) En la imagen de RM axial potenciada en T1 se identifica mejor la relación del tumor (HF) con el cordón espermático (CEI). E) Fotografía quirúrgica en que se exponen teste (TI), cordón espermático (CEI) y masa (HF).
Los tumores malignos suelen ser sarcomas, ya que la mayoría de estructuras del cordón espermático derivan de tejidos mesodérmicos25, sobre todo rabdomiosarcomas en menores de 3 años.
Las técnicas de imagen ayudan a localizar la lesión, pero no permiten realizar un diagnóstico definitivo3,5. No obstante, pueden demostrar hallazgos relevantes, ya que los tumores benignos suelen ser homogéneos y bien delimitados, y los malignos, heterogéneos y con zonas de necrosis.
Además, con la RM se determina la existencia de grasa intratumoral, dato importante ya que los lipomas típicamente son isointensos con la grasa y solo presentan una fina cápsula fibrosa y algún fino septo. El hamartoma fibroso de la infancia y el lipoblastoma también presentan grasa, pero con otros componentes. El primero demuestra tejido fibroso hipointenso en las secuencias potenciadas en T1 y T2 y el segundo grasa inmadura y estroma mixoide que pueden ser tan abundantes que no se detecte la grasa26,27.
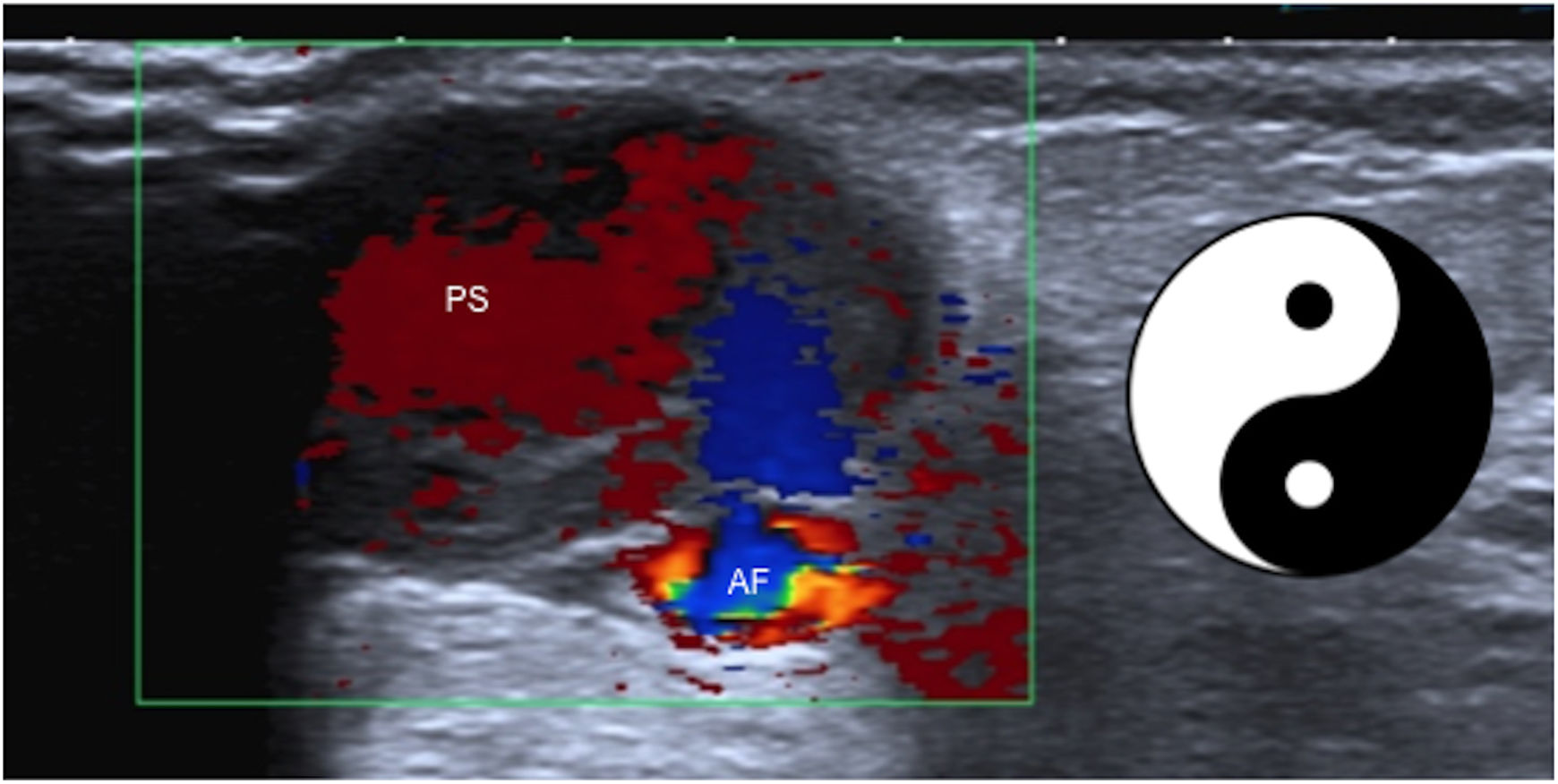
Lesiones vascularesDestacan sobre todo complicaciones de cateterismos de la arteria femoral como hematomas o seudoaneurismas (fig. 11)28. Estos últimos se presentan en la ecografía como lesiones quísticas que comunican con la luz arterial, identificándose en su interior un componente de sangre que entra en la lesión y otro que sale, cuya traducción en el Doppler-color es la “imagen en yin-yang”29.
También pueden existir malformaciones vasculares paratesticulares arteriovenosas, linfáticas, venosas (fig. 12) o mixtas30.
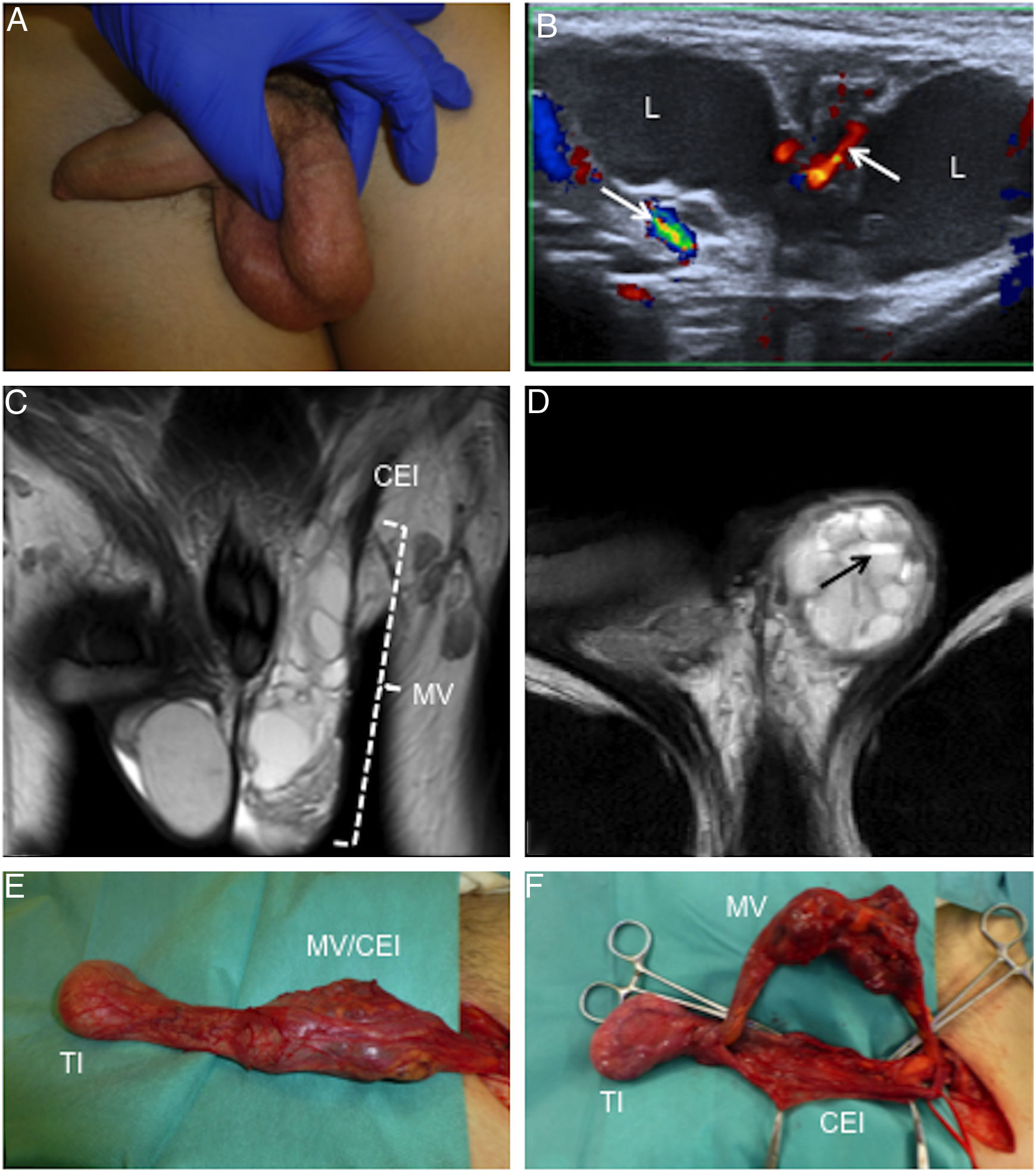
Niño de 14 años con malformación venosa inguinoescrotal izquierda. A) En la fotografía se señala la masa paraescrotal izquierda. B) La eco-Doppler muestra una masa quística multiloculada con vasos (flechas) entre los lóculos (L). C) Imagen de resonancia magnética (RM) coronal potenciada en T2 que confirma la existencia de una masa quística inguinoescrotal (MV) en íntima relación con el cordón espermático izquierdo (CEI). D) Imagen de RM axial potenciada en T2 que muestra niveles líquido-líquido (flecha). E y F) Fotografías quirúrgicas en que se exponen teste (TI), cordón espermático (CEI) y masa (MV) antes y durante la disección.
La ingle puede ser asiento de patología diversa y cada vez se requieren más estudios de imagen para su evaluación. Por tanto, el radiólogo debe conocer el diagnóstico diferencial a plantear y tratar de rentabilizar al máximo las técnicas de imagen.
Autoría- 1.
Responsable de la integridad del estudio: AAD.
- 2.
Concepción del estudio: AAD, MVTA, MMLP.
- 3.
Diseño del estudio: AAD, MVTA, MMLP.
- 4.
Obtención de los datos: NA.
- 5.
Análisis e interpretación de los datos: NA.
- 6.
Tratamiento estadístico: NA.
- 7.
Búsqueda bibliográfica: SBG y MGP.
- 8.
Redacción del trabajo: AAD y SBG.
- 9.
Revisión crítica del manuscrito con aportaciones intelectuales relevantes: MVTA, MMLP, SBG y MGP.
- 10.
Aprobación de la versión final: AAD, MVTA, MMLP, SBG y MGP.
Los autores declaran no tener ningún conflicto de intereses.
Al Dr. Adolfo Bautista Casasnovaspor sus espléndidas imágenes quirúrgicas y su labor en la revisión del manuscrito.