Analizar los valores del flujo obtenidos con un catéter endovascular y demostrar que son más fiables que los hallazgos angiográficos y clínicos para planificar y determinar el resultado del tratamiento radiológico invasivo de las fístulas de hemodiálisis, así como demostrar su seguridad durante los procedimientos intervencionistas.
Material y métodosMedimos con el catéter 341 fístulas de hemodiálisis en 598 procedimientos. En total, se hicieron 3.051 medidas de flujo. Fueron 162 fístulas distales (47,6%), 132 humerales (38,4%) y 47 injertos protésicos (14%). Los motivos de disfunción más frecuentes fueron las presiones elevadas y el déficit de flujo.
ResultadosEl catéter se utilizó para medir el resultado del tratamiento radiológico en 419 casos (70%) y solo para medir el control del flujo del acceso en 179 casos (30%). En los casos en los que se trataron radiológicamente las lesiones del acceso, el flujo mejoró en 312ml/min de media. Los casos no tratados presentaron un flujo medio de 1.232ml/min. En 2 casos (0,35%) la punta del catéter perforó la pared de la vena, que se resolvió inflando un balón a pocas atmósferas.
ConclusionesEl catéter endovascular medidor de flujos es una herramienta útil en los procedimientos invasivos de radiología vascular para hemodiálisis. Al valorar el estado hemodinámico del acceso vascular, su mayor utilidad es que ayuda a tomar la decisión de tratar o no una estenosis.
To analyze the values of flow obtained with an endovascular catheter, and to determine whether they are more reliable than angiographic and clinical findings for planning and for determining the outcome of invasive radiologic treatment of hemodialysis fistulas, as well as to determine the safety of this technique during interventional radiology procedures.
Material and methodsWe used endovascular catheters to measure flow in 341 vascular accesses for hemodialysis (162 [47.6%] distal fistulas, 132 [38.4%] humeral fistulas, and 47 [14%] arteriovenous grafts) in 598 procedures (a total of 3,051 flow measurements). Dysfunction was most commonly due to high pressures and flow deficits.
ResultsThe catheter was used to measure the results of radiologic treatment in 419 (70%) cases and only to measure the control of flow in the hemodialysis access in 179 (30%) cases. In the cases where lesions of the access had been treated radiologically, the flow improved by a mean of 1,232ml/min. In 2 (0.35%) cases, the tip of the catheter perforated the wall of the vein; this complication was resolved by inflating a low pressure balloon.
ConclusionsEndovascular catheters are useful for measuring flow in invasive vascular radiology procedures for hemodialysis. In assessing the hemodynamic status of a vascular access, they are most helpful in determining whether stenosis is present.
Las fistulas de hemodiálisis tienden a desarrollar con el tiempo estenosis que disminuyen el flujo y deterioran la calidad de la diálisis1. A principios de los años 90, estudios clínicos demostraron que medir el flujo de la fístula predecía la trombosis2. Se comprobó que, si no se corregía la estenosis con una angioplastia, la fístula acababa trombosándose3. Pero más tarde se demostró que no todas las angioplastias consideradas como un éxito por el radiólogo mejoraban el flujo de la fístula4. Habitualmente, el éxito de la angioplastia en una estenosis de una fístula de hemodiálisis se ha determinado con la exploración física y una angiografía5. Sin embargo, estos no son datos objetivos y, en determinadas situaciones, puede haber dudas acerca del resultado final del tratamiento6. De ahí la necesidad de tener un instrumento que establezca la mejoría del flujo tras una angioplastia, y, de esta forma, evitar un mal resultado hemodinámico a pesar del buen resultado angiográfico7. Un sistema que permita medir in situ el flujo inmediatamente después de una angioplastia informará objetivamente de su aumento7.
La ecografía doppler es una herramienta que se emplea para valorar el flujo de la fístula. Es útil para diagnosticar la disfunción de las fístulas y para controlarla en el tiempo. Su desventaja en la sala de radiología vascular es que se necesita ser experto en ella. El procedimiento del catéter medidor de flujo es rápido, no necesita conocimientos especiales para manejarlo, no es costoso y rentabiliza los balones de angioplastia que hay que utilizar en cada procedimiento6.
El objetivo principal de este trabajo es analizar los valores del flujo obtenidos con el catéter endovascular y demostrar que son más fiables que los hallazgos angiográficos y clínicos para planificar y determinar el resultado del tratamiento radiológico invasivo de las fístulas de hemodiálisis. También ha sido un objetivo mostrar las posibles complicaciones y la seguridad del catéter durante los procedimientos intervencionistas.
Material y métodosPacientes y accesos vascularesEstudiamos retrospectivamente los resultados de los 6 últimos años con el catéter endovascular medidor de flujo ReoCath™ Flow Catheter (Transonic Systems Inc., Ithaca, New York, EE. UU.) en 341 fístulas de diálisis. A todos los pacientes se les explicó el procedimiento y se obtuvo el consentimiento informado, contando con el permiso del comité de ética hospitalario. Incluimos todas las fístulas de diálisis que presentaban algún tipo de disfunción según los parámetros dialíticos. No se incluyeron aquellas en las que la ecografía descartó cualquier actuación radiológica invasiva. La edad media de los pacientes fue de 62 años (rango: 21-88 años; 60% hombres). El 48% de las fístulas eran distales (radiales o cubitales), el 38% humerales y el 14% injertos protésicos de politetrafluoroetileno.
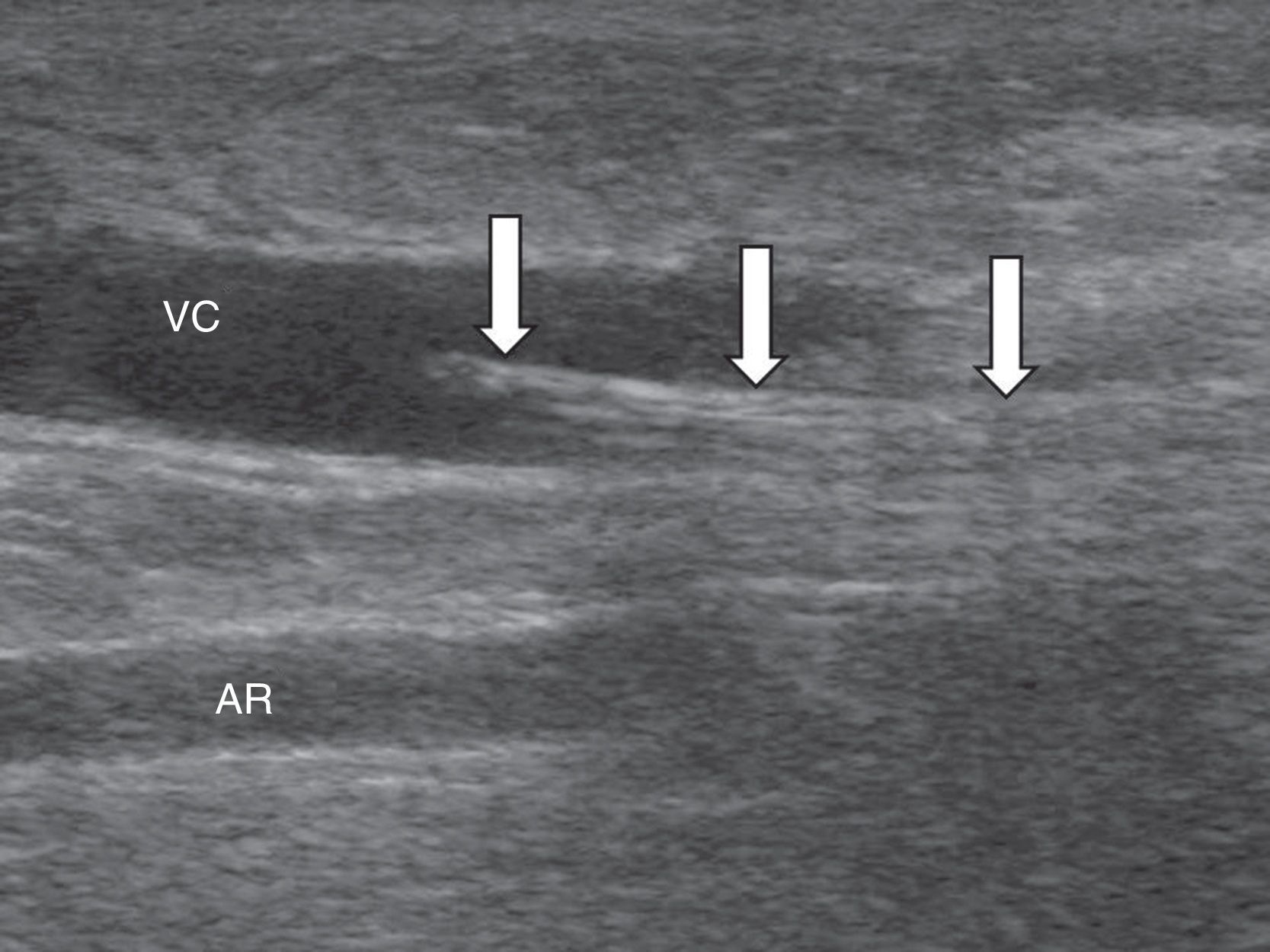
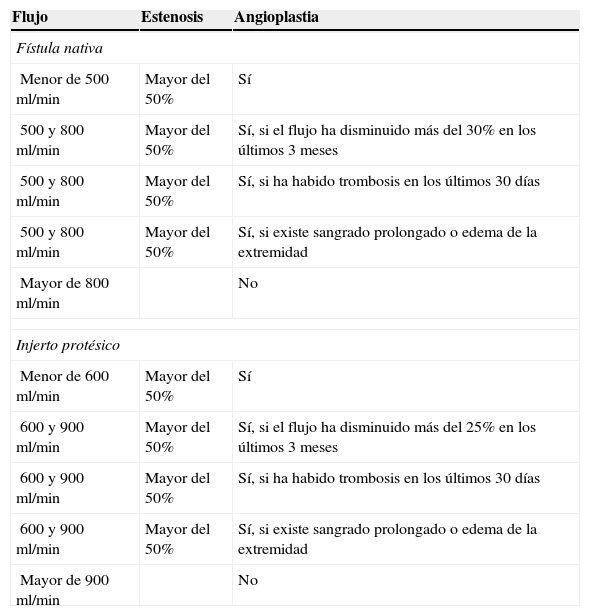
Técnica de estudioEl ReoCath™ Flow Catheter es un catéter desechable con un cable de extensión que se conecta a una máquina que mide el flujo. Dependiendo de la dirección del flujo en la que se trabaje, el catéter puede ser anterógrado y retrógrado; ambos son del calibre 6French y no tienen luz interna, y, por lo tanto, no avanzan sobre guía. Antes de medir el flujo se realiza una fistulografía por abordaje retrógrado de la arteria o por punción de la vena, ya sea hacia la anastomosis (sentido retrógrado) o a favor del flujo (sentido anterógrado), para valorar todo el territorio vascular desde la arteria aferente hasta las cavidades cardíacas. Una vez hecho el diagnóstico, se introduce el catéter a través de un introductor, con guía fluoroscópica o ecográfica (fig. 1). A continuación, el catéter se conecta mediante una alargadera a un monitor, y se mide inyectando por el catéter un bolo de 10ml de suero salino a temperatura ambiente. El catéter tiene un sensor proximal que registra la temperatura de la solución salina inyectada, y un segundo sensor, más distal, que registra la termodilución en el acceso vascular. El sistema calcula el flujo sanguíneo por el cambio de temperatura que experimenta el suero salino inyectado al entrar en la circulación sanguínea. En total se realizan 3 medidas y se calcula la media. Las indicaciones de la angioplastia basadas en las medidas del flujo7 se muestran en la tabla 1.
Indicaciones de la angioplastia
| Flujo | Estenosis | Angioplastia |
|---|---|---|
| Fístula nativa | ||
| Menor de 500ml/min | Mayor del 50% | Sí |
| 500 y 800ml/min | Mayor del 50% | Sí, si el flujo ha disminuido más del 30% en los últimos 3 meses |
| 500 y 800ml/min | Mayor del 50% | Sí, si ha habido trombosis en los últimos 30 días |
| 500 y 800ml/min | Mayor del 50% | Sí, si existe sangrado prolongado o edema de la extremidad |
| Mayor de 800ml/min | No | |
| Injerto protésico | ||
| Menor de 600ml/min | Mayor del 50% | Sí |
| 600 y 900ml/min | Mayor del 50% | Sí, si el flujo ha disminuido más del 25% en los últimos 3 meses |
| 600 y 900ml/min | Mayor del 50% | Sí, si ha habido trombosis en los últimos 30 días |
| 600 y 900ml/min | Mayor del 50% | Sí, si existe sangrado prolongado o edema de la extremidad |
| Mayor de 900ml/min | No | |
Fuente: Vesely et al.7.
El catéter medidor de flujo se utilizó en 598 procedimientos en 341 fístulas. En total, se hicieron 3.051 medidas de flujo. En el 70% de los casos, se pretendía valorar el resultado de algún tratamiento y en el 30% restante no se hizo ningún tratamiento. Describimos las aplicaciones prácticas del procedimiento.
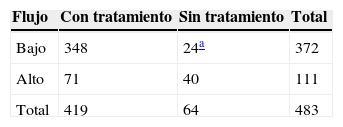
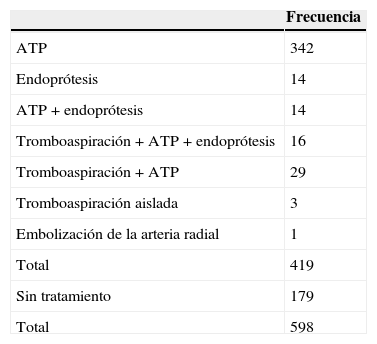
ResultadosDe los 598 casos realizados, en 483 (81%) se detectaron lesiones en la angiografía (tabla 2). De estos, se trataron radiológicamente 419 (87%) y no los 64 restantes, que se remitieron al cirujano (24, con flujos bajos) o no se trataron para no provocar un síndrome de robo o una isquemia en la extremidad (40, con flujos altos). En 179 procedimientos (30%) no se hizo ningún tratamiento (flujo medio detectado de 1.232ml/min; rango: 140-3.378ml/min) (tabla 3). En los 419 procedimientos en los que se hizo algún tipo de tratamiento, el gradiente de flujo medio quedó en 312ml/min (rango: 60-1.443ml/min). El tratamiento más frecuente fue la angioplastia aislada (342 casos) (tabla 4 y fig. 2). En 44 casos se implantó algún tipo de endoprótesis (fig. 3). En 48 casos se realizó tromboaspiración manual con catéter. De las fístulas tratadas, en 82 casos (19,57%) (51 anterógrados y 31 retrógrados) no se consiguió medir el flujo inmediatamente antes del tratamiento. De ellos, se consiguió que la máquina detectara el flujo en 37 casos, recolocando la punta del catéter. En los 45 restantes se midió el flujo postratamiento en todos menos en 5, en quienes tampoco se detectó flujo y la máquina dio «error». En 2 fue debido a defectos de fábrica del catéter. De los 82 casos en los que hubo problemas para medir el flujo, 65 (79,26%) lo fueron en fístulas radiocefálicas.
Fístulas con estenosis: correlación flujo/tratamiento radiológico
| Flujo | Con tratamiento | Sin tratamiento | Total |
|---|---|---|---|
| Bajo | 348 | 24a | 372 |
| Alto | 71 | 40 | 111 |
| Total | 419 | 64 | 483 |
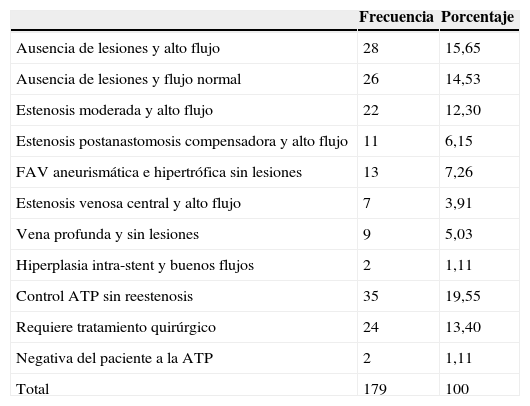
Accesos no tratados radiológicamente
| Frecuencia | Porcentaje | |
|---|---|---|
| Ausencia de lesiones y alto flujo | 28 | 15,65 |
| Ausencia de lesiones y flujo normal | 26 | 14,53 |
| Estenosis moderada y alto flujo | 22 | 12,30 |
| Estenosis postanastomosis compensadora y alto flujo | 11 | 6,15 |
| FAV aneurismática e hipertrófica sin lesiones | 13 | 7,26 |
| Estenosis venosa central y alto flujo | 7 | 3,91 |
| Vena profunda y sin lesiones | 9 | 5,03 |
| Hiperplasia intra-stent y buenos flujos | 2 | 1,11 |
| Control ATP sin reestenosis | 35 | 19,55 |
| Requiere tratamiento quirúrgico | 24 | 13,40 |
| Negativa del paciente a la ATP | 2 | 1,11 |
| Total | 179 | 100 |
ATP: angioplastia transluminal percutánea; FAV: fístula arteriovenosa.
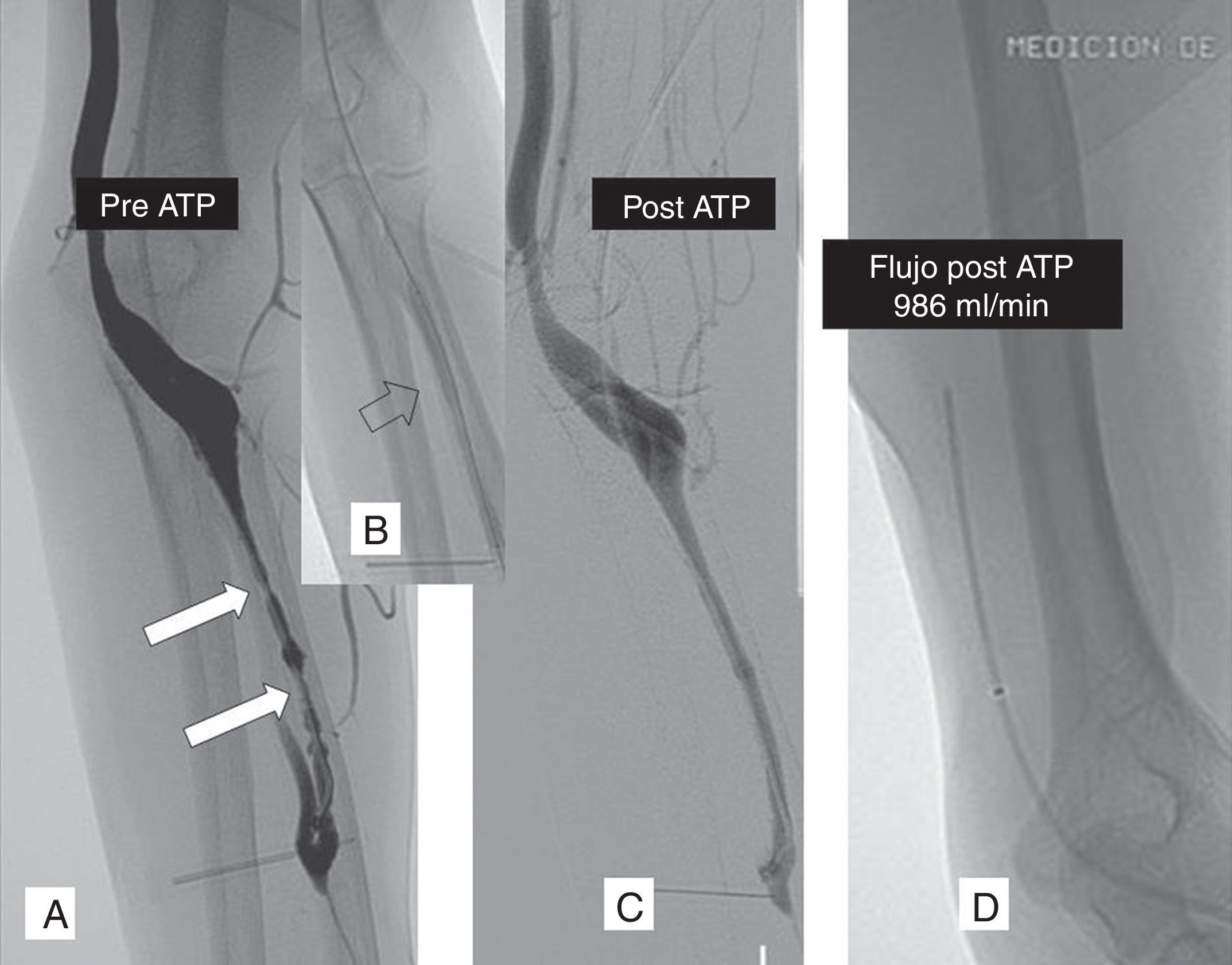
Fístula radiocefálica izquierda con déficit de flujo (250ml/min). La fistulografía mediante cateterización retrógrada de la vena cefálica en el codo muestra lesiones estenóticas en la vena cefálica (A), que se dilataron con balón de angioplastia de 7mm de diámetro (B), con un resultado angiográfico moderado (C). La medida del flujo con catéter anterógrado demostró un flujo final de 986ml/min, por lo que no se dilató con un balón de mayor diámetro (D). ATP: angioplastia transluminal percutánea.
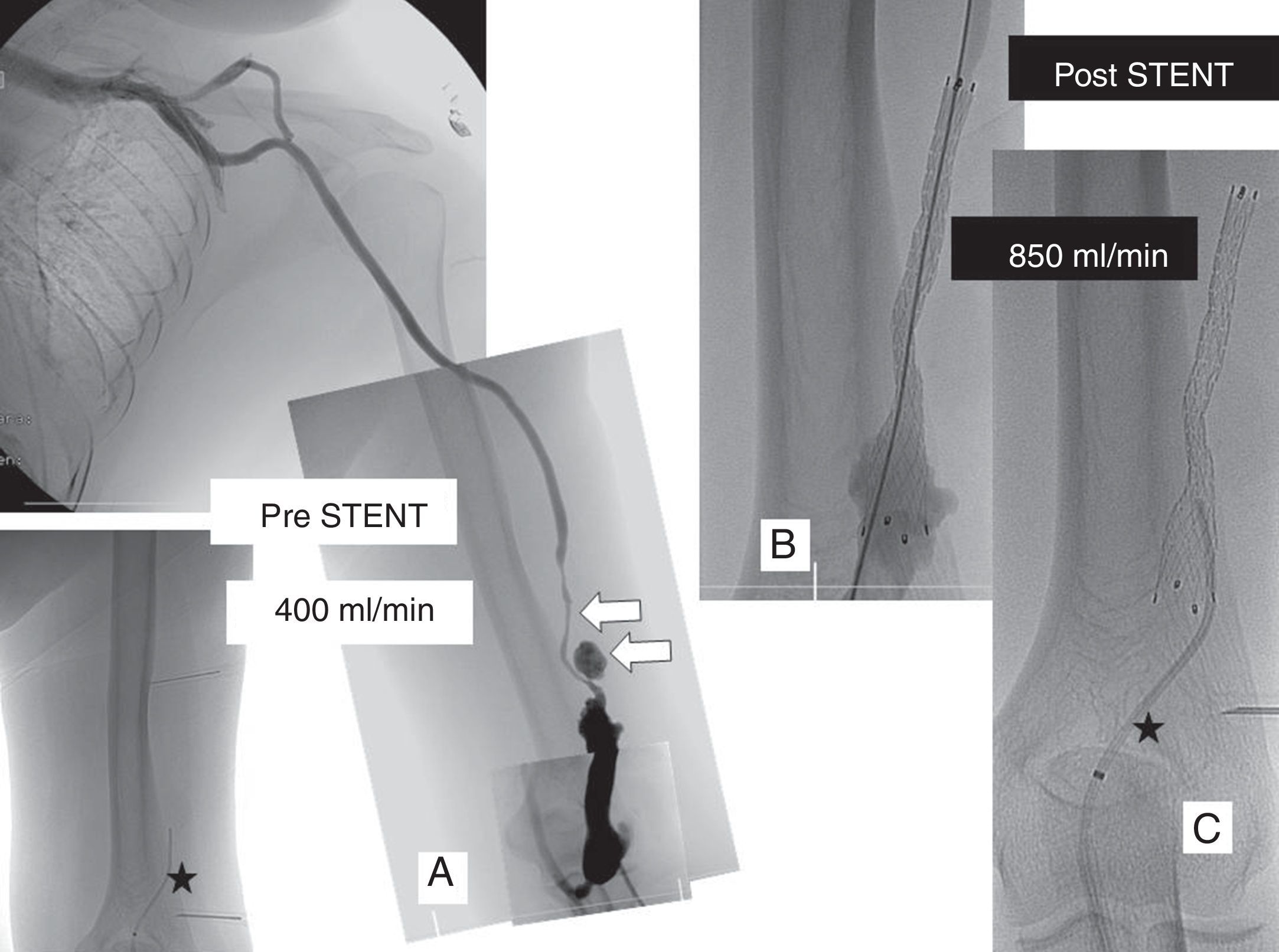
Fístula humerocefálica izquierda con seudoaneurisma en las zonas de punción y estenosis grave (flechas). Flujo de 400ml/min medido con catéter ReoCath™ anterógrado (estrella) (A). Se implantó una endoprótesis recubierta «Fluency» (Bard de España, Barcelona, España) de 10mm de diámetro por 8cm de longitud (B). La medida del flujo con catéter anterógrado demostró un flujo final de 850ml/min (C).
En 2 casos (0,35%) la punta del catéter perforó la vena. Uno de ellos, una fístula arteriovenosa humerocefálica aneurismática y tortuosa, desarrolló un hematoma que fue controlado con compresión manual externa. En el segundo, una fístula arteriovenosa radiocefálica con un catéter retrógrado, la punta se avanzó por una colateral de la muñeca al nivel de una estenosis postanastomótica, y se resolvió inflando un balón de 6mm de diámetro a 2 atmósferas durante 3min.
La detección de flujos altos (mayor de 800 en las fístulas nativas y de 900 en los injertos protésicos) sirvió para poner en aviso a los nefrólogos y recomendar controles cardiológicos, por el riesgo de sobrecarga cardíaca. Cuando se detectaron estenosis con flujos altos no se dilataron con balón de angioplastia porque aumentaría el flujo y podría producir isquemia por robo vascular o sobrecarga cardíaca. Este problema es mayor en las fístulas humerales que en las distales8. Una estenosis podrá ser «compensadora» reduciendo el flujo cuando este es alto. La medida del flujo evitará que se dilate la estenosis «compensadora». Cuando no hubo indicación de angioplastia, por ejemplo, en estenosis yuxtaanastomóticas en fístulas radiales, la medida del flujo alertó al cirujano de que la nueva anastomosis no debía ser amplia si el flujo era suficiente, por el riesgo de convertirla en una fístula de alto flujo.
A veces, las medidas no reflejaron el verdadero resultado clínico y angiográfico del tratamiento radiológico. Esto ocurrió en los rescates de las fístulas trombosadas, cuando tras la tromboaspiración manual y la angioplastia de las lesiones los 2 introductores gruesos (hasta 9French) y las guías de seguridad en la luz de la fístula alteraron las medidas. En estos casos hubo que retirar uno de los introductores y las guías de seguridad para volver a medir mejor el flujo cuando la luz vascular estaba más libre. Lo mismo ocurrió en los casos en los que tras una angioplastia satisfactoria, un espasmo junto a la entrada del introductor, que se comportaba como una estenosis, impedía reflejar la mejoría del flujo. En estos casos hubo que puncionar en sentido contrario y dilatar el espasmo con un balón de angioplastia a 2 o 3atmósferas. Algo similar ocurría con la retracción elástica postangioplastia («elastic recoil»), que había también que tratar. Cuando el flujo no mejoraba tras la angioplastia y no se detectaba espasmo o retracción elástica, había que pensar en lesiones de la arteria de la fístula o en un gasto cardíaco alterado9.
DiscusiónHabitualmente, palpar la fístula tras un tratamiento radiológico suele dar una idea subjetiva del éxito5. Con nuestro estudio proponemos que medir el flujo antes y después de la angioplastia es más objetivo que la exploración física. Además, nuestros resultados nos han permitido determinar en qué casos hay que hacer angioplastia o no, y cuándo tenemos que finalizar el tratamiento.
Los estándares internacionales8–11 recomiendan que se valore el resultado del procedimiento tras la angioplastia de una fístula de diálisis basándose en la estenosis residual (menor del 30%) y el gradiente de presión transestenótico12. Sin embargo, estas 2 medidas solo valoran la lesión tratada y no dan información hemodinámica del circuito tras el tratamiento. De hecho, los criterios angiográficos para valorar el éxito de una angioplastia no predicen cambios en el flujo del acceso vascular5,8,12,13. Muchas veces se tiende a sobrestimar el grado de estenosis antes de la angioplastia y el éxito técnico, basándose en el grado de estenosis residual14. Por el contrario, el flujo de la fístula de diálisis aporta información hemodinámica que refleja mejor su funcionamiento15–17. La medida del flujo valora cuantitativamente toda la fístula, incluyendo la arteria donante, la anastomosis y el lecho venoso distal a la lesión tratada18. Además, el catéter compara los valores del flujo antes y después del tratamiento, da una medida real del resultado, puede decidir si utilizar otro balón de mayor diámetro, investiga lesiones no detectadas (si no ha habido mejoría del flujo) o da por finalizado el procedimiento.
Aunque no hemos realizado un estudio en términos de rentabilidad económica, creemos que el ahorro en catéteres de angioplastia cuando las medidas del flujo o el aumento de la permeabilidad del acceso no la aconsejaran (fístulas de alto flujo), y cuando la trombosis del acceso se evitara por detectar lesiones que de otro modo podrían pasar desapercibidas, compensaría el precio del catéter ReoCath™ a corto y medio plazo.
En la práctica diaria, una de las principales objeciones que se le hacen al ReoCath™ es que no avanza sobre guía, con el consiguiente peligro de perforación del vaso. En las 598 sesiones en las que lo hemos empleado solo hemos tenido 2 perforaciones, lo que supone el 0,35%. Esta cifra tan baja ha sido fundamentalmente debida a las precauciones tomadas durante el manejo del catéter, empleando el road mapping o la guía ecográfica mientras se avanzaba. No obstante, un futuro diseño de catéter sobre guía podría dar más seguridad al radiólogo vascular con menos experiencia en su manejo.
Correlacionar la medida del flujo con ReoCath™ con la ecografía doppler durante los procedimientos en la misma sala de radiología vascular es difícil de realizar. Creemos que el método de dilución ultrasónica del catéter ReoCath™ es más fiable que la ecografía, porque no está sometido a la subjetividad del operador y a la variabilidad del ecógrafo18–20. No obstante, un estudio ulterior podría comparar las medidas del flujo con la ecografía antes y después del procedimiento invasivo, es decir, con las medidas ecográficas realizadas fuera de la sala de radiología vascular y hechas a doble ciego.
Por último, nos hemos visto limitados en ocasiones a seleccionar los casos en los que íbamos a emplear el catéter medidor sin atender a un estricto criterio de selección. Estos defectos nos ayudarán a ser más rigurosos en el futuro.
En definitiva, el catéter medidor de flujo ReoCath™ proporciona información «cuantitativa» de la funcionalidad del acceso vascular de hemodiálisis durante los procedimientos de radiología vascular intervencionista, evalúa el éxito de la angioplastia, aumenta la longevidad del acceso y evita la reintervención.
Responsabilidades éticasProtección de personas y animalesEl autor declara que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosEl autor declara que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoEl autor declara que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.
A la Dra. Noelia Lacasa Pérez, por su participación en la recogida de los datos. Al Dr. Vicente García Medina, por la supervisión general del equipo de investigación.