Valorar la sobrecarga férrica mediante el cálculo del valor T2* en el hígado y el miocardio en los pacientes con hemocromatosis secundaria. Evaluar la correlación de los valores obtenidos con los niveles de ferritina en sangre y la concentración de hierro hepático (CHH) calculada mediante resonancia magnética (RM), y la correlación de los valores T2* entre sí.
Material y métodosSe incluyeron 16 pacientes (13 varones y 3 mujeres), evaluados entre los años 2008 y 2009, con una edad media de 61 años. Quince eran pacientes politransfundidos y uno estaba diagnosticado de anemia sideroblástica hereditaria.
Se estudió la ferritina en sangre, la CHH por RM, la función cardíaca mediante RM y el valor T2* mediante secuencias multieco en el hígado (TR/TE1/ΔTE/n°ecos/α: 21/1,18/1.0/20/35°) y el miocardio (26/1,04/0.8/30/60°). Se realizó el análisis de correlación-regresión de los valores T2* cardíaco y hepático con los valores de ferritina y CHH, y entre sí.
ResultadosTrece pacientes mostraron valores de ferritina superiores a 1.000ng/ml (mediana/mínimo/máximo: 1.762/294/3.785ng/ml). Trece pacientes presentaron CHH elevada, mayor de 80μmol/g (mediana/mínimo/máximo: 125,4/41,2/241,5μmol/g). En todos los casos la función cardíaca estaba preservada. En 15 pacientes el valor T2* hepático fue menor de 6,3ms. Solo en un caso, el valor T2*miocárdico fue menor de 20ms. Se observó una alta correlación para los valores T2*hepático/CHH (r:-0,912). La correlación fue estadísticamente significativa para T2* hepático/ferritina (r:-0,541). La correlación T2*miocárdico/ferritina, T2*miocárdico/CHH y T2*miocárdico/T2*hepático no fue estadísticamente significativa.
ConclusiónLos valores T2* hepático muestran una alta correlación con la CHH y una correlación estadísticamente significativa con la ferritina. No se observó correlación entre los valores T2* miocárdico y la ferritina en sangre, la CHH, ni con el valor T2* hepático.
To determine whether there is iron overload by calculating the T2* value in the liver and myocardium in patients with secondary haemochromatosis. To analyse the correlation of the values obtained with the iron levels in blood, with the liver iron concentration (LIC) calculated using magnetic resonance (MR) imaging, and the correlation between them.
Material and methodsA total of 16 patients (13 males, 3 females), with a mean age of 61 years, were included and evaluated in the years 2008 and 2009. Fifteen of them had received multiple transfusions, and one was diagnosed with hereditary sideroblastic anaemia.
The measurements included, blood ferritin, LIC by MRI, cardiac function using MRI and the T2* value by means of multi-echo sequences in the liver (TR/TE1/ΔTE/No of echos/α: 21/1,18/1.0/20/35°) and myocardium (26/1.04/0.8/30/60°). A correlation-regression analysis was performed by comparing the cardiac and liver T2* values with the ferritin, LIC and between each of them.
ResultsA total of 13 patients had ferritin values greater than 1000ng/ml (median/minimum/maximum: 1762/294/3785ng/ml). An increased LIC greater than 80μmol/g (median/minimum/maximum: 125.4/41.2/241.5μmol/g) was observed in 13 patients. In all cases cardiac function was conserved, and in 15 cases the liver T2* value was less than 6.3ms. The myocardium T2* value was less than 20ms. in only one case. A high correlation was observed between the liver T2* values and the LIC (r:-0.912). The correlation was statistically significant between the liver T2* value and ferritin (r:-0.541). The correlations between myocardium T2* and ferritin, myocardium T2* and LIC, and myocardium T2* and liver T2* were not statistically significant.
ConclusionsThe liver T2* showed a high correlation with LIC and a statistically significant correlation with ferritin. No association was observed between the myocardium T2* values and ferritin in blood, the LIC or the liver T2* value.
El hierro es un elemento esencial en numerosos procesos metabólicos y biológicos. Los niveles de hierro en el organismo dependen exclusivamente de la regulación de su absorción en el sistema gastrointestinal, ya que el cuerpo humano no cuenta con mecanismos de excreción. Cuando está presente en exceso, produce importantes daños tisulares debido a que genera radicales libres e induce al estrés oxidativo. Si la sobrecarga férrica no se trata oportunamente, los daños provocados pueden llegar a ser irreversibles.
La sobrecarga férrica puede deberse a una absorción gastrointestinal del hierro anormalmente elevada (hemocromatosis primaria o hereditaria) o bien puede ser secundaria a transfusiones múltiples. En este último grupo se encuentran además enfermedades hematológicas que cursan con diseritropoyesis, lo que a su vez puede condicionar un aumento de la absorción del hierro y contribuir o ser la causa de la sobrecarga férrica.
El exceso de hierro se acumula en distintos órganos entre los que se encuentran el hígado y el corazón, lo que puede conducir a la cirrosis hepática y hepatocarcinoma en el caso de sobrecarga férrica hepática, y a la cardiomiopatía, arritmia, insuficiencia cardíaca e incluso muerte súbita en el caso de sobrecarga férrica cardíaca1,2. La transfusión de más de 20-30 unidades puede provocar depósitos altos de hierro. La aparición de fármacos quelantes del hierro abre la posibilidad de controlar el exceso de hierro en el organismo, pero son fármacos que no están exentos de reacciones adversas y cuyo coste es elevado. Por tanto, la determinación precoz de la existencia y el grado de la sobrecarga férrica en estos órganos es crucial.
Los marcadores séricos que se utilizan en el seguimiento tienen un valor predictivo limitado para determinar la aparición de la enfermedad en estos órganos3. Valores de ferritina mayores que 1.000ng/ml pueden estar indicando una sobrecarga férrica, pero estos valores también pueden estar elevados por otras condiciones distintas a la sobrecarga férrica.
El mejor parámetro para evaluar el depósito real de hierro es la cuantificación de la concentración de hierro hepático (CHH) para lo que se requiere una biopsia hepática, método invasivo y no exento de morbilidad.
La resonancia magnética es una técnica no invasiva que ha sido evaluada en múltiples trabajos dirigidos a analizar la sobrecarga férrica hepática y cardíaca, con muy buenos resultados4–9. Esta técnica detecta indirectamente la sobrecarga de hierro debido al efecto paramagnético de los depósitos de dicho elemento en los tejidos, lo que determina un acortamiento del T2 que conlleva una disminución de la señal tisular proporcional a la concentración de hierro. Los dos métodos utilizados en resonancia magnética (RM) para la estimación del hierro son la ratio de intensidad de señal y la relaxometría10. En el método de la ratio de la intensidad de señal, se divide la intensidad de señal medida en el órgano diana por la intensidad de señal medida en un órgano al que no afecta la sobrecarga férrica, como pueden ser el músculo o la grasa. La relaxometría mide directamente el tiempo de relajación transversal T2, o T2* si se utilizan secuencias eco de gradiente, que será tanto más corto cuanto mayor sea la sobrecarga férrica.
Algunos trabajos han demostrado que cuantificar la CHH por el método de la ratio de intensidad de señal se correlaciona bien con la medida de CHH con la biopsia hepática4,5. Nuestro centro validó en 2002 un modelo de cuantificación de la CHH basado en la medida de la ratio de intensidad de señal hígado/músculo. La correlación con la concentración de hierro medida mediante biopsia fue alta, de manera que, en nuestro hospital, la RM ha sustituido a la biopsia para determinar los niveles de hierro hepático. Cuando la CHH medida con este modelo es mayor de 85μmol/g, el valor predictivo positivo para determinar una sobrecarga férrica hepática es del 100%. Una CHH menor de 20μmol/g va en contra de la sobrecarga férrica4.
El método de la relaxometría permite evaluar la concentración de hierro hepático y cardiaco midiendo el acortamiento del tiempo de relajación T2 o T2* debido al aumento de la heterogeneidad de campo causado por el depósito de hierro en los tejidos. En el hígado se considera que un valor T2*hepático (T2*H) mayor de 6,3ms va en contra de una sobrecarga férrica, y un valor T2*H menor de 1,4ms, sugiere una sobrecarga férrica grave11. En el corazón, el valor T2* ha demostrado ser útil en el manejo de pacientes con sobrecarga férrica secundaria, ya que es altamente predictivo del riesgo de miocardiopatía por sobrecarga férrica7,8,12,13. Los pacientes con valores T2*miocárdico (T2*M) mayores de 20ms (no se detecta hierro cardíaco) no desarrollan disfunción cardíaca, mientras que los pacientes con T2*M menores de 10ms tienen un alto riesgo de descompensación cardíaca3,13. Además, esta técnica ha demostrado ser reproducible y transferible7,8,14,15.
Teniendo estos datos en cuenta, y dado el creciente interés por determinar el hierro hepático y cardíaco mediante RM en el Servicio de Hematología de nuestro hospital, nuestro objetivo fue valorar mediante RM el valor T2*H y T2*M en pacientes con hemocromatosis secundaria y evaluar su correlación con los valores de ferritina, y CHH entre sí.
Material y métodoPacientesDurante los años 2008 y 2009 se incluyeron 16 pacientes (13 varones y tres mujeres), con edades comprendidas entre los 19 y 78 años (media: 61 años). Los 16 estudios se realizaron por petición médica para estudiar la sobrecarga férrica cardíaca y hepática mediante RM. Para ello, se realizó el protocolo habitual y las secuencias dirigidas al estudio de sobrecarga férrica que posteriormente se describen. Ello no supuso una prolongación significativa de la exploración ni riesgo añadido para los pacientes. Todos ellos dieron su consentimiento informado para la prueba. Por estas razones no se solicitó el permiso del comité de ética. Quince fueron pacientes politransfundidos (4 por síndrome mielodisplásico, 3 por mielofibrosis, por aplasia medular, 1 en el contexto de transplante hepático, 1 linfoma no Hodking, 1 leucemia aguda linfocítica, 1 leucemia mieloide aguda y 1 leucemia aguda no linfocítica). En un caso, la sobrecarga férrica fue secundaria a una anemia sideroblástica hereditaria. En 14 de los 15 casos postransfusionales se administraron más de 20 unidades transfundidas. En un paciente se realizó una politransfusión intensa, pero no hemos podido conocer el número de unidades (tabla 1). En todos ellos se obtuvieron los valores de ferritina en sangre (valor normal: varón adulto: 12-300ng/ml; mujer adulta: 10-150ng/ml).
Descripción de los pacientes
| Pacientes | Afección | Sexo/edad | Unidades transfundida |
| 1 | Síndrome mielodisplásico | F/75 | 121 |
| 2 | Síndrome mielodisplásico | F/77 | 33 |
| 3 | Aplasia medular | V/73 | 138 |
| 4 | Síndrome mielodisplásico | V/73 | 51 |
| 5 | Mielofibrosis idiopática | V/73 | 60 |
| 6 | Insuficiencia renal crónica | V/61 | 21 |
| 7 | Mielofibrosis idiopática | V/68 | 30 |
| 8 | Síndrome mielodisplásico | V/63 | 86 |
| 9 | Lifoma no Hodking+autotrasplante | V/61 | 30 |
| 10 | Anemia sideroblástica hereditaria | V/52 | * |
| 11 | Mielofibrosis idiopática | V/57 | 22 |
| 12 | Leucemia aguda linfoblástica | V/32 | 41 |
| 13 | Leucemia aguada no linfoblástica | F/78 | 58 |
| 14 | Aplasia medular | V/54 | 23 |
| 15 | Aplasia medular | V/19 | 236 |
| 16 | Leucemia mieloide aguda | V/54 | ** |
*Sobrecarga férrica por anemia sideroblástica hereditaria; **Politransfusión intensa (número de unidades transfundidas no conocido). V: Hombre; F: Mujer.
Las exploraciones de RM se llevaron a cabo en un equipo RM 1.5T (Philips Health Care, Achieva). En un mismo estudio se evaluaron la concentración de hierro hepático (CHH) por RM siguiendo el modelo previamente validado en nuestro centro4, la función cardíaca y el valor T2* mediante secuencias eco de gradiente (EG) multieco en el hígado (T2*H) y el miocardio (T2*M). La duración media del estudio completo fue de 60 minutos.
Para determinar la CHH se obtuvieron dos secuencias EG (densidad protónica y T2; TR/TE/α: 120/4-14/20°) con una bobina de cuadratura integrada en el equipo, en incidencia el plano axial, con una apnea de 20 segundos. En cada secuencia se midió la intensidad de señal (IS) con regiones de interés (ROI) de más de 1cm2 en el lóbulo hepático derecho y en la musculatura paravertebral derecha e izquierda (fig. 1). Todos los valores se introdujeron en una hoja de cálculo para cuantificar la CHH (fig. 2).
Resonancia Magnética. Planos axiales abdominales a la altura del centro del hígado. Colocación de las ROI en las secuencias ponderadas en densidad protónica* y T2* en el parénquima hepático libre de estructuras vasculares, y sobre la musculatura paravertebral, para calcular de la CHH.
El cálculo de T2*H se realizó mediante una secuencia axial EG multieco (TR/primer eco (TE1)/intervalo entre ecos (ΔTE)/n°ecos/α: 21/1,18/1.0/20/35°), con un solo corte a través del centro del hígado, en una apnea de 15 segundos. La señal de los diferentes ecos se ajustó a un modelo monoexponencial, con la ecuación:
donde S(TE) es la intensidad de señal para cada uno de los ecos; S0 es el valor de la señal para TE igual a cero; T2* es el tiempo de relajación y TE es el tiempo de eco para cada una de las imágenes. De este ajuste se estimó el valor T2* para cada píxel de la imagen16 construyendo un mapa paramétrico de imágenes T2*. Para la medición se colocó una ROI en el mapa paramétrico T2* excluyendo estructuras vasculares (fig. 3).Resonancia Magnética. Secuencia axial en eco de gradiente multieco en una sola sección a la altura del centro del hígado. Colocación del ROI para la estimación del valor T2*H (gráfico superpuesto). Nótese la caída de señal del parénquima hepático a medida que el tiempo de eco aumenta.
Para el cálculo de T2* M se realizaron tres cortes paralelos en la proyección eje corto sobre el ventrículo izquierdo, uno en la base, otro en el tercio medio y otro en el segmento apical, utilizando la secuencia EG multieco T2* (TR/TE1/ΔTE/n°ecos/α: 26/1,04/0.8/30/60°), con sincronización cardiaca y una apnea de 17 segundos. Cada corte fue adquirido al final de la diástole. De la misma manera que en el estudio hepático, con la señal de los diferentes ecos se estimó un mapa paramétrico T2*. En dicho mapa se dibujó una ROI en el septo interventricular, excluyendo la luz endocavitaria y áreas próximas a las venas coronarias (fig. 4).
El cálculo de la fracción de eyección ventricular izquierda (FEVI) se realizó mediante el método Simpson17 utilizando secuencias cine multieco multicorte SSFP, proyección eje corto (TR/TE/fases: 3,1/1,5/30).
Tanto para el cálculo T2*H como para el estudio cardiaco completo utilizamos la bobina phase-array de 5 elementos.
Los datos fueron recogidos por diferentes personas experimentadas. Todos estos datos fueron supervisados por una misma persona también con una alta experiencia.
Análisis estadísticoSe realizó el estudio de correlación-regresión de los valores T2*H con los valores de ferritina y CHH, de los valores T2*M con los valores de ferritina y CHH y de los valores T2*H y T2*M entre sí. En los análisis se consideró α=0,05. El estudio estadístico se realizó mediante el paquete estadístico SYSTAT V9.0. (Chicago, IL). Para determinar la distribución de las variables se utilizó el test de Shapiro-Wilk.
ResultadosLos valores de ferritina en sangre oscilaron entre 294 y 3.785ng/ml (mediana: 1.762ng/ml). Trece pacientes mostraron valores de ferritina en sangre mayores de 1.000ng/ml. Trece pacientes presentaron una CHH alta, mayor de 80μmol/g (mediana: 125,4μmol/g). En 15 pacientes el valor T2*H fue menor de 6,3ms (mediana: 2,90ms). Solo en un caso el valor T2*M fue menor de 20ms (mediana: 29,1ms).
Los valores de la FEVI variaron entre 50,9 y 75,2% (mediana: 63,7%). En ningún caso fueron sugestivos de disfunción ventricular izquierda.
Según el test de Shapiro-Wilk todas las variables siguieron una distribución normal, salvo la CHH que se alejó ligeramente de la normalidad (p=0,045).
En la tabla 2 se detallan los valores de FEVI, T2*M, T2*H, CHH y ferritina, obtenidos para cada paciente. En la tabla 3 se describen las variables.
Valores obtenidos para cada paciente
| Pacientes | CHH (μmol/g) | T2*H (ms) | T2*C (ms) | FE (%) | Ferritina (ng/ml) |
| 1 | 226 | 1,8 | 15 | 59,7 | 2.374 |
| 2 | 102,8 | 4 | 27,2 | 72,3 | 855 |
| 3 | 226,2 | 1,5 | 26,1 | 64 | 2.000 |
| 4 | 225 | 1,7 | 25,7 | 51 | 3.785 |
| 5 | 229,5 | 1,5 | 34 | 63 | 2.859 |
| 6 | 52,4 | 5,6 | 20,6 | 57,9 | 1.923 |
| 7 | 106 | 4,5 | 33,3 | 63,7 | 1.708 |
| 8 | 232,4 | 1,8 | 33,8 | 63,7 | 1.227 |
| 9 | 113,8 | 3,3 | 38,2 | 55,8 | 1.973 |
| 10 | 78 | 4,1 | 31,8 | 67,4 | 294 |
| 11 | 104,1 | 3,2 | 24,5 | 68,1 | 1.000 |
| 12 | 104,2 | 3,2 | 29,6 | 71,9 | 1.200 |
| 13 | 137 | 2,3 | 34,2 | 75,2 | 1.816 |
| 14 | 41,2 | 6,8 | 29,2 | 61,1 | 911 |
| 15 | 241,5 | 1,5 | 27,6 | 67,6 | 2.257 |
| 16 | 144,3 | 2,6 | 28,6 | 58,7 | 1.276 |
CHH: concentración de hierro hepático; T2*H: T2* hepatico; T2* c: T2* cardiac.
Descripción de las variables
| Variables | N.° | Mínimo | Máximo | Media | Desviación estándar | Mediana |
| T2* hepático (ms) | 16 | 1,5 | 6,8 | 3,09 | 1,58 | 2,90 |
| T2* cardíaco (ms) | 16 | 15 | 38,2 | 28,7 | 5,7 | 29,1 |
| CHH (μmol/g) | 16 | 41,2 | 2.41,5 | 147,7 | 70,7 | 1.25,4 |
| Ferritina (ng/ml) | 16 | 294 | 3.785 | 1.778,6 | 944,7 | 1.762 |
| FEVI (%) | 16 | 50,9 | 75,2 | 63,8 | 0,06 | 63,7 |
CHH: concentracion de hierro hepatico; FEVI: fracción de eyección ventricular izquierda.
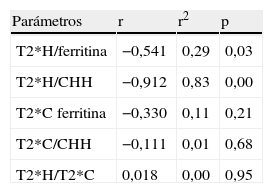
De los 15 pacientes para los que el valor T2*H fue menor de 6,3ms, 13 mostraron valores de ferritina mayores de 1.000ng/ml. En 1 el valor obtenido fue de 855ng/ml y en 1 fue normal (294ng/ml). La correlación estimada entre el valor T2*H y la ferritina fue significativa (r:-0,541; r2:0,29).
En los 15 pacientes con valores T2*H menor de 6,3ms, la CHH reveló la existencia de sobrecarga férrica. En trece casos fue mayor de 80μmol/g. De los otros 2, en 1, el valor obtenido fue próximo al valor considerado como sobrecarga férrica grave (78μmol/g). En el otro caso, la CHH indicaba una sobrecarga férrica moderada (52μmol/g). La correlación obtenida entre ambos parámetros fue alta (r:-0,912; r2:0,83; p<0,05).
No se encontró correlación significativa entre el valor T2*M y la ferritina (r:-0,330; r2: 0,11; p>0,05) ni entre el valor T2*M y la CHH (r:-0,111; r2:0,01; p>0,05).
Igualmente, la correlación T2*H/T2*M (r:0,018; r2:0,00; p>0,05) no fue significativa.
En la tabla 4 se detalla la relación de las variables.
DiscusiónEn nuestro estudio, la gran mayoría de los pacientes con hemocromatosis secundaria presentaron una alta sobrecarga férrica en el hígado y altos niveles de ferritina.
Tras el análisis de la asociación de T2*M y T2*H con la ferritina y la CHH, y la relación de T2*M-T2*H mediante el análisis de correlación-regresión, se observó que la asociación fue principalmente significativa para los valores T2*H y CHH. A mayor nivel de CHH, menor T2*H. Por tanto, el cálculo en RM de la concentración de hierro hepático y del valor T2* hepático resultaron herramientas útiles y con resultados similares para la determinación de la sobrecarga férrica hepática. La alta correlación era esperable, dados los buenos resultados que ambas técnicas han ido mostrando en la bibliografía para la medición del hierro hepático mediante RM5,18–20.
Los valores T2*H también se asociaron con el nivel de ferritina. La determinación de ferritina es una buena técnica de cribado para conocer el nivel de hierro corporal y puede reflejar una sobrecarga férrica hepática, pero hay que recordar que puede estar elevada por otras condiciones distintas a la sobrecarga férrica como procesos inflamatorios activos, determinadas hepatopatías o neoplasias21,22. Por el contrario, puede ocurrir que la ferritina sea normal y el valor T2* indique sugiera una sobrecarga férrica hepática, como sucedió en uno de nuestros casos. Se trata del paciente con anemia sideroblástica hereditaria, afección encuadrada dentro del grupo de las «anemias de sobrecarga férrica», ya que es una anemia congénita que con la edad se acompaña de sobrecarga por la propia diseritropoyesis antes de tener que iniciar las transfusiones. El paciente había sido diagnosticado 20 años antes de realizar el estudio por RM. En este período fue transfundido de forma esporádica. Siempre cursó con valores de ferritina normales o no muy elevados, para el nivel de hierro detectado en RM. La discordancia entre los niveles de ferritina y la concentración de hierro en el hígado podría deberse a que en los pacientes con diseritropoyesis, el exceso de hierro absorbido queda almacenado en el hígado durante un largo período de tiempo y, por ello, los niveles de ferritina en sangre son menores. Dicha discordancia también ha sido descrita en las talasemias intermedias que, como en nuestro caso, apenas se transfunden, y pueden cursar con ferritina baja y sobrecarga hepática23.
A diferencia de lo que ocurrió en el hígado, la asociación de los valores T2*M con los de ferritina, CHH y T2*H no fue estadísticamente significativa. Desde la aparición de la RM como método de estudio del acúmulo de hierro cardíaco se ha observado que no hay una asociación significativa entre la concentración de hierro cardíaco y la concentración de hierro hepático y los niveles de ferritina. Ello se debe a que el mecanismo de recepción y eliminación del hierro del hígado y el corazón es diferente. El hierro se deposita y aclara más rápido en el hígado que en el corazón24. De hecho, la sobrecarga hepática supone un factor de riesgo de sobrecarga cardíaca. Sin embargo, no existe un valor de sobrecarga hepática que determine si existe o no sobrecarga cardíaca. Por otro lado, estas diferencias entre la cinética del hierro para ambos tejidos van a determinar diferentes respuestas de estos órganos a los distintos tratamientos quelantes3,7,25. Así, tras un tratamiento quelante intenso, se puede producir una importante reducción de los niveles de hierro en el hígado y persistir la sobrecarga de hierro en el corazón.
En ningún paciente la FEVI fue sugestiva de una disfunción sistólica cardíaca, incluido aquél para el que el valor T2* fue menor de 20ms. El deterioro de la función sistólica cardíaca es un signo tardío de toxicidad por sobrecarga férrica cardíaca. La detección de valores anómalos de T2* cardíaco se produce antes de que el depósito anómalo de hierro repercuta en la función sistólica. Ello se debe a que la RM detecta principalmente el hierro almacenado en forma de hemosiderina, no ferritina o hierro libre. La disfunción cardíaca se debe al hierro libre. A medida que el hierro se acumula en los sistemas de almacenaje, el T2* cae, pero apenas produce efecto sobre la función cardíaca. Cuando ya no existe capacidad de almacenamiento, el hierro libre plasmático aumenta y se produce el daño miocárdico y las consiguientes alteraciones miocárdicas7,25. En nuestro estudio no se valoró la función diastólica. No obstante, cabe señalar que dicha valoración es de gran interés ya que el acúmulo de hierro en la pared ventricular provoca alteraciones en el llenado ventricular por afectación de la elasticidad miocárdica y altera la función diastólica antes que la función sistólica26,27. Esta valoración puede hacerse de forma no invasiva tanto mediante ecografía como RM28.
Nuestro estudio se encuentra limitado por el escaso número de pacientes. No obstante, los resultados se asemejan a los de otras publicaciones7,29. Aunque es también una limitación el que no se realizara el estudio de la variabilidad intra-interobservador, cabe señalar que actualmente está ampliamente aceptado el que existe una buena correlación intra-interobservador7,30.
En la actualidad, la relaxometría no es una técnica disponible en todos los equipos. Cabe esperar que, dada la importancia progresiva que la RM está adquiriendo en el manejo del paciente con sobrecarga férrica, la instauración de la técnica vaya ampliándose a otros centros. Es deseable que en un futuro se consiga la estandarización del valor T2* con parámetros de adquisición y postproceso que permitan comparar los resultados entre diferentes centros y la calibración de los valores T2* en μmol/g.
En conclusión, el valor T2* muestra una alta correlación con la CHH obtenida por RM. El cálculo T2* permite evaluar la sobrecarga cardíaca incluso antes de que se produzca disfunción sistólica. La ferritina puede alertar sobre existencia de sobrecarga de hierro hepático, pero no sería de utilidad para la sobrecarga férrica cardiaca. La CHH medida por RM y el valor T2* hepático tampoco reflejan el contenido de hierro en el corazón, por lo que cada órgano necesitaría ser evaluado de forma específica e independiente.
La RM es una técnica no invasiva que puede contribuir al diagnóstico de los pacientes con sobrecarga férrica cardíaca y/o hepática. El cálculo T2* miocárdico y hepático no solo pueden tener valor diagnóstico, sino que su uso puede ser extensible al seguimiento y contribuir al manejo del paciente con hemocromatosis secundaria en cuanto a las pautas de tratamiento se refiere.
Autorías- 1.
Responsable de la integridad del estudio: MCB.
- 2.
Concepción del estudio: MCB, JMA y JS.
- 3.
Diseño del estudio: MCB, JMA y JS.
- 4.
Obtención de los datos: MCB y MU.
- 5.
Análisis e interpretación de los datos: MCB, CG y AG.
- 6.
Tratamiento estadístico: MCB.
- 7.
Búsqueda bibliográfica: MCB y JMA.
- 8.
Redacción del trabajo: MCB, CG y JMA.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: JMA, MU, CG y AG.
- 10.
Aprobación de la versión final: CG, AG, MCB, JMA, MU y JS.
Los autores declaran no tener ningún conflicto de intereses.