La pancreatitis aguda es una patología común y potencialmente grave que tiene un curso clínico muy variable. Este artículo pretende revisar el papel de las distintas técnicas de imagen en el manejo de esta entidad, describir sus principales manifestaciones radiológicas y la nomenclatura específica asociada a esta entidad.
ConclusionesLas técnicas de imagen desempeñan un papel clave en el manejo de la pancreatitis aguda, desde el diagnóstico y la estadificación hasta la identificación y el tratamiento de las complicaciones, así como en la determinación de la etiología subyacente. Por ello, el radiólogo debería conocer las ventajas y limitaciones de cada modalidad de imagen en la valoración de esta patología, estar familiarizado con el amplio espectro de hallazgos radiológicos asociados a esta entidad, y conocer y usar adecuadamente la nomenclatura específica derivada de los criterios de Atlanta, lo que permitiría una mayor estandarización y calidad de los informes.
Acute pancreatitis is common; the clinical course of this potentially severe condition varies widely. This paper aims to review the role of different imaging techniques in the management of acute pancreatitis, describe the main imaging findings for this entity, and explain the terms and criteria used to classify them.
ConclusionsImaging techniques play a key role in the management of acute pancreatitis, from diagnosis and staging to identifying and treating complications, as well as in determining the underlying causes of the condition. For these reasons, radiologists should know the advantages and limitations of each imaging technique in the evaluation of acute pancreatitis, be familiar with the wide spectrum of imaging findings associated with it, and how to use the specific terminology derived from the Atlanta classification to ensure the standardization and quality of reports.
La pancreatitis aguda (PA) es una enfermedad potencialmente grave y con una incidencia creciente1. El diagnóstico de la PA se realiza habitualmente mediante una combinación de criterios clínicos y analíticos: dolor abdominal de inicio súbito epigástrico asociado a niveles sanguíneos de amilasa y lipasa de al menos el triple del límite alto de la normalidad1. Es posible hacer el diagnóstico de PA en función de diferentes hallazgos de imagen cuando dichos criterios no sean concluyentes1–11 (fig. 1). Además, el continuo avance de las técnicas de imagen ha abierto nuevas oportunidades para el estudio de la PA12,13. Los objetivos de este trabajo son revisar el papel de las técnicas de imagen y describir los hallazgos clave radiológicos asociados a la PA.
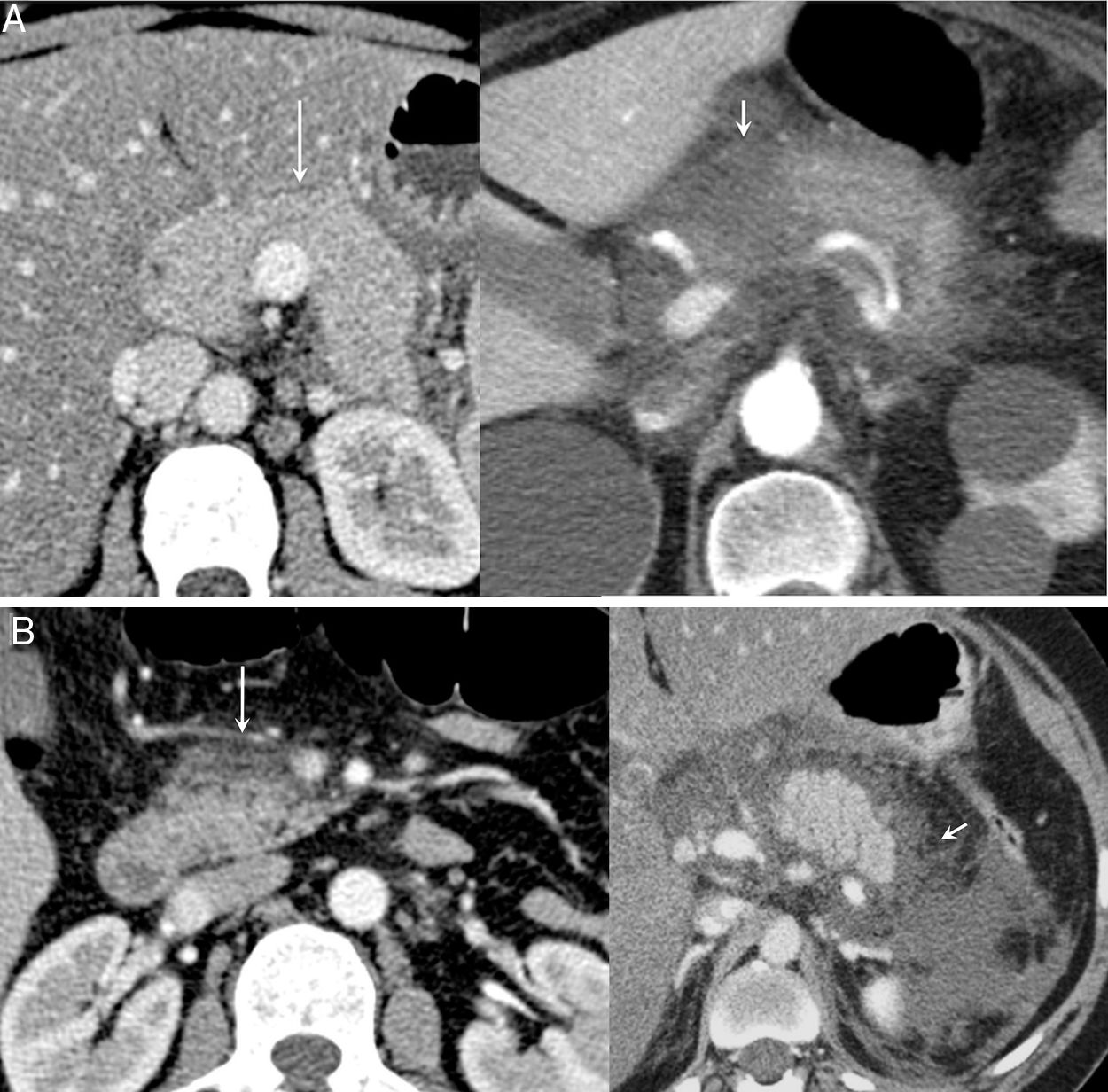
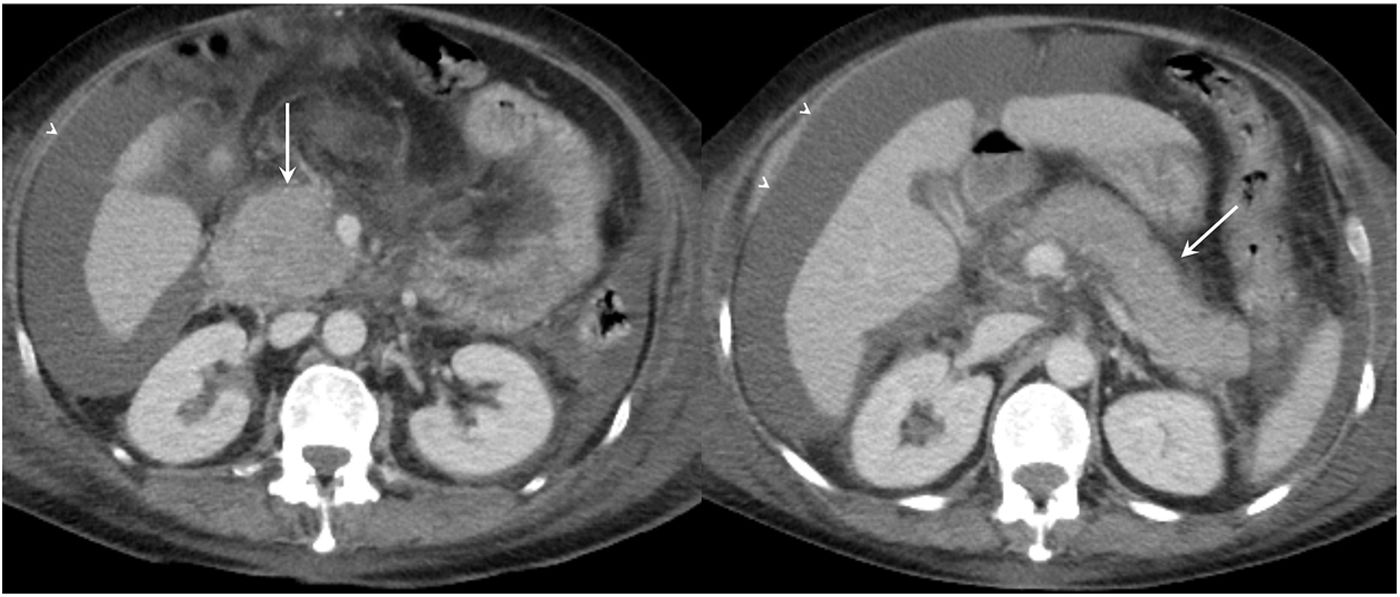
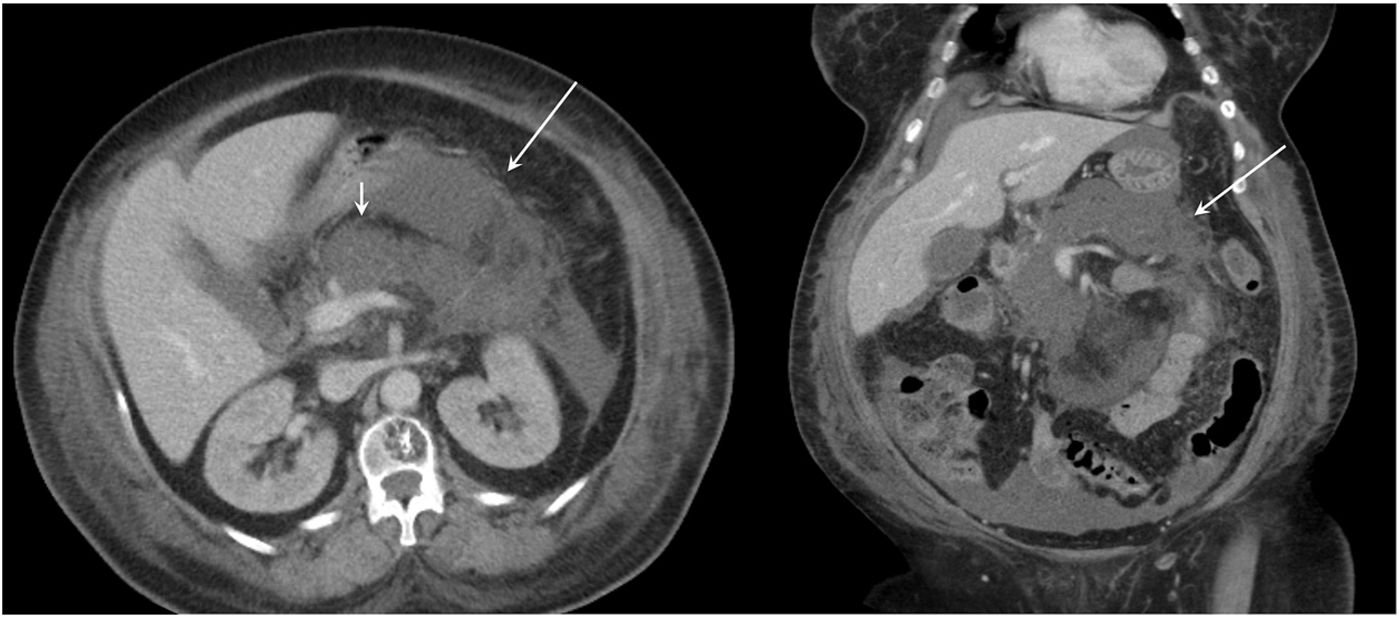
A) Diagnóstico de pancreatitis. Hallazgos radiológicos parenquimatosos que confirman el diagnóstico de pancreatitis aguda. Imágenes de tomografía computarizada (TC) con contraste del páncreas en el plano axial, de dos pacientes diferentes con aumento de tamaño de la glándula pancreática en una pancreatitis edematosa-intersticial (izquierda, flecha larga) y la heterogeneidad y ausencia del realce del parénquima pancreático en el caso de una pancreatitis necrotizante (derecha, flecha corta).B) Diagnóstico de pancreatitis. Hallazgos radiológicos extraparenquimatosos que confirman el diagnóstico de pancreatitis aguda. Imágenes de TC con contraste del páncreas en plano axial mostrando reticulación o borramiento de la grasa peripancreática (izquierda, flecha larga) (hallazgo no contemplado en la revisión de los Criterios de Atlanta) y la presencia de colecciones peripancreáticas agudas (derecha, flecha corta).
Aunque el diagnóstico y la clasificación mediante imagen de la PA se basan fundamentalmente en características morfológicas, diferentes modalidades de imagen pueden ser útiles en su evaluación1–11 (tabla 1). Inicialmente, el principal papel de la imagen en la PA sería filiar su etiología, con la ecografía como principal herramienta4–6. Las causas más frecuentes de PA son las colelitiasis (30-45%) y el consumo abusivo de alcohol (30-35%); un 20% de las PA se consideran idiopáticas (aunque se piensa que dos tercios de ellas estarían causadas por barro biliar o microlitiasis). Otras causas menos comunes serían fármacos, neoplasias, procedimientos endoscópicos, alteraciones metabólicas y funcionales o anomalías congénitas, pudiendo la imagen determinar su etiología1 (fig. 2). Además, las técnicas de imagen son básicas para valorar el grado de gravedad de la PA, detectar complicaciones asociadas y dirigir su tratamiento2–11.
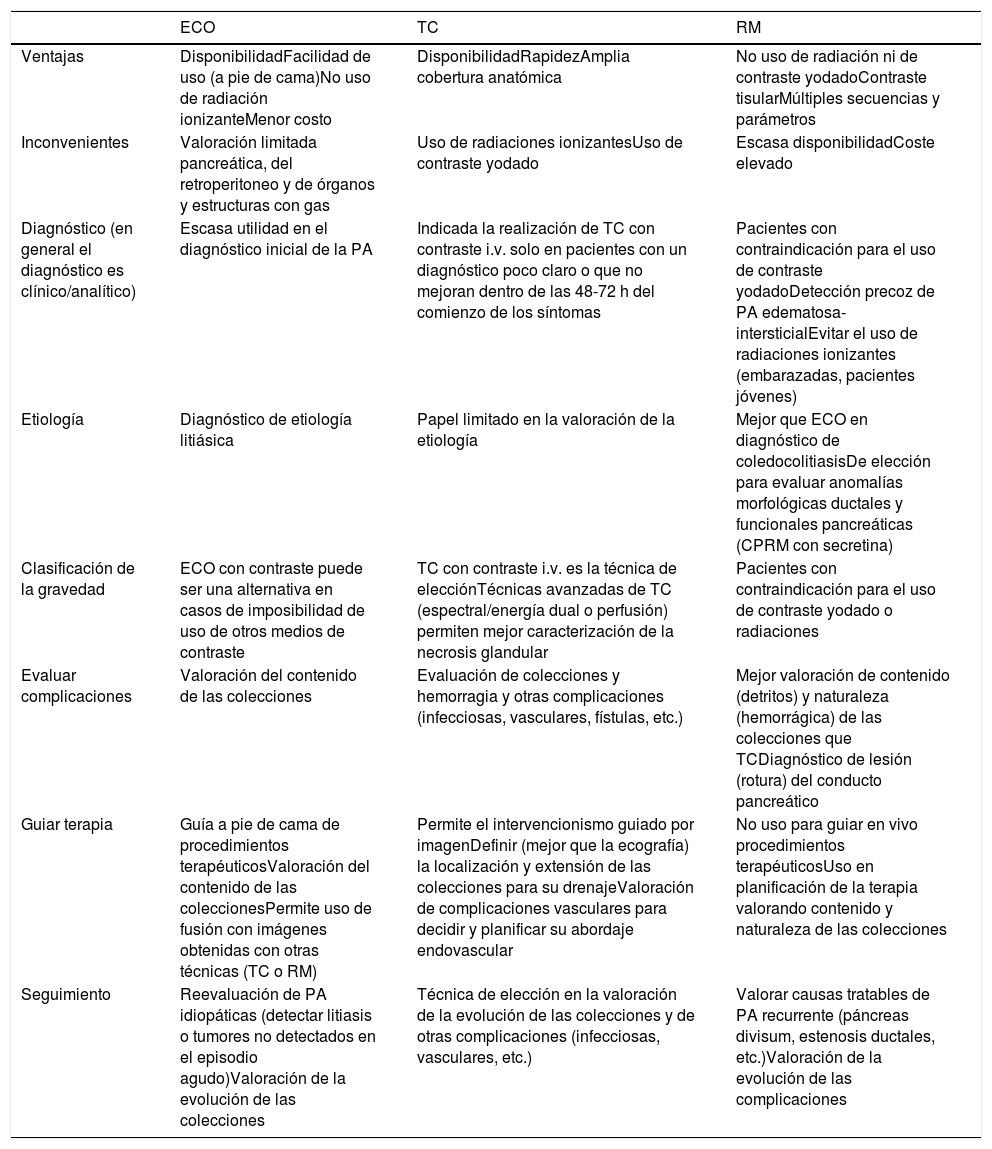
Uso, ventajas e inconvenientes de las principales técnicas de imagen en la pancreatitis aguda
| ECO | TC | RM | |
|---|---|---|---|
| Ventajas | DisponibilidadFacilidad de uso (a pie de cama)No uso de radiación ionizanteMenor costo | DisponibilidadRapidezAmplia cobertura anatómica | No uso de radiación ni de contraste yodadoContraste tisularMúltiples secuencias y parámetros |
| Inconvenientes | Valoración limitada pancreática, del retroperitoneo y de órganos y estructuras con gas | Uso de radiaciones ionizantesUso de contraste yodado | Escasa disponibilidadCoste elevado |
| Diagnóstico (en general el diagnóstico es clínico/analítico) | Escasa utilidad en el diagnóstico inicial de la PA | Indicada la realización de TC con contraste i.v. solo en pacientes con un diagnóstico poco claro o que no mejoran dentro de las 48-72 h del comienzo de los síntomas | Pacientes con contraindicación para el uso de contraste yodadoDetección precoz de PA edematosa-intersticialEvitar el uso de radiaciones ionizantes (embarazadas, pacientes jóvenes) |
| Etiología | Diagnóstico de etiología litiásica | Papel limitado en la valoración de la etiología | Mejor que ECO en diagnóstico de coledocolitiasisDe elección para evaluar anomalías morfológicas ductales y funcionales pancreáticas (CPRM con secretina) |
| Clasificación de la gravedad | ECO con contraste puede ser una alternativa en casos de imposibilidad de uso de otros medios de contraste | TC con contraste i.v. es la técnica de elecciónTécnicas avanzadas de TC (espectral/energía dual o perfusión) permiten mejor caracterización de la necrosis glandular | Pacientes con contraindicación para el uso de contraste yodado o radiaciones |
| Evaluar complicaciones | Valoración del contenido de las colecciones | Evaluación de colecciones y hemorragia y otras complicaciones (infecciosas, vasculares, fístulas, etc.) | Mejor valoración de contenido (detritos) y naturaleza (hemorrágica) de las colecciones que TCDiagnóstico de lesión (rotura) del conducto pancreático |
| Guiar terapia | Guía a pie de cama de procedimientos terapéuticosValoración del contenido de las coleccionesPermite uso de fusión con imágenes obtenidas con otras técnicas (TC o RM) | Permite el intervencionismo guiado por imagenDefinir (mejor que la ecografía) la localización y extensión de las colecciones para su drenajeValoración de complicaciones vasculares para decidir y planificar su abordaje endovascular | No uso para guiar en vivo procedimientos terapéuticosUso en planificación de la terapia valorando contenido y naturaleza de las colecciones |
| Seguimiento | Reevaluación de PA idiopáticas (detectar litiasis o tumores no detectados en el episodio agudo)Valoración de la evolución de las colecciones | Técnica de elección en la valoración de la evolución de las colecciones y de otras complicaciones (infecciosas, vasculares, etc.) | Valorar causas tratables de PA recurrente (páncreas divisum, estenosis ductales, etc.)Valoración de la evolución de las complicaciones |
CPRM: colangiopancreatografía por resonancia magnética; ECO: ecografía; i.v.: intravenoso; PA: pancreatitis aguda; RM: resonancia magnética; TC: tomografía computarizada.
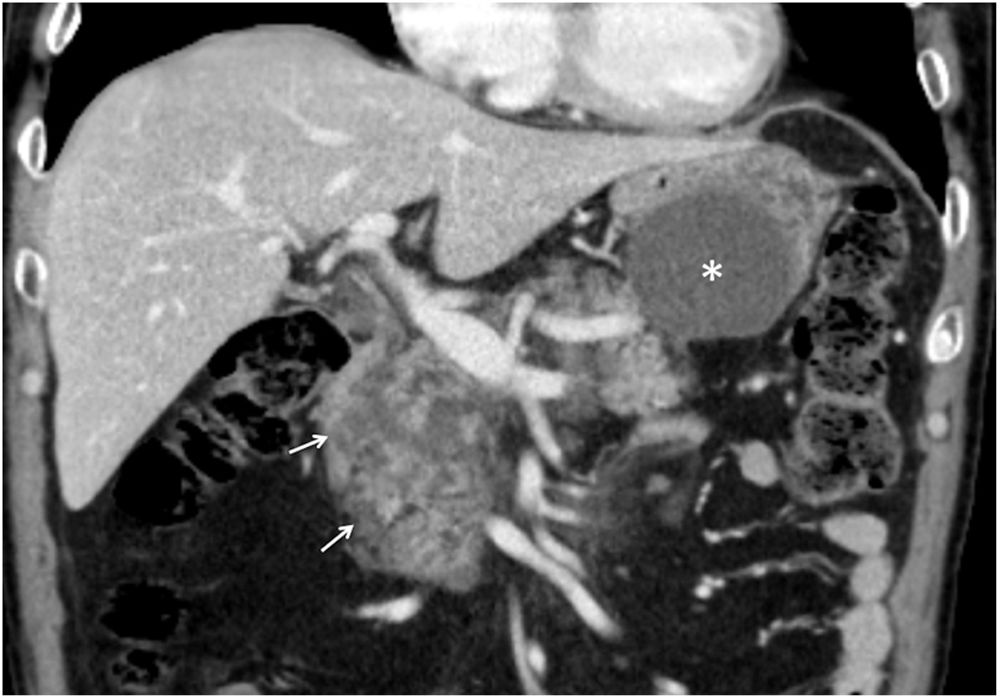
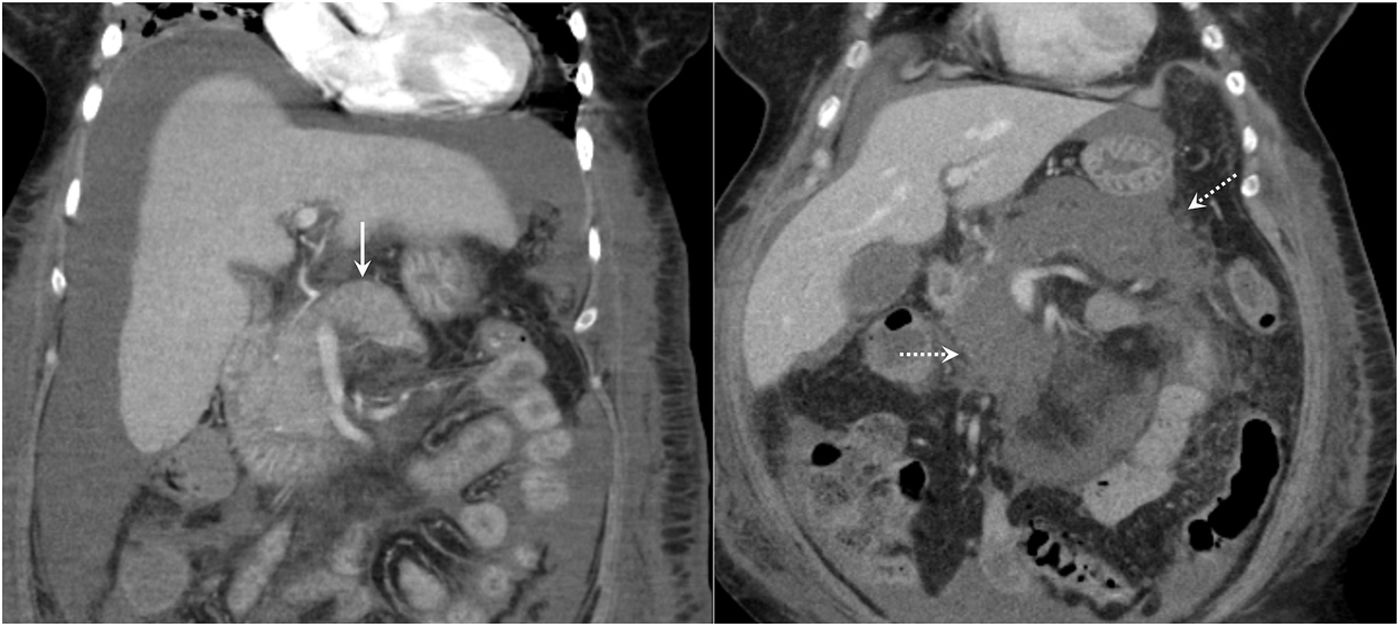
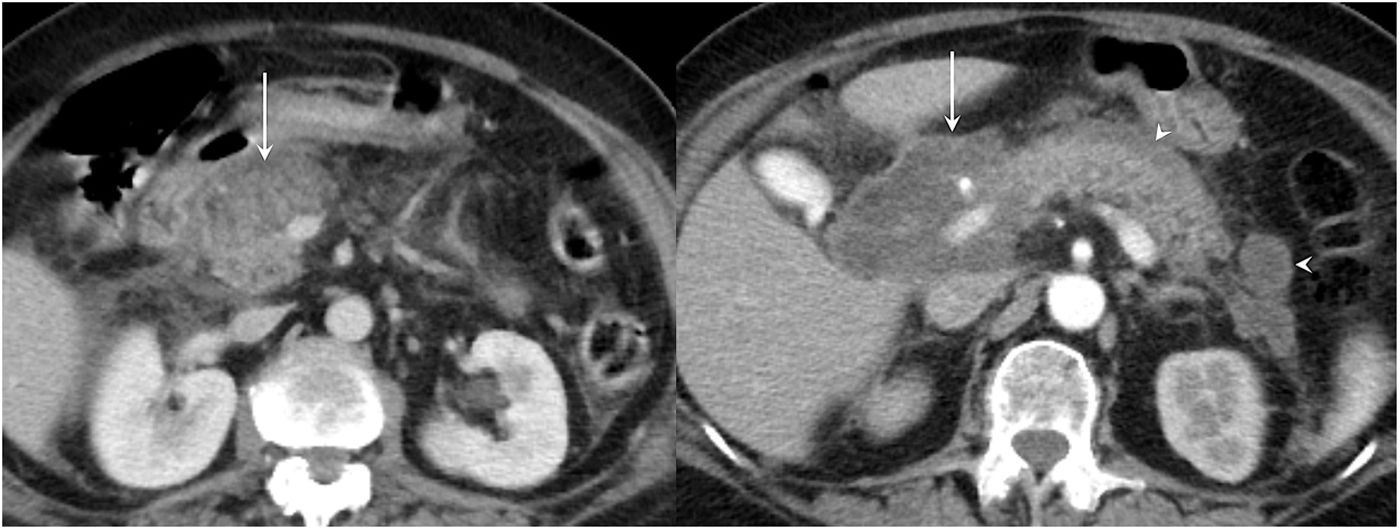
Pancreatitis por fármacos. Hombre de 62 años en tratamiento con un inhibidor de la tirosina-cinasa por carcinoma de células claras metastásico. Quince días después del inicio del tratamiento comienza con dolor abdominal y pruebas analíticas inconcluyentes. Posteriormente, un estudio de tomografía computarizada con contraste en reconstrucción coronal objetiva un aumento de tamaño de la cabeza glandular con áreas hipodensas de menos de 3cm en su interior, compatible con áreas de edema intrapancreático (flechas), y una colección aguda en cola glandular (asterisco).
La valoración ecográfica transabdominal tiene una utilidad limitada en la PA en sus fases iniciales. Su función principal sería filiar su etiología, siendo útil para la detección de colelitiasis, aunque menos sensible que la tomografía computarizada (TC) o la resonancia magnética (RM) para detectar coledocolitiasis4–6,10. La ecografía permitiría, además, caracterizar las colecciones asociadas a la PA y guiar su drenaje percutáneo9–11,14.
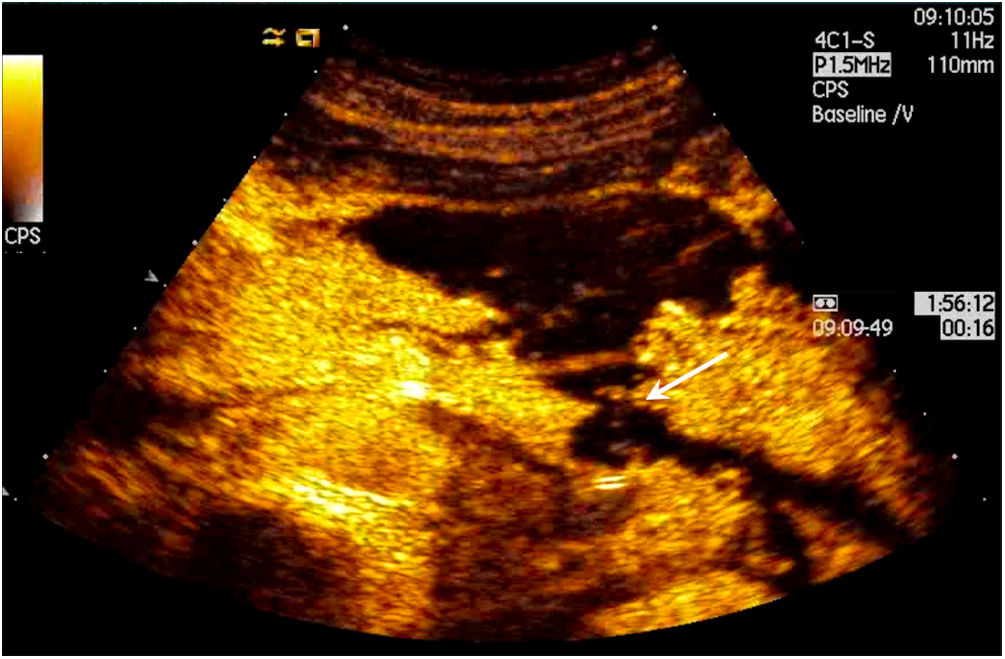
Por otra parte, nuevas técnicas ecográficas como la ecografía con contraste muestran una capacidad diagnóstica similar a la TC en la detección de necrosis pancreática, por lo que podría ser una alternativa cuando esta estuviese contraindicada15 (fig. 3). Sin embargo, también presenta limitaciones derivadas tanto de la necesidad de disponer de una adecuada ventana ecográfica como de la difícil la valoración de áreas como la cola pancreática. Otras técnicas como la elastografía han sido poco usadas en la valoración de la PA, aunque con prometedores resultados para su diagnóstico16.
Tomografía computarizadaLa mayoría de las PA suelen ser leves y asociarse a una buena evolución, resolviéndose tras tratamiento conservador y no precisando de posterior seguimiento mediante imagen. Sin embargo, en la PA de grado moderado-grave o PA leves con mala evolución tras 72 horas, estaría indicada la realización de una técnica de imagen para el diagnóstico, clasificación morfológica y valoración de gravedad de la PA1–11 (fig. 4). El protocolo de estudio varía entre los diferentes centros hospitalarios y el problema clínico a valorar (diagnóstico, seguimiento, etc.). El momento óptimo para su realización sería a partir de las 72 horas desde el inicio de la clínica, dado que antes va a existir una baja sensibilidad para la detección de la necrosis17. Además, la TC serviría para seguimiento de los pacientes que presenten necrosis/complicaciones locales y como guía para intervenciones terapéuticas (drenaje percutáneo)7,9–11.
Subtipos de pancreatitis aguda. Tomografía computarizada en plano coronal tras la administración de contraste de 2 pacientes con pancreatitis aguda. Pancreatitis aguda intersticial (izquierda) con realce homogéneo de la glándula pancreática (flecha) mientras que en el caso de la pancreatitis aguda necrotizante (derecha) se demuestra una ausencia completa de realce del páncreas, indicativa de necrosis (flechas punteadas).
Técnicas avanzadas como la TC de energía dual podrían ser útiles en la identificación de aquellos pacientes con riesgo de desarrollar necrosis y en su diagnóstico18,19 (fig. 5). Las áreas de necrosis muestran valores en los mapas de cuantificación de yodo muy inferiores a las áreas de PA sin necrosis19. Por su parte, la perfusión ha sido poco utilizada en la PA, fundamentalmente dadas las elevadas dosis de radiación asociadas a esta técnica, su complejidad y la falta de estandarización. Sin embargo, podría ayudar a identificar muy precozmente a aquellos pacientes en riesgo de desarrollo de necrosis12.
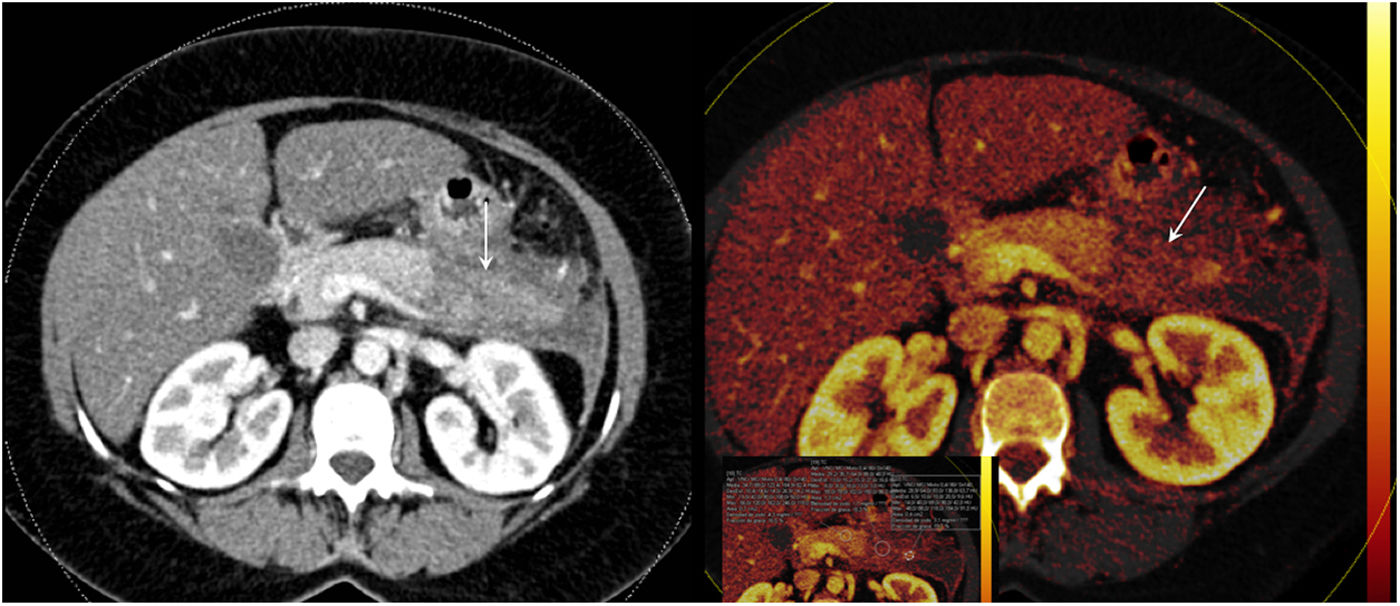
Tomografía computarizada (TC) de energía dual. Paciente con pancreatitis aguda necrotizante, con ausencia de realce de la cola pancreática en TC con contraste en fase arterial (flecha, izquierda) y en un mapa de cuantificación de yodo (derecha), con disminución de la densidad de yodo en el área de necrosis (1,7mg/ml), en relación con las porciones viables del parénquima pancreático en la cola glandular (3,1mg/ml) y en la cabeza (4,3mg/ml).
Recientemente, se ha usado la TC para la cuantificación de la grasa abdominal en pacientes con PA, lo que según Gupta et al. permitiría predecir mejor la gravedad y evolución20.
Resonancia magnéticaLa RM es una técnica de imagen capaz de aportar múltiples secuencias y parámetros para la valoración pancreática. La RM es superior a la TC para la caracterización del contenido (líquido/hemorrágico/sólido) de las colecciones y sería una buena alternativa a la TC en casos de alergia a contraste yodado o insuficiencia renal14,21–23. Además, la colangiopancreatografía por RM (CPRM) permitiría detectar pequeñas coledocolitiasis (de hasta 3 mm) (fig. 6) y valorar la integridad del ducto pancreático y su comunicación con las colecciones presentes, y tras la administración de secretina posibilitaría el estudio no invasivo de la morfología ductal y de casos con sospecha de disrupción del conducto pancreático (DCP)9–11,21,22.
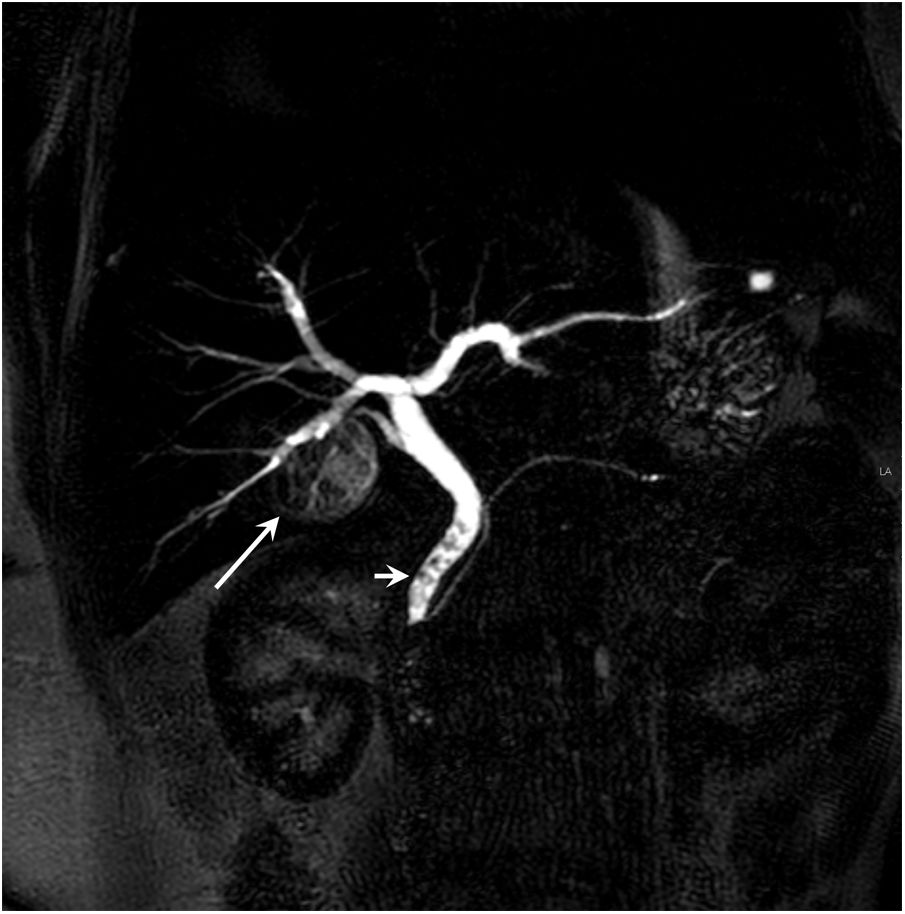
Colangiopancreatografía por resonancia magnética (CPRM). Mujer de 52 años, con dolor abdominal inespecífico y ecografía con colelitiasis. El estudio de CPRM muestra múltiples cálculos de entre 6 y 8mm (flecha corta) en el colédoco distal que producen mínima dilatación. También se identifican múltiples colelitiasis (flecha larga). La paciente fue tratada endoscópicamente.
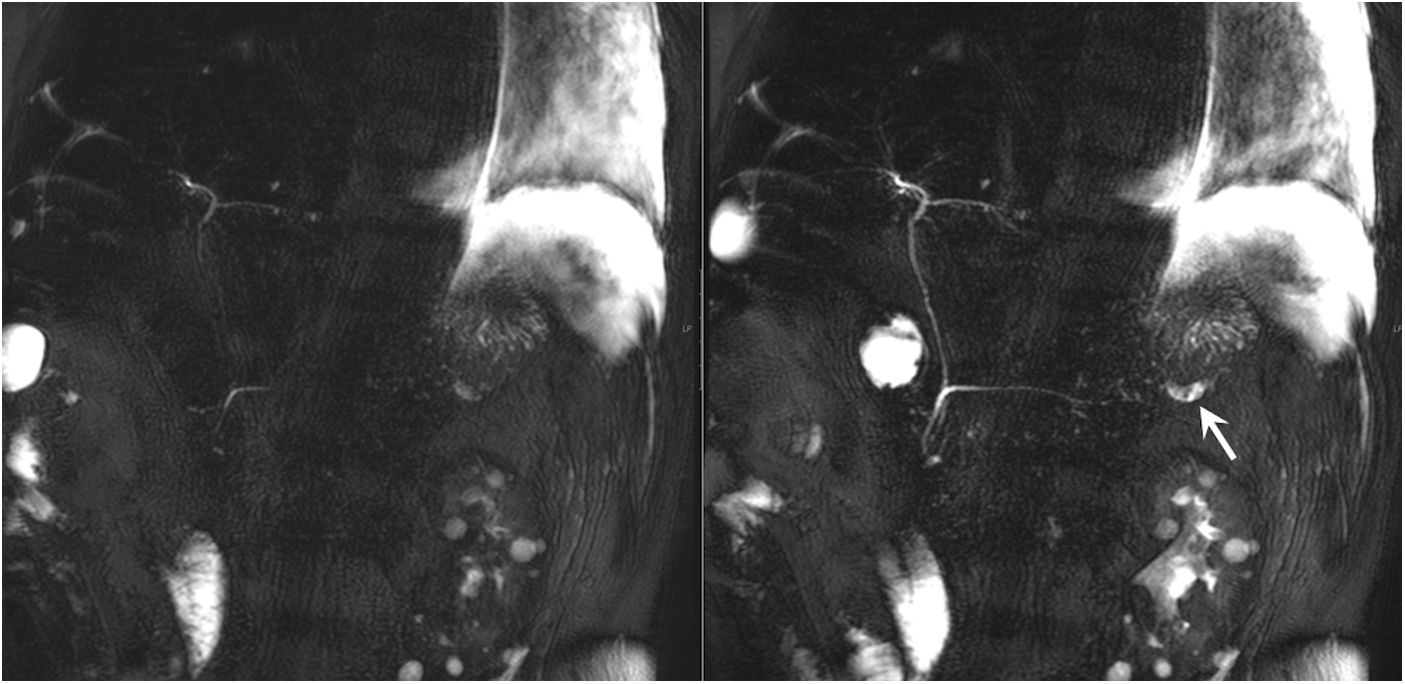
Otras técnicas de RM avanzadas han mejorado la valoración del páncreas. La difusión es actualmente una técnica fundamental dentro del protocolo de los estudios de imagen abdominal. En el caso de la PA, permitiría detectar la presencia de infección en la PA con una sensibilidad superior a la TC21–23 (fig. 7). Las técnicas de mapeo T1, T2 y T2* han mostrado un aumento de sus valores en la PA21. Finalmente, estudios preliminares han mostrado el posible valor de la elastografía mediante RM en el diagnóstico y valoración de pronóstico de la PA24.
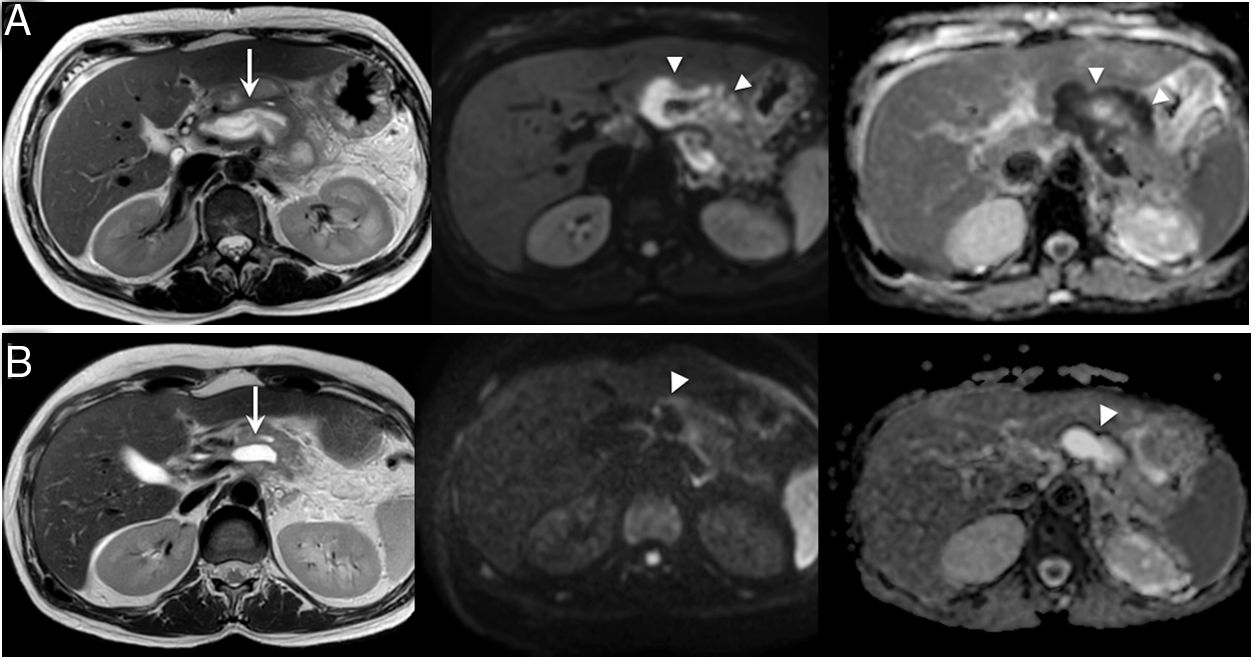
A) Resonancia magnética (RM) potenciada en difusión. RM realizada en varón con pancreatitis aguda necrotizante con colecciones infectadas. Imágenes potenciadas en T2 (izquierda), difusión b800 (centro) y mapa de ADC donde se identifica una voluminosa colección encapsulada con señal heterogénea en T2 (flecha) que muestra hiperseñal en valores altos de difusión (centro, cabezas de flecha) e hiposeñal en ADC (derecha, cabezas de flecha), hallazgos sugestivos de sobreinfección. Se inició terapia antibiótica. B) RM potenciada en difusión. RM realizada en varón con pancreatitis aguda necrotizante con colecciones infectadas tras tratamiento antibiótico. Imágenes potenciadas en T2 (izquierda), difusión b800 (centro) y mapa de ADC donde se identifica disminución de tamaño de colección encapsulada en T2 (izquierda, flecha) y clara disminución restricción de la difusión con reducción de áreas de hiperseñal en b800 (centro, cabezas de flecha) e hiposeñal en mapa de ADC (derecha, cabezas de flecha) en relación con respuesta de la infección.
Distintos biomarcadores y escalas de clasificación/pronóstico han sido usados en la PA, entre los que la imagen ocupa un papel fundamental en la definición de los tipos de PA al valorar la viabilidad del parénquima pancreático y las colecciones asociadas25. Según la última revisión de Atlanta (2012), la PA puede dividirse en dos subtipos en función de la presencia o no de necrosis: PA edematosa-intersticial y PA necrotizante2–7,9–11,26,27. La PA edematosa-intersticial (70-80% del total) presenta una microcirculación intacta y se manifiesta en imagen con un aumento de tamaño de la glándula pancreática, borrosidad de la grasa peripancreática y presencia de colecciones limitadas por los planos interfasciales (fig. 8). Por su parte, la PA necrotizante (20-30%) se asocia a pérdida de la microcirculación y a la presencia de áreas necróticas (sin realce) (fig. 9). Además, diferentes elementos relacionados con las colecciones y las áreas de necrosis asociadas a la PA deben ser considerados para su clasificación y valoración de pronóstico, incluyendo su localización y tamaño o el tiempo de evolución del cuadro 2,9–11,25–27 (tabla 2).
Pancreatitis aguda intersticial de etiología alcohólica en una mujer de 52 años. Las imágenes de tomografía computarizada con contraste intravenoso en plano axial obtenidas 7 días después del inicio del cuadro muestran un aumento de tamaño difuso de la glándula pancreática con realce homogéneo (flechas largas) y colecciones líquidas agudas peripancreáticas. Se observa también ascitis de predominio perihepático (cabezas de flecha) y un contorno nodular del hígado dado que el paciente tenía hepatopatía crónica.
Pancreatitis aguda necrotizante en una mujer de 65 años. La imagen de tomografía computarizada con contraste obtenida 6 días después del inicio de los síntomas muestra necrosis de la totalidad de la glándula pancreática (flecha corta) y una gran colección necrótica aguda (flecha larga).
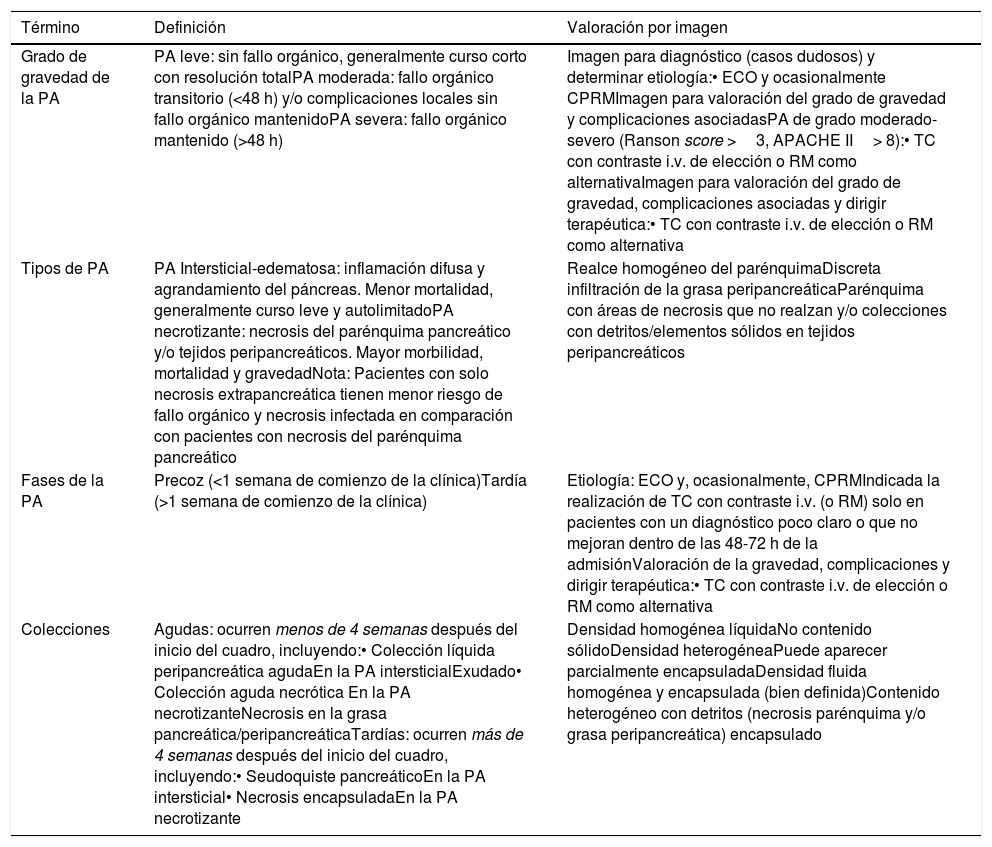
Clasificación de Atlanta revisada. Definición de sus principales conceptos y hallazgos de imagen
| Término | Definición | Valoración por imagen |
|---|---|---|
| Grado de gravedad de la PA | PA leve: sin fallo orgánico, generalmente curso corto con resolución totalPA moderada: fallo orgánico transitorio (<48 h) y/o complicaciones locales sin fallo orgánico mantenidoPA severa: fallo orgánico mantenido (>48 h) | Imagen para diagnóstico (casos dudosos) y determinar etiología:• ECO y ocasionalmente CPRMImagen para valoración del grado de gravedad y complicaciones asociadasPA de grado moderado-severo (Ranson score >3, APACHE II> 8):• TC con contraste i.v. de elección o RM como alternativaImagen para valoración del grado de gravedad, complicaciones asociadas y dirigir terapéutica:• TC con contraste i.v. de elección o RM como alternativa |
| Tipos de PA | PA Intersticial-edematosa: inflamación difusa y agrandamiento del páncreas. Menor mortalidad, generalmente curso leve y autolimitadoPA necrotizante: necrosis del parénquima pancreático y/o tejidos peripancreáticos. Mayor morbilidad, mortalidad y gravedadNota: Pacientes con solo necrosis extrapancreática tienen menor riesgo de fallo orgánico y necrosis infectada en comparación con pacientes con necrosis del parénquima pancreático | Realce homogéneo del parénquimaDiscreta infiltración de la grasa peripancreáticaParénquima con áreas de necrosis que no realzan y/o colecciones con detritos/elementos sólidos en tejidos peripancreáticos |
| Fases de la PA | Precoz (<1 semana de comienzo de la clínica)Tardía (>1 semana de comienzo de la clínica) | Etiología: ECO y, ocasionalmente, CPRMIndicada la realización de TC con contraste i.v. (o RM) solo en pacientes con un diagnóstico poco claro o que no mejoran dentro de las 48-72 h de la admisiónValoración de la gravedad, complicaciones y dirigir terapéutica:• TC con contraste i.v. de elección o RM como alternativa |
| Colecciones | Agudas: ocurren menos de 4 semanas después del inicio del cuadro, incluyendo:• Colección líquida peripancreática agudaEn la PA intersticialExudado• Colección aguda necrótica En la PA necrotizanteNecrosis en la grasa pancreática/peripancreáticaTardías: ocurren más de 4 semanas después del inicio del cuadro, incluyendo:• Seudoquiste pancreáticoEn la PA intersticial• Necrosis encapsuladaEn la PA necrotizante | Densidad homogénea líquidaNo contenido sólidoDensidad heterogéneaPuede aparecer parcialmente encapsuladaDensidad fluida homogénea y encapsulada (bien definida)Contenido heterogéneo con detritos (necrosis parénquima y/o grasa peripancreática) encapsulado |
CPRM: colangiopancreatografía por resonancia magnética; ECO: ecografía; i.v.: intravenoso; PA: pancreatitis aguda; RM: resonancia magnética; TC: tomografía computarizada.
La necrosis es un factor pronóstico determinante en la PA, ya que se asocia a altas tasas de morbilidad (34-95%) y mortalidad (2-39%) y con el desarrollo de complicaciones locales y a distancia2–7,9–11,25–27.
TiempoLa necrosis es un proceso dinámico que tarda días en establecerse. La literatura científica no establece con precisión cuál es el momento óptimo para su identificación17. Sin embargo, debería esperarse entre 3 y 5 días desde el inicio del cuadro clínico para realizar una TC, dado que antes podría existir una captación heterogénea de contraste que dificultaría la distinción entre edema y necrosis3,5,11. Estos casos se clasificarían como pancreatitis aguda indeterminada y debería repetirse la TC en unos días3 (fig. 10).
Pancreatitis aguda indeterminada en una mujer de 69 años. Imagen de TC con contraste intravenoso en plano axial, realizada a los 2 días del inicio de los síntomas (izquierda), en la que se observa un área hipodensa heterogénea en la cabeza pancreática (flecha). El poco tiempo de evolución del cuadro hace difícil distinguir si dicha hipodensidad se debe a edema en el contexto de una pancreatitis edematosa intersticial o si está en relación con necrosis pancreática, por lo que se clasificó como pancreatitis aguda indeterminada. En la tomografía computarizada con contraste realizada 5 semanas después del inicio del cuadro (derecha) se observa una clara necrosis pancreática en la cabeza glandular (flecha), así como múltiples focos de necrosis grasa extrapancreática.
Consideraremos necrosis a aquellas áreas heterogéneas con ausencia de realce (densidad <30 UH en la fase pancreática) que presenten un tamaño mayor de 3cm. Las áreas de menor tamaño se considerarán edema más que necrosis5,16 (fig. 2). Un punto importante es la cuantificación del porcentaje de necrosis del parénquima, dado que determina la gravedad de la PA, aunque el porcentaje con valor pronóstico variaría entre las distintas escalas propuestas25 (tabla 3).
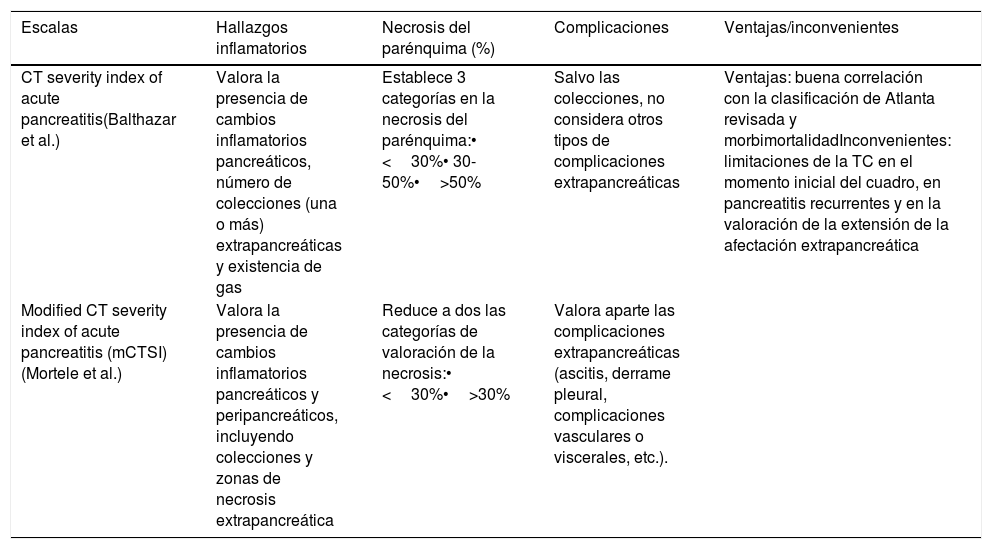
Principales escalas de valoración de la pancretitis aguda mediante tomografía computarizada
| Escalas | Hallazgos inflamatorios | Necrosis del parénquima (%) | Complicaciones | Ventajas/inconvenientes |
|---|---|---|---|---|
| CT severity index of acute pancreatitis(Balthazar et al.) | Valora la presencia de cambios inflamatorios pancreáticos, número de colecciones (una o más) extrapancreáticas y existencia de gas | Establece 3 categorías en la necrosis del parénquima:• <30%• 30-50%•>50% | Salvo las colecciones, no considera otros tipos de complicaciones extrapancreáticas | Ventajas: buena correlación con la clasificación de Atlanta revisada y morbimortalidadInconvenientes: limitaciones de la TC en el momento inicial del cuadro, en pancreatitis recurrentes y en la valoración de la extensión de la afectación extrapancreática |
| Modified CT severity index of acute pancreatitis (mCTSI)(Mortele et al.) | Valora la presencia de cambios inflamatorios pancreáticos y peripancreáticos, incluyendo colecciones y zonas de necrosis extrapancreática | Reduce a dos las categorías de valoración de la necrosis:• <30%•>30% | Valora aparte las complicaciones extrapancreáticas (ascitis, derrame pleural, complicaciones vasculares o viscerales, etc.). |
La localización de la necrosis es un dato importante para el manejo de los pacientes. Esta puede localizarse simultáneamente en el páncreas y en los tejidos peripancreáticos (75% de los casos) o únicamente a nivel pancreático (5%) o peripancreático (25%)2–7,9–11,25–27. Dentro del parénquima, muestra predilección por afectar al cuello y cuerpo pancreáticos dada su peor vascularización.
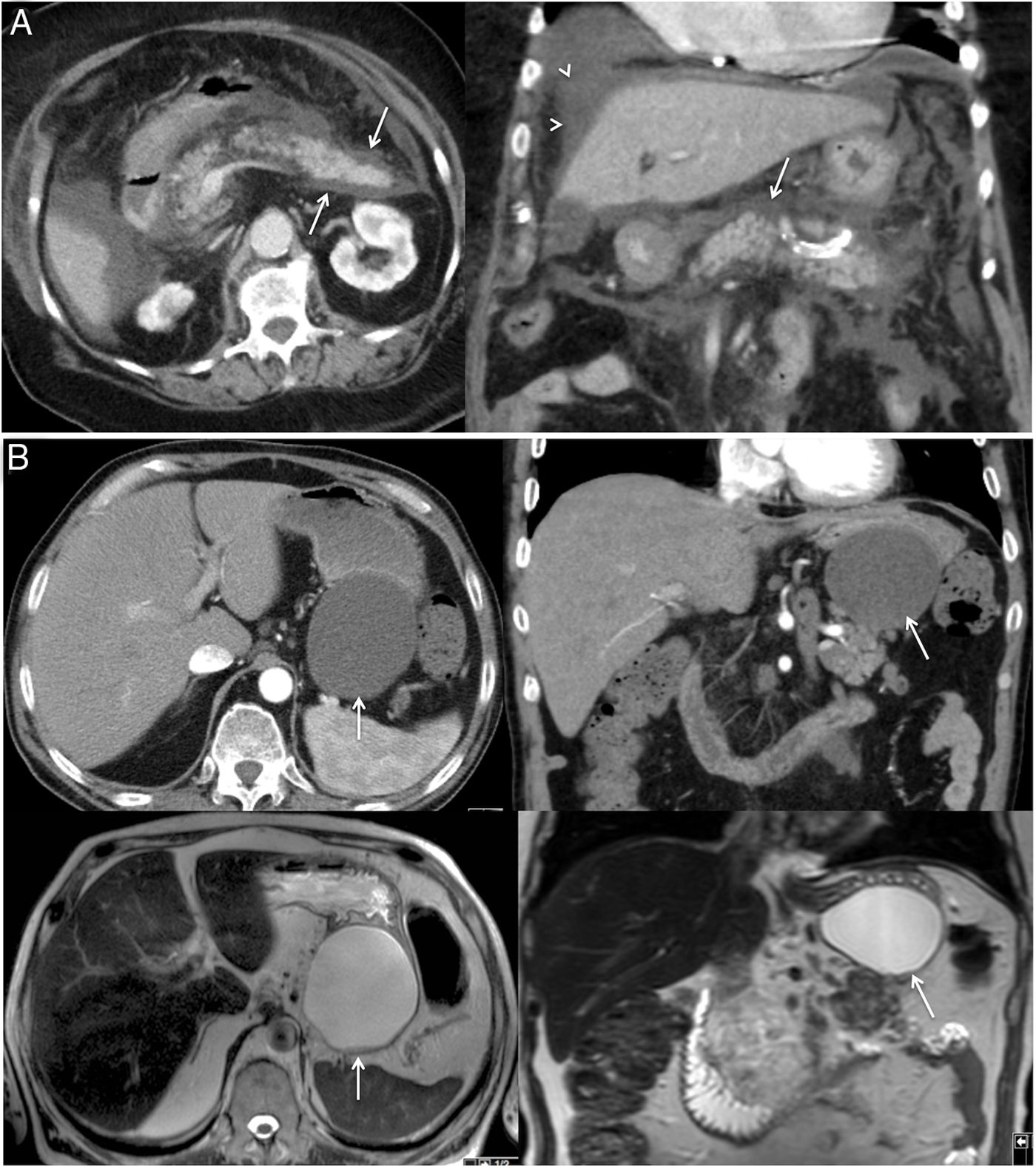
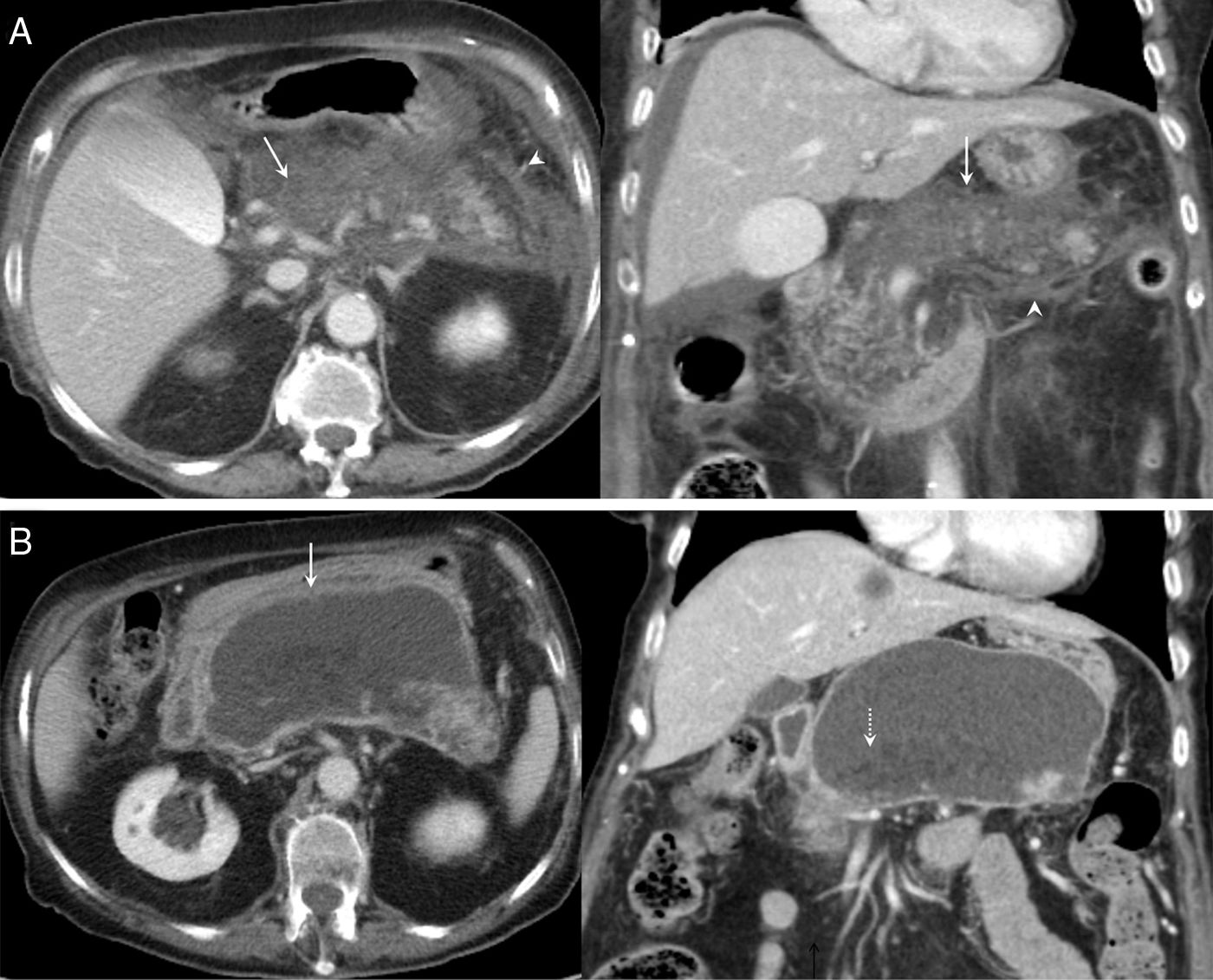
ColeccionesEl tipo de colecciones asociadas a la PA y su tiempo de evolución (mayor o menor de 4 semanas) también definen los subtipos de pancreatitis. En la PA edematosa-intersticial, las colecciones son homogéneas y de baja atenuación en TC, al no presentar restos necróticos2–7,9–11 (fig. 11A) y suelen localizarse a nivel peripancreático (más frecuentemente en el saco menor). En el primer mes, estas colecciones carecen de pared y se delimitan mediante los planos fasciales, denominándose colecciones líquidas peripancreáticas agudas. Generalmente, se resuelven en pocos días y si persisten más de un mes evolucionan a la formación de un seudoquiste (fig. 11B), que presentará una pared definida y con realce26,27.
A) Colección líquida peripancreática aguda. Imágenes de tomografía computarizada (TC) con contraste intravenoso en plano axial y coronal, realizadas a los 5 días del inicio de los síntomas, en las que se observan colecciones líquidas que se adaptan al contorno de la glándula pancreática (flechas blancas) y que no presentan ni contenido sólido en su interior ni paredes claramente definidas, en relación con colecciones líquidas peripancreáticas agudas. Se observa también líquido perihepático sugestivo de ascitis (cabezas de flecha). B) Seudoquiste. Imágenes de TC con contraste intravenoso en plano axial y coronal que muestran una colección adyacente a la cola del páncreas, de paredes bien definidas y contenido líquido homogéneo (flechas). Las imágenes de resonancia magnética potenciadas en T2 en plano axial y coronal confirman los mismos hallazgos: una colección de paredes bien definidas y contenido homogéneo hiperintenso en secuencias T2 (flechas), que descarta la presencia de contenido sólido en su interior.
Por su parte, en la PA necrotizante, las colecciones serán heterogéneas debido a la presencia de detritos sólidos y pueden localizarse a nivel pancreático y extrapancreático (fig. 12A)26,27. Inicialmente, este tipo de colecciones carecerán de pared y se denominarán colecciones necróticas agudas. Pueden resolverse o persistir, desarrollando una pared definida, con realce tras la administración de contraste intravenoso y denominándose entonces necrosis encapsulada (fig. 12B) 2,9–11,26,27.
A) Colección necrótica aguda. Imágenes de tomografía computarizada (TC) con contraste intravenoso en plano axial y coronal, realizadas en una mujer de 80 años a los 3 días del inicio del cuadro, que muestran ausencia de realce en extensas áreas del parénquima pancreático en relación con necrosis pancreática (flechas) así como colecciones líquidas peripancreáticas y pararrenales izquierdas (cabezas de flecha) sugestivas de colecciones necróticas agudas. B) Colección necrótica encapsulada. Imágenes de TC con contraste intravenoso en plano axial y coronal de la misma paciente realizadas 5 semanas después, que muestran la evolución de dichas colecciones a una colección de paredes bien definidas, que afecta a la glándula pancreática y también a los tejidos peripancreáticos (flechas blancas), con contenido sólido en su interior (flecha punteada), sugestivas de colección necrótica encapsulada.
Debe recordarse que tanto la RM como la ecografía son útiles para caracterizar colecciones de difícil valoración mediante TC.
Complicaciones de la pancreatitis agudaLa PA es un cuadro clínico asociado a una importante morbimortalidad y con distintos tipos de complicaciones descritas en la literatura científica.
InfecciónTodas las colecciones asociadas a la PA pueden infectarse, pero es más frecuente que suceda en las necróticas, en el 75% de los casos por bacilos gramnegativos22. La incidencia de infección representa un factor de mal pronóstico: causa el 80% de las muertes en la PA6. El principal signo de infección es la presencia de gas en el interior del tejido necrótico, aunque solo se encuentra en el 12-22% de los casos26,27 (fig. 13). Sin embargo, la ausencia de gas en una colección no permite descartar que esté infectada. Como ya se ha comentado, la difusión es una técnica útil para detectar infección23 (fig. 7).
Aire en una colección necrótica aguda infectada. Varón de 74 años al que se le realiza tomografía computarizada con contraste intravenoso en plano axial y coronal, obtenida 2 semanas tras el inicio del cuadro, que muestra una colección pancreática y peripancreática (flechas) con gas en su interior (cabezas de flecha) que traduce la infección de dicha colección.
La DCP es una complicación frecuente (40%) de las PA necrotizantes. La necrosis pancreática puede englobar el conducto pancreático principal y dañarlo focalmente. Como resultado, un segmento viable del páncreas no puede drenar sus secreciones al tracto gastrointestinal y estas se acumularán a nivel peripancreático9–11,26–28. Deberíamos sospechar su presencia cuando se evidencie una necrosis de más de 2cm en cuello y/o cuerpo pancreáticos, con extensas colecciones adyacentes y con presencia de tejido pancreático viable proximal. Además, una orientación del conducto de 90 grados con respecto a la colección también apoyará el diagnóstico26,28. Aunque la técnica de elección para confirmar la DCP es la colangiopancreatografía retrógrada endoscópica, la CPRM puede ser una alternativa no invasiva con elevada sensibilidad diagnóstica (fig. 14).
Disrupción del conducto pancreático. Colangiopancreatografía por resonancia magnética sin y tras la administración de secretina en varón de 56 años que muestra cómo se rellena una cavidad de aproximadamente 17×7mm, localizada en la transcavidad de los epiplones (flecha), entre la cola del páncreas y la cámara gástrica, hallazgos en relación con pequeña fuga/fístula pancreática a ese nivel.
La erosión de la pared vascular por las enzimas pancreáticas liberadas puede causar complicaciones vasculares2–4,7,9–11.
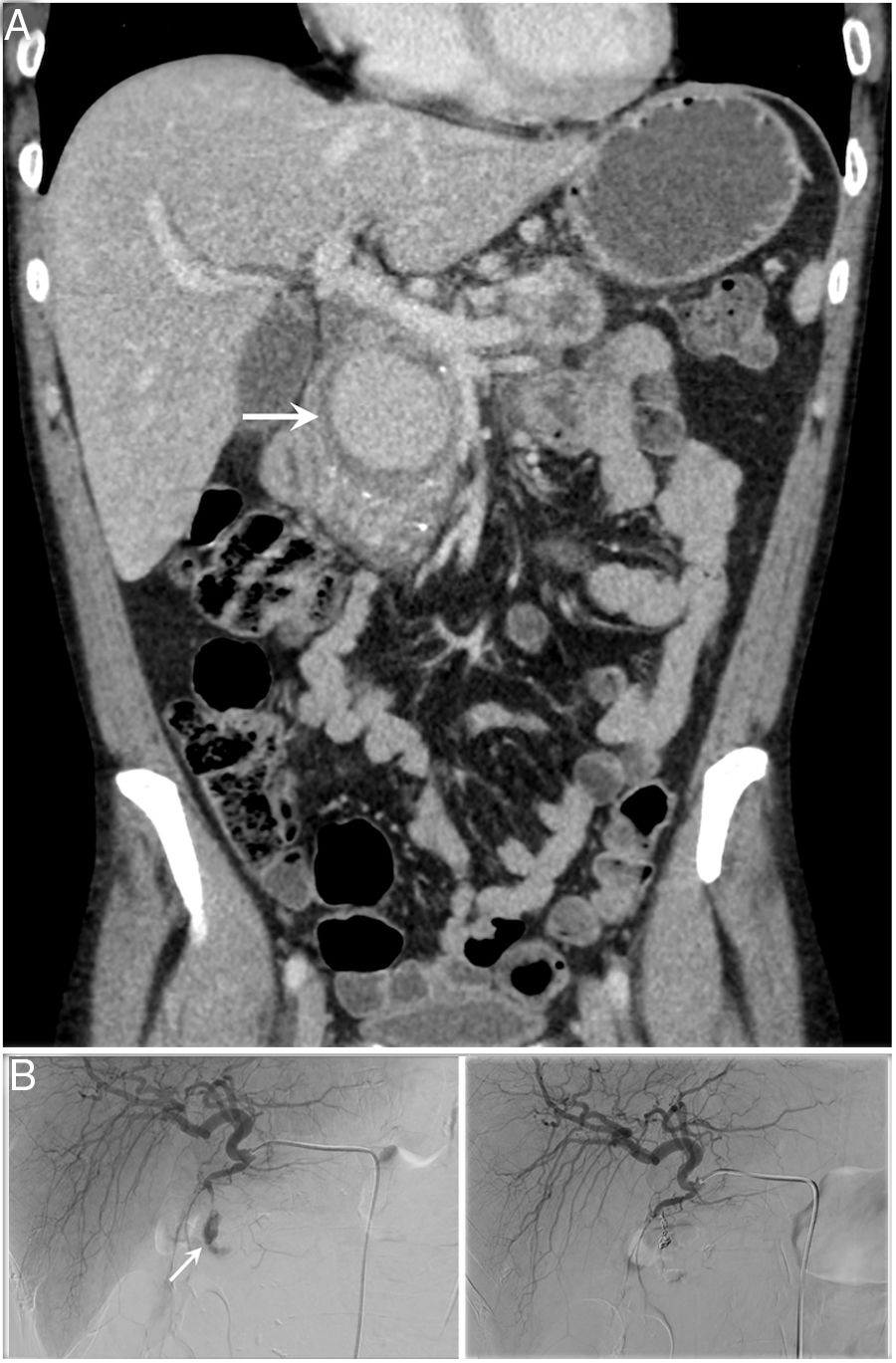
ArterialesLa afectación de la pared de arterias pancreáticas o peripancreáticas puede dar lugar a la formación de seudoaneurismas o al desarrollo de un cuadro hemorrágico grave. Las arterias más frecuentemente afectadas son la esplénica (40%), la gastroduodenal (30%) y la pancreaticoduodenal (20%)7,9–11 (fig. 15A). Debemos recordar que las técnicas de radiología intervencionista tienen un papel fundamental en el manejo de dichas complicaciones arteriales (fig. 15B).
Complicación arterial. A) Varón de 44 años que acude por anemia severa sintomática con dudosa exteriorización (2 episodios de melena). La tomografía computarizada abdominal muestra un saco aneurismático dependiente de la arteria gastroduodenal (flecha). B) Angiografía supraselectiva de la arteria hepática que muestra el sangrado de la arteria gastroduodenal pre- (izquierda) y postratamiento (derecha) mediante embolización.
La trombosis de la vena esplénica es la complicación vascular más común (10-40%) en la PA y es el resultado tanto de la lesión inflamatoria de la íntima como de la compresión vascular por las colecciones7,9–11. Esta trombosis puede derivar en infartos esplénicos e hipertensión portal. Aunque menos frecuentes, también se han descrito en la PA trombosis portal o de la vena mesentérica superior.
Otras complicacionesLa acción proteolítica de las enzimas puede causar otras complicaciones menos frecuentes, como fístulas externas o internas o afectar órganos sólidos cercanos como el bazo o el riñón.
Avances en la valoración por imagen de la pancreatitis agudaDiferentes elementos podrían potenciar el papel de la imagen en la valoración de la PA. De un lado, vista la variabilidad entre radiólogos en la clasificación de la PA y en la terminología usada, se ha sugerido la importancia de realizar informes estructurados que los homogenicen y faciliten el trabajo multidisciplinar29. Además, recientes mejoras en la tecnología de adquisición y procesado de imágenes (incluyendo aceleración de la adquisición en RM o técnicas de reconstrucción 3D) permitirían una mejor valoración de los pacientes13,22,30. Finalmente, estudios preliminares han evidenciado la utilidad de la inteligencia artificial, pudiendo los “radiomics” predecir complicaciones o recurrencias de la PA y posibilitando la valoración automática de hallazgos de imagen asociados a PA en función del “machine learnIng”13.
En conclusión, la imagen forma parte fundamental del algoritmo de diagnóstico y manejo de la PA y, por ello, el radiólogo debería estar familiarizado con el uso de las distintas técnicas de imagen y con sus manifestaciones radiológicas y usar adecuadamente la nomenclatura específica de esta entidad.
Autoría- 1.
Responsable de la integridad del estudio: SBG, RGF.
- 2.
Concepción del estudio: SBG, MCA.
- 3.
Diseño del estudio: SBG, JCM, RGF.
- 4.
Obtención de los datos: SBG, MCA, RGF, SJO.
- 5.
Análisis e interpretación de los datos: SBG, RGF, MCA, JCM, SJO.
- 6.
Tratamiento estadístico: N/A.
- 7.
Búsqueda bibliográfica: SBG, JCM, SJO.
- 8.
Redacción del trabajo: SBG, RGF, JCM.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: SBG,RGF. Aprobación de la versión final: SBG,RGF, MCA, JCM, SJO.
Los autores declaran no tener ningún conflicto de intereses.