De la fusión visual a la tecnología PET-TC
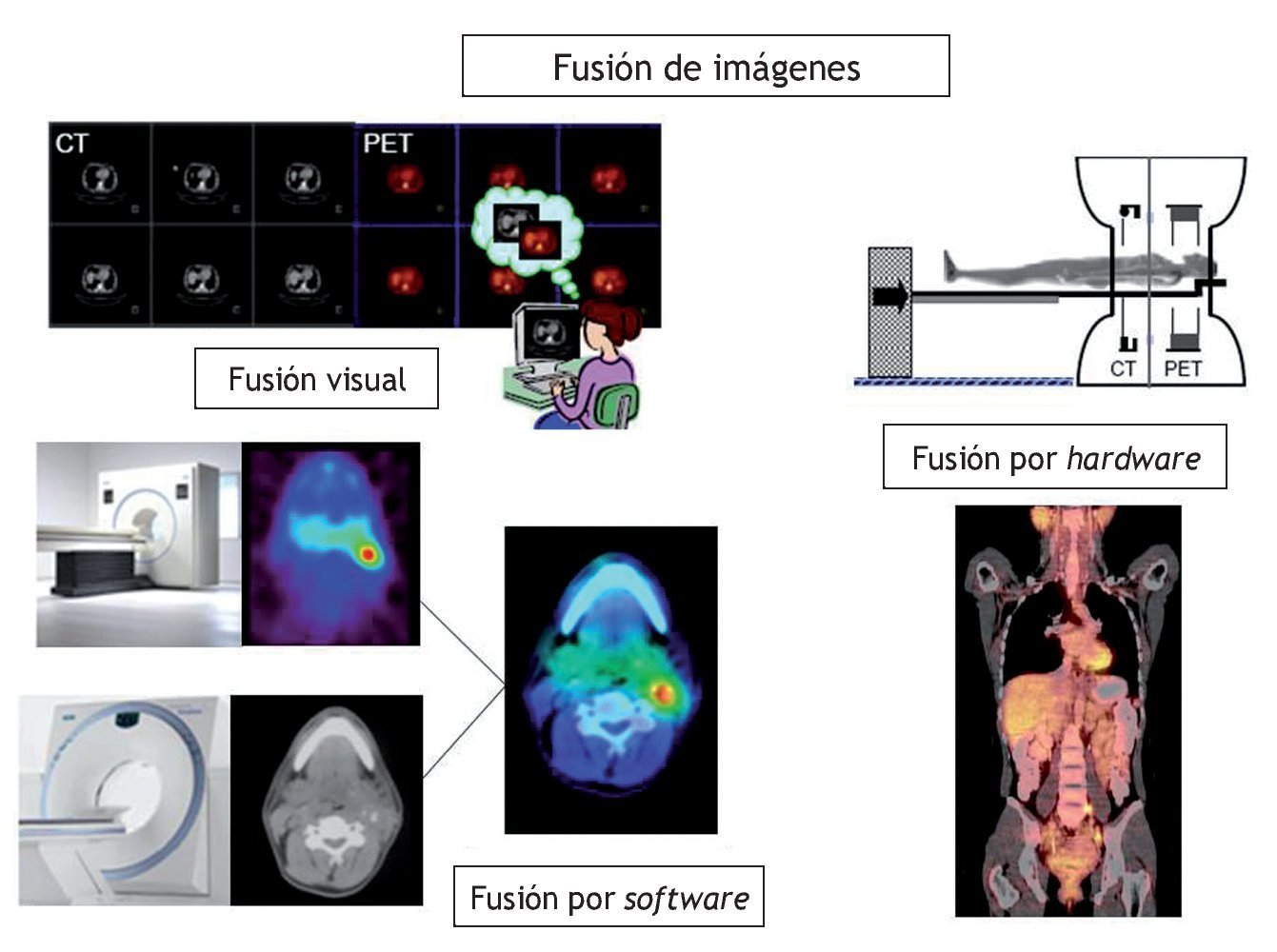
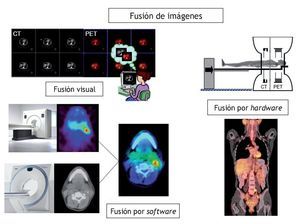
Durante décadas la TC ha sido la prueba de elección en el paciente oncológico, proporcionando información morfológica de las alteraciones que conlleva la enfermedad tumoral. Sin embargo, la aparición de la tomografía por emisión de positrones (PET) en los años noventa supuso un cambio fundamental en el manejo de estos pacientes al aportar una valiosísima información acerca del metabolismo de la enfermedad. A pesar de ello, uno de los principales inconvenientes de la PET ha sido su falta de resolución anatómica, que impedía en muchas ocasiones localizar adecuadamente las lesiones que detectaba de forma precoz en comparación con el resto de pruebas de imagen. Han sido varios los intentos de paliar este defecto con el fin de aumentar el rendimiento diagnóstico de la prueba PET (fig. 1). El primero de ellos fue
Figura 1 Evolución de la ima gen de fusión anatomometabólica.
la llamada "fusión visual", que permitía valorar de forma separada y por 2 expertos los datos de ambas exploraciones, lo que conllevaba muchas inexactitudes diagnósticas. Más recientemente se desarrollaron potentes sistemas de "fusión por software" que permitían integrar en una sola estación de trabajo la información aportada de forma independiente por un equipo de TC y otro de PET. A pesar de la mejora en la correlación de las imágenes, el hecho de que los estudios fuesen realizados al mismo paciente en diferentes tiempos y en diferentes equipos conllevaba también importantes defectos metodológicos que impedían obtener una imagen de fusión anatomometabólica de calidad diagnóstica. El paso definitivo para solucionar este problema lo dio el equipo de investigadores dirigidos por el Prof. Townsend (Universidad de Pittsburgh) el cual consiguió en 1998 diseñar un único equipo que integraba una TC y en cerca del 30-40% de los casos1. Esta irrupción de los equipos integrados se ha extendido a la medicina nuclear convencional con la aparición de los modernos sistemas SPECT-TC y tiene su siguiente desafío en los equipos PET-RM y SPECT-RM que en pocos años se implantarán en los departamentos de diagnóstico por imagen2.
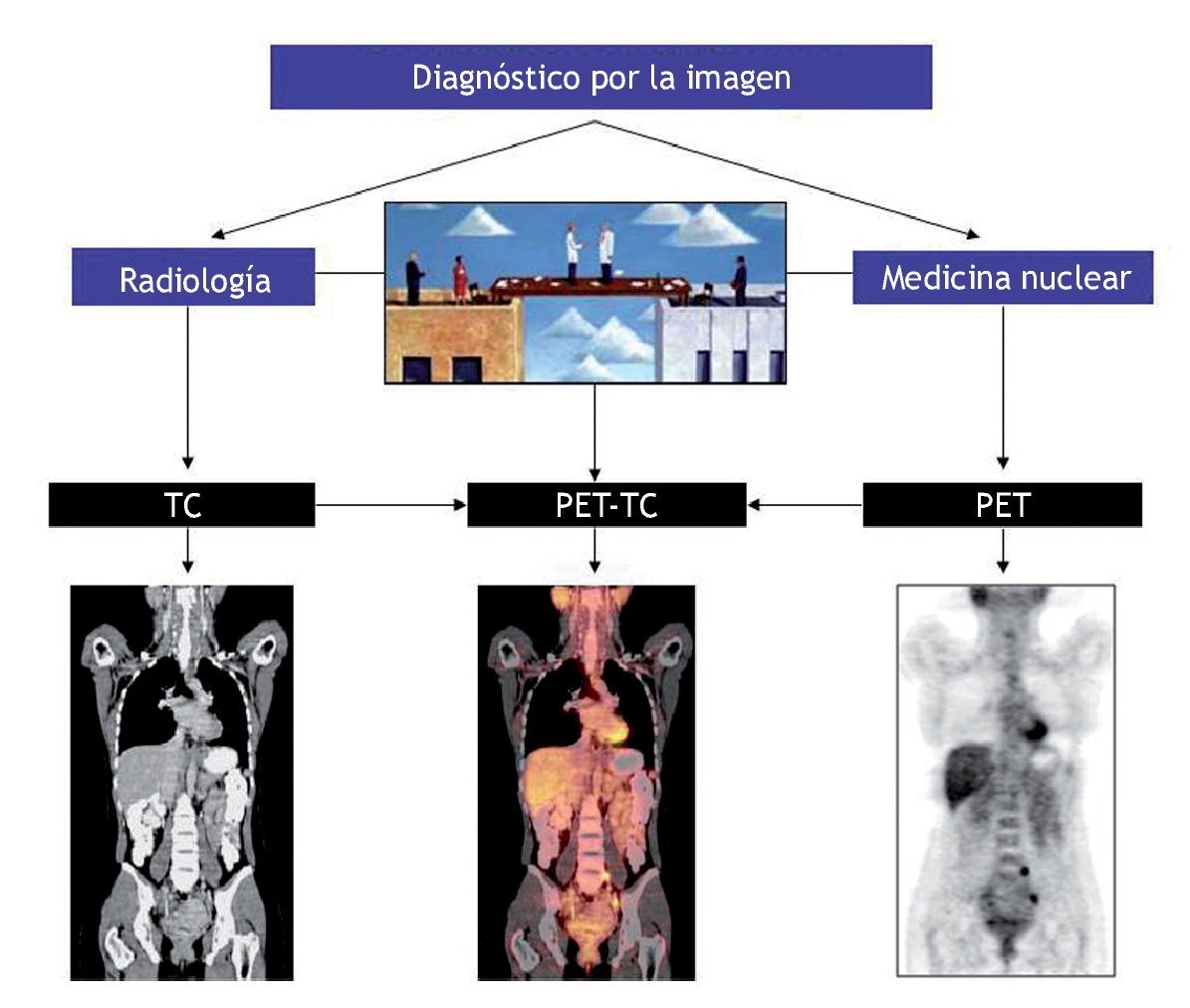
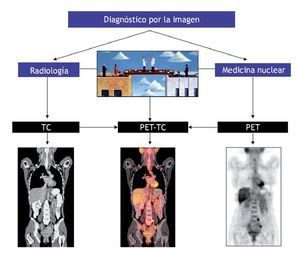
A esta revolución tecnológica que ha supuesto la PET-TC se ha unido, desde su implantación en el ámbito hospitalario en 2001, la necesidad de integración de los especialistas de medicina nuclear y radiodiagnóstico en la interpretación de los estudios obtenidos (fig. 3). Estos equipos utilizan en su diseño lo último en tecnología PET y TC, lo que permite obtener estudios de similar calidad diagnóstica a la que se obtendría por separado, especialmente en el caso de la TC. Hay equipos en el momento actual que incorporan una TC de 64 detectores junto a sistemas PET que proporcionan una resolución de aproximadamente 2 mm. Por tanto, el correcto uso de los equipos PET-TC hace innecesaria la realización de otros estudios de TC, lo que conlleva la consiguiente optimización desde el punto de vista de protección radiológica y del manejo clínico de los pacientes. Frente a la disyuntiva de hace unos años entre usar equipos PET o PET-TC, en el momento actual se asiste a la controversia entre el modo de utilizar los equipos PET-TC: si sólo en su vertiente PET o de forma completa sacando el máximo rendimiento de las prestaciones diagnósticas que ofrecen la PET y la TC. La evolución tecnológica de las técnicas híbridas hará que en poco tiempo esta última controversia quede diluida y el dilema se centre entre una PET de última generación (fig. 2). Nacía así la tecnología híbrida que permitía obtener en una sola exploración imágenes de fusión anatómicas (TC) y metabólicas (PET) del mismo paciente con una gran precisión. Desde entonces, la implantación de estos equipos híbridos en el ámbito hospitalario ha sido tan importante que se han convertido en la exploración diagnóstica de referencia en oncología, cambiando el manejo del paciente utilizar equipos PET-TC o PET-RM, dependiendo del tipo de patología que se tenga que estudiar; será impensable que surja la controversia entre usar la RM sólo para localizar las lesiones PET como ocurre actualmente con la PET-TC. Por ello es fundamental que la tecnología híbrida se integre en departamentos de diagnóstico por imagen que permitan sacar el máximo rendimiento posible a ambas exploraciones, siendo necesario que la información final que se proporcione al especialista solicitante sea única y conjunta de la aportada por la imagen anatómica y metabólica. Un valor añadido de este trabajo conjunto de los especialistas de imagen es la posibilidad de obtener estudios de fusión PET-RM tan importantes en neurooncología o como serán en poco tiempo en patología osteoarticular.
Figura 2 Equipos de PET-TC comerciales disponibles en la actualidad.
Figura 3 Integración de los especialistas por imagen en la valoración de los estudios obtenidos por los equipos híbridos.
Los equipos PET-TC fueron diseñados desde el principio para poderse usar en la planificación de los tratamientos de radioterapia3. La posibilidad de obtener estudios de sincronización respiratoria (4D), el uso de los mismos sistemas de fijación para simular los tratamientos radioterápicos o la mayor anchura de las carcasas respecto de los equipos PET tradicionales, ha permitido el uso de los equipos PET-TC en los protocolos de oncología radioterápica cambiando el manejo del paciente en cerca del 50% de los casos en algunos tumores, como los de pulmón o cabeza y cuello4. Todo ello hace necesario el trabajo conjunto multidisciplinar, no sólo de los especialistas de diagnóstico por imagen con los radioterapeutas, sino también con los profesionales sanitarios responsables de la radiofísica hospitalaria.
Por tanto, se está ante una tecnología que precisa del trabajo conjunto de diversos especialistas formando equipos multidisciplinares para obtener el máximo rendimiento de una prueba que puede modificar en un alto porcentaje de casos el manejo y supervivencia del paciente con cáncer.
En este artículo se abordan algunas situaciones clínicas que reflejan la importancia de la estrecha colaboración de los especialistas de medicina nuclear y radiodiagnóstico en la correcta interpretación de los estudios PET-TC en el paciente oncológico. En concreto, se expondrán aquellas en las cuales la información proporcionada por la TC modifica sustancialmente el diagnóstico que de forma individualizada se hubiera hecho con la imagen metabólica PET por las limitaciones intrínsecas que esta exploración conlleva. No se abordarán las limitaciones de la TC o las inherentes a la adquisición conjunta de ambas exploraciones, tan importantes o más que las que únicamente se deben a la PET. Sin embargo, como médico nuclear, he creído importante reflejar los aspectos de mejora que supone la colaboración diaria con el radiólogo en la interpretación de los estudios PET-TC. También se expondrán las ventajas que desde el punto de vista clínico ha supuesto la utilización conjunta de la PET-TC frente a la PET en diversos tumores. En el artículo se hará referencia al único trazador PET aprobado por el Ministerio de Sanidad5, la fluorodesoxiglucosa marcada con 18F (18F-FDG), y no se abordará la problemática de otros trazadores como la 11C-colina, la 11C-metionina o la 18F-timidina por mencionar algunos de los que en pocos años serán utilizados de forma rutinaria en el ámbito hospitalario.
Limitaciones de la imagen metabólica en oncología: captaciones fisiológicas
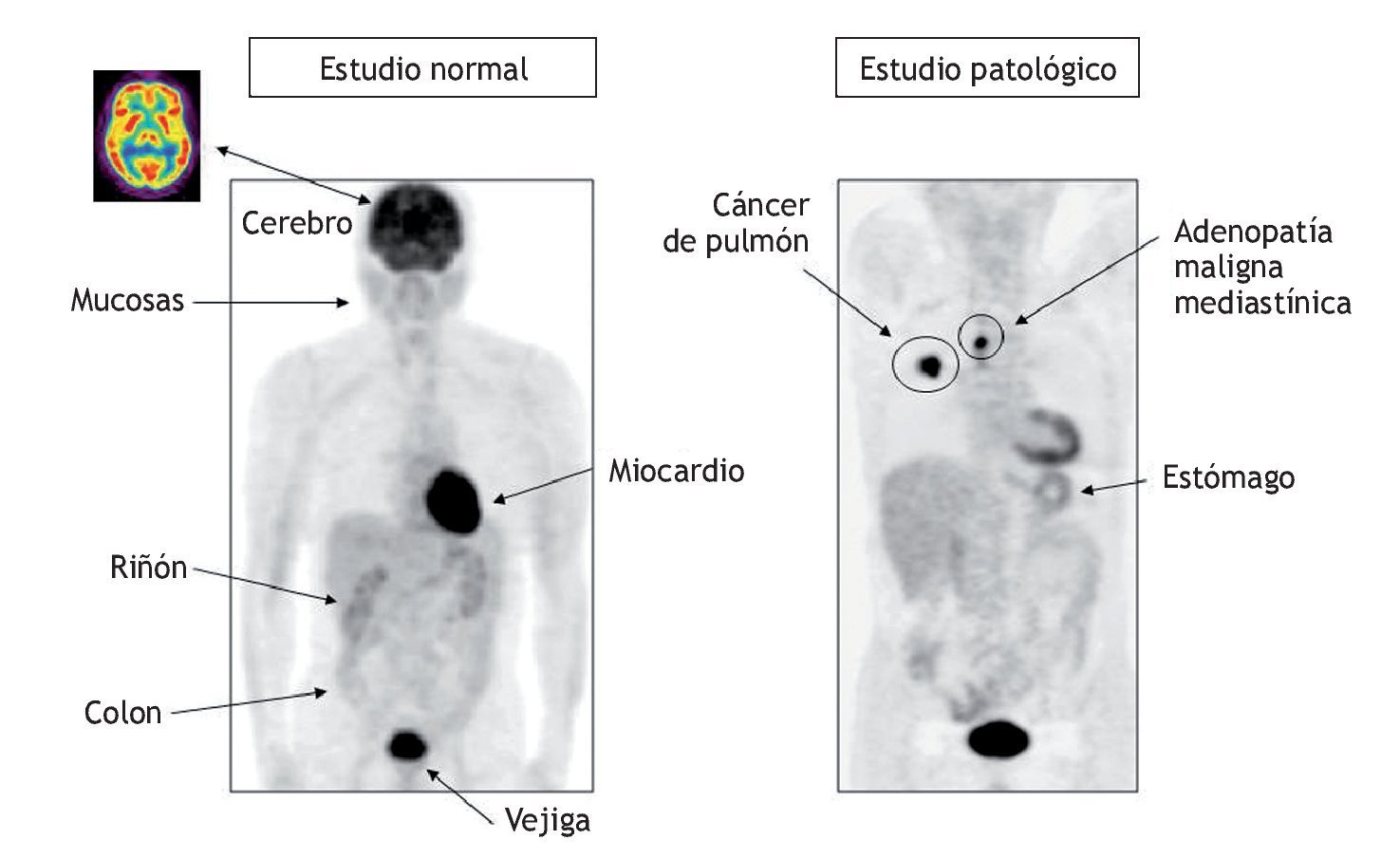
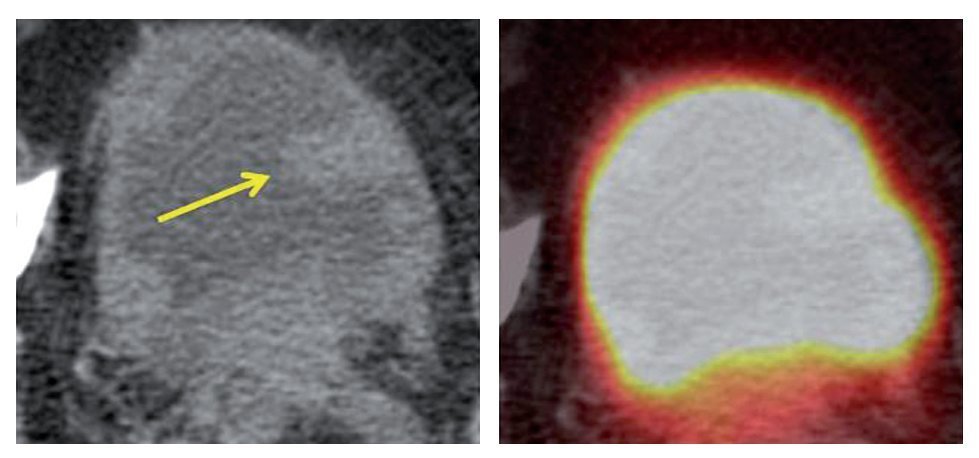
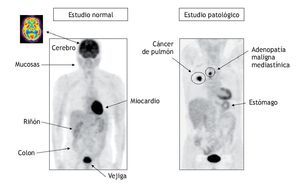
La FDG, como análogo de la glucosa, nos proporciona información acerca del metabolismo glucídico, así como sobre la distribución de la glucosa en el cuerpo (fig. 4). Por tanto, algunas de las captaciones fisiológicas de la FDG se localizan en el córtex cerebral, el miocardio, la musculatura, las mucosas y el sistema gastrointestinal. Al no ser propiamente glucosa, la FDG además será eliminada por el sistema excretor. Todo ello conlleva que la posible presencia de patología tumoral en todas estas localizaciones puede quedar enmascarada por la captación normal de FDG. Esta limitación puede compensarse por la información que nos proporciona la TC. Como ejemplo de lo descrito, en la figura 5 se observa el caso de un paciente en el cual la eliminación fisiológica de la FDG impide detectar la patología tumoral en la vejiga, observada únicamente gracias a la TC.
Figura 4 Distribución normal de la FDG en el cuerpo. Comparación con lesiones malignas.
Figura 5 Detección de patología tumoral vesical gracias a la TC. En la imagen de PET-FDG no se ven lesiones, al ser una vía normal de eliminación del trazador metabólico.
Limitaciones de la imagen metabólica en oncología: patología inflamatoria/ infecciosa
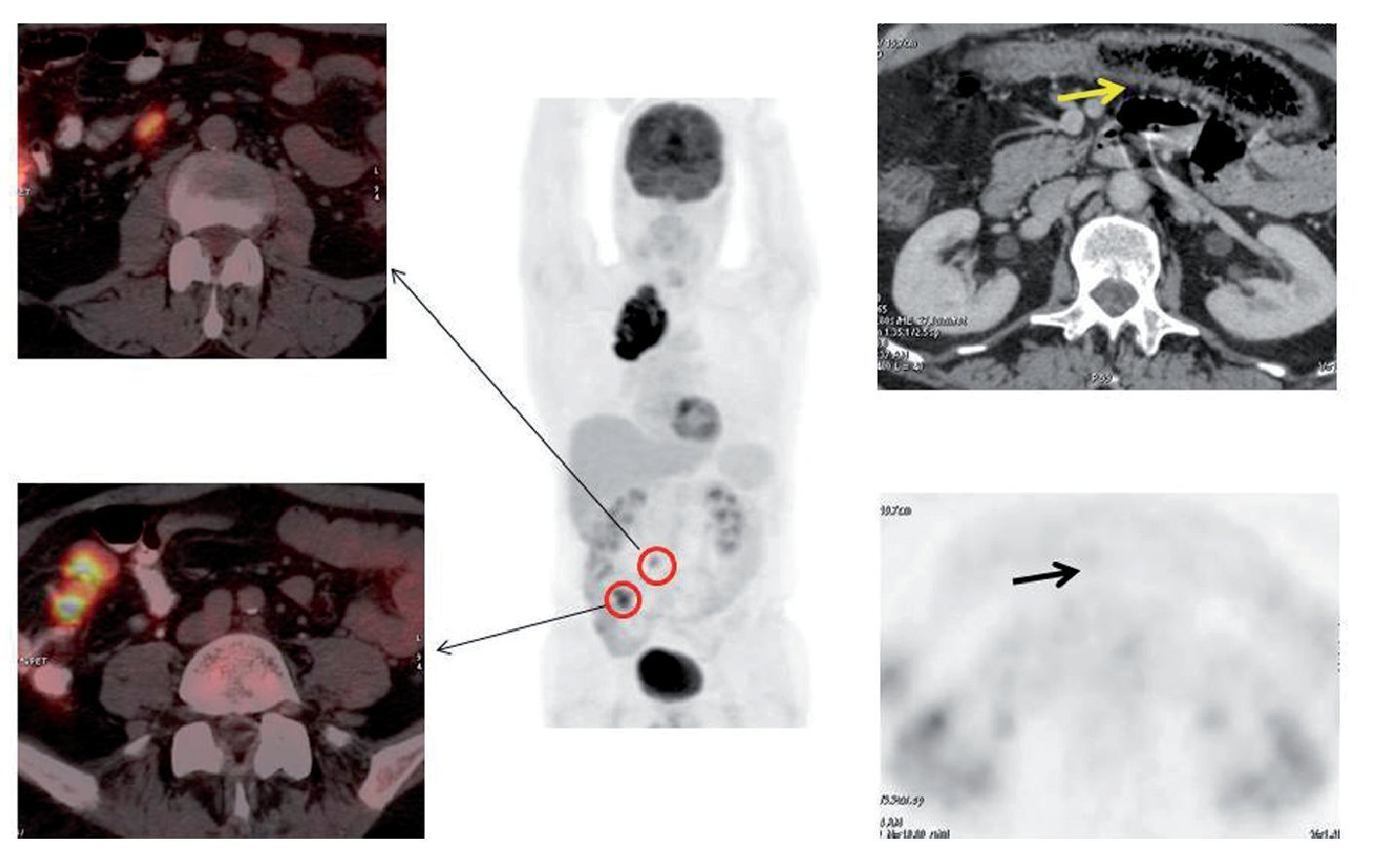
La captación de FDG refleja la actividad celular. Ésta es mucho más intensa y evidente en el caso de los procesos malignos. Sin embargo, otras entidades, como la patología inflamatoria/infecciosa, provocan un incremento del metabolismo glucídico celular, especialmente a expensas de los macrófagos. Esta captación de la FDG es con frecuencia una fuente de resultados falsos positivos en las exploraciones PET. Aunque una adecuada metodología y la información clínica del caso pueden evitar esta circunstancia, en muchas ocasiones sólo la información aportada por la imagen de TC permite obtener un adecuado diagnóstico (fig. 6).
Figura 6 Estudio de estadificación de un cáncer de pulmón en el lóbulo superior derecho. Presencia de adenopatías mesentéricas captantes de FDG. Destaca en la TC un engrosamiento de la pared del colon transverso, con pequeñas imágenes que podrían corresponder a úlceras submucosas (todo ello sin aumento de captación de FDG), y que sugiere enfermedad inflamatoria intestinal. Se descarta la posibilidad de M1 gracias a la información aportada por la TC que orienta hacia el origen benigno de las adenopatías.
Limitaciones de la imagen metabólica en oncología: lesiones de pequeño tamaño
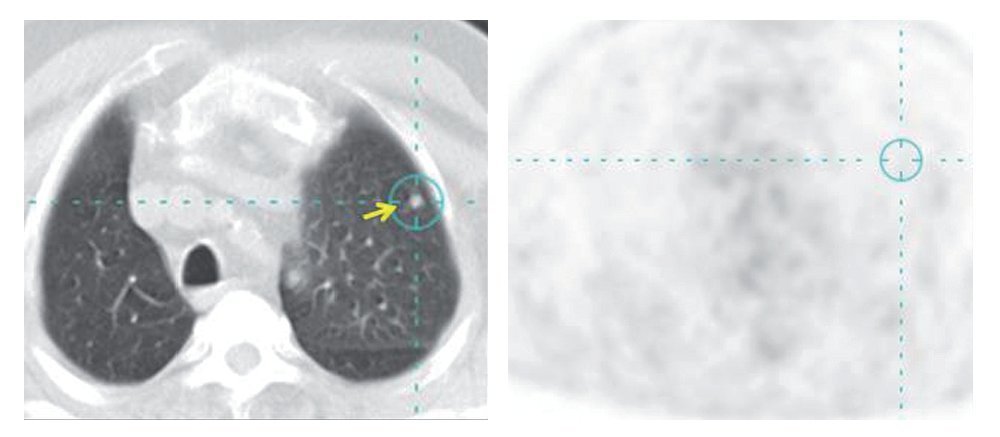
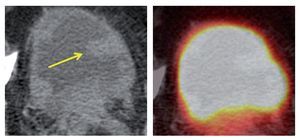
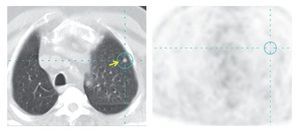
A pesar de la progresión tecnológica de la PET en los últimos años, una de las limitaciones más importantes continúa siendo la resolución de los equipos y su capacidad para detectar lesiones de pequeño tamaño. Lejos quedan los equipos que eran incapaces de detectar lesiones por debajo de 1 cm, siendo ésta una barrera superada por la casi totalidad de los sistemas implantados en el ámbito hospitalario. En el momento actual se puede considerar que el límite de resolución de la imagen PET integrada en los equipos híbridos oscila entre 4 y 6 mm, habiéndose obtenido recientemente dispositivos que permiten detectar lesiones de hasta 2 mm de tamaño6. La investigación sobre nuevos detectores permitirá, en breve, conseguir que el límite de resolución se aproxime a los obtenidos por la RM7. Esta limitación técnica de la imagen PET se manifiesta con mayor intensidad en la patología torácica, siendo en muchas ocasiones la imagen de TC la única que permite detectar pequeñas lesiones metastásicas pulmonares (fig. 7). Situaciones similares pueden observarse en diseminaciones miliares de tumores, tanto en el abdomen como en el tórax, que debido a su pequeño tamaño y metabolismo pasan desapercibidas para la imagen de PET con FDG.
Figura 7 Metástasis pulmonar izquierda de pequeño tamaño que no presenta captación de FDG.
Limitaciones de la imagen metabólica en oncología: grado de diferenciación tumoral
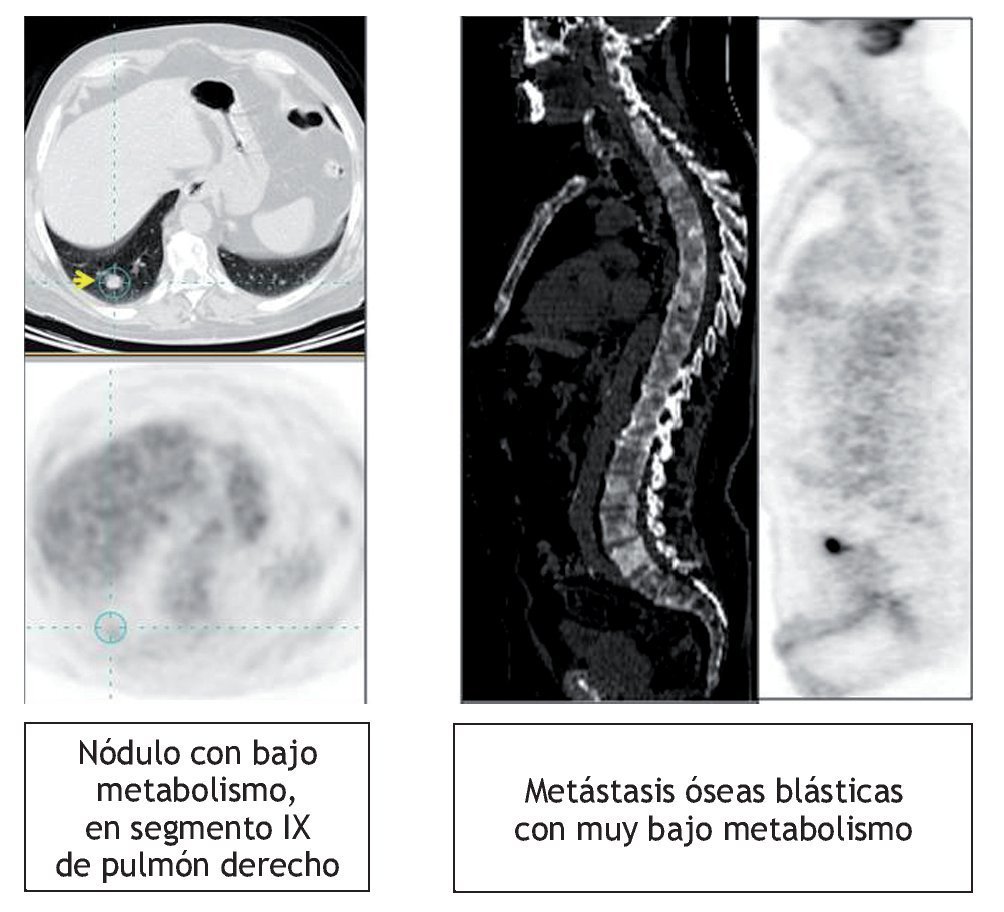
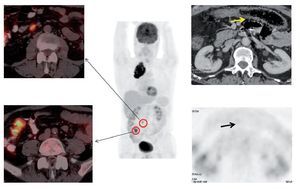
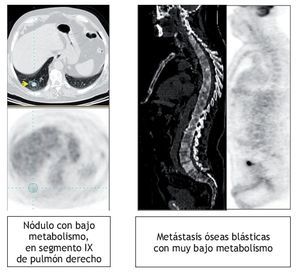
La FDG permite obtener información de las lesiones tumorales de moderado/alto grado de actividad metabólica8. Cuanto más diferenciado o cuanto más lento es el ritmo de crecimiento celular en un tumor, menor actividad glucídica presenta y, por ende, mayor es la posibilidad de falsos negativos en la imagen de PET. El rendimiento diagnóstico de la PET-FDG suele ser bajo en patologías como el cáncer de próstata, los sarcomas de bajo grado, los tumores broncoalveolares, algunos adenocarcinomas bien diferenciados, los tumores neuroendocrinos o algunas estirpes celulares de bajo grado en linfomas no hodgkinianos. Aun cuando hay otros trazadores que permiten detectar el bajo grado histológico9, como la 11C-colina, la 11C-metionina, la 18F-timidina, la 18F-DOPA o la 68Ga-DOTA-NOC, por poner sólo algunos ejemplos, éstos no están disponibles en la mayoría de los centros con tecnología PET-TC. Estas limitaciones pueden ser compensadas en algunas situaciones clínicas por la información que proporciona la TC, como ocurre con frecuencia en el cáncer de próstata o en la detección de metástasis óseas de características blásticas (fig. 8).
Figura 8 Metástasis pulmonar y óseas sin captación significativa de FDG en un paciente con cáncer de próstata.
Ventajas del uso de los protocolos radiológicos en las exploraciones PET-TC
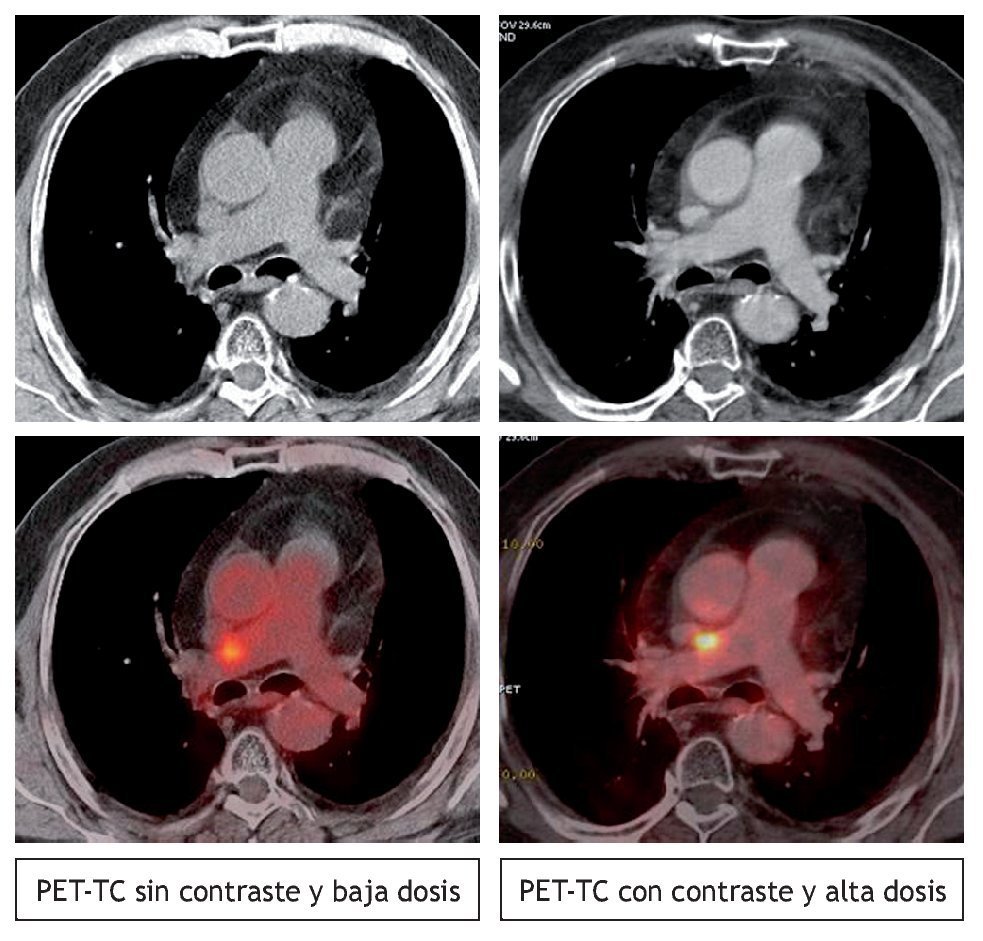
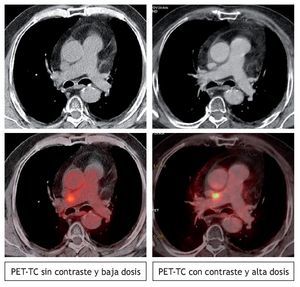
Uno de los puntos más controvertidos respecto al manejo de los equipos híbridos se relaciona con la utilización de los mismos protocolos de TC que se aplican en la práctica clínica diaria. Muchos centros, especialmente en nuestro país, han optado por el uso de la TC de baja dosis y sin la administración de contraste por vía intravenosa, y utilizan la imagen de TC principalmente para la localización anatómica de las lesiones captantes de FDG. El argumento esgrimido para adoptar esta sistemática de trabajo es el hecho real que muchos de los pacientes remitidos a la PET-TC han sido sometidos a un estudio de TC reciente. La realización de nuevo de un estudio de TC "diagnóstico" conllevaría la duplicidad de exploraciones y un problema desde el punto de vista de protección radiológica, especialmente en el caso de la población pediátrica. A pesar de esta realidad, la tendencia en la mayoría de los países es integrar la exploración PET-TC dentro del algoritmo diagnóstico habitual, evitando la redundancia de exploraciones y optimizando el rendimiento clínico de las diversas pruebas de imagen. Sólo cuando hay un departamento de diagnóstico por imagen que coordina las diferentes pruebas que se realizan, es posible evitar la duplicidad de exploraciones y que la única TC "diagnóstica" a la que sea sometido un paciente oncológico sea la del equipo híbrido. La realización de estudios PET-TC de alta dosis administrando contrastes por vía oral e intravenosa10 permitirá un correcto diagnóstico de la enfermedad en muchas ocasiones, como ocurre, por ejemplo, cuando se precisa aplicar tratamientos de radioterapia (fig. 9). Otro de los aspectos que hay que considerar desde el punto de vista metodológico es el uso de protocolos específicos de adquisición del estudio torácico que permitirán una mayor fiabilidad en la delimitación de lesiones en la PET al evitar los artefactos por movimientos respiratorios, en especial en lesiones próximas al diafragma11.
Figura 9 Localización precisa de una adenopatía medias tínica previa al tratamiento de radiocirugía, gracias a la utilización de contraste intravenoso y TC de alta dosis. (Baja dosis: 8 mm de espesor de corte. Alta dosis: 3,5 mm de espesor de corte)
Importancia de la PET-TC en el manejo clínico del paciente oncológico
Aunque la tecnología PET-TC se implantó en el ámbito hospitalario en 2001, las primeras publicaciones con resultados clínicos de la prueba no aparecieron hasta 2004. A pesar de este corto intervalo de experiencia clínica con la técnica híbrida, han sido numerosos los grupos que han publicado la gran rentabilidad de la exploración en el paciente oncológico. Bar-Shalom et al12 encontraron que la imagen de PET-TC en diversos tumores sólidos mejoró la interpretación de los hallazgos en la PET en cerca del 49% de los casos, cambiando el manejo clínico en alrededor del 14%. Varios estudios han demostrado el valor de la PET-TC en el cáncer de pulmón no microcítico, tanto en la estadificación como en la reestadificación y en la detección de recidivas respecto de las detectadas únicamente por la PET. El rendimiento global de la prueba oscila entre el 84 y el 93%, mejorando la fiabilidad de los hallazgos respecto de la PET entre un 22 y un 30%13-15. En el cáncer colorrectal la PET-TC muestra una eficacia global del 89-97 frente al 74-85% de la PET, mejorando la fiabilidad de la detección de los hallazgos en un 30-50% de los casos16-18. Freudenberg et al19 compararon el valor de diversas pruebas de imagen en 27 pacientes diagnosticados de linfoma. Frente al 84-95% de la PET por separado, la PET-TC proporcionó un rendimiento diagnóstico global del 99% a expensas, fundamentalmente, de un incremento en la fiabilidad de las lesiones detectadas. Gutzeit et al20 en el caso de los tumores de origen desconocido muestran como la PET-TC frente a la PET mejora la sensibilidad (el 28 frente al 35%) y el valor predictivo positivo (el 65 frente al 83%). Una reciente publicación21 de los resultados del National Oncologic PET Registry mostró que en el caso de los tumores de próstata, ovario y páncreas, la PET-TC modificó el manejo terapéutico de los pacientes incluidos en el estudio en el 36, 5% de los casos.
Discusión
La PET-TC es la prueba de imagen diagnóstica de elección para un gran número de procesos neoplásicos, como el cáncer de pulmón, linfomas, cáncer colorrectal, tumores de cabeza y cuello, melanomas y cáncer de mama, entre otros22. Su introducción en el algoritmo diagnóstico ha conllevado en muchos tumores una mejora en la supervivencia al facilitar la aplicación de forma precoz y adecuada de las modernas dianas terapéuticas disponibles en la actualidad. Ha permitido reducir en un porcentaje importante de casos las secuelas postratamiento mejorando la calidad de vida de los pacientes, en especial tras los diversos tratamientos radioterápicos. Estamos ante lo que los expertos denominan "oncología guiada por PET-TC". Pero todas estas expectativas dependen de cómo se use e integre la prueba en el ámbito hospitalario. El espectacular desarrollo tecnológico vivido en los últimos años ha permitido que en el momento actual se dispongan de equipos PET-TC que aúnan lo mejor del equipamiento de la PET y de la TC. Sin embargo, y a pesar del esfuerzo desarrollado, la introducción de la prueba en el ámbito asistencial no ha logrado alcanzar el nivel de colaboración necesaria entre los especialistas de medicina nuclear y radiodiagnóstico que permita obtener el máximo rendimiento a esta potente herramienta diagnóstica. El clásico distanciamiento de ambas especialidades ha conllevado con frecuencia renunciar a las grandes posibilidades diagnósticas del componente TC. Realizar una exploración PET-TC basándose principalmente en la información proporcionada por la imagen metabólica, obviando los datos morfológicos por no aplicar protocolos diagnósticos como el uso de contrastes (intravenosos y orales) o la utilización de dosis adecuadas de voltaje en la obtención de las imágenes TC, significa utilizar la técnica de forma incompleta. No se trata de aportar datos morfológicos básicos (como la existencia de un aneurisma o la presencia de litiasis renal), sino de evitar la realización de una nueva exploración de TC tras la prueba de PET-TC. Esto es fundamental en los tumores como los linfomas, en los que es necesario utilizar la PET-TC como herramienta que permita valorar la eficacia de los tratamientos administrados, especialmente en la población pediátrica. El informe final remitido al especialista debe contener toda la información que pueda obtenerse de ambas pruebas por separado y tras el análisis conjunto de éstas. Los especialistas de medicina nuclear debemos acostumbrarnos a informar como patológicos, desde el punto de vista oncológico, estudios sin lesiones captantes de FDG pero con alteraciones en las imágenes anatómicas (p. ej., metástasis pulmonares de un cáncer de próstata sin captación de FDG). Cuanto más completa sea la información que acerca de la enfermedad se le transmita al médico solicitante, mayor será la confianza que tendrá en la técnica y mayor el beneficio que en términos de supervivencia y calidad de vida se le proporcionará al paciente.
La tecnología híbrida se ha extendido también al mundo de la medicina nuclear convencional con la aparición de los sistemas SPECT-TC. En pocos años seremos también testigos de una nueva revolución en la imagen con los modernos equipos PET-RM y SPECT-RM que en el momento actual están en plena fase de desarrollo. Todo ello hará necesaria la creación de la figura del "especialista en diagnóstico por imagen" que podrá evaluar de forma individual cualquier técnica diagnóstica, tanto metabólica como estructural. En este sentido, las sociedades europeas de medicina nuclear y radiología han empezado a colaborar estrechamente en la elaboración de un documento único23 que permita establecer las bases para la futura formación de estos especialistas. Mientras ello llega, es necesaria la máxima colaboración entre los especialistas de medicina nuclear y radiodiagnóstico a la hora del manejo de los modernos y sofisticados equipos PET-TC. La creación de los departamentos de diagnóstico por imagen es la plataforma ideal para realizar esta colaboración, tan necesaria para el correcto manejo del paciente oncológico.
* Autor para correspondencia.
Correo electrónico:amaldonado@ruberinternacional.es (A. Maldonado).
Recibido el 18 de julio de 2008;
aceptado el 21 de octubre de 2008