El cáncer de cérvix es el tercer cáncer ginecológico más frecuente. El tratamiento depende de la estadificación del tumor en el momento del diagnóstico, siendo la combinación de quimioterapia y radioterapia el tratamiento de elección para cánceres localmente avanzados. El uso combinado de radioterapia externa y braquiterapia aumenta la supervivencia en estas pacientes. La braquiterapia permite proporcionar mayor dosis de radiación al tumor con menor toxicidad de los tejidos vecinos en comparación con la radioterapia externa exclusiva. La planificación de la braquiterapia se ha realizado durante años exclusivamente con tomografía computarizada (TC). La reciente incorporación de la resonancia magnética (RM) ha demostrado que aporta información esencial del tumor y de las estructuras vecinas, y permite definir mejor los volúmenes blanco. No obstante, la RM presenta limitaciones, algunas de las cuales se pueden compensar con la fusión de imágenes de TC y RM, con lo que se consigue una planificación óptima al combinar las ventajas de cada técnica.
Cervical cancer is the third most common gynecological cancer. Its treatment depends on tumor staging at the time of diagnosis, and a combination of chemotherapy and radiotherapy is the treatment of choice in locally advanced cervical cancers. The combined use of external beam radiotherapy and brachytherapy increases survival in these patients. Brachytherapy enables a larger dose of radiation to be delivered to the tumor with less toxicity for neighboring tissues with less toxicity for neighboring tissues compared to the use of external beam radiotherapy alone. For years, brachytherapy was planned exclusively using computed tomography (CT). The recent incorporation of magnetic resonance imaging (MRI) provides essential information about the tumor and neighboring structures making possible to better define the target volumes. Nevertheless, MRI has limitations, some of which can be compensated for by fusing CT and MRI. Fusing the images from the two techniques ensures optimal planning by combining the advantages of each technique.
El cáncer de cérvix es el tercer cáncer ginecológico en frecuencia después del cáncer de endometrio y el de ovario1. La estadificación del cáncer de cérvix se realiza de forma clínica siguiendo la última revisión de la FIGO (International Federation of Gynecology and Obstetrics) del año 2009 (tabla 1), y la resonancia magnética (RM) es la prueba de imagen de elección para valorar la extensión local del tumor2. En este artículo hacemos una revisión del tratamiento del cáncer de cérvix localmente avanzado (estadios IB2 a IVA), presentamos la utilidad de la RM en la delimitación del cáncer de cérvix previo a la administración de braquiterapia, describimos las técnicas habituales de RM para esta planificación y discutimos las implicaciones técnicas y de seguridad del uso de la RM para esta aplicación clínica. Todo ello ilustrado con ejemplos prácticos de la utilidad de la RM para planificar la braquiterapia para el tratamiento de pacientes con cáncer de cérvix avanzado.
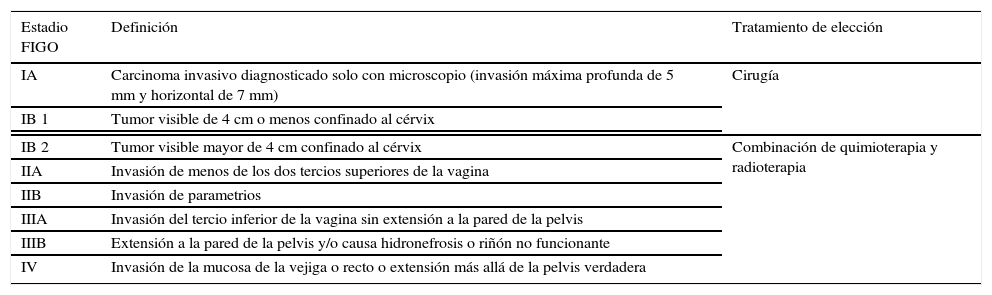
Estadificación del cáncer de cérvix (International Federation of Gynecology and Obstetrics [FIGO], 2009)
| Estadio FIGO | Definición | Tratamiento de elección |
|---|---|---|
| IA | Carcinoma invasivo diagnosticado solo con microscopio (invasión máxima profunda de 5 mm y horizontal de 7 mm) | Cirugía |
| IB 1 | Tumor visible de 4 cm o menos confinado al cérvix | |
| IB 2 | Tumor visible mayor de 4 cm confinado al cérvix | Combinación de quimioterapia y radioterapia |
| IIA | Invasión de menos de los dos tercios superiores de la vagina | |
| IIB | Invasión de parametrios | |
| IIIA | Invasión del tercio inferior de la vagina sin extensión a la pared de la pelvis | |
| IIIB | Extensión a la pared de la pelvis y/o causa hidronefrosis o riñón no funcionante | |
| IV | Invasión de la mucosa de la vejiga o recto o extensión más allá de la pelvis verdadera | |
Adaptado de De Los Santos et al.3
El tratamiento del cáncer de cérvix depende del estadio del tumor en el momento del diagnóstico, y la combinación de quimioterapia y radioterapia con intención curativa se considera el tratamiento de elección para los cánceres localmente avanzados (estadios IB2 a IVA)3. La quimioterapia más utilizada se basa en un régimen de cisplatino, con o sin 5-fluorouracilo, y es más efectiva en los estadios iniciales de los tumores localmente avanzados (IB a IIB)3. Aunque la cirugía se ofrece como tratamiento para pacientes en estadio IIA en algunos centros, la tendencia actual es ofrecer quimioterapia y radioterapia como tratamiento de elección, ya que la cirugía suele ser no curativa y la radioterapia tras la cirugía tiene mayor toxicidad y morbilidad para la paciente3.
Los protocolos actuales de radioterapia incluyen la aplicación de radioterapia externa y local (braquiterapia). El uso combinado de radioterapia externa y braquiterapia aumenta la supervivencia a los 4 años en pacientes con carcinoma de cérvix avanzado en comparación con el uso exclusivo de radioterapia externa3,4. La braquiterapia facilita la administración de dosis superiores de radiación al tumor cervical, con menor afectación de las estructuras vecinas en comparación con la radiación externa3.
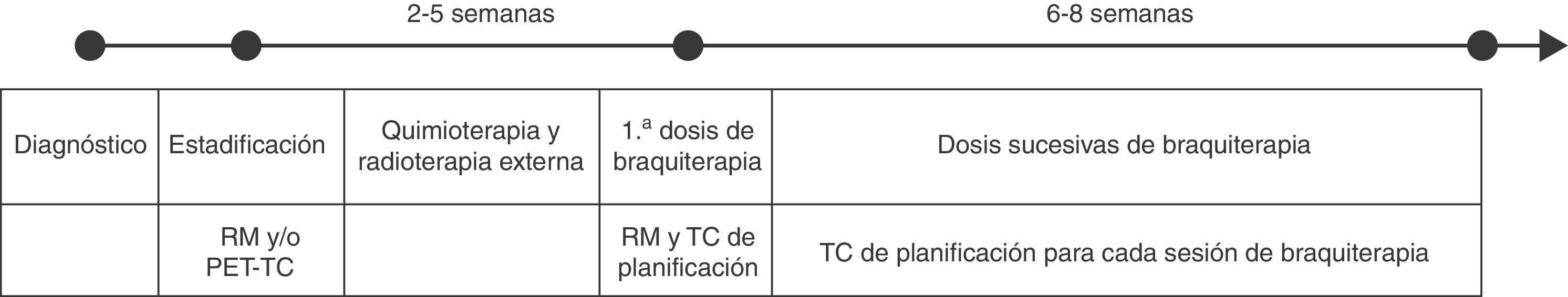
Habitualmente, la braquiterapia se inicia una vez el tumor se ha reducido de tamaño, entre dos y cinco semanas después del comienzo del tratamiento con radiación externa (fig. 1). La dosis total de radiación aplicada con braquiterapia se administra en varias sesiones, una o dos sesiones en caso de braquiterapia de baja dosis (0,4-2Gy/h) y entre tres y seis sesiones si se utilizan dosis elevadas (>12Gy/h). Ambos protocolos de aplicación de la radiación tienen una eficacia similar3. Sin embargo, la braquiterapia de alta dosis tiene la ventaja de que se puede aplicar de forma ambulatoria y permite mayor control sobre la distribución de la dosis. Aunque teóricamente existe un riesgo más elevado de toxicidad en el tejido sano con este tipo de braquiterapia debido a la dosis más elevada, los estudios aleatorizados completados hasta la fecha no han demostrado un mayor índice de complicaciones secundarios a la radiación de órganos adyacentes al tumor3,5. La radioterapia con dosis bajas requiere el ingreso de la paciente con aplicación del tratamiento durante varios días, pero ocasiona menos toxicidad en el tejido sano, ya que la dosis de radiación es menor.
Además de las diferencias en la dosis, existen diferentes formas de administrar el tratamiento con braquiterapia: intracavitaria, con aplicadores introducidos en la vagina y el útero; o intersticial, insertando directamente en el tumor agujas con las fuentes de radiación. Esta última se utiliza generalmente cuando hay afectación extensa de la vagina3 o cuando los fórnices vaginales son fibróticos5.
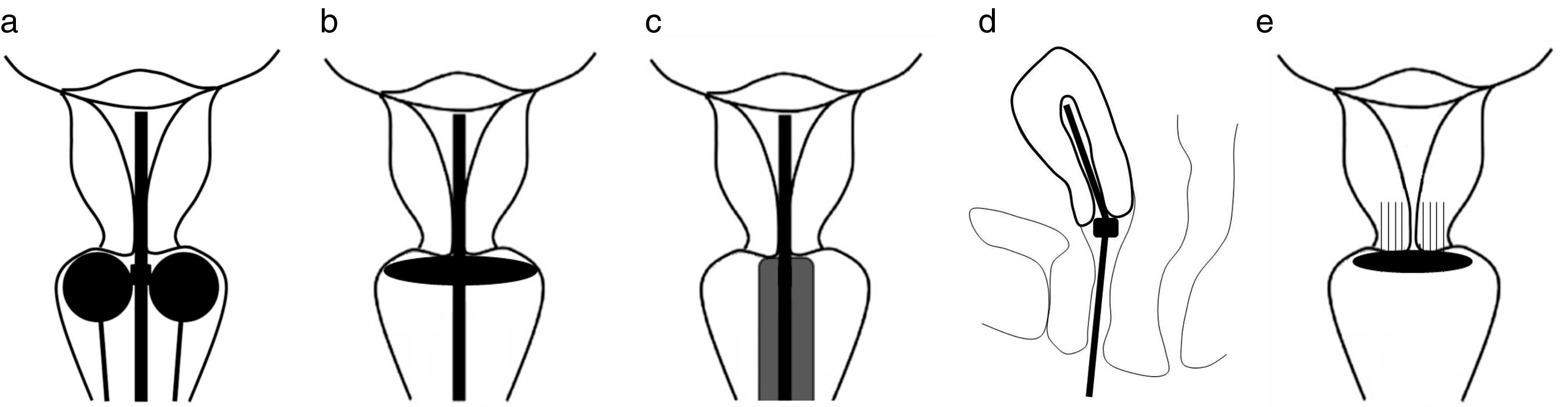
Los aplicadores para la braquiterapia intracavitaria pueden ser metálicos o no metálicos. Entre ellos se pueden encontrar, por ejemplo, un tándem uterino con anillo vaginal, un tándem uterino con ovoides vaginales o un tándem uterino con cilindro vaginal3 (fig. 2). El tipo de aplicador utilizado depende de las preferencias del radioterapeuta, el confort de la paciente y las consideraciones anatómicas (en casos de pacientes histerectomizadas no se puede utilizar tándem uterino, por lo que solo se usará un cilindro vaginal). En la Universidad de Texas Southwestern se utiliza generalmente un tándem uterino de titanio con ovoides vaginales. Los aplicadores tienen canales por donde se introduce la fuente radiactiva. El aplicador ideal de braquiterapia ha de ser simple, confortable para la paciente, resistente a la tensión, barato, duradero, seguro, no tóxico, esterilizable, compatible con dosis de radiación alta (pulsada y baja), con material para su fijación y recolocación, fácil de identificar en la TC y la RM, y que cause la menor cantidad de artefactos posibles6.
Dibujos esquemáticos de los aplicadores correctamente colocados. a) Tándem uterino con ovoides vaginales; los ovoides vaginales deben situarse próximos al orificio cervical externo. b) Tándem uterino con anillo. c) Tándem uterino con cilindro. d) El extremo del tándem uterino debe colocarse en el fundus uterino. e) Aplicador de braquiterapia intersticial con las agujas introducidas en el estroma cervical.
El objetivo de la planificación de la braquiterapia es definir el volumen blanco para aplicar la máxima radiación al tumor y minimizar la dosis en los tejidos normales adyacentes7. En los inicios de la braquiterapia para el tratamiento del cáncer de cérvix la planificación se realizaba mediante radiografías simples3,8. Una vez colocado el aplicador se obtenía una radiografía anteroposterior de la pelvis y se localizaba el punto de referencia denominado «punto A», el cual está situado 2cm por encima de los ovoides y 2cm lateral al aplicador. Este punto se utilizaba como referencia antómica para la estandarización de la dosis de radiación2,5. No se tenían en cuenta, sin embargo, las características del tumor ni la anatomía de la paciente. Este abordaje era simple, rápido y generalmente seguro, pero no permitía obtener resultados óptimos en todos los casos, ya que la planificación no estaba individualizada específicamente para la anatomía de la paciente o el tumor en cuestión.
En los últimos años, la adopción de la TC ha permitido la planificación de la braquiterapia en tres dimensiones (3D)2,3, y su uso se está extendiendo a la mayoría de los centros que aplican este tratamiento en pacientes con cáncer de cérvix6,8. Esta planificación 3D también puede llevarse a cabo mediante RM2,8,9 y algunos autores proponen realizarla mediante tomografía por emisión de positrones (PET)-TC6,10. Además, se pueden fusionar las imágenes de TC y RM para aprovechar las ventajas de cada modalidad en la delimitación del aplicador así como del tumor y los órganos adyacentes, respectivamente. Estas técnicas 3D permiten al oncólogo radioterapeuta administrar mayor dosis de radiación al volumen blanco para un mejor control local de la enfermedad y reducir la dosis a los tejidos normales, de modo que disminuye la probabilidad de toxicidad6.
El volumen blanco clínico de alto riesgo (HR CTV) comprende áreas de alto riesgo de recurrencia por la persistencia de tumor residual macroscópico tras la radioterapia externa e incluye, además, todo el cérvix. La dosis total aplicada a este volumen debe ser la mayor posible para erradicar todo el tumor macroscópico residual. El volumen blanco clínico de riesgo intermedio (IR CTV) comprende áreas donde existía tumor macroscópico en el momento del diagnóstico (antes de la radioterapia externa) pero no al inicio de la braquiterapia, por lo que son áreas con potencial enfermedad microscópica residual. El volumen blanco de planificación (PTV) incluye el volumen blanco clínico, de alto riesgo y de riesgo intermedio, con un margen de seguridad que considera posibles movimientos de la paciente e inexactitudes en la administración de la braquiterapia2,7.
Técnicas de imagen: ventajas y limitacionesTomografía computarizadaLa TC localiza de forma precisa el aplicador intracavitario, define el grosor de la pared uterina y muestra las relaciones anatómicas del aplicador con las estructuras vecinas11. La limitación fundamental de la TC radica en una mala visualización del volumen tumoral debido a un nivel bajo de contraste en los tejidos de partes blandas, con la consiguiente dificultad para distinguir el tumor cervical del útero y para definir el límite entre el cérvix y la vagina, así como para delinear con precisión la vejiga y el recto8. Esta última distinción es particularmente difícil en aquellas pacientes con atrofia del plexo perivaginal y escasa grasa pélvica en las que los planos anatómicos de separación entre la vagina, el cérvix, el útero y/o el tumor con la vejiga y el recto pueden estar adelgazados o ser inexistentes. Además, los aplicadores estándar de metal pueden producir artefactos en las imágenes de TC, lo que puede dificultar la determinación del volumen tumoral, la pared anterior del recto y la pared posterior de la vejiga.
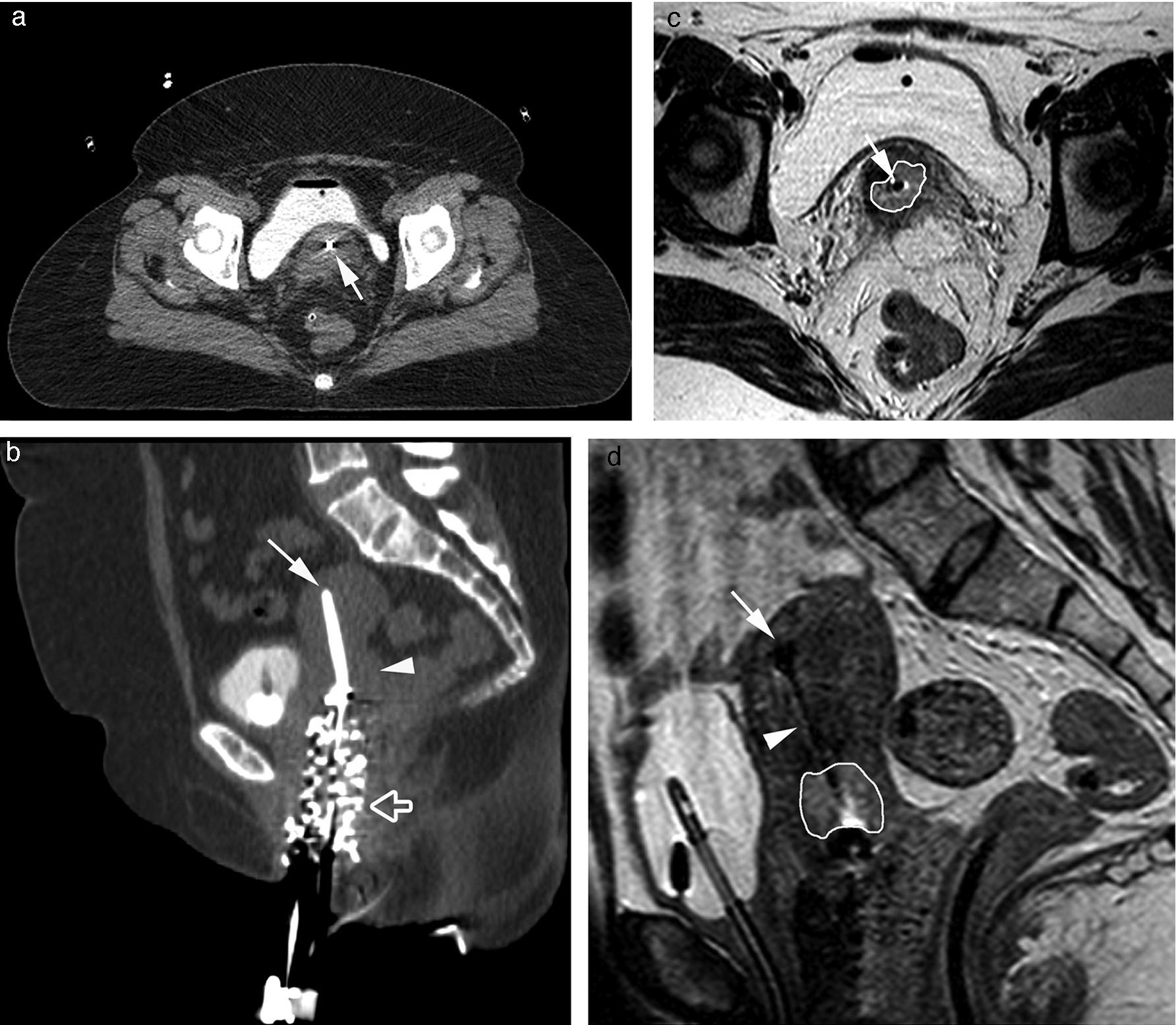
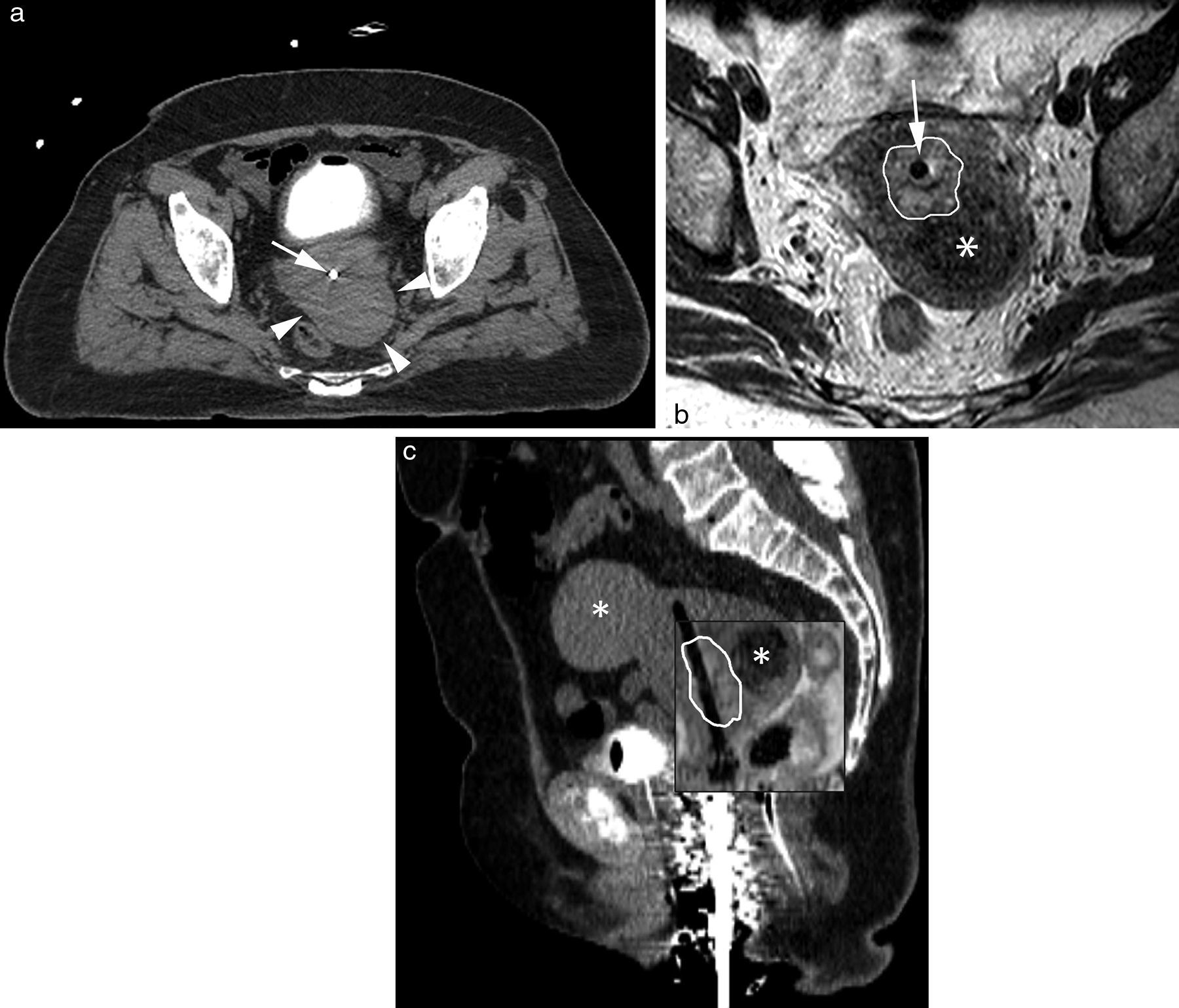
Resonancia magnéticaLa RM presenta algunas ventajas e inconvenientes frente a la TC para planificar la braquiterapia8,12–14. La RM presenta un mejor contraste de tejidos de partes blandas, lo que proporciona una mejor definición del tamaño y la localización del cáncer de cérvix, que es moderadamente hiperintenso en secuencias potenciadas en T2 respecto al estroma cervical normal, y permite diferenciarlo del útero normal (fig. 3). Asimismo, la RM facilita la visualización de tejidos adyacentes y otras patologías que dificultan la delineación del tumor en la TC (fig. 4). La optimización de la planificación mediante el uso de la RM mejora sustancialmente la dosimetría aplicada al recto, al sigma y a la vejiga comparada con el tratamiento tras la planificación convencional con radiografías, especialmente en pacientes con tumores de pequeño tamaño en el momento del diagnóstico o que disminuyen significativamente de tamaño tras la radioterapia externa15.
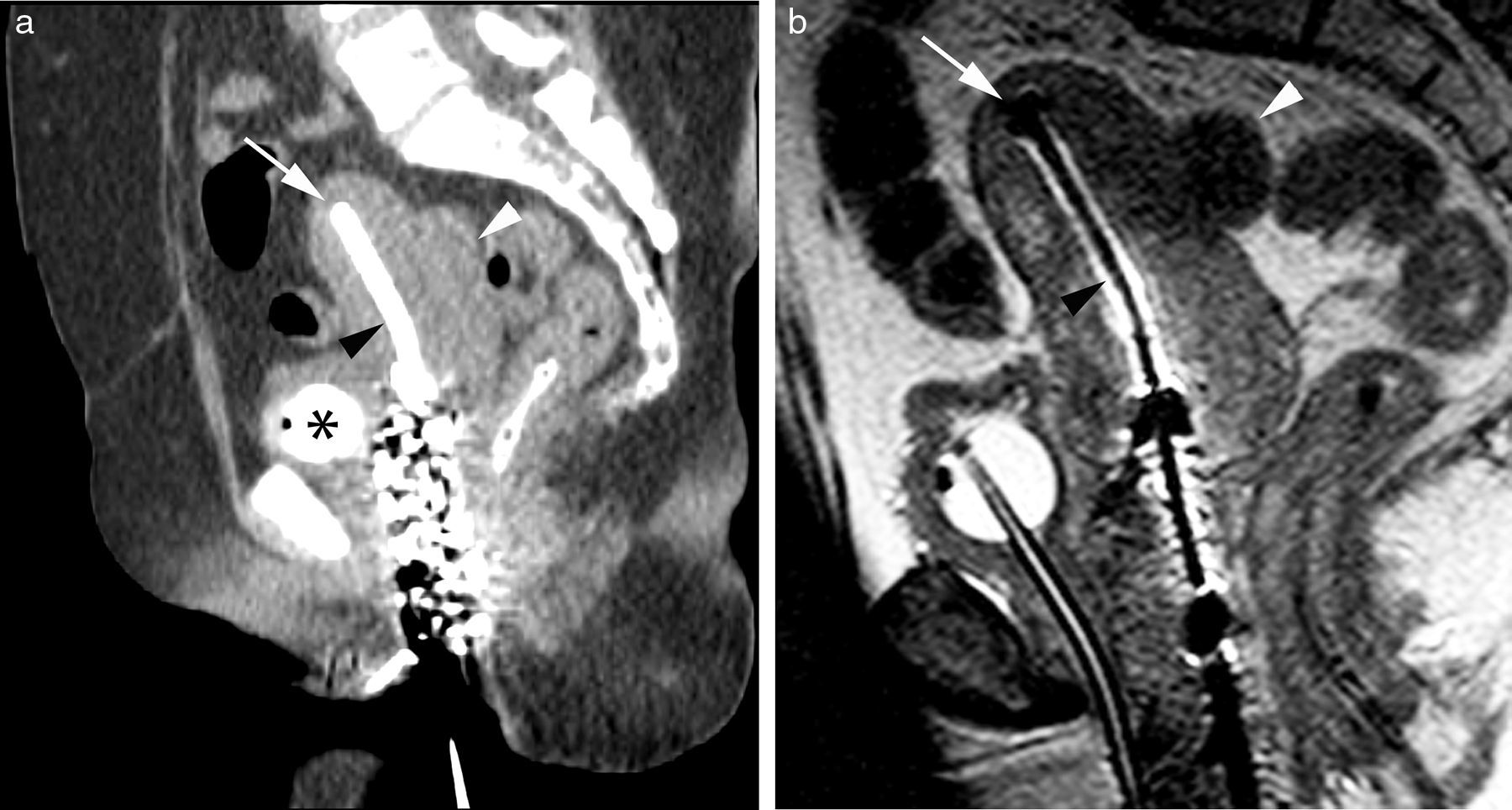
Imágenes de planificación de braquiterapia intracavitaria de alta dosis en una paciente con cáncer de cérvix. Imagen de TC axial (a) y sagital (b) donde se observa el tándem uterino (flecha blanca) con artefactos de endurecimiento del haz en el cérvix. No se identifica el tumor en el cérvix (cabeza de flecha blanca). Se observa la vejiga con sonda de Foley parcialmente rellena de contraste y material de empaquetamiento en la vagina (flecha blanca hueca). En las imágenes de resonancia magnética 2D FSE axial (c) y sagital (d) potenciadas en T2 se observa el tándem uterino (flecha blanca) y se delimita con exactitud el tumor que muestra una señal intermedia en las secuencias potenciadas en T2 (línea blanca) rodeado del estroma cervical hipointenso, pero existe peor visualización del tándem uterino (cabeza de flecha blanca) y del extremo del mismo en el fundus uterino (flecha blanca).
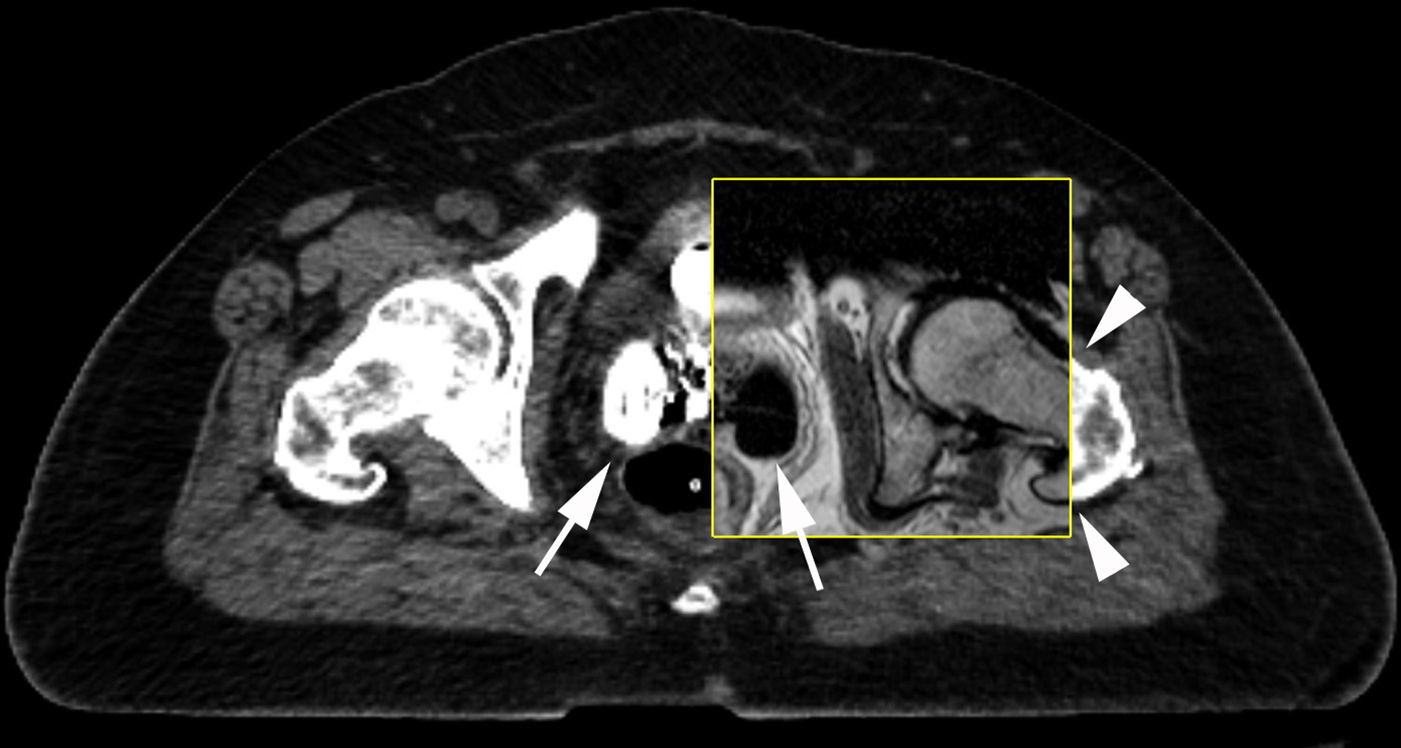
Imágenes de planificación de braquiterapia intracavitaria de alta dosis en una paciente con cáncer de cérvix. Imagen de TC axial (a) donde se observa el tándem uterino del aplicador (flecha blanca) y una masa en la vertiente posterolateral izquierda del cérvix (cabezas de flecha blancas). La imagen de RM axial 2D FSE potenciada en T2 (b) muestra el tándem uterino del aplicador (flecha blanca) y la extensión del cáncer de cérvix (línea blanca), y confirma que la masa cervical posterolateral izquierda que se observa en la TC corresponde a un fibroma (asterisco). En las imágenes sagitales fusionadas de TC y RM (c) se identifica con precisión la extensión tumoral en la RM (línea blanca). Se observan dos fibromas (asteriscos), la vejiga con sonda de Foley y el material de empaquetamiento en la vagina.
Entre los inconvenientes de la RM frente a la TC destacan el mayor tiempo de adquisición de las imágenes de RM, peor definición de la anatomía ósea respecto a la TC, peor delimitación del aplicador, especialmente de la punta del mismo, y la necesidad de utilizar aplicadores compatibles con la RM, que son más caros que los aplicadores convencionales6.
Tomografía por emisión de positronesAlgunos autores proponen utilizar la PET para planificar la braquiterapia6,10. Esta técnica tiene la ventaja de que no son necesarios aplicadores específicos y las imágenes pueden fusionarse con las de TC para mejorar la resolución espacial. No obstante, tiene el inconveniente de que el tejido inflamatorio no tumoral puede presentar captación de 18F-fluorodeoxiglucosa6 y llevar al consiguiente error en la planificación de la braquiterapia. La PET-TC tiene, además, el mismo inconveniente que la TC en la dificultad para delinear estructuras anatómicas adyacentes. En nuestra experiencia, la baja resolución de la PET puede dificultar la identificación de extensión tumoral sutil, por ejemplo, en el parametrio.
Consideraciones técnicas en resonancia magnética para la planificación de la braquiterapiaLa RM proporciona información sobre la extensión del tumor y ayuda a localizar las estructuras adyacentes en las tres dimensiones del espacio, todo ello con el aplicador intracavitario colocado en su posición terapéutica. Es recomendable realizar un estudio de RM antes del inicio del tratamiento con radioterapia externa y otro antes de la braquiterapia con el aplicador colocado en su posición terapéutica habitual.
AplicadoresLos aplicadores considerados «condicionales», y por tanto utilizables en el entorno de la RM, son los no metálicos y de titanio9. Los aplicadores de plástico, por ejemplo, no interfieren con el campo magnético y aparecen como un vacío de señal en las imágenes de RM. Para facilitar la detección del aplicador pueden rellenarse los canales con una solución de sulfato de cobre (CuSO4), que reduce el tiempo de relajación del agua, aunque el pequeño volumen que se puede usar por el pequeño tamaño de los canales limita la señal en la RM. Las imágenes eco de gradiente potenciadas en T1 permiten visualizar mejor el aplicador con CuSo4 en comparación con las secuencias espín eco potenciadas en T29. Estos aplicadores con CuSo4 pueden reutilizarse aunque la señal se degrada aproximadamente a los 3 meses de su uso inicial9.
Los aplicadores de titanio son seguros en campos magnéticos de hasta 1,5T, pero se han descrito casos de calentamiento y desplazamiento del aplicador en estudios con fantomas en campos magnéticos de 3T16. La reconstrucción de las imágenes de RM de los aplicadores de titanio es más complicada que la de los de plástico porque producen artefactos de susceptibilidad, particularmente en las zonas de mayor grosor del aplicador (extremo del tándem, ovoides y anillo), y además hace inútil el uso de la solución CuSO4 en los canales. El artefacto de susceptibilidad se puede minimizar cuando el aplicador se coloca en paralelo al campo magnético principal9,17,18. La fusión de imágenes de RM y TC facilita la visualización del extremo del aplicador.
Preparación de la pacientePara colocar el aplicador se utiliza sedación o anestesia general5. No es necesario realizar una preparación intestinal antes del procedimiento. Los autores colocan el aplicador bajo sedación moderada (midazolam y fentanilo) en el Departamento de Oncología Radioterápica, el cual se encuentra cercano a la zona de RM en el Departamento de Radiología. El tándem debe colocarse en la cavidad uterina con el extremo distal en el fundus uterino y los ovoides en la vagina, cerca del orificio cervical externo (fig. 2). Tras la colocación del aplicador, la vagina se empaqueta con gasas de algodón para mantener el tándem en la posición deseada y evitar que se desplace cuando se mueve a la paciente. Una vez se ha asegurado la posición del aplicador, la paciente se desplaza en camilla a la sala de RM y se coloca en la mesa de RM en posición supina. Es imprescindible que la paciente se encuentre en una posición similar durante la adquisición de la RM y la TC, para la correcta fusión de las imágenes y la sesión de tratamiento. La repleción de la vejiga debe ser similar durante la adquisición de las imágenes de RM y la TC de planificación. En la mayoría de los casos, un catéter vesical (Foley) permite mantener la vejiga colapsada durante la RM, la TC y el tratamiento. La distensión de la vejiga es útil, sin embargo, cuando los estudios de imagen previos al tratamiento muestran asas de intestino delgado cerca del cérvix uterino. En estos casos los autores distienden la vejiga con 200ml de contraste yodado diluido (Isovue, 10% en suero salino). La vejiga distendida, con contenido líquido en su interior con intensidad de señal elevada en las imágenes potenciadas en T2 y atenuación elevada en la TC de planificación, desplaza el intestino delgado superiormente disminuyendo la posibilidad de toxicidad por radiación del mismo. Una vez concluido el examen de RM, se traslada de nuevo a la paciente al Departamento de Oncología Radioterápica para la adquisición de un examen de TC de la pelvis y el subsecuente tratamiento, con especial precaución para que el aplicador no se mueva durante el traslado.
Protocolo de imagen por resonancia magnética para planificación de braquiterapiaSe utiliza una antena de superficie en la pelvis para aumentar la relación señal-ruido de la zona de interés. Las secuencias básicas en el protocolo de imagen son las secuencias bidimensionales (2D) espín eco rápidas (fast spin echo, FSE) potenciadas en T2 porque el contraste de partes blandas inherente a estas adquisiciones ofrece una visualización óptima del tumor, las estructuras vecinas y el aplicador6,9. El tumor es, en general, levemente hiperintenso en relación con el estroma cervical no afectado. La hipointensidad de señal del estroma cervical no afectado en estas secuencias proporciona un referente anatómico para la determinación de la extensión tumoral fuera del cérvix6. Es preferible usar secuencias FSE frente a las espín eco convencionales porque requieren menor tiempo de adquisición6. Las secuencias FSE potenciadas en T2 sin saturación de la grasa, en plano axial y sagital, facilitan la identificación de la extensión tumoral en el parametrio, así como la visualización de las paredes posterior de la vejiga y anterior del recto y su posición en relación con el tumor gracias a la hiperintensidad de señal de los planos grasos6. Los autores utilizan habitualmente las adquisiciones 2D en el plano axial o reconstrucciones axiales de la adquisición sagital 3D (veáse más adelante) para trazar el volumen blanco debido a la facilidad para fusionar estas imágenes con las imágenes axiales de la TC. Las imágenes sagitales o reconstrucciones multiplanares en otros planos del espacio son útiles para esclarecer la extensión del tumor en la dirección cráneo-caudal y evitar problemas de volumen parcial con los fórnices vaginales orientados horizontalmente debido a la posición de los ovoides.
En general, las secuencias eco de gradiente potenciadas en T1 no son necesarias pero es posible que sean útiles en algunos casos para evaluar la presencia de adenopatías pélvicas o caracterizar tejidos blandos. Se ha descrito un mejor contraste útero-tándem con las secuencias potenciadas en densidad de protones en comparación con las adquisiciones potenciadas en T219. Sin embargo, si se realiza la fusión de las imágenes FSE potenciadas en T2 con las imágenes de TC de forma rutinaria, probablemente el beneficio en la visualización del tándem es mínimo.
Recientemente se ha propuesto el uso de la imagen por difusión (DWI) con secuencias espín eco ecoplanar para delinear el volumen tumoral. Se ha sugerido que el área que demuestra restricción en el mapa del coeficiente de difusión aparente (ADC) se corresponde con el volumen de tumor metabólicamente activo en la PET-TC20. Aunque las secuencias DWI son parte del protocolo de imagen, en nuestra experiencia la distorsión causada por la presencia del tándem puede limitar la obtención de imágenes con suficiente calidad para delinear el tumor de forma adecuada. Es díficil valorar el impacto que esta distorsión pueda tener en la cuantificación del ADC en el tumor. Además, la correlación entre el volumen de tumor en el mapa de ADC y el volumen de tumor metabólicamente activo en la PET-TC puede ser fruto de la limitada resolución espacial de ambos métodos. Es posible, sin embargo, que nuevos avances en secuencias DWI, como por ejemplo adquisiciones FSE y adquisiciones con campo de visión (field of view) limitado puedan solventar en parte ambos problemas. Igualmente, es previsible que la resolución espacial de la PET mejore con los recientes avances en la tecnología de detectores.
El protocolo de imagen de la Universidad de Texas Southwestern incluye secuencias axiales 2D FSE y secuencias sagitales 3D FSE, ambas potenciadas en T2 (tabla 2). La ventaja fundamental de la secuencia 3D sagital comparada con una adquisición 2D es la posibilidad de realizar reconstrucciones multiplanares con buena resolución espacial en todos los planos, facilitada por la interpolación en la dirección del espesor de corte (adquisición 3D con espesor de corte de 2mm e interpolada para generar cortes de 1mm de espesor). Sin embargo, en nuestra experiencia, las reconstrucciones axiales de la adquisición 3D no reemplazan las adquisiciones 2D en el plano axial debido a una mayor vulnerabilidad al movimiento y menor resolución espacial en el plano axial de las primeras. Consideramos por tanto que las adquisiciones 2D y 3D son complementarias.
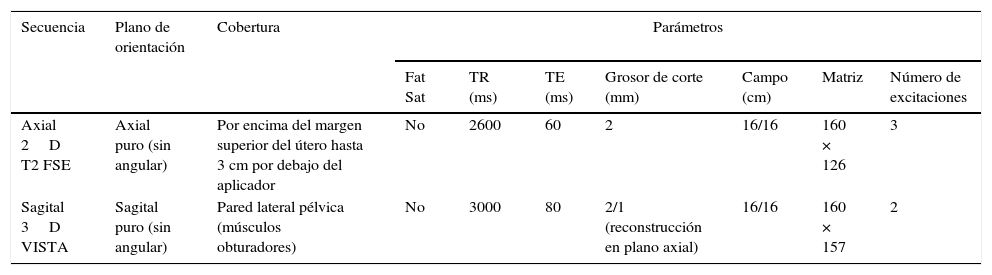
Protocolo de resonancia magnética para la planificación de la braquiterapia intracavitaria en el tratamiento del cáncer de cérvix utilizado en la Universidad de Texas Southwestern
| Secuencia | Plano de orientación | Cobertura | Parámetros | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Fat Sat | TR (ms) | TE (ms) | Grosor de corte (mm) | Campo (cm) | Matriz | Número de excitaciones | |||
| Axial 2D T2 FSE | Axial puro (sin angular) | Por encima del margen superior del útero hasta 3 cm por debajo del aplicador | No | 2600 | 60 | 2 | 16/16 | 160 × 126 | 3 |
| Sagital 3D VISTA | Sagital puro (sin angular) | Pared lateral pélvica (músculos obturadores) | No | 3000 | 80 | 2/1 (reconstrucción en plano axial) | 16/16 | 160 × 157 | 2 |
Por último, es importante mantener el tiempo total del estudio de RM tan corto como sea posible, ya que las pacientes con el aplicador colocado en posición terapéutica tienden a sentirse incómodas a medida que transcurre el tiempo. El desplazamiento del aplicador ocasionado por el movimiento de la paciente hace inútil la información proporcionada por el estudio de RM, por lo que es importante utilizar un protocolo de imagen de RM corto pero que proporcione la información necesaria para planificar el tratamiento.
Selección de campo magnético: 1,5T vs. 3TLas RM de 1,5T ofrecen una calidad óptima para la adquisición de las imágenes para la planificación de la braquiterapia del cáncer de cérvix. El uso de RM de 3T es limitado debido a la distorsión de las imágenes y la presencia de artefactos causados por el aplicador. Además, el potencial calentamiento de los aplicadores durante la realización del estudio es también problemático en las RM de 3 T16. Es probable que, en el futuro, mejoras en las secuencias de RM que utilicen niveles más bajos de energía y/o parámetros de imagen que corrijan la distorsión geométrica causada por el aplicador permitan hacer estudios de RM en equipos de 3T con calidad de imagen similar o incluso superior a los de 1,5T. Igualmente, es posible que el uso de aplicadores no metálicos facilite la incorporación de la RM de 3T en esta aplicación clínica.
Fusión de la tomografía computarizada y la resonancia magnéticaAunque la RM puede usarse como modalidad única para la planificación de la braquiterapia2,8,9, esta proposición tiene limitaciones debido a la incapacidad para delimitar con precisión el contorno del aplicador mediante RM9. Este inconveniente puede solucionarse en gran parte mediante la utilización de la RM conjuntamente con la TC fusionando las imágenes generadas por ambas modalidades.
En la Universidad de Texas Southwestern se realizan dos estudios de planificación: el de RM seguido de la TC. Tras completar el estudio de RM con el aplicador en posición terapéutica, las imágenes axiales de TC para la planificación se obtienen sin contraste intravenoso, con un grosor de corte de 2mm (en ocasiones con la vejiga rellena de contraste, como se ha descrito previamente). A continuación se fusionan las imágenes de RM y TC, se planifica el tratamiento y se procede a la administración de la primera fracción de braquiterapia.
Para fusionar las imágenes de TC y RM, estas se importan a una estación de trabajo con software específico para esta aplicación. En general, se utilizan las adquisiciones sagitales de RM y una reconstrucción sagital de la TC de planificación para el registro anatómico de los dos exámenes, ya que esta última ofrece una identificación superior del aplicador intracavitario (fig. 5). El punto guía para la fusión es la zona de unión entre el tándem y el ovoide del aplicador, que debe estar adyacente al orificio cervical externo. Se utiliza este referente anatómico porque es fácil de identificar, tiene una forma fija y está en la proximidad del volumen blanco clínico de alto riesgo. Tras alinear las imágenes en el plano sagital, se confirma la correcta superposición de las imágenes en el plano axial de la RM y la TC (fig. 6), que se utilizan como se ha descrito previamente para delinear el volumen blanco (fig. 7).
Imágenes de planificación de la braquiterapia intracavitaria de alta dosis en una paciente con cáncer de cérvix. La reconstrucción sagital de la TC (a) muestra el tándem uterino (cabeza de flecha negra) con el extremo (flecha blanca) en el fundus uterino. La pared posterior del útero muestra un borde lobulado (cabeza de flecha blanca) que podría corresponder a extensión tumoral. La vejiga tiene una sonda de Foley con el globo hinchable relleno de contraste yodado (asterisco). Se observa el material de empaquetamiento en la vagina. La imagen de RM sagital 2D FSE potenciada en T2 (b) de la misma paciente muestra el tándem uterino (cabeza de flecha negra) con mala definición del extremo del mismo por artefacto de susceptibilidad (flecha blanca). En cambio, se define mejor la pared uterina, con clara distinción de la misma y del colon sigmoide adyacente (cabeza de flecha blanca).
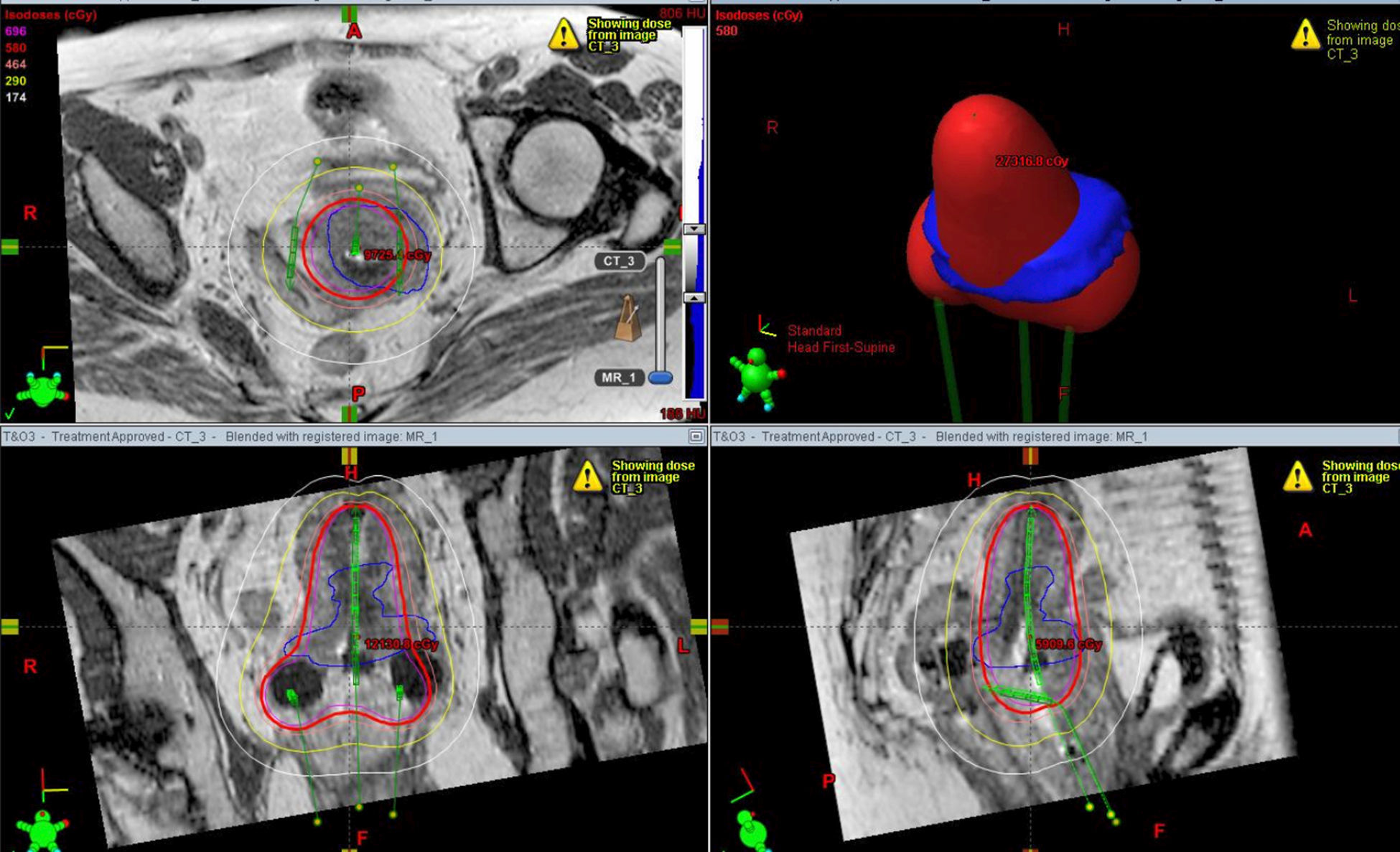
Ejemplo de planificación multiplanar con RM de la braquiterapia intracavitaria del cáncer de cérvix. La línea azul marca el contorno externo del tumor, mientras que la línea roja muestra la isodosis de radiación prescrita. El aplicador de braquiterapia intracavitaria está marcado en verde.
Para las siguientes sesiones de braquiterapia se realiza una nueva TC de planificación en cada visita, y cada uno de estos exámenes de TC se fusionan con las imágenes de la RM inicial, usando como punto de referencia para la fusión la misma zona de unión entre el tándem y el ovoide del aplicador. En general no se repiten losestudios de RM. Tras la fusión se planifica la braquiterapia identificando el aplicador en las imágenes de TC y determinando el volumen blanco en las imágenes de RM.
ConclusiónLa RM para la planificación de la braquiterapia del cáncer de cérvix proporciona información esencial sobre el tumor y la localización de otras estructuras anatómicas adyacentes importantes. El análisis sistemático de los hallazgos con el aplicador colocado en posición terapéutica ofrece una mejor definición de los volúmenes blanco en comparación con la planificación convencional, lo que permite optimizar la dosis administrada al tumor y reducir la dosis administrada al recto, el sigma y la vejiga.
La visualización del aplicador con RM es limitada, pero se puede mejorar fusionando las imágenes de RM con las de TC mediante el uso de software especializado. Es posible que otras secuencias de RM, como las potenciadas en densidad de protones, permitan mejorar la visualización del aplicador. Es deseable que el desarrollo tecnológico permita en un futuro superar las limitaciones de la RM para poder generalizar el uso de esta técnica como modalidad única en la planificación de la braquiterapia en pacientes con cáncer de cérvix.
El éxito de la implantación de un protocolo de planificación con RM de la braquiterapia del cáncer de cérvix requiere ajustes en los protocolos de imagen por RM, así como consideraciones sobre las medidas de seguridad y necesidades logísticas en la sala de la RM durante el manejo de la paciente con el aplicador intracavitario colocado en la posición terapéutica. Es imprescindible formar un equipo multidisciplinar mediante la colaboración entre los Departamentos de Imagen y Oncología Radioterápica.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Autoría- 1.
Responsable de la integridad del estudio: MOM, IP.
- 2.
Concepción del estudio: IP.
- 3.
Diseño del estudio: IP.
- 4.
Obtención de los datos: MOM, DFP, ZW, KA.
- 5.
Análisis e interpretación de los datos: MOM, DFP, IP.
- 6.
Tratamiento estadístico: no aplica en este trabajo.
- 7.
Búsqueda bibliográfica: MOM, DFP, IP.
- 8.
Redacción del trabajo: MOM, IP.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: DFP, ZW, KA, IP.
- 10.
Aprobación de la versión final: MOM, DFP, ZW, KA, IP.