El tumor desmoplástico de células pequeñas, redondas y azules (TDCPR) es un tumor maligno muy poco frecuente, que fue descrito por primera vez en 1991 por Gerald y Rosai, y en la bibliografía hay un número reducido de casos1.
Ocurre mayoritariamente en varones adolescentes y adultos jóvenes, y afecta predominantemente las membranas serosas, principalmente el peritoneo2–5.
Histológicamente pertenece a la familia de los tumores clasificados como de células pequeñas, redondas y azules, en la que se incluyen el linfoma no hodgkiniano, el neuroblastoma, el rabdomiosarcoma, el sarcoma de Ewing, el tumor de Wilms, el tumor neuroectodérmico periférico y el tumor de Askin2–7.
El TDCPR tiene un patrón inmunohistoquímico y citogenético característico y diagnóstico, que permite diferenciarlo de otros tumores de células pequeñas y redondas.
Se ha revisado retrospectivamente a 3 pacientes con diagnóstico de TDCPR abdominal, estudiados en nuestro centro entre los años 1996 y 2007. Todos los pacientes fueron sometidos a biopsia con aguja percutánea guiada por tomografía computarizada (TC) y el diagnóstico definitivo se hizo mediante análisis inmunohistoquímicos y citogenéticos.
El objetivo de este artículo es presentar los hallazgos radiológicos por TC y las características clinicopatológicas del TDCPR abdominal, resaltando el papel fundamental de la TC en su diagnóstico y estadificación.
Presentación de los casosPresentación clínicaTodos los pacientes eran varones, con edades de 11, 14 y 24 años (media de 17 años).
Los síntomas de presentación fueron: masa palpable o distensión abdominal (n=3), pérdida de peso (n=1), sudoración nocturna (n=1). Dos pacientes presentaron un aumento de las enzimas hepáticas.
Dos pacientes fallecieron, con una supervivencia media de 3 años desde el diagnóstico; 1 paciente continúa vivo y permanece libre de enfermedad desde hace 6 meses.
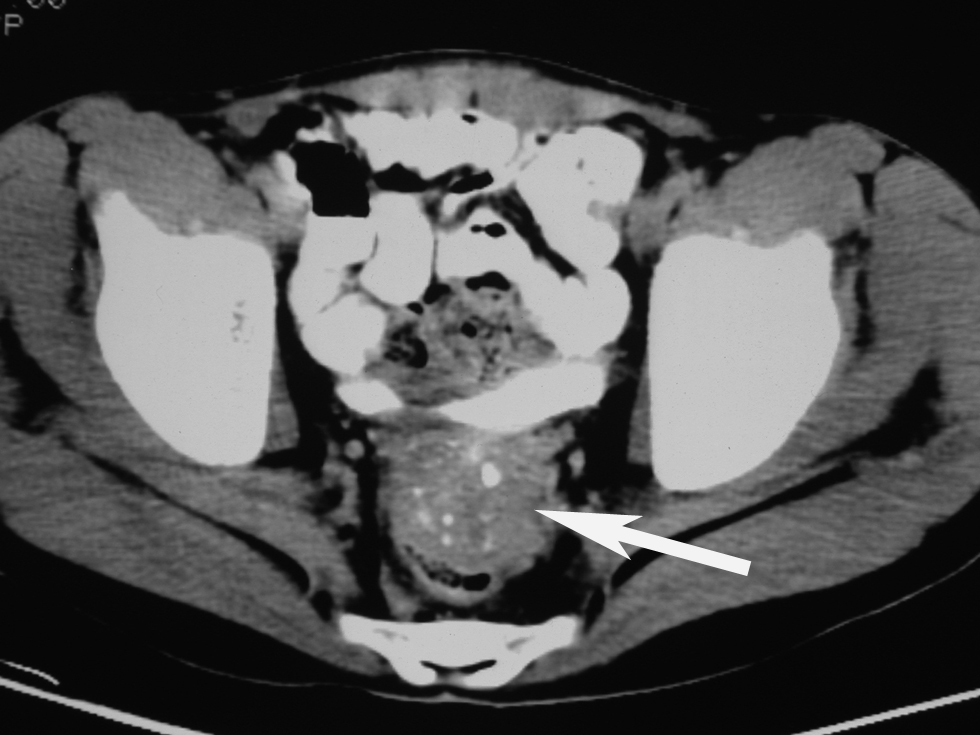
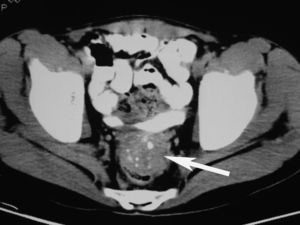
Hallazgos radiológicosCaso 1. El primer caso fue diagnosticado en septiembre de 1996, en un adolescente varón de 14 años de edad, observándose en las imágenes de TC abdominopélvica una masa de 4 cm de diámetro de densidad de partes blandas y contornos bien definidos, heterogénea, con pequeñas calcificaciones dispersas en su interior, de localización intraperitoneal en el espacio retrovesical. Se identificaron múltiples metástasis hepáticas en ambos lóbulos, hipodensas, heterogéneas, la mayor de unos 6 cm, así como múltiples adenopatías en las cadenas ganglionares celíacas y lumboaórticas, parcialmente calcificadas. No había ascitis ni uropatía obstructiva (fig. 1).
Figura 1. Tomografía computarizada de abdomen sin contraste intravenoso. En la pelvis se observa una masa tumoral localizada anterior al recto (flecha), al que desplaza posteriormente. Hay pequeñas calcificaciones en su interior.
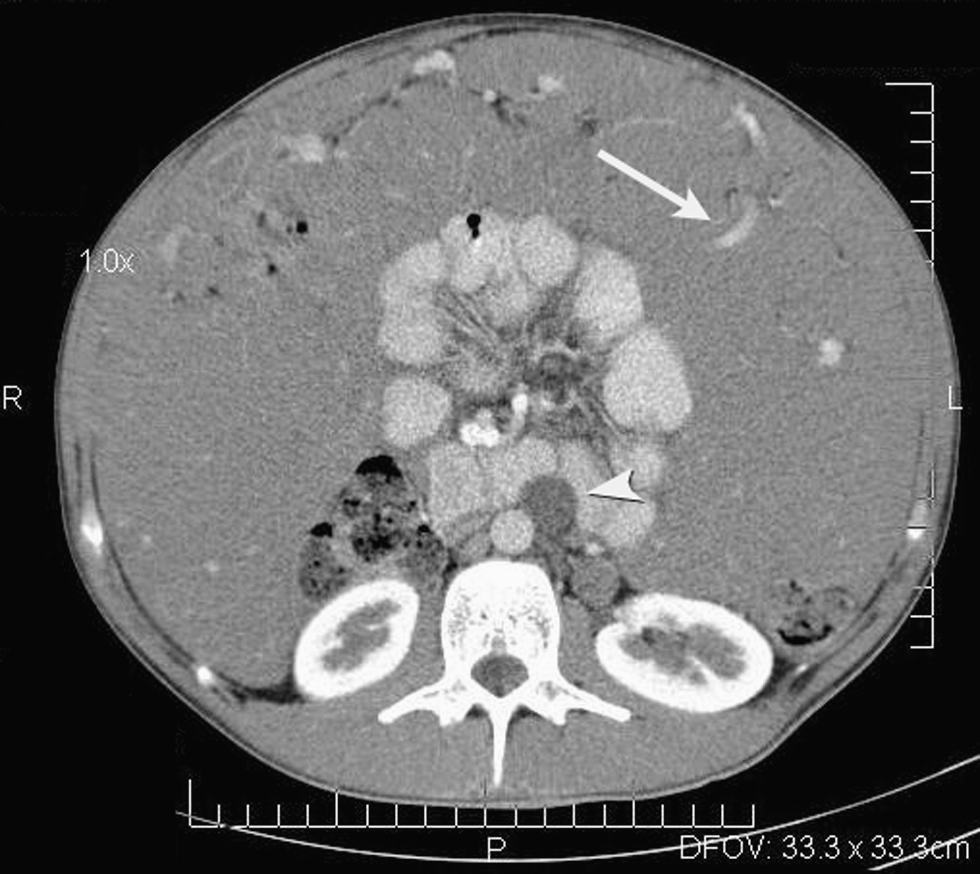
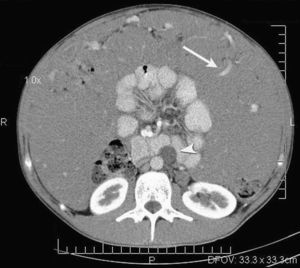
Caso 2. El segundo caso que se presenta fue diagnosticado en noviembre de 2004 en un joven varón de 24 años, que presentaba en la TC abdominal una voluminosa masa tumoral de densidad de partes blandas, homogénea, que ocupaba casi la totalidad de la cavidad peritoneal, con prominente vascularización intratumoral. Esta masa condicionaba un importante efecto de masa sobre los órganos de la cavidad peritoneal, con desplazamiento de las asas intestinales hacia una posición central. Habían varias adenopatías en las cadenas ganglionares lumboaórticas y en el hilio renal izquierdo, la de mayor tamaño de unos 5 cm, así como una pequeña cantidad de líquido ascítico perihepático. No se identificaron metástasis ni uropatía obstructiva (fig. 2).
Figura 2. Tomografía computarizada de abdomen con contraste intravenoso. Se observa una ocupación total de la cavidad peritoneal por una masa con densidad de partes blandas relativamente homogénea y con vasos prominentes en su interior (flecha). Hay un marcado efecto masa sobre las asas intestinales, que están rechazadas al centro del abdomen. Se identifican adenopatías localizadas en región preaortica y en el hilio renal izquierdo (cabeza de flecha).
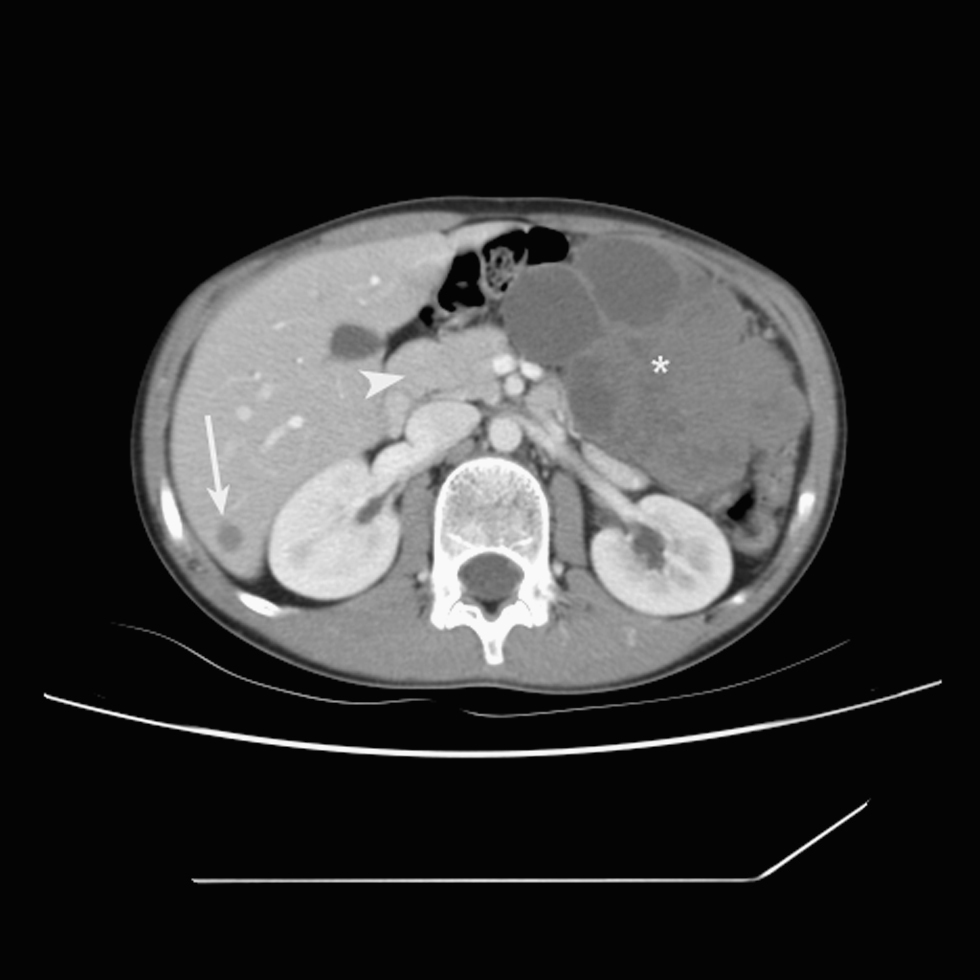
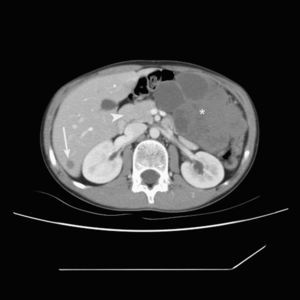
Caso 3. El tercer caso se presentó en abril de 2007 en un niño de 11 años, cuya TC abdominal mostró una masa de densidad de partes blandas, heterogénea, de contornos lobulados, con áreas quísticas en su interior en relación con necrosis intratumoral y localización intraperitoneal en la transcavidad de los epiplones, entre el estómago y el páncreas, que medía 10 cm de diámetro. Se identificaron múltiples metástasis hepáticas hipodensas y homogéneas en ambos lóbulos hepáticos, la mayor en el lóbulo hepático izquierdo, de 3 cm. Habían múltiples adenopatías en cadenas ganglionares celíacas y periportales, homogéneas, formando conglomerados. No había ascitis ni metástasis fuera del abdomen (fig. 3).
Figura 3. Tomografía computarizada abdominal con contraste intravenoso, que muestra una voluminosa masa de densidad de partes blandas heterogénea con localización intraperitoneal entre el páncreas y el estómago (*). Metástasis hipodensa en el segmento hepático VI (flecha).
En la tabla 1 se exponen las principales características radiológicas de los 3 casos.
Tabla 1. Características radiológicas de los 3 tumores
| Caso 1 | Caso 2 | Caso 3 | |
| Masa dominante peritoneal | Sí, en el espacio retrovesical | Sí, ocupando gran parte de la cavidad peritoneal | Sí, localizada entre el estomago y el páncreas |
| Necrosis/calcificaciones intratumorales | Calcificaciones puntiformes | Ausentes | Áreas necróticas intratumorales |
| Adenopatias pélvicas/retroperitoneales | Celíacas y lumboaórticas | Lumboaórticas y en el hilio renal izquierdo | Celíacas y portales formando conglomerados |
| Metástasis | Hepáticas múltiples | Ausentes | Hepáticas múltiples |
| Ascitis | Ausente | Perihepática | Ausente |
| Obstrucción ureteral/intestinal | No | No | No |
| Engrosamiento peritoneal | Ausente | Ausente | Ausente |
Características histopatológicas
El diagnóstico histopatológico se llevó a cabo por biopsia percutánea con aguja fina guiada por TC de las masas peritoneales (2 casos) o de las metástasis hepáticas (1 caso). Ningún paciente fue sometido a cirugía.
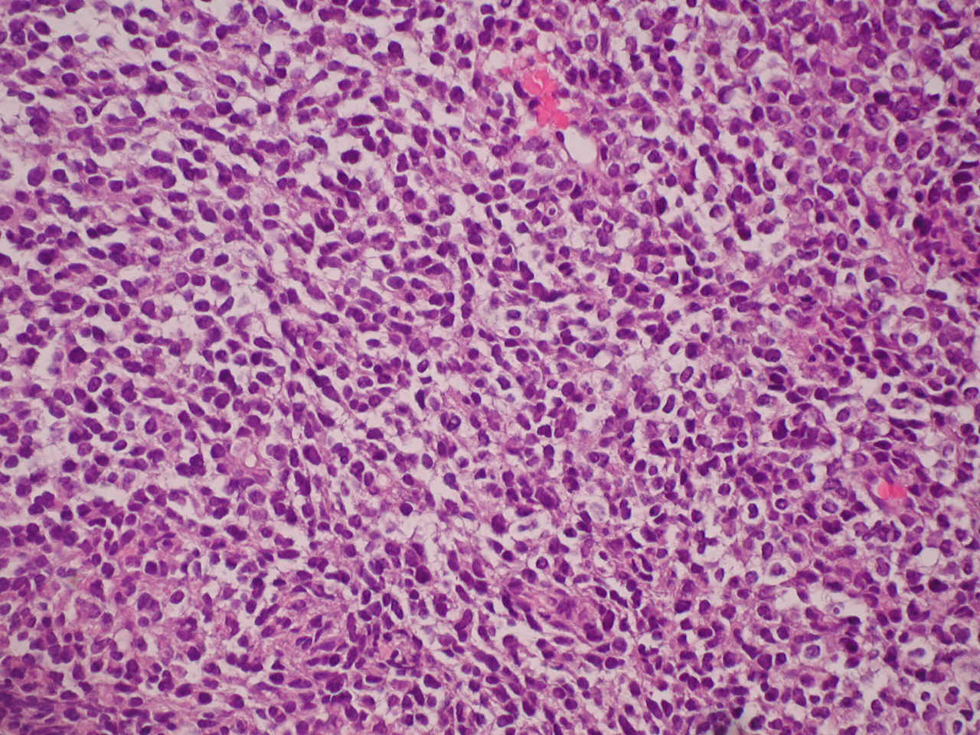
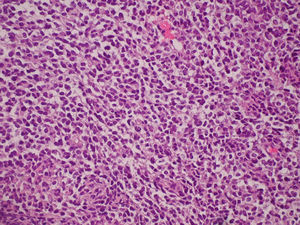
El análisis microscópico de las muestras identificó la presencia de nidos de células redondas, pequeñas y con núcleo hipercromático rodeados por una estroma fibrosa desmoplástica hipocelular (fig. 4).
Figura 4. Preparación histológica del caso n.° 2. Se observan nidos de células pequeñas, redondas y azules (HE, ×400).
El estudio inmunohistoquímico mostró la presencia de múltiples marcadores epiteliales (queratina, EMA 1/3 casos), mesenquimales (vimentina 2/3 casos, desmina 3/3 casos) y neurales (enolasa neuroespecífica 2/3 casos), así como CD 99 (2/3 casos) en las células tumorales, permitiendo la diferenciación del TDCPR de otras neoplasias de células redondas y pequeñas. En los análisis citogenéticos realizados se comprobó la translocación t (11;22) (p12;q13) en los 3 casos.
DiscusiónEl TDCPR es una neoplasia poco frecuente y muy agresiva, que asienta con más frecuencia en las membranas serosas del abdomen, y afecta mayoritariamente a adolescentes y adultos jóvenes varones2–6.
Aunque el TDCPR asienta predominantemente en el peritoneo, también puede encontrarse en otras membranas serosas, como la pleura y la serosa paratesticular2–6. Se han descrito algunos casos en otras localizaciones, como el pulmón, el riñón, el sistema nervioso central, el estómago, los senos paranasales y el ovario. En esta última localización es difícil de distinguir de una neoplasia primaria, por lo que es imprescindible la realización de una biopsia8.
Las manifestaciones clínicas del TDCPR abdominal son inespecíficas; las más frecuentes son el dolor abdominal vago y la presencia de una masa abdominal o pélvica palpable2,4,6. Debido a lo inespecífico de los síntomas, los pacientes suelen remitirse para estudio mediante ecografía y TC. Esta última es la que aporta más datos para el diagnóstico2,3.
En la TC el TDCPR se presenta típicamente como una o múltiples masas de contornos lobulados bien definidos, de densidad de partes blandas, heterogéneas, mostrando áreas hipodensas en relación con focos de necrosis y hemorragia, con localización intraperitoneal, sin aparente origen en un órgano abdominal2,4,6. Pueden observarse pequeñas calcificaciones en el interior de estos tumores o en sus metástasis3,4.
En la resonancia magnética el TDCPR se muestra como una o múltiples masas peritoneales con señal intermedia en las secuencias potenciadas en T1 y aumento de señal en las secuencias potenciadas en T2, con poca captación del contraste paramagnético intravenoso5. Las ventajas de esta técnica con relación a la TC son una mayor capacidad de detección de pequeñas metástasis peritoneales y de la invasión local de órganos abdominales, facilitando la estadificación.
En el momento del diagnóstico es frecuente que la enfermedad esté diseminada con múltiples implantes peritoneales, metástasis hepáticas y/o adenopatías abdominopélvicas2–6. Se ha descrito una mayor incidencia de metástasis hepáticas, adenopatías y ascitis en pacientes con masas en localización retrovesical3, lo que está en probable relación con los sitios de circulación del líquido peritoneal.
Las metástasis pulmonares, linfáticas extraabdominales y óseas son poco frecuentes. En estadios más avanzados puede aparecer ascitis, engrosamiento difuso del peritoneo o hidronefrosis secundaria a obstrucción tumoral3,4.
El diagnóstico diferencial radiológico debe hacerse con entidades que se presentan con múltiples masas peritoneales, incluyendo patología inflamatoria y tumoral. Se debe considerar el mesotelioma maligno, el tumor carcinoide gastrointestinal, la carcinomatosis peritoneal, la leiomiomatosis peritoneal, el tumor desmoide intraperitoneal, la linfomatosis peritoneal, los sarcomas peritoneales (histiocitoma fibroso maligno), la esplenosis, la amiloidosis y la tuberculosis peritoneal2–6.
Para el diagnóstico definitivo es siempre necesaria la confirmación histológica por biopsia, que puede hacerse guiada por TC.
La visualización en el estudio histológico de nidos de células tumorales pequeñas, redondas y con núcleo hipercromático envueltas en una estroma hipercromática hipocelular, así como la presencia de marcadores epiteliales (queratina, EMA), mesenquimales (vimentina, desmina) y neurales (enolasa neuroespecífica) y la presencia de alteraciones citogenéticas características, como la translocación t (11:22) (p12:q13) en las células tumorales, son diagnósticos de este tumor, permitiendo el diagnóstico diferencial con otros tumores de células pequeñas, redondas y azules4,9–13.
El tratamiento del TDCPR consiste en cirugía radical, con quimioterapia sistémica y radioterapia ampliada adyuvante2. El pronóstico es poco favorable, con recidivas frecuentes y elevada mortalidad. La supervivencia media es de 17 meses2,3.
En conclusión, la TC tiene un papel fundamental en el diagnóstico y estadificación tumorales. Aunque las características radiológicas del TDCPR no son específicas, en esta técnica de imagen suele aparecer como múltiples masas de partes blandas intraperitoneales, sin origen aparente en un órgano abdominal, y es frecuente la enfermedad diseminada en el momento del diagnóstico. El diagnóstico definitivo siempre será histológico, basado en unos hallazgos inmunohistoquímicos y citogenéticos característicos.
AgradecimientosA la Dra. Gema Medrano y al Dr. Luís Hernández del Servicio de Radiología del Hospital General Universitario Gregorio Marañón de Madrid por su amable colaboración en la revisión lingüística y de estilo.
Autoría
Sergio Eiriz Martínez ha contribuido decisivamente en la redacción del estudio, en la obtención de los datos y en su análisis e interpretación.
João Paulo Conceição e Silva ha intervenido en la revisión crítica del trabajo, haciendo aportaciones intelectuales relevantes.
Todos los autores han dado la aprobación final del manuscrito.
Declaración de conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Autor para correspondencia.
S. Eiriz Martínez
Dirección: eirizmartinez@gmail.com