Análisis de coste-efectividad de apixaban frente a dabigatrán en la prevención de la tromboembolia venosa (TEV) en la artroplastia total de rodilla (ATR) o cadera (ATC).
MétodosModelo con 2 periodos: posprevención de 90 días (corto plazo) y a 5 años (Markov). Se incluyeron las complicaciones de la TEV (trombosis venosa profunda distal y proximal, embolia pulmonar, sangrados y síndrome postrombótico). La eficacia comparada se obtuvo de un metaanálisis y los costes de fuentes españolas. Se aplicó una tasa de descuento del 3,5% anual para costes y beneficios.
ResultadosSegún el metaanálisis, el riesgo relativo (RR) de TEV o muerte, frente a enoxaparina, fue menor con apixaban que con dabigatrán en ATR (RR: 0,89; IC 95% 0,32-1,65 y RR: 1,35, IC 95% 0,19-3,39) y en ATC (RR: 0,35, IC 95% 0,05-2,51 y RR: 0,89, IC 95% 0,22-3,21, respectivamente). A corto plazo, con apixaban se obtendrían más años de vida (AVG) y más años de vida ajustados por calidad (AVAC) por paciente, tanto en ATR (0,2037; 0,1908) como en ATC (0,2417; 0,1921) que con dabigatrán (0,1818; 0,1901, y 0,2345; 0,1918, respectivamente). Habría menos costes por paciente con apixaban en ATR (-14 €) por lo que este sería el tratamiento dominante. En ATC se producirían costes adicionales (15 €) con un coste por AVG de 2.083 y de 50.000 € por AVAC ganado. A 5 años, apixaban fue más barato y más efectivo en ATR y en ATC.
ConclusionesSegún el presente estudio, apixaban es un tratamiento coste-efectivo en comparación con dabigatrán en la prevención de la TEV.
Cost-effectiveness analysis of apixaban vs. dabigatran in preventing venous thromboembolism (VTE) in total knee (TKR) or hip (THR) replacement.
MethodsModel with two periods: post-prophylaxis period of 90 days (short term) and 5 years (Markov). VTE complications (distal and proximal deep vein thrombosis, pulmonary embolism, bleeding and post-thrombotic syndrome) were included. The comparative efficacy was obtained from a meta-analysis, and the costs from Spanish sources. An annual discount rate of 3.5% for costs and benefits was applied.
ResultsAccording to the meta-analysis, the relative risk (RR) of VTE or death, compared with enoxaparin, was lower with apixaban than with dabigatran in TKR (RR 0.89, 95% CI 0.32 to 1.65 and RR 1.35, 95% CI, 0.19 to 3.39) and THR (RR 0.35, 95% CI, 0.05 to 2.51 and RR 0.89, 95% CI 0.22 to 3.21, respectively). In the short term, there were more life years (LYG) and more quality-adjusted life years (QALY) per patient in TKR (0.2037; 0.1908) and THR (0.2417; 0.1921) with apixaban than with dabigatran (0.1818; 0.1901 and 0.2345; 0.1918, respectively) were obtained. With apixaban lower costs per patient in TKR (-14 €) were generated, so it was the dominant treatment. Additional costs (15 €) could be incurred in THR, with a cost per LYG of 2,083 € and 50,000 € per QALY gained. In 5 years, apixaban was cheaper and more effective in both TKR and THR.
ConclusionsAccording to this study, apixaban was shown to be a cost-effective treatment compared with dabigatran for VTE prevention.
La trombosis venosa profunda (TVP) y la embolia pulmonar (EP) son 2 manifestaciones de la tromboembolia venosa (TEV)1. A pesar de que la mayoría de estas trombosis son asintomáticas, constituyen un serio peligro para la vida del paciente, siendo la primera causa de mortalidad hospitalaria prevenible2. Uno de los factores de riesgo más frecuentemente relacionado con la TEV es la cirugía mayor ortopédica, como la artroplastia total de rodilla (ATR) y la de cadera (ATC)3.
Hay una serie de razones objetivas que explican la necesidad de una prevención tromboembólica en la cirugía mayor ortopédica: la alta prevalencia de la TEV sin prevención (40-80% de TVP distal, 10-20% de TVP proximal, 4-10% de EP y 1-5% de EP mortal)4,5; la sintomatología de la TEV puede ser silente o asintomática, y su primera manifestación podría ser una EP mortal; las técnicas incruentas de diagnóstico (eco-Doppler) son poco sensibles en las TVP asintomáticas; y, finalmente, la TVP no tratada conlleva una gran morbilidad a largo plazo por síndrome postrombótico (SPT) y TVP recurrentes. Con la prevención con anticoagulantes, se consigue una reducción del riesgo de tromboembolia del 50 al 75%4.
En España, el 96% de la prevención de la TEV se realiza con heparinas de bajo peso molecular (HBPM), mayoritariamente con enoxaparina6, que se ha mostrado muy efectiva en esa indicación7. Pero las HBPM presentan 3 problemas importantes, como son el efecto acumulativo en la insuficiencia renal, la no disponibilidad de un antídoto plenamente eficaz y, aunque con menor frecuencia que las heparinas no fraccionadas, su implicación en la trombocitopenia inmunitaria inducida por heparina8,9. Por otra parte, la enoxaparina se administra mediante inyección subcutánea, lo que constituye un considerable inconveniente para el paciente, principalmente durante el tratamiento ambulatorio, siendo necesario formar a los pacientes en su autoadministración o, en su caso, debiendo ser administrada por una enfermera mediante visitas domiciliarias o en el centro de salud9. Finalmente, otro posible inconveniente de la enoxaparina se debe a la recomendación de administrar la primera inyección 12 h antes de la intervención quirúrgica10, lo que obligaría (en algunos casos, según la práctica clínica) al ingreso hospitalario del paciente con una considerable antelación.
Los nuevos anticoagulantes orales tienen ciertas ventajas de índole práctica sobre las HBPM, en la prevención de la TEV: se administran por vía oral, no deben administrarse antes de la intervención quirúrgica, no requieren monitorización rutinaria (coagulación o recuento de plaquetas) y no precisan ajustes de dosis7,8.
Apixaban y dabigatrán son 2 nuevos anticoagulantes orales. Apixaban es un inhibidor de la propagación de la cascada de la coagulación, que ejerce una inhibición directa sobre el factor Xa8 y está indicado en la prevención primaria de episodios tromboembólicos venosos en pacientes adultos sometidos a una ATR o una ATC. Dabigatrán es un inhibidor oral directo de la trombina8, con las mismas indicaciones que apixaban.
Según un reciente metaanálisis de comparaciones directas e indirectas, que compara los efectos de los diferentes fármacos indicados en la prevención de la TEV en pacientes a los que se les ha realizado ATR o ATC11,12, el riesgo (odds ratio, OR) de TEV totales y muertes por cualquier causa es mayor con dabigatrán que con apixaban, tanto en la ATR (OR: 1,72; IC 95% 1,22-2,42) como en la ATC (OR: 2,51; IC 95% 1,50-4,21). Respecto al riesgo de hemorragias, aunque es mayor con dabigatrán, no hubo diferencias estadísticamente significativas entre ambos tratamientos (OR: 1,16; IC 95% 0,86-1,56)11,12.
El coste anual sanitario de la TEV en España se estima en 66,5 millones de €. La EP supone el 67,7% del coste (45 millones de €) y la TVP, el 33,3% restante (21,4 millones de €). El 90% del coste se deriva de la atención hospitalaria3.
Las diferencias de eficacia observadas entre apixaban y dabigatrán, podrían tener un cierto impacto tanto sobre los resultados como sobre el gasto sanitario que se produce en la prevención de la TEV. En consecuencia, el presente estudio tiene como objetivo realizar un análisis de coste-efectividad de la prevención de la TEV con apixaban o dabigatrán en pacientes intervenidos de ATR o ATC.
MétodosEl análisis de coste-efectividad es un instrumento de especial relevancia para la toma de decisiones del Sistema Nacional de Salud. Se realizó este tipo de análisis con el objetivo de valorar la eficiencia de la introducción de apixaban para la prevención de la TEV en los pacientes intervenidos de ATR o ATC.
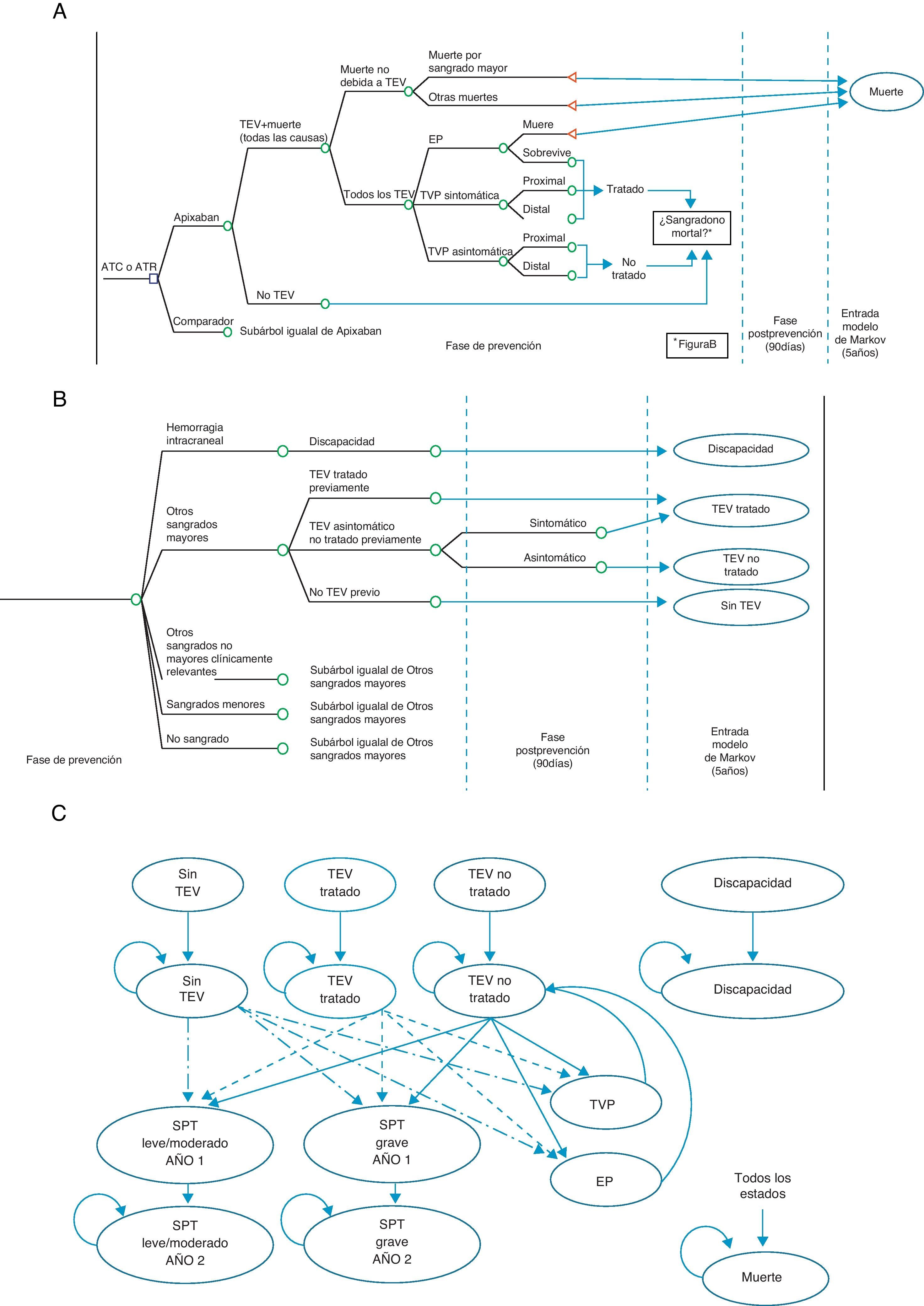
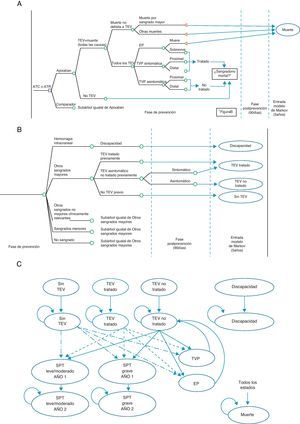
El modelo económico recoge la evolución de un paciente al que se realiza una ATR o una ATC12. Está integrado por un árbol de decisiones, que simula la evolución a corto plazo (fase de prevención y hasta 90 días después), y por un modelo de Markov13, que simula la evolución a 5 años (fig. 1). A corto plazo, se producen o no las TEV (TVP sintomática o asintomática, EP) y la mortalidad asociada o debida a otras causas (fig. 1 A), así como acontecimientos adversos como los posibles sangrados, mortales o no, que se clasifican como hemorragia intracraneal, otros sangrados mayores, sangrados menores clínicamente relevantes y sangrados menores (fig. 1 B). A 5 años, se consideran 9 estados de Markov (fig. 1 C): 1) sin TEV; 2) TEV no tratada (con TVP asintomática que no se convierte en sintomática en el corto plazo); 3) TEV tratada (con TVP sintomática o EP no mortal en el corto plazo); 4) discapacidad (ocasionada por una hemorragia intracraneal en el corto plazo); 5) SPT de leve a moderado (pacientes que entran en la fase a 5 años con TEV tratada o no, que sufren un episodio de SPT leve o moderado; este estado se subdivide en el primer año, debido a su mayor coste, y a partir del segundo año); 6) SPT grave; 7) TVP que se produce en el periodo de 5 años; 8) EP que se produce en el periodo de 5 años, y, finalmente, 9) muerte por todas las causas12.
Modelo económico de la prevención de la tromboembolia venosa. ATC: artroplastia total de cadera; ATR: artroplastia total de rodilla; EP: embolia pulmonar; SPT: síndrome postrombótico; TEV: tromboembolia venosa; TVP: trombosis venosa profunda. A) Corto plazo: TEV y muerte. B) Corto plazo: sangrados. C) Periodo de 5 años: proceso de Markov.
Las características de la cohorte simulada en el modelo se ajustaron a las de la población española, siempre que se dispuso de datos. Se consideró que un 26,2% de los pacientes intervenidos de ATR y un 36,1% de los intervenidos de ATC serían hombres14,15, siendo la edad de la cohorte al inicio de la simulación de 71,9 y 73,3 años, respectivamente14,15.
La eficacia de la prevención con apixaban y dabigatrán se estimó mediante un metaanálisis de comparaciones directas o, de no haberlas, indirectas (mixed treatment comparison, MTC)11 con el objetivo de proporcionar una evidencia sólida en ausencia de ensayos clínicos con comparaciones directas de los tratamientos16–18. El metaanálisis incluyó únicamente ensayos clínicos aleatorizados a doble ciego en pacientes intervenidos de ATC o ATR que recibieron prevención farmacológica de la TEV con alguno de los fármacos antes mencionados11. Para obtener todos los estudios disponibles con resultados de eficacia o de sangrados, se efectuó una búsqueda bibliográfica sistemática en bases de datos electrónicas (The Cochrane Library, Medline, Embase, CINAHL) y se revisaron las comunicaciones de los congresos de las sociedades médicas relacionadas con la enfermedad, hasta el 8 de julio de 201011. Una vez eliminadas las publicaciones duplicadas, se obtuvieron 1.809 publicaciones potencialmente relevantes e incluibles en el análisis. De estas, fueron excluidas 1.610 mediante la revisión de sus resúmenes. Se revisaron los artículos originales de las 199 publicaciones restantes y de otras 4 identificadas mediante una búsqueda manual, excluyéndose 164, por lo que finalmente se incluyeron 39 publicaciones con datos de 42 ensayos clínicos que cumplieron los criterios de inclusión previamente establecidos11.
Todas las variables de interés (mortalidad, incidencia de TEV, EP, TVP y sangrados) se midieron de manera dicotómica, realizándose los análisis por intención de tratar (respecto a todos los pacientes aleatorizados)11. Se hicieron análisis separados para ATC y ATR.
El metaanálisis se hizo mediante un modelo de efectos aleatorios utilizando el método de DerSimonian y Laird19 y estimando la heterogeneidad mediante el modelo de Mantel-Haenszel20. Las comparaciones indirectas entre apixaban y otro tratamiento a través de un comparador común (enoxaparina) se hizo mediante el método de Bucher21. El MTC se efectuó con simulaciones de Monte Carlo en cadenas de Markov bayesianas11, utilizando la versión 1.4.1. del programa WinBUGS22–24. El modelo calculó los riesgos relativos de TEV, EP, TVP y sangrados con los diferentes fármacos, en comparación con enoxaparina (tabla 1)11.
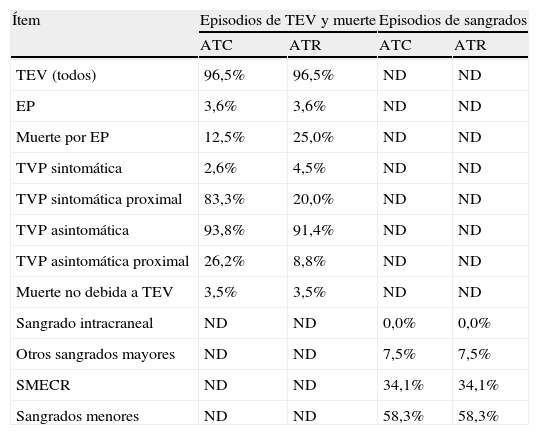
Probabilidades de los acontecimientos posteriores a la tromboembolia venosa o al sangrado, adoptadas en el modelo económico
| Ítem | Episodios de TEV y muerte | Episodios de sangrados | ||
| ATC | ATR | ATC | ATR | |
| TEV (todos) | 96,5% | 96,5% | ND | ND |
| EP | 3,6% | 3,6% | ND | ND |
| Muerte por EP | 12,5% | 25,0% | ND | ND |
| TVP sintomática | 2,6% | 4,5% | ND | ND |
| TVP sintomática proximal | 83,3% | 20,0% | ND | ND |
| TVP asintomática | 93,8% | 91,4% | ND | ND |
| TVP asintomática proximal | 26,2% | 8,8% | ND | ND |
| Muerte no debida a TEV | 3,5% | 3,5% | ND | ND |
| Sangrado intracraneal | ND | ND | 0,0% | 0,0% |
| Otros sangrados mayores | ND | ND | 7,5% | 7,5% |
| SMECR | ND | ND | 34,1% | 34,1% |
| Sangrados menores | ND | ND | 58,3% | 58,3% |
ATC: artroplastia total de cadera; ATR: artroplastia total de rodilla; EP: embolia pulmonar; ND: estos acontecimientos no se describieron en los ensayos clínicos incluidos en el metaanálisis; SMECR: sangrados menores clínicamente relevantes; TEV: tromboembolia venosa; TVP: trombosis venosa profunda.
La variable de eficacia considerada en el análisis económico fue la combinación de TVP sintomática y asintomática, EP no mortal y muerte por cualquier causa durante el tratamiento11,12,25. El modelo económico utilizó los resultados del metaanálisis, expresados como riesgos relativos (RR)11. Los RR de la combinación de TEV y muerte de apixaban y dabigatrán frente a un comparador común (enoxaparina, administrada con la pauta europea de 40mg/día) utilizados en el modelo fueron los siguientes11: a) en los pacientes intervenidos de ATR: 0,895 con apixaban y 1,354 con dabigatrán, y b) en los pacientes intervenidos de ATC: 0,359 con apixaban y 0,883 con dabigatrán.
La efectividad de los tratamientos se midió como años de vida ganados (AVG) y como años de vida ajustados por calidad (AVAC) ganados con el tratamiento más efectivo12. Los AVAC se estimaron, tanto a corto plazo como a 5 años, partiendo de la utilidad basal de la población general en hombres y mujeres (0,78 en una escala de 0 a 1, siendo 0 la muerte o el peor estado de salud imaginable y 1 la salud perfecta)26 y aplicando a esta la pérdida de utilidades asociada a cada episodio de TEV o de sangrado27–32: -0,08 para la EP y la TVP sintomática proximal o distal; -0,49 para la hemorragia intracraneal; -0,03 para otras hemorragias mayores; -0,00029 para el impacto anual del envejecimiento; -0,01 para el TEV tratado; -0,02 para el SPT leve a moderado en el primer año o en los años siguientes, y, finalmente, -0,07 para el SPT grave en el primer año o en los años siguientes. La mortalidad relacionada con la edad se obtuvo del Instituto Nacional de Estadística33. Las probabilidades de los acontecimientos posteriores a la TEV o a los sangrados se obtuvieron de los ensayos clínicos ADVANCE-234 y ADVANCE-335 (tabla 1).
Se consideraron tanto los costes de adquisición de los fármacos comparados (apixaban y dabigatrán) como los de las posibles complicaciones de la TEV a corto plazo y a 5 años (TVP distal y proximal, EP, sangrados intracraneales, otros sangrados mayores, menores clínicamente relevantes, sin relevancia clínica y SPT).
Se incluyeron las siguientes pautas de tratamiento, aprobadas en España para la tromboprevención26: 2,5mg dos veces al día por vía oral de apixaban (12 días en ATR y 35 días en ATC) y 220mg diarios por vía oral de dabigatrán (10 días en ATR y 31,5 días en ATC)12,36. Se consideró que el coste de los fármacos está incluido en el coste de la hospitalización, por lo que solo se incluyó como coste desagregado después del alta hospitalaria.
La duración media del ingreso hospitalario (7,8 días en la ATR y 11,5 días en la ATC) se obtuvo de las estancias medias de los grupos relacionados por el diagnóstico (GRD) 219 y 818, recogidos en las estadísticas del ministerio de Sanidad y Consumo37. El coste sanitario de la EP, la TVP distal y la TVP proximal se estimó mediante un panel Delphi compuesto por 3 expertos clínicos españoles (2 especialistas en medicina interna y un especialista en traumatología). Este panel se eligió atendiendo a los siguientes criterios: a) tener una experiencia contrastada en el manejo de la TEV, y b) cubrir las áreas clínicas involucradas en el manejo de la enfermedad (traumatología y/o medicina interna).
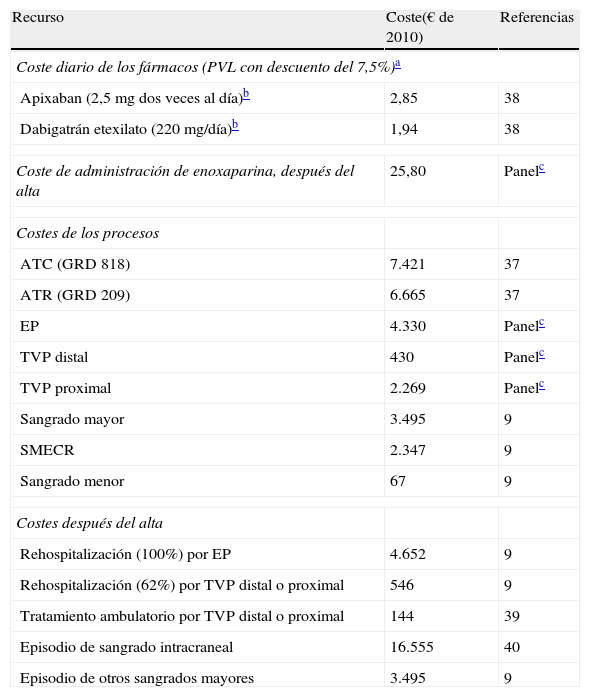
Los costes unitarios (medicamentos, administración de estos, ATR, ATC, EP, TVP, sangrados y rehospitalización) considerados en el modelo se resumen en la tabla 2 y provienen de fuentes españolas. Se consideró el precio de venta del laboratorio (PVL) de los medicamentos, con un descuento del 7,5%28. Los costes de los GRD de la ATR y la ATC, así como los de la TEV o los sangrados, se obtuvieron de otras fuentes españolas37–40.
Costes unitarios considerados en el modelo económico
| Recurso | Coste(€ de 2010) | Referencias |
| Coste diario de los fármacos (PVL con descuento del 7,5%)a | ||
| Apixaban (2,5mg dos veces al día)b | 2,85 | 38 |
| Dabigatrán etexilato (220 mg/día)b | 1,94 | 38 |
| Coste de administración de enoxaparina, después del alta | 25,80 | Panelc |
| Costes de los procesos | ||
| ATC (GRD 818) | 7.421 | 37 |
| ATR (GRD 209) | 6.665 | 37 |
| EP | 4.330 | Panelc |
| TVP distal | 430 | Panelc |
| TVP proximal | 2.269 | Panelc |
| Sangrado mayor | 3.495 | 9 |
| SMECR | 2.347 | 9 |
| Sangrado menor | 67 | 9 |
| Costes después del alta | ||
| Rehospitalización (100%) por EP | 4.652 | 9 |
| Rehospitalización (62%) por TVP distal o proximal | 546 | 9 |
| Tratamiento ambulatorio por TVP distal o proximal | 144 | 39 |
| Episodio de sangrado intracraneal | 16.555 | 40 |
| Episodio de otros sangrados mayores | 3.495 | 9 |
ATC: artroplastia total de cadera; ATR: artroplastia total de rodilla; EP: embolia pulmonar; SMECR: sangrados menores clínicamente relevantes; PVL: precio de venta del laboratorio; TVP: trombosis venosa profunda.
Se analizó el coste-efectividad incremental de apixaban frente a dabigatrán respecto a 2 horizontes temporales (a corto plazo, hasta 90 días después de la artroplastia, y hasta 5 años). Todos los costes (€ de 2010) se descontaron anualmente un 3,5%.
Se efectuaron análisis separados para pacientes intervenidos de ATR y ATC. Se analizó un caso base, con los valores medios de todos los parámetros, a corto plazo y a 5 años. También se realizaron varios análisis de sensibilidad simples univariantes para las siguientes variables: a) costes de los episodios de TEV y sangrados (± 20%); b) pérdida de utilidades asociada a los episodios de TEV o de sangrados (± 10%), y, por último, c) tasa de descuento anual para costes, años de vida y utilidades (0 y 6%). Los 2 últimos análisis solo se efectuaron para el análisis a corto plazo, ya que los efectos de la pérdida de utilidades y de los descuentos solo se aprecian o tienen sentido, respectivamente, en periodos prolongados.
Finalmente, se efectuó un análisis probabilístico (simulación de Monte Carlo, 2.000 simulaciones) del modelo de Markov, que incluyó las variables siguientes: a) eficacia de los tratamientos; b) riesgo de TEV en el periodo de 5 años; c) costes, y d) utilidades. Las distribuciones estadísticas empleadas para las distintas variables fueron las siguientes: a) β para la eficacia de los tratamientos, las probabilidades de transición y las utilidades a corto plazo, y b) γ para los costes y la pérdida de utilidades en el periodo de 5 años12.
Los resultados de la comparación de apixaban y dabigatrán se presentan como sigue: a) número de episodios obtenidos con uno y otro fármaco; b) diferencia de costes por paciente; c) diferencia de utilidades por paciente, y d) ratio coste-efectividad incremental (RCEI, coste de ganar un año de vida y coste de ganar un AVAC con el tratamiento más eficaz).
ResultadosEpisodios evitados de tromboembolia venosaEl metaanálisis mostró una mayor eficacia de apixaban en la prevención de la TEV. El riesgo relativo (RR) de presentar una TEV o una muerte por todas las causas, en comparación con enoxaparina, fue menor con apixaban que con dabigatrán tanto en ATR (RR: 0,89, IC 95% 0,32-1,65, y RR: 1,35, IC 95% 0,19-3,39) como en ATC (RR: 0,35, IC 95% 0,05-2,51, y RR: 0,89, IC 95% 0,22-3,21, respectivamente)11,12.
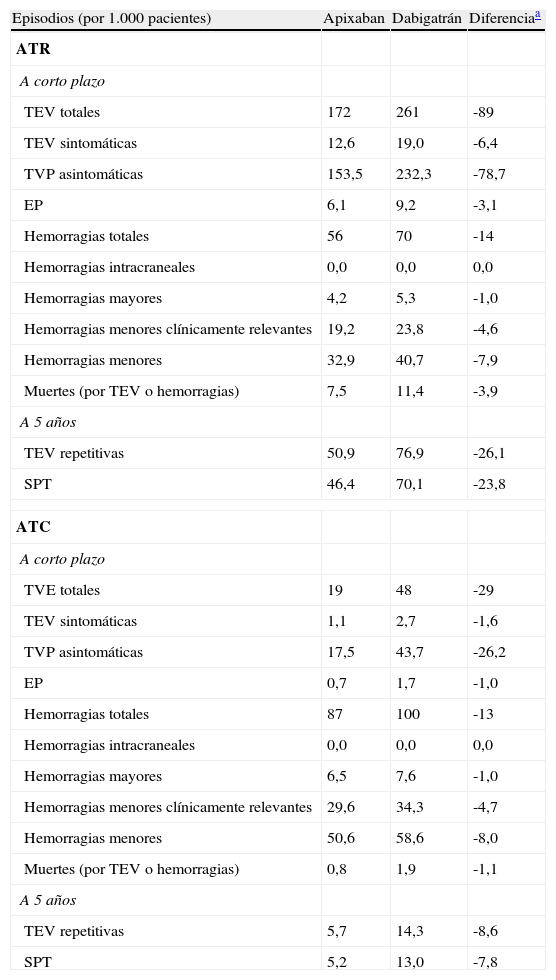
A corto plazo, en una cohorte de 1.000 pacientes intervenidos de ATR, con apixaban se evitarían 89 episodios de TEV en comparación con dabigatrán. Los casos evitados en pacientes intervenidos de ATC serían 29. Al cabo de 5 años, se evitarían 26 TEV repetitivas y 24 casos de SPT en ATR; 9 y 8 casos, respectivamente, en ATC (tabla 3).
Episodios esperados en una cohorte de 1.000 pacientes intervenidos de artroplastia total de cadera y artroplastia total de rodilla y tratados preventivamente con apixaban o dabigatrán a corto plazo y 5 años
| Episodios (por 1.000 pacientes) | Apixaban | Dabigatrán | Diferenciaa |
| ATR | |||
| A corto plazo | |||
| TEV totales | 172 | 261 | -89 |
| TEV sintomáticas | 12,6 | 19,0 | -6,4 |
| TVP asintomáticas | 153,5 | 232,3 | -78,7 |
| EP | 6,1 | 9,2 | -3,1 |
| Hemorragias totales | 56 | 70 | -14 |
| Hemorragias intracraneales | 0,0 | 0,0 | 0,0 |
| Hemorragias mayores | 4,2 | 5,3 | -1,0 |
| Hemorragias menores clínicamente relevantes | 19,2 | 23,8 | -4,6 |
| Hemorragias menores | 32,9 | 40,7 | -7,9 |
| Muertes (por TEV o hemorragias) | 7,5 | 11,4 | -3,9 |
| A 5 años | |||
| TEV repetitivas | 50,9 | 76,9 | -26,1 |
| SPT | 46,4 | 70,1 | -23,8 |
| ATC | |||
| A corto plazo | |||
| TVE totales | 19 | 48 | -29 |
| TEV sintomáticas | 1,1 | 2,7 | -1,6 |
| TVP asintomáticas | 17,5 | 43,7 | -26,2 |
| EP | 0,7 | 1,7 | -1,0 |
| Hemorragias totales | 87 | 100 | -13 |
| Hemorragias intracraneales | 0,0 | 0,0 | 0,0 |
| Hemorragias mayores | 6,5 | 7,6 | -1,0 |
| Hemorragias menores clínicamente relevantes | 29,6 | 34,3 | -4,7 |
| Hemorragias menores | 50,6 | 58,6 | -8,0 |
| Muertes (por TEV o hemorragias) | 0,8 | 1,9 | -1,1 |
| A 5 años | |||
| TEV repetitivas | 5,7 | 14,3 | -8,6 |
| SPT | 5,2 | 13,0 | -7,8 |
ATC: artroplastia total de cadera; ATR: artroplastia total de rodilla; EP: embolia pulmonar; SPT: síndrome postrombótico; TEV: tromboembolia venosa; TVP: trombosis venosa profunda.
Según el metaanálisis, en comparación con enoxaparina, el RR de sangrados fue menor con apixaban (RR: 0,81; IC 95% 0,48-1,31) que con dabigatrán (RR: 1,00; IC 95% 0,44-2,49)11,12.
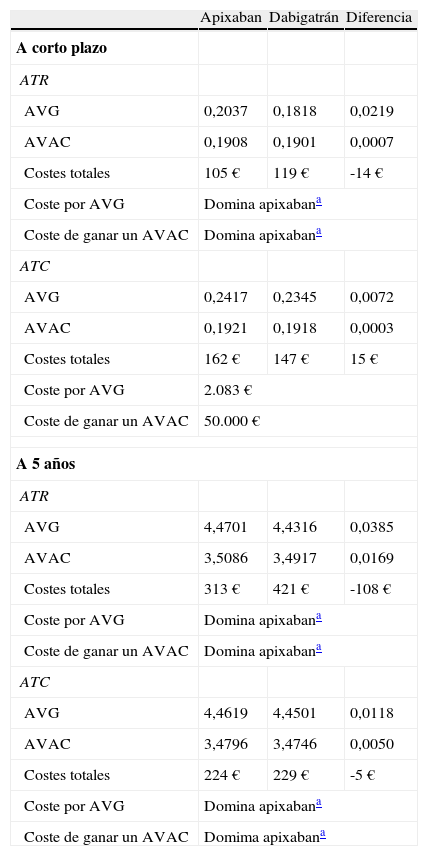
Coste-efectividadEn consecuencia, en el análisis a corto plazo, con apixaban se obtendrían más años de vida (AVG) y más años de vida ajustados por calidad (AVAC) por paciente, tanto en ATR (0,2037; 0,1908) como en ATC (0,2417; 0,1921) que con dabigatrán (0,1818; 0,1901 y 0,2345; 0,1918, respectivamente). Con apixaban se generarían menos costes por paciente que con dabigatrán en ATR (-14 €) por lo que apixaban sería el tratamiento dominante en ATR. En ATC se producirían costes adicionales (15 €) con un coste por AVG de 2.083 € y de 50.000 € por AVAC ganado (tabla 4). En el análisis a 5 años apixaban fue dominante tanto en ATR como en ATC (tabla 4).
Resultados del análisis de coste-efectividad de apixaban frente a dabigatrán a corto plazo y a 5 años
| Apixaban | Dabigatrán | Diferencia | |
| A corto plazo | |||
| ATR | |||
| AVG | 0,2037 | 0,1818 | 0,0219 |
| AVAC | 0,1908 | 0,1901 | 0,0007 |
| Costes totales | 105 € | 119 € | -14 € |
| Coste por AVG | Domina apixabana | ||
| Coste de ganar un AVAC | Domina apixabana | ||
| ATC | |||
| AVG | 0,2417 | 0,2345 | 0,0072 |
| AVAC | 0,1921 | 0,1918 | 0,0003 |
| Costes totales | 162 € | 147 € | 15 € |
| Coste por AVG | 2.083 € | ||
| Coste de ganar un AVAC | 50.000 € | ||
| A 5 años | |||
| ATR | |||
| AVG | 4,4701 | 4,4316 | 0,0385 |
| AVAC | 3,5086 | 3,4917 | 0,0169 |
| Costes totales | 313 € | 421 € | -108 € |
| Coste por AVG | Domina apixabana | ||
| Coste de ganar un AVAC | Domina apixabana | ||
| ATC | |||
| AVG | 4,4619 | 4,4501 | 0,0118 |
| AVAC | 3,4796 | 3,4746 | 0,0050 |
| Costes totales | 224 € | 229 € | -5 € |
| Coste por AVG | Domina apixabana | ||
| Coste de ganar un AVAC | Domima apixabana | ||
ATC: artroplastia total de cadera; ATR: artroplastia total de rodilla; AVAC: año de vida ajustado por calidad; AVG: año de vida ganado.
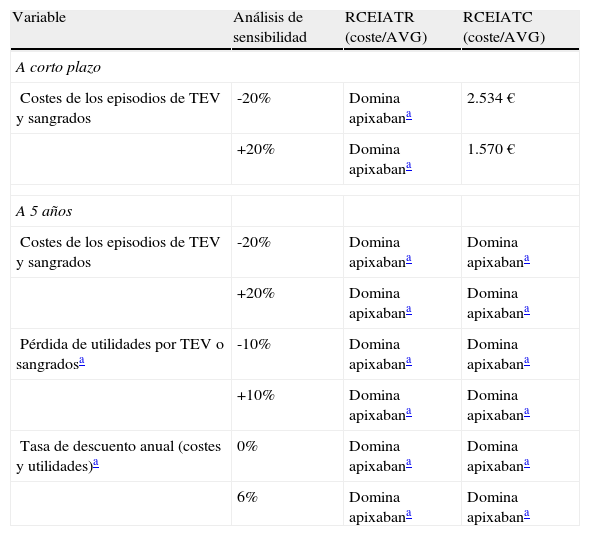
Los análisis de sensibilidad confirmaron la estabilidad del caso base. Como se observa en la tabla 5, apixaban fue el tratamiento dominante (más eficaz, con menos costes) en todos los análisis efectuados en un periodo de 5 años, pero no a corto plazo: cuando se modificó (± 20%) el coste de los episodios de TEV y sangrados, el coste de ganar un año de vida osciló entre los 1.570 y los 2.534 € (muy por debajo de la disponibilidad a pagar de 30.000 € por AVAC ganado, considerada como aceptable en España)41.
Resultados del análisis de coste-efectividad de apixaban frente a dabigatrán. Análisis de sensibilidad simples univariantes a corto plazo y a 5 años
| Variable | Análisis de sensibilidad | RCEIATR (coste/AVG) | RCEIATC (coste/AVG) |
| A corto plazo | |||
| Costes de los episodios de TEV y sangrados | -20% | Domina apixabana | 2.534 € |
| +20% | Domina apixabana | 1.570 € | |
| A 5 años | |||
| Costes de los episodios de TEV y sangrados | -20% | Domina apixabana | Domina apixabana |
| +20% | Domina apixabana | Domina apixabana | |
| Pérdida de utilidades por TEV o sangradosa | -10% | Domina apixabana | Domina apixabana |
| +10% | Domina apixabana | Domina apixabana | |
| Tasa de descuento anual (costes y utilidades)a | 0% | Domina apixabana | Domina apixabana |
| 6% | Domina apixabana | Domina apixabana | |
ATC: artroplastia total de cadera; ATR: artroplastia total de rodilla; AVG: año de vida ganado; RCEI: ratio coste efectividad incremental.
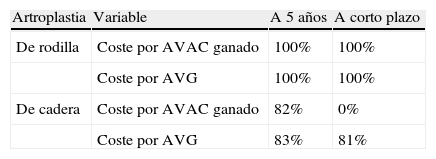
El análisis de sensibilidad probabilístico en ATR confirmó que apixaban es coste-efectivo en el 100% de los análisis realizados tanto a corto plazo como a 5 años, para una disponibilidad a pagar de 30.000 € (tabla 6).
Resultados del análisis de sensibilidad probabilístico: probabilidad de que apixaban sea coste-efectivo frente a dabigatrán para una disponibilidad a pagar de 30.000 € por año de vida ajustado por la calidad de vida ganado o por año de vida ganado
| Artroplastia | Variable | A 5 años | A corto plazo |
| De rodilla | Coste por AVAC ganado | 100% | 100% |
| Coste por AVG | 100% | 100% | |
| De cadera | Coste por AVAC ganado | 82% | 0% |
| Coste por AVG | 83% | 81% |
AVAC: año de vida ajustado por calidad; AVG: año de vida ganado.
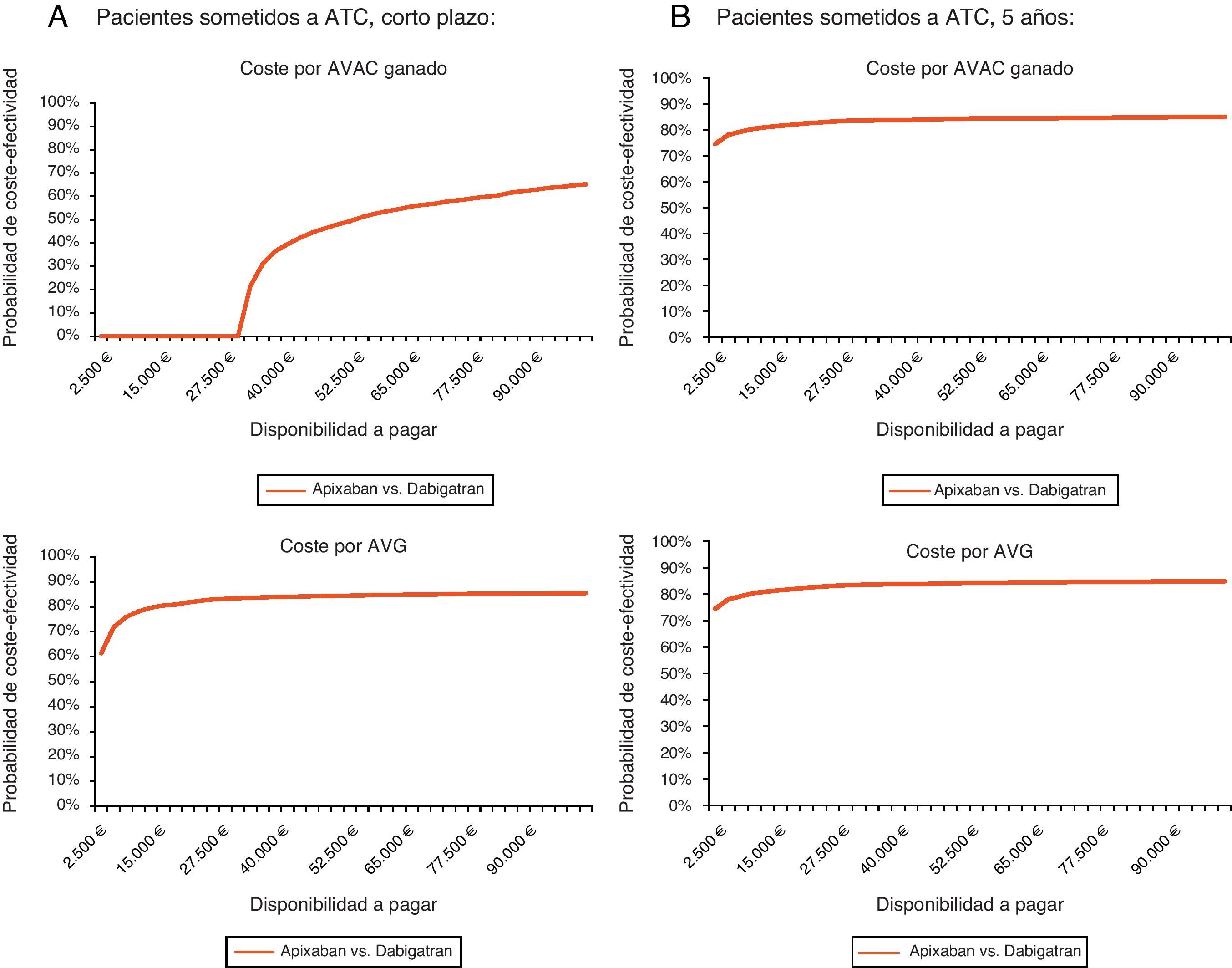
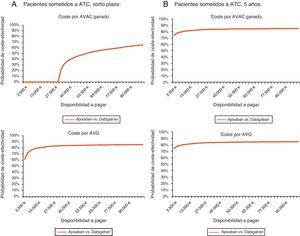
Por lo que se refiere a la ATC y para la misma disponibilidad a pagar, apixaban no sería coste-efectivo a corto plazo (coste por AVAC ganado) y sí lo sería tanto a corto plazo (probabilidad del 81% para el coste por AVG) como a 5 años (probabilidades del 82 y del 83% para el coste por AVAC ganado y por AVG, respectivamente) (tabla 6, fig. 2).
Curva de aceptabilidad en artroplastia total de cadera (ATC): probabilidad de que apixaban sea coste-efectivo frente a dabigatrán para diferentes disponibilidades a pagar. A) A corto plazo. A corto plazo, para una disponibilidad a pagar de 30.000 € por AVAC ganado y por AVG, apixaban no sería coste-efectivo y sí lo sería con una probabilidad del 81%, respectivamente. B) Periodo de 5 años. En el periodo de 5 años, para una disponibilidad a pagar de 30.000 € por AVAC ganado y por AVG, apixaban sería coste-efectivo con una probabilidad del 82 y del 83%, respectivamente. AVAC: año de vida ajustado por la calidad de vida; AVG: año de vida ganado.
De acuerdo con el presente modelo, apixaban es un tratamiento coste-efectivo en comparación con dabigatrán en la prevención de la TEV, tanto en ATR como en ATC.
En la valoración de los resultados del estudio debemos tener en cuenta tanto las posibles limitaciones como las consistencias del mismo. En primer lugar, debe recordarse que se trata de un modelo teórico que es, por definición, una simulación simplificada de la realidad. Respecto a las diferencias de efectividad entre apixaban y dabigatrán, éstas son mayores en los análisis a 5 años que a corto plazo (90 días). En el análisis a 5 años, cada paciente ganaría 0,0385 años de vida y 0,0169 AVAC en ATR, así como 0,0118 años de vida y 0,0050 AVAC en ATC. Sin embargo, en el corto plazo con apixaban se ganarían frente a dabigatrán 0,0219 años de vida y 0,0007 AVAC en ATR, así como 0,0072 años de vida y 0,0003 AVAC en ATC. La diferencia mínima clínicamente relevante en la utilidad de 2 tratamientos o intervenciones sanitarias observada con los instrumentos EQ-5D, HUI2, HUI3 y SF-6D es de 0,07442, 0,03043, 0,03043 y 0,03344, respectivamente45. En el caso de que las pequeñas diferencias en AVAC obtenidas a corto plazo, favorables a apixaban, no se considerasen clínicamente relevantes, se concluiría que el tratamiento con apixaban genera menos costes en los pacientes con ATR tanto a corto plazo como a 5 años, con un ahorro por paciente de 14 € y 108 €, respectivamente. Por lo que se refiere a la indicación en ATC, en el periodo de 5 años también se produciría un ahorro con apixaban (5 € por paciente); sin embargo, a corto plazo habría un coste adicional de 15 € en cada paciente tratado con apixaban.
Respecto a lo indicado anteriormente, debemos tener en cuenta que el enfoque más realista de este estudio es el que incluye los acontecimientos a 5 años ligados a las ATR o ATC, del mismo modo que en la mayoría de los análisis económicos españoles previamente publicados9,46–48. En el presente estudio, se modelizó una fase crónica de 5 años para una edad de 72 o 73 años en el momento de la intervención, al igual que en un estudio español publicado en el año 200648. Sin embargo, en el trabajo de Monreal et al.9 se consideró un periodo de seguimiento mucho más prolongado, que abarcó los 60 años posteriores a la intervención ortopédica, para pacientes de 40 años de edad. En otros estudios españoles, la edad media de los pacientes que recibieron cirugía fue de 62 a 70 años y se simuló un seguimiento posterior de 15 a 19 años de acuerdo con su esperanza de vida46,47. La duración del seguimiento de la cohorte en el presente estudio fue considerablemente menor, más restrictiva, que la aplicada en la mayoría de los modelos españoles previamente publicados. En el caso de un seguimiento de la cohorte de 15 a 20 años, los AVAC ganados en cada paciente tratado con apixaban en lugar de dabigatrán serían de 0,037-0,041 AVAC en ATR y de 0,010-0,011 AVAC en ATC.
Estos resultados para un paciente individual deben ponerse, no obstante, en el contexto de la población que se beneficiaría de las diferencias de eficacia entre apixaban y dabigatrán. Según el metaanálisis de Cohen et al.11,12,25, la OR de TEV totales y muertes por cualquier causa es mayor con dabigatrán que con apixaban, tanto en ATR (OR: 1,72; IC 95% 1,22-2,42) como en ATC (OR: 2,51; IC 95% 1,50-4,21), con diferencias estadísticamente significativas. Esto daría lugar a que, tal y como se indica en la tabla 3, en una cohorte de 1.000 pacientes intervenidos de ATR se evitaran 89 episodios de TEV a corto plazo y 26 episodios de TEV repetitivos a 5 años en el caso de que fueran tratados con apixaban. En una cohorte de 1.000 pacientes intervenidos de ATC con apixaban se evitarían 29 y 9 episodios, respectivamente. Por otra parte, en el periodo de 5 años con apixaban se evitarían 24 episodios de SPT en los pacientes con ATR y 4 episodios en los pacientes con ATC.
Aunque los resultados publicados del metaanálisis de Cohen et al.11 se presentan únicamente como OR, también se calcularon como RR, que es como se utilizaron en el análisis económico. A este respecto, debe indicarse que los resultados obtenidos en OR fueron muy aproximados a los RR, dado que la frecuencia de los acontecimientos tromboembólicos fue muy inferior al 20%49. Por ejemplo, en el estudio ADVANCE-335 la frecuencia de TEV fue del 0,8% con apixaban y del 2,5% con enoxaparina.
Se dispone de otros metaanálisis, recientemente publicados, que comparan la eficacia de apixaban, dabigatrán y enoxaparina en la prevención de la TEV. Según el metaanálisis de Huang et al.50 con apixaban se reduce el riesgo de TVP frente a enoxaparina (OR: 0,47; IC 95% 0,27 a 0,82) en la ATR. De acuerdo con el metaanálisis de comparaciones indirectas de Gómez-Outes et al.51, en pacientes intervenidos tanto de ATR como de ATC, no habría diferencias en el riesgo de TEV entre apixaban y dabigatrán (RR: 1,16; IC 95% 0,31 a 4,28). Esta discrepancia con el metaanálisis de Cohen et al.11 podría deberse a que, a diferencia de este, no se analizaron separadamente los resultados de ATR y ATC sino de manera conjunta, y el resultado clínico analizado no fue el compuesto de TEV totales y muertes sino solamente las TEV sintomáticas11,51. En el metaanálisis de Nieto et al.52, en comparación con 40mg/día de enoxaparina, apixaban mostró superioridad en la reducción de la TEV (RR: 0,63; IC 95% 0,36 a 1,01), siendo la eficacia de dabigatrán similar a la de enoxaparina (RR: 1,02; IC 95% 0,86 a 1,20).
Respecto al riesgo de sangrados, los nuevos metaanálisis indican que apixaban se asocia con una menor tasa de hemorragias que enoxaparina (OR: 0,55; IC 95% 0,32 a 0,96)50, menos hemorragias clínicamente relevantes que dabigatrán (RR: 0,73; IC 95% 0,57 a 0,94)51 y el menor riesgo de sangrados de los nuevos anticoagulantes orales (RR: 0,81; IC 95% 0,64 a 1,01)52.
Como fortaleza del modelo, cabe destacar que los datos de eficacia y de efectos adversos se han obtenido del metaanálisis de ensayos clínicos aleatorizados antes mencionado, lo que proporciona un alto nivel de evidencia a ese respecto. Además, los costes de los diferentes episodios de la TEV y de los sangrados relacionados con la tromboprofilaxis se obtuvieron en su totalidad de fuentes españolas y fueron contrastados con un panel de expertos clínicos.
El presente análisis económico, adaptado al sistema sanitario español, está basado en un modelo previamente publicado para el sistema sanitario de Reino Unido53. Los resultados obtenidos en ese país indican que apixaban es un tratamiento más eficiente que dabigatrán en la prevención de la TEV en los pacientes intervenidos de cirugía mayor ortopédica. Con apixaban se producirían menos TEV y menos hemorragias que con dabigatrán y se ganarían más AVAC y más años de vida al cabo de 5 años de seguimiento.
No se dispone de ningún otro análisis del coste-efectividad de apixaban realizado en España. No obstante, la metodología utilizada en este estudio es muy similar a la empleada en los estudios españoles de coste-efectividad de la prevención de la TEV anteriormente publicados9,46–48.
De acuerdo con las premisas del estudio, puede concluirse que la introducción de apixaban podría reducir la tasa de TEV en comparación con dabigatrán, reduciéndose asimismo el gasto del SNS en la tromboprofilaxis de los pacientes intervenidos de cirugía mayor ortopédica.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEste estudio ha sido financiado conjuntamente por Pfizer S.L.U. y Bristol-Myers Squibb S.A. Marina de Salas es empleada de Pfizer S.L.U, y Lourdes Betegón es empleada Bristol-Myers Squibb S.A. El resto de los autores no tiene ningún conflicto de intereses.
Los autores del estudio quieren agradecer al Dr. Emilio J. Alegre del Rey, del Servicio de Farmacia del Hospital Universitario Puerto Real de Cádiz, la revisión del manuscrito y sus útiles comentarios.