Comparar a eficácia de duas concentrações de heparina para a desobstrução por coágulo do cateter venoso central de inserção periférica (CCIP) neonatal in vitro.
MétodosEstudo experimental in vitro quantitativo que usou 76 CCIPs neonatais de tamanho 2 French coagulados in vitro. Os cateteres foram divididos em dois grupos com 38 CCIPs cada. Ambos os grupos receberam infusão de heparina de baixo peso molecular, com dose de 25UI/mL no Grupo I e de 50UI/mL no Grupo II. Os cateteres de ambos os grupos foram submetidos à técnica de pressão negativa com cinco, 15 e 30 minutos e com quatro horas e testou‐se sua permeabilidade. Usou‐se a análise de sobrevivência para verificar o desfecho dos grupos conforme os intervalos de tempo.
ResultadosA comparação dos dois grupos no intervalo de tempo de cinco minutos mostrou um número maior de desobstrução de cateteres no Grupo II (57,9%) em relação ao grupo 1 (21,1%). A análise de Kaplan Meier indicou menor tempo para desobstrução dos cateteres quando a heparina em maior concentração (50UI/mL) foi usada (p<0,001).
ConclusõesO uso de heparina de baixo peso molecular na concentração de 50UI/mL foi mais eficaz na restauração da permeabilidade de CCIPs neonatais ocluídos in vitro por coágulo e situou‐se tal concentração dentro da margem de segurança indicada na literatura científica.
To compare the efficacy of two concentrations of heparin to clear the lumen of in vitro clotted neonatal peripherally inserted central catheters (PICCs).
MethodsThis is an in vitro, experimental quantitative study of 76 neonatal 2.0Fr PICCs coagulated in vitro. The catheters were divided into two groups of 38 PICCs each. In both groups an infusion of low molecular weight heparin was administered with a dose of 25IU/mL for Group 1 and 50IU/mL for Group 2. The negative pressure technique was applied to the catheters of both groups at 5, 15 and 30minutes and at 4hours to test their permeability. Kaplan‐Meier survival analysis was used to verify the outcome of the groups according to time intervals.
ResultsThe comparison between both groups in the first five minutes showed that more catheters from Group 2 were cleared compared to Group 1 (57.9 vs. 21.1%, respectively). Kaplan‐Meier survival analysis showed that less time was needed to clear catheters treated with 50IU/mL of heparin (p<0.001).
ConclusionsThe use of low‐molecular weight heparin at a concentration of 50IU/mL was more effective in restoring the permeability of neonatal PICCs occluded in vitro by a clot, and the use of this concentration is within the safety margin indicated by scientific literature.
O cateter central de inserção periférica (CCIP), originado do termo peripherally inserted central catheter (PICC), tem se mostrado seguro para a infusão de soluções intravenosas em neonatos.1,2 Apresenta menor incidência de complicações quando comparado com outros cateteres venosos centrais e fortalece a tese de ser um dispositivo seguro e útil em situações em que o acesso seja limitado e difícil.3
Eventualmente, complicações podem ocorrer e antecipar a remoção não programada do cateter.2 Dentre as principais complicações estão a obstrução, com índices que podem variar de 11%‐50%, e a ruptura do cateter.2‐8 A obstrução pode ser causada por formação de trombos, má posição da ponta do cateter ou precipitação de drogas.9,10
Essas complicações podem ser prevenidas e minimizadas por meio de intervenções específicas. Muitas são as práticas relacionadas à manutenção da permeabilidade do CCIP, embora existam poucas evidências cientificas sobre o melhor agente trombolítico e sua concentração segura e eficaz que possam respaldar uma única prática.11‐13
Apesar de a heparina ser usada quase que universalmente na prática clínica, seus benefícios não foram firmemente estabelecidos, bem como a dose eficaz e segura dessa substância para cateteres venosos e arteriais na neonatologia.12,13 A falta de evidência científica e a não padronização por meio de protocolos levam ao uso de concentrações diversas, muitas vezes abusivas, e outras com subdosagens, que podem resultar em efeitos colaterais desconhecidos ou o insucesso na desobstrução.14
Nesse contexto, o objetivo deste estudo foi comparar duas concentrações diferentes de Heparina Sódica de Baixo Peso Molecular (HSBPM) quanto à eficácia para restaurar a permeabilidade do CCIP neonatal obstruído por coágulo em laboratório.
MétodoEstudo experimental in vitro, de abordagem quantitativa, desenvolvido no laboratório de análises de um hospital universitário no município de Londrina de julho a dezembro de 2013. A amostra do estudo foi composta por 76 CCIP usados nos recém‐nascidos hospitalizados na Unidade de Terapia Intensiva Neonatal (UTIN). Nessa unidade a indicação dos CCIP é para administração de antibióticos por tempo superior a sete dias, início de drogas vasoativas, necessidade de velocidade de infusão de glicose (VIG) superior a sete e nutrição parenteral e, portanto, todos os cateteres usados neste estudo receberam todos ou alguma dessas terapêuticas. Os cateteres foram obtidos na UTIN do referido hospital, após a sua retirada dos neonatos devido ao término do tratamento. Depois da retirada, os cateteres foram lavados imediatamente com seringa de 10mL com água destilada por no mínimo duas vezes, até que estivessem limpos e testados quanto à sua integridade e permeabilidade, e foram armazenados em embalagem plástica original do próprio cateter. Esses cateteres permaneceram armazenados em um armário longe da luz ou umidade por aproximadamente seis meses, tempo necessário para a obtenção de um número de cateteres suficientes para o início do estudo.
Os critérios para inclusão dos cateteres foram ter comprimento mínimo 11cm, calibre 2,0Fr, poliuretano, única marca e ter permanecido no recém‐nascido por um tempo mínimo de uma semana e máximo de 30 dias. Os critérios de exclusão adotados foram, na retirada do cateter, não ter sido possível manter a permeabilidade. Para isso, foram testados por meio da infusão de água destilada com o uso de uma seringa de 10mL em sua extremidade distal e visualizada a saída dessa água na extremidade proximal. Além disso, foram excluídos os cateteres não armazenados corretamente após sua remoção.
O calculo amostral foi obtido por meio de um arquivo que contém o registro de todos os cateteres usados nos recém‐nascidos na referida UTIN. Constam nome do paciente, marca, lote, calibre, motivo da instalação do cateter, comprimento do cateter introduzido e motivo da retirada. Foram usados os dados dos últimos seis meses do ano anterior à coleta, ou seja, de julho a dezembro 2012. Foram sacados nesse período 68 CCIPs devido ao término de tratamento e/ou a obstruções. Considerando erro amostral de 5%, nível de confiança 95% e diferença de desobstrução entre os Grupos I e II de 50%, verificou‐se a necessidade de 36 cateteres em cada grupo.
Na maioria dos neonatos, o comprimento do CCIP introduzido varia de 8‐28cm, a depender do comprimento do recém‐nascido e da localização da punção. Por isso, para o estudo, os CCIP foram cortados com lâmina de bisturi na marcação específica de cada cateter na indicação de 11cm. Após, os 76 CCIPs foram divididos em dois grupos com 38 cateteres aleatoriamente, independentemente do tempo de armazenamento, visto já terem sido testados quanto a sua permeabilidade, e foram devidamente identificados em Grupos I e II seguidos de sequência numérica de 1 a 38. A escolha aleatória ocorreu por sorteio. Para tanto, o pesquisador colocou sobre a bancada os 76 cateteres e solicitou que o profissional bioquímico escolhesse 38, denominados de Grupo I, e os 38 que permaneceram na bancada foram denominados de Grupo II. Esses CCIPs foram coagulados in vitro com sangue humano obtido por punção venosa de dois colaboradores saudáveis, que aceitaram fazer a doação por meio de consentimento escrito, ambos com tipagem sanguínea O Rh+ e com hematócrito 39,2% (doador 1) e 42,2% (doador 2) e plaquetas 410.000 (doador 1) e 400.000 (doador 2), ou seja, dentro dos valores normais. Imediatamente após a coleta feita com escalpe n° 23 e seringa de 10mL, o sangue foi transferido para seringas de 1mL e foi introduzido nos cateteres que estavam dispostos sobre um campo cirúrgico com um volume de 0,04mL. Esse volume se fez necessário, pois se adotou a obstrução de 10cm de cateter, que corresponde a aproximadamente 0,04mL da capacidade do seu volume interno (priming). O preenchimento dos cateteres foi feito por dois profissionais com habilidade e destreza comprovadas, treinados previamente para evitar a coagulação do sangue fora do cateter. O tempo médio entre a retirada do sangue e o preenchimento de cada cateter foi de dois minutos. Logo depois do preenchimento dos cateteres com sangue, a extremidade distal foi conectada a uma torneira de três vias devidamente fechada e a extremidade proximal foi ocluída por uma pinça Kelly, a fim de impedir o escape de sangue ou a secagem pelo ar. A técnica adotada nesta pesquisa para fazer a coagulação dos cateteres in vitro e para os testes de permeabilidade foi baseada em outro estudo que teve como objetivo testar uma nova técnica para restaurar a permeabilidade de CCIP ocluídos por coágulos em laboratório.15
A seguir, cada cateter foi transferido e submerso em cuba com 100mL de solução salina aquecida a 37°C, com o objetivo de simular a temperatura corpórea do neonato. Cada cuba continha 14 cateteres de um mesmo grupo. As cubas com os cateteres foram colocadas em banho‐maria (Quimis Aparelhos Científicos Ltda.) e manteve‐se a solução entre 36,5‐7°C, com rigoroso controle térmico por meio de termômetros acoplados à solução. Os cateteres ficaram imersos por seis horas e, posteriormente, removidos e cortados na marcação de 10cm para eliminar qualquer dano ao cateter que pudesse decorrer do pinçamento prévio. Foi então testada sua permeabilidade por meio da infusão de 1mL de solução salina, considerando‐se como completamente obstruídos aqueles em que não foi possível a infusão da solução salina e o sangue não pôde ser aspirado pela seringa. Em seguida os cateteres foram colocados novamente no aparelho de banho‐maria para o início da infusão das duas concentrações de heparina. A sala usada no laboratório ficou restrita para a feitura do procedimento, não foi permitida a entrada de outros profissionais que não fossem os executores. A temperatura da sala foi mantida entre 22‐24°C e o tempo escolhido de armazenamento dos cateteres na solução salina teve como objetivo não inferir nos resultados.
Foi usada a HSBPM (5000UI/mL) pelo seu mecanismo de ação, por ser a mais usada nas unidades de cuidados intensivos neonatais e pelo menor custo. HSBPM exerce ação anticoagulante por ativação da antitrombina III, que tem a sua atividade acelerada em até 1.000 vezes no sentido de inibir os fatores da coagulação IIa e Xa e, em menor proporção, IXa, XIa e XIIa. A ligação à antitrombina III depende da presença de uma única sequência de pentassacárides contida em cerca de um terço das moléculas de heparina. Os dois terços restantes têm mínima atividade anticoagulante nas concentrações terapêuticas usuais. Essa sequência de pentassacárides confere alta afinidade da HSBPM pela antitrombina III. Qualquer molécula de heparina ou HSBPM que contenha o pentassacáride pode inibir a ação Xa simplesmente pela ativação da AT III. Para inativar a trombina (IIa), a HSBPM tem de se ligar à antitrombina III e ao fator IIa simultaneamente e formar um complexo ternário, que só ocorre com cadeias mais longas, com pelo menos 18 sacárides. Além da redução do efeito anti‐IIa, a HSBPM apresenta outras vantagens farmacocinéticas, tais como: menor ligação com proteínas plasmáticas e proteínas de fase aguda; menor ligação com os macrófagos e as células endoteliais, menor ligação com as plaquetas e o fator plaquetário 4 (PF4) e menor ligação com os osteoblastos. Tais diferenças proporcionam vantagens terapêuticas, como resposta anticoagulante mais previsível, meia‐vida plasmática mais longa, maior biodisponibilidade, redução da trombocitopenia induzida pela heparina e menor osteopenia.16
O Grupo I recebeu a infusão de HSBPM na concentração de 25UI/mL diluída em solução salina em uma seringa de 10mL; o Grupo II recebeu a mesma HSBPM na concentração de 50UI/mL também diluída em solução salina. A escolha do grupo a qual o cateter pertencia ocorreu às cegas para o pesquisador. No momento do experimento participaram dois enfermeiros, um ficou responsável pela desobstrução dos cateteres do Grupo I e outro pelos do Grupo II, ambos foram treinados para a execução do experimento, tinham um tempo de três minutos para aplicar a técnica, o qual era controlado pelo bioquímico por meio de cronômetro digital. O bioquímico era responsável pela entrega das duas seringas: uma com HSBPM com 25UI/mL e outra com 50UI/mL e somente ele tinha conhecimento das concentrações usadas em cada cateter. Segundo a literatura, as doses intermitentes de heparina recomendadas são de 50‐100UI/kg/dose a cada quatro horas, sem provocar alterações significativas na coagulação,17 o que não foi ultrapassado neste estudo, visto que a concentração máxima de heparina foi de 50UI/mL a cada quatro horas no grupo com maior concentração. A opção por concentração inferior à encontrada em literatura científica ocorreu com o objetivo de manter uma dose segura e possibilitar que doses menores possam ser usadas na população neonatal.
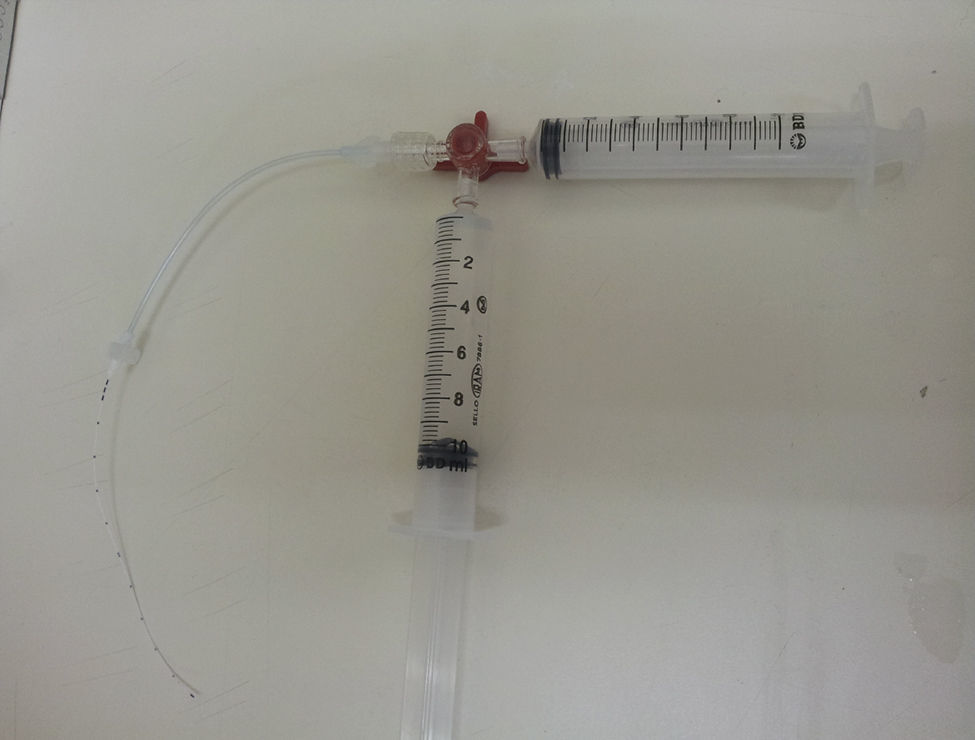
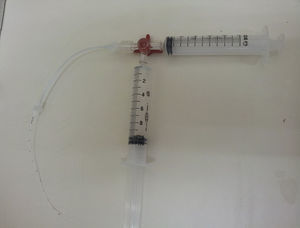
Para as tentativas de desobstrução, foi usada a técnica de pressão negativa18 conforme demonstrado na figura 1. Essa técnica consiste no uso de uma torneira de três vias conectada ao cateter com duas seringas de 10mL conectadas à torneira, uma com 10mLda solução de heparina conforme o grupo e a outra, vazia. O conteúdo do cateter foi aspirado até a graduação de 10mL pela seringa vazia, formou um vácuo em seu interior e fechou‐se essa via logo após. A via da torneira com solução foi então aberta, com o objetivo de preencher o cateter apenas com o volume aspirado pelo vácuo. O sistema ficou bloqueado dessa forma, foi repetida por quatro vezes a técnica de pressão negativa com cinco, 15, 30 minutos e quatro horas. A mesma solução de heparina foi usada nos quatro intervalos. Sempre antes da infusão da solução, fazia‐se a tentativa de aspirar o coágulo e avaliar a permeabilidade dos cateteres e, quando desobstruídos, não se faziam os testes subsequentes.
No fim de cada tentativa, em ambos os grupos, a solução de heparina foi totalmente aspirada, na tentativa de aspirar juntamente o coágulo, a permeabilidade foi novamente testada por meio da infusão de 1mL de solução salina em uma seringa de 10mL. A permeabilidade do cateter foi considerada restaurada quando houve a capacidade de aspiração do coágulo e foi possível a infusão de 1mL de solução salina da extremidade distal para a proximal do cateter. Para garantir que a permeabilidade havia sido restabelecida, a solução salina era desprezada em um cálice com graduação precisa de 0,1mL para que os pesquisadores pudessem verificar se todo o volume infundido havia sido devolvido no cálice. Para garantir que a velocidade de infusão entre os enfermeiros fosse a mais precisa possível, eles usaram um cronômetro digital manipulado pelo bioquímico que controlava o tempo de um minuto para a infusão de solução salina. O operador responsável pelo teste de permeabilidade foram os dois enfermeiros responsáveis pelos grupos I e II, que determinavam se o cateter havia restabelecido sua permeabilidade, e o bioquímico era o segundo a confirmar e anotar o resultado.
Caso a permeabilidade do cateter não fosse atingida, seria permitida a repetição das doses de heparina nas duas concentrações estudadas mais cinco vezes, com novas diluições a cada quatro horas, devido ao tempo de estabilidade da heparina. O tempo máximo para a desobstrução do cateter seria de 24 horas após a infusão da primeira concentração de heparina. Esses intervalos de tempo foram adotados de acordo com relato informal dos profissionais de enfermagem da referida UTIN, que já usam como protocolo para a desobstrução de cateteres a concentração de heparina 50UI/mL.
Os resultados obtidos foram anotados em um instrumento previamente estruturado e digitados em uma planilha no Microsoft Office Excel 2007 e posteriormente foi feita análise de sobrevivência com a Curva de Kaplan‐Meier e foram aplicados os testes de Log Rank (Mantel‐Cox), Breslow (Generalized Wilcoxon) e Tarone‐Ware para verificar o desenvolvimento dos grupos conforme os intervalos de tempo. O intervalo de confiança considerado foi de 95%.
A pesquisa foi feita mediante parecer favorável do Comitê de Ética em Pesquisa da Universidade Estadual de Londrina, sob n° CEP/UEL: 066/2013. CAAE: 13890613.8.0000.5231 e foi conduzida de acordo com os padrões éticos exigidos.
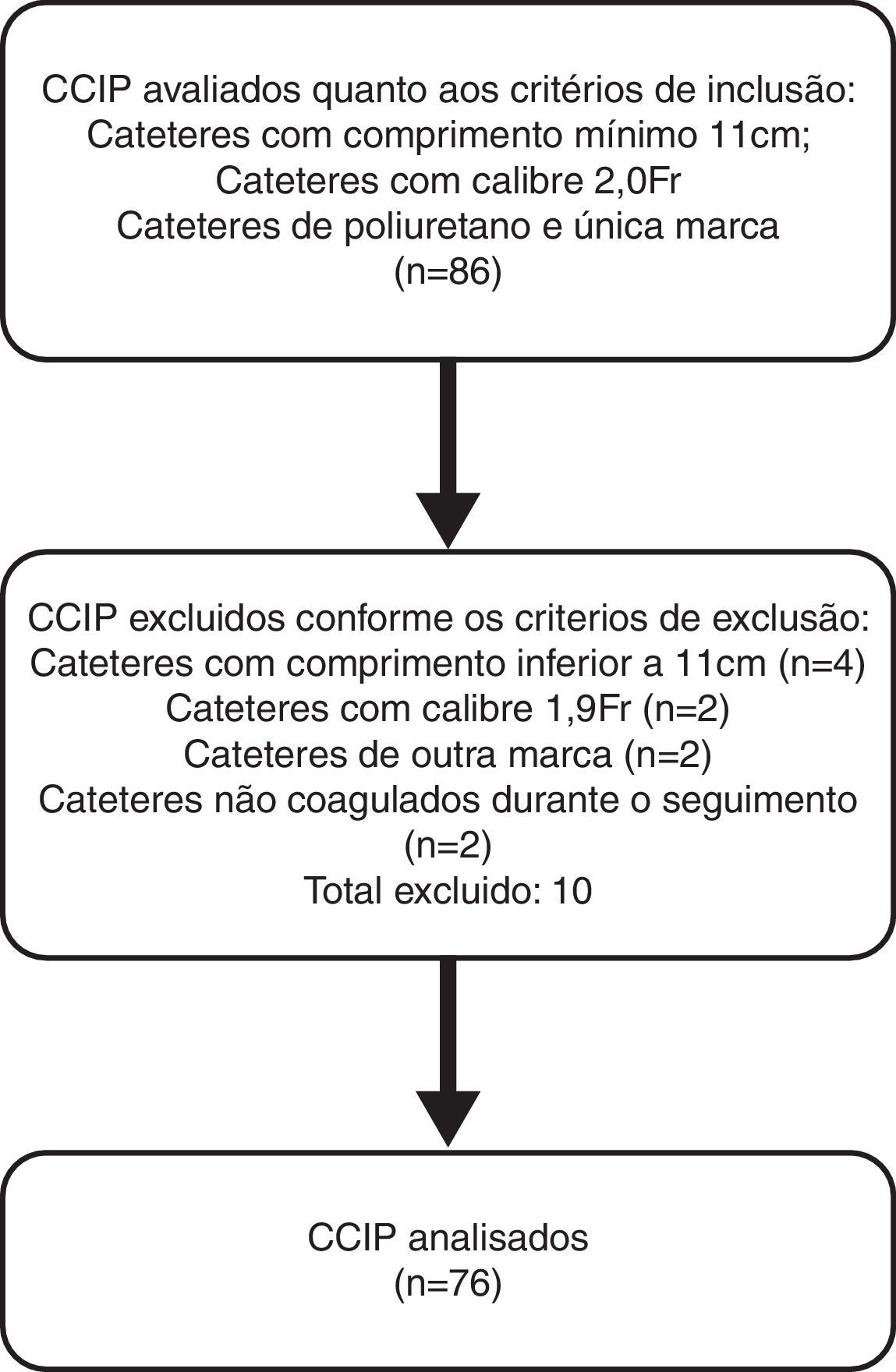
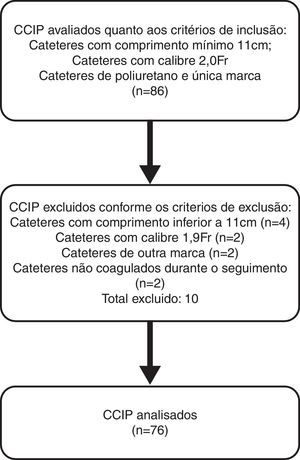
ResultadosDurante o período de coleta de dados acompanhou‐se diariamente a retirada dos CCIPs na UTIN com a finalidade de identificar os cateteres elegíveis para inclusão na amostra do presente estudo, conforme figura 2. Por fim 76 compuseram a amostra. Dessa forma, os grupos ficaram compostos por 38 cateteres cada, todos pertencentes à mesma marca com 2.0Fr e 11cm de comprimento, com tempo médio de uso de 30 dias. Desses, 35 (46%) tiveram uso exclusivo de Nutrição Parenteral Parcial (NPP) e 41 (54%) de infusão de antibióticos e soluções de glicose e eletrólitos.
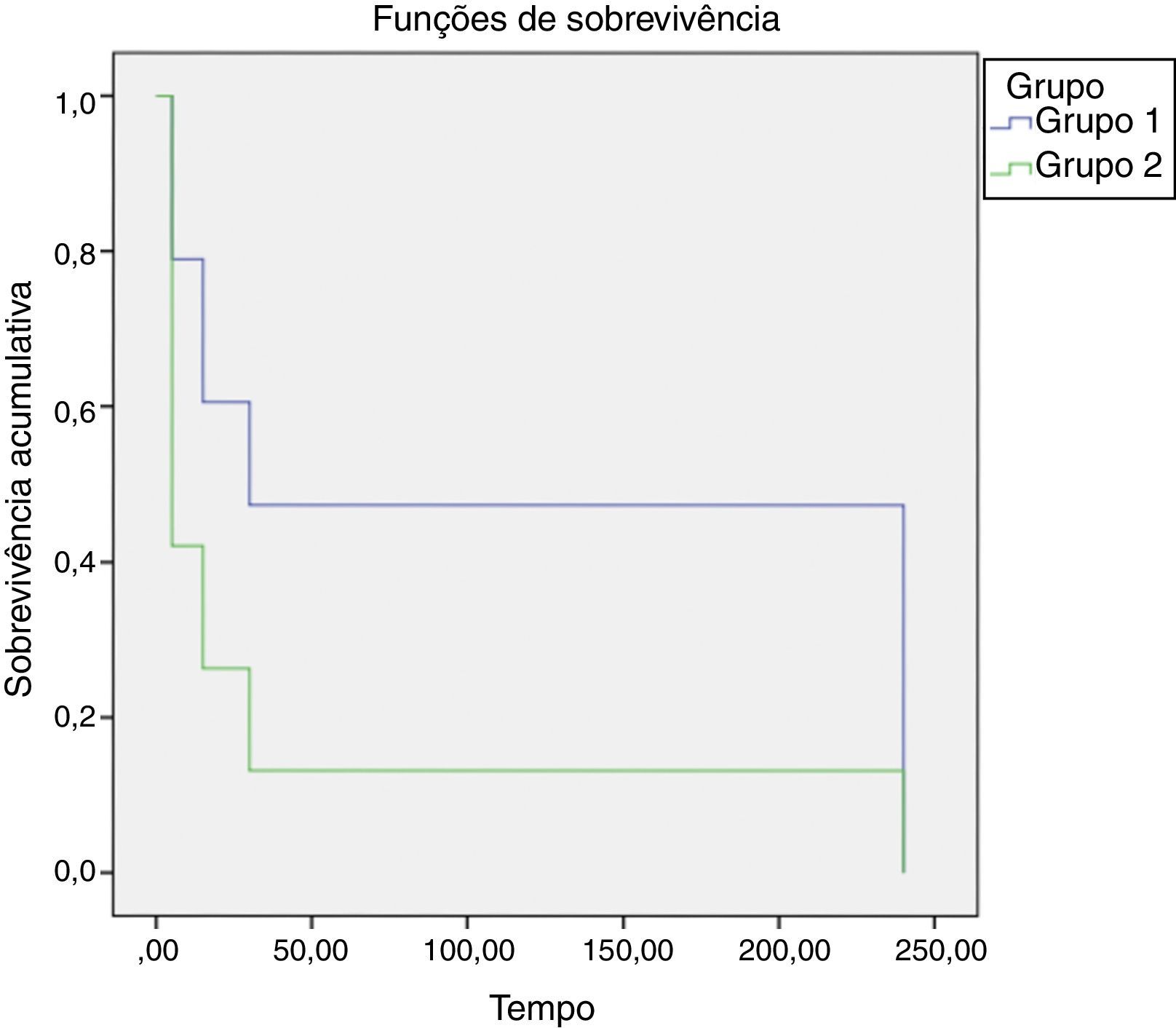
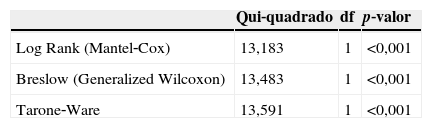
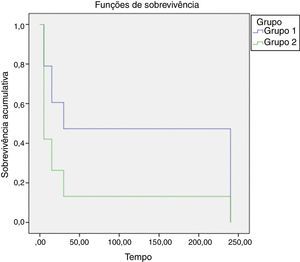
O comportamento dos grupos conforme os intervalos de tempo estão apresentados na figura 3 que demonstra haver diferença significativa entre as diferentes concentrações, com menor tempo para desobstrução dos cateteres no Grupo II, com maior concentração de heparina. O teste de igualdade de distribuições de sobrevivência para os diferentes níveis de grupo (tabela 1) encontrou p<0,001, confirmando que o Grupo II, com maior concentração, houve desobstrução dos cateteres em um menor tempo.
Esses dados foram reafirmados na tabela 2, a qual indica que, na comparação entre os resultados dos dois grupos no intervalo de tempo de cinco minutos, ocorreu um número maior de desobstrução de cateteres no Grupo II (57,9%) em relação ao Grupo I (21,1%), enquanto no intervalo de tempo de quatro horas ocorreu o inverso, o que permite afirmar que os cateteres do Grupo II, que receberam concentração de heparina de baixo peso molecular de 50UI/mL, foram desobstruídos de maneira mais rápida do que os do o Grupo I, que foram tratados com 25UI/mL de heparina de baixo peso molecular.
Desobstrução dos CCIPs preenchidos por coágulos em laboratório de acordo com duas concentrações de heparina, segundo os quatro tempos do estudo. Londrina, 2013
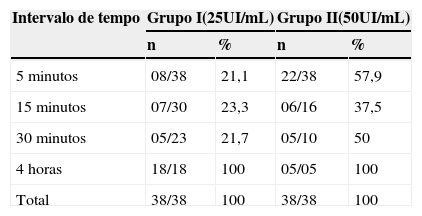
| Intervalo de tempo | Grupo I(25UI/mL) | Grupo II(50UI/mL) | ||
|---|---|---|---|---|
| n | % | n | % | |
| 5 minutos | 08/38 | 21,1 | 22/38 | 57,9 |
| 15 minutos | 07/30 | 23,3 | 06/16 | 37,5 |
| 30 minutos | 05/23 | 21,7 | 05/10 | 50 |
| 4 horas | 18/18 | 100 | 05/05 | 100 |
| Total | 38/38 | 100 | 38/38 | 100 |
A obstrução intraluminal do cateter central é mais frequente nos pacientes em uso de CCIP, pois, como sua inserção ocorre através de vasos periféricos que têm menor calibre à introdução, o cateter ocupa a maior parte do diâmetro luminal e dificulta o fluxo sanguíneo e possibilita a formação de coágulos e a consequente obstrução. Outro fator responsável pela formação de trombos é o inadequado posicionamento do cateter, que pode levar sua ponta a encostar‐se à parede do vaso e possibilitar sua obstrução. Além disso, o membro escolhido pode contribuir para essa complicação, pois a movimentação dos membros pode ocasionar o deslocamento do cateter e favorecer a formação de coágulos e sua obstrução.19 Dessa maneira, existe a opção por fazer manobras de desobstrução por coágulos, visto que esses podem ocorrer mesmo com a adequada manipulação e manutenção do cateter, ao contrário da obstrução por formação de cristais por medicamentos incompatíveis e de baixa solubilidade, os quais são considerados eventos iatrogênicos pela assistência de enfermagem.
Para simular o que ocorre in vivo, optou‐se, no processo de coagulação dos cateteres, sua imersão em solução aquecida entre 36‐37°C com o objetivo de mimetizar a temperatura corpórea do neonato e estipulou‐se um tempo de seis horas para depois testar sua permeabilidade. Esse tempo foi estipulado levando em consideração uma das recomendações mais difundidas para a manutenção da permeabilidade dos CCIP: a feitura de flush no cateter em intervalos estabelecidos, geralmente a cada oito horas.20 Considerando o processo de trabalho da enfermagem, adota‐se usualmente a lavagem do cateter a cada turno. Por esse motivo, na prática da enfermagem, é um cuidado importante fazer a lavagem do cateter sempre antes e após a administração de medicamentos quando o intervalo dessas medicações é superior a seis‐oito horas. Ou seja, a equipe deve ser capaz de identificar e iniciar a manobra de desobstrução de um cateter ocluído o mais precocemente possível após o início do evento.
Ao considerar que o conceito de obstrução também inclui o fluxo lentificado através do cateter,9 questiona‐se se o procedimento de desobstrução por meio da técnica de pressão negativa com concentração de heparina também deveria ser usado nesses casos. É sabido que o cateter pode romper, caso sejam usadas seringas com volumes inferiores a 10mL, pois quanto menor o volume da seringa, maior será a pressão exercida no cateter. Por isso, neste estudo foram usadas, na técnica de pressão negativa, somente seringas de 10mL e, no momento do procedimento, todos os êmbolos eram tracionados até a marcação de 10mL. Dessa forma, controlou‐se a pressão exercida e garantiu‐se que todos os cateteres receberam a mesma pressão durante o processo de desobstrução.
O mecanismo de ação da heparina depende da ligação de um cofator do plasma, a antitrombina, que inativa a trombina (fator IIa) e o fator de coagulação X ativado e previne a conversão da protrombina em trombina e do fibrinogênio em fibrina.21 As vantagens HSBPM incluem: não interferência da dieta ou medicamentos sobre seu mecanismo de ação; monitoração mínima; quando comparada à heparina não fracionada, não apresenta maior risco de sangramento e diminui a incidência de trombocitopenia induzida por heparina quando em uso isolado.22
As concentrações de heparina escolhidas (25 e 50UI/mL) para comparação foram baseadas na prática clínica e científica quanto à sua eficácia para desobstrução e a dose máxima segura a fim de evitar eventos adversos e outras complicações que poderiam ocorrer durante o seu uso no neonato.17 Dentre os estudos que usaram diversas concentrações de heparina contínua ou intermitente nos neonatos, não foram encontrados eventos adversos.12,13,23 Este estudo optou por considerar a concentração mais baixa de heparina considerada segura, visto que foi feito in vitro e não havia como verificar a ocorrência de eventos adversos nos recém‐nascidos.
Entretanto, este estudo testou duas concentrações diferentes de heparina associada à técnica de pressão negativa. Foram encontradas na literatura duas técnicas de desobstrução de cateteres, a de pressão negativa,18 descrita anteriormente, e a de procedimento operacional padrão (POP).15 Na técnica POP o êmbolo da seringa é puxado para trás e lançado em intervalos regulares sob o cateter, envia uma onda de choque que desloca o coágulo do lúmen do cateter e permite que o trombo seja aspirado.15 Pelo fato de essa última técnica ter sido testada em cateteres de 3,0 e 4,0Fr, não usados na neonatologia, optou‐se por usar a técnica de pressão negativa. Vale ressaltar que,em todos os procedimentos feitos com os cateteres foram usadas apenas seringas de 10mL, conforme recomendações da literatura, pois seringas de menor volume exercem maior pressão intravascular e aumentam a ocorrência de eventos adversos, como, por exemplo, a ruptura do cateter.4,24 Tentativas de desobstrução de cateteres feitas por meio de pressão positiva, mesmo com a infusão de agentes trombolíticos, podem causar rompimento dos mesmos devido à alta resistência. Por esse motivo, foi usada a técnica de pressão negativa, a qual propicia o contato do agente trombolítico com o coágulo sem promover a pressão positiva, o que facilita a remoção do coágulo.13
É preciso enfatizar que no Grupo II a heparina em concentração superior foi mais eficaz na desobstrução dos cateteres, visto terem sido desobstruídos em um intervalo de tempo mais curto, em comparação com o Grupo I. Talvez as intervenções feitas tenham sido resultantes da associação da heparina com a técnica de pressão negativa. Entretanto, não é possível fazer essa afirmativa, uma vez que o estudo não tinha como objetivo testar a técnica de pressão negativa para a desobstrução dos cateteres. Porém, durante o experimento foram mantidos os critérios referentes à técnica de pressão negativa, tais como usar apenas seringa de 10mL considerada mais segura; tentativa de aspiração do coágulo pela seringa vazia antes da infusão da solução; manutenção do cateter obstruído banhado pela solução por pelo menos cinco minutos antes da tentativa de aspiração, um tempo mínimo para que a heparina possa agir e desprender o coágulo do lúmen do cateter. Cabe ressaltar que o coágulo não é diluído pela ação da heparina, e sim possibilita o seu desprendimento da parede. Por isso a importância de aspirá‐lo a fim de evitar nova obstrução ou a introdução do coágulo na corrente sanguínea do neonato.
O fato de os coágulos de todos os cateteres terem sido aspirados para a seringa antes do teste de permeabilidade não permite afirmar a eficácia e segurança do experimento. A técnica de pressão negativa associada às concentrações de heparina testadas permitiu restabelecer a permeabilidade do cateter, visualizar a aspiração do trombo e impedir que esse fosse introduzido para a corrente sanguínea, o que pode levar a sérias consequências para o neonato. Apesar de não ser visualizado coágulo após a infusão de solução salina durante o teste de permeabilidade, não é possível afirmar a total ausência de coágulos, pois essa solução não foi filtrada e analisada microscopicamente.
É necessário lembrar que as medidas para manter a permeabilidade dos cateteres venosos centrais são essenciais para a adequada terapia intravenosa. Porém, eventualmente, quando a obstrução do cateter ocorre, são identificados muitos prejuízos aos recém‐nascidos, como a necessidade de repetidas punções, o que é doloroso e pode ser difícil, a interrupção da terapêutica medicamentosa ou da nutrição parenteral contínua, a maior manipulação do cateter com predisposição à infecção e o maior estresse para o neonato e a equipe.
Cabe enfatizar que apesar de o estudo procurar simular as condições clínicas do cateter dentro do vaso do neonato, o mesmo ocorreu em laboratório e apresentou algumas limitações relacionadas à ausência de fatores presentes na corrente sanguínea, como o turbilhonamento de sangue dentro dos vasos. Outro ponto de limitação do estudo foi a impossibilidade de verificação de desprendimento de microcoágulos pelo cateter após a infusão salina para verificar a permeabilidade do cateter. Foram necessários novos estudos que possibilitassem que essa solução seja filtrada e analisada microscopicamente, pois a presença desses microcoágulos poderá desencadear novas obstruções ou embolização para a corrente sanguínea. Outro fator limitador do estudo está relacionado ao uso prévio dos cateteres, pois vários dispositivos poderiam estar mais propensos a ter os coágulos mais ou menos aderidos em decorrência de os cateteres terem sido usados em diferentes neonatos para infusão de NPP, antibióticos, soluções de glicose e eletrólitos, o que independeria da heparina usada.
Para que a equipe de enfermagem obtenha o sucesso com a implantação do cateter, deve ter conhecimento dos riscos envolvidos no seu uso. Os cuidados de enfermagem são fatores essenciais na manutenção do CCIP e a identificação das possíveis complicações relacionadas ao seu uso torna‐se uma necessidade para esses profissionais que atuam diretamente na sua manipulação.10 Dessa forma, a pesquisa de evidência científica torna‐se essencial para o processo de tomada de decisão acerca do aprimoramento do CCIP, notadamente sobre qual é a solução mais efetiva na prevenção da obstrução do cateter.25
Pode‐se concluir que o uso de heparina de baixo peso molecular na concentração de 50UI/mL foi mais eficaz na restauração da permeabilidade de CCIPs neonatais (2,0Fr) ocluídos in vitro por coágulo do que as concentrações de 25UI/mL. Ressalta‐se que essa concentração ainda está dentro da margem de segurança indicada na literatura científica.
FinanciamentoO estudo não recebeu financiamento.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.