La gastrectomía vertical laparoscópica (GVL) está aportando resultados muy adecuados tanto en pérdida de peso como en mejoría de comorbilidad1–3. El hecho de que esta técnica se haya considerado erróneamente como sencilla y fácilmente reproducible ha llevado a un gran número de cirujanos a practicarla. Podría parecer que, en comparación con el bypass gástrico y las derivaciones biliopancreáticas, es una cirugía más asumible desde el punto de vista laparoscópico, pero se debe saber que sus complicaciones pueden incluso ser más serias que las de otras técnicas. Nos referimos principalmente a la aparición de fístulas gástricas. Comentamos el caso de una paciente con ingreso hospitalario superior a los 15 meses secundario a una fístula gástrica tras GVL.
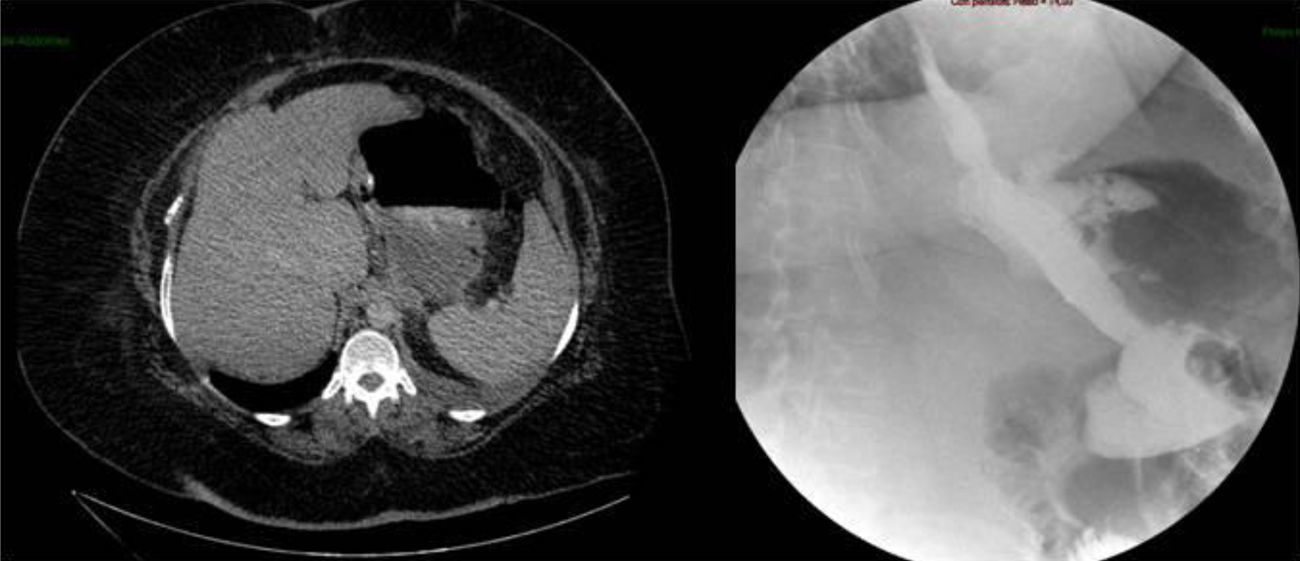
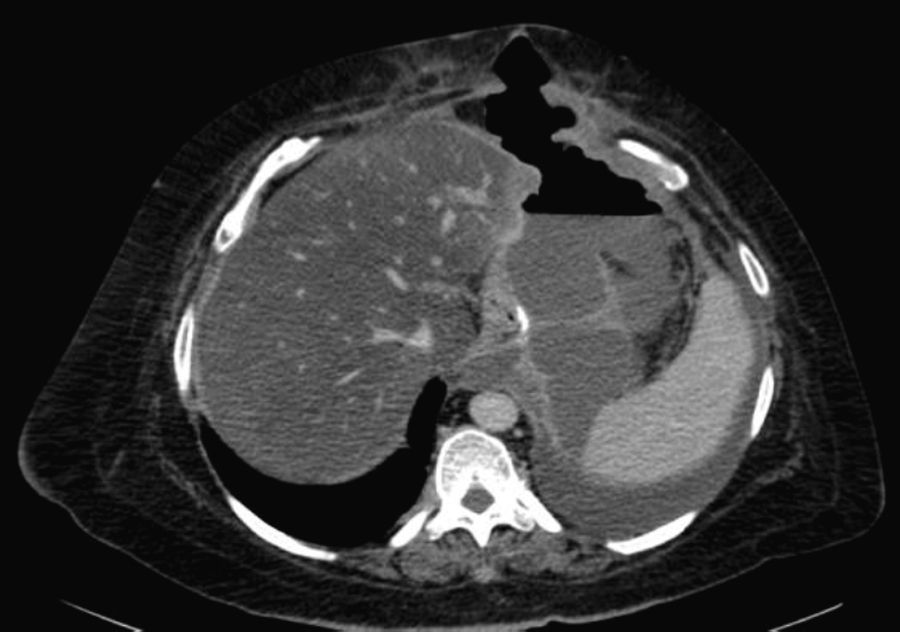
Paciente con IMC de 61,3kg/m2, con SAOS en tratamiento con cPAP. Se intervino practicando una GVL. La sección gástrica se realizó bajo tutela de una bujía de 34 F. Tras la sección gástrica, se invaginó la línea de grapado mediante una sutura continua de monofilamento 2-0. A las 48h se realizó prueba de estanqueidad con azul de metileno y a las 72h la paciente fue dada de alta con dieta líquida. Dos semanas después, la paciente ingresó por cuadro de fiebre sin dolor abdominal, y en la TAC urgente realizada se objetivó una colección abdominal importante secundaria a una fístula gástrica (fig. 1). Ante la situación de la paciente, se decidió intervenir con el objetivo de drenar el absceso, lavar la cavidad y dejar un drenaje (intraoperatoriamente nos fue imposible objetivar la fístula ya que los test realizados con aire y azul de metileno fueron negativos). Tres días después de la cirugía, se realizó un tránsito gastroduodenal que puso en evidencia la existencia de una fuga en tercio proximal sin estenosis distal asociada (fig. 1). Se comenzó con tratamiento conservador (dieta absoluta, nutrición parenteral y alimentación mediante catéter de yeyunostomía). Tras mes y medio, el débito por drenaje disminuyó de forma importante, pero en las pruebas de imagen se mantuvieron los signos de la fístula. Se intentó colocación de stent recubierto que tuvo que ser retirado a los 4 días por mala tolerancia de la paciente. Tras 5 meses íntegros de tratamiento conservador, y ante la demanda de la paciente, se decidió intervenir para intentar solucionar quirúrgicamente el problema. Durante la intervención se objetivó una fístula puntiforme centrada de tejido sano, por lo que se decidió cierre simple e invaginación (doble sutura). Durante las 2 semanas posteriores a la cirugía, los test de estanqueidad fueron negativos, por lo que la paciente fue dada de alta. Dos meses después volvió a ingresar por fiebre y disnea con una TAC que informó de gran absceso abdominal y derrame pleural izquierdo secundario a fístula gástrica (fig. 2). El absceso se drenó bajo punción endoscópica y la fístula se mantuvo con un débito diario de 20 cc durante 2 meses. Se decidió nueva intervención con la idea de disminuir la presión intraluminal y se realizó bypass gástrico. Desde la última intervención, la paciente se encuentra asintomática, tolerando dieta y con pruebas radiológicas negativas.
La GVL es una técnica aparentemente sencilla en el tratamiento de la obesidad mórbida, sin embargo, sus complicaciones, aunque son poco frecuentes, ponen en peligro la vida del paciente. Las principales complicaciones con esta técnica son la hemorragia (0-6,4%) y la fístula gástrica en tercio proximal (0-20%), con una mortalidad que oscila entre el 0 y el 3,2%3–5. El manejo de la fístula tras GVL es difícil, ya que el tratamiento conservador no siempre tiene buen resultado y puede cronificarse durante meses4–8. Cuando el tratamiento conservador no es exitoso, la mayoría de los autores defienden como siguiente paso la utilización de stents flexibles recubiertos5,9,10 con la intención de conseguir un «bypass temporal» de la fístula. Otros tratamientos propuestos son los sellantes (pegamentos biológicos) vía endoscópica5,7 con resultados controvertidos. En aquellos casos que no respondan a ningún tratamiento, debe valorarse la posibilidad de actuar sobre la estenosis distal (en caso de que esta exista) mediante dilataciones endoscópicas. Si no queda otra opción que la quirúrgica, se debe evitar el cierre simple de la fístula, aun cuando se localice, y se debe intentar disminuir la presión intraluminal gástrica mediante la conversión de la técnica en bypass gástrico.