La punción lumbar (PL) es una técnica ampliamente usada por distintos especialistas (anestesistas, intensivistas, internistas, oncólogos, médicos de urgencias, de medicina nuclear y por supuesto neurólogos) con fines diagnósticos y/o terapéuticos. A pesar de ser un procedimiento invasivo es bastante seguro, pero no está exento de posibles complicaciones, como cefalea, dolor lumbar o parestesia transitoria de un miembro inferior por irritación radicular ipsilateral. Mucho menos comunes son las complicaciones infecciosas, hemorrágicas o la afectación de nervios craneales (NC). Presentamos un caso tras una anestesia epidural y revisamos la bibliografía.
Mujer de 35 años de edad sin antecedentes de interés que acude a urgencias por diplopía 6 días después de una anestesia epidural con una aguja de 18 Gauge por su primer parto que discurrió sin complicaciones. Nunca se había realizado una PL. Desde el día siguiente del procedimiento anestésico refería una cefalea de intensidad leve, opresiva, de localización nucal que no se modificaba con los cambios posturales. No presentó vértigo, nauseas o vómitos ni ningún otro síntoma añadido. La cefalea le pareció trivial y probablemente relacionada con las pocas horas de sueño y con el estrés propio de la situación de madre primeriza, por lo que no consultó.
La exploración general fue normal y neurológicamente tan sólo se detectó una paresia del VI par craneal derecho, siendo el resto de la exploración normal.
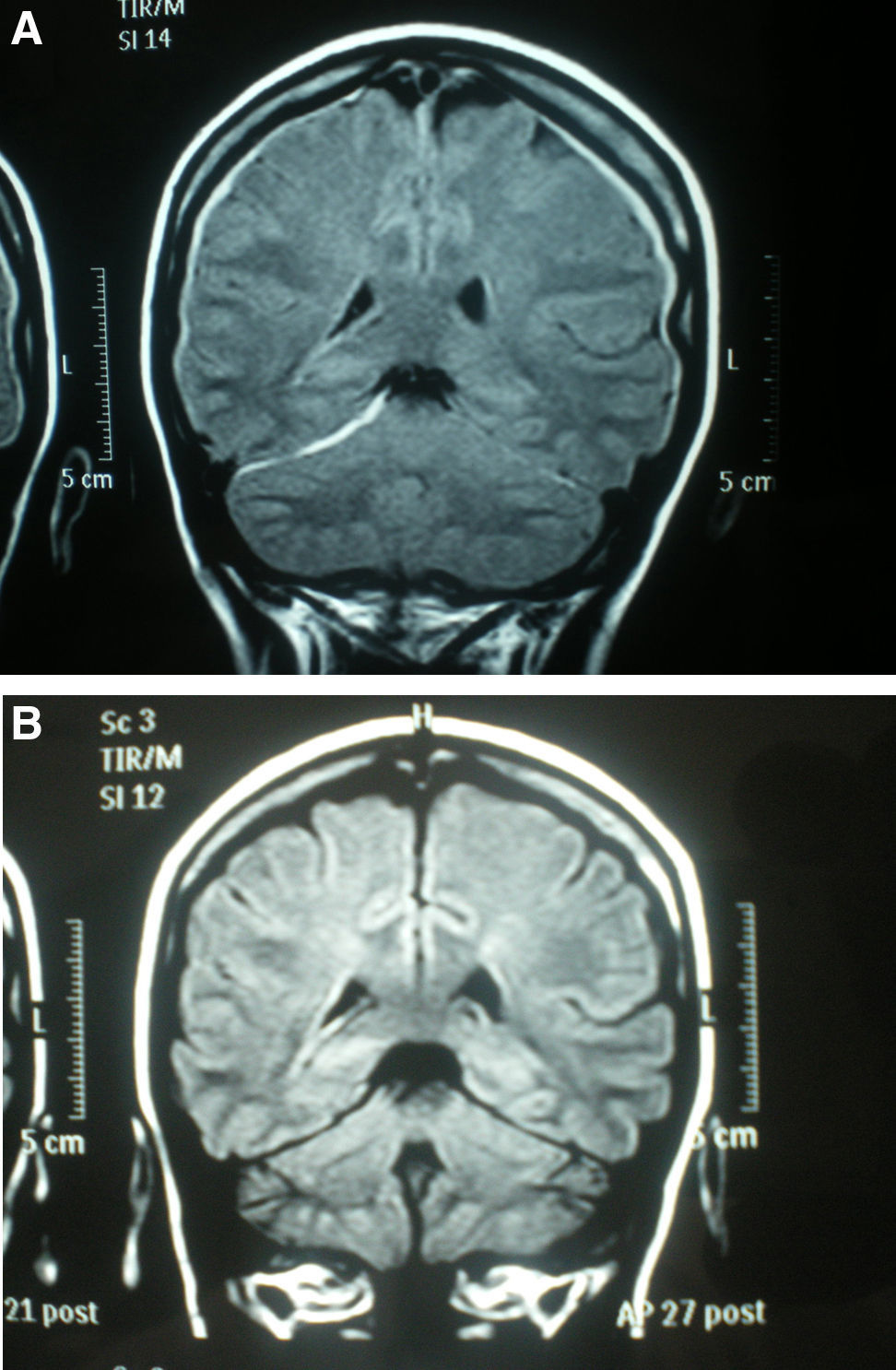
La analítica general (hemograma, bioquímica, coagulación), ECG, radiografía de tórax y escáner craneal fueron normales. Una semana después de comenzar con la clínica se realiza una resonancia magnética (RM) craneal que muestra una pequeña colección de líquido cefalorraquídeo (LCR) en el espacio subdural supra e infratentorial (fig. 1A). Se decide tratamiento conservador y 16 días después de comenzar la diplopía había desaparecido. Dos meses después de la primera se realiza una nueva RM que muestra resolución ad integrum de la colección subdural (fig. 1B), por lo que la paciente fue dada de alta.
En 1891 Quincke realizó la primera PL para tratar una hipertensión intracraneal asociada a una meningitis tuberculosa. La primera complicación de esta técnica la describió tras sufrirla el mismo Bier en 1898 y fue la cefalea post-PL1. Posteriormente se han descrito otras complicaciones. Una de las muy poco habituales es la afectación de NC2, sobre todo los oculomotores que se manifestan con diplopía.
Nishio et al3 han recogido en una excelente revisión los casos descritos, incluido el primero documentado en 1930. El NC que más frecuentemente se afecta es el VI par (motor ocular externo o abducens) como ocurrió en nuestro caso, dado que es el que posee el recorrido intracraneal más largo y se daña cuando existe una compresión local o un aumento o disminución de la presión del LCR3,4. El abducens puede afectarse uni o bilateralmente3. Debemos señalar que salvo el olfatorio, el glosofaríngeo y el vago todos los NC pueden afectarse5. También se ha descrito la lesión de más de un NC3,6 e incluso sintomatología combinada de pares y de vías largas7. La afectación de NC suele acontecer en el contexto de un síndrome de hipotensión intracraneal (hTIC) con la cefalea característica y el resto de síntomas típicos como mareo, nauseas o vómitos. Sin embargo, en nuestro caso y en otros5 la diplopía no se precedió de dicha cefalea.
Los datos de incidencia varían mucho entre los distintos autores2,3,5. El grosor de la aguja y el que el objetivo de la PL sea alcanzar el espacio epi o intradural son factores que explican esta diferencia. En las primeras no se pincha la duramadre salvo por error, con lo cual no existe la posibilidad de hTIC, dado que no existiría orificio de salida. En cuanto al grosor o anchura de la aguja hay que recordar que se mide en Gauge, siendo más ancha y por tanto con mayor probabilidad de hipotensión licuoral a menor Gauge. Así, con una aguja de 16 Gauge presentaron paresia del VI par 8 de 839 pacientes, y ninguno de los más de 7.500 si aguja de 20 o22 Gauge5.
Se desconoce la fisiopatología de este proceso, aunque la hipótesis más aceptada es que la hTIC por la fuga dural de LCR tras la PL ocasionaría una pérdida de la suspensión hidráulica del encéfalo. Esto provoca tracción mecánica3 de estructuras dolorosas intracraneales produciendo cefalea2 y del VI par que acaba dañándose3. Por tanto, la hTIC desempeña un papel clave, y no así la propia PL. De hecho, se han descrito casos de paresia del VI par en pacientes con hTIC espontánea8. Es posible que exista predisposición individal, aunque hay pacientes que les ha ocurrido en la tercera anestesia epidural, no habiendo presentado incidencias en las dos previas9.
Aunque también existe en varones3, la mayoría de los pacientes descritos, como en nuestro caso, eran mujeres. Siempre se ha considerado más probable la hTIC en este género3, posiblemente por presentar en general menor índice de masa corporal. Es poco probable que aparezca antes de la pubertad y a partir de los 60 años.
La coexistencia temporal de una colección subdural de LCR y la clínica y el procedimiento anestésico nos hace pensar que existe una relación entre ambos de causalidad. El higroma subdural, descrito también por otros autores5,10, se debe a la tracción que el encéfalo realiza a través de sus estructuras de anclaje sobre la interfase duramadre-aracnoides, sin rotura de vasos al contrario del hematoma subdural11. Otros hallazgos descritos en la hTIC son el descenso del encéfalo, la disminución de tamaño de las cisternas subaracnoideas o la captación de gadolinio en las meninges11.
El cuadro clínico no es agudo, sino que suele aparecer a partir de los 4 días del procedimiento, siendo la máxima incidencia al décimo día3. En nuestra paciente apareció al sexto día tras la PL. Dado que a veces ocurre hasta 3 semanas después, el paciente o incluso un facultativo puede no relacionarla con dicha técnica (sobre todo si no se predede de la cefalea característica del síndrome de hTIC como en nuestro caso), por lo que acude al oftalmólogo o al servicio de urgencias. Por dicho motivo estos especialistas deben estar alerta y ante un afectación de un nervio oculomotor, sobre todo el abducens, una PL los días previos debe ser considerada5. El curso suele ser benigno con resolución en pocas semanas3, como ocurrió en nuestro caso, aunque en algunas ocasiones la clínica ha durado más allá de 3 meses, llegando incluso hasta 75, 183 o 21 meses12 o ha sido recurrente13.
Respecto al tratamiento se ha propuesto la hidratación2,11 y la utilización de parches epidurales de sangre autóloga con buena respuesta14, aunque no siempre esta terapia es eficaz para el tratamiento de la paresia12. Esta divergencia de resultados puede deberse, entre otras razones, a la prontitud con que se incia el tratamiento, debiendo hacerse en las primeras 24 horas desde el inicio del cuadro14. Algunos pacientes han llegado a precisar tratamiento quirúrgico para corregir las alteraciones oculares6. La actitud expectante como en nuestro caso también permite la autorresolución del cuadro4, sobre todo si la severidad de la hTIC es leve. La magnitud del orificio dural (relacionado con el grosor de la aguja) puede estar también implicada. Como tantas veces en Medicina, lo ideal es la prevención usando las agujas de menor calibre posible5,15, pues así se produce con menor frecuencia hipotensión intracraneal, que es la responsable de las complicaciones15. La mayoría de los autores no describen el tamaño de la aguja, aunque en algunos que sí lo hacen3,9 ha aparecido incluso con una aguja de 25 Gauge3,5. En nuestro caso el calibre fue de 18.
A modo de conclusión, una posible causa de una diplopía es una hipotensión de LCR, por lo que debe sopesarse esta posibilidad (incluso si no se precede de la cefalea característica) ante una paresia oculomotora, sobre todo si se trata del VI par.