Historicamente, pacientes com cirurgia de revascularização do miocárdio (CRM) prévia submetidos à intervenção coronária percutânea (ICP) primária têm pior prognóstico que pacientes sem CRM prévia. No entanto, análises mais contemporâneas contestam esses achados. Nosso objetivo foi avaliar os desfechos clínicos de 30 dias em pacientes com e sem CRM prévia submetidos à ICP primária.
MétodosEstudo de coorte prospectivo extraído do banco de dados do Instituto de Cardiologia do Rio Grande do Sul, contendo 1.854 pacientes submetidos à ICP primária.
ResultadosPacientes com CRM prévia (3,8%) mostraram perfil clínico, em geral, mais grave. O tempo de início dos sintomas até a chegada ao hospital foi menor nesse grupo (2,50 horas [1,46‐3,66] vs. 3,99 horas [1,99‐6,50]; p < 0,001) e o tempo porta‐balão foi semelhante (1,33 hora [0,85‐2,07] vs. 1,16 hora [0,88‐1,58]; p = 0,12). O acesso femoral foi mais usado no grupo com CRM prévia (91,5% vs. 62,5%; p < 0,001). O uso de tromboaspiração manual foi menor nesse grupo (16,9% vs. 31,1%; p = 0,007), mas não houve diferença no uso de inibidor da glicoproteína IIb/IIIa (28,2% vs. 32,4%; p = 0,28). O sucesso angiográfico foi menor no grupo com CRM prévia (80,3% vs. 93,3%; p = 0,009). Aos 30 dias, pacientes com CRM prévia apresentaram taxas similares de eventos cardíacos adversos maiores (14,1% vs. 11,2%; p = 0,28), e a mortalidade, embora numericamente mais alta, não foi estatisticamente significativa (13,2% vs. 7,0%; p = 0,07).
ConclusõesNessa análise contemporânea, pacientes com CRM prévia submetidos à ICP primária apresentaram perfil clínico mais grave e menor sucesso angiográfico, porém não mostraram diferenças nos desfechos clínicos em 30 dias.
Historically, patients with prior coronary artery bypass graft (CABG) surgery undergoing primary percutaneous coronary intervention (PCI) have a worse prognosis than patients without prior CABG. However, more contemporary analyses have contested these findings. This study's aim was to evaluate the 30‐day clinical outcomes in patients with and without prior CABG submitted to primary PCI.
MethodsProspective cohort study, extracted from the database of Instituto de Cardiologia do Rio Grande do Sul, containing 1,854 patients undergoing primary PCI.
ResultsPatients with prior CABG (3.8%) showed, in general, a more severe clinical profile. The time of symptom onset until arrival at the hospital was shorter in this group (2.50hours [1.46 to 3.66] vs. 3.99 hour [1.99 to 6.50]; p < 0.001), while the door‐to‐balloon time was similar (1.33 hour [0.85 to 2.07] vs. 1.16 hour [0.88 to 1.58]; p = 0.12). Femoral access was more often used in the group with prior CABG (91.5% vs. 62.5%; p < 0.001). Manual thrombus aspiration was less often performed in this group (16.9% vs. 31.1%; p = 0.007), but there was no difference regarding the use of glycoprotein IIb/IIIa inhibitors (28.2% vs. 32.4%, p = 0.28). Angiographic success was lower in the group with prior CABG (80.3% vs. 93.3%; p = 0.009). At 30 days, patients with prior CABG had similar rates of major adverse cardiac events (14.1% vs. 11.2%; p = 0.28), and mortality, although numerically higher, was not statistically significant (13.2% vs. 7.0%, p = 0.07).
ConclusionsIn this contemporary analysis, patients with prior CABG undergoing primary PCI had a more severe clinical profile and lower angiographic success, but showed no differences regarding 30‐day clinical outcomes.
O número de cirurgias de revascularização do miocárdio (CRM) teve seu pico na década de 1990 e, atualmente, permanece uma alternativa muito utilizada como método de revascularização em pacientes com doença aterosclerótica coronariana.1 Sabe‐se, também, que a metade dos enxertos venosos torna‐se doentes, e um quarto é ocluído em um período de 5 anos pós‐cirurgia. Muitos desses pacientes apresentam‐se em serviços de emergência com quadro de síndromes coronarianas agudas.2 Os dados epidemiológicos de nosso país são escassos, mas, conforme a literatura internacional, trata‐se de um evento relativamente frequente. Segundo o National Cardiovascular Data Registry (NCDR®) a taxa de pacientes com CRM prévia que se apresentam com infarto do miocárdio com supradesnivelamento do segmento ST (IAMCST) foi em torno de 7,0 a 7,5% entre os anos 2000 e 2010.3
A presença de CRM prévia já foi reportada como um fator de risco independente de desfechos clínicos adversos no IAMCST. Nesse cenário, o diagnóstico e a terapêutica são sempre desafiadores. Os achados clínicos, eletrocardiográficos e laboratoriais nem sempre são completamente elucidativos4 e, face a questões anatômicas e comorbidades existentes, a intervenção coronária percutânea (ICP) é, por vezes, mais complexa e de pior prognóstico.5
Dados da literatura demonstram que, em pacientes com IAMCST e CRM prévia, submetidos à ICP primária por balão, as taxas de mortalidade hospitalar e em 6 meses após o evento eram maiores quando comparadas com pacientes sem CRM prévia, especialmente quando o vaso culpado tratava‐se de um enxerto de safena.6 Não há dados recentes na literatura nacional avaliando esse grupo de pacientes nesse cenário.
O presente estudo teve como objetivo avaliar os desfechos em 30 dias de uma coorte contemporânea de pacientes com e sem CRM, que foram submetidos à ICP primária em um hospital terciário de referência e com alto volume de atendimentos.
MétodosPacientesEstudo de coorte prospectivo que selecionou pacientes de um registro ativo incluindo consecutivamente todos os pacientes que se apresentaram com IAMCST submetidos à ICP primária no Instituto de Cardiologia do Rio Grande do Sul, Fundação Universitária de Cardiologia, em Porto Alegre (RS). Os dados e pacientes avaliados foram aqueles incluídos no registro no período de janeiro de 2010 até dezembro de 2013. O projeto foi aprovado pelo Comitê de Ética local. Todos os pacientes receberam informações sobre o estudo e assinaram o Termo de Consentimento Livre e Esclarecido.
Os critérios de inclusão foram a presença de IAMCST tratado nas primeiras 12 horas. IAMCST foi definido como dor torácica típica em repouso associado com elevação do segmento ST de pelo menos 1mm em duas derivações contíguas no plano frontal, ou 2mm no plano horizontal, ou dor torácica típica em repouso em paciente com bloqueio de ramo esquerdo novo, ou presumivelmente novo, no eletrocardiograma de 12 derivações. Os critérios de exclusão foram tempo de apresentação dos sintomas até a chegada ao hospital maior de 12 horas, idade menor de 18 anos ou desejo de não participar do estudo.
Intervenção coronária percutânea primáriaA decisão de acionar o Serviço de Hemodinâmica foi feita pela equipe assistente responsável pelo atendimento do paciente na sala de emergência, na chegada do mesmo. De acordo com as rotinas institucionais, a farmacologia antiplaquetária adjunta inicial incluía dose de ataque de 300mg de ácido acetilsalicílico e um inibidor P2Y12 (300 a 600mg de clopidogrel, 180mg de ticagrelor ou 60mg de prasugrel). Facultava‐se o uso de terapia anticoagulante adicional (heparina 70 a 100 UI/kg) ainda na sala de emergência, conforme julgamento da equipe responsável pelo atendimento inicial. Àqueles pacientes que não tinham recebido a heparina na sala de emergência, o fármaco era prescrito na sala de hemodinâmica, pela equipe de cardiologia intervencionista, no ato do procedimento. Estes também foram responsáveis pela decisão ou não do uso inibidores da glicoproteína IIb/IIIa, bem como outras medicações adjuntas.
A demonstração da lesão considerada culpada foi realizada em pelo menos duas projeções. Via de acesso, técnica de ICP, uso de tromboaspiração e número de stents utilizados foram deixados a critério do operador. O fluxo coronariano antes e depois do procedimento foi avaliado e descrito de acordo com o critério Thrombolysis in Myocardial Infarction (TIMI).7
Coleta de dados, desfechos e seguimento clínicoTodos os pacientes foram entrevistados pelos investigadores na admissão hospitalar. Os dados angiográficos, clínicos e laboratoriais foram coletados utilizando um questionário padrão. Os pacientes foram visitados diariamente durante a estadia hospitalar por um dos investigadores para avaliar a ocorrência de desfechos clínicos hospitalares. A ocorrência de eventos cardiovasculares 30 dias após o procedimento foi avaliada por meio de contato telefônico e/ou revisão de registros médicos.
Eventos cardíacos adversos maiores (ECAM) foram definidos como a combinação de mortalidade por todas as causas, infarto do miocárdio ou necessidade de revascularização de urgência. Infarto do miocárdio foi caracterizado como a presença de dor torácica recorrente associada à nova elevação de biomarcadores séricos (após o declínio inicial da curva natural) associada à elevação do segmento ST e/ou novas ondas Q patológicas. Revascularização de urgência foi considerada como a necessidade de realizar novo procedimento de revascularização, percutâneo ou cirúrgico, devido à isquemia recorrente.
Definimos, ainda, o acidente vascular encefálico como o desenvolvimento de défice focal súbito de causa presumivelmente cerebrovascular, irreversível e/ou ocasionando morte dentro de 24 horas. Sangramento maior foi considerado como a ocorrência de hemorragia clinicamente evidente, com queda dos níveis de hemoglobina > 5g/dL ou hematócrito > 15%, ou desenvolvimento de acidente vascular encefálico hemorrágico. Classificou‐se como trombose do stent a oclusão súbita do vaso tratado, confirmada por angiografia, durante a fase hospitalar.
Análise estatísticaOs resultados foram expressos como média e desvio padrão ou frequências absolutas e relativas, quando apropriado. Variáveis com distribuição assimétrica foram apresentadas como média e intervalo interquartil. Para variáveis categóricas, foi utilizado o teste qui quadrado ou teste exato de Fischer. Para variáveis contínuas foram utilizados os testes de Análise de Variância (ANOVA) e Turkey para múltiplas comparações, no caso de distribuição normal, e o teste de Kruskal‐Wallis, para variáveis de distribuição assimétrica. Significância estatística foi definida como um valor de p bicaudal < 0,05.
Os dados foram coletados em uma base de dados Microsoft Access (Microsoft Corporation, Redmond, EUA) e a análise estatística foi realizada utilizando as ferramentas do programa Statistical Package for Social Science (SPSS) para Windows, versão 17.0 (IBM Corp., Armonk, EUA).
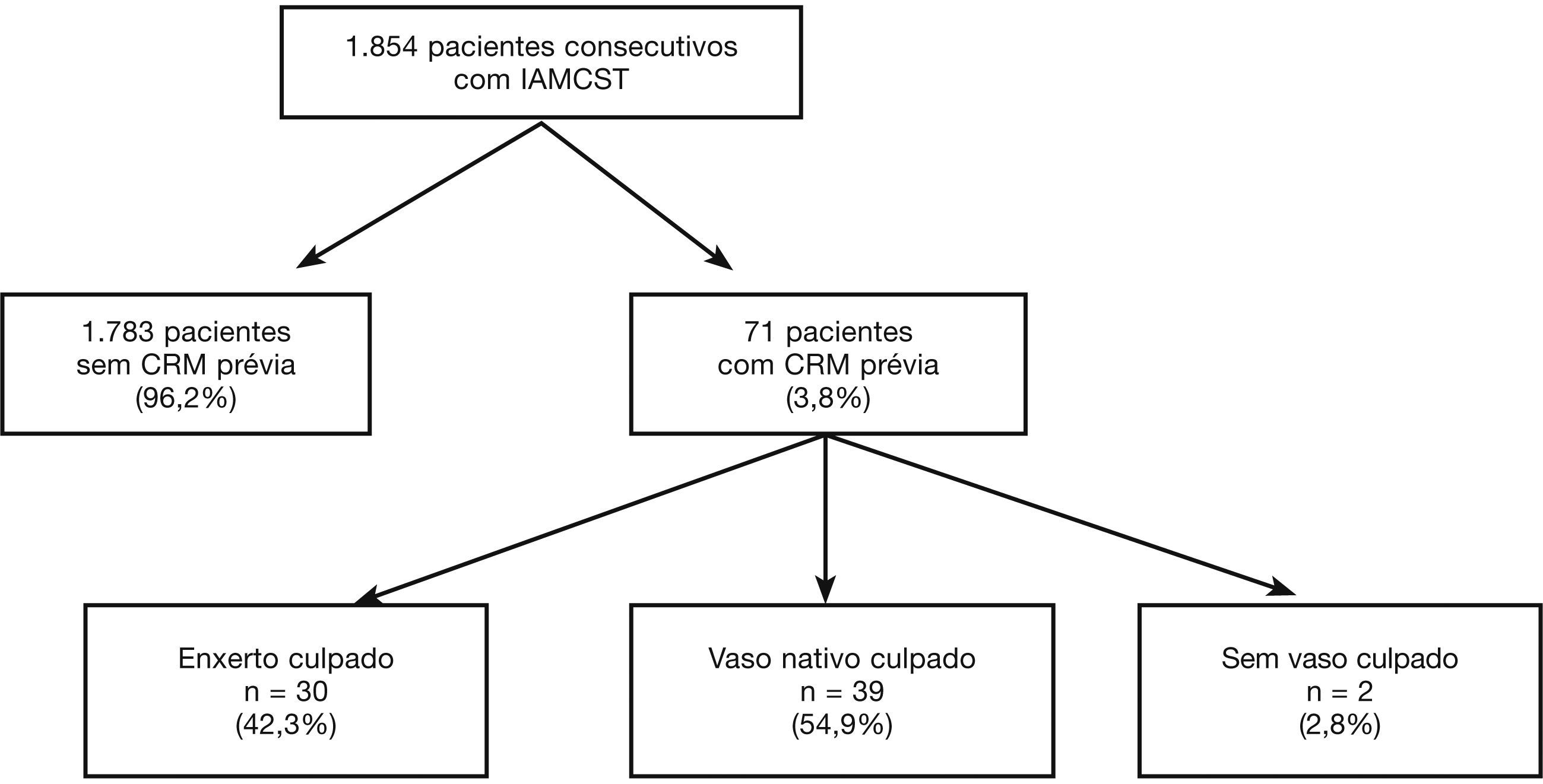
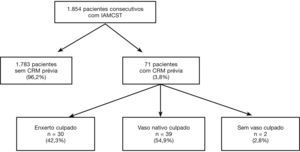
ResultadosDentre os 1.854 pacientes consecutivos com IAMCST e submetidos à ICP primária, analisados no período compreendido entre 2010 e 2013, 71 (3,8%) tinham história prévia de CRM (fig. 1). A tabela 1 descreve as características clínicas, angiográficas e do procedimento. Pacientes com CRM prévia eram mais idosos, com maior prevalência de diabetes melito, dislipidemia, hipertensão arterial, infarto agudo do miocárdio e ICP prévios, mas com menor número de tabagistas e de infartos de parede anterior. Não houve diferenças significativas na incidência de choque cardiogênico (Killip IV), infarto de ventrículo direito ou presença de bloqueio de ramo esquerdo no eletrocardiograma entre os grupos.
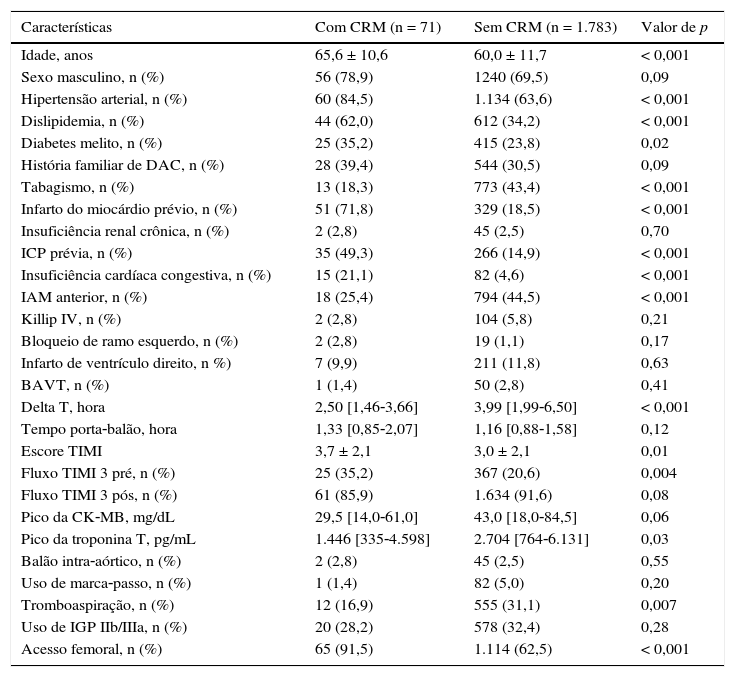
Características clínicas, angiográficas e do procedimento
| Características | Com CRM (n = 71) | Sem CRM (n = 1.783) | Valor de p |
|---|---|---|---|
| Idade, anos | 65,6 ± 10,6 | 60,0 ± 11,7 | < 0,001 |
| Sexo masculino, n (%) | 56 (78,9) | 1240 (69,5) | 0,09 |
| Hipertensão arterial, n (%) | 60 (84,5) | 1.134 (63,6) | < 0,001 |
| Dislipidemia, n (%) | 44 (62,0) | 612 (34,2) | < 0,001 |
| Diabetes melito, n (%) | 25 (35,2) | 415 (23,8) | 0,02 |
| História familiar de DAC, n (%) | 28 (39,4) | 544 (30,5) | 0,09 |
| Tabagismo, n (%) | 13 (18,3) | 773 (43,4) | < 0,001 |
| Infarto do miocárdio prévio, n (%) | 51 (71,8) | 329 (18,5) | < 0,001 |
| Insuficiência renal crônica, n (%) | 2 (2,8) | 45 (2,5) | 0,70 |
| ICP prévia, n (%) | 35 (49,3) | 266 (14,9) | < 0,001 |
| Insuficiência cardíaca congestiva, n (%) | 15 (21,1) | 82 (4,6) | < 0,001 |
| IAM anterior, n (%) | 18 (25,4) | 794 (44,5) | < 0,001 |
| Killip IV, n (%) | 2 (2,8) | 104 (5,8) | 0,21 |
| Bloqueio de ramo esquerdo, n (%) | 2 (2,8) | 19 (1,1) | 0,17 |
| Infarto de ventrículo direito, n %) | 7 (9,9) | 211 (11,8) | 0,63 |
| BAVT, n (%) | 1 (1,4) | 50 (2,8) | 0,41 |
| Delta T, hora | 2,50 [1,46‐3,66] | 3,99 [1,99‐6,50] | < 0,001 |
| Tempo porta‐balão, hora | 1,33 [0,85‐2,07] | 1,16 [0,88‐1,58] | 0,12 |
| Escore TIMI | 3,7 ± 2,1 | 3,0 ± 2,1 | 0,01 |
| Fluxo TIMI 3 pré, n (%) | 25 (35,2) | 367 (20,6) | 0,004 |
| Fluxo TIMI 3 pós, n (%) | 61 (85,9) | 1.634 (91,6) | 0,08 |
| Pico da CK‐MB, mg/dL | 29,5 [14,0‐61,0] | 43,0 [18,0‐84,5] | 0,06 |
| Pico da troponina T, pg/mL | 1.446 [335‐4.598] | 2.704 [764‐6.131] | 0,03 |
| Balão intra‐aórtico, n (%) | 2 (2,8) | 45 (2,5) | 0,55 |
| Uso de marca‐passo, n (%) | 1 (1,4) | 82 (5,0) | 0,20 |
| Tromboaspiração, n (%) | 12 (16,9) | 555 (31,1) | 0,007 |
| Uso de IGP IIb/IIIa, n (%) | 20 (28,2) | 578 (32,4) | 0,28 |
| Acesso femoral, n (%) | 65 (91,5) | 1.114 (62,5) | < 0,001 |
CRM: cirurgia de revascularização do miocárdio; DAC: doença arterial coronariana; ICP: intervenção coronária percutânea; IAM: infarto agudo do miocárdio; BAVT: bloqueio atrioventricular total; TIMI: Thrombolysis in Myocardial Infarction; CK‐MB, isoenzima miocárdica da creatina‐quinase; IGP IIb/IIIa: inibidores da glicoproteína IIb/IIIa.
O tempo de início dos sintomas até a chegada ao hospital (delta T) foi significativamente menor no grupo com CRM prévia (2,50 horas [1,46‐3,66] vs. 3,99 horas [1,99‐6,50]; p < 0,001). O tempo porta‐balão foi semelhante entre ambos (1,33 hora [0,85‐2,07] vs. 1,16 hora [0,88‐1,58]; p = 0,12). Pacientes com CRM prévia tinham maior incidência de fluxo TIMI 3 pré‐procedimento, mas houve tendência a menor fluxo TIMI 3 ao final do procedimento (85,9% vs. 91,6%; p = 0,08). Os pacientes com CRM prévia apresentaram níveis de troponina sérica menor do que aqueles sem CRM prévia e tendência um nível de creatinoquinase de banda miocárdica (CK‐MB) menor.
O acesso femoral foi mais frequentemente usado nesse grupo (91,5% vs. 62,5%; p < 0,001). O uso de tromboaspiração manual foi significativamente menor no grupo com CRM prévia (16,9% vs. 31,1%; p = 0,007); no entanto, não houve diferença no uso de inibidor da glicoproteína IIb/IIIa entre os dois grupos. O sucesso angiográfico foi menor no grupo com CRM prévia (80,3% vs. 93,3%; p = 0,009).
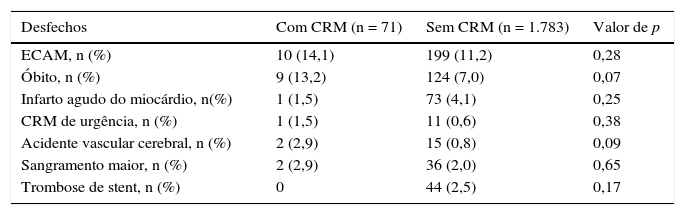
Pacientes com CRM prévia apresentaram taxas similares de ECAM (14,1% vs. 11,2%; p = 0,28), e a mortalidade, embora numericamente mais alta, não foi estatisticamente significativa (13,2% vs. 7,0%; p = 0,07) em relação aos pacientes sem CRM prévia (tabela 2).
Desfechos clínicos em 30 dias
| Desfechos | Com CRM (n = 71) | Sem CRM (n = 1.783) | Valor de p |
|---|---|---|---|
| ECAM, n (%) | 10 (14,1) | 199 (11,2) | 0,28 |
| Óbito, n (%) | 9 (13,2) | 124 (7,0) | 0,07 |
| Infarto agudo do miocárdio, n(%) | 1 (1,5) | 73 (4,1) | 0,25 |
| CRM de urgência, n (%) | 1 (1,5) | 11 (0,6) | 0,38 |
| Acidente vascular cerebral, n (%) | 2 (2,9) | 15 (0,8) | 0,09 |
| Sangramento maior, n (%) | 2 (2,9) | 36 (2,0) | 0,65 |
| Trombose de stent, n (%) | 0 | 44 (2,5) | 0,17 |
CRM: cirurgia de revascularização do miocárdio; ECAM: eventos cardiovasculares adversos maiores.
Conforme apresentado nas tabelas 3 e 4, pacientes com CRM prévia foram estratificados de acordo com o tipo vaso tratado. Este foi identificado como sendo o enxerto de safena em 30 pacientes (42,3%) e como o vaso nativo em 39 pacientes (54,9%); em 2 pacientes não foi possível definir o vaso culpado.
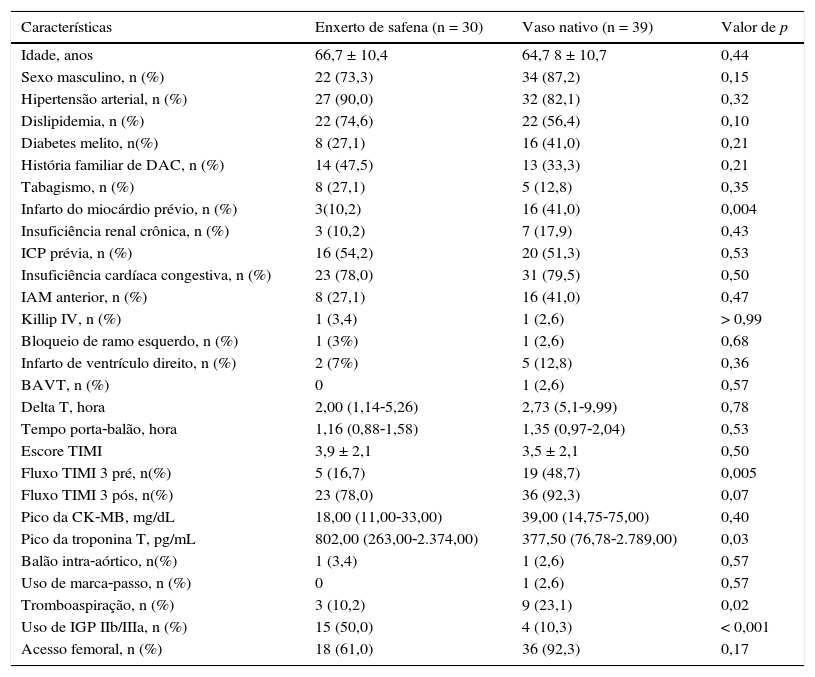
Características clínicas entre pacientes com cirurgia de revascularização prévia, de acordo com o tipo de vaso tratado
| Características | Enxerto de safena (n = 30) | Vaso nativo (n = 39) | Valor de p |
|---|---|---|---|
| Idade, anos | 66,7 ± 10,4 | 64,7 8 ± 10,7 | 0,44 |
| Sexo masculino, n (%) | 22 (73,3) | 34 (87,2) | 0,15 |
| Hipertensão arterial, n (%) | 27 (90,0) | 32 (82,1) | 0,32 |
| Dislipidemia, n (%) | 22 (74,6) | 22 (56,4) | 0,10 |
| Diabetes melito, n(%) | 8 (27,1) | 16 (41,0) | 0,21 |
| História familiar de DAC, n (%) | 14 (47,5) | 13 (33,3) | 0,21 |
| Tabagismo, n (%) | 8 (27,1) | 5 (12,8) | 0,35 |
| Infarto do miocárdio prévio, n (%) | 3(10,2) | 16 (41,0) | 0,004 |
| Insuficiência renal crônica, n (%) | 3 (10,2) | 7 (17,9) | 0,43 |
| ICP prévia, n (%) | 16 (54,2) | 20 (51,3) | 0,53 |
| Insuficiência cardíaca congestiva, n (%) | 23 (78,0) | 31 (79,5) | 0,50 |
| IAM anterior, n (%) | 8 (27,1) | 16 (41,0) | 0,47 |
| Killip IV, n (%) | 1 (3,4) | 1 (2,6) | > 0,99 |
| Bloqueio de ramo esquerdo, n (%) | 1 (3%) | 1 (2,6) | 0,68 |
| Infarto de ventrículo direito, n (%) | 2 (7%) | 5 (12,8) | 0,36 |
| BAVT, n (%) | 0 | 1 (2,6) | 0,57 |
| Delta T, hora | 2,00 (1,14‐5,26) | 2,73 (5,1‐9,99) | 0,78 |
| Tempo porta‐balão, hora | 1,16 (0,88‐1,58) | 1,35 (0,97‐2,04) | 0,53 |
| Escore TIMI | 3,9 ± 2,1 | 3,5 ± 2,1 | 0,50 |
| Fluxo TIMI 3 pré, n(%) | 5 (16,7) | 19 (48,7) | 0,005 |
| Fluxo TIMI 3 pós, n(%) | 23 (78,0) | 36 (92,3) | 0,07 |
| Pico da CK‐MB, mg/dL | 18,00 (11,00‐33,00) | 39,00 (14,75‐75,00) | 0,40 |
| Pico da troponina T, pg/mL | 802,00 (263,00‐2.374,00) | 377,50 (76,78‐2.789,00) | 0,03 |
| Balão intra‐aórtico, n(%) | 1 (3,4) | 1 (2,6) | 0,57 |
| Uso de marca‐passo, n (%) | 0 | 1 (2,6) | 0,57 |
| Tromboaspiração, n (%) | 3 (10,2) | 9 (23,1) | 0,02 |
| Uso de IGP IIb/IIIa, n (%) | 15 (50,0) | 4 (10,3) | < 0,001 |
| Acesso femoral, n (%) | 18 (61,0) | 36 (92,3) | 0,17 |
DAC: Doença arterial coronariana; ICP: intervenção coronária percutânea; IAM: infarto agudo do miocárdio; BAVT: bloqueio atrioventricular total; TIMI: Thrombolysis in Myocardial Infarction; CK‐MB, isoenzima miocárdica da creatina‐quinase; IGP IIb/IIIa: inibidores da glicoproteína IIb/IIIa.
Desfechos clínicos em 30 dias nos pacientes com cirurgia de revascularização prévia, de acordo com o tipo de vaso tratado
| Desfechos | Enxerto de safena (n = 30) | Vaso nativo (n = 39) | Valor de p |
|---|---|---|---|
| ECAM, n (%) | 4 (13,3) | 7 (17,9) | 0,15 |
| Óbito, n (%) | 2 (6,6) | 4 (10,3) | 0,23 |
| Infarto agudo do miocárdio, n (%) | 0 | 1 (2,6) | 0,57 |
| Revascularização de urgência, n (%) | 1 (3,3) | 0 | 0,44 |
| Acidente vascular cerebral, n (%) | 1 (3,3) | 1 (2,6) | 0,85 |
| Sangramento maior, n (%) | 1 (3,3) | 0 | 0,25 |
| Trombose de stent, n (%) | 0 | 0 | NA |
ECAM: eventos cardiovasculares adversos maiores; NA: não aplicável.
Pacientes dos dois grupos não apresentaram, em geral, diferenças em relação às características clínicas. Os fluxos TIMI 3 pré (16,7% vs. 48,7%; p = 0,005) e pós‐procedimento (78,0% vs. 92,3%; p = 0,07) foram menores no grupo enxerto venoso. O uso da tromboaspiração (10,2% vs. 23,1%; p = 0,02) foi menor, mas a utilização de glicoproteína IIb/IIIa foi maior (50,0% vs. 10,3%; p < 0,001) nesse grupo. O sucesso angiográfico foi semelhante (80,2% vs. 82,1%; p = 0,37), assim como a incidência de ECAM em 30 dias (13,3% vs. 17,9%; p = 0,15).
DiscussãoEste estudo apresenta uma amostra representativa e contemporânea de pacientes com IAMCST e CRM prévia. A taxa de 3,8% de pacientes com CRM prévia presente nessa análise é compatível com a maioria dos relatos da literatura (2,5 a 5,3%) e um pouco menor que alguns estudos mais recentes, nos quais a taxa de CRM prévia foi em torno de 7%.8
A tendência a maior mortalidade em 30 dias no grupo com CRM prévia, embora possa ter sido influenciada pelo tamanho da amostra, pode sugerir que esses pacientes não apresentam necessariamente um pior prognóstico no primeiro mês após o evento índice. Da mesma forma, não existe diferença na taxa de ECAM ou mortalidade entre os pacientes com enxerto venoso culpado, em relação ao vaso nativo culpado, naqueles pacientes com CRM prévia.
Análises prévias sugerem mortalidade aumentada em paciente com IAMCST e CRM prévia, especialmente naqueles que têm como vaso culpado o enxerto venoso. Estudo realizado no início dos anos 2000 demonstrou taxa de sucesso significativamente menor de ICP com balão e fluxo TIMI 3 pós‐procedimento em 58 pacientes com CRM prévia.6 A mortalidade hospitalar foi maior entre os pacientes com CRM prévia e naqueles com enxerto venoso como vaso culpado. Essa diferença entre as análises deve estar relacionada a uma combinação de terapêutica adjunta inadequada, pois não existia uma dupla antiagregação plaquetária padrão àquela época; a não utilização rotineira de stents; e a baixas taxas de reperfusão com sucesso com o uso de ICP primária.
Nikolski et al.,9 em subanálise do estudo HORIZONS‐AMI, demonstraram que os pacientes que tinham CRM prévia, quando comparados a pacientes sem história de cirurgia, ao final de 3 anos, apresentavam maiores taxas ECAM, às custas de diferenças significativas nas taxas de reinfarto, acidente vascular encefálico e, inclusive, mortalidade. Além disso, pacientes com CRM prévia estavam associados a maior atraso para a reperfusão mecânica, além de menores taxas de ICP primária e patência do vaso relacionado ao evento.
Em outra análise, Brodie et al.10 também demonstraram piores desfechos a médio e longo prazo, 1 ano e 5 anos, nos pacientes com CRM prévia tendo como vaso culpado o enxerto venoso. A taxa de mortalidade deste grupo foi cerca de três vezes maior em relação ao grupo com vaso nativo culpado, com significância estatística. No entanto, este estudo reúne pacientes desde a década de 1980 até o início dos anos 2000 e tem como principal limitação o uso de stents em apenas 33% dos casos, dispositivos de proteção distal em minoria absoluta de pacientes e, principalmente, a ausência de protocolos para dupla antiagregação plaquetária fato que difere bastante da realidade apresentada no nosso estudo, no qual o uso otimizado de antiagregação plaquetária e implante de stents foi a regra.
Já em estudo bastante recente, Kohl et al.11 demonstraram que não houve diferença de mortalidade entre os grupo com e sem CRM prévia em 30 dias e 1 ano, respectivamente. Já na análise de 5 anos, observa‐se aumento significativo na mortalidade nos pacientes com CRM prévia. Assim como observado na nossa casuística, neste estudo não houve diferenças de mortalidade quando estratificados os grupos de acordo com o vaso culpado, sendo o nativo ou o enxerto venoso.
Limitações do estudoTrata‐se de um estudo observacional e, portanto, conclusões definitivas a respeito do efeito de certas terapias sobre os desfechos podem ter sido afetadas por viés de confusão. O número de pacientes incluídos no estudo, embora bastante representativo, pode não ter sido suficiente para demonstrar diferenças entre os dois grupos, em relação aos desfechos. Além disso, nossos resultados podem não ser generalizados em relação aos de outros centros de menor volume. A análise angiográfica não foi avaliada independentemente por um laboratório angiográfico distinto, uma limitação que também é compartilhada por outros registros de pacientes com ICP primária. Da mesma forma, não foi realizado um seguimento a longo prazo desses pacientes, o que poderia confirmar ou não os achados de curto prazo.
ConclusõesNesta coorte contemporânea de pacientes com cirurgia de revascularização prévia submetidos à intervenção coronária percutânea primária para o tratamento de infarto do miocárdio com supradesnivelamento do segmento ST, observou‐se que, apesar de os pacientes com cirurgia de revascularização prévia apresentarem sucesso angiográfico menor, não houve diferença significativa na mortalidade geral nem nas taxas de eventos cardíacos adversos maiores a curto prazo em comparação àqueles sem cirurgia de revascularização prévia. Quando estratificamos o grupo com cirurgia de revascularização prévia de acordo com o vaso culpado, também não se verificaram diferenças nos desfechos entre os tipos de vaso tratado. Estes achados demonstram a importância de um centro terciário utilizar protocolos bem definidos no tratamento contemporâneo do infarto do miocárdio com supradesnivelamento do segmento ST, fazendo com que, possivelmente, os desfechos de pacientes com cirurgia de revascularização prévia sejam semelhantes aos de uma população não selecionada de pacientes. Estudos adicionais, com maior poder, são necessários para corroborar ou refutar estes achados.
Fonte de financiamentoNão há.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
AgradecimentosAgradecemos aos colegas Carlos Roberto Cardoso, Cláudio Antonio Ramos de Moraes, Flavio Celso Leboute, La Hore Correa Rodrigues e Mauro Regis Silva Moura pela participação nos procedimentos de intervenção coronária percutânea primária.
A revisão por pares é da responsabilidade Sociedade Brasileira de Hemodinâmica e Cardiologia Intervencionista.