O desenvolvimento dos medicamentos antirretrovirais (ARV) segue a evolução do conhecimento sobre a infecção pelo vírus da imunodeficiência humana (HIV). Assim, como a indicação para o tratamento cada vez mais precoce é a tendência à medida que cresce o entendimento sobre a infecção, a qualidade dos ARV é cada vez melhor. A classe dos inibidores da integrase (INI), em sua totalidade, se insere nesse seguimento.
Desde a sua descrição inicial, ainda nos meados dos anos 1990, a inibição da integrase do HIV era esperada com grande expectativa, por ser uma enzima com maior conservação – isto é, apresenta menor variabilidade genética. Do ponto de vista teórico, por ser mais conservada, apresenta maior dificuldade para selecionar mutações associadas com resistência. Além disso, apresentava sinergismo de potência com os outros ARV, inclusive com vírus que apresentava resistência aos inibidores da transcriptase reversa.1-4
Embora tenha sido testada em humanos há mais de 30 anos,5 seu desenvolvimento apresentou diversas barreiras. Seus representantes iniciais apresentavam potência contra o HIV; todavia, além do elevado custo de produção, limitações farmacocinéticas (tais como pouca seletividade pela integrase, uso injetável e tempo de meia--vida extremamente curto) impediram seu uso clínico.
Como esperado, com o passar do tempo essas limitações foram superadas e novas moléculas de qualidade superior foram selecionadas e sintetizadas, e entraram nos estudos clínicos. Inicialmente, foram utilizados com sucesso no resgate do tratamento em pacientes multirresistentes.6-8 Posteriormente, de acordo com a expectativa, em função de suas características bioquímicas (avidez pela integrase), dificuldade da integrase em selecionar mutação de resistência em indivíduos sem tratamento prévio, potência, conveniência e segurança, mostram sua utilidade no tratamento inicial da infecção pelo HIV. Além disso, apresenta perfil de toxicidade mais limpo e tem sido pouco associado com inflamação, alterações lipídicas e dano em órgãos alvo, tais como coração, rim ou fígado.
A presente revisão tem como objetivo mostrar que os atuais representantes disponíveis dessa classe – raltegravir (RAL), elvitegravir (EVG) e dolutegravir (DTG) – merecem fazer parte da terapia antirretroviral (TARV) inicial da infecção pelo HIV.
Por que devemos considerar a utilização dos inibidores da integrase para o início da TARV?
Para que os integrantes da classe dos INI sejam colocados como agentes de primeira linha da TARV, eles devem mostrar que apresentam vantagens, nos estudos clínicos, sobre os atuais esquemas indicados na primeira linha ou tratamento inaugural da terapia anti-HIV. Esses estudos devem ter como critérios analisados seus possíveis desvios, limitações, robustez dos resultados, magnitude dos efeitos e qualidade de sua publicação.
É importante salientar uma característica especial da classe dos INI: sua utilização causa uma queda mais rápida na carga viral do indivíduo.
É importante salientar uma característica especial da classe dos INI: sua utilização causa uma queda mais rápida na carga viral do indivíduo.
Para esta análise, as questões PICO9 são consideradas:
• Pacientes e problema (infecção pelo HIV em adultos)
• Intervenção (TARV inicial)
• Comparador (versus efavirenz [EFV] ou inibidor da protease/ritonavir [IP/r])
• “Outcome” (desfecho; supressão viral, efeitos adversos)
Os representantes de classe serão descritos a seguir, conforme liberação para uso na prática clínica no tratamento da infecção pelo HIV em adultos.
Estudos que colocam os inibidores da protease para utilização no início da TARV
Raltegravir
Esse foi o primeiro INI a ser incorporado ao armamentário anti-HIV.
No entanto, antes de mostrar que pode ser indicado para o início do tratamento, o RAL demonstrou ser de extrema importância para o resgate de pacientes multiexperimentados.10 Posteriormente, por meio de estudos clínicos, tem comprovado sua utilidade em outras fases do tratamento da infecção pelo HIV.
Estudos clínicos randomizados
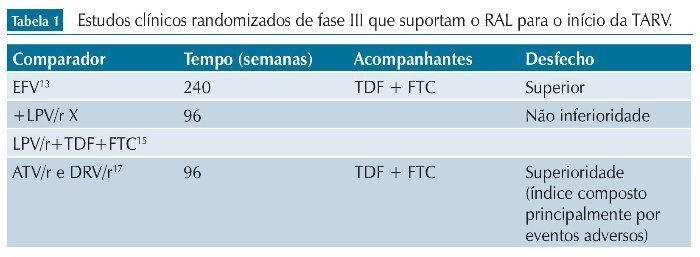
O primeiro estudo a demonstrar superioridade de algum INI para o início do tratamento foi o STARTMRK. Todavia, o caminho não foi tão simples assim. Após 96 semanas de estudo, o RAL, quando comparado ao EFV, mostrou que não era inferior e que os resultados eram comparáveis.11 Entretanto, após 156 semanas de estudo, ainda que a supressão viral e recuperação imunológica fossem comparáveis, os efeitos adversos e as alterações nos lipídios plasmáticos foram menores nos voluntários que utilizaram RAL,12 colocando-o como medicação para início do tratamento. A continuação desse estudo por 240 semanas, junto com outro estudo (fase II), mostra que após esse período o uso de RAL é superior ao de EFV.13,14
Posteriormente, o estudo Progress demonstrou que o RAL pode ser combinado com outras classes de medicações para o início da TARV. A utilização do RAL com lopinavir/ritonavir (LPV/r) foi equivalente à combinação tenofovir (TDF) + emtricitabina (FTC) + LPV/r.15 Além disso, após 96 semanas, a combinação de LPV/r + RAL não esteve associada com perda óssea, medida por meio do exame de densitometria e com menor perda na capacidade de filtração glomerular.16
Por fim, um estudo do ACTG (AIDS Clinical Trials Group) compara de maneira aberta (não cega) o RAL com darunavir/ ritonavir (DRV/r) com atazanavir/ritonavir (ATV/r) associados com TDF + FTC.17 Após 96 semanas, os indivíduos randomizados para ATV/r apresentaram maior abandono por evento adverso (basicamente por hiperbilirrubinemia) e menor taxa de supressão viral do que RAL e DRV/r. No entanto, quando a tolerabilidade e a resposta virológica são consideradas em conjunto, RAL apresenta superioridade. Nesse estudo, também fica demonstrado que o grupo que utilizou RAL apresentou menor dislipidemia e perda óssea do que aqueles que utilizaram IP/r (tabela 1).18
Grupos especiais O RAL apresenta uma vantagem sobre os outros representantes dos INI. Ele foi mundialmente testado em diversas situações de populações especiais.
O RAL é considerado um INI de primeira geração.
Pode ser utilizado da mesma maneira em homens ou mulheres. Sua utilização em gestantes está documentada e está associada com segurança, tolerabilidade e supressão viral.19 Nessa circunstância especial, talvez deva ser incluído como um dos medicamentos padrão.
Seu uso também está plenamente validado para o tratamento da coinfecção por tuberculose, inclusive com a utilização de rifampicina de modo concomitante.20 Sua dose não precisa ser modificada e pode representar uma alternativa importante à utilização do EFV.
Sua utilização está bem-documentada no tratamento, e de maneira concomitante, com os medicamentos antivirais contra o vírus da hepatite C, com diferentes fármacos utilizados, sem necessidade de modificação na dose.21
Da mesma forma, o RAL é o INI de indicação para pacientes pediátricos.22
Potenciais limitações
O RAL é considerado um INI de primeira geração. Sua utilização inicial se deu no resgate do tratamento, e somente após foi utilizado para o início da TARV. Assim, apresenta, atualmente, na comparação com seus similares, algumas limitações.
Seu perfil de resistência está bem-definido, e sua barreira genética contra mutações associadas com resistência não é elevada.23
Dessa forma, eventualmente, na falha do tratamento em esquemas que utilizam o RAL, embora não frequente em pacientes que iniciam TARV, pode haver resistência a esse fármaco. O desenvolvimento de mutações atreladas com resistência ao RAL está associada com resistência cruzada ao ELV. No entanto, na maior parte das vezes, o DTG permanece ativo. Portanto, em esquemas que utilizam o RAL, a detecção precoce da falha associada com mutações de resistência pode ser importante para preservar a atividade do DTG.
Comentários
O RAL ainda não pode ser administrado uma vez ao dia24 e não existe combinação com medicamentos fixos que incluem esse fármaco. Infelizmente, essas duas restrições ainda podem comprometer a adesão ao tratamento, fundamental para o seu sucesso. Por outro lado, é o INI com mais experiência clínica e segurança para uso em diversas populações especiais.
Elvitegravir
O EVG foi o segundo INI a ser testado clinicamente e liberado para uso geral. Como o RAL, o EVG é um INI de primeira geração e apresenta um perfil de resistência semelhante por ser o “irmão” mais velho. Atualmente, apresenta uma importante vantagem sobre seu antecessor: pode ser utilizado uma única vez ao dia quando coadministrado com /r ou cobicistat (COB), pois sua principal rota de metabolização é no CIP 450, isoenzima 3A4. Além disso, nos estudos clínicos foi utilizado em combinações em dose fixa com outros ARVs uma única vez ao dia, desde o início do seu desenvolvimento.
O EVG pode se tornar opção importante para o tratamento inicial da infecção pelo HIV.
Estudos clínicos randomizados Inicialmente, em um estudo de fase II, mostrou que era equivalente ao EFV e com menos eventos adversos no sistema nervoso central (SNC) ao final de 48 semanas.25
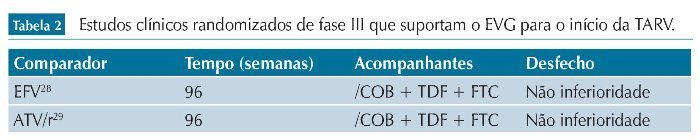
Logo após, em estudo de fase III utilizando combinações de ARVs em doses fixas uma única vez ao dia, mostrou equivalência ao EFV após 48 semanas.26 No mesmo período, também utilizando ARVs em combinações fixas, mostrou não ser inferior ao ATV/r para o início da TARV.27 Esses resultados puderam ser estendidos até a semana 96, sem que houvesse diferenças entre os tratamentos nesses dois estudos de fase III.28,29 Os resultados foram semelhantes até 144 semanas de um dos estudos (utilizando EFV como comparador) (tabela 2).30
Grupos especiais
Atualmente, não existem estudos publicados que abordem especificamente sua segurança e eficácia em populações especiais. Esse fato pode restringir seu uso em grupos específicos.
Nos estudos clínicos realizados e já publicados, funciona de maneira equivalente em homens ou mulheres.
Potenciais limitações
O EVG é um INI de primeira geração e compartilha resistência cruzada com o RAL. Entretanto, por ser coadministrado com /r ou COB, oferece maior dificuldade para o HIV selecionar resistência em pacientes sem TARV prévia. Isto é, para o início do tratamento, se houver falha viral, a chance de desenvolvimento de resistência ao EVG é baixa.
O EVG é coadministrado usualmente com COB. Essa substância é mais bem-tolerada que o /r; no entanto, pode diminuir a taxa de filtração glomerular e apresentar interações medicamentosas importantes com fármacos que utilizam o CIP450, isoenzima 3A4 como rota de metabolismo.
Comentários
O EVG pode se tornar opção importante para o tratamento inicial da infecção pelo HIV. Primeiro, existe combinação de ARVs em dose fixa, em comprimido único, administrado uma vez ao dia. Nessa combinação em dose fixa, o TDF (fumarato de disoproxil tenofovir) está sendo substituído pela tenofovir alafenamida (TAF) com sucesso.31 Isso representa a mesma eficácia clínica, mas sem toxicidade renal ou óssea, comumente associada com TDF. Enfim, esta é uma composição atrativa para o uso na prática clínica geral (sabendo das restrições do seu uso), principalmente se for de custo acessível e de acordo com a realidade atual do Brasil.
Dolutegravir
O DTG talvez tenha sido um dos medicamentos mais aguardados para o tratamento da infecção pelo HIV. Ele é um INI de segunda geração, com elevada barreira genética para mutações, e desde seus estudos pré-clínicos, mostra grande potência contra o HIV e um perfil farmacológico extremamente atraente, que permite uma dose baixa, uma vez ao dia, com poucos eventos adversos em indivíduos que iniciam TARV.32,33 Como será visto a seguir, ele demonstra superioridade aos seus comparadores em praticamente todos os estudos.
Estudos clínicos randomizados
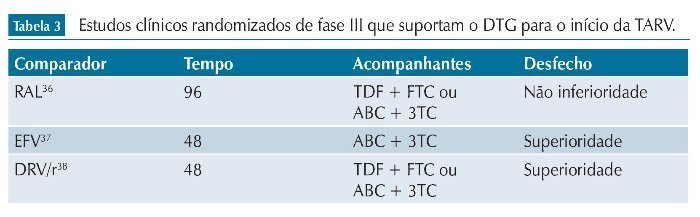
No estudo inicial, de fase II, mostrou que, independentemente da dose, era mais bem--tolerado que o EFV e apresentava o mesmo desfecho virológico.34 Posteriormente, num estudo de fase III, em 48 semanas mostrou sua equivalência com RAL para o início da TARV,35 que foi mantida após 96 semanas.36 Quase simultaneamente, outro estudo de fase III, agora com a utilização do EFV como comparador e abacavir (ABC) e lamivudina (3TC) como integrantes do comprimido em formulação com dose fixa única ao dia, o DTG já mostrou superioridade com apenas 48 semanas de estudo.37 O DTG, quando comparado ao darunavir/r (DRV/r), em um estudo aberto de fase III (com ABC + 3TC ou TDF + FTC, conforme a escolha do investigador), também mostrou superioridade (tabela 3).38
Grupos especiais
O DTG tem ação equivalente em homens ou mulheres.
O DTG já demonstrou sua utilidade e segurança no tratamento de resgate de crianças HIV-positivas.39 Recentemente, sua utilização em crianças com mais de 30 quilos e com mais de seis anos foi autorizada pelas autoridades legais dos Estados Unidos.40
Sua utilização em outras populações especiais não foi ainda devidamente comprovada.
Potenciais limitações
A potencial limitação é decorrente de sua “menor” experiência clínica. Ainda existe um potencial de interação medicamentosa, mas que é inferior ao EVG. Embora não esteja estabelecida sua nefrotoxicidade, seu uso está associado com diminuição na taxa estimada de filtração glomerular (por diminuir a taxa de excreção da creatinina urinária). Além disso, o DTG não é removível na hemodiálise.41
Comentários
O uso do DTG é extremamente atraente, principalmente no início da TARV. Ainda não foi documentado o desenvolvimento de mutações de resistência ao DTG em indivíduos que iniciam TARV. Aliás, em estudos, mutações associadas com 3TC e TDF previnem o desenvolvimento de resistência a esse ARV.42 Além disso, suas características farmacológicas permitem que seja utilizado em dose única, uma vez ao dia. Mais do que isso, pelo já exposto, talvez possa ter seu uso validado com uma combinação de compostos mais simples e menos tóxica para o indivíduos (como por exemplo: DTG + 3TC apenas, combinação fixa, uma vez ao dia).
Ainda não foi documentado o desenvolvimento de mutações de resistência ao DTG em indivíduos que iniciam TARV.
Conclusões
Pelo exposto neste artigo, parece claro que a classe dos INI deve ser incluída como primeira linha no tratamento da infecção pelo HIV. Tal afirmação é tão verdadeira, que a Organização Mundial da Saúde recomenda, em suas diretrizes, o DTG como opção para início da TARV.43
Com base nas evidências científicas, o EVG e o DTG devem ser indicados para a população geral e o RAL para os grupos específicos.
Apresentam boa tolerabilidade e são isentos, até o momento, de toxicidade metabólica. Nessa situação clínica é difícil a falha virológica com o desenvolvimento de mutações do HIV associadas com resistência. Com base nas evidências científicas, o EVG e o DTG devem ser indicados para a população geral e o RAL para os grupos específicos. Os ARVs para acompanhar os INI ainda devem ser melhor estudados, pois certamente EFV e TDF não mais se encaixam para o início da TARV com as opções que atualmente dispomos. Entretanto, que sejam, de preferência, de fácil utilização e sem efeitos adversos que comprometam o tratamento.