Este artículo es continuación de la revisión iniciada en el número anterior sobre la utilidad de la ecografía clínica abdominal en Atención Primaria (AP), y completa los escenarios de grandes vasos abdominales, bazo, nefrourológicos y ginecológicos.
This article is a continuation of the review initiated in the previous issue about the usefulness of point of care ultrasound in Primary Care, completing the scenarios of large abdominal vessels, spleen, nephrourological and gynecological ultrasound.
La ecografía es en la actualidad una técnica diagnóstica accesible al médico de familia (MF) para el abordaje de las enfermedades abdominales, como la enfermedad de los grandes vasos abdominales: aorta abdominal (AA) y vena cava inferior (VCI).
Los grandes vasos abdominales son fáciles de valorar mediante ecografía por sus características estructurales y su localización en el abdomen. Son estructuras lineales que contienen líquido y, por tanto, se observan en la ecografía como estructuras anecoicas. Además, facilitan la localización de los distintos órganos abdominales por la relación que mantienen con ellos.
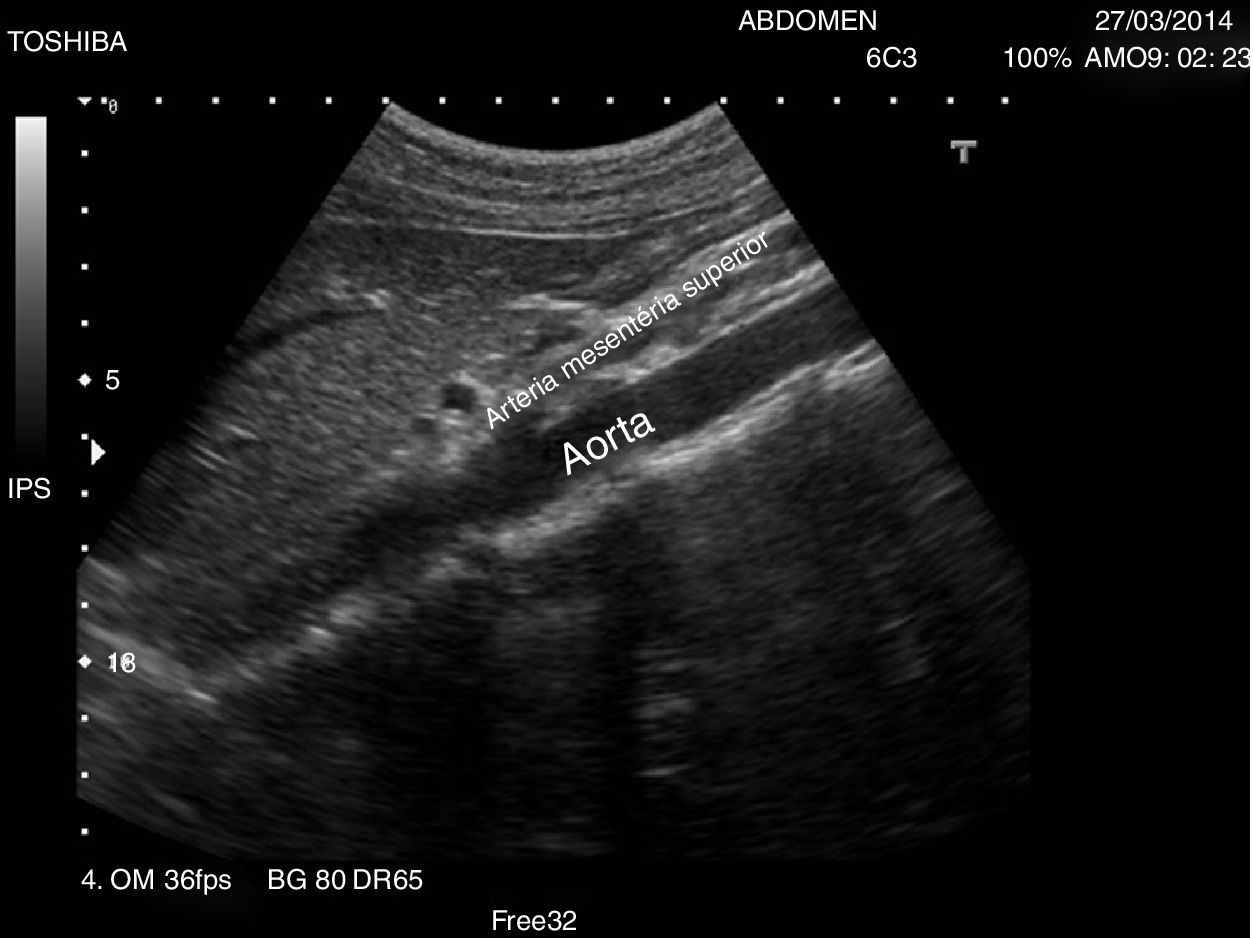
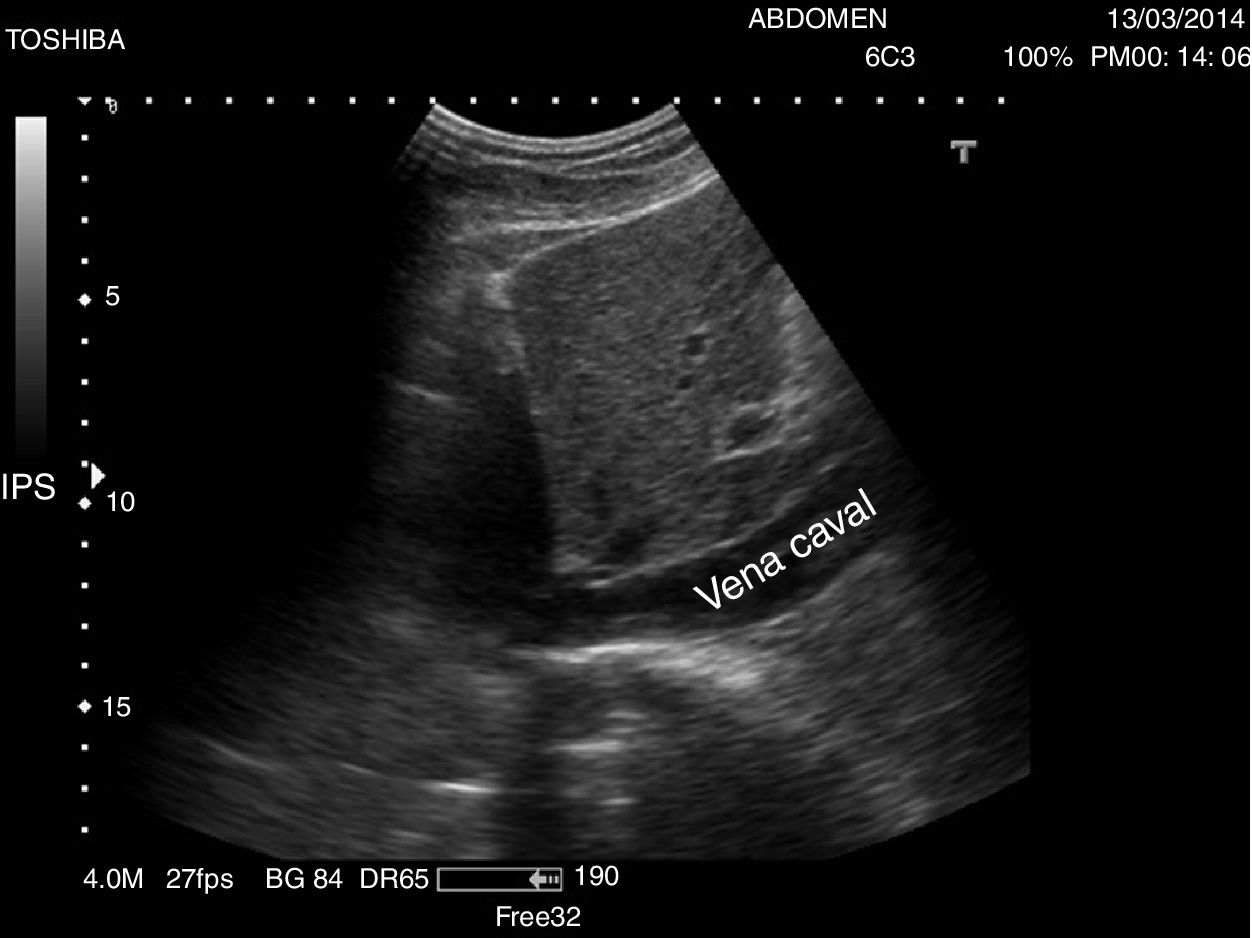
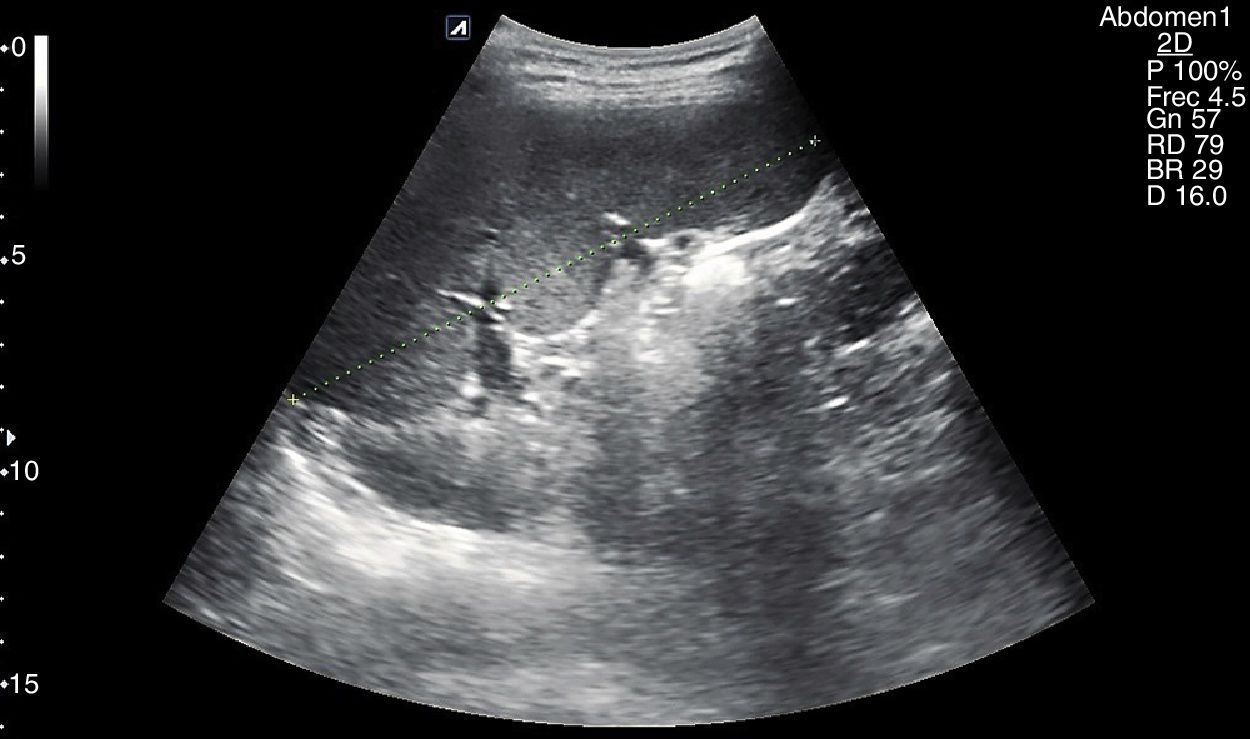
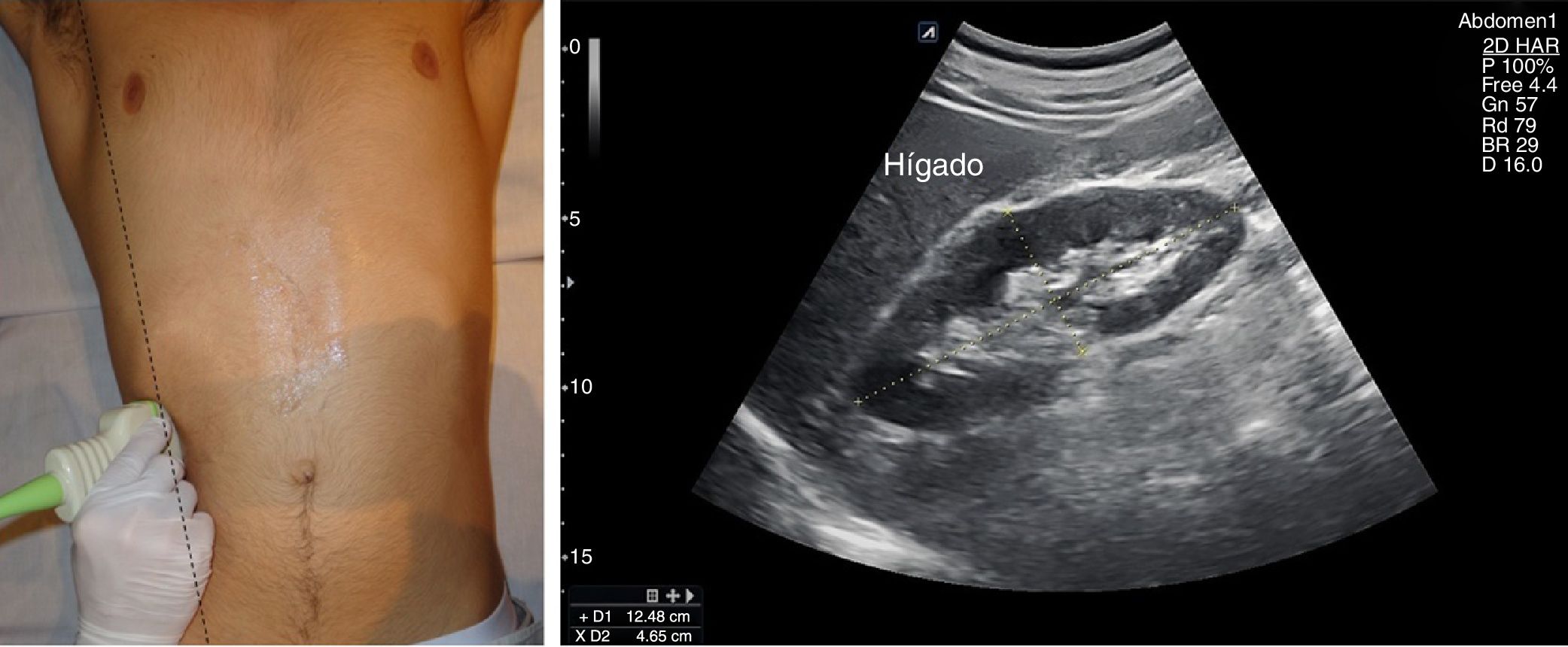
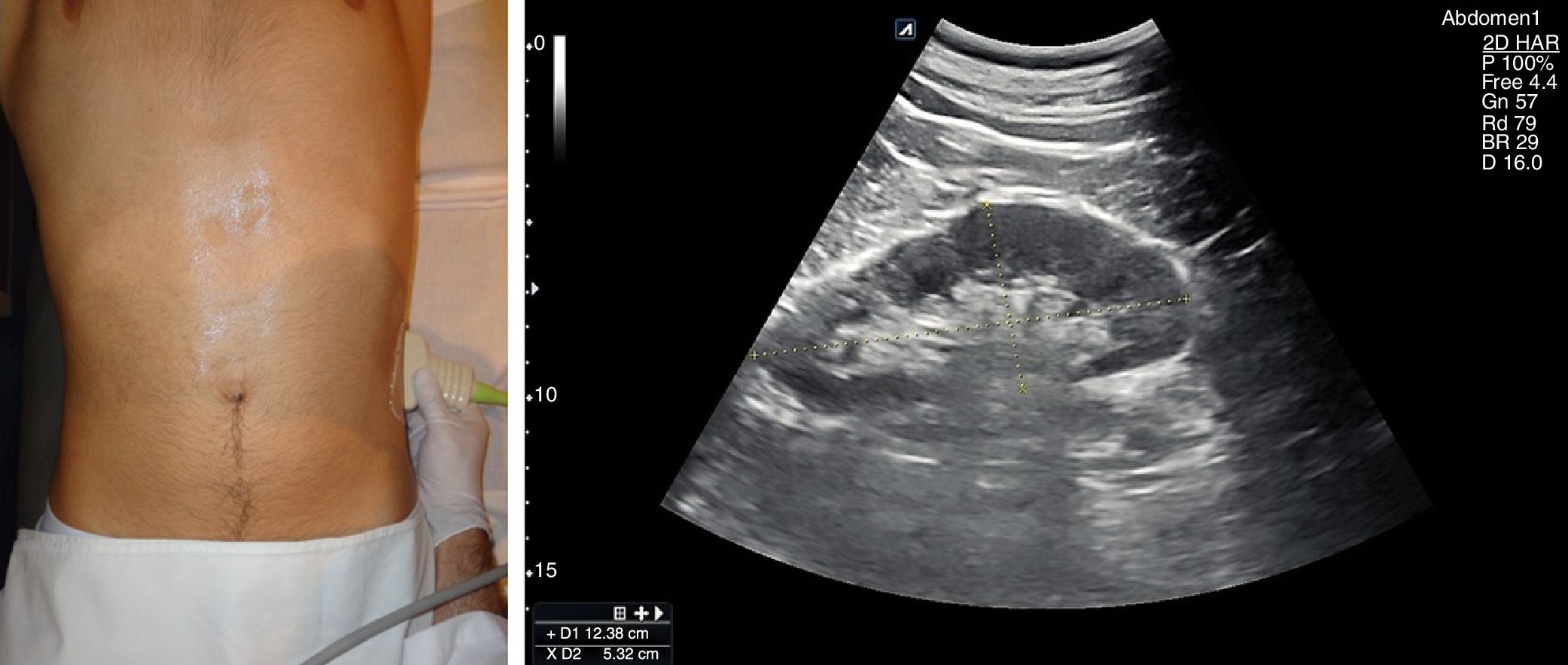
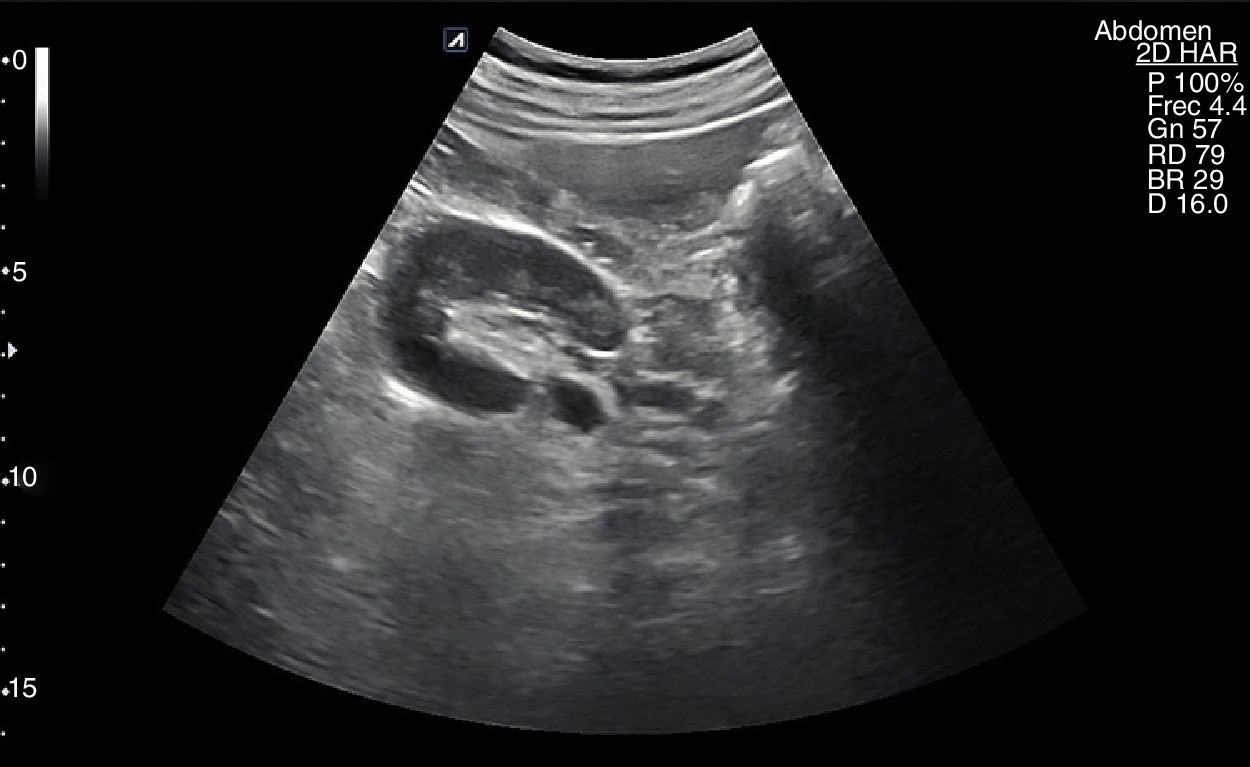
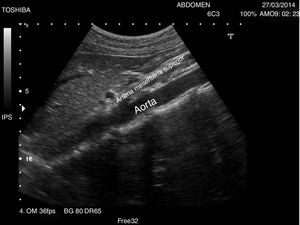
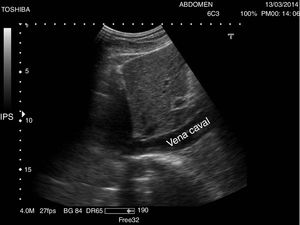
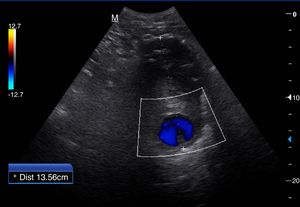
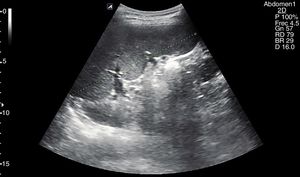
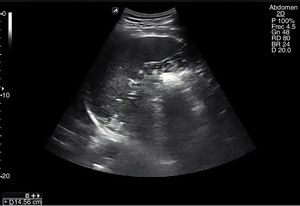
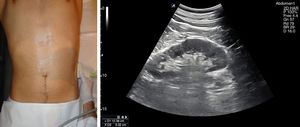
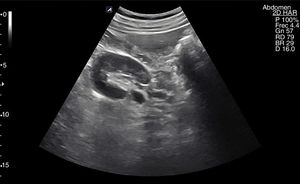
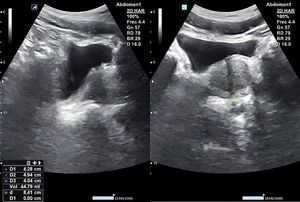
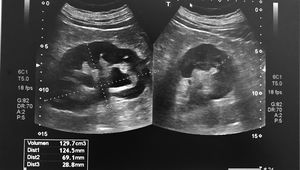
Se recomienda un ayuno de al menos 6-8 h para evitar la presencia de gas en el intestino que impida la visualización completa de los vasos. El paciente se situará en la camilla en decúbito supino y se realizarán cortes ecográficos longitudinales, ligeramente a la izquierda de la línea media abdominal para la exploración de la AA (fig. 1) y ligeramente a la derecha para la exploración de la VCI (fig. 2). El estudio se complementará con cortes transversales (fig. 3), similares a los utilizados en el páncreas a nivel de línea media abdominal en el epigastrio, deslizando la sonda hasta el hipogastrio siguiendo el trayecto craneocaudal de los vasos.
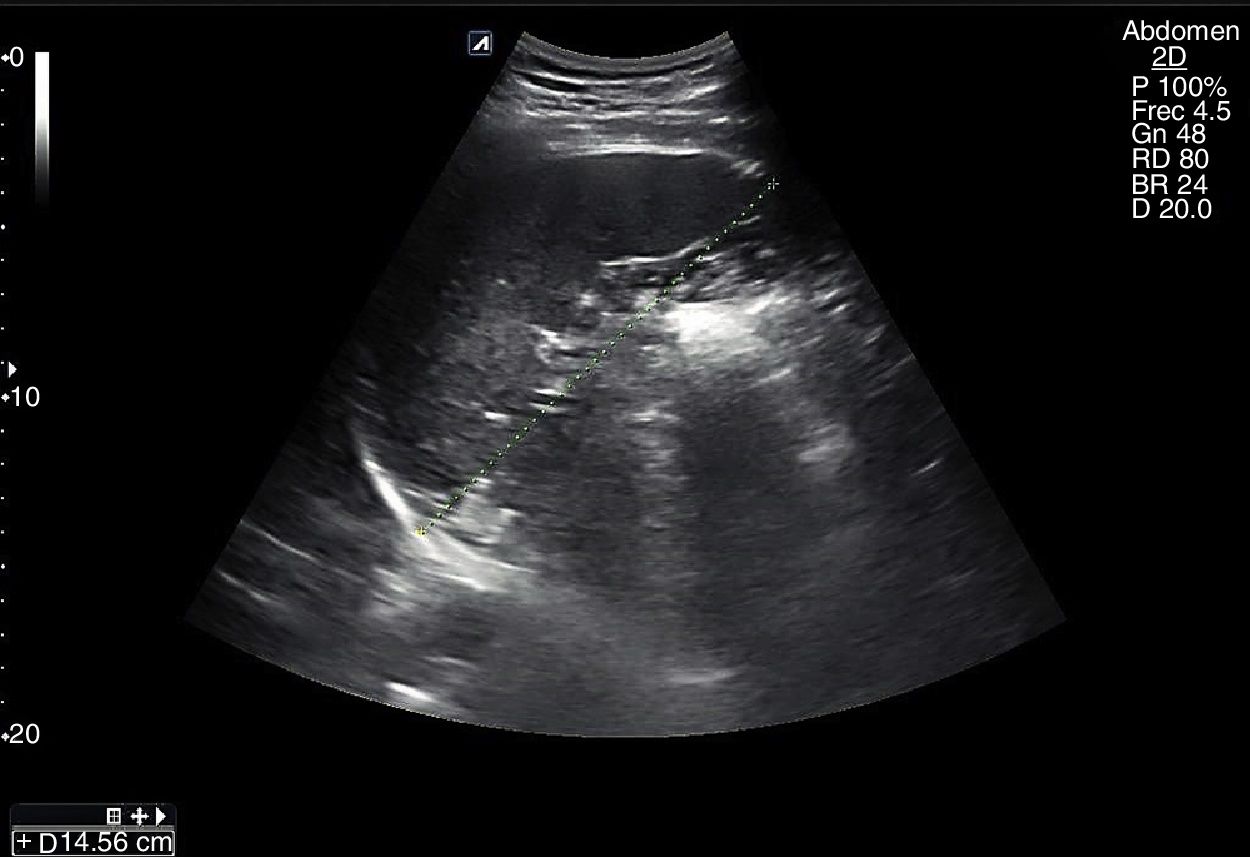
La AA recorre el abdomen longitudinalmente desde su entrada a través del hiato diafragmático hasta su bifurcación a nivel caudal en las 2arterias ilíacas y da lugar durante su trayecto a los siguientes vasos identificables mediante ecografía en orden craneocaudal: tronco celíaco, arteria mesentérica superior, arteria renal izquierda y derecha y arteria mesentérica inferior. De sección casi circular, su diámetro mayor en abdomen no debe superar los 3cm: es identificativo de aneurisma un diámetro superior a esta cifra1.
La VCI se forma por la confluencia de los troncos venosos ilíacos y recorre el abdomen en dirección caudocraneal, a la derecha de la aorta. Las venas renales izquierda y derecha y las venas suprahepáticas son los vasos tributarios de la VCI visibles en ecografía.
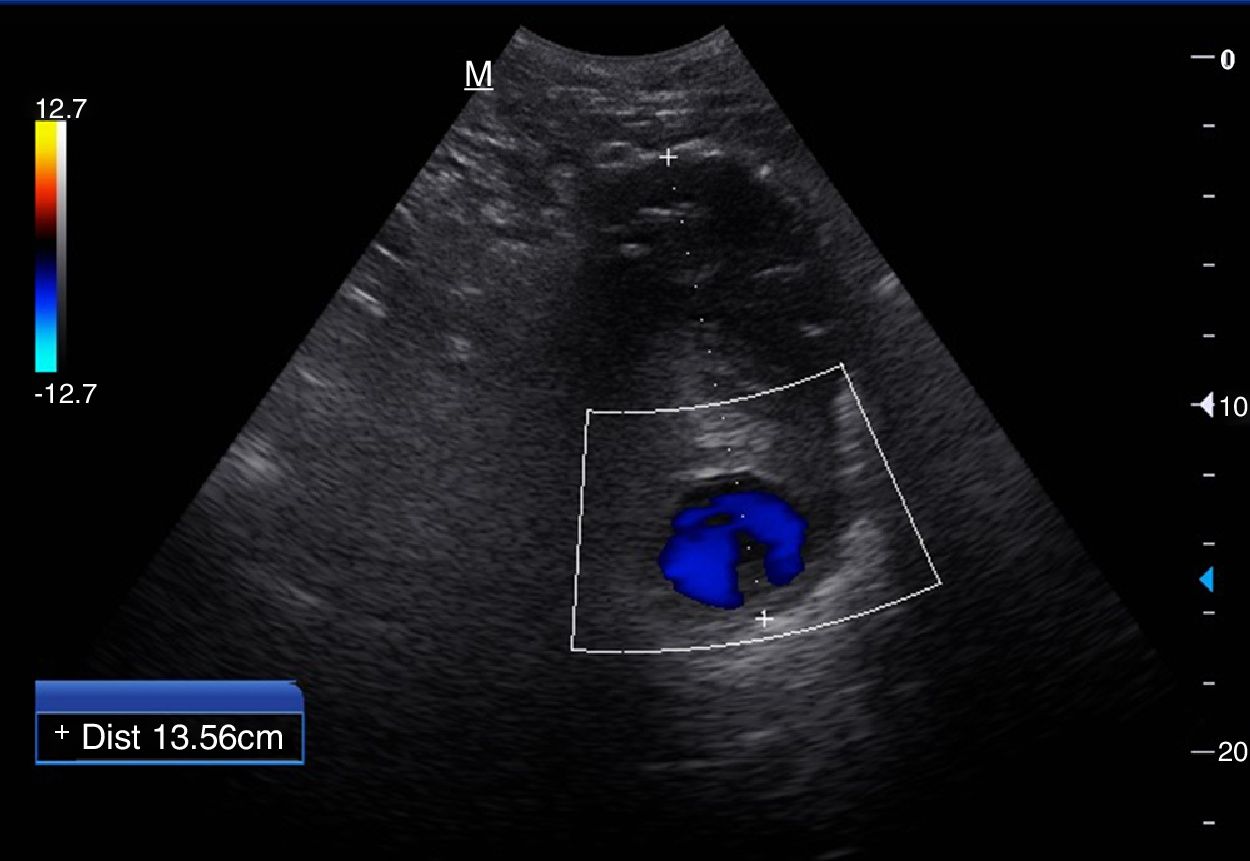
Escenarios clínicos en Atención Primaria y evidenciaSegún la evidencia científica disponible, el escenario clínico ideal para la ecografía abdominal de grandes vasos por el MF es el cribado de aneurisma de AA (AAA). La ecografía abdominal ha demostrado ser el método de imagen diagnóstico de elección para el diagnóstico del AAA (fig. 3), con una sensibilidad mayor del 95% y una especificidad cercana al 100%2,3. Diferentes estudios multicéntricos y metaanálisis han demostrado la efectividad del cribado de AAA mediante ecografía abdominal (disminución de mortalidad por AAA), incluso en AP2-11.
Según la US Preventive Services Task Force, la realización de ecografía abdominal de cribado de AAA en hombres de entre 65 y 75 años que alguna vez hayan fumado tiene un nivel de evidencia 1A2. Existen también diferentes guías de práctica clínica que recomiendan cribado en AP3,8,9.
Algunos estudios correlacionan el calibre de la VCI y su modificación durante la inspiración directamente con la volemia, los datos hemodinámicos del ventrículo derecho y la presión intratorácica. En ellos se ha demostrado que en pacientes con depleción de volumen el diámetro de la VCI está disminuido y su grado de colapsabilidad (índice cava) está aumentado respecto a pacientes normovolémicos o con aumento del volumen intravascular12. Sin embargo, otros estudios consideran que la medida de la VCI no puede constituirse, en pacientes críticos, como un sustituto de la medida de la presión venosa central13.
Utilidad de la ecografía clínica de los grandes vasos abdominales en Atención PrimariaLa ecografía abdominal ha demostrado ser un método diagnóstico, en manos de MF entrenados y formados para ello, muy sensible y específico para el cribado del AAA en pacientes varones de entre 65 y 75 años y con antecedentes de tabaquismo. El cribado en AP de esta entidad ha demostrado, además, ser costo eficiente y posiblemente sea la única forma de realizar este cribado sin sobrecargar los servicios hospitalarios.
La ecografía abdominal puede ser considerada como un buen método para estimar la existencia de hipovolemia en pacientes no críticos y puede ser utilizada por el MF en AP, sobre todo en el ámbito de urgencias, para valorar el estado volémico y monitorizar la respuesta a diuréticos de los pacientes crónicos complejos. Ambos escenarios se resumen en la tabla 1.
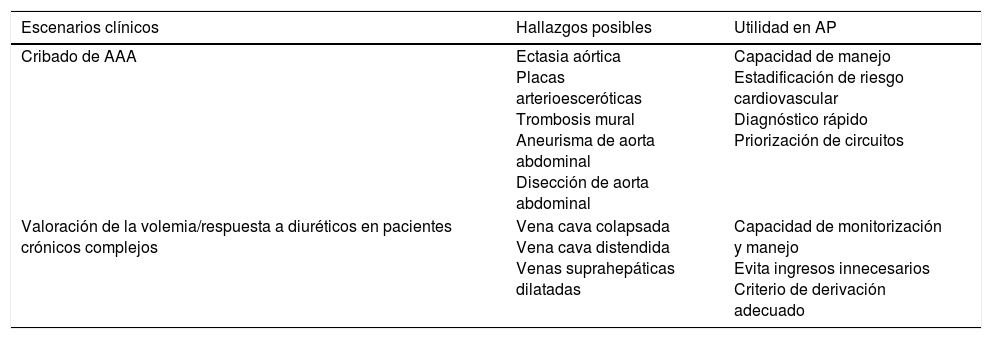
Escenarios clínicos y hallazgos ecográficos de grandes vasos abdominales en AP
| Escenarios clínicos | Hallazgos posibles | Utilidad en AP |
|---|---|---|
| Cribado de AAA | Ectasia aórtica Placas arterioesceróticas Trombosis mural Aneurisma de aorta abdominal Disección de aorta abdominal | Capacidad de manejo Estadificación de riesgo cardiovascular Diagnóstico rápido Priorización de circuitos |
| Valoración de la volemia/respuesta a diuréticos en pacientes crónicos complejos | Vena cava colapsada Vena cava distendida Venas suprahepáticas dilatadas | Capacidad de monitorización y manejo Evita ingresos innecesarios Criterio de derivación adecuado |
Aunque la TC y la RM son las técnicas de elección para evaluar el bazo y las estructuras que lo rodean, la ecografía es particularmente útil en su estudio. Debido a que su ecogenicidad es muy uniforme, las anomalías de su parénquima destacan claramente, así como las colecciones líquidas periesplénicas14.
El bazo se sitúa intraperitoneal, por debajo del ángulo costofrénico izquierdo y por encima del riñón izquierdo, del ángulo esplénico del colon, cola del páncreas y del estómago. Una referencia útil para localizarlo es la vena esplénica, que además identifica el hilio, en cuya estrecha vecindad se localiza la cola del páncreas, de modo que el bazo es una perfecta ventana ecográfica para localizarla15.
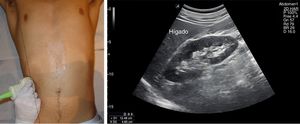
No es necesaria ninguna preparación, pero el ayuno facilita su estudio. El paciente estará en decúbito supino, y realizaremos un abordaje oblicuo intercostal a nivel de línea axilar posterior izquierda, con el que obtenemos una sección coronal del órgano, suficiente para evaluar su interior y su tamaño (fig. 4). Es habitual encontrar sombras por la interposición de los arcos costales, que evitamos rotando el eje mayor de la sonda paralelo al espacio intercostal. A veces es necesario un abordaje subcostal o en línea axilar anterior con el paciente en decúbito lateral derecho, favorecido por una inspiración profunda y mantenida16.
El tamaño del bazo se puede determinar mediante corte longitudinal y transversal, así como midiendo el área en sección longitudinal por planimetría. Se consideran normales medidas <12cm en longitudinal (superiores a 12 o 13cm según la constitución del sujeto se consideran claramente patológicas), <5cm en transversal y un área longitudinal <50-55cm2. Su ecogenicidad es muy uniforme, y algo mayor que la del hígado, aunque este último parezca más denso por su mayor contenido en vasos reflexivos.
Escenarios clínicos en Atención Primaria y evidenciaLa ecografía del bazo puede ser útil al MF en todas aquellas situaciones en las que se precise diagnosticar o excluir una anomalía esplénica (por ejemplo, confirmar una esplenomegalia detectada en la exploración física), así como en aquellas en las que forma parte de la exploración sistematizada del abdomen, en los traumatismos toracoabdominales y en el seguimiento de lesiones conocidas. Su exploración minuciosa se requiere también en pacientes con linfoma17. El estudio ecográfico del bazo puede además mostrar otros hallazgos como quistes, abscesos o infartos esplénicos18,19.
La ecografía clínica se ha mostrado útil para la valoración de la esplenomegalia (fig. 5) tanto mediante uso de equipos ecográficos convencionales como de bolsillo20 con una elevada correlación (r=0,89) entre radiólogos y otros especialistas, incluso por médicos residentes (r=0,81)21, aunque existen estudios que muestran una menor concordancia entre MF y ecografistas expertos en cuanto a la valoración del bazo22 respecto a otros órganos abdominales. En el seguimiento de hepatopatías conocidas también es útil la evaluación esplénica23.
Utilidad de la ecografía clínica del bazo en Atención PrimariaLos escenarios más habituales en los que la ecografía del bazo resulta útil al MF se ilustran en la tabla 2. Dado que el bazo se suele comportar como un «órgano mudo» que rara vez es protagonista del cuadro clínico que lo afecta, es necesario incluir su estudio en todas las exploraciones abdominales de forma sistemática. Los hallazgos permitirán al MF un enfoque diagnóstico rápido e inmediato de la normalidad y las alteraciones morfológicas, le permitirá orientar la causa y motivar la solicitud de nuevas exploraciones y derivaciones a otros especialistas, así como justificar el empleo de circuitos de priorización o atención urgente en el ámbito hospitalario.
Escenarios clínicos y hallazgos ecográficos del bazo posibles en AP
| Escenarios clínicos | Hallazgos ecográficos | Utilidad en AP |
|---|---|---|
| Esplenomegalia | Bazo > 12cm o área > 55 cm2 | Diagnóstico rápido Orientación etiológica - Área > 100 cm2: neoplasia hematológica - Lesiones focales: linfoma, metástasis, quiste, absceso, hematoma, sarcoidosis - Adenopatías: linfoma - ↑circulación colateral en el abdomen: hipertensión portal (causa más frecuente en AP) Derivación motivada y priorizada |
| Hallazgos incidentales | Bazo supernumerario, bazo ectópico, asplenia, poliesplenia Quistes con pared (hidatídicos, congénitos) Quistes sin pared (pseudoquistes) | Diagnóstico rápido Orientan diagnóstico y posibles cuadros malformativos Derivación motivada |
| Sospecha de linfoma | a) Afectación difusa microscópica no detectable por ecografía b) Esplenomegalia difusa sin lesiones focales c) Esplenomegalia con lesiones focales casi siempre de aspecto hipoecogénico | Ayuda al diagnóstico Orienta al tipo de linfoma en muy expertos Derivación urgente y motivada |
| Traumatismos toracoabdominales | Líquido libre en receso esplenorrenal Imagen de doble contorno subcapsular Imagen hipoanecoica lineal Imagen hipoecoica mal delimitada | Diagnóstico rápido orientado a: - Sangrado en cavidad abdominal - Hematoma subcapsular - Laceración/rotura de bazo - Hematoma esplénico Derivación motivada Urgencia motivada |
Para la visualización de los riñones y de la vejiga urinaria utilizamos una sonda convex de 3,5 a 5MHz, con el paciente en decúbito supino. La valoración de la vejiga exige además su repleción por orina, para lo que basta la ingesta de unos 2-3 vasos de agua una hora antes de la exploración.
El riñón derecho se estudia situando la sonda perpendicular a las costillas, a nivel de la línea axilar anterior derecha (fig. 6). El hígado nos será útil como ventana acústica. Se debe valorar su longitud y después rotar la sonda para obtener una proyección transversal (eje corto) y angular, con la sonda recorriendo los planos para medir sus dimensiones y realizar una visualización completa.
El riñón izquierdo, en general de tamaño algo mayor, suele estar ubicado más alto que el derecho y parcialmente oculto por las costillas: es más difícil su valoración debido al aire de la cámara gástrica y de las asas intestinales del colon transverso y del ángulo esplénico del colon. Su abordaje ecográfico es más fácil a nivel de línea axilar posterior izquierda, en un corte intercostal o subcostal oblicuo (fig. 7).
Para mejorar la visualización de los riñones es muy útil que el paciente mantenga una inspiración profunda, con la que el riñón desciende y evita la sombra de las costillas y gases del tubo digestivo. Otra opción es colocar al paciente en decúbito lateral izquierdo o derecho (para estudiar el riñón contralateral) o mejorar la ventana situando la sonda entre las últimas costillas.
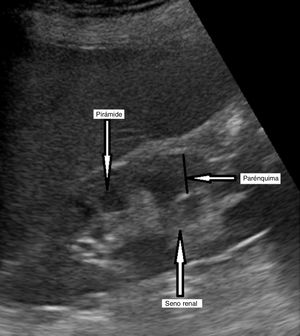
El riñón sano mide 10-12cm de longitud y 4-5cm de anchura (se relaciona con peso y talla); el izquierdo es discretamente mayor que el derecho. Es significativa una diferencia >1,5-2cm de longitud entre ambos riñones. En el eje transverso el riñón tiene forma de letra C (fig. 8), abierta hacia el hilio renal, útil para evaluar la posible dilatación del sistema excretor, así como los vasos renales. El grosor cortical normal mide alrededor de 1,1 ± 0,9cm y disminuye con la edad y con las situaciones que ocasionan pérdida de nefronas.
La ecogenicidad del parénquima se valora comparando los del riñón derecho e izquierdo con los de hígado y bazo, respectivamente; el riñón sano es menos ecogénico (menos brillante) que dichos órganos. Con la edad, el riñón se vuelve más hiperecogénico, presumiblemente debido a fibrosis parenquimatosa.
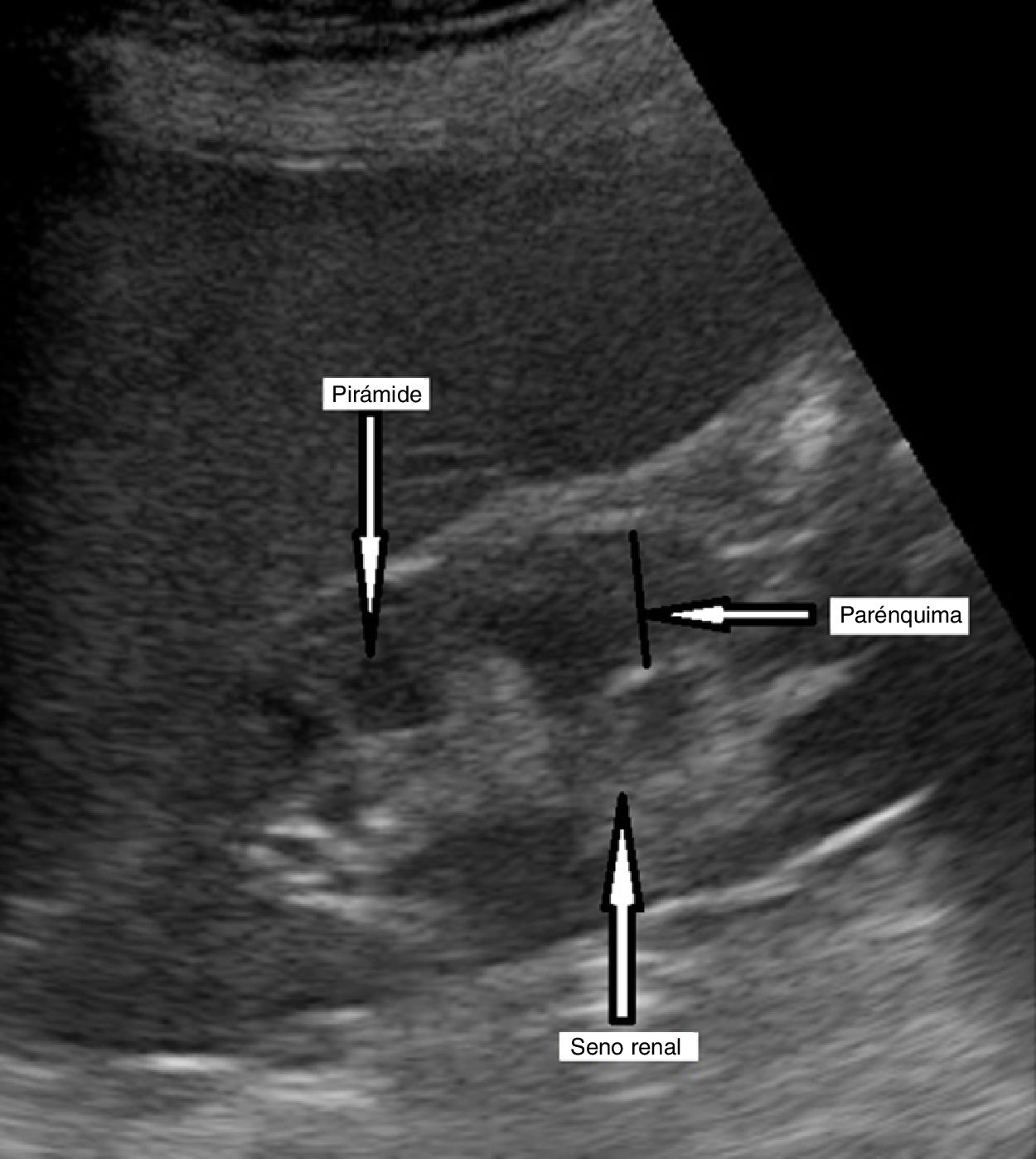
La médula renal está constituida fundamentalmente por pirámides que no conectan entre sí, cuyo vértice apunta hacia la pelvis renal, que es menos ecogénica que la corteza. En una ecografía, estas estructuras se denominan parénquima renal y engloban la corteza y las pirámides medulares (fig. 9).
El seno renal normal se visualiza como una elipse hiperecogénica en el centro del riñón, formado por el sistema colector, ramas principales de la arteria y vena renal y grasa. El sistema pielocalicial y los uréteres no son visibles en situaciones normales.
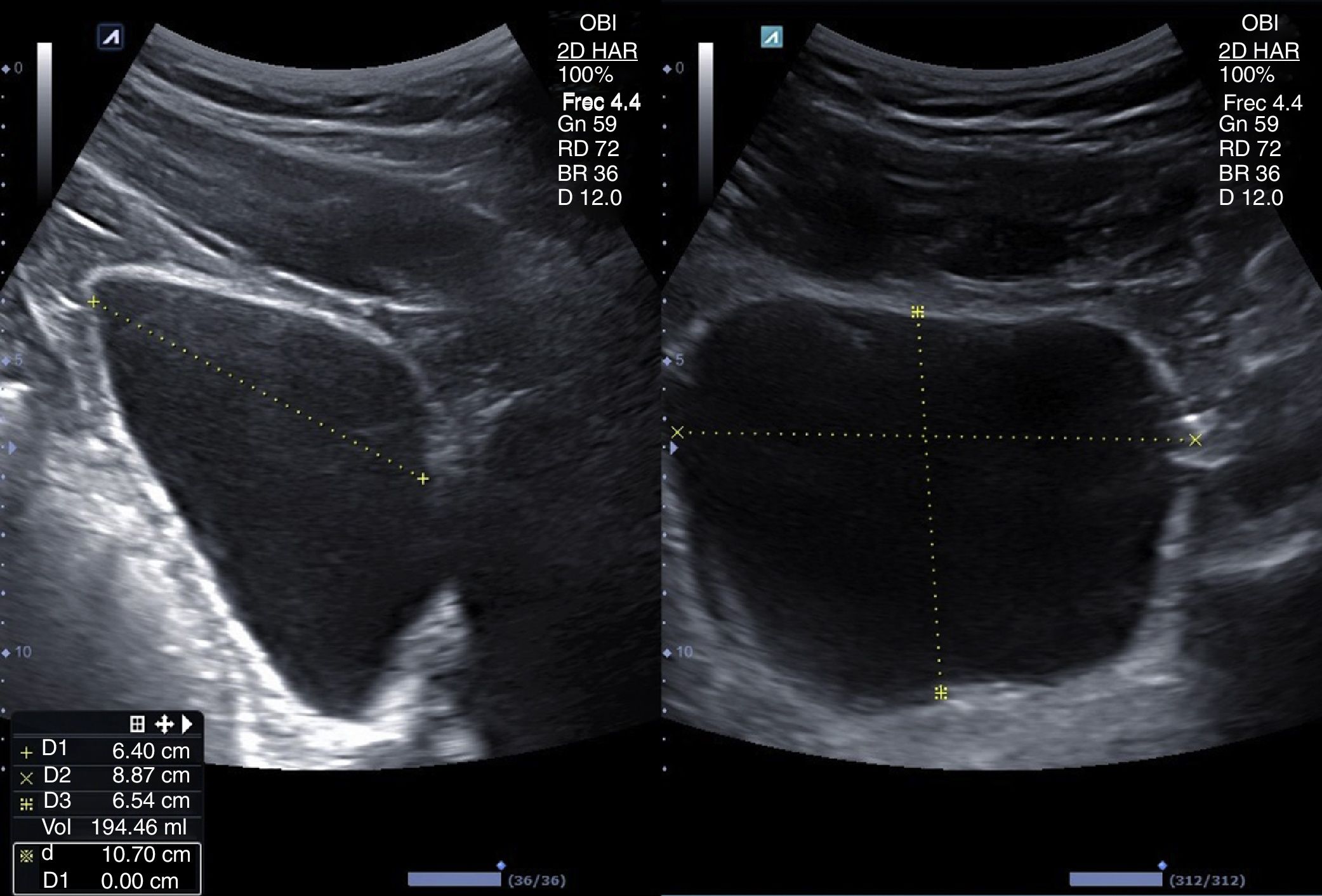
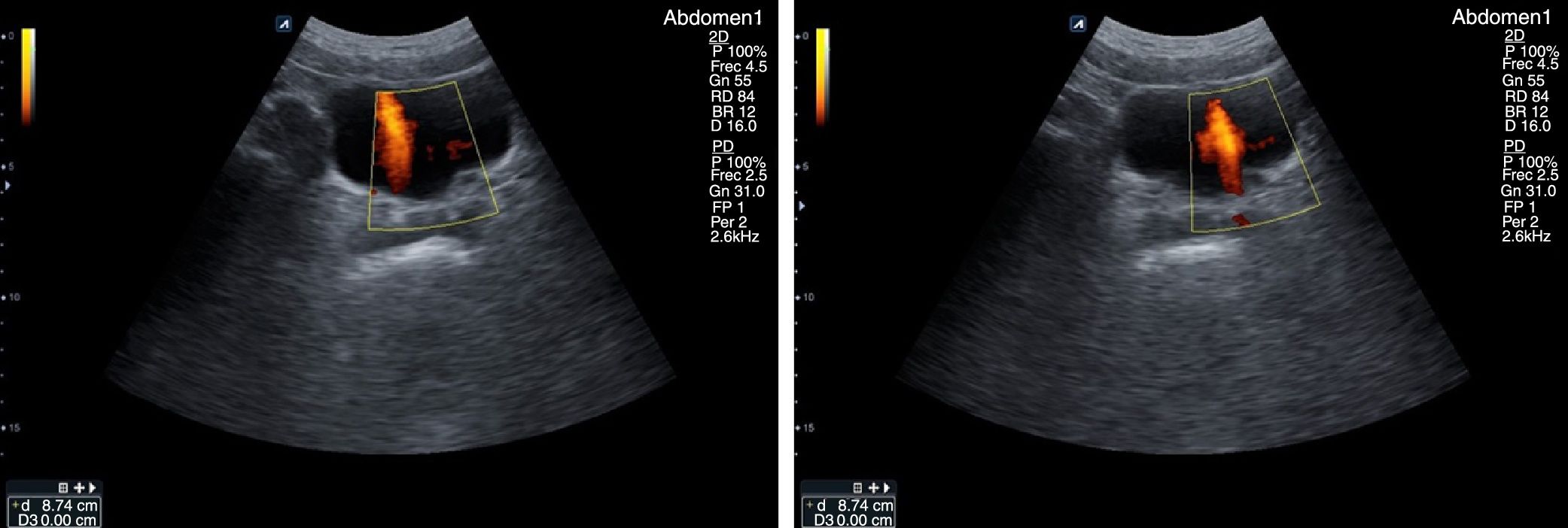
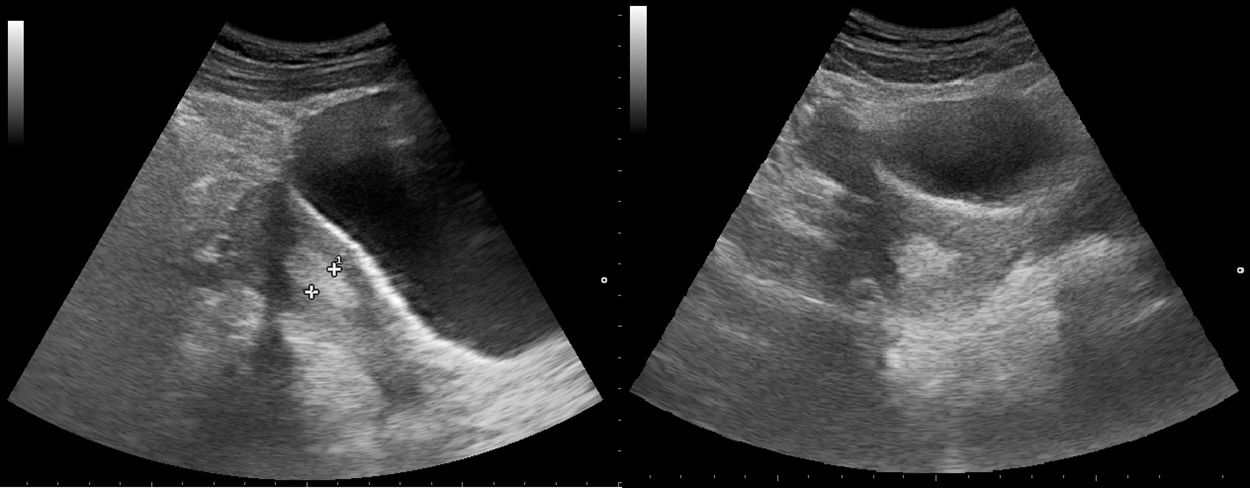
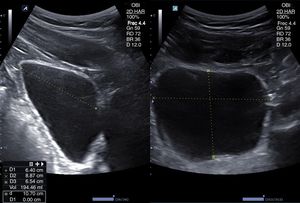
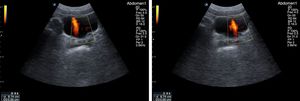
La vejiga se sitúa en la pelvis. Para su estudio se angula la sonda hacia el vértice vesical, barriendo el corte longitudinal para su completa visualización, y se rota el transductor 90° sobre su eje vertical para valorar el corte transversal. La vejiga llena es anecoica, tiene forma triangular en sección longitudinal y ovalada o cuadrangular en sección transversal y muestra un refuerzo acústico posterior (fig. 10). En su vértice inferior se puede visualizar el meato uretral y, en su pared posteroinferior, el relieve de la embocadura de los uréteres, lugares donde podemos visualizar litiasis en cuadros de cólicos renales expulsivos. Además, la observación de jet ureteral de llenado mediante Doppler (fig. 11) indica permeabilidad del uréter y del sistema excretor renal del mismo lado. Cuando se contrae, la pared normal se engruesa de manera uniforme. El grosor de la pared normalmente replecionada no debe superar los 6mm y no es valorable con la vejiga vacía, en la que se observan pliegues y engrosamientos asimétricos sin significado clínico.
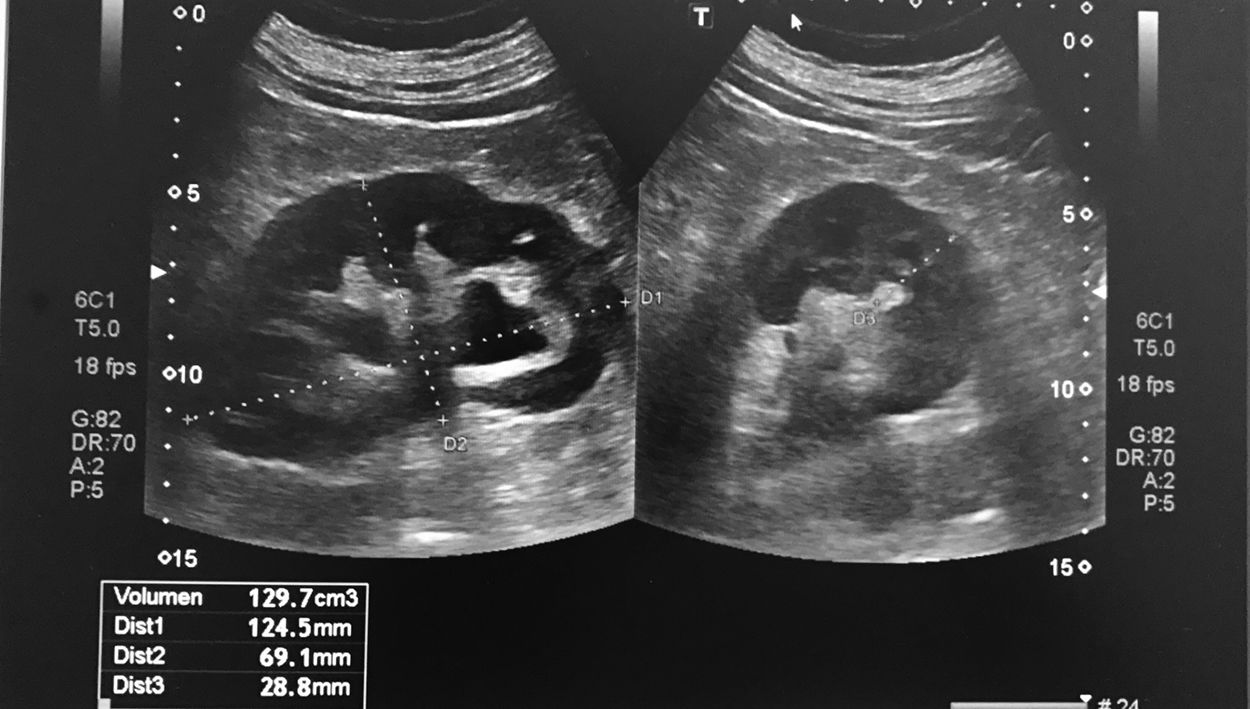
La próstata es un órgano impar situado bajo la vejiga, con forma de castaña o pirámide invertida, ecogenicidad homogénea y contorno regular. Se explora con la vejiga replecionada, apoyando la sonda en su borde inferior sobre la sínfisis del pubis apuntando hacia el vértice vesical y realizando una presión moderada. Se estudia en sentido longitudinal y transversal, y se necesitan ambos planos para el cálculo de su volumen (fig. 12). Sus dimensiones normales son próximas a 5cm de diámetro transversal en la base, 2cm en anteroposterior y 3cm de longitud craneocaudal, para un peso aproximado de 20 g en el adulto joven. La determinación del volumen prostático mediante ecografía abdominal suprapúbica se ha mostrado tan precisa como la transrectal24,25, además, es menos laboriosa y mejor tolerada. Estas dimensiones aumentan a lo largo de la vida. El estudio del varón con síntomas del tracto urinario inferior debe incluir también la medida del residuo posmiccional.
Escenarios clínicos en Atención Primaria y evidenciaLa ecografía renoureteral se utiliza en presencia de un cuadro clínico sugerente de origen nefrourológico. El dolor cólico en fosas renales o flancos irradiado o no a pelvis, la hematuria, las alteraciones de la función renal o del sedimento urinario, las infecciones urinarias de repetición y los síntomas del tracto urinario inferior en varones son escenarios al alcance del MF26,27 (tabla 3).
Escenarios clínicos y hallazgos ecográficos nefrourológicos frecuentes en AP
| Escenarios clínicos | Hallazgos posibles | Utilidad en AP |
|---|---|---|
| Dolor cólico en fosa renal o flanco | Litiasis renal, dilatación de sistema excretor, cálculos ureterovesicales, centelleo Doppler, hipertrofia de próstata, coágulos vesicales Aneurisma de aorta abdominal | Confirmación diagnóstica Valoración de posibles complicaciones Capacidad de manejo clínico Derivación motivada y priorizada |
| Dolor en fosa renal y fiebre que no evoluciona bien | Aumento de tamaño renal, compresión del seno renal, pérdida de la diferenciación corticomedular, gas en pelvis renal, lesiones hiperecoicas focales | Orientación diagnóstica Capacidad de manejo clínico Derivación motivada y priorizada |
| Alteración de las pruebas de función renal o del sedimento urinario | Valoración de ecogenicidad y grosor cortical, tamaño renal Presencia de masas o lesiones focales sólidas, o quísticas Enfermedad quística renal | Orientación diagnóstica Correlación con los datos del laboratorio Derivación motivada Prioridad de la derivación |
| Hematuria | Presencia de masas o lesiones focales sólidas o quísticas Valoración de la pared vesical Identificación de litiasis renal o centelleo | Orientación diagnóstica Correlación con los datos del laboratorio Derivación motivada Prioridad de la derivación |
| Infecciones urinarias de repetición | Malformaciones de sistema excretor Hiperplasia prostática | Orientación diagnóstica Derivación orientada Capacidad de manejo |
Síntomas de tracto urinario inferior en el varón | Volumen prostático Residuo posmiccional Vejiga de lucha Divertículos vesicales Litiasis vesical | Capacidad de manejo Orientación diagnóstica Derivación motivada |
La ecografía presenta elevada sensibilidad para detectar agenesia renal, determinar el tamaño o volumen renal (atrofia, hipoplasia, hipertrofia renal), detectar la presencia de malformaciones o variantes anatómicas, valorar la corteza y la médula renal, evaluar la vascularización renal, la presencia de lesiones focales sólidas o quísticas y poner de manifiesto la presencia de litiasis. Estas se han de buscar en los cálices o pelvis renal, unión pieloureteral, embocadura ureterovesical o en la vejiga, y cuando no son visibles se pueden inferir por la presencia de dilatación pielocalicial o ureteral proximal a la obstrucción. La presencia de orina permite la valoración de la vejiga, su pared, y la forma y tamaño de la próstata.
El sistema pielocalicial normalmente no es visible en ecografía, al igual que los uréteres, por lo que su visualización indica ectasia o hidronefrosis obstructiva. La visualización de las paredes vesicales nos puede indicar su normalidad, la presencia de signos de lucha (indentación en la cúpula de los haces fibrosos del músculo detrusor que le dan un aspecto serrado) o la presencia de un pólipo o tumoración.
Aunque los consensos actuales no consideran la ecografía como prueba de primera intención en el varón con síntomas de tracto urinario inferior28, probablemente por su escasa disponiblidad y la gran demora de los servicios de diagnóstico de referencia, su uso cuando está disponible es de un gran valor para evaluar su volumen (criterio de progresión de la hiperplasia benigna de próstata), la presencia de complicaciones (divertículos, litiasis) y el residuo posmiccional (criterio de gravedad de la obstrucción e indicación quirúrgica cuando supera los 150ml).
Utilidad de la ecografía clínica nefrourológica en Atención PrimariaLa ecografía es la prueba de elección en la mayoría de las dolenciasrenoureterales y, por su inocuidad, disponibilidad y bajo coste, debe ser la primera en realizarse y la única necesaria en muchas ocasiones29.
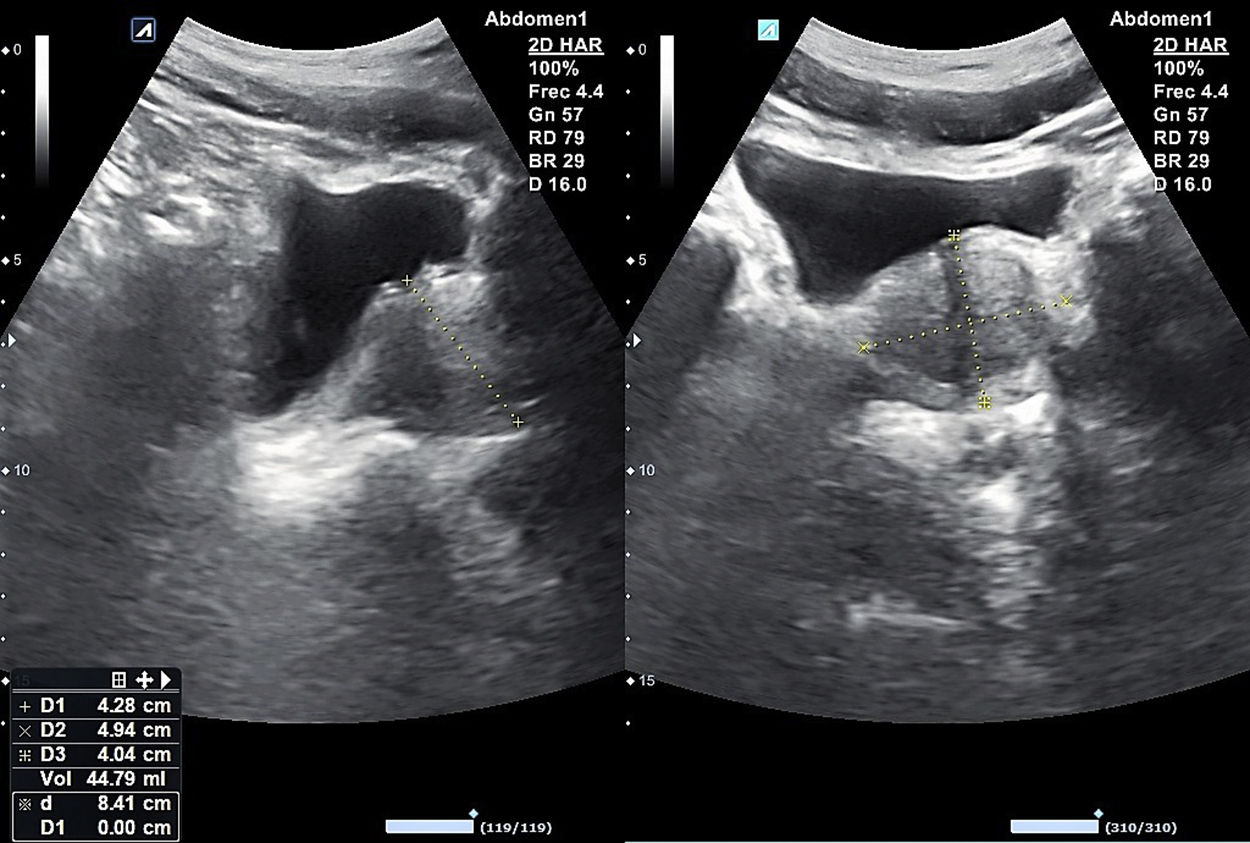
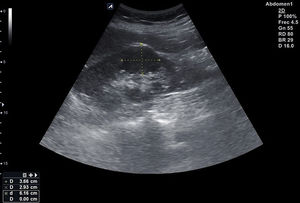
El diagnóstico a tiempo de la hidronefrosis (fig. 13) en el cólico nefrítico y en la insuficiencia renal aguda es de gran valor y puede modificar el tratamiento con rapidez y, con ello, la evolución30-32. La ausencia de pielectasia grave y la identificación de la progresión de la litiasis en exploraciones seriadas permite al MF el manejo clínico del cólico renal hasta su resolución sin necesidad de derivación.
Algunos trabajos han puesto de manifiesto que emplear la ecografía como primera prueba en el cólico renal en lugar de TAC puede suponer un gran ahorro económico y que, por tanto, no solo proporciona un enfoque seguro y efectivo33,34, sino que además es mucho más rentable para el paciente y el sistema de salud.
La ecografía en la hematuria35 permite valorar la morfología renovesical y descartar masas renales (fig. 14) o pólipos vesicales36,37 (fig. 15), así como evaluar la morfología y el tamaño prostático29,37,38 (fig. 12).
En todos estos supuestos la ecografía clínica permitirá orientar el diagnóstico, al confirmar o excluir las hipótesis. También permitirá mejorar la capacidad de manejo por parte del MF, evitar pruebas y derivaciones innecesarias, y motivar nuevas pruebas, interconsultas e ingresos hospitalarios cuando a la luz de su contribución estén indicados.
Ecografía clínica ginecológicaTécnica de exploraciónLa ecografía es la modalidad de imagen de primera línea para el estudio de las enfermedades ginecológicas, dada la ausencia de radiación ionizante y la excelente visualización de útero y ovarios. La TC y la RM se reservan habitualmente para resolver dudas diagnósticas o para la estadificación de tumores.
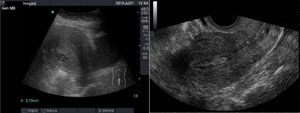
La exploración ecográfica puede realizarse por vía pélvica o transvaginal. En el abordaje pélvico utilizamos una sonda convex de 3,5 Mhz y la vejiga llena como ventana acústica para estudiar el útero y los ovarios (fig. 16). En una ecografía vaginal usaremos una sonda endocavitaria de mayor frecuencia (a menudo no disponible en AP), recubierta por una funda estéril, y desde los fondos de saco vaginales obtendremos cortes longitudinales y transversos de los genitales internos.
La sistemática de estudio incluirá: tamaño uterino, forma y posición; evaluación de miometrio, endometrio y cérvix; identificación y morfología de los ovarios; valoración de útero y anejos en busca de masas, quistes, hidrosalpinx, colecciones líquidas y movilidad y evaluación del fondo de saco de Douglas para descartar masas y líquido libre.
La vía transabdominal puede mostrar muchas de las entidades reseñadas (masa uterina, quiste anexial, gestación ectópica, líquido libre peritoneal…) y es la técnica usualmente disponible; se completará el estudio con sonda vaginal si disponemos de ella, dada la mayor resolución de la imagen obtenida (mayor proximidad al órgano estudiado y, por tanto, posibilidad de usar transductor con frecuencia más alta). En algunas situaciones es totalmente necesario (caracterización de un quiste ovárico o de un endometrio patológico), por lo que la ausencia de dicha sonda obliga a derivar al ginecólogo. Sin embargo, la vía abdominal continúa siendo imprescindible para el estudio de masas que exceden la pelvis menor.
Técnicas como la ecografía 3D o la histerosonografía (mediante instilación de suero salino en la cavidad uterina para evaluar lesiones endometriales) quedan por el momento fuera del ámbito de la AP.
Escenarios clínicos en Atención Primaria y evidenciaEl dolor pélvico y la hemorragia uterina anormal son motivos frecuentes de consulta en AP y urgencias y pueden estar causados tanto por procesos banales como por una dolencia que puede comprometer la vida de la paciente (por ejemplo, embarazo ectópico roto). La ecografía permite visualizar gestaciones intrauterinas normales y anormales, dolencias uterinas y ováricas, o procesos inflamatorios pélvicos.
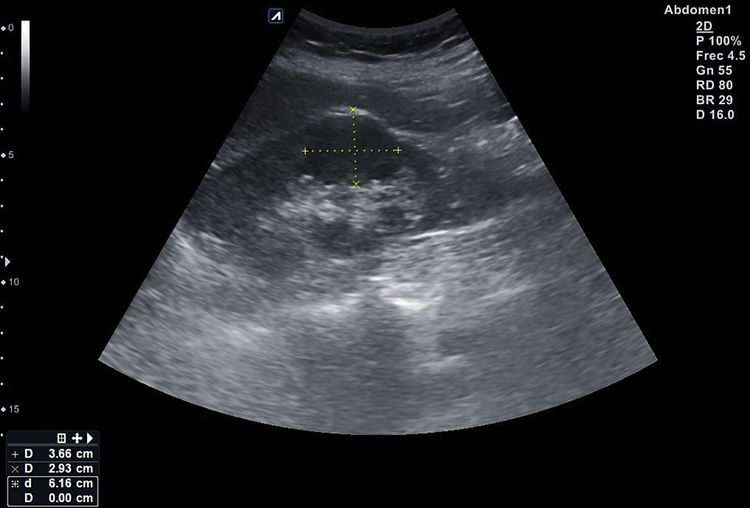
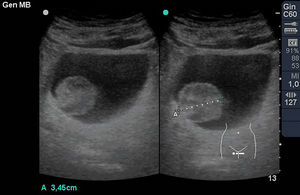
Entre los hallazgos patológicos más frecuentes está el leiomioma — masa pélvica más frecuente en la mujer (20-50%)— sintomático en un 25% de los casos como menorragia o sangrado anormal. Ecográficamente se presenta como masa hipo- o heteroecoica (intramural, subseroso, submucoso) (fig. 17). Plantea diagnóstico diferencial con masas anexiales (miomas subserosos pediculados), adenomiosis y leiomiosarcoma38-40.
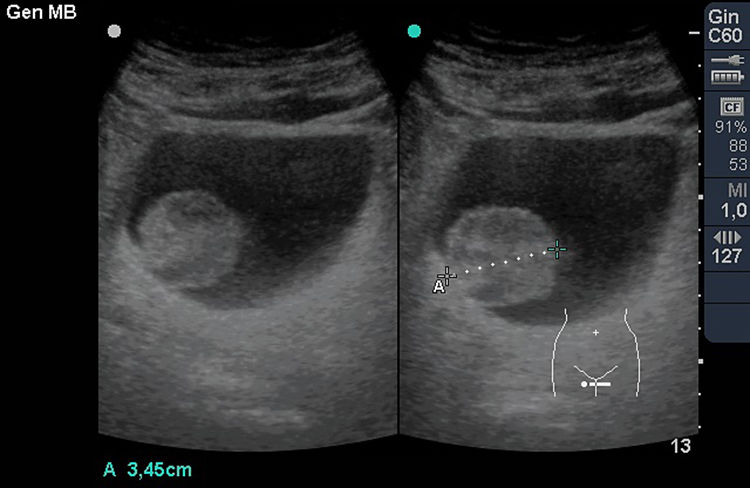
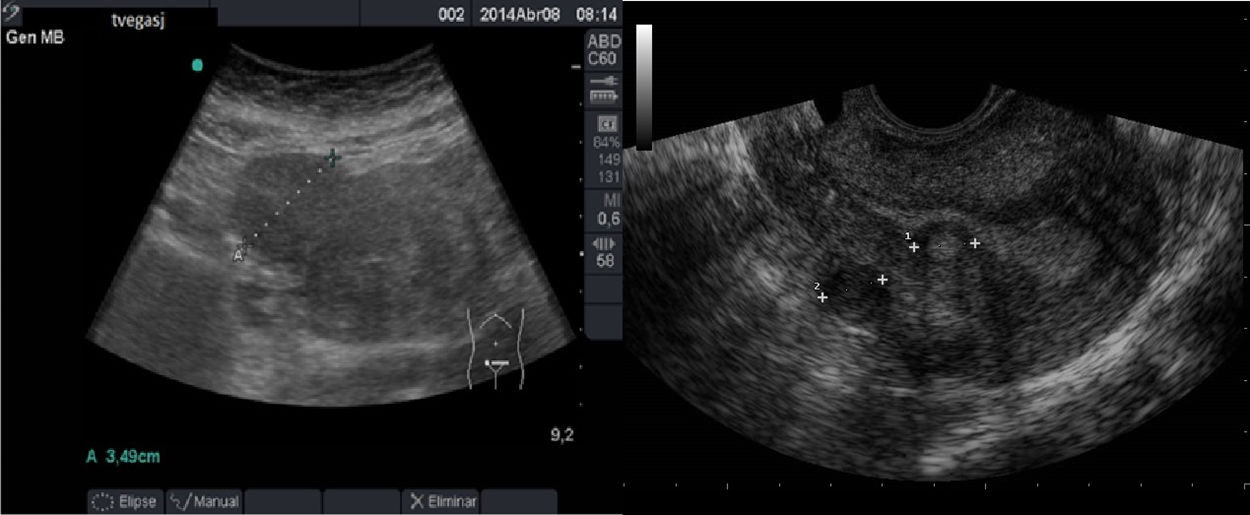
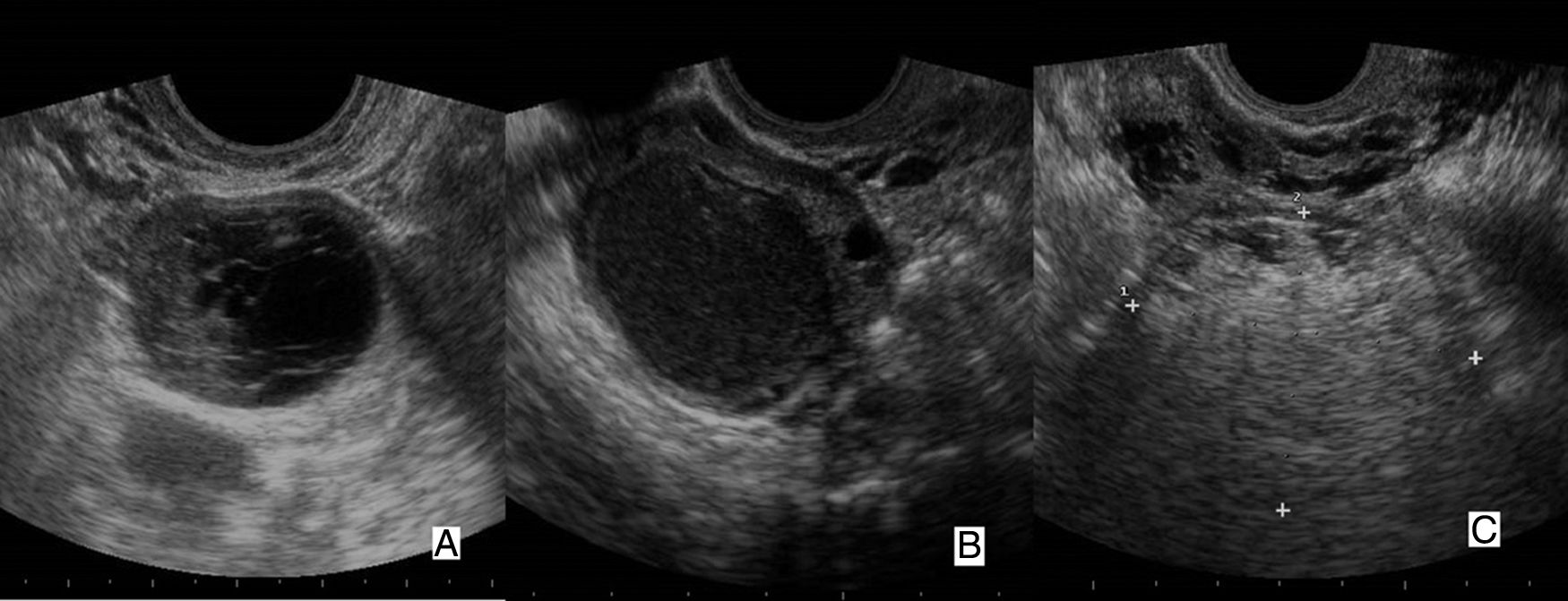
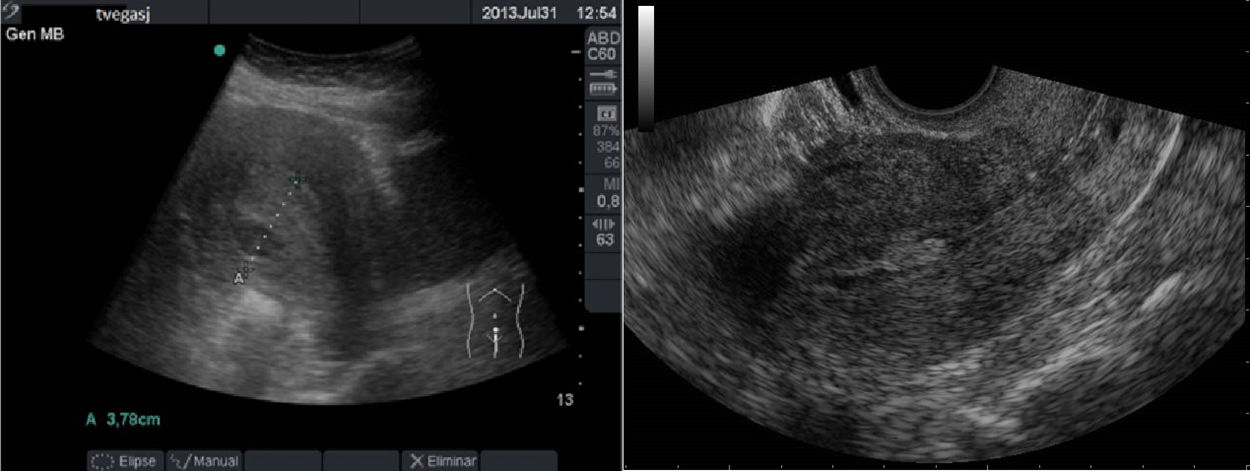
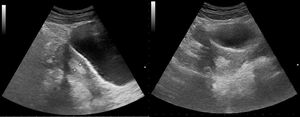
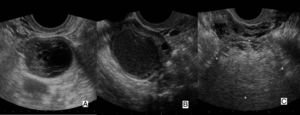
El hallazgo de una masa anexial nos obliga a descartar proceso maligno41. Los criterios «Simple Rules» del Grupo IOTA permiten predecir malignidad con una sensibilidad del 89-99,7% y una especificidad del 33,7-84,7%42,43 en función de la prevalencia del cáncer de ovario y la experiencia del examinador. Apuntan a malignidad: la apariencia predominantemente sólida, los quistes con septos gruesos (>3 mm) o papilas y la presencia de ascitis, adenopatías o masas peritoneales. Indican causa disfuncional u orgánica benigna: el quiste simple (persistencia folicular); el quiste «en red de pesca» (cuerpo lúteo hemorrágico)41 (fig. 18A), trastorno frecuente con apariencias «de gran simulador» que pueden hacer pensar en absceso o tumor; el quiste con ecos de intensidad media homogénea (endometrioma típico)44 (fig. 18B); la formación quística de predominio o con nódulo hiperecoico, imágenes puntiformes hiperecoicas, nivel líquido-líquido y calcificación (nos hará sospechar un teratoma maduro45) (fig. 18C). Finalmente, una apariencia tubular y con pequeñas proyecciones redondeadas y estrechamiento pueden corresponder a un hidrosalpinx46.
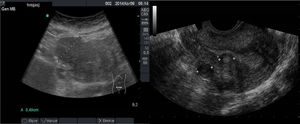
La hemorragia uterina anormal47 es un motivo frecuente de consulta al MF. Las causas más frecuentes en la mujer en edad fértil no gestante son entidades estructurales uterinas (pólipo endometrial, mioma, adenomiosis, cáncer de endometrio, hiperplasia endometrial), coagulopatía y disfunción ovulatoria. La ecografía transvaginal es la técnica de imagen de elección para evaluar el endometrio, por lo que si no dispone de ella, el MF deberá derivar al ginecólogo. Una proliferación focal única o múltiple (pólipo endometrial) (fig. 19) se muestra como una o varias imágenes hiperecoicas o multiquísticas con vaso nutricio demostrable en Doppler color. La sensibilidad y especificidad de la ecografía transvaginal con relación a la histerosonografía y la histeroscopia están entre el 90 y el 95%48. Se define la hipertrofia endometrial como un engrosamiento difuso >15mm (Bajo Arenas). Puede ser homogénea o quística y corresponder histológicamente a un pólipo, una hiperplasia (con o sin atipia) o un adenocarcinoma. El empleo del espesor endometrial para el diagnóstico del cáncer de endometrio en la premenopausia tiene alta tasa de falsos positivos (77-95%)49. Aunque no hay recomendación clara en la literatura para indicar la biopsia, se indica realizarla cuando sea >11mm, con base en estudios que muestran un riesgo de cáncer del 6,7% a partir de este punto de corte, mientras que por debajo el riesgo es extremadamente bajo50.
Un escenario clínico diferente es la metrorragia en la paciente posmenopáusica. Aunque suele tener un origen benigno (fundamentamente atrofia endometrial, también pólipo e hiperplasia) y solo el 10% estará provocada por un adenocarcinoma de endometrio51,52, su manejo diagnóstico está orientado a descartar malignidad. La biopsia endometrial es habitualmente el test inicial, debido a su alta sensibilidad, bajo coste y baja tasa de complicaciones. La ecografía transvaginal es una alternativa válida en aquellas mujeres que no toleran la biopsia ambulatoria o que necesitan evaluar también los anejos. Un punto de corte de ≤4mm de espesor endometrial ecográfico conlleva una tasa de falsos negativos para carcinoma endometrial tan favorable como la biopsia endometrial. Si el endometrio no es visualizado en su totalidad, presenta un espesor focal o global mayor de 4mm o la paciente presenta sangrado recurrente, estará indicada una biopsia endometrial ciega (engrosamiento difuso) o la histeroscopia (de elección si existe anomalía endometrial focal)53-56.
Una breve mención a la utilidad de la ecografía ginecológica es la consulta de anticoncepción, donde es la técnica de elección para el seguimiento y la detección de complicaciones en la paciente portadora de un DIU.
Por último, no existe evidencia concluyente en el momento actual para recomendar la ecografía como método de screening del cáncer de ovario57.
Utilidad de la ecografía clínica ginecológica en Atención PrimariaLa ecografía ginecológica constituye una herramienta valiosísima en la consulta del MF a la hora de evaluar clínicamente a una paciente que se presenta con dolor abdominal, alteraciones del ciclo menstrual o ante el hallazgo de una masa pélvica en la exploración física. El amplio abanico de escenarios ginecológicos58, que resumimos en la tabla 4, condicionará el diverso manejo. En algunos casos será preciso derivar a la paciente al Servicio de Ginecología de manera urgente (sospecha de embarazo ectópico roto, absceso en el tubo ovárico, tumoración con alta sospecha de malignidad…), mientras que en otros casos nos permitirá hacer una derivación orientada preferente (metrorragia posmenopáusica…) o normal (miomas submucosos sintomáticos, pólipo endometrial, teratoma…). Y en un significativo número de casos estableceremos un diagnóstico para el que no será necesario derivar a la paciente (formaciones ováricas disfuncionales, leiomiomas…) o excluiremos una causa ginecológica como responsable de la clínica, lo que sin duda redundará en una mayor calidad de la asistencia y en un uso más eficiente de los recursos.
La ecografía clínica es una herramienta que facilita y agiliza la toma de decisiones en cualquier entorno de atención médica.
El MF es el especialista que más se puede beneficiar del empleo de la ecografía porque debe ser competente en todos los terrenos de la patología
La ecografía abdominal por su fiabilidad, seguridad, reproducibilidad y bajo coste debe estar accesible para su empleo en AP.
La ecografía clínica abdominal, aplicada en escenarios concretos y con una técnica de estudio definida, confirma o descarta dolencias con elevada fiabilidad.
Escenarios clínicos y hallazgos frecuentes de la ecografía ginecológica en AP
| Escenarios clínicos | Hallazgos ecográficos | Utilidad en AP |
|---|---|---|
| Dolor pélvico y fiebre | EIP (endometritis, hidro- o piosalpinx, absceso tuboovárico) | Rapidez diagnóstica Derivación a especialista adecuado Circuito adecuado (urgente) |
| Dolor pélvico | Gestación extrauterina rota Masa anexial Masa pélvica Torsión ovárica Mioma pediculado torsionado Dolencia no ginecológica | Rapidez diagnóstica Seguimiento ecográfico Derivación a especialista adecuado Circuito adecuado (urgente, preferente, normal) |
| Masa pélvica | Leiomioma Adenomiosis Masa anexial | Rapidez diagnóstica Seguimiento ecográfico Derivación a especialista adecuado Circuito adecuado (urgente, preferente, normal) |
| HUA edad fértil | Leiomioma Pólipo endometrial Hipertrofia endometrial | Rapidez diagnóstica Derivación a especialista adecuado Circuito adecuado (urgente, preferente, normal) |
| Metrorragia posmenopáusica | Atrofia endometrial Pólipo endometrial Hipertrofia endometrial Carcinoma de endometrio | Aproximación diagnóstica Derivación a especialista adecuado Circuito adecuado (urgente, preferente, normal) |
| DIU | Expulsión Malposición Perforación | Rapidez diagnóstica Derivación a especialista adecuado Circuito adecuado (urgente, preferente, normal) |
Los autores declaran no tener ningún conflicto de intereses.