El shock séptico es la manifestación más grave de una infección. Esta se produce como consecuencia de una respuesta inflamatoria sistémica severa que lleva a un colapso cardiovascular y/o microcirculatorio, y a hipoperfusión tisular. La hipoperfusión constituye el elemento central que define la condición de shock y esta debe ser detectada y revertida en forma urgente desde la atención inicial. La evaluación de la perfusión periférica, la diuresis, y la medición del lactato y de la saturación venosa central, son las principales herramientas para evaluar la perfusión sistémica.
La reanimación debe comenzar en forma inmediata con la administración agresiva de fluidos, la cual puede ser guiada por parámetros dinámicos de respuesta a fluidos, y continuada hasta normalizar u optimizar las metas de perfusión. En forma paralela se debe iniciar vasopresores en caso de hipotensión marcada, siendo el agente de elección noradrenalina, y conectar precozmente al paciente a ventilación mecánica frente a hipoperfusión severa que no responde a fluidos, o frente a un aumento del trabajo respiratorio. Adicionalmente, el foco infeccioso debe ser tratado agresivamente iniciando antibióticos lo antes posible.
Septic shock is the most severe manifestation of an infection. It is caused by a systemic inflammatory response syndrome, which leads to cardiovascular and/or microcirculatory failure, and to tissue hypoperfusion. Hypoperfusion is the most important feature, which defines the shock state, and which must be detected and treated urgently from the very first attention. Peripheral perfusion, urine output, and lactate and central venous saturation measurements, are the main tools to assess systemic perfusion.
Resuscitation must start immediately with fluid administration, which can be guided by dynamic predictors of fluid responsiveness, and continued until normalizing or optimizing perfusion goals. In the presence of hypotension, vasopressors should be started in parallel, with noradrenaline being the preferred option. If hypoperfusion persists, or if respiratory work is too high, mechanical ventilation should be started promptly. In addition, infection should be treated aggressively starting antibiotics as soon as possible.
La sepsis es una importante causa de mortalidad y morbilidad especialmente cuando evoluciona a shock séptico y disfunción multiorgánica (1). La sepsis determina altos costos hospitalarios, estadías prolongadas tanto en la Unidad de Terapia Intensiva (UTI) como en el hospital, y una disminución en la calidad de vida de los sobrevivientes.
IFisiopatologla del shock sépticoRespuesta inflamatoria sistémicaSepsis es la respuesta inflamatoria sistémica ante una injuria infecciosa. El proceso se inicia cuando los microorganismos o sus componentes son reconocidos por células inmunológicamente activas, principalmente macrófagos y células endoteliales. Estas células tienen unos receptores que eficientemente reconocen los productos microbacterianos. Entre estos receptores el grupo de los Toll-like receptor (TLR) desempeñan un papel importante en la activación de la respuesta inflamatoria. En el caso de las bacterias Gram negativas, los lipo polisacáridos (LPS) liberados por la membrana bacteriana se unen a dos proteínas séricas con funciones similares: la LPS binding protein (LBP) y el factor soluble CD14. Cuando los LPS son captados por estas proteínas son reclutados por el factor CD14. El complejo LPS-CD14 se une al TLR, el cual después de algunos pasos adicionales finalmente activa la trascripción del factor nuclear kappa B (NF-kB). El NF-kB se une a diversos genes y es el encargado de inducir la producción de las diversas citoquinas y mediadores.
El resultado final es la producción de mediadores pro inflamatorios. En una fase temprana el factor de necrosis tumoral (TNF), la IL-6 y la IL-1B son los principales mediadores y alcanzan su máxima producción en pocas horas. Por otro lado existe una respuesta anti-inflamatoria en la que participan varias citoquinas como la IL-10, el TGF- B y el sistema nervioso parasimpático con el nervio vago regulando la respuesta inflamatoria a través de la producción y acción de la acetilcolina sobre receptores nicotínicos presentes en los macrófagos.
Destaca la función de un órgano que en la fisiopatología de la sepsis es de crítica importancia, el endotelio. En condiciones normales, la célula endotelial tiene cuatro funciones básicas:
- 1.
control de la coagulación manteniendo un balance entre la coagulación y la fibrinolísis,
- 2.
regulación del tono vascular,
- 3.
control de la permeabilidad vascular, y
- 4.
regulación de la adhesión y migración de los leucocitos y macrófagos. Durante la sepsis estas funciones reguladoras del endotelio se afectan significativamente, lo cual puede traducirse en grados variables de coagulación intravascular, así como en disfunción vascular y un tráfico anómalo de leucocitos a diversos tejidos alejados del foco infeccioso.
Desde un punto de vista clínico, el síndrome de respuesta inflamatoria sistémica (SIRS) se define por la presencia de fiebre o hipotermia, taquicardia, polipnea y alteración de los leucocitos circulantes (leucocitosis, leucopenia o desviación izquierda). Cuando esta respuesta es producida por una infección se plantea el diagnóstico de sepsis, y si ésta se asocia a disfunción de órganos, el cuadro se cataloga como una sepsis severa, la cual conlleva una elevada morbimortalidad. El shock séptico es la forma de presentación más grave de la sepsis y se produce cuando la sepsis se asocia a hipotensión e hipoperfusión tisular (2).
Hipoperfusión en shock sépticoEl shock se define por la presencia de hipoperfusión e hipoxia tisular. En la sepsis normalmente existe un aumento en el consumo y por ende, en la demanda de oxígeno (VO2). El estado de shock se produce cuando el sistema circulatorio no es capaz de satisfacer esta mayor demanda con un aumento proporcional del transporte de oxígeno (DO2). Este desbalance DO2 / VO2 determina disoxia tisular, la cual puede ocurrir a nivel global o regional. A nivel global la hipoperfusión puede darse aún cuando el DO2 esté aumentado respecto a los valores basales, e incluso sin presencia de hipotensión.
A nivel regional la hipoperfusión puede comprometer selectivamente algunos órganos debido a redistribución de flujos desde la circulación esplácnica y periférica hacia otros territorios, o puede comprometer selectivamente a algunos tejidos o células cuando existe una alteración en la microcirculación.
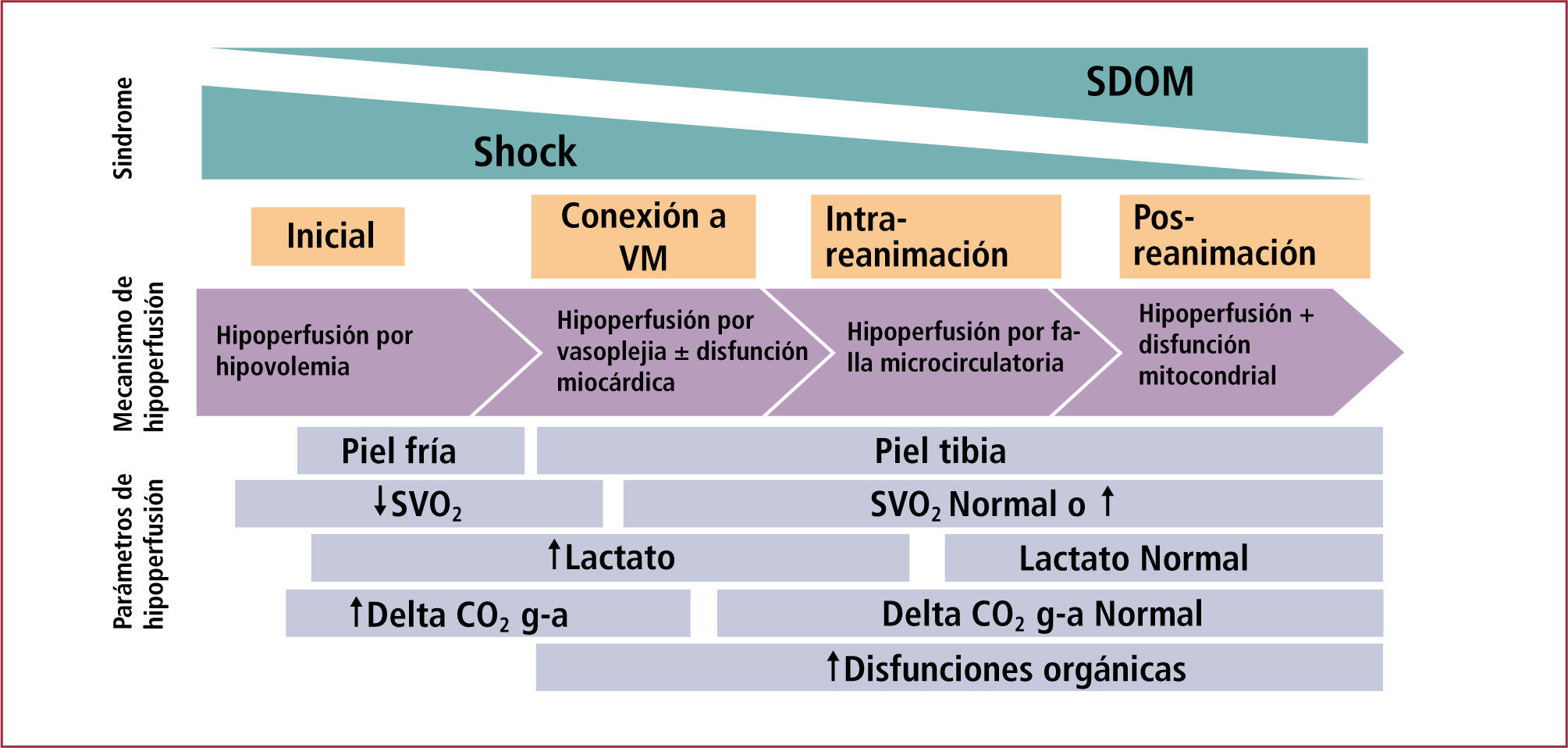
Diversos mecanismos contribuyen a la hipotensión e hipoperfusión asociadas al shock séptico: hipovolemia, hiporeactividad vascular, disfunción miocárdica, y disfunción microcirculatoria (Figura 1). La hipovolemia se produce tanto por pérdida absoluta de fluidos hacia el extravascular, como por una hipovolemia relativa producto de un aumento en la capacitancia venosa, lo cual determina una disminución del volumen circulante efectivo. La hiporeactividad vascular se produce en respuesta a la sobreproducción de óxido nítrico, por activación de canales de potasio ATP-dependientes, y por un déficit en la síntesis de vasopresina (ADH). La disfunción miocárdica tiene un origen multifactorial, siendo explicada por la liberación de diversos productos inflamatorios con capacidades cardiodepresoras, así como por disfunción celular de los miocardiocitos. Finalmente, la disfunción microcirculatoria podría estar explicada por alteraciones del endotelio, así como por adhesión excesiva de plaquetas y leucocitos a la superficie endotelial, aunque aún se desconoce la relevancia real de cada uno de estos mecanismos.
Manifestaciones y mecanismos de hipoperfusión en el shock séptico
En la etapa inicial de la reanimación del Shock Séptico el mecanismo central que determina la hipoperfusión es la hipovolemia. Durante esta etapa las manifestaciones de hipoperfusión más evidentes son la vasoconstricción periférica, la reducción del flujo hepatoesplácnico que puede detectarse por tonometría gástrica (Delta CO2 g-a, delta CO2 gastrico - arterial), y la disminución de la saturación venosa central (SVO2). Una vez que se corrige la hipovolemia estas manifestaciones de hipoperfusión pueden revertirse, sin embargo, se hace evidente la disfunción vascular y miocárdica que pueden determinar persistencia de hipoperfusión, la cual en esta etapa se expresa fundamentalmente como hiperlactatemia, y que coincide con la expresión de disfunciones orgánicas progresivas. Estas alteraciones normalmente se van corrigiendo con el uso de vasopresores, inótropos y eventualmente la conexión del paciente a ventilación mecánica (VM). Sin embargo, en aquellos pacientes que evolucionan desfavorablemente con un Sindrome de disfunción multiorgánica (SDOM) se piensa que este está determinado por alteraciones microcirculatorias y mitocondriales, las cuales ya no dependen de la reanimación.
Clínicamente, el shock séptico puede tener presentaciones muy variables: típicamente se observa un estado hiperdinámico, con aumento del gasto cardiaco y de la frecuencia cardiaca, mientras que la resistencia vascular sistémica está disminuida. Sin embargo, hasta un tercio de los pacientes puede presentarse con estados hipodinámicos, definidos como un índice cardiaco 2<,5l/min/m2. Independiente del gasto cardiaco, cuando se estudia mediante ecocardiografía la función cardiaca de los pacientes con shock séptico en la etapa inicial, más de la mitad de los pacientes presenta una fracción de eyección disminuida (3). Sin embargo, la taquicardia frecuentemente determina un gasto cardiaco aumentado a pesar de la disminución en la contractilidad.
La hipoperfusión tisular puede manifestarse como hiperlactatemia, oliguria, alteración del sensorio, o como hipoperfusión periférica. Sin embargo, ninguna de estas manifestaciones es específica para indicar hipoperfusión. Posiblemente este factor determina que no exista una definición única para el diagnóstico de shock séptico, y que por lo mismo las mortalidades reportadas sean altamente variables con cifras que van de 30 a 70% dependiendo de la serie y de la definición empleada. Algunos mecanismos de hipoperfusión tales como la vasoconstricción periférica y esplácnica, constituyen mecanismos de compensación simpática para preservar el volumen circulante efectivo y el transporte de oxígeno, frente a reducciones de la volemia. Estos mecanismos compensatorios se pueden monitorear mediante la evaluación de la perfusión cutánea y la tonometría gástrica. Por lo tanto, el monitoreo de estos parámetros permite detectar manifestaciones precoces de hipoperfusión que están estrechamente relacionados con la volemia y la respuesta hiperadrenérgica, y que por lo mismo tienden a revertir cuando se corrige la hipovolemia, o bien cuando se reduce la hiperadrenergia (Figura 1).
La reducción de la saturación venosa central o mixta corresponde a otro mecanismo de compensación: la capacidad de los tejidos de aumentar la extracción de oxígeno frente a reducciones del transporte o cada vez que disminuye la relación transporte / consumo. Esta fase de compensación se observa en diversos estados de shock y corresponde a una fase en que a pesar de la respuesta compensatoria simpática se ha producido una reducción del transporte global de oxígeno, o bien su incapacidad de aumentar en proporción al hipermetabolismo asociado a la sepsis. En esta perspectiva, la reducción de la SvcO2 es relativamente precoz en el desarrollo del shock séptico, y altamente sensible a cambios ya sea en el DO2 (4), o en el VO2 (5) (Figura 1).
La hiperlactatemia en el contexto del shock séptico refleja normalmente un aumento en la producción de lactato. Clásicamente se ha considerado que este aumento corresponde a metabolismo anaeróbico por hipoxia tisular. Sin embargo, crecientemente se ha reconocido que este aumento puede ser aeróbico, secundario al hipermetabolismo y la hiperestimulación adrenérgica, o bien producto del metabolismo anaeróbico de los leucocitos (6).
A pesar de estas limitaciones, el reconocimiento y la corrección oportuna de la hipoperfusión tisular constituyen la primera prioridad en el manejo del shock séptico. Actualmente existe consenso en que la medición del lactato es un elemento esencial en el manejo inicial del shock séptico (7). Recientemente demostramos que la presencia de hiperlactatemia en pacientes con shock séptico se asocia a una mortalidad en torno al 40%, mientras que su ausencia predice una sobrevida >90% (8). Si bien se reconoce que la hiperlactatemia no siempre es producida por hipoperfusión, sino que también puede ser una manifestación de hipermetabolismo, hiperadrenergia o de insuficiencia hepática, existe claridad respecto a su valor pronóstico. Cualquiera sea el mecanismo responsable de la elevación del lactato, este dato constituye un signo de gravedad.
IITratamiento del shock sépticoReconocimiento de la sepsis severa y del shock sépticoEl reconocimiento de la sepsis severa y el shock séptico constituyen un factor esencial para lograr un manejo oportuno de estos cuadros. Este reconocimiento debe realizarse precozmente, antes de que el paciente ingrese a la unidad de pacientes críticos, ya que cualquier retraso en el tratamiento compromete gravemente el pronóstico de los pacientes.
El reconocimiento de la sepsis severa requiere una evaluación sistemática de las funciones de diversos sistemas: respiratorio, cardiovascular, renal, sistema nervioso central, coagulación y hepático. Muchas de estas alteraciones pueden ser sospechadas mediante la simple evaluación clínica (Ej. signos vitales, nivel de conciencia), mientras que otras requieren exámenes de laboratorio (Ej. creatinina, recuento de plaquetas, bilirrubina). La alteración de cualquiera de estos sistemas como resultado de la respuesta inflamatoria del paciente a la infección determina un riesgo de morbi-mortalidad significativamente más elevado.
El reconocimiento del shock séptico normalmente se ha asociado a la presencia de hipotensión, sin embargo, este concepto es absolutamente insuficiente ya que en la mayoría de los pacientes la hipoperfusión tisular precede la aparición de hipotensión. La hipotensión muchas veces no se manifiesta, o lo hace tardíamente, debido a la respuesta hiperadrenérgica del paciente. Sin embargo, la perfusión tisular puede verse severamente comprometida a nivel global o regional sin que necesariamente exista hipotensión asociada. Cuando existe hiperlactatemia sin hipotensión asociada algunos autores han acuñado el término de “hipoperfusión oculta”. Por otro lado, muchos pacientes manifiestan hipotensión y requieren tratamientos prolongados con vasopresores, sin embargo, nunca presentan signos de hipoperfusión. Para estos casos empleamos el término de “disfunción vascular persistente” (8).
Por las razones antes expuestas, el reconocimiento del shock séptico debe basarse no sólo en la presencia de hipotensión, sino que también en la identificación de hipoperfusión tisular. Como se mencionó previamente no existe un criterio único y específico para identificar la hipoperfusión de manera que necesariamente se deben evaluar varios parámetros.
En nuestra experiencia la evaluación de la perfusión periférica y del lactato son las herramientas más potentes para reconocer el shock séptico así como para evaluar la respuesta a la reanimación inicial. La saturación venosa central (SvcO2) en cambio es una buena herramienta para identificar un desbalance global DO2/VO2, pero su normalización no asegura una adecuada perfusión sistémica. Otro inconveniente es que requiere la instalación de un catéter venoso central. Esto no siempre puede conseguirse con facilidad en nuestros servicios de urgencia y la evidencia actual es insuficiente para recomendar la instalación rutinaria de un catéter venoso central (CVC) en el servicio de urgencia en pacientes que se presentan con shock séptico. En nuestra experiencia, el momento de instalación del CVC debe definirse según la situación clínica particular, la disponibilidad y el nivel de entrenamiento del personal a cargo del paciente, y el tiempo de espera estimado para transferir al paciente a una unidad de paciente crítico. En la práctica, todas las medidas de reanimación prioritarias se pueden implementar rápidamente en el servicio de urgencia aunque aún no se cuente con un CVC (fluidos, vasopresores, ventilación mecánica).
Reanimación inicial y otras medidas urgentesEl manejo inicial de la sepsis incluye maniobras básicas de reanimación, con el objetivo de restablecer una entrega adecuada de oxigeno a los tejidos, así como la administración de antibióticos y el control del foco infeccioso. Las maniobras de reanimación inicial comprenden la administración de fluidos intravenosos, uso de vasoactivos / inótropos, transfusión de glóbulos rojos, y el soporte ventilatorio. Todas estas medidas deben estar dirigidas no sólo a la estabilización macrohemodinámica, sino que muy especialmente a la normalización de la perfusión. Este conjunto de medidas administrada en forma protocolizada y guiada por objetivos claros se conoce como terapia temprana dirigida por metas (Early Goal-Directed Therapy, [EGDT]) (4), y en ella se basan las recomendaciones para el paquete (bundle) de reanimación inicial (primeras 6 horas) de la Campaña Sobreviviendo a la Sepsis (7).
- 1.
Medir lactato arterial.
- 2.
Tomar hemocultivos antes de iniciar la administración de antibióticos.
- 3.
Administrar antibióticos de amplio-espectro dentro de las primeras 3 horas de ingreso al servicio de urgencia o dentro de 1 hora de ingreso a la Unidad de Pacientes Críticos, cuando no viene desde la urgencia.
- 4.
En presencia de hipotensión y/o lactato ≥ 4mmol/L:
- a)
Administrar 2 litros de cristaloide (o coloide equivalente).
- b)
Administrar noradrenalina cuando la hipotensión no responda a la reanimación inicial con fluidos, con la finalidad de mantener una presión arterial media (PAM) entre 65 a 75mm Hg.
- a)
- 5.
Si la hipotensión persiste a pesar de la resucitación con fluidos, y/o lactato es ≥ 4mmol/L:
Este paquete de medidas de reanimación inicial tiene el mérito fundamental de que imprime un sentido de urgencia tanto a la reanimación como al tratamiento del foco infeccioso, y que plantea metas de reanimación que van más allá de la normalización de la macro-hemodinamia. Sin embargo, no todas las medidas tienen una aceptación universal. Particularmente, se discute la necesidad de guiar la reanimación de acuerdo a SvcO2 ya que el clásico estudio de Rivers et al., que fundamenta dicha estrategia, se realizó sólo en un centro y la mortalidad del grupo control fue demasiado elevada (4). Por otro lado, diversos estudios realizados en pacientes críticos con sepsis no han podido confirmar la alta incidencia de SvcO2 7<0% encontrada en el estudio de Rivers (9). Recientemente un estudio de Bakker et al. encontró que una estrategia guiada por lactato era igual de eficaz que una estrategia guiada por SvcO2 (10). Mientras no se publiquen estudios multicéntricos que confirmen los resultados de Rivers se recomienda implementar protocolos locales de EGDT orientados a metas de perfusión, ya sea SvcO2, o lactato.
Otra de las indicaciones controversiales de este paquete es el uso de la PVC para guiar la administración de fluidos. Múltiples estudios han demostrado que la PVC es un muy mal predictor de respuesta a fluidos (11). Por otro lado, en los últimos años se han publicado numerosos estudios que avalan el uso de parámetros dinámicos tales como la variabilidad de la presión de pulso, en pacientes conectados a ventilación mecánica y en ritmo sinusal, o la respuesta a una maniobra de elevación de piernas, la cual no requiere que el paciente esté conectado a ventilación mecánica, ni que esté en ritmo sinusal (12). Estos parámetros se pueden obtener fácilmente en el servicio de urgencia y constituyen una alternativa mucho más racional para guiar la administración de fluidos durante la reanimación.
El rol de la dobutamina y de las transfusiones de glóbulos rojos en las primeras horas de reanimación, los cuales estaban insertos en el protocolo de Rivers, también es controvertido ya que su sustento fisiológico es relativamente pobre y resulta contradictorio con evidencia previa. Mientras no existan estudios que confirmen los datos de Rivers no recomendamos el uso liberal de transfusiones o de inótropos en las primeras horas de reanimación, excepto en casos de anemia severa o ante evidencias de alteración severa de la contractilidad, respectivamente.
Monitoreo hemodinámicoEl monitoreo hemodinámico básico de un paciente en shock séptico debe incluir la presión arterial invasiva, el trazado electrocardiográfico, y la oximetría de pulso, además del monitoreo de la perfusión sistémi-ca, el cual se discute en la siguiente sección. Adicionalmente, la gran mayoría de los pacientes requiere algún método de evaluación del volumen circulante efectivo para guiar la administración de fluidos, y una fracción menor de pacientes puede requerir la medición o estimación del gasto cardiaco, o de la contractilidad.
Es bien conocido que la primera línea de tratamiento en el shock séptico es la expansión de volumen. Sin embargo varios estudios han demostrado que solo la mitad de los pacientes críticos incrementan el gasto cardíaco luego de una expansión de volumen (rama ascendente de la curva de Frank - Starling) y son denominados respondedores o dependientes de precarga. Determinar qué pacientes serán respondedores o no a la expansión de volumen repercutirá en el tratamiento y su pronóstico, ya que una insuficiente resucitación con fluidos en fases tempranas del shock determina mayor hipoperfusión tisular y mayor probabilidad de disfunción multiorgánica (4). Por otro lado una resucitación excesiva con fluidos también es deletérea, con complicaciones derivadas de la acumulación de agua extracelular en el pulmón y el abdomen, y una mayor probabilidad de disfunción respiratoria, gastrointestinal y de hipertensión intra-abdominal (13).
Como se mencionó previamente, los parámetros dinámicos son las alternativas de elección para guiar la administración de fluidos (12). Estos pueden obtenerse a través del simple trazado de la presión arterial invasiva, o bien a partir de variables ecocardiográficas. Consisten en variaciones controladas de la precarga y se evalúa su efecto sobre marcadores indirectos del volumen eyectivo del corazón tales como la presión de pulso, o señales de doppler obtenidos ultrasonográficamente a nivel de la válvula aórtica. La alternativa más simple es la variación de la presión de pulso que se produce por el efecto de la ventilación cíclica con presión positiva. Fisiológicamente su racionalidad radica en que constituye una prueba de precarga altamente reproducible y dinámica, siendo prácticamente equivalente a una rápida administración de fluidos. Métodos sofisticados de análisis de la onda de pulso tales como Flo-Trac Vigileo, PiCCO y LiDCO permiten estimar el volumen sistólico a partir del área bajo la curva de la onda de presión arterial y calcular su variabilidad con el ciclo respiratorio. Estos métodos automatizados entregan mayor comodidad y probablemente en el futuro cercano estarán incluidos en la mayoría de los monitores sin necesidad de emplear un catéter especial. Sin embargo, por ahora su uso requiere catéteres especiales de alto costo, lo cual puede no ser costo efectivo ya que el mismo tipo de información puede ser fácilmente obtenida con cualquier catéter arterial y monitor de UTI. Las principales limitaciones de los parámetros dinámicos radican en que se requiere que el paciente esté en ventilación controlada con presión positiva, en ritmo sinusal, y que el volumen corriente sea al menos de 8 ml/kg para tener una señal confiable. Alternativamente, en los últimos años se ha acumulado una evidencia creciente que respalda el uso de la maniobra de elevación de piernas como una potente opción para predecir la respuesta a fluidos. La elevación de las piernas es una prueba también dinámica, equivalente a la administración de fluidos, en la cual el volumen circulante efectivo se aumenta transitoriamente mediante una reducción de la capacitancia venosa. El efecto de esta maniobra puede evaluarse tanto a nivel de la presión de pulso, como de la señal ecocardiográfica. Estas nuevas tendencias de monitoreo de parámetros dinámicos se conoce como monitoreo hemodinámico funcional, el cual ha reemplazado progresivamente el uso de variables estáticas clásicos. Las variables estáticas como la PVC, la presión de oclusión de arteria pulmonar (POAP), o la medición del tamaño de las cavidades cardiacas, tienen una capacidad de predicción muy baja y por lo tanto no se recomiendan para guiar la administración de fluidos, aunque si pueden ser útiles para evidenciar una sobrecarga de fluidos ya establecida.
La medición del gasto cardiaco también se emplea con frecuencia en la reanimación de los pacientes con shock séptico de mayor gravedad. El estándar para su medición es la termodilución obtenida a partir del catéter de arteria pulmonar (catéter de Swan - Ganz). Desde hace varios años se vienen desarrollando técnicas alternativas para la medición del gasto cardiaco, muchas de ellas consideradas poco invasivas, sin embargo, su precisión es muy variable. Basado en la evidencia actual, las alternativas técnicas que permiten medir el gasto cardiaco de manera relativamente confiable son la ecocardiografía, la termodilución transcardiopulmonar mediante catéter PICCO, y la dilución de un bolo de litio (LIDCO). El resto de las técnicas si bien puede proveer estimaciones aproximadas que pueden ser útiles como tendencia, tienen grados de precisión menores.
La utilidad de la medición del gasto cardiaco es controversial. No existen a la fecha estudios que hayan mostrado que la medición del gasto tenga un impacto en el pronóstico. Ello bien podría estar relacionado a la falta de protocolos racionales que promuevan un buen uso de la información. Sin embargo, desde el punto de vista fisiológico también resulta controversial ya que no hay ningún valor absoluto de gasto cardiaco que pueda considerarse normal o apropiado per se. Lo adecuado o inadecuado del gasto cardiaco no depende de su valor absoluto sino que de sus efectos sobre la perfusión. Un gasto de 2l/ min puede ser adecuado si permite una perfusión normal, mientras que un gasto de 10l/min puede ser inadecuado si se asocia a hipoperfusión. Asimismo, el valor absoluto del gasto tampoco permite estimar la contractilidad, aunque el volumen sistólico derivado de la medición del gasto cardiaco se correlaciona bien con la fracción de eyección. Ante la necesidad o duda de usar inótropos tampoco es esencial el valor del gasto ya que esta medida puede implementarse basado en la evaluación de la perfusión y de la contractilidad. Nuestro protocolo de manejo del shock séptico si contempla el uso del catéter de arteria pulmonar en los pacientes con hipoperfusión severa, sin embargo, en muchas unidades del mundo se utiliza preferentemente la evaluación ecocardiográfica de la contractilidad y/o del gasto. Esta decisión depende de la disponibilidad y experiencia local con ecocardiografía, aunque probablemente en el futuro esta última irá restringiendo cada vez más el uso del catéter de arteria pulmonar.
Monitoreo de la perfusiónEl monitoreo de la perfusión debe ser multimodal ya que como se mencionó en secciones previas, involucra distintos componentes de naturaleza diversa. En la evaluación inicial se debe priorizar la perfusión periférica y la medición del lactato plasmático (una medición en sangre venosa periférica es igualmente confiable). Una vez que el paciente ha sido transferido a la unidad de paciente crítico, o que las medidas iniciales de reanimación y estabilización cardiovascular ya se han implementado, el monitoreo de la perfusión debe complementarse con la medición de la SvcO2 y de la diuresis. La reanimación inicial con fluidos debe continuarse idealmente hasta obtener la normalización de todos estos parámetros. Sin embargo, en ciertos casos, la persistencia de alteraciones aisladas en algún parámetro puede no reflejar hipoperfusión, sino corresponder a otras alteraciones, por ejemplo, una insuficiencia renal oligúrica ya establecida, o la persistencia de hiperlactatemia moderada secundaria a hipermetabolismo. Para definir esta condición se debe integrar activamente la evolución de todos los parámetros hemodinámicos y de perfusión, y así establecer hasta donde debe continuarse la reanimación agresiva con fluidos o inótropos.
En los últimos años han emergido nuevas técnicas de evaluación de la perfusión tales como la videomicroscopía para evaluar la microcirculación, la evaluación de la saturación tisular de hemoglobina mediante espectroscopia cercana al infrarojo (NIRS), o la medición del clearance de verde indocianina, para evaluar el flujo hepatoesplácnico. Estas técnicas entregan información novedosa pero por ahora su uso está circunscrito fundamentalmente a investigación. En nuestros protocolos de manejo frecuentemente evaluamos estos parámetros, así como la tonometría gástrica, en los pacientes con formas de shock muy severas, o en el contexto de protocolos de investigación.
Administración de fluidosLa administración de fluidos intravenosos ha sido siempre un pilar fundamental del manejo de pacientes críticos de distintas etiologías. Sin embargo, existe poca claridad sobre la mejor estrategia de volemización, incluyendo el tipo de fluido, momento de la volemización, cantidad de fluido administrado, metas y límites de seguridad en los distintos escenarios clínicos. En las secciones previas discutimos acerca de la fisiopatología de la hipovolemia de la sepsis, así como sobre las metas de administración de fluidos. En esta sección abordaremos algunos conceptos referentes a la estrategia de administración de fluidos.
En la actualidad no existe evidencia clínica que demuestre la superioridad de un fluido en particular. Sin embargo, existe evidencia indirecta que sugiere que los balances hídricos excesivos se asocian a mayor mortalidad en el contexto de la sepsis (13). Por otra parte, un gran estudio multicéntrico australiano-neozelandés que comparó una reanimación basada en albúmina al 4% (diluido en solución fisiológica) v/s solución fisiológica exclusiva, en pacientes críticos, encontró que en el subgrupo de pacientes con sepsis hubo una fuerte tendencia a una menor mortalidad en aquellos tratados con albúmina (14). Estos pacientes requirieron un menor aporte total de fluidos y tuvieron balances menos positivos que los tratados con solución fisiológica. Estos datos, si bien no constituyen una evidencia clara en contra de los cristaloides, sugieren que se debe poner atención en evitar los balances excesivamente positivos. En esa perspectiva una combinación de cristaloides / coloides parece una estrategia razonable mientras no se cuente con evidencia de mayor nivel.
Desde el punto de vista de la temporalidad de la administración de fluidos la estrategia más racional desde el punto de vista fisiopatológico y también de acuerdo a la evidencia reciente es focalizar la administración de fluidos en las primeras horas de reanimación y restringir su uso una vez que se ha logrado revertir la hipoperfusión. El estudio de Rivers et al. indica que la reanimación con fluidos debe ser agresiva, inmediata, y dirigida a metas de perfusión (4). Un retraso en la administración de fluidos puede tener graves consecuencias para la evolución posterior del paciente. Por otra parte, un cúmulo de evidencia sugiere que mantener una estrategia agresiva de fluidos hacia el 2° o 3er día de reanimación puede también tener consecuencias adversas para el paciente, al condicionar balances excesivamente positivos. Esta estrategia agresiva de aporte de fluidos sólo debe mantenerse en la medida que persisten manifestaciones de hipoperfusión y que la respuesta a fluidos es favorable. La persistencia de dependencia de vasopresores en dosis moderadas a bajas, sin manifestaciones asociadas de hipoperfusión, no justifica mantener una estrategia agresiva de administración de fluidos.
Drogas vasoactivas e inótroposLas catecolaminas vasopresores más empleadas son dopamina, no-radrenalina, y adrenalina. Todas estas drogas tienen un efecto alfa adrenérgico en grado variable.
Dopamina: Parece efectiva en aumentar la presión arerial media (PAM) en pacientes que permanecen hipotensos, pese a una expansión óptima de volumen. Este aumento de PAM está asociado a un aumento del gasto cardíaco. Debido a que para lograr aumentar la PAM se debe pasar necesariamente por una estimulación cardíaca, y que la droga sólo ejerce efectos vasoconstrictores en altas dosis asociadas inevitablemente a taquicardia, se le podría considerar como una droga alternativa en el shock séptico hiperdinámico. Las mayores desventajas de dopamina son sus potenciales efectos negativos a nivel cardíaco (taquicardia, isquemia o arritmias). Por otra parte, el tiempo se ha encargado de demostrar el carácter mítico del supuesto efecto protector esplácnico y renal de dopamina (15). El consenso es que actúa fundamentalmente como diurético, y que su eventual efecto protector renal no existe.
Noradrenalina: Tiene sólo moderada actividad beta 1 e intensa actividad alfa adrenérgica. La experiencia clínica sugiere fuertemente que puede aumentar la PAM sin deteriorar el gasto cardiaco ni las funciones orgánicas. Se ha empleado la noradrenalina en dosis desde 0,01 hasta 3,3μg/kg/mm. En general, la droga aumenta el gasto cardiaco entre 10 a 20%, y el volumen sistólico en 10 a 15%. Un estudio reciente comparó el efecto de noradrenalina versus dopamina como vasopresor inicial en pacientes con shock. Si bien el estudio no demostró diferencias estadísticamente significativas hubo un 4% de reducción absoluta de mortalidad a favor de noradrenalina (16).
Adrenalina: Esta droga puede aumentar la PAM en pacientes que no responden a agentes tradicionales, especialmente por su intenso estímulo inotrópico y vasoconstrictor. Por ello, en diversos protocolos tradicionales se emplea como droga de rescate. Sin embargo, debido a sus efectos negativos en el consumo de oxígeno miocárdico, su arritmogenicidad, su potencial impacto negativo en flujo esplácnico, y su tendencia a aumentar las concentraciones de lactato, su uso como rescate tiene poco sustento. En cambio, datos recientes sugieren que podría emplearse más precozmente como primer vasopresor, en dosis más bajas y alternativamente a noradrenalina. Un estudio multicéntrico francés comparó el efecto de adrenalina versus una combinación de noradrenalina y dobutamina en pacientes con shock séptico. Si bien no hubo diferencias estadísticamente significativas, se observó un 6% de aumento absoluto de mortalidad con el uso de adrenalina (17)
Adicionalmente a las catecolaminas en el último tiempo se ha discutido extensamente en torno al rol de la vasopresina como agente vasopresor. Los estudios clínicos muestran que su efecto vasopresor es muy potente y que permite reducir fuertemente los requerimientos de catecolaminas. Sin embargo, no está claro que este efecto sea una ventaja pues se han descrito numerosos casos de eventos isquémicos gatillados por vasopresina, así como importantes caídas del gasto cardiaco, particularmente en dosis altas. Un estudio multicéntrico randomizado comparó el uso de vasopresina versus noradrenalina en pacientes con shock séptico sin encontrar diferencias estadísticamente significativas (18). Actualmente no se recomienda emplearlo como agente de primera línea aunque puede constituir un agente opcional en determinados casos. Eso si, sólo deben emplearse dosis muy bajas (0,02 unidades/min), y fijas.
Respecto al uso de inótropos en el shock séptico su rol no está claro. A pesar de que muchos pacientes presentan alteraciones de la contractilidad se desconoce si dicha alteración es adaptativa y por tanto contribuye a proteger al miocardio, o si por el contrario es una alteración patológica que debe ser revertida con inótropos. El inótropo más empleado es la dobutamina, droga con la cual existe una larga experiencia y cuya seguridad está bien establecida. En general se recomienda utilizar inótropos cuando existan evidencias de bajo débito con aumento de presiones intracardiacas, y/o una disminución importante de la contractilidad, asociados a la presencia de hipoperfusión que no responde a la reanimación inicial con fluidos y vasopresores. Sin embargo, esta recomendación está basada principalmente en opinión de expertos ya que no existen estudios multicéntricos randomizados que hayan evaluado en forma específica el impacto de dobutamina sobre la evolución de los pacientes con shock séptico. En la gran mayoría de los casos una dosis baja entre 2,5 y 5ug/kg/min es suficiente para mejorar la contractilidad y no se asocia a taquiarritmias u otros efectos adversos.
CorticoidesSu uso en el manejo del shock séptico tiene una larga y controversial historia cuyo análisis escapa a los objetivos de este artículo. Desde un punto de vista práctico es necesario mencionar que actualmente no existe evidencia clara que justifique su uso rutinario en pacientes con shock séptico. Está bien establecido que dosis moderadas de hidrocortisona entre 200 a 300mg/día aumentan la reactividad vascular y permiten disminuir los requerimientos de vasopresores. Asimismo, estas dosis tienen un importante efecto antiinflamatorio que puede evidenciarse por una disminución de los marcadores clínicos de respuesta inflamatoria. Sin embargo, la evidencia actual no indica que disminuya la mortalidad ni la morbilidad. Si bien un estudio multicéntrico francés inicialmente mostró que si habría un efecto protector de hidrocortisona (19), un estudio multicéntrico europeo posterior no pudo confirmar este efecto benéfico (estudio CORTICUS) (20). A pesar de estos resultados contradictorios existe la posibilidad de que el beneficio de los corticoides esté restringido a aquellas formas más severas de shock, con mayor vasoplejia. De hecho, el estudio original francés incluyó pacientes con shock refractario y cuya gravedad general era mucho mayor a la de los pacientes del estudio CORTICUS. De ahí que muchos autores aún recomiendan considerar el uso de hidrocortisona en forma precoz en aquellos pacientes que manifiestan una severa vasoplejia. En nuestro protocolo utilizamos un límite de 0,3 μg/ kg/min de requerimiento de noradrenalina para definir aquellos pacientes con vasoplejia severa, y en quienes indicamos hidrocortisona 100mg cada ocho horas (21).
Terapias de rescate en shock refractarioDiversas terapias han sido ensayadas como forma de rescate en pacientes con shock séptico refractario. Entre ellas podemos mencionar algunas terapias farmacológicas tales como el azul de metileno, adrenalina, vasopresina, etc. Ninguna de estas terapias ha demostrado ser eficaz en reducir la mortalidad en pacientes con shock séptico. Otro grupo de terapias de rescate son las técnicas extracorpóreas, que buscan remover de la sangre uno o varios mediadores inflamatorios. Muchas de estas terapias se encuentran aún en fase experimental pero la hemofiltración de alto volumen (HFAV) ha sido empleada ya por varios años en diversas experiencias clínicas (22, 23). En nuestra propia experiencia la HFAV ha mostrado ser una terapia eficaz y factible de implementar con la tecnología actualmente disponible. La HFAV permite reducir el requerimiento de vasopresores y acelera el aclaramiento del lactato y la corrección de las alteraciones microcirculatorias (22, 24). A partir del año 2002, cuando incorporamos la HFAV como terapia de rescate en nuestro protocolo de manejo del shock séptico, observamos una reducción de la mortalidad en el subgrupo de pacientes con shock grave. Sin embargo, es una técnica relativamente compleja y de alto costo lo cual hace que su uso esté restringido a unos pocos centros y que por lo mismo aún no existan estudios randomizados que respalden su uso de manera más extendida.
IIIConclusionesDurante muchos años el foco principal del manejo del paciente en shock séptico fue la estabilización de las cifras macrohemodinámicas. Este enfoque ha cambiado radicalmente durante los últimos años dando lugar a una visión más fisiológica centrada en la perfusión tisular, y que pone a la hipoperfusión tisular como el elemento distintivo que define un shock séptico. La detección precoz de hipoperfusión y una reanimación agresiva dirigida a la normalización de los parámetros de perfusión constituyen el pilar del manejo del shock séptico en la actualidad. Para evaluar la perfusión se debe integrar diversos elementos tales como el lactato arterial, la saturación venosa central, y la perfusión periférica. Respecto a las intervenciones, la reanimación con fluidos sigue constituyendo la principal herramienta terapéutica, pero en la actualidad se sabe que su mayor eficacia se consigue cuando se concentra en las primeras horas de reanimación y se dirige por metas de perfusión.
Los autores declaran no tener conflictos de interés, en relación a este artículo.