To explore the proportion of patients with higher risk localized prostate cancer (PCa) that would become safely biopsy negative 12 months after non-thermal focal therapy with padeliporfin vascular-targeted photodynamic therapy (VTP).
MethodsMulticenter study in a scenario of prostate-specific antigen (PSA)≤20ng/ml and variable PCa target volumes Gleason pattern 3 or low-volume secondary Gleason pattern 4, all patients received VTP, consisting of intravenous 4mg/kg padeliporfin activated by light-diffusing fibers in the prostate. The prostate was biopsied at baseline, months 6 and 12, PSA, patient-reported functional outcomes and quality of life (QoL) questionnaires were recorded at baseline, months 3, 6, and 12 and adverse events (AE) throughout the study.
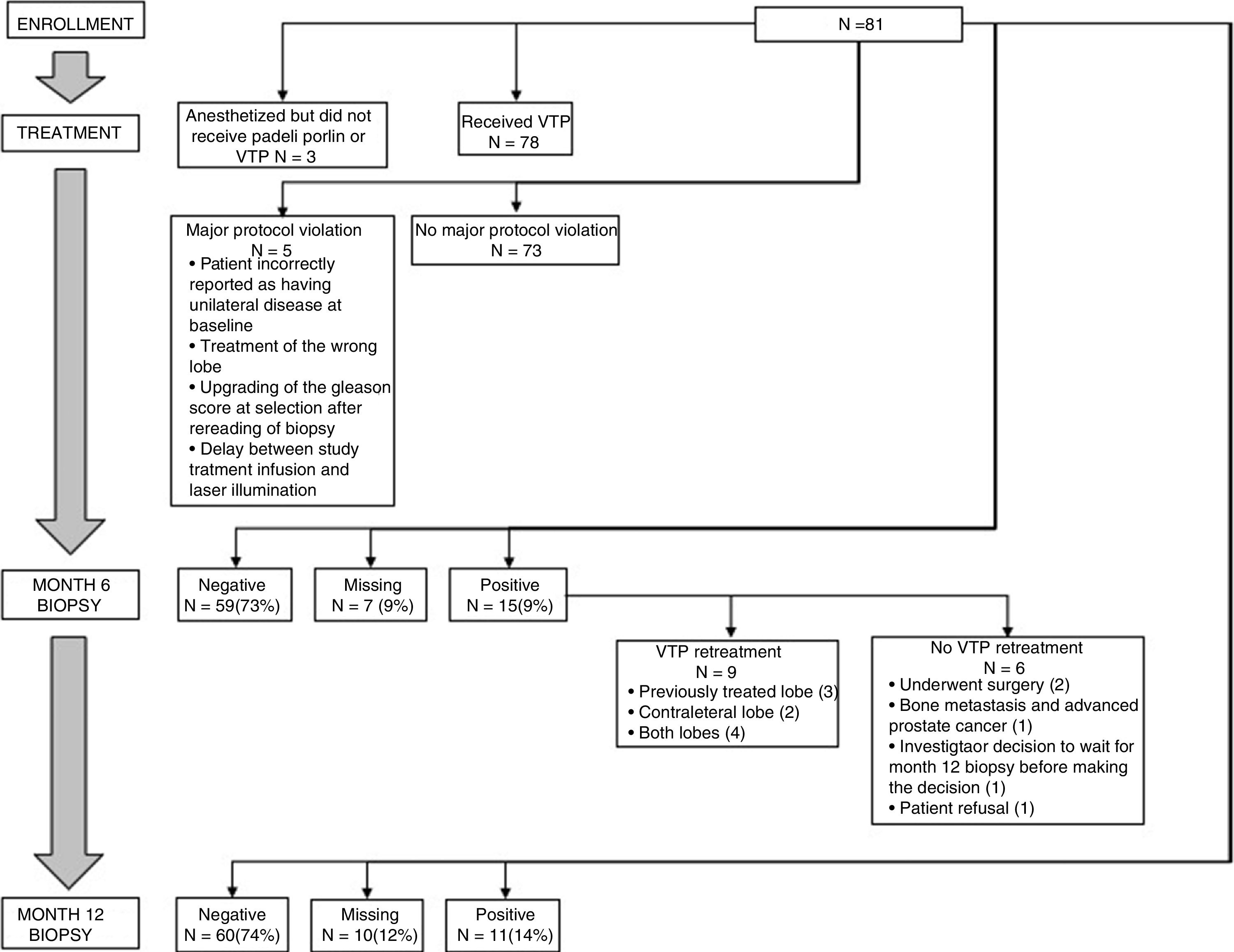
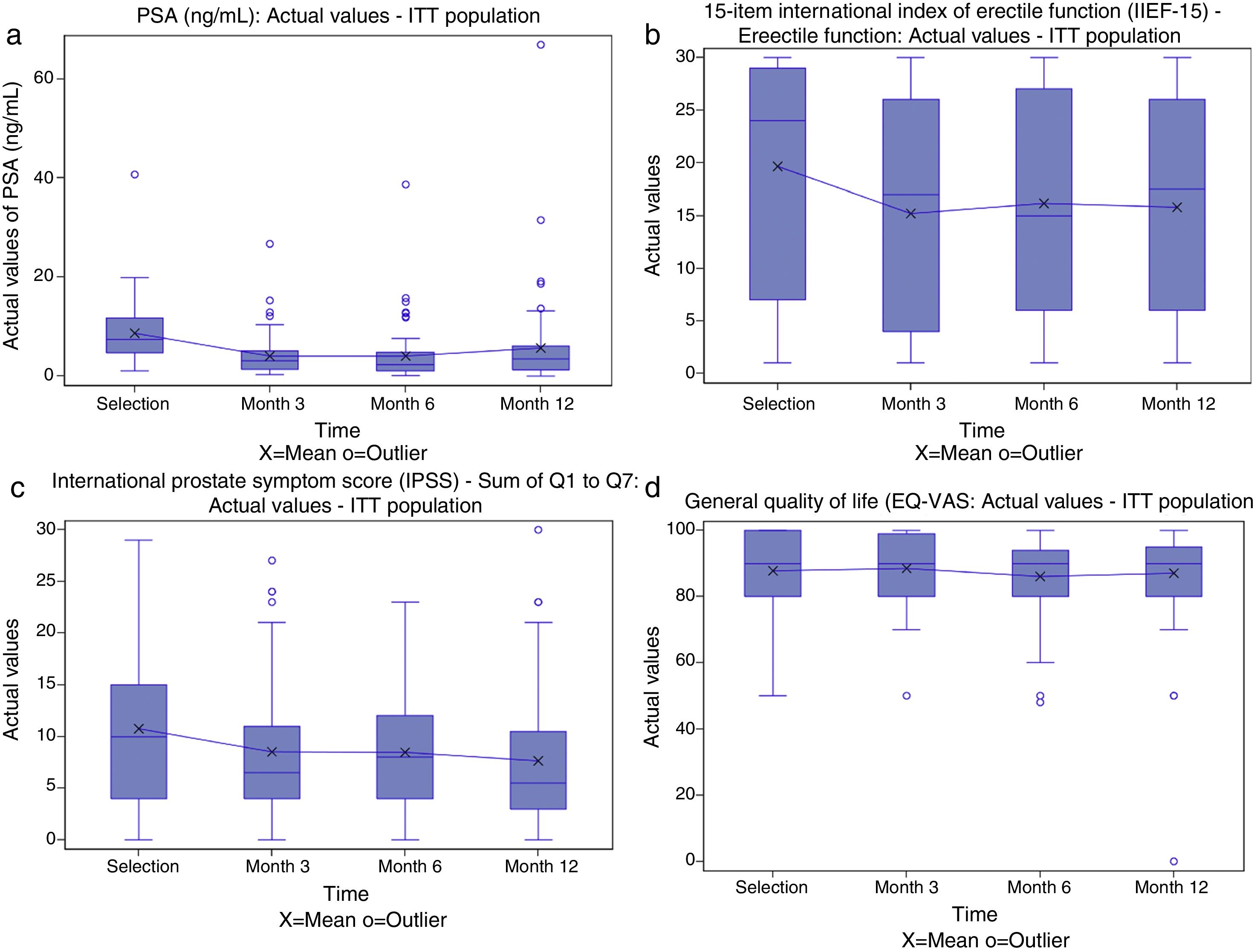
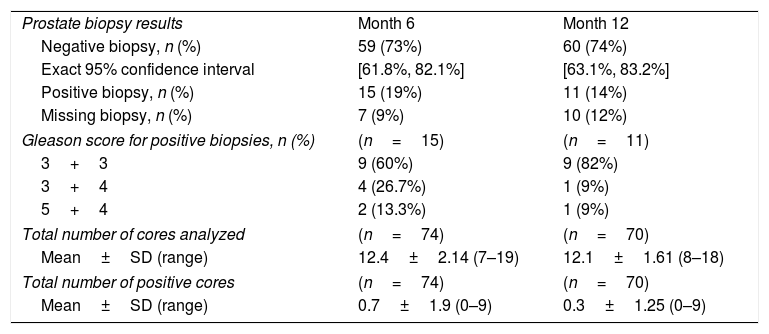
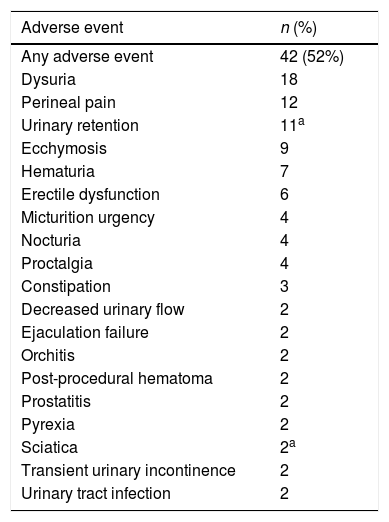
ResultsIn the intention-to-treat population (n=81), the proportion of patients with negative biopsies at month 12 was 74% (60/81 patients; 95% CI: 63.1%, 83.2%). In the per-protocol population, the proportion was 79% (58/73 patients; 95% CI: 68.4%, 88.0%). Questionnaire results indicated a slight improvement in urinary function and limited deterioration in sexual function. No difference in QoL was observed over time. A total of 42/81 (52%) patients reported mild or moderate and 4 of 81 (4.9%) experienced serious AE, all resolved without sequelae. No phototoxicity, cardiovascular event, fistula or prolonged urinary incontinence, secondary cancer or death was reported.
ConclusionsResults support the efficacy, safety, and QoL associated with padeliporfin focal treatment for low/intermediate risk localized PCa.
Explorar la proporción de pacientes con cáncer de próstata localizado (CaP) de mayor riesgo que se convertiría en una biopsia negativa con seguridad 12 meses después de la terapia focal no térmica con terapia fotodinámica dirigida vascular de padeliporfina (TFV).
MétodosEstudio multicéntrico en un escenario de antígeno prostático específico (PSA)≤20ng/ml y patrón 3 de Gleason de volúmenes objetivo de CaP variable o patrón 4 de Gleason secundario de volumen bajo. Todos los pacientes recibieron TFV, que consistió en 4mg/kg de padeliporfina intravenosa activada por fibras difusoras de luz en la próstata. La próstata se biopsió al inicio del estudio y a los meses 6 y 12. El PSA, los resultados funcionales informados por los pacientes y los cuestionarios de calidad de vida (CdV) se registraron al inicio y a los meses 3, 6 y 12; los eventos adversos (EA) se registraron a lo largo del estudio.
ResultadosEn la población con intención de tratar (n=81), la proporción de pacientes con biopsias negativas al mes 12 fue del 74% (60/81 pacientes, IC 95%: 63,1, 83,2%). En la población por protocolo, la proporción fue del 79% (58/73 pacientes, IC 95%: 68,4, 88,0%). Los resultados del cuestionario indicaron una ligera mejoría en la función urinaria y un deterioro limitado en la función sexual. No se observó diferencia en la CdV con el tiempo. Un total de 42/81 (52%) pacientes comunicaron EA leves o moderados y 4 de 81 (4,9%) experimentaron EA graves, todos resueltos sin secuelas. No se informó fototoxicidad, evento cardiovascular, fístula o incontinencia urinaria prolongada, cáncer secundario o muerte.
ConclusionesLos resultados respaldan la eficacia, la seguridad y la CdV asociadas con el tratamiento focal de padeliporfina para el CaP localizado de riesgo bajo/intermedio.
Artículo
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora