El objetivo de esta revisión sistemática es identificar el tratamiento óptimo para la infertilidad masculina derivada del abuso de esteroides anabólicos androgénicos (EAA).
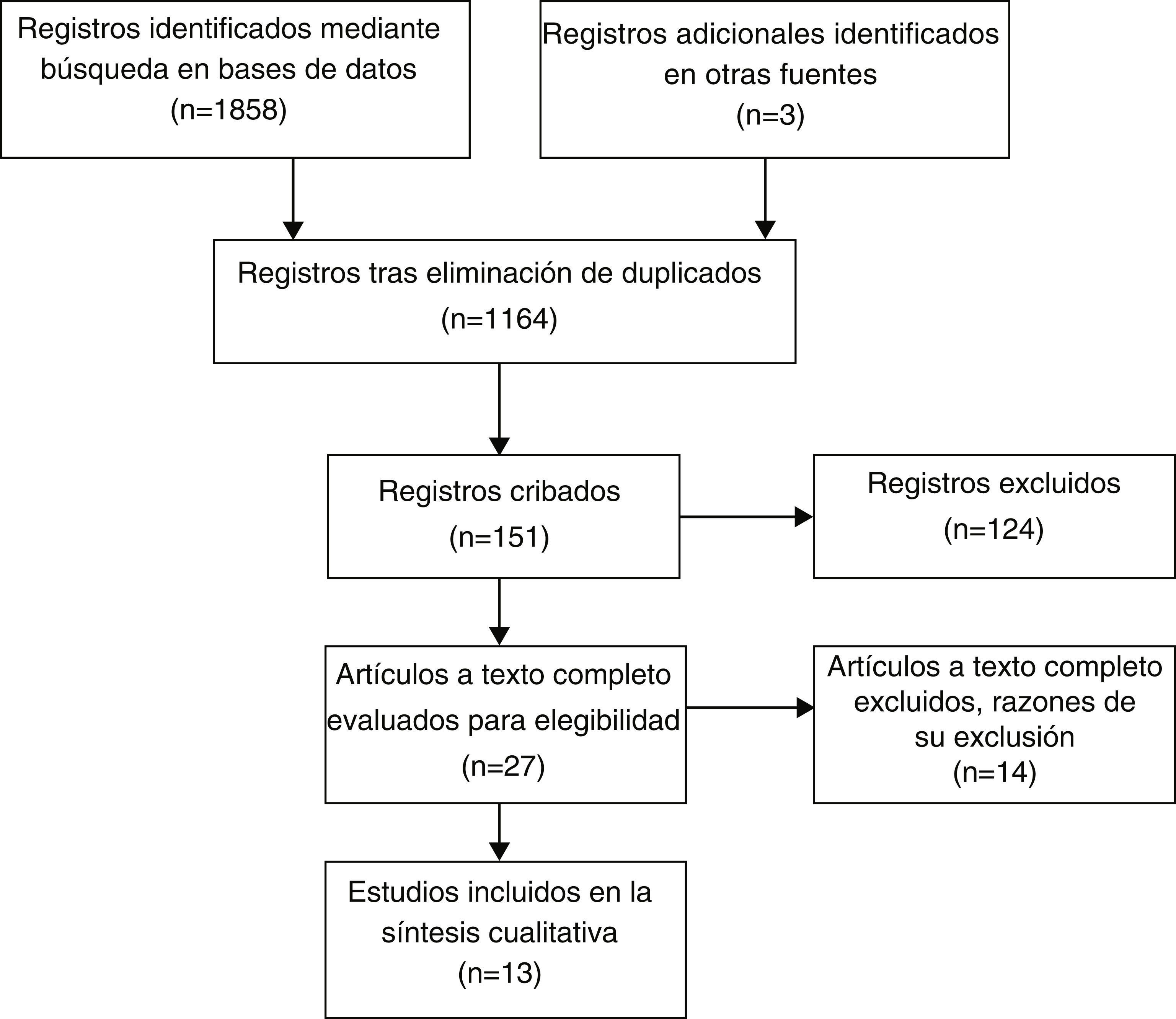
MétodosSe llevó a cabo una revisión sistemática según la declaración Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA). Se incluyeron estudios que comparaban distintos protocolos para la recuperación de la espermatogénesis tras el uso de EAA.
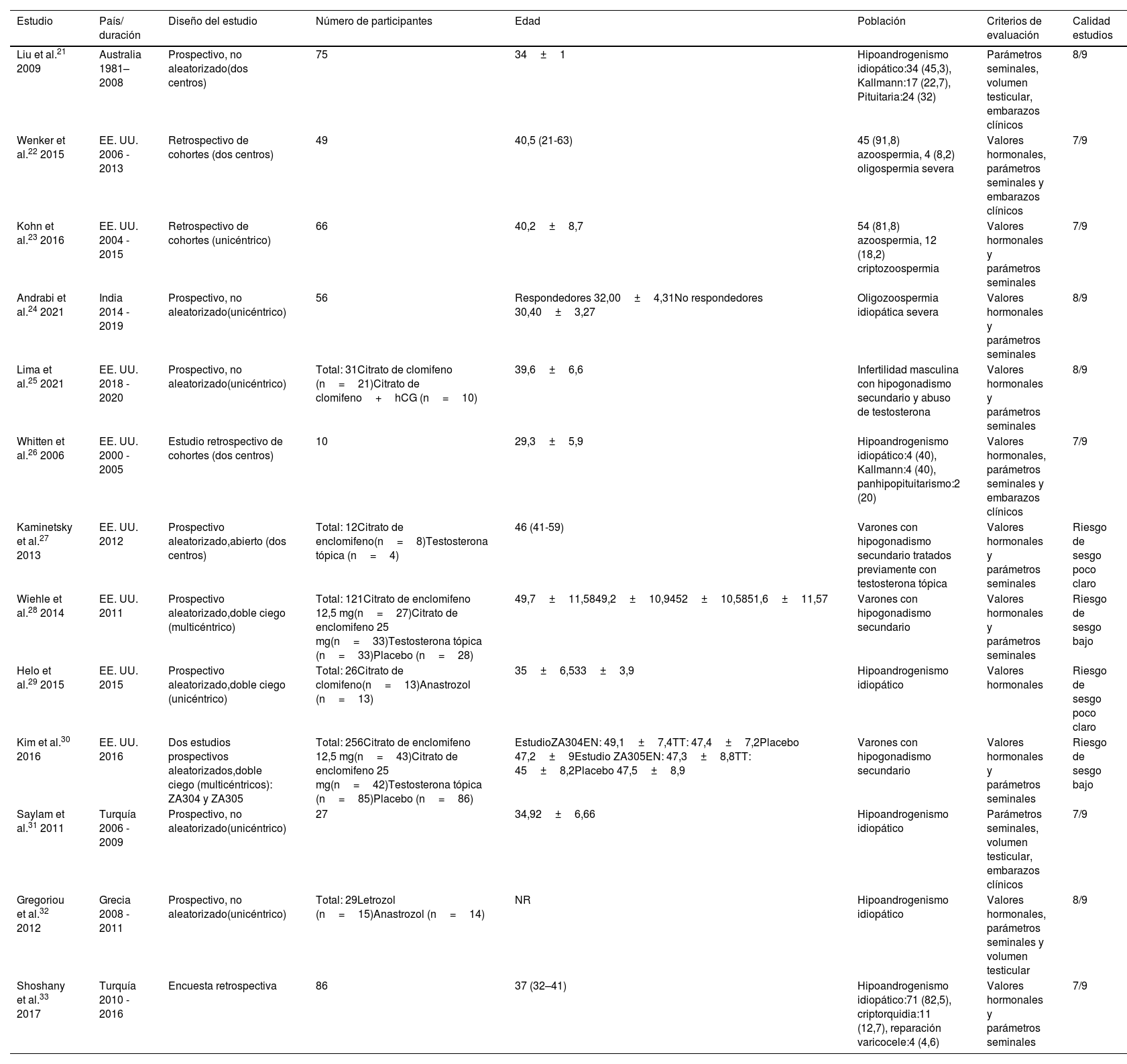
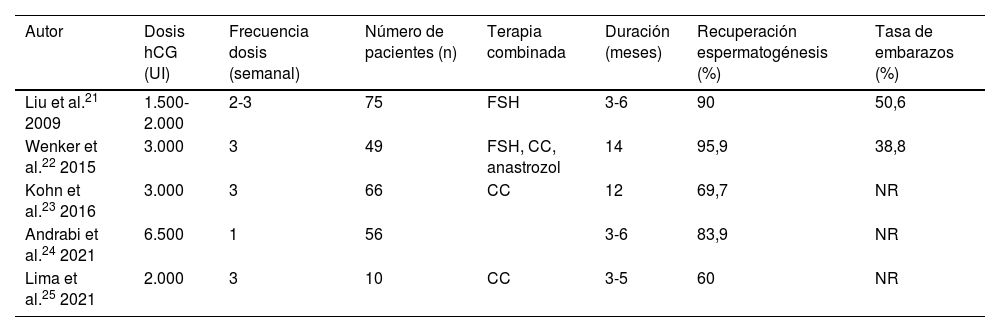
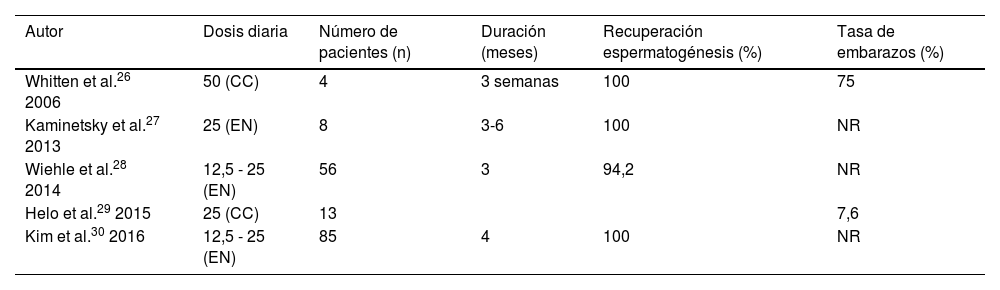
ResultadosUn total de 13 estudios que investigaban diferentes protocolos para recuperar la espermatogénesis en pacientes con abuso de EAA cumplieron los criterios de inclusión. Entre los agentes disponibles que demostraron eficacia en el reestablecimiento de la espermatogénesis se encuentran las gonadotropinas inyectables, los moduladores selectivos de los receptores de estrógenos (SERM) y los inhibidores de la aromatasa (AI), pero su uso apenas ha sido descrito en la literatura.
ConclusionesLos médicos deben conocer los efectos adversos que los EAA pueden tener sobre la espermatogénesis. La infertilidad asociada a estos agentes puede ser de carácter reversible, pero la producción de espermatozoides puede tardar más de un año en normalizarse. Tanto el tratamiento conservador como el agresivo pueden estimular la espermatogénesis con resultados satisfactorios. Se requiere una mayor comprensión de la endocrinología reproductiva masculina y datos de alta calidad sobre la recuperación de la espermatogénesis tras el abuso de EAA.
This systematic review aims to evaluate the optimal treatment for male infertility resulting from Anabolic Androgenic Steroids (AAS) abuse.
MethodsA systematic review was performed according to the Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA) statement. Studies that compared different protocols for the recovery of spermatogenesis in patients after AAS use were included.
Results13 studies investigating different protocols to restore spermatogenesis in patients with AAS abuse met the inclusion criteria. The available agents that showed restoration of spermatogenesis include injectable gonadotropins, selective estrogen receptor modulators, and aromatase inhibitors, but their use is still poorly described in the literature.
ConclusionsClinicians need to be aware of the detrimental effects of AAS on spermatogenesis. AAS-associated infertility may be reversible, but sperm production may take over a year to normalize. Both conservative and aggressive treatment can boost spermatogenesis with positive results. Further understanding of male reproductive endocrinology and high-quality data on the field of restoration of spermatogenesis after AAS abuse are warranted.