La endocarditis infecciosa (EI) es una enfermedad sistémica con afectación multiorgánica. Se trata de una entidad grave, que con frecuencia requiere de tratamiento quirúrgico, a pesar del cual las tasas de mortalidad pueden ser elevadas debido a complicaciones derivadas de una respuesta inflamatoria sistémica exacerbada y/o sepsis. Los sistemas de hemadsorción (HA) como Cytosorb® (Cytosorbents Corporation, Nueva Jersey, EE. UU.) permiten la eliminación de citocinas proinflamatorias y endotoxinas para poder mejorar el pronóstico de estos pacientes. Realizamos una búsqueda sistemática en PubMed y Cochrane para identificar trabajos comparativos controlados del uso perioperatorio de Cytosorb® en sujetos intervenidos de cirugía cardiaca por EI. Se efectuó un metaanálisis contrastando diferentes resultados clínicos en el que se incluyeron nueve documentos. La aplicación de la terapia con HA no redujo la mortalidad en el posoperatorio temprano (riesgo relativo [RR]=0,75; p=0,05). Tanto la duración de la ventilación mecánica (diferencia de medias [DM]=-6,91 h; p=0,01) como la del soporte vasopresor (DM=-34,47 h; p=0,03) fueron significativamente menores en el caso de los pacientes tratados con HA. Sin embargo, las estancias posoperatorias, la incidencia de fallo renal posoperatorio o la necesidad de revisión quirúrgica por sangrado no presentaron diferencias entre grupos. Como conclusión, la utilización del filtro de HA Cytosorb® en la cirugía cardiaca por EI permitió un mejor control de la actividad inflamatoria posoperatoria, con menores requerimientos de soporte vasoconstrictor y duración de la ventilación mecánica, pero sin impacto sobre la mortalidad perioperatoria ni otras complicaciones relacionadas.
Infective endocarditis (IE) is a systemic disease with multiorgan involvement. It is a severe disease, which frequently requires surgical treatment, despite which mortality rates can be high due to complications related to an uncontrolled systemic inflammatory response and/or sepsis. Hemadsorption systems such as Cytosorb® allow the removal of proinflammatory cytokines and endotoxins to improve the prognosis of these patients. We performed a systematic review in Pubmed and Cochrane to identify controlled comparative studies of the perioperative use of Cytosorb® in patients undergoing cardiac surgery for IE. A meta-analysis was performed comparing different clinical outcomes. 9 studies were finally included in the meta-analysis. The use of hemadsorption therapy did not reduce mortality in the early postoperative period (RR=0.75; p=0.05). Both, the duration of mechanical ventilation (mean difference=-6.91hours; p=0.01) and the duration of support with vasopressor drugs (mean difference=-34.47hours; p=0.03) were significantly shorter in the case of patients treated with hemadsorption. However, postoperative stays, the incidence of postoperative renal failure or the need for surgical revision due to bleeding did not show differences between groups. To conclude, the use of the Cytosorb® hemadsorption filter in cardiac surgery for IE allowed better control of postoperative inflammatory activity, with lower requirements for vasopressor support and duration of mechanical ventilation, but without impact on perioperative mortality or other related complications.
La endocarditis infecciosa (EI) es una enfermedad sistémica con afectación multiorgánica, que tiene como origen el asentamiento de un proceso infeccioso sobre el endocardio valvular, endotelio vascular y/o cualquier dispositivo protésico intravascular1. Se trata de una entidad grave que, con frecuencia, requiere de terapia quirúrgica para el control de la infección, la retirada del material protésico infectado y/o la corrección de los defectos en la función valvular ocasionados por la destrucción tisular. Esto motiva que, en nuestros días, tenga tasas de mortalidad elevadas llegando a alcanzar 7,6% e incluso 25%2,3. Aun en condiciones óptimas de tratamiento antibiótico, el desarrollo de sepsis suele ser una de las principales causas de resultados posoperatorios adversos4. A esta situación proinflamatoria se añaden los efectos deletéreos del uso de la circulación extracorpórea (CEC) que, a pesar de los avances experimentados en las últimas décadas, sigue siendo un factor independiente de morbimortalidad de los pacientes sometidos a cirugía cardiaca 5,6.
Aquellos que padecen EI, presentan un alto riesgo de desarrollar complicaciones, muchas de ellas relacionadas con el contexto proinflamatorio perioperatorio. De hecho, los sujetos con una situación inflamatoria más exacerbada suelen asociar peor control del proceso infeccioso y mayor daño valvular estructural que se correlacionan con niveles de mediadores séricos más altos6. Como consecuencia, surge la posibilidad de utilizar sistemas de hemadsorción (HA) como Cytosorb® (Cytosorbents Corporation, Nueva Jersey, EE. UU.). Se trata de un filtro extracorpóreo diseñado para la adsorción de citocinas proinflamatorias y otras moléculas circulantes de entre 10 y 55 kDa, la mayoría de ellas son responsables del síndrome vasopléjico y la respuesta inflamatoria exacerbada en pacientes críticos6,7. Estos filtros pueden instalarse en sistemas de CEC similares a la hemodiafiltración o hemodiálsis, pero también a la propia máquina corazón-pulmón empleada durante la intervención, pudiendo aplicarse en las fases pre, intra y posoperatoria en sujetos afectados de EI. Debido a su capacidad adsorbente no selectiva, también es capaz de reducir los niveles plasmáticos de agentes antitrombóticos como el ticagrelor o el rivaroxabán, disminuyendo el riesgo de sangrado en procedimientos emergentes7, aunque también podría aminorar los niveles de antibióticos. Todo ello hace que su aplicación a diferentes campos de la cirugía cardiaca haya mostrado resultados prometedores. Sin embargo, hasta la fecha, no se ha publicado ningún trabajo focalizado en su uso en personas intervenidas de cirugía cardiaca por EI. Realizamos, por tanto, una revisión sistemática y un metaanálisis para poder determinar la utilidad de este sistema de HA en este contexto.
MétodosEstrategia de búsqueda bibliográficaPara cumplir los objetivos del trabajo, se siguió una metodología acorde con las directrices best evidence topic. Se planteó la correspondiente pregunta Patient/Population, Intervention, Comparison, Outcomes (PICO) como: ¿en pacientes intervenidos de cirugía cardiaca por EI, la aplicación del filtro hemadsorbente durante el perioperatorio modifica la morbimortalidad posoperatoria, frente al manejo perioperatorio convencional? Los términos integrantes de la pregunta PICO se recogen en la tabla 1. La cuestión se resolvería con el análisis crítico de la literatura disponible, realizando una búsqueda bibliográfica sistemática.
Para ello, se consultaron las bases de datos PubMed y Cochrane mediante las correspondientes estrategias de búsqueda por palabras clave, identificándose todos los trabajos disponibles hasta el 13 de febrero de 2023. En el caso de PubMed, se utilizó la cadena «CytoSorb» AND «cardiac surgery». Para Cochrane, se aplicó únicamente el criterio «Cytosorb» para la detección de protocolos, revisiones y ensayos clínicos. En ninguno de los casos se plantearon filtros en lo referente al diseño de los trabajos, límite en su fecha de publicación o lengua, de igual manera, se tradujeron al inglés aquellos que no se presentaran en este idioma o en español. Como criterios de exclusión, se eliminaron todos los estudios referentes a pacientes<18 años, los que no estuvieran centrados en sujetos sometidos a tratamiento quirúrgico de EI y los que carecieran de un grupo control comparativo.
Criterios de selección de trabajosDos investigadores realizaron un cribado jerárquico de los artículos obtenidos de la búsqueda, inicialmente por su título, posteriormente, por la evaluación de sus resúmenes y, finalmente, por la valoración del trabajo completo. Se seleccionaron aquellos que ofrecían una comparación entre los resultados clínicos y bioquímicos de los pacientes con EI tratada quirúrgicamente, incluyendo la utilización de un filtro hemadsorbente en el protocolo de manejo frente a aquellos en los que se efectuó un abordaje perioperatorio convencional. Tras la exclusión de los trabajos duplicados, se analizó el contenido para determinar su elegibilidad. Las divergencias entre investigadores se resolvieron por consenso.
Recogida de datos y características de los estudios incluidosSe consideraron las siguientes características de los trabajos analizados: año de publicación, primer autor, diseño del estudio, país de procedencia de la serie de pacientes incluidos, periodo de inclusión, número de participantes, etiología de las endocarditis, método de utilización del filtro de HA, mortalidad y otros resultados posoperatorios (incidencia de fallo renal, duración de la ventilación mecánica, del soporte vasoconstrictor, necesidad de reintervención por sangrado, estancias en Unidad de Cuidados Intensivos/Críticos [UCI] y hospitalaria, así como variación en los niveles plasmáticos de citocinas proinflamatorias). Todas las variables anteriores quedan registradas en la tabla 2. La mortalidad para cada una de las opciones de tratamiento (uso de filtro hemadsorbente vs. manejo convencional), así como los otros resultados posoperatorios fueron analizados por intención de tratar.
Resumen de las principales características y hallazgos de los trabajos incluidos en la revisión
| Primer autor | Año de publicación | Diseño del estudio | País | Periodo de inclusión | n HA | n control | Etiología de la EI | Uso de HA | Reducción CK con HA | CK no alteradas por HA | Principales conclusiones |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Asch et al.9 | 2021 | Ensayo clínico | Multicéntrico, Alemania | 2018-2020 | 10 | 10 | n/d | En CEC | IL-6, TNF alfa, PCR, PCT | La HA no redujo las complicaciones posoperatorias: fallo renal, respiratorias, sangrado, etc. ni demostró niveles significativamente más bajos de CK proinflamatorias en los primeros días del posoperatorio | |
| Diab et al.10 | 2022 | Ensayo clínico | Multicéntrico, Alemania | 2018-2020 | 138 | 144 | 88% G+, 5% G-, 1% hongos, 7% otras | En CEC | IL-1beta, IL-10 8, IL-6, CT-proET-1 | IL-10, TNF alfa, PCT, PCR, MR-proADM, CT-proAVP, MR-proANP | Sin diferencias en términos de necesidad de soporte vasopresor, duración de la ventilación mecánica o terapia de sustitución renal. La HA redujo significativamente algunas de las CK proinflamatorias estudiadas en los primeros días del posoperatorio, particularmente la IL-6 |
| Holmén et al.11 | 2022 | Ensayo clínico | Unicéntrico, Suecia | 2019-2020 | 10 | 9 | n/d | En CEC | n/d | n/d | Reducción del soporte vasopresor a la mitad y de la trasfusión de CH y PP con la utilización de HA. El fallo renal no presentó diferencias significativas |
| Haidari et al.13 | 2020 | Observacional retrospectivo | Unicéntrico, Alemania | 2014-2018 | 30 | 28 | n/d | En CEC | PCT, PCR | Mayor estabilidad hemodinámica con HA y uno de los pocos trabajos que demuestra reducción significativa de la mortalidad relacionada con la sepsis, vinculado con la disminución de algunos marcadores séricos asociados con la misma | |
| Santer et al.14 | 2021 | Observacional retrospectivo | Unicéntrico, Suiza | 2009-2019 | 41 | 200 | n/d | En CEC | PCR, FNG | El grupo con HA presentó mayores requerimientos de soporte vasoconstrictor, revisión quirúrgica por sangrado, trasfusión de CH y PP y similar incidencia de fallo renal, FA y complicaciones respiratorias. Probablemente los pacientes con HA presentaron mayor grado de morbilidad posoperatoria y procesos de EI más agresivos | |
| Totsugawa et al.15 | 2011 | Observacional retrospectivo | Unicéntrico, Japón | 2006-2009 | 11 | 7 | 50% G+, 5% hongo, 45% otras | En CEC (PMX-B) | n/d | n/d | La HA mostró marcada reducción en los requerimientos de soporte vasoconstrictor y duración de la ventilación mecánica |
| Träger et al.16 | 2017 | Observacional retrospectivo | Unicéntrico, Alemania | 2013-2016 | 39 | 28 | 85% G+, 6% G-, 9% otras | En CEC | IL-6, IL-8 | Reducción del tiempo de soporte vasopresor posoperatorio cuando se utilizó la HA. Sin embargo, no se demostró una reducción significativa en los niveles posoperatorios de IL-6 e IL-8 | |
| Kühne et al.17 | 2019 | Observacional retrospectivo | Unicéntrico, Alemania | 2017-2018 | 20 | n/a | 87% G+, 10% G-, 3% otras | 10 en CEC y 10 en CEC y posCEC | n/d | n/d | Único trabajo que extiende la HA al posoperatorio temprano durante las 24 h siguientes. A pesar de que los pacientes con continuación de la HA posCEC eran más comórbidos y graves, tuvieron similares necesidades de soporte vasoconstrictor y fallo renal |
| Kalisnik et al.18 | 2022 | Observacional retrospectivo ajustado por propensity score | Unicéntrico, Alemania | 2015-2021 | 99 | 99 | 80% G+, 5% G-, 15% otras | En CEC | n/d | n/d | Otro de los trabajos que demuestra reducción de la sepsis y la mortalidad posoperatoria, identificando en el análisis multivariante el uso de HA como factor protector independiente |
| Haidari et al.19 | 2023 | Observacional retrospectivo | Dicéntrico, Alemania | 2015-2022 | 75 | 55 | 100% G+ (Staphylococcus aureus) | En CEC | n/d | n/d | La HA demostró menores requerimientos posoperatorios de vasopresores e inotrópicos, siendo el tercer trabajo que observó reducción de la mortalidad relacionada con la sepsis a 30 y 90 días |
CEC: circulación extracorpórea; CT-proAVP: copéptido proarginina-vasopresina; CT-proET-1: péptido C-terminal proendotelina-1; EI: endocarditis infecciosa; FNG: fibrinógeno; G+: grampositivos; G-: gramnegativos; HA: hemadsorción; IL: interleucina; MR-proADM: proadrenomedulina medio-regional; MR-proANP: propéptido atrial natriurético medio-regional; PCR: proteína C reactiva; PCT: procalcitonina; PMX-B: polimixina B; TNF: factor de necrosis tumoral; CK: citokinas; CH: concentrado de hematíes; PP: pool de plaquetas; FA: fibrilación auricular; n/d: no disponible.
La validez interna y el riesgo de sesgos de los estudios incluidos fueron analizados por otros dos revisores independientes, de acuerdo con las guías propuestas por la Cochrane Collaboration Methods, resolviendo las diferencias surgidas por consenso. En el análisis estadístico, los sesgos de publicación se revisaron gráficamente mediante funnel-plot. Se estableció un límite en el nivel de heterogeneidad de 50%, medido a través del estadístico Q de Cochrane. La inconsistencia fue evaluada mediante el estadístico I2.
Análisis cuantitativoPara el análisis cuantitativo se llevó a cabo un cálculo estadístico mediante la plataforma RevMan versión 5.3 (RevMan, Cochrane Collaboration, Oxford, UK), de conformidad con lo establecido según la Quality of Reporting of Meta-Analyses guidelines (QUORUM) y la Preferred Reporting Items for Systematic Reviewers and Meta-Analyses (PRISMA)8. La magnitud del efecto fue expresada como diferencia de medias (DM) para las variables continuas y como riesgo relativo (RR) para las dicotómicas junto a su correspondiente valor de intervalo de confianza al 95% (IC 95%). La interpretación de los valores adoptados por la magnitud de efecto consistió, en el caso de la DM: DM <0 y sin inclusión en el IC 95%, que se tradujo como superioridad estadísticamente significativa de la terapia con HA o DM >0 y sin inclusión en el IC 95%, que se interpretó como superioridad significativa del manejo estándar; para las variables dicotómicas, se tradujo el valor del RR <1 y sin inclusión en el IC 95%, como superioridad estadísticamente significativa de la terapia con HA o RR >1 y sin inclusión en el IC 95%, que reveló superioridad significativa del enfoque estándar. El cálculo de la magnitud de efecto se llevó a cabo por medio de la prueba inversa de la varianza para las variables continuas y la de Mantel-Haenszel para las dicotómicas, con base en un modelo de efectos aleatorios cuando la inconsistencia estadística fue alta (I2 ≥25%) o de efectos fijos cuando esta fue baja (I2 <25%). El análisis de la sensibilidad se efectuó por medio de la exclusión secuencial de cada uno de los trabajos incluidos en el modelo, repitiendo el metaanálisis y comprobando la influencia en el resultado global de la magnitud de efecto. Se estableció un nivel de significación estadística para las pruebas de contraste de hipótesis de 5% y para las de heterogeneidad de 10%. Para aquellos resultados que no siguieron una forma de presentación homogénea en los diferentes estudios, se realizó una revisión simple expresando un resumen de los principales hallazgos que quedaron plasmados en la tabla 2.
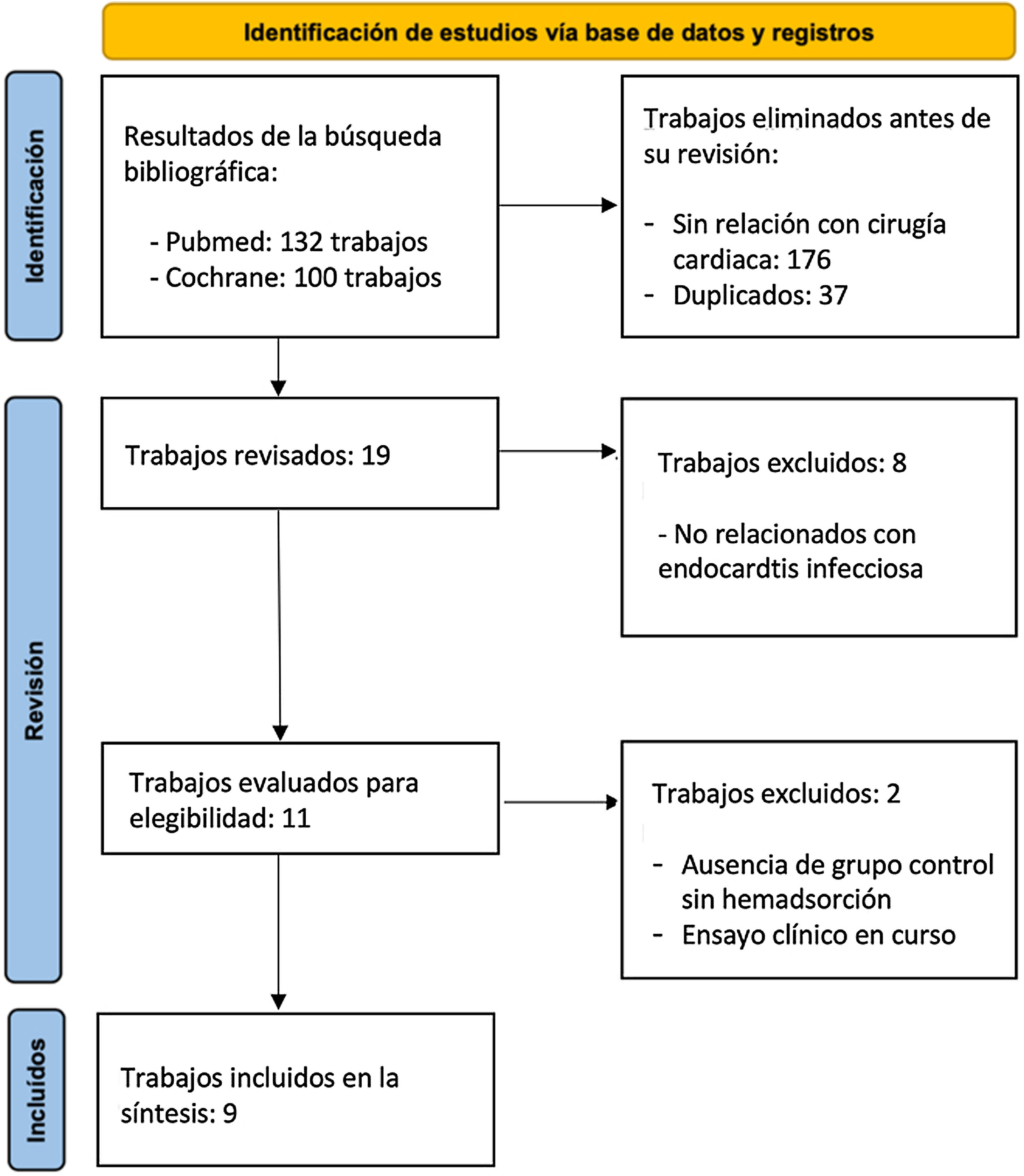
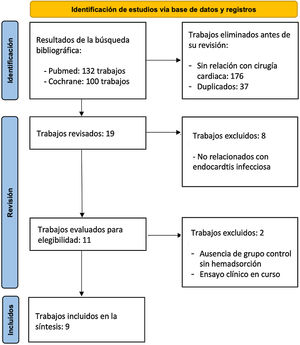
ResultadosResultados de la búsqueda bibliográficaPor medio de la estrategia de búsqueda por palabras clave, se obtuvieron 132 trabajos en PubMed y 100 entradas en Cochrane correspondientes a ensayos clínicos. De estos, 17 en PubMed correspondieron a aquellos relacionados con cirugía cardiaca que cumplieron los criterios de selección, siendo 11 los focalizados en EI9–19. En el caso de Cochrane, cuatro estudios se refirieron al uso de filtros de HA en el contexto del tratamiento quirúrgico de la EI9–12. No se han realizado revisiones en Cochrane hasta la fecha con referencia al uso de Cytosorb®. Con la retirada de duplicados, trabajos sin datos suficientes o sin grupo control, nueve se incluyeron en el análisis cuantitativo9–11,13–16,18,19. El flujo de selección queda resumido en el diagrama PRISMA de la figura 1.
La evidencia analizada comprendió cuatro ensayos clínicos9–11, excluyendo aquel que se encontraba en curso12, y seis trabajos observacionales retrospectivos13–16,18,19. No se han realizado revisiones ni metaanálisis previos focalizados en la aplicación de la HA en el perioperatorio de cirugía valvular por EI. Solo se identificó un trabajo de metaanálisis previo7 que agregaba pacientes donde se utilizó la HA por diferentes indicaciones clínicas. Desde el punto de vista metodológico, los ensayos comprendieron variables diferentes y las ponderaron con distintos criterios en lo que respecta a la valoración de la actividad proinflamatoria y las variaciones séricas de los mediadores implicados. Otras complicaciones posoperatorias como la necesidad de soporte vasoconstrictor, la duración de la ventilación mecánica, la incidencia de fallo renal (con/sin necesidad de terapia de sustitución renal), la necesidad de reoperación por sangrado o la duración de la estancia posoperatoria en UCI y la hospitalaria, fueron reportadas en algunos documentos, lo cual posibilitó su análisis agregado. La mortalidad de los diferentes grupos de estudio se refirió al posoperatorio temprano en todas las investigaciones (durante el ingreso y/o en los primeros 30 días) y se incluyeron datos de todos los artículos en la síntesis cuantitativa. En todos se utilizó el sistema de HA con Cytosorb® excepto en uno donde se aplicó un sistema basado en fibras de polimixina B (Toraymyxin, Toray Industries, Tokio, Japón) con el mismo objetivo. El análisis conjunto de ambos ya ha sido efectuado en trabajos previos7.
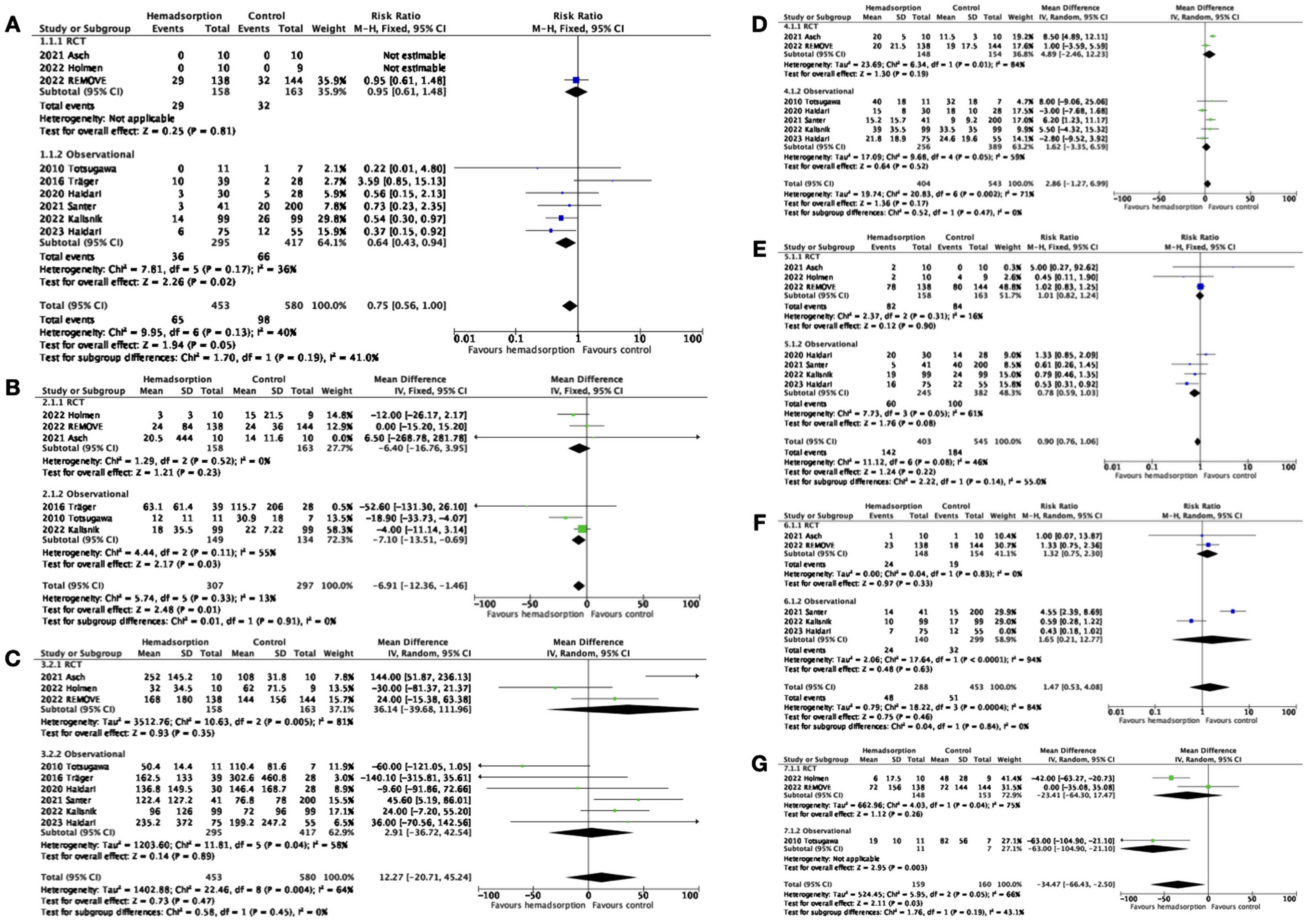
Síntesis de la evidencia y análisis cuantitativoLa tabla 2 recoge un resumen pormenorizado de las características metodológicas de los estudios, así como uno de sus principales hallazgos. En lo que se refiere al análisis cuantitativo, la aplicación de la terapia con HA no redujo significativamente la mortalidad en el posoperatorio temprano (RR=0,75; IC 95% = 0,56-1,00; p=0,05; I2=40%) tanto en ensayos clínicos como en estudios observacionales. La duración de la ventilación fue significativamente mayor en los pacientes manejados sin filtro de HA (DM=-6,91 h; IC 95% = -12,36 a -1,46; p=0,01; I2=13%). Las estancias posoperatorias tanto en UCI (DM=12,27 h; IC 95% = -20,71 a 45,24; p=0,47; I2=64%) como hospitalaria (DM=2,86 días; IC 95% = -1,27 a 6,99; p=0,17; I2=71%) no fueron significativamente diferentes entre grupos. Tampoco lo fueron la incidencia de fallo renal posoperatorio (RR=0,90; IC 95% = 0,76-1,06; p=0,22; I2=46%) o la necesidad de revisión quirúrgica por sangrado (RR=1,47; IC 95% = 0,53-4,08; p=0,46; I2=64%). Sin embargo, la duración del soporte con vasopresores fue marcadamente menor en el caso de los pacientes tratados con HA (DM=-34,47 h; IC 95% = -66,43 a -2,50; p=0,03; I2=66%). En el caso de los ensayos clínicos, no se encontraron diferencias significativas en uno de ellos, mientras que en el otro y el trabajo observacional que reportaron este resultado, hallaron variaciones en favor de la HA. El trabajo de Haidari et al.19 también observó diferencias significativas en la necesidad de soporte vasopresor, pero la expresión en un formato diferente al de los otros estudios no permitió incluirlo en la síntesis cuantitativa. La figura 2 recoge los hallazgos del análisis cuantitativo y la figura 3 los funnel-plot, que no demostraron sesgos de publicación relevantes.
Resultados del metaanálisis de A) mortalidad posoperatoria, B) duración de la ventilación mecánica, C) duración de la estancia posoperatoria en unidad de cuidados críticos/intensivos, D) duración de la estancia posoperatoria hospitalaria, E) fallo renal posoperatorio, F) necesidad de revisión quirúrgica por sangrado, G) duración del soporte vasoconstrictor. 95% CI: intervalo de confianza al 95%; IV: test de inversa de la varianza; M-H: test de Mantel-Haenszel; RCT: ensayo clínico aleatorizado; SD: desviación estándar.
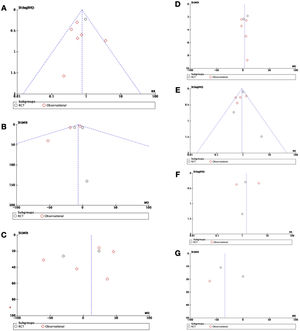
Análisis del sesgo de publicación mediante funnel-plots de A) mortalidad posoperatoria, B) duración de la ventilación mecánica, C) duración de la estancia posoperatoria en unidad de cuidados críticos/intensivos, D) duración de la estancia posoperatoria hospitalaria, E) fallo renal posoperatorio, F) necesidad de revisión quirúrgica por sangrado, G) duración del soporte vasoconstrictor. RCT: ensayo clínico aleatorizado.
Se trata de la revisión sistemática sobre la utilización del filtro de HA de citocinas inflamatorias CytoSorb® en el contexto de cirugía cardiaca de pacientes afectados por EI más extensa realizada hasta la fecha. Las principales conclusiones que podemos obtener de la revisión efectuada se enumeran de la siguiente manera:
- -
Se demuestra una eficacia del sistema, en términos de reducción de los niveles séricos de algunos mediadores inflamatorios estudiados.
- -
También se revela la repercusión clínica del anterior efecto en forma de una reducción de la duración del soporte con aminas vasopresoras, así como de ventilación mecánica, al conseguirse una estabilización hemodinámica más temprana de los pacientes.
- -
Algunos trabajos18,19 consiguieron reportar un beneficio en cuanto a la mejor supervivencia de los sujetos de forma global18,19 y/o relacionada con sepsis13.
- -
No se demostró una disminución significativa del tiempo de estancia en la UCI u hospitalaria posoperatoria, ni en complicaciones como la incidencia de fallo renal posoperatorio o la necesidad de revisión por sangrado.
Los resultados de los estudios aleatorizados fueron globalmente congruentes con la literatura observacional, excepto en la necesidad de revisión por sangrado, donde esta fue superior en el subgrupo de pacientes manejados con filtro de HA. Este hallazgo probablemente se justifique por el diseño retrospectivo de los trabajos donde, a personas con riesgo aumentado de sangrado, se les añadió esta terapia con el fin de tratar de reducir esta complicación.
Trabajos previos han demostrado la utilidad de los filtros de HA en personas con diferentes condiciones7 (retirada de fármacos anticoagulantes circulantes, EI, cirugía compleja con CEC prolongada: síndrome aórtico agudo, trasplante cardiaco, etc.) particularmente en el contexto de la cirugía urgente/emergente. Sin embargo, el carácter multifactorial2 en la etiología de diferentes complicaciones posoperatorias como el fallo renal, el sangrado o incluso la propia mortalidad posoperatoria, hacen que la corrección de un único factor, como es el contexto proinflamatorio del síndrome de respuesta inflamatoria sistémica (SRIS), no sea suficiente para mostrar diferencias entre pacientes tratados con estos sistemas y aquellos que reciben un manejo terapéutico convencional.
Además, a pesar de estudiar la aplicación de Cytosorb® en pacientes afectados de una sola patología, no es suficiente para controlar la marcada heterogeneidad con que esta se presenta, tanto por la afectación valvular, como de microorganismos causales, como de otras condiciones perioperatorias3. De hecho, estudios como el de Santer et al.14 hacen hincapié en la falta de selectividad de la HA, la cual ha demostrado ser eficaz en la retirada de múltiples agentes proinflamatorios que se han recogido en la tabla 2. Sin embargo, otros como el cortisol20, el tromboxano21, la pro-endotelina-122 o la albúmina23 también contribuyen a mantener la homeostasis del tono vasomotor y el equilibrio hidroelectrolítico y presentan una reducción de sus niveles plasmáticos durante la HA. De hecho, es posible que cada paciente exhiba diferentes causas por las que se instaura el shock distributivo o el SRIS y, por consiguiente, los efectos de la HA poco discriminativa puedan ser beneficiosos en unos casos, pero en otros no conseguir el efecto buscado, cuando incluso podrían ser deletéreos.
En definitiva, el conocimiento en el campo del uso de este tipo de dispositivos todavía es incipiente, identificándose trabajos en la literatura que merecen especial mención. El primero, de Kühne et al.17 revisó los efectos de extender el uso de la HA más allá de la aplicación exclusivamente durante la CEC, práctica común a todos los artículos analizados. Los autores concluyeron que se trataba de una práctica segura al realizarla durante aproximadamente las 24 horas siguientes a la intervención, y que podía aportar beneficio especialmente en el subgrupo de pacientes intervenidos de EI que desarrollan fallo renal en relación con inestabilidad hemodinámica por la presencia de sepsis derivada de una infección sistémica mal controlada y/o procedimientos de alta complejidad. El segundo trabajo, de Scheier et al.24, sirve de referencia para conocer aquellos agentes farmacológicos (analgésicos, antiarrítmicos, anticonvulsivantes, antidepresivos, antihipertensivos, antibióticos, anticoagulantes, ansiolíticos e inmunosupresores) que se ven afectados por la instauración del filtro de HA y que constituyen parte del tratamiento perioperatorio de los individuos intervenidos de cirugía cardiaca. Se trata de un trabajo de revisión en sí mismo que actualiza la evidencia a este respecto. A efectos de la terapia antibiótica aplicada a los sujetos afectados de EI, la tabla 3 (modificada del trabajo de Scheier et al.24) registra los agentes farmacológicos que sufren modificaciones o permanecen inalterados con la aplicación de la terapia de HA. Estos factores deben tenerse en cuenta en la redosificación de los agentes antibióticos para mantener su eficacia durante el empleo de la HA y podrían haber supuesto un sesgo en el diseño y en los resultados de los estudios, ya que la tipificación del tratamiento antibiótico de los grupos comparados está mal reflejada en los trabajos analizados. De hecho, en el seguimiento no se disponen de datos de ninguno de los artículos que nos pudieran revelar las consecuencias de la aplicación de la HA a medio plazo, como, por ejemplo, la tasa de recidiva de endocarditis, que hubiera obligado a expresar resultados al menos a un año. No obstante, la reducción de los niveles séricos de antibiótico que puede provocar la terapia de HA solo habría tenido lugar intraoperatoriamente, ya que fue la forma de aplicación en la práctica totalidad de los artículos revisados, por lo que no cabría esperar diferencias significativas entre los grupos de estudio. Sin embargo, la prolongación de la terapia con HA en el posoperatorio debería tener en cuenta aspectos como el de los niveles séricos de antibiótico, ya que podría generar resultados paradójicamente deletéreos en relación con la recidiva de la endocarditis.
Efectos de la hemadsorción sobre los niveles plasmáticos de antibióticos
| Reducción >60% de los niveles plasmáticos in vivo | Niveles plasmáticos inalterados in vivo |
|---|---|
| Amfotericina A | Anidalfungina |
| Fluconazol | Cefalosporinas |
| Linezolid | Quinolonas |
| Vancomicina | Claritromicina |
| Teicoplanina | Clindamicina |
| Tobramicina | Meropenem |
| Metronidazol | |
| Piperacilina |
Modificación de niveles plasmáticos in vivo de algunos agentes antibióticos aplicados en el tratamiento de la endocarditis infecciosa durante la hemadsorción (modificado de Scheier et al.24).
La utilización del filtro de HA Cytosorb® durante la CEC en personas intervenidas de cirugía cardiaca por EI permitió un mejor control de la actividad inflamatoria posoperatoria, con menores requerimientos de soporte vasoconstrictor y duración de la ventilación mecánica en la mayoría de los artículos analizados. Estos resultados se tradujeron en una reducción de la mortalidad posoperatoria en una minoría de los trabajos, sin existir diferencias en el resto. La HA no disminuyó la duración de las estancias en UCI u hospitalaria posoperatorias, así como tampoco otras complicaciones (fallo renal, sangrado y requerimientos transfusionales). Se necesitan estudios aleatorizados con tamaños muestrales suficientes que homogeneicen las características clínicas y los tratamientos perioperatorios de los grupos de ensayo para neutralizar los potenciales sesgos y poder emitir conclusiones sólidas sobre los beneficios de la HA en pacientes con EI.
FinanciaciónEl trabajo no ha recibido ningún tipo de financiación para su elaboración.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.