La gangrena de Fournier (GF) es la fascitis necrosante del periné y área genital que presenta una elevada mortalidad. El objetivo es analizar los factores pronósticos de mortalidad, creación de una nueva escala predictiva de mortalidad y compararla con las ya validadas en los pacientes diagnosticados de GF en nuestro Servicio de Urgencias.
MétodosEstudio analítico, retrospectivo entre 1998 y 2012.
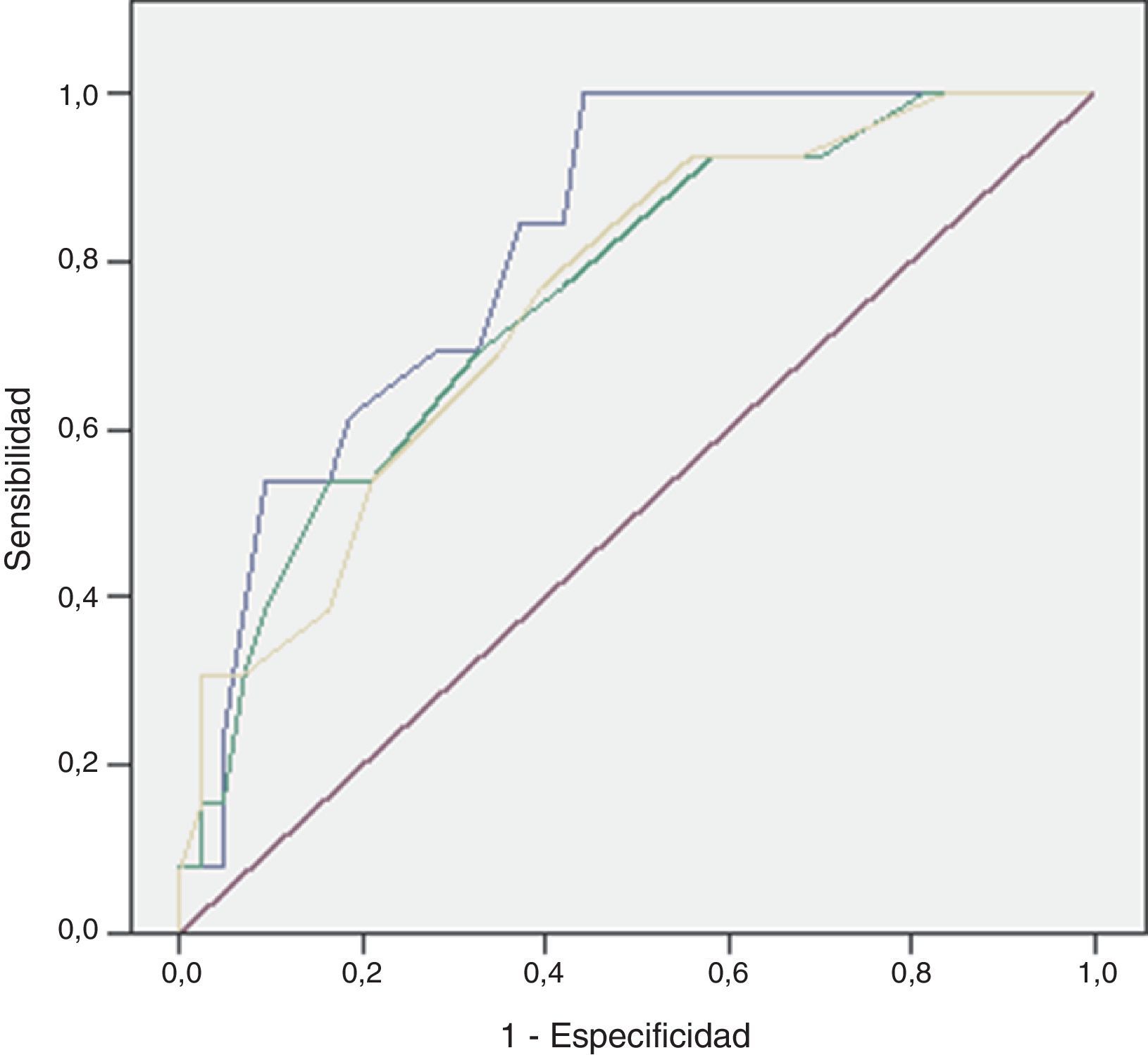
ResultadosDe los 59 casos, 44 sobrevivieron (74%) (S) y 15 fallecieron (26%) (E). Se encontraron diferencias significativas en la vasculopatía periférica (S 5 [11%]; E 6 [40%]; p=0,023), hemoglobina (S 13; E 11; p=0,014), hematocrito (S 37; E 31,4; p=0,009), leucocitos (S 17.400; E 23.800; p=0,023), urea (S 58; E 102; p<0,001), creatinina (S 1,1; E 1,9; p=0,032), potasio (S 3,7; E 4,4; p=0,012) y fosfatasa alcalina (S 92; E 133; p=0,014). Escalas predictivas: índice de Charlson (S 1; E 4; p=0,013), criterios de sepsis grave (S 16 [36%]; E 13 [86%]; p=0,001), Fournier's gangrene severity index score (FGSIS) (S 4; E 7; p=0,002) y Uludag Fournier's Gangrene Severity Index (UFGSI) (S 9; E 13; p=0,004). Los factores predictores independientes fueron la vasculopatía periférica, el potasio sérico y criterios de sepsis grave, creando un modelo con área bajo la curva de 0,850 (0,760-0,973) superior al FGSIS (0,746 [0,601-0,981]) y al UFGSI (0,760 [0,617-0,904]).
ConclusionesLa GF presentó una tasa de mortalidad elevada cuyos factores predictores independientes fueron la vasculopatía periférica, el potasio sérico y criterios de sepsis grave, creando un modelo con una capacidad discriminativa superior al resto.
Fournier's gangrene (FG) is the necrotizing fasciitis of the perineum and genital area and presents a high mortality rate. The aim was to assess prognostic factors for mortality, create a new mortality predictive scale and compare it with previously published scales in patients diagnosed with FG in our Emergency Department.
MethodsRetrospective analysis study between 1998 and 2012.
ResultsOf the 59 patients, 44 survived (74%) (S) and 15 died (26%) (D). Significant differences were found in peripheral vasculopathy (S 5 [11%]; D 6 [40%]; P=.023), hemoglobin (S 13; D 11; P=.014), hematocrit (S 37; D 31.4; P=.009), white blood cells (S 17,400; D 23,800; P=.023), serum urea (S 58; D 102; P<.001), creatinine (S 1.1; D 1.9; P=.032), potassium (S 3.7; D 4.4; P=.012) and alkaline phosphatase (S 92; D 133; P=.014). Predictive scores: Charlson index (S 1; D 4; P=.013), severe sepsis criteria (S 16 [36%]; D 13 [86%]; P=.001), Fournier's gangrene severity index score (FGSIS) (S 4; D 7; P=.002) and Uludag Fournier's Gangrene Severity Index (UFGSI) (S 9; D 13; P=.004). Independent predictive factors were peripheral vasculopathy, serum potassium and severe sepsis criteria, and a model was created with an area under the ROC curve of 0.850 (0.760-0.973), higher than FGSIS (0.746 [0.601-0.981]) and UFGSI (0.760 [0.617-0.904]).
ConclusionsFG showed a high mortality rate. Independent predictive factors were peripheral vasculopathy, potassium and severe sepsis criteria creating a predictive model that performed better than those previously described.
La gangrena de Fournier (GF) es la fascitis necrosante polimicrobiana del periné y área genital, cuya etiología puede ser colorrectal, genitourinaria, traumática o idiopática. Afecta principalmente a varones entre la 5.a-7.a décadas de la vida con factores predisponentes en la mayoría. Su tratamiento es multidisciplinar, incluyendo soporte hemodinámico en unidad de cuidados intensivos (UCI), antibioterapia de amplio espectro y desbridamiento quirúrgico siendo, en ocasiones, necesaria la realización de colostomía, cistostomía suprapúbica u orquiectomía. Su tasa de mortalidad es elevada (7-75%) siendo las escalas predictivas validadas complejas y potencialmente mejorables, dado que están constituidas parcialmente por variables que no han demostrado diferencias significativas, lo que disminuye su capacidad predictiva1–4.
El objetivo del estudio es analizar los factores pronósticos de mortalidad, creación de una nueva escala predictiva de mortalidad y compararla con las ya validadas en una serie de pacientes diagnosticados de GF en nuestro Servicio de Urgencias.
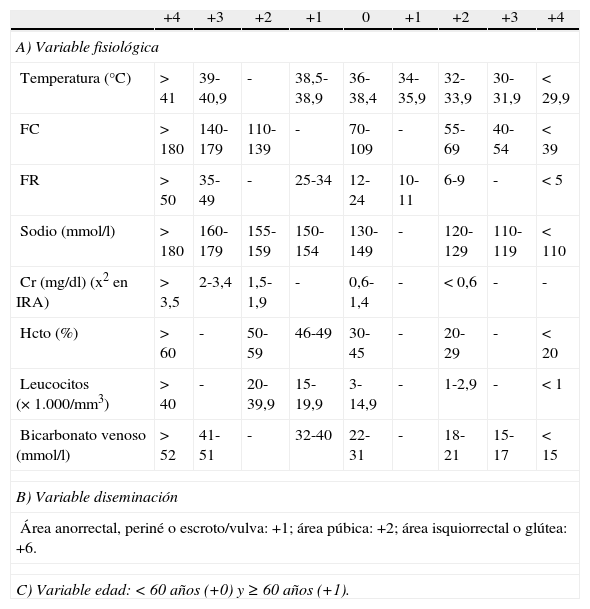
MétodosEstudio observacional, analítico de cohortes, retrospectivo durante un período de 15 años (1998-2012), realizado en el Servicio de Urgencias del Hospital General Universitario Gregorio Marañón. Se incluyó a todos los pacientes diagnosticados de GF en el Servicio de Urgencias mediante la clínica y, en los casos en los que procediese, confirmándolo mediante prueba radiológica. Se excluyó a aquellos pacientes con una historia clínica incompleta. Las variables independientes recogidas fueron la edad, sexo, comorbilidades asociadas, índice de comorbilidad de Charlson (ICC) e índice de comorbilidad de Charlson ajustado a la edad (ICCAE)5, etiología, constantes (temperatura, tensión arterial, frecuencia cardíaca y respiratoria), sintomatología, analítica (los valores de potasio sérico dados por nuestro laboratorio se consideraron normales al estar comprendidos en 3,5-4,5mmol/l), síndrome de respuesta inflamatoria sistémica (SRIS) (definido como el cumplimiento de 2 o más de los siguientes criterios: frecuencia cardíaca >90 latidos por min, frecuencia respiratoria >20 por min o PaC02 <32mmHg, temperatura >38°C o <36°C, leucocitos >12.000/mm3, <4.000/mm3 o >10% de formas inmaduras), sepsis grave (definida como sepsis [SRIS más una infección documentada clínica o microbiológicamente] asociada a disfunción de órganos, hipotensión o hipoperfusión tisular. Variables de disfunción orgánica: renal [creatinina >2mg/dl, incremento>0,5mg/dl o diuresis <0,5ml//kg/h durante al menos 2 h], pulmonar [hipoxemia arterial con PaO2/FIO2 <300], hepática [plaquetas <100.000/mm3, bilirrubina total >2mg/dl, INR >1,5 o tiempo de tromboplastina parcial activada >60 segundos]. Variables de hipotensión arterial: tensión arterial sistólica <90mmHg, tensión arterial media <70mmHg o descenso de la tensión arterial sistólica >40mmHg con respecto a su valor basal. Variables de hipoperfusión tisular: lactato >3mmol/l)6, estancia en UCI y uso de fármacos vasoactivos, antibiótico empleado, superficie corporal afecta (SCA) medida con el normograma empleado en pacientes quemados según el cual pene (1%), cada escroto (1%), periné (1%) y cada fosa isquiorrectal (2,5%)3,4, tratamiento quirúrgico asociado al desbridamiento (colostomía, cistostomía u orquiectomía), cultivo microbiológico y escalas predictivas (Fournier's Gangrene Severity Index Score [FGSIS] y Uludag Fournier's Gangrene Severity Index [UFGSI]) (tabla 1)2–4. La variable dependiente recogida fue la mortalidad. La recogida de datos se realizó mediante revisión de historias clínicas. El protocolo de estudio fue aprobado por el Comité Ético de Investigación Clínica considerándolo, dado el carácter retrospectivo en el que no se realiza ninguna intervención, una investigación sin riesgo.
Escalas de gravedad en la gangrena de Fournier
| +4 | +3 | +2 | +1 | 0 | +1 | +2 | +3 | +4 | |
| A) Variable fisiológica | |||||||||
| Temperatura (°C) | > 41 | 39-40,9 | - | 38,5-38,9 | 36-38,4 | 34-35,9 | 32-33,9 | 30-31,9 | < 29,9 |
| FC | > 180 | 140-179 | 110-139 | - | 70-109 | - | 55-69 | 40-54 | < 39 |
| FR | > 50 | 35-49 | - | 25-34 | 12-24 | 10-11 | 6-9 | - | < 5 |
| Sodio (mmol/l) | > 180 | 160-179 | 155-159 | 150-154 | 130-149 | - | 120-129 | 110-119 | < 110 |
| Cr (mg/dl) (x2 en IRA) | > 3,5 | 2-3,4 | 1,5-1,9 | - | 0,6-1,4 | - | < 0,6 | - | - |
| Hcto (%) | > 60 | - | 50-59 | 46-49 | 30-45 | - | 20-29 | - | < 20 |
| Leucocitos (× 1.000/mm3) | > 40 | - | 20-39,9 | 15-19,9 | 3-14,9 | - | 1-2,9 | - | < 1 |
| Bicarbonato venoso (mmol/l) | > 52 | 41-51 | - | 32-40 | 22-31 | - | 18-21 | 15-17 | < 15 |
| B) Variable diseminación | |||||||||
| Área anorrectal, periné o escroto/vulva: +1; área púbica: +2; área isquiorrectal o glútea: +6. | |||||||||
| C) Variable edad: < 60 años (+0) y ≥ 60 años (+1). | |||||||||
A: Fournier's Gangrene Severity Index Score; A+B+C: Uludag Fournier's Gangrene Severity; Cr: creatinina; FC: frecuencia cardíaca; FR: frecuencia respiratoria; Hcto: hematocrito; IRA: insuficiencia renal aguda.
El análisis estadístico se realizó con el programa SPSS® versión 21.0 para Windows, definiendo las variables cualitativas mediante frecuencia y porcentaje y las cuantitativas mediante la mediana y percentiles 25-75. Los test estadísticos empleados en el análisis univariante fueron el de chi cuadrado y el exacto de Fisher para las cualitativas y Mann-Whitney y Kruskal-Wallis para las cuantitativas. El estudio multivariante se realizó mediante un modelo de regresión logística binaria, incluyendo aquellas variables significativas en el estudio univariante (p<0,05). Para valoración de la capacidad discriminativa del modelo creado y de los existentes se empleó el área bajo la curva (ABC) ROC y para la comparación de estas se empleó el test de Sidak del programa estadístico STATA para Windows.
ResultadosDe los 59 pacientes incluidos, 53 eran varones (90%) y 6 mujeres (10%) con una mediana de edad de 68 años (51-73) y antecedentes personales en 48 de ellos (81%) que englobaron hipertensión arterial en 29 (49%), diabetes mellitus (DM) en 25 (36%), cardiopatía en 17 (29%), inmunodepresión en 14 (24%) (10 neoplasias, 2 tratamientos quimioterápicos, un tratamiento corticoideo y un síndrome de inmunodeficiencia adquirida), alcoholismo en 12 (20%), tabaquismo en 12 (20%), nefropatía en 9 (15%) y neumopatía en 8 (14%), con un ICC de 1 (0; 3) e ICCAE de 4 (2; 6).
La etiología fue colorrectal en 31 casos (52%) (26 abscesos y 5 neoplasias), genitourinaria en 12 (20%) (10 orquiepididimitis y 2 neoplasias vesicales), traumática en 9 (15%) (5 úlceras por presión, 2 sondajes vesicales, un accidente de tráfico y una perforación por cuerpo extraño) e idiopática en 7 (12%).
De los 59 pacientes, 44 (74%) sobrevivieron y 15 (25%) fallecieron con una estancia hospitalaria de 30 (18-56) y 8 (4-16) días respectivamente. La mortalidad por etiología fue: colorrectal 5 (16%), genitourinaria 6 (50%), traumática 4 (44%) e idiopática 0 (0%), p=0,095. Las causas de la muerte fueron: fallo multiorgánico en 12 (80%), neumonía en uno, tromboembolismo pulmonar en uno e infarto agudo de miocardio en otro caso. El análisis de los factores predictores de mortalidad se muestra en las tablas 2 y 3. El análisis multivariante mostró que las variables predictoras independientes fueron la vasculopatía periférica, niveles altos de potasio sérico y los criterios de sepsis grave (tabla 4). El modelo creado se caracterizó por: constante de −7,566, una correcta calibración interna (Hosmer-Lemeshow: p=0,405) y un ABC de 0,850 (0,760-0,973).
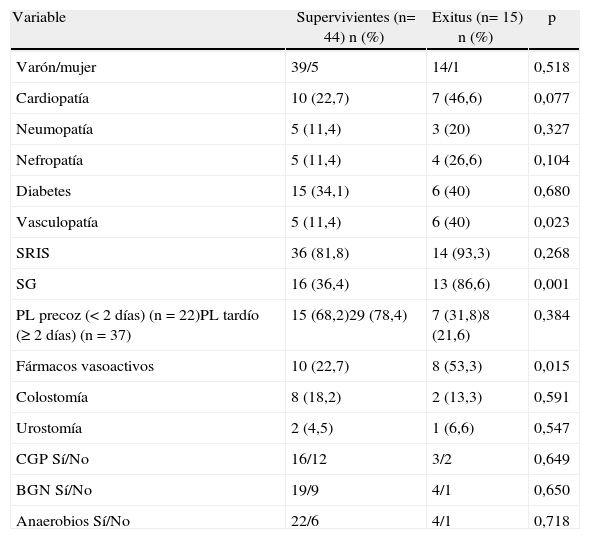
Análisis univariante de variables cualitativas predictoras de mortalidad
| Variable | Supervivientes (n= 44) n (%) | Exitus (n= 15) n (%) | p |
| Varón/mujer | 39/5 | 14/1 | 0,518 |
| Cardiopatía | 10 (22,7) | 7 (46,6) | 0,077 |
| Neumopatía | 5 (11,4) | 3 (20) | 0,327 |
| Nefropatía | 5 (11,4) | 4 (26,6) | 0,104 |
| Diabetes | 15 (34,1) | 6 (40) | 0,680 |
| Vasculopatía | 5 (11,4) | 6 (40) | 0,023 |
| SRIS | 36 (81,8) | 14 (93,3) | 0,268 |
| SG | 16 (36,4) | 13 (86,6) | 0,001 |
| PL precoz (< 2 días) (n=22)PL tardío (≥ 2 días) (n=37) | 15 (68,2)29 (78,4) | 7 (31,8)8 (21,6) | 0,384 |
| Fármacos vasoactivos | 10 (22,7) | 8 (53,3) | 0,015 |
| Colostomía | 8 (18,2) | 2 (13,3) | 0,591 |
| Urostomía | 2 (4,5) | 1 (6,6) | 0,547 |
| CGP Sí/No | 16/12 | 3/2 | 0,649 |
| BGN Sí/No | 19/9 | 4/1 | 0,650 |
| Anaerobios Sí/No | 22/6 | 4/1 | 0,718 |
BGN: bacilos gramnegativos; CGP: cocos grampositivos; PL: período de latencia (inicio de síntomas hasta diagnóstico); SG: sepsis grave; SRIS: síndrome de respuesta inflamatoria sistémica.
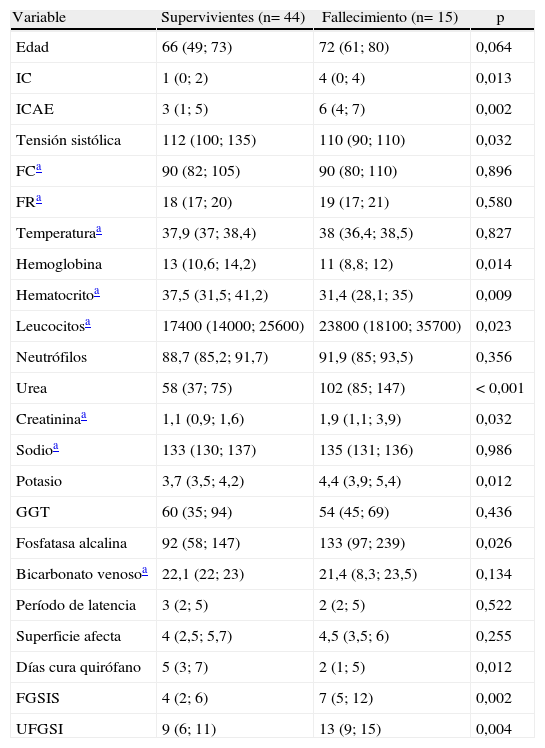
Análisis univariante de las variables cuantitativas predictoras de mortalidad
| Variable | Supervivientes (n= 44) | Fallecimiento (n= 15) | p |
| Edad | 66 (49; 73) | 72 (61; 80) | 0,064 |
| IC | 1 (0; 2) | 4 (0; 4) | 0,013 |
| ICAE | 3 (1; 5) | 6 (4; 7) | 0,002 |
| Tensión sistólica | 112 (100; 135) | 110 (90; 110) | 0,032 |
| FCa | 90 (82; 105) | 90 (80; 110) | 0,896 |
| FRa | 18 (17; 20) | 19 (17; 21) | 0,580 |
| Temperaturaa | 37,9 (37; 38,4) | 38 (36,4; 38,5) | 0,827 |
| Hemoglobina | 13 (10,6; 14,2) | 11 (8,8; 12) | 0,014 |
| Hematocritoa | 37,5 (31,5; 41,2) | 31,4 (28,1; 35) | 0,009 |
| Leucocitosa | 17400 (14000; 25600) | 23800 (18100; 35700) | 0,023 |
| Neutrófilos | 88,7 (85,2; 91,7) | 91,9 (85; 93,5) | 0,356 |
| Urea | 58 (37; 75) | 102 (85; 147) | < 0,001 |
| Creatininaa | 1,1 (0,9; 1,6) | 1,9 (1,1; 3,9) | 0,032 |
| Sodioa | 133 (130; 137) | 135 (131; 136) | 0,986 |
| Potasio | 3,7 (3,5; 4,2) | 4,4 (3,9; 5,4) | 0,012 |
| GGT | 60 (35; 94) | 54 (45; 69) | 0,436 |
| Fosfatasa alcalina | 92 (58; 147) | 133 (97; 239) | 0,026 |
| Bicarbonato venosoa | 22,1 (22; 23) | 21,4 (8,3; 23,5) | 0,134 |
| Período de latencia | 3 (2; 5) | 2 (2; 5) | 0,522 |
| Superficie afecta | 4 (2,5; 5,7) | 4,5 (3,5; 6) | 0,255 |
| Días cura quirófano | 5 (3; 7) | 2 (1; 5) | 0,012 |
| FGSIS | 4 (2; 6) | 7 (5; 12) | 0,002 |
| UFGSI | 9 (6; 11) | 13 (9; 15) | 0,004 |
FC: frecuencia cardíaca; FGSIS: Fournier's Gangrene Severity Index Score; FR: frecuencia respiratoria; GGT: gammaglutamiltranspeptidasa; IC: índice de Charlson; ICAE: índice de Charlson ajustado a la edad; UFGSI: Uludag Fournier Gangrene Severity Index.
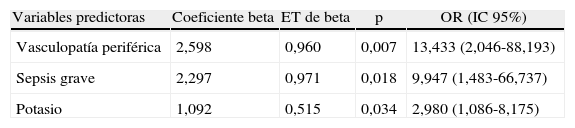
Factores predictores de mortalidad en regresión logística
| Variables predictoras | Coeficiente beta | ET de beta | p | OR (IC 95%) |
| Vasculopatía periférica | 2,598 | 0,960 | 0,007 | 13,433 (2,046-88,193) |
| Sepsis grave | 2,297 | 0,971 | 0,018 | 9,947 (1,483-66,737) |
| Potasio | 1,092 | 0,515 | 0,034 | 2,980 (1,086-8,175) |
ET: error típico; IC: intervalo de confianza; OR: odds ratio.
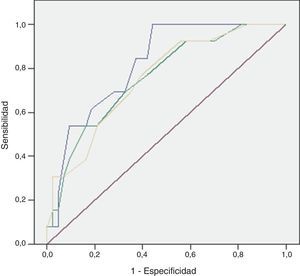
La capacidad discriminativa de las escalas establecidas se muestra en la tabla 5 y la comparación de los diferentes modelos en la figura 1.
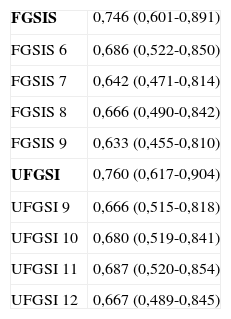
Capacidad discriminativa de FGSIS y UFGSI y sus puntos de corte
| FGSIS | 0,746 (0,601-0,891) |
| FGSIS 6 | 0,686 (0,522-0,850) |
| FGSIS 7 | 0,642 (0,471-0,814) |
| FGSIS 8 | 0,666 (0,490-0,842) |
| FGSIS 9 | 0,633 (0,455-0,810) |
| UFGSI | 0,760 (0,617-0,904) |
| UFGSI 9 | 0,666 (0,515-0,818) |
| UFGSI 10 | 0,680 (0,519-0,841) |
| UFGSI 11 | 0,687 (0,520-0,854) |
| UFGSI 12 | 0,667 (0,489-0,845) |
FGSIS: Fournier's Gangrene Severity Index Score; UFGSI: Uludag Fournier's Gangrene Severity Index.
La tasa de mortalidad de la GF es elevada, desde un 7-75% en series clásicas, hasta un 10-40% en series más recientes, siendo 25% en la nuestra, cuyos factores predictores independientes fueron la vasculopatía periférica, niveles altos de potasio sérico y criterios de sepsis grave1,7–10.
Los factores predictores descritos son múltiples. La edad ha ido incrementándose de forma progresiva en las series publicadas, siendo cada vez más los estudios que demuestran una mayor edad en los que fallecen, como en la nuestra, aunque no se alcanzó significación estadística1–3,7–13.
Las comorbilidades más frecuentes han sido la insuficiencia renal crónica y las neoplasias mientras que en la nuestra lo fue solo la vasculopatía periférica. La DM, pese a ser un factor predisponente frecuente y estar relacionada con una disminución de la función de las células defensivas, no se ha asociado en la mayoría de las series, al igual que en la nuestra, con una mayor tasa de mortalidad9,12,14–18. De forma reciente, el ICC e ICCAE se han descrito, al igual que nuestra serie, como factores predictores de mortalidad10,18.
En cuanto a la etiología, la mayoría de las series no muestran diferencias entre los distintos grupos etiológicos (colorrectal, genitourinaria, traumática e idiopática); en el presente estudio, la mortalidad fue superior en los casos colorrectales y traumáticos, sin alcanzar significación estadística2,8,9,19.
Los parámetros de laboratorio más frecuentemente observados son niveles bajos de hematocrito, bicarbonato y albúmina así como los niveles elevados de urea, creatinina, leucocitos, sodio, potasio, fosfatasa alcalina y lactato9–13,19. En nuestra serie, la mortalidad fue significativamente superior en pacientes con niveles bajos de hemoglobina (p=0,014) y hematocrito (p=0,009) así como con niveles elevados de fosfatasa alcalina (p=0,026), urea (p<0,001), creatinina (p=0,032) y potasio (p=0,012) lo que refleja el papel importante de la insuficiencia renal en la predicción de la mortalidad.
El retraso en el tratamiento debería conllevar una mayor tasa de mortalidad. Sin embargo, hay evidencia de distintas series en las que el período de latencia y un punto de corte de 2 días como diferencia entre un tratamiento precoz y tardío resultó predictor de mortalidad y otras, como en la nuestra, en las que no fue así1,9,11,13,19.
La realización de colostomía derivativa o de cistostomía, al igual que en nuestra serie, no ha demostrado valor pronóstico1,2,7,9,12,19,20.
En los cultivos microbiológicos, los diferentes grupos (aerobios grampositivos y negativos y anaerobios) no se han correlacionado con la mortalidad, igual que en nuestra serie21,22.
En cuanto a la SCA, su valor pronóstico no está claro, si bien son cada vez más las series que muestran, como la presente, una SCA mayor en los que fallecen, aunque sin alcanzar diferencias significativas1,7–11,15,19.
Algunos autores han descrito una mayor mortalidad cuanto mayor es el número de desbridamientos, argumentando una progresión de la enfermedad con mayor superficie afecta y sepsis; sin embargo, este dato no se ha corroborado en la mayoría de las series, de forma similar a la nuestra3,7,11,12,15,19.
Toda escala pronóstica debería predecir lo mejor posible y de la manera más sencilla un determinado evento. En el caso de la GF, el principal evento es la mortalidad para lo cual existen validadas hasta el momento 2, el FGSIS y el UFGSI2.
Laor creó en 1995 el FGSIS mediante modificación de la escala Acute Physiology and Chronic Health Evaluation II (APACHE-II) y estableció un punto de corte de tal forma que, cuando FGSIS >9 la probabilidad de mortalidad era del 75% y cuando era ≤ 9, la de supervivencia era del 78%23. Su valor predictor así como del punto de corte han sido confirmados en la mayoría de las series2,9–11,15,19. En la nuestra, la puntuación del FGSIS fue significativamente superior en los pacientes que fallecieron, siendo su capacidad discriminativa aceptable; sin embargo, aunque las diferencias existentes con el punto de corte de 9 fueron significativas, la capacidad discriminativa fue mejor con el punto de corte de 6. Yilmazlar creó en 2010 un nuevo score (UFGSI) añadiendo 2 parámetros, edad y extensión de la enfermedad, mejorando en su serie la capacidad discriminativa, aunque también haciéndola más compleja, con respecto al FGSIS; empleó el punto de corte de 9 según el cual, cuando el UFGSI >9 la probabilidad de mortalidad era del 94% y, cuando UFGSI ≤ 9 la de supervivencia era del 81%2. En nuestra serie, la capacidad discriminativa del UFGSI mejoró ligeramente la del FGSIS; sin embargo, el punto de corte con mejor capacidad discriminativa fue 11.
El uso de escalas pronósticas es importante por diversas razones:
- a)
Modificación de actitudes terapéuticas: Yilmazlar planteó que cuando el UFGSI >9, dado que la probabilidad de mortalidad era elevada, debería ser manejado en UCI mientras que cuando UFGSI ≤ 9, la de supervivencia era elevada, siendo raro el requerimiento de UCI, con lo que podrían evitarse costes innecesarios y la morbilidad derivada de su estancia2.
- b)
Realización de retroalimentación y corrección de errores tanto diagnósticos como terapéuticos en todos los pacientes pero sobre todo en aquellos que fallecieron cuando su probabilidad era baja según la escala.
El principal problema de estas escalas radica en que su capacidad discriminativa se encuentra mermada y, por tanto, serían potencialmente mejorables, tal y como han demostrado algunos estudios, al estar constituidas por variables que no presentan diferencias significativas entre los que sobreviven y los que fallecen, de forma similar a la nuestra, en la que 5 de 8 en el FGSIS y 7 de 10 en UFGSI no fueron significativas9,10,15,19. Nuestro modelo tuvo una capacidad discriminativa mayor que el FGSIS y UFGSI ya que, a diferencia de estos, todos sus parámetros presentaron diferencias significativas entre los que sobreviven y fallecen.
Consideramos que la principal limitación del estudio radica en su carácter retrospectivo y en un bajo tamaño muestral, lo que ocurre en la mayoría de los estudios debido a la baja incidencia de la GF.
En conclusión, la GF es una enfermedad con baja incidencia y alta tasa de mortalidad, sin un modelo de predicción ideal de esta. Los autores hemos creado un modelo predictivo cuyos factores fueron la vasculopatía periférica, los niveles altos de potasio sérico y los criterios de sepsis grave, con una capacidad discriminativa superior a los modelos previamente descritos, cuya utilidad radicaría en el mejor conocimiento de esta enfermedad, en poder identificar errores ante una mortalidad inesperada y en mejorar la supervivencia, pero que necesitará validación en series más largas.
Contribución de los autoresAndrés García Marín: diseño del estudio, adquisición y recogida de datos, análisis e interpretación de los resultados, redacción del artículo, revisión crítica y aprobación de la versión final.
Fernando Turégano Fuentes: diseño del estudio, análisis e interpretación de los resultados, redacción del artículo, revisión crítica y aprobación de la versión final.
Marta Cuadrado Ayuso: adquisición y recogida de datos, redacción del artículo, revisión crítica y aprobación de la versión final.
Juan Antonio Andueza Lillo: redacción del artículo, revisión crítica y aprobación de la versión final.
Juan Carlos Cano Ballesteros: redacción del artículo, revisión crítica y aprobación de la versión final.
Mercedes Pérez López: redacción del artículo, revisión crítica y aprobación de la versión final.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Presentación parcial en la XIX Reunión Nacional de Cirugía (Burgos, del 23 al 25 de octubre de 2013).